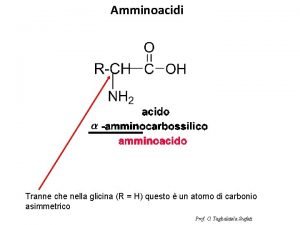
AMMINOACIDI Tutti gli amminoacidi tranne la glicina hanno
![Titolazione della glicina con una base forte p. H = p. Ka quando [A-] Titolazione della glicina con una base forte p. H = p. Ka quando [A-]](https://slidetodoc.com/presentation_image_h2/5754b5ca9dc8cb9d336b23e9606e535d/image-11.jpg)
- Slides: 13

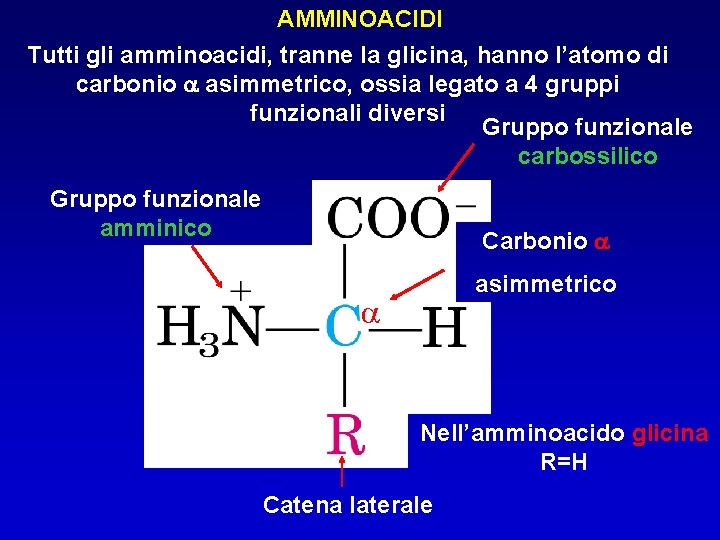
AMMINOACIDI Tutti gli amminoacidi, tranne la glicina, hanno l’atomo di carbonio a asimmetrico, ossia legato a 4 gruppi funzionali diversi Gruppo funzionale carbossilico Gruppo funzionale amminico Carbonio a asimmetrico a Nell’amminoacido glicina R=H Catena laterale

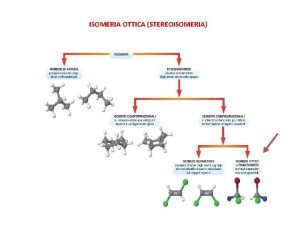
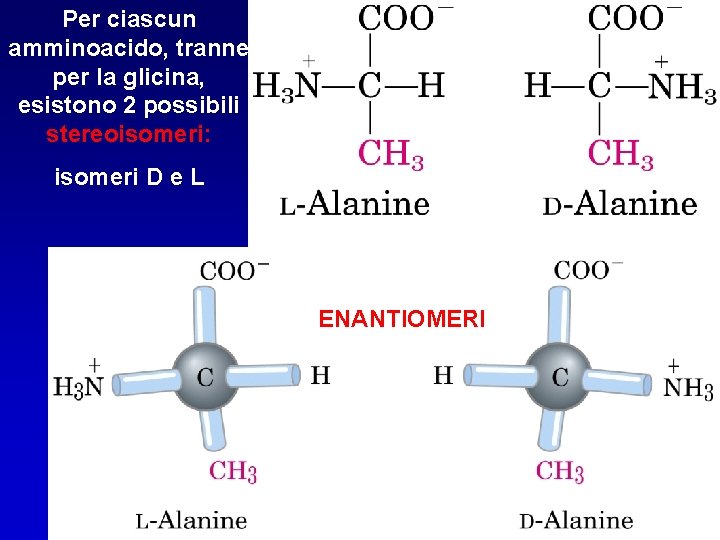
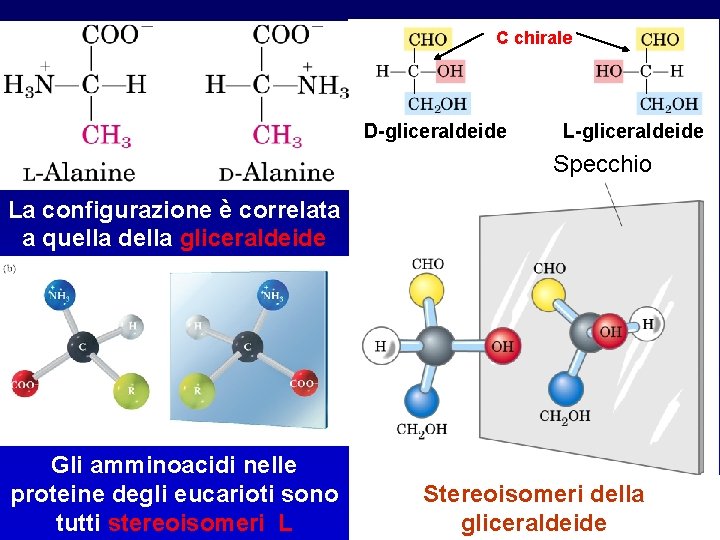
Per ciascun amminoacido, tranne per la glicina, esistono 2 possibili stereoisomeri: isomeri D e L ENANTIOMERI

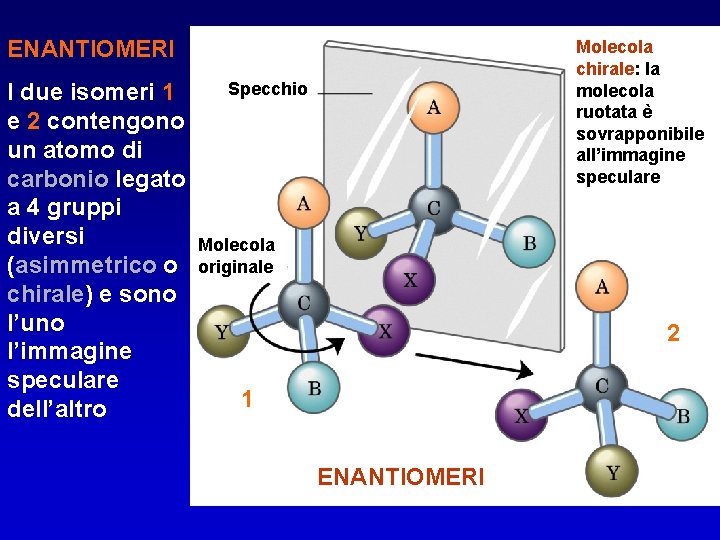
ENANTIOMERI I due isomeri 1 e 2 contengono un atomo di carbonio legato a 4 gruppi diversi (asimmetrico o chirale) e sono l’uno l’immagine speculare dell’altro Molecola chirale: la molecola ruotata è sovrapponibile all’immagine speculare Specchio Molecola originale 2 1 ENANTIOMERI

C chirale 1 2 * * 3 D-gliceraldeide L-gliceraldeide Specchio La configurazione è correlata a quella della gliceraldeide Gli amminoacidi nelle proteine degli eucarioti sono tutti stereoisomeri L Stereoisomeri della gliceraldeide

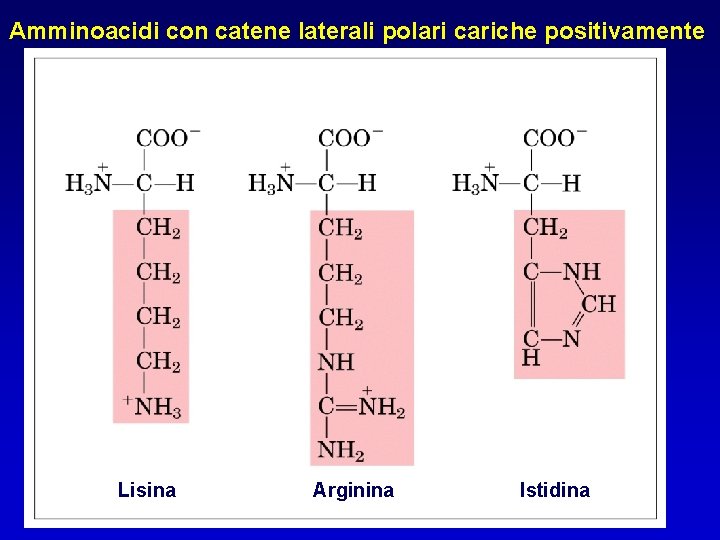
Amminoacidi con catene laterali polari cariche positivamente Lisina Arginina Istidina

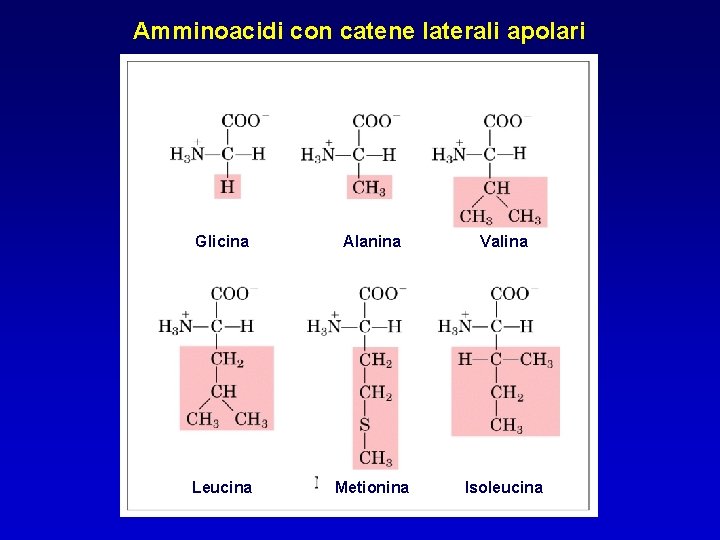
Amminoacidi con catene laterali apolari Glicina Alanina Valina Leucina Metionina Isoleucina

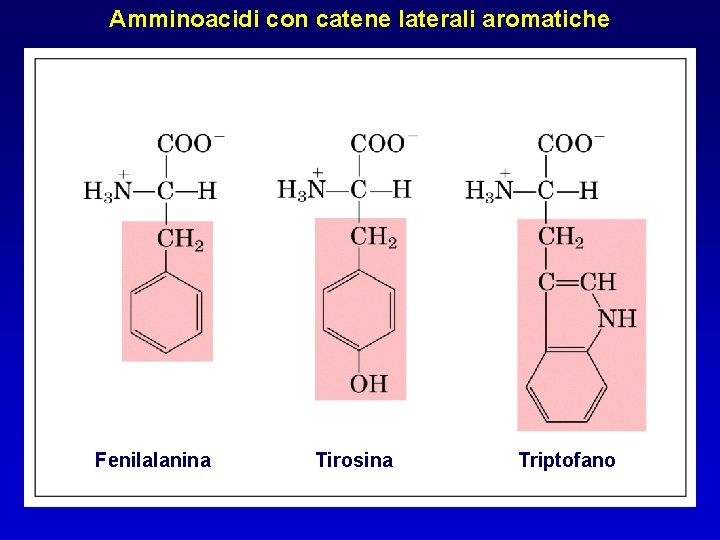
Amminoacidi con catene laterali aromatiche Fenilalanina Tirosina Triptofano

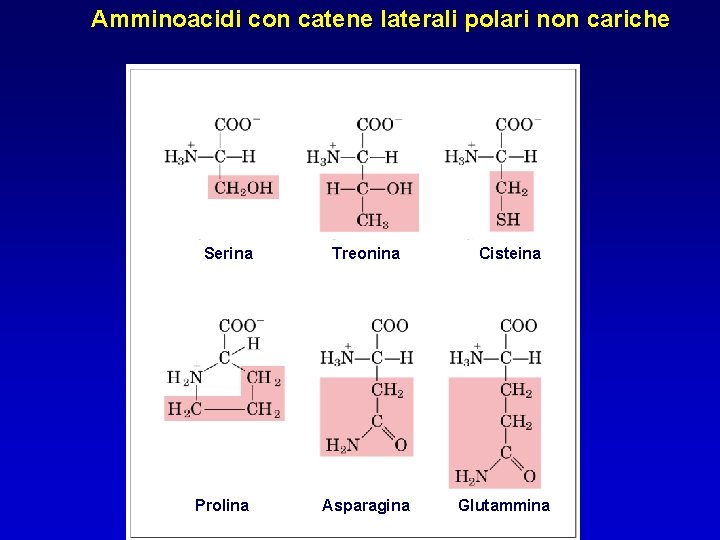
Amminoacidi con catene laterali polari non cariche Serina Prolina Treonina Asparagina Cisteina Glutammina

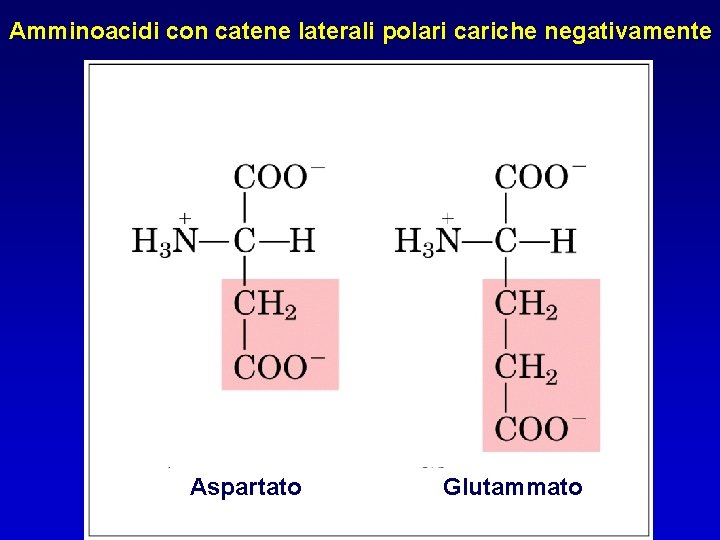
Amminoacidi con catene laterali polari cariche negativamente Aspartato Glutammato

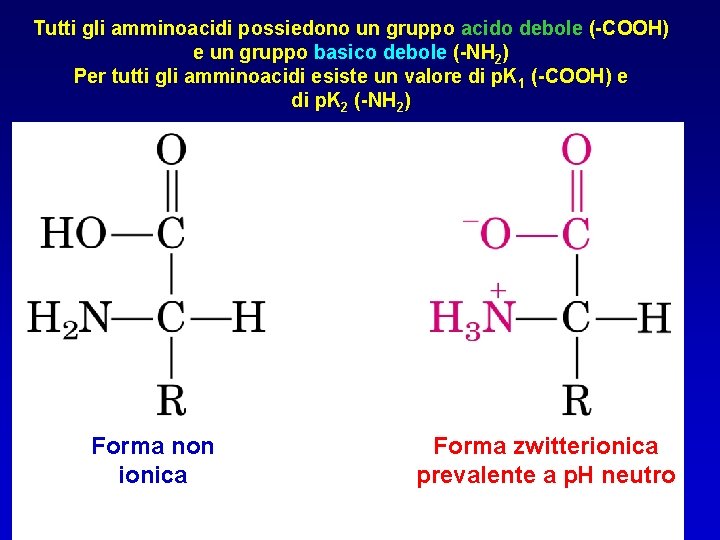
Tutti gli amminoacidi possiedono un gruppo acido debole (-COOH) e un gruppo basico debole (-NH 2) Per tutti gli amminoacidi esiste un valore di p. K 1 (-COOH) e di p. K 2 (-NH 2) Forma non ionica Forma zwitterionica Triptofano prevalente a p. H neutro
![Titolazione della glicina con una base forte p H p Ka quando A Titolazione della glicina con una base forte p. H = p. Ka quando [A-]](https://slidetodoc.com/presentation_image_h2/5754b5ca9dc8cb9d336b23e9606e535d/image-11.jpg)
Titolazione della glicina con una base forte p. H = p. Ka quando [A-] = [HA] HA ha rilasciato la metà dei protoni HA è dissociato per il 50% Glicina p. H = p. K 2 quando [-NH 3+] = [NH 2] p. H = p. I = ½ (p. K 1+ p. K 2) Al punto isoelettrico la carica netta della molecola = 0 [-NH 3+] = [-COO-] p. H = p. K 1 quando [-COO-] = [-COOH] OH- (equivalenti) Tutti gli amminoacidi, tranne l’Istidina, hanno valori simili di p. K 1 (1, 8 -2, 4) e di p. K 2 (8, 8 -11)

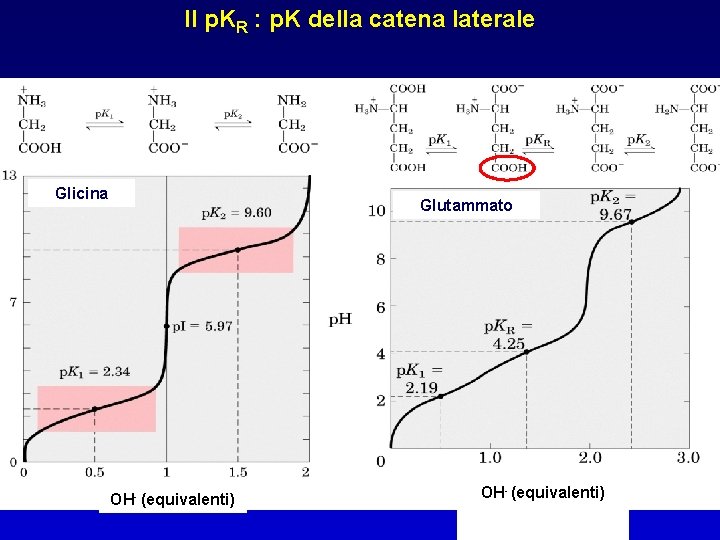
Il p. KR : p. K della catena laterale Glicina Glutammato OH- (equivalenti)

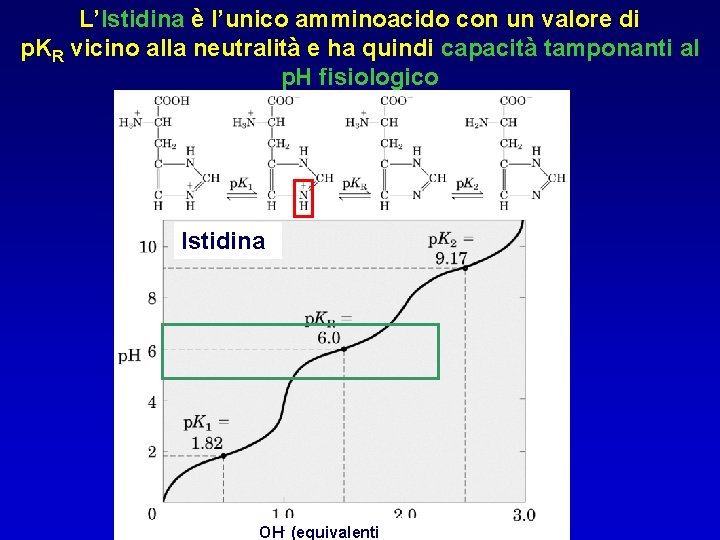
L’Istidina è l’unico amminoacido con un valore di p. KR vicino alla neutralità e ha quindi capacità tamponanti al p. H fisiologico Istidina OH- (equivalenti
 Stereoisomeria ottica
Stereoisomeria ottica Quali caratteristiche hanno gli esseri viventi
Quali caratteristiche hanno gli esseri viventi Quali sono gli animali invertebrati
Quali sono gli animali invertebrati Figure con 4 lati
Figure con 4 lati Animali invertebrati
Animali invertebrati Glicina y serina
Glicina y serina Glicina
Glicina Aminoacidos nombres
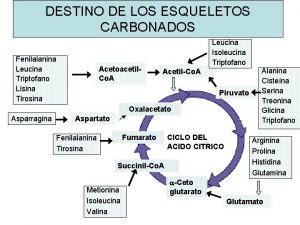
Aminoacidos nombres Destino de los esqueletos carbonados
Destino de los esqueletos carbonados Liquido intravascular
Liquido intravascular Carater anfotero
Carater anfotero Aminoácido
Aminoácido Glicolisi mappa concettuale
Glicolisi mappa concettuale Endopeptidasi
Endopeptidasi