DESTINO DE LOS ESQUELETOS CARBONADOS Fenilalanina Leucina Triptofano
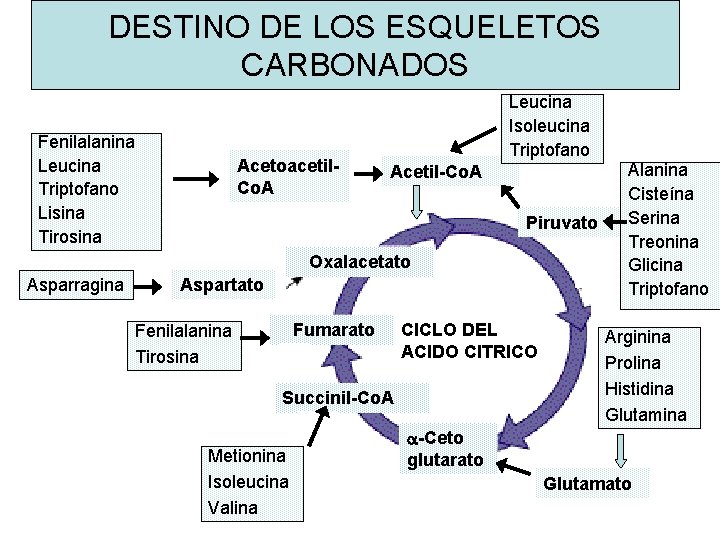
DESTINO DE LOS ESQUELETOS CARBONADOS Fenilalanina Leucina Triptofano Lisina Tirosina Acetoacetil. Co. A Leucina Isoleucina Triptofano Acetil-Co. A Piruvato Oxalacetato Asparragina Aspartato Fumarato Fenilalanina Tirosina CICLO DEL ACIDO CITRICO Succinil-Co. A Metionina Isoleucina Valina Alanina Cisteína Serina Treonina Glicina Triptofano Arginina Prolina Histidina Glutamina a-Ceto glutarato Glutamato

AMINOACIDOS CETOGENICOS Y GLUCOGENICOS • Aminoácidos Glucogénicos: Los esqueletos carbonados pueden utilizarse para la síntesis de glucosa (aa. no esenciales) • Aminoácidos Cetogénicos: Los esqueletos carbonados pueden ser convertidos en cuerpos cetónicos (Leucina y Lisina) • Aminoácidos glucogénicos y cetogénicos: Fenilalanina, Tirosina, Isoleucina y Triptofano

COFACTORES UTILIZADOS EN REACCIONES DE DEGRADACION DE ESQUELETOS CARBONADOS • TETRAHIDROFOLATO (FH 4): Transferencia de unidades de un carbono (metilo, formilo, metileno, etc. ) • S-ADENOSILMETIONINA (SAM): Transferencia de metilos. • TETRAHIDROBIOPTERINA (BH 4): Transportador de electrones
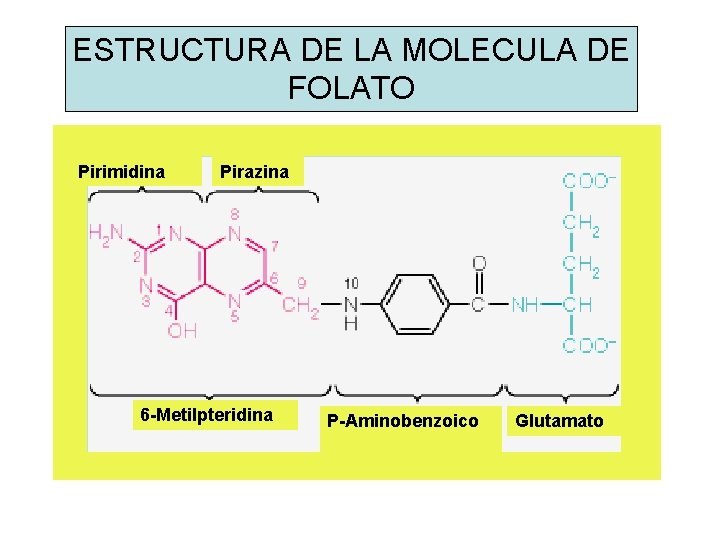
ESTRUCTURA DE LA MOLECULA DE FOLATO Pirimidina Pirazina 6 -Metilpteridina P-Aminobenzoico Glutamato
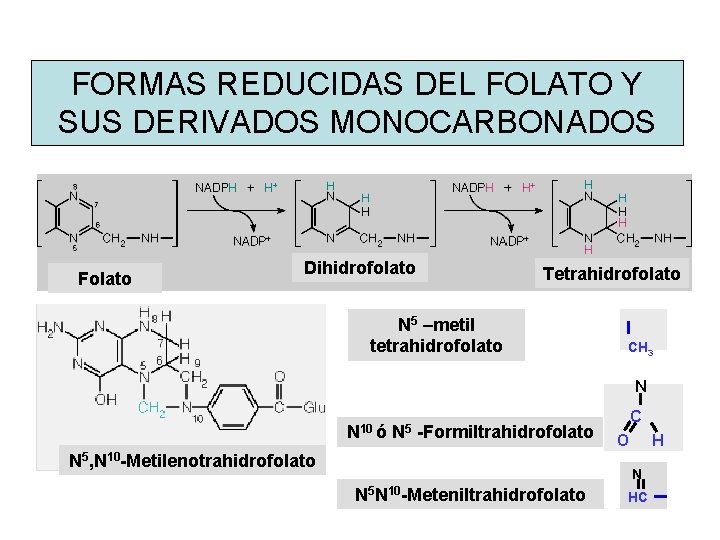
FORMAS REDUCIDAS DEL FOLATO Y SUS DERIVADOS MONOCARBONADOS Folato Dihidrofolato Tetrahidrofolato N 5 –metil tetrahidrofolato CH 3 N C 10 5 N ó N -Formiltrahidrofolato O H N 5, N 10 -Metilenotrahidrofolato N N 5 N 10 -Meteniltrahidrofolato HC
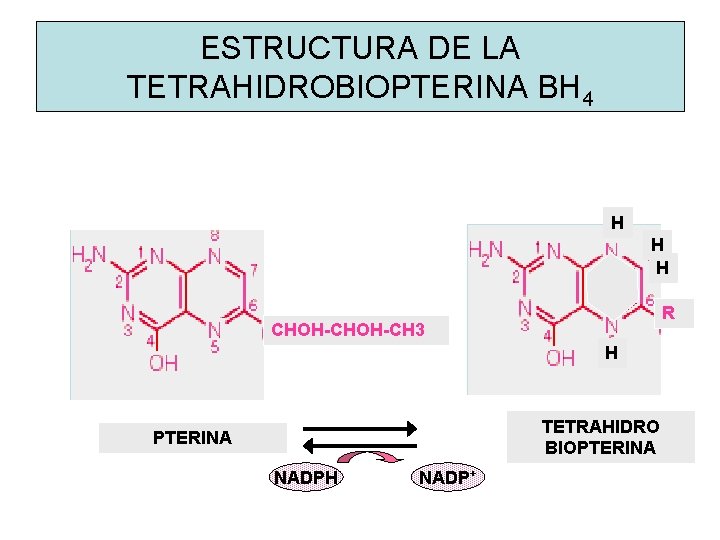
ESTRUCTURA DE LA TETRAHIDROBIOPTERINA BH 4 H H H R CHOH-CH 3 H TETRAHIDRO BIOPTERINA NADPH NADP+
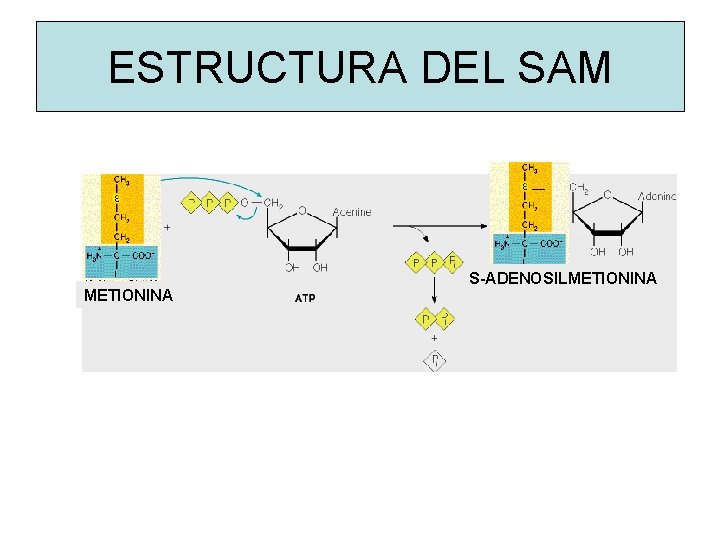
ESTRUCTURA DEL SAM ─ METIONINA S-ADENOSILMETIONINA
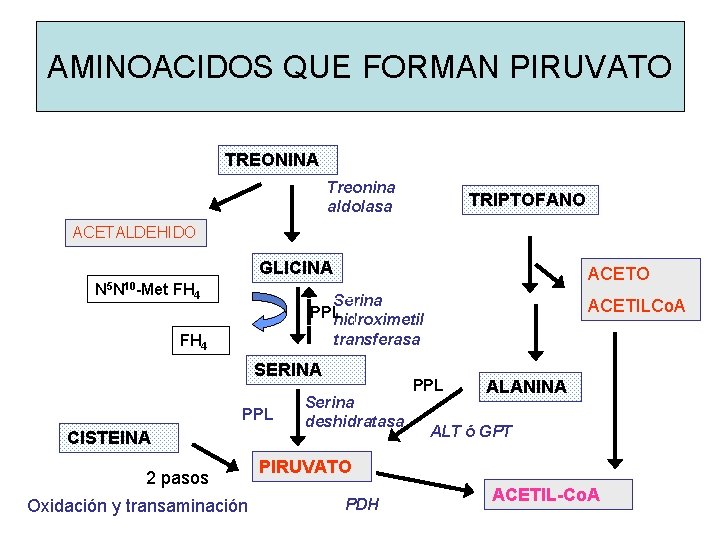
AMINOACIDOS QUE FORMAN PIRUVATO TREONINA Treonina aldolasa TRIPTOFANO ACETALDEHIDO GLICINA N 5 N 10 -Met FH 4 ACETO Serina PPL hidroximetil transferasa FH 4 SERINA PPL CISTEINA 2 pasos Oxidación y transaminación Serina deshidratasa ACETILCo. A PPL ALANINA ALT ó GPT PIRUVATO PDH ACETIL-Co. A
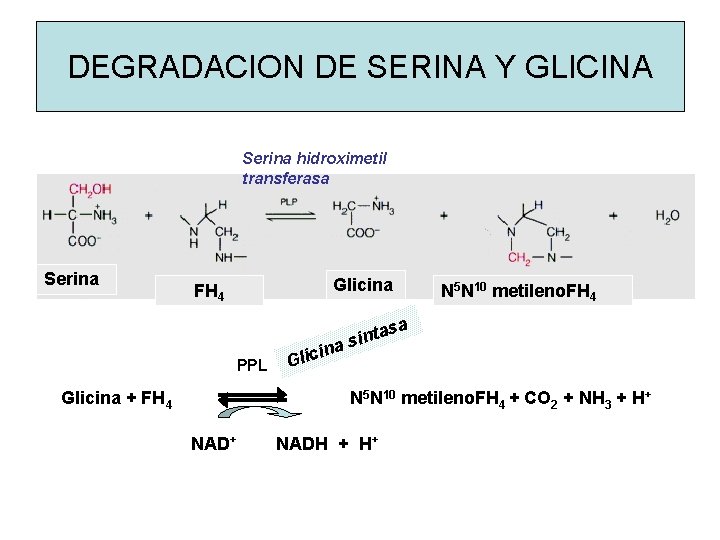
DEGRADACION DE SERINA Y GLICINA Serina hidroximetil transferasa Serina Glicina FH 4 N 5 N 10 metileno. FH 4 a PPL Glicina + FH 4 in Glic a as sint N 5 N 10 metileno. FH 4 + CO 2 + NH 3 + H+ NAD+ NADH + H+
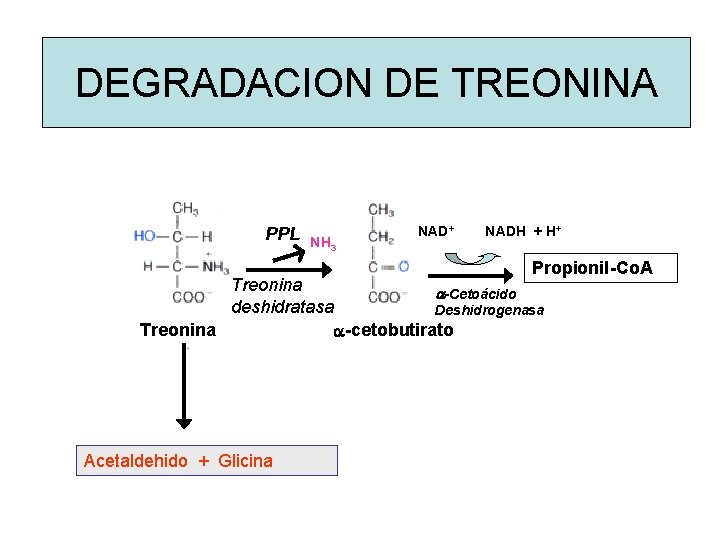
DEGRADACION DE TREONINA PPL NH 3 NAD+ NADH + H+ Propionil-Co. A Treonina a-Cetoácido deshidratasa Deshidrogenasa Treonina a-cetobutirato Acetaldehido + Glicina
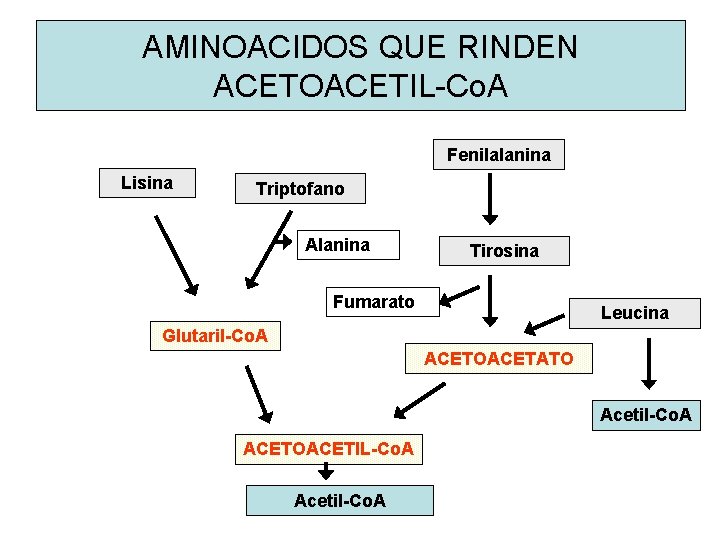
AMINOACIDOS QUE RINDEN ACETOACETIL-Co. A Fenilalanina Lisina Triptofano Alanina Tirosina Fumarato Leucina Glutaril-Co. A ACETOACETATO Acetil-Co. A ACETOACETIL-Co. A Acetil-Co. A
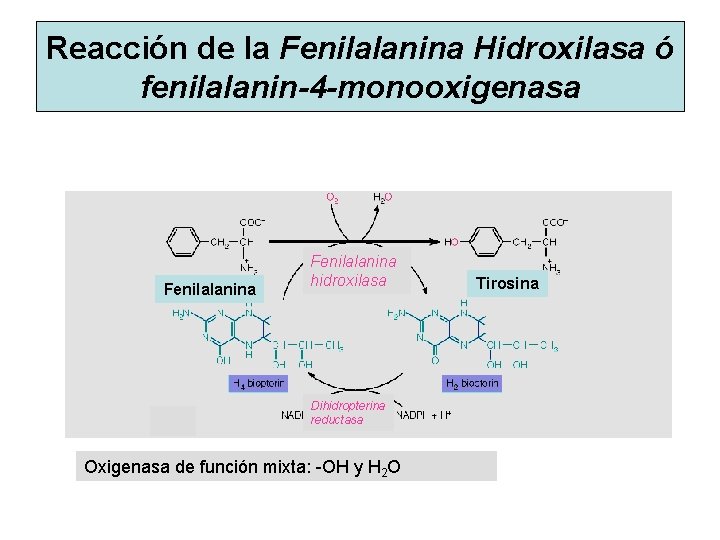
Reacción de la Fenilalanina Hidroxilasa ó fenilalanin-4 -monooxigenasa Fenilalanina hidroxilasa Dihidropterina reductasa Oxigenasa de función mixta: -OH y H 2 O Tirosina
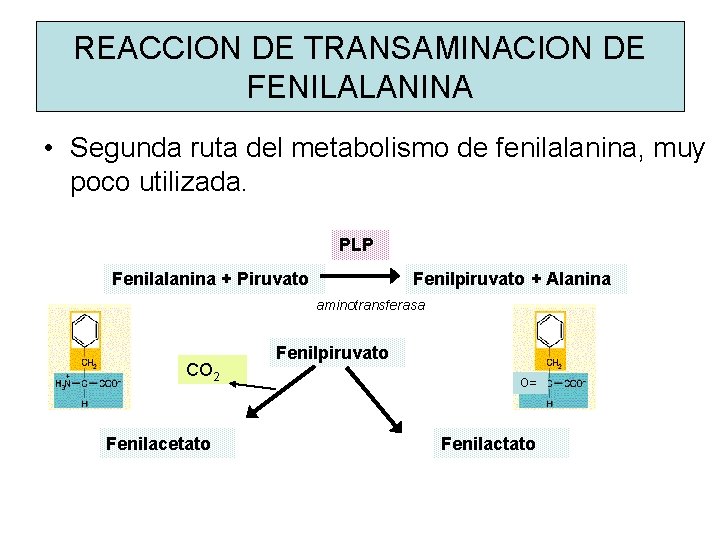
REACCION DE TRANSAMINACION DE FENILALANINA • Segunda ruta del metabolismo de fenilalanina, muy poco utilizada. PLP Fenilalanina + Piruvato Fenilpiruvato + Alanina aminotransferasa CO 2 Fenilacetato Fenilpiruvato O= Fenilactato
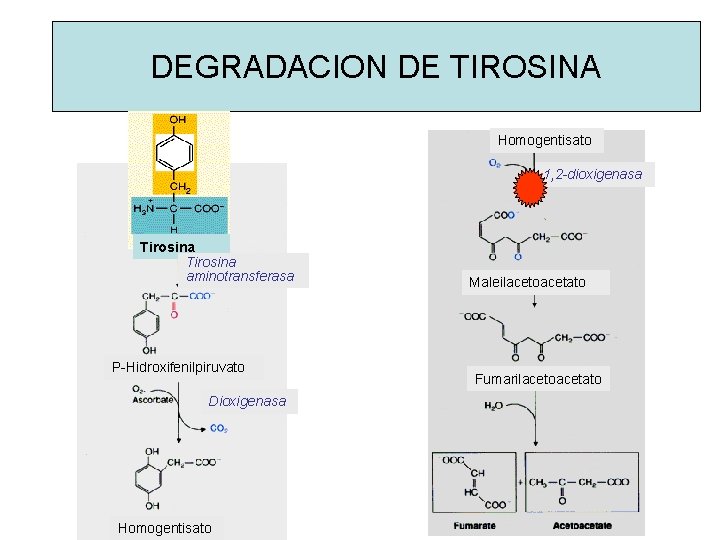
DEGRADACION DE TIROSINA Homogentisato 1, 2 -dioxigenasa Tirosina aminotransferasa P-Hidroxifenilpiruvato Dioxigenasa Homogentisato Maleilacetoacetato Fumarilacetoacetato
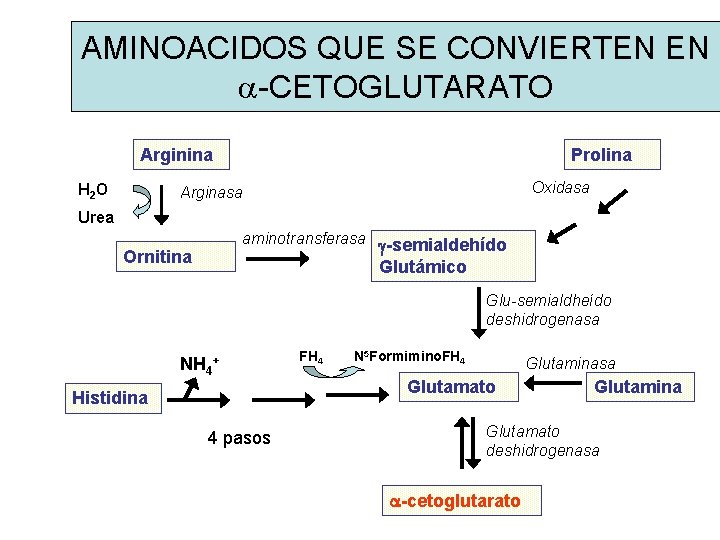
AMINOACIDOS QUE SE CONVIERTEN EN a-CETOGLUTARATO Arginina H 2 O Prolina Oxidasa Arginasa Urea aminotransferasa g-semialdehído Ornitina Glutámico Glu-semialdheído deshidrogenasa NH 4+ Histidina 4 pasos FH 4 N 5 Formimino. FH 4 Glutaminasa Glutamato Glutamina Glutamato deshidrogenasa a-cetoglutarato
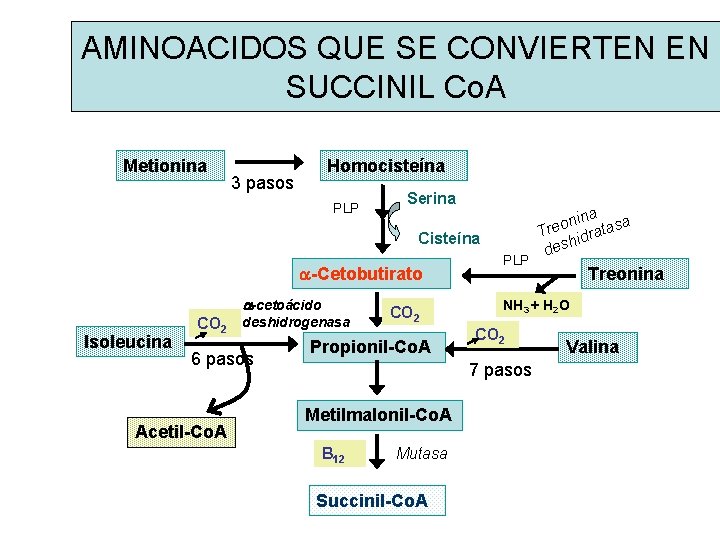
AMINOACIDOS QUE SE CONVIERTEN EN SUCCINIL Co. A Metionina Homocisteína 3 pasos PLP Serina Cisteína a-Cetobutirato a-cetoácido Isoleucina CO 2 deshidrogenasa 6 pasos Acetil-Co. A CO 2 Propionil-Co. A PLP B 12 Mutasa Succinil-Co. A Treonina NH 3 + H 2 O CO 2 7 pasos Metilmalonil-Co. A ina sa n o Tre idrata h des Valina
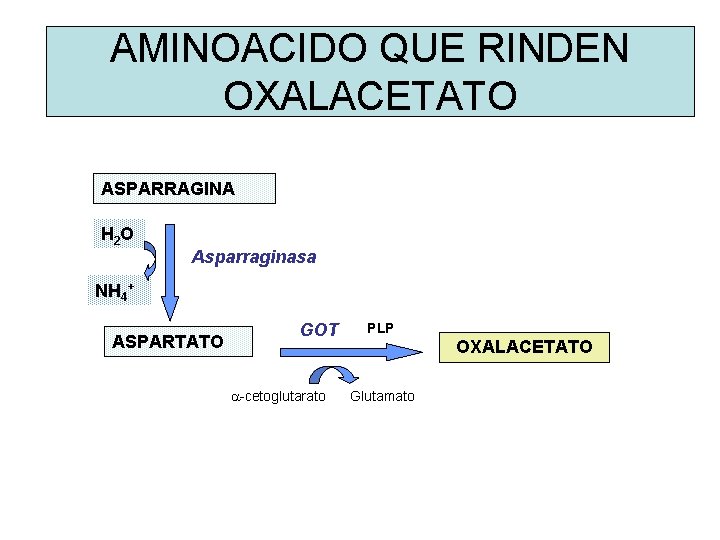
AMINOACIDO QUE RINDEN OXALACETATO ASPARRAGINA H 2 O Asparraginasa NH 4+ ASPARTATO GOT a-cetoglutarato PLP OXALACETATO Glutamato
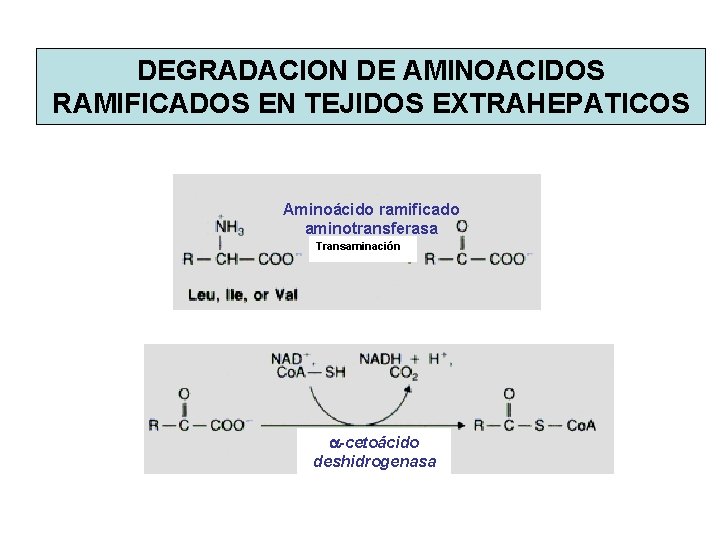
DEGRADACION DE AMINOACIDOS RAMIFICADOS EN TEJIDOS EXTRAHEPATICOS Aminoácido ramificado aminotransferasa Transaminación a-cetoácido deshidrogenasa

FUNCIONES PRECURSORAS DE LOS AMINOACIDOS • • • GLICINA: Purinas, Hemo, Glutatión SERINA: Derivados de folato, esfingosina. METIONINA: SAM GLUTAMINA y GLUTAMATO: GABA FENILALANINA y TIROSINA: Catecolaminas TIROSINA: Tiramina, Melanina, Hormonas tiroideas. TRIPTOFANO: Serotonina, Triptamina, Melatonina, Acido nicotínico. . ARGININA: Oxido Nítrico SERINA Y METIONINA: Acetilcolina HISTIDINA: Histamina. ARGININA, GLICINA Y METIONINA: Creatina
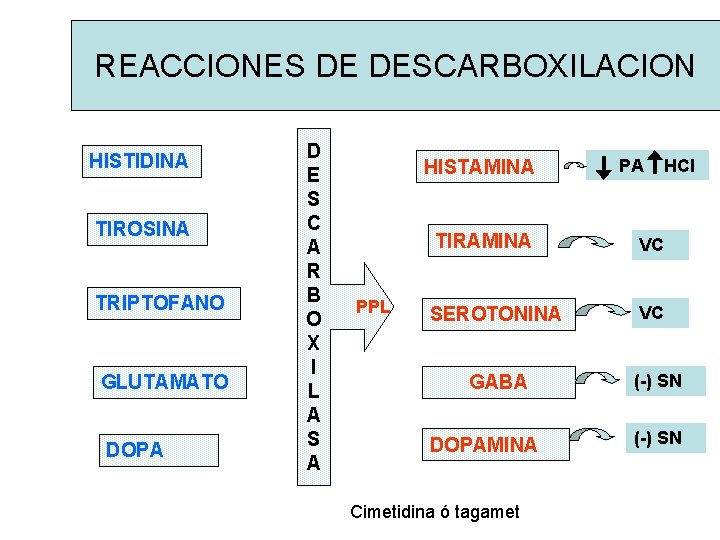
REACCIONES DE DESCARBOXILACION HISTIDINA TIROSINA TRIPTOFANO GLUTAMATO DOPA D E S C A R B O X I L A S A HISTAMINA TIRAMINA PPL SEROTONINA GABA DOPAMINA Cimetidina ó tagamet PA HCl VC VC (-) SN
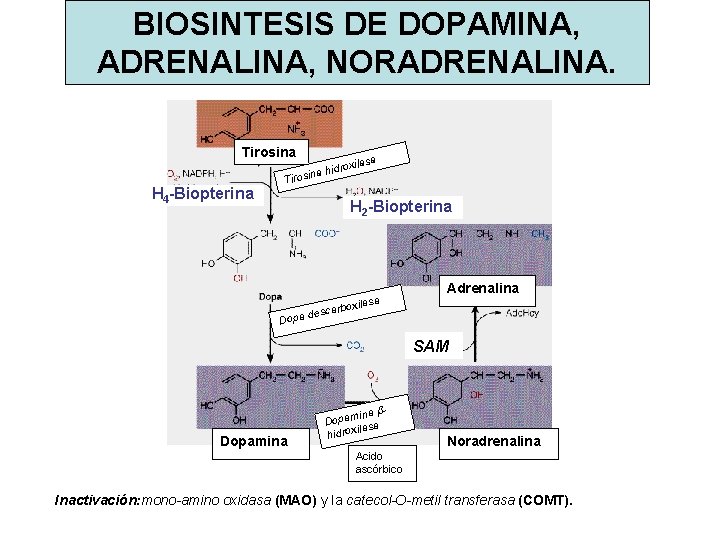
BIOSINTESIS DE DOPAMINA, ADRENALINA, NORADRENALINA. Tirosina H 4 -Biopterina na hi Tirosi sa a droxil H 2 -Biopterina xilasa carbo s e d Dopa Adrenalina SAM Dopamina b. Dopam sa ila hidrox Noradrenalina Acido ascórbico Inactivación: mono-amino oxidasa (MAO) y la catecol-O-metil transferasa (COMT).
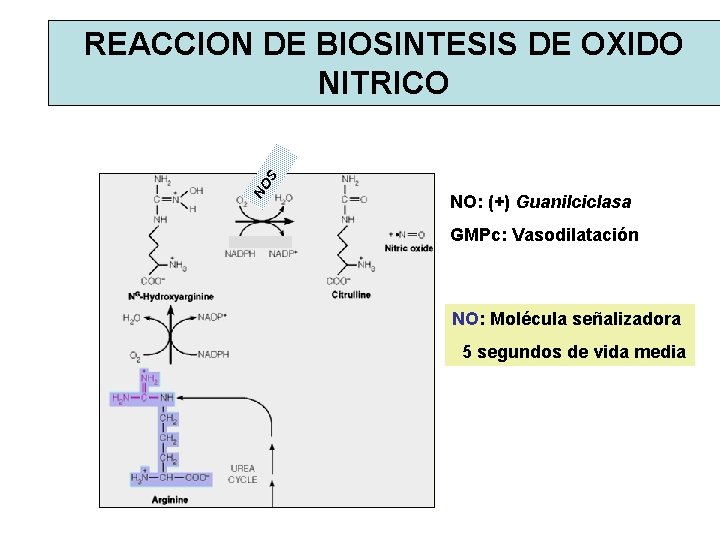
NO S REACCION DE BIOSINTESIS DE OXIDO NITRICO NO: (+) Guanilciclasa GMPc: Vasodilatación NO: Molécula señalizadora 5 segundos de vida media
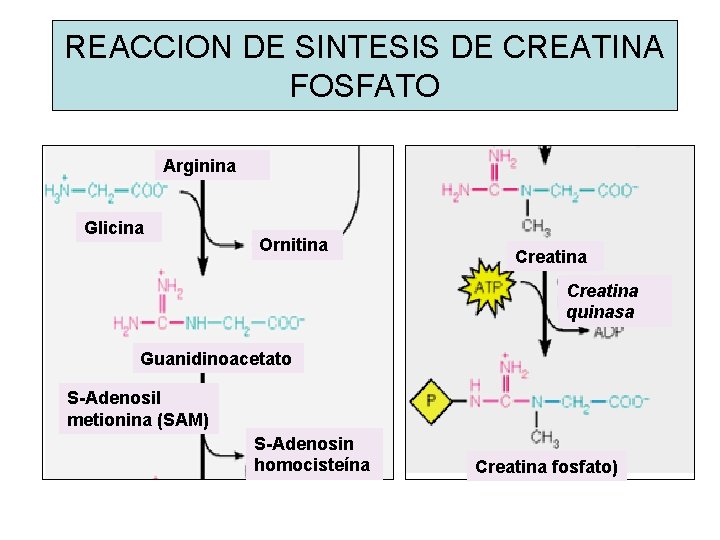
REACCION DE SINTESIS DE CREATINA FOSFATO Arginina Glicina Ornitina Creatina quinasa Guanidinoacetato S-Adenosil metionina (SAM) S-Adenosin homocisteína Creatina fosfato)

BIOSINTESIS DE AMINOACIDOS • Los mamíferos sintetizan los aminoácidos no esenciales. • El esqueleto carbonado de la mayoría de los aminoácidos proceden de: Glicerato-3 -fosfato, piruvato, a-cetoglutarato ó oxalacetato. • Varios aminoácidos se obtienen por reacciones de transaminación. • En varias reacciones de síntesis, se utilizan como dadores de equivalentes de reducción NADPH ó NADH y como dadores de carbono derivados de Folato ó SAM. • Se gasta energía metabólica del ATP
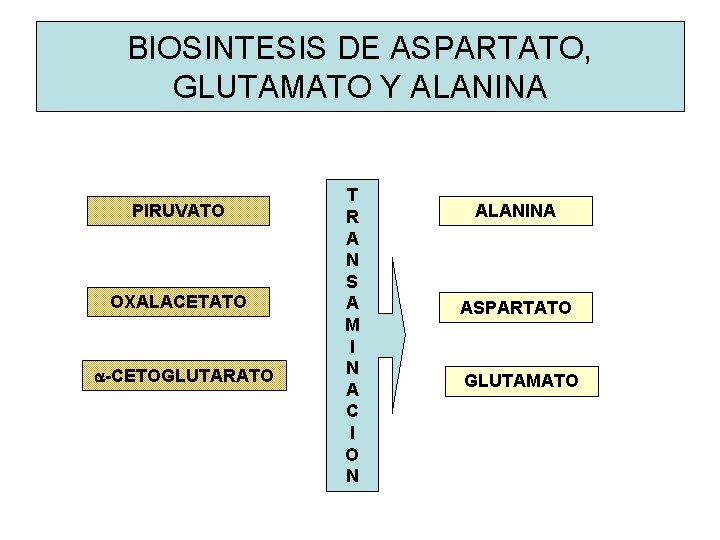
BIOSINTESIS DE ASPARTATO, GLUTAMATO Y ALANINA PIRUVATO OXALACETATO a-CETOGLUTARATO T R A N S A M I N A C I O N ALANINA ASPARTATO GLUTAMATO
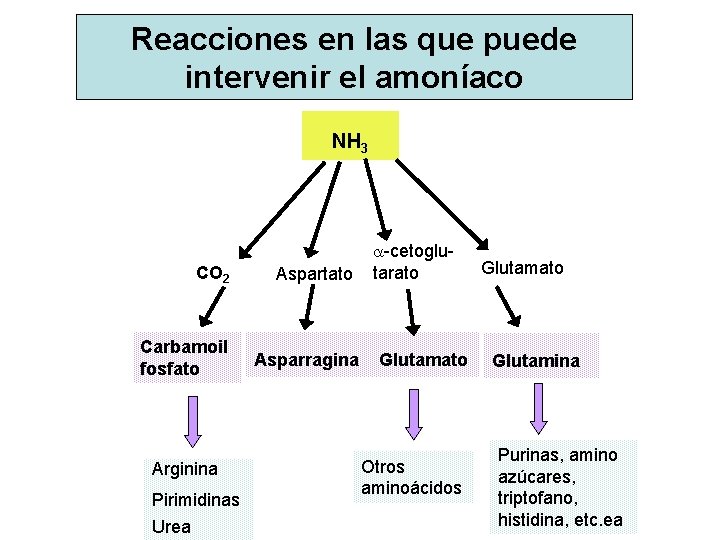
Reacciones en las que puede intervenir el amoníaco NH 3 CO 2 Aspartato Carbamoil fosfato Asparragina Arginina Pirimidinas Urea a-cetoglu- tarato Glutamato Otros aminoácidos Glutamato Glutamina Purinas, amino azúcares, triptofano, histidina, etc. ea
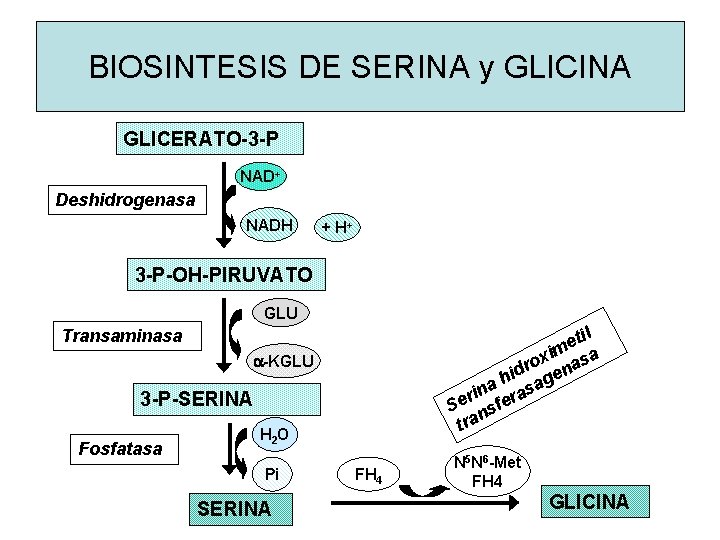
BIOSINTESIS DE SERINA y GLICINA GLICERATO-3 -P NAD+ Deshidrogenasa NADH + H+ 3 -P-OH-PIRUVATO GLU til e im sa x o a r n d i e a h asag n i r r Se nsfe tra Transaminasa a-KGLU 3 -P-SERINA Fosfatasa H 2 O Pi SERINA FH 4 N 5 N 6 -Met FH 4 GLICINA
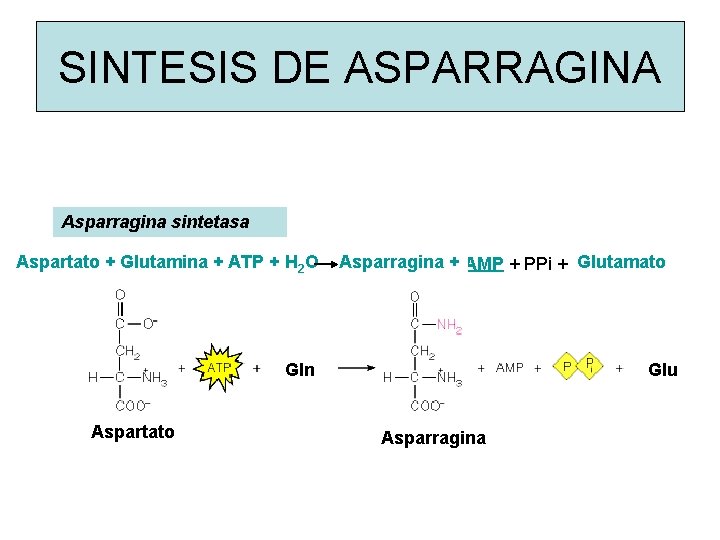
SINTESIS DE ASPARRAGINA Asparagine synthetase Asparragina sintetasa Aspartato + Glutamina + ATP + H Asparragina + Glutamato Aspartate + ATP + NH (Glutamine) -> Asparagine + AMP + PPi + (Glutamate) 2 O 3 + Pi. Gln Aspartato Glu Asparragina

PRECURSORES PARA LA BIOSÍNTESIS DE AMINOÁCIDOS ESENCIALES Molécula Precursora Ribosa-5 fosfato Eritrosa 4 -Fosfato Aminoácidos Histidina Fenilalanina Triptofano Piruvato Valina Leucina Oxalacetato (Aspartato) Metionina Treonina Lisina Isoleucina a-Cetoglutarato (Glutamato) Arginina

Antimetabolitos que actuan sobre metabolismo de neurotrasmisores • Anfetaminas: Análogo de catecolaminas- Psicofármaco • Clorpromazina: Antagonista dopamina- Bloquea la unión de dopamina al receptor • LSD (dietilamida del ác. lisérgico): Psicotropico- Mimetiza la acción de serotonina en los receptores del SN • Fluoxetina (Prozac): Antidepresivo- Bloquea la captación de serotonina • Ritalina: Hiperactividad, déficit de atención. A dosis bajas aumenta la conc. de serotonina (efecto calmante). A dosis alta aumenta la conc. de dopamina.
- Slides: 30