AMINOCIDOS E PROTENAS Faculdade de Odontologia de Piracicaba

AMINOÁCIDOS E PROTEÍNAS Faculdade de Odontologia de Piracicaba UNICAMP


ü Conceito: “primeiro” ou “o mais importante” ü Classificação: a) Constituição: simples – ribonuclease b) conjugadas – grupos prostéticos; lipoproteínas, glicoproteínas e metaloproteínas b) Forma: fibrosas – queratina e colágeno globulares – enzimas c) Funções Biológicas: -Enzimas: amilase, lipase, sacarase, glicosiltransferase

- Proteínas nutrientes e de reserva: do leite e ovoalbumina na clara de ovo - Proteínas lipoproteínas transportadoras: - Proteínas contráteis: caseína hemoglobina, actina, miosina, tubulina - Proteínas estruturais e de proteção: colágeno, elastina e queratina - Proteínas reguladoras (hormônios): e glucagon - Proteínas de fibrinogênio e trombina defesa: insulina Imunoglobulinas,

Aminoácidos ü aa padrão, primários, normais ou comuns: fazem parte das proteínas. ü aa de proteínas oticamente ativos são L -estereoisômeros, exceto a glicina ü Classificação segundo a polaridade dos seus grupos R
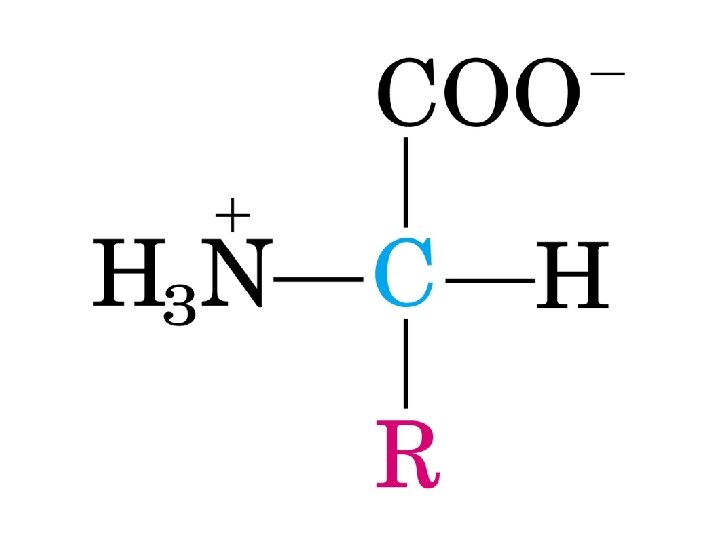
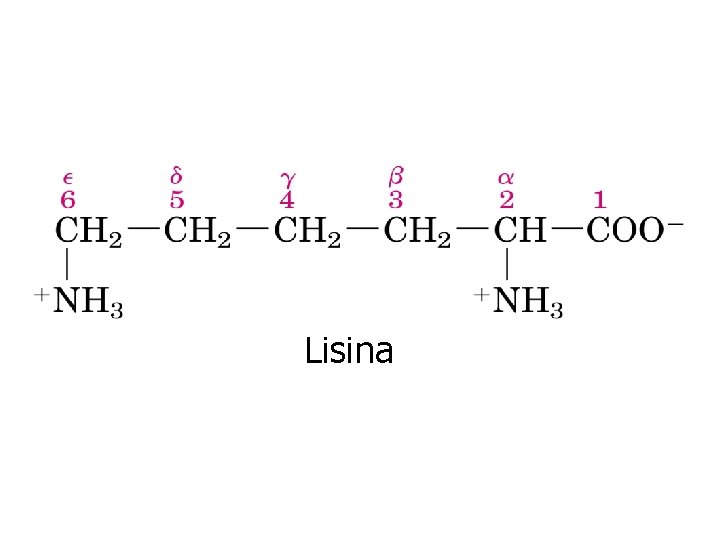
Lisina
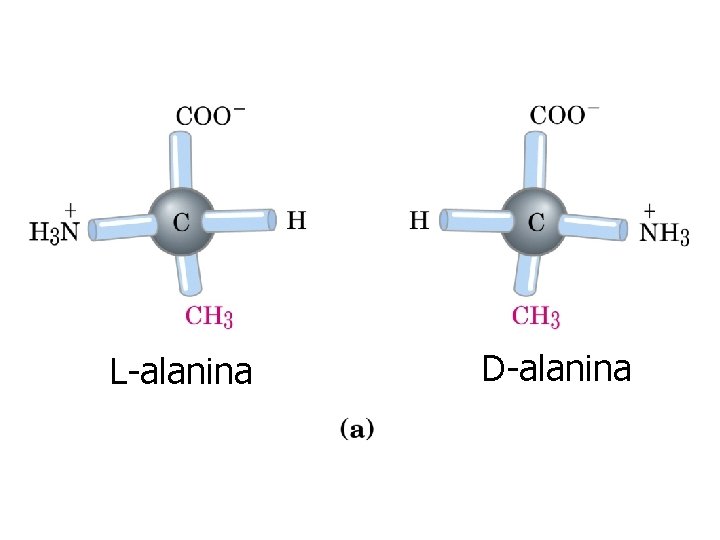
L-alanina D-alanina
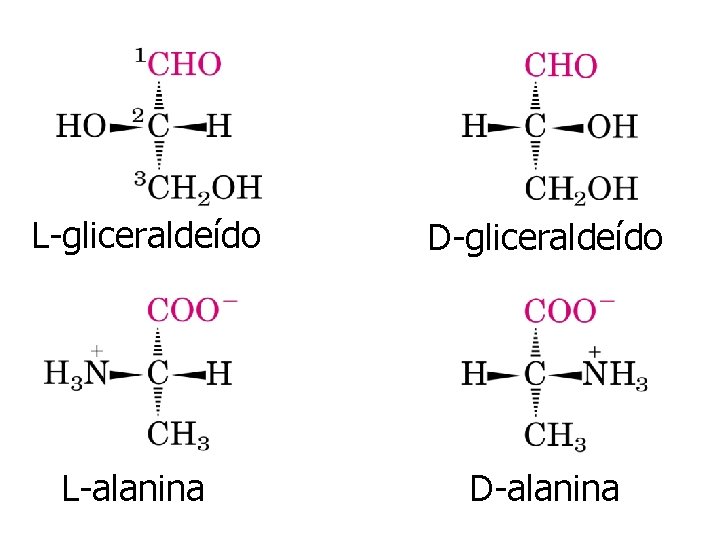
L-gliceraldeído L-alanina D-gliceraldeído D-alanina
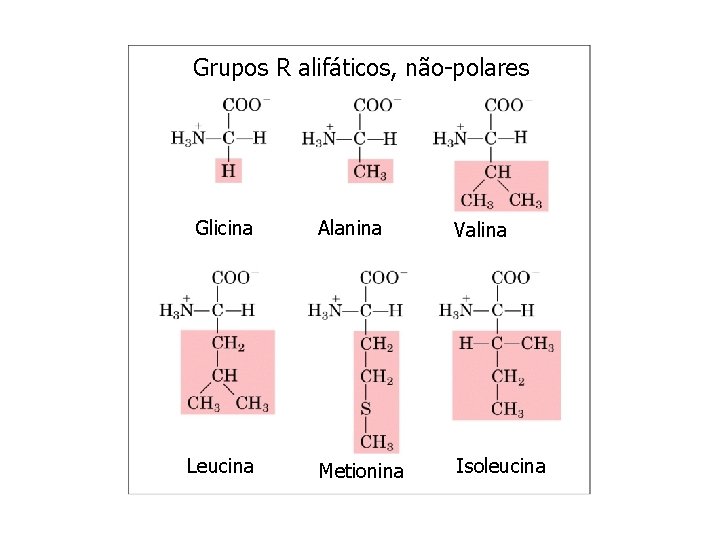
Grupos R alifáticos, não-polares Glicina Leucina Alanina Valina Metionina Isoleucina

Grupos R aromáticos Fenilalanina Tirosina Triptofano

Grupos R polares mas não carregados Serina Prolina Treonina Cisteína Asparagina Glutamina
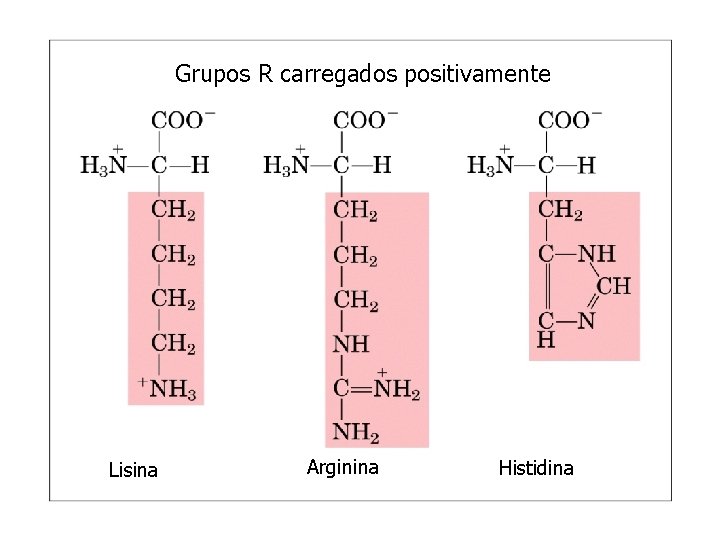
Grupos R carregados positivamente Lisina Arginina Histidina
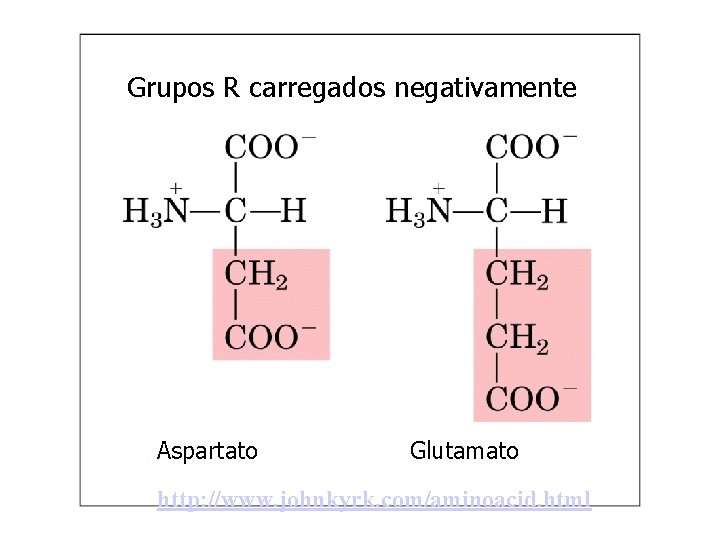
Grupos R carregados negativamente Aspartato Glutamato http: //www. johnkyrk. com/aminoacid. html
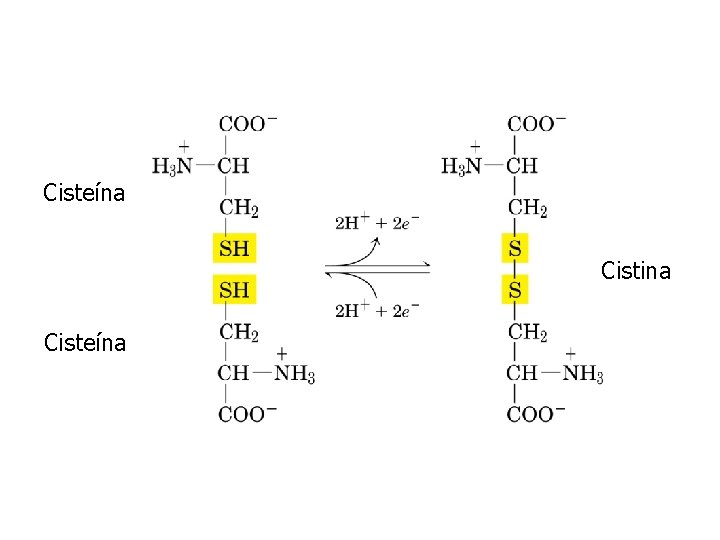
Cisteína Cistina Cisteína

Aminoácidos Especiais -carboxiglutamato (protrombina) 4 -hidroxiprolina (colágeno) 5 -hidroxilisina (colágeno) 6 -N-metilisina (miosina) Desmosina (elastina) selenocisteína
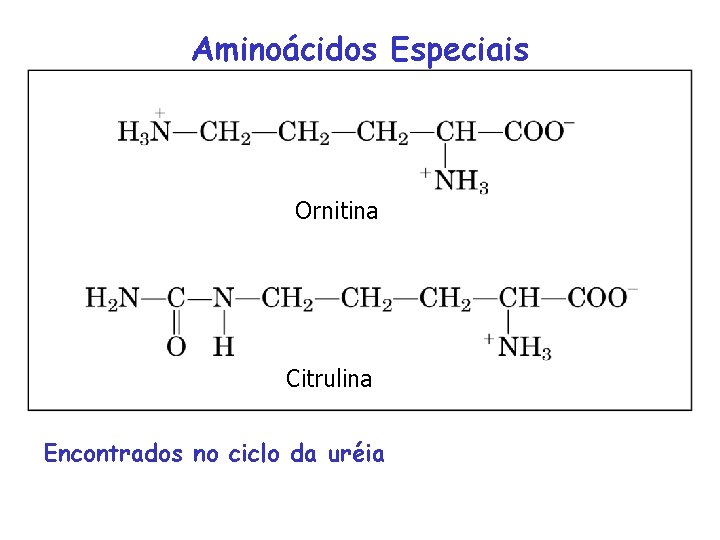
Aminoácidos Especiais Ornitina Citrulina Encontrados no ciclo da uréia
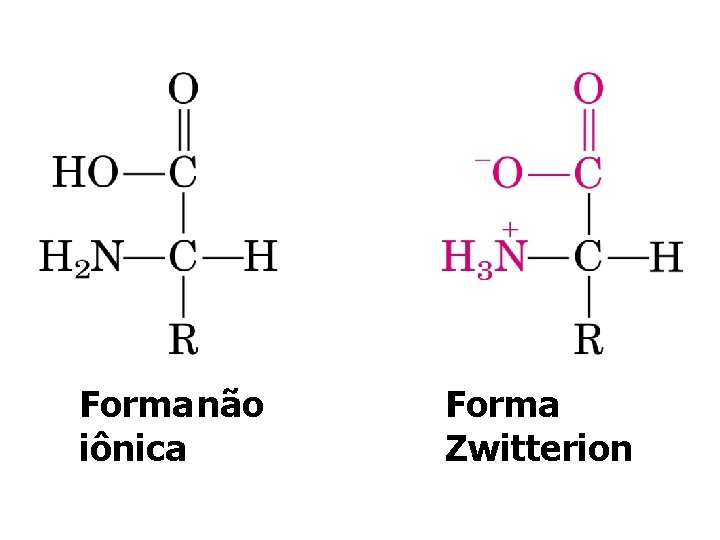
Forma não iônica Forma Zwitterion
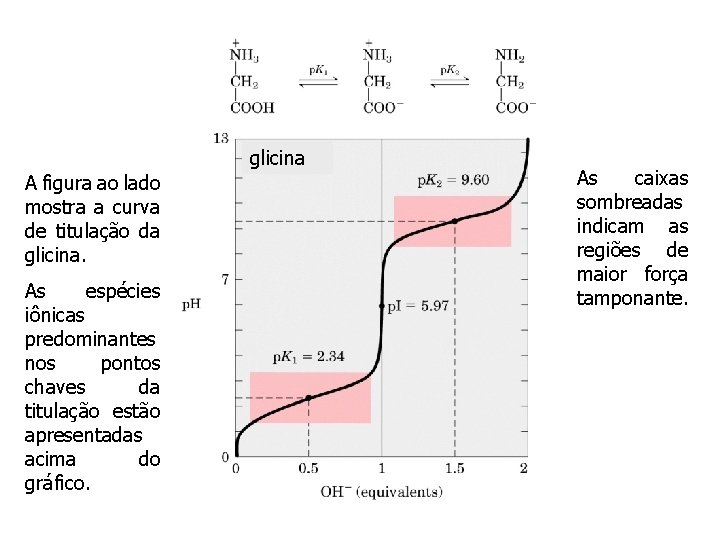
glicina A figura ao lado mostra a curva de titulação da glicina. As espécies iônicas predominantes nos pontos chaves da titulação estão apresentadas acima do gráfico. As caixas sombreadas indicam as regiões de maior força tamponante.
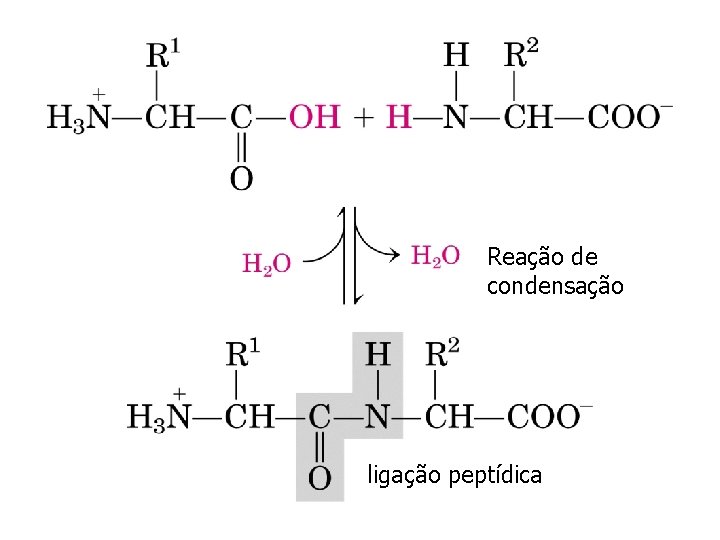
Reação de condensação ligação peptídica
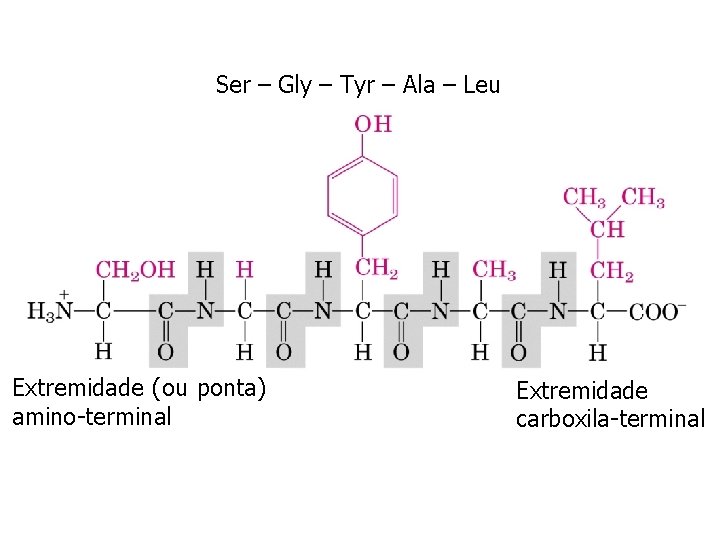
Ser – Gly – Tyr – Ala – Leu Extremidade (ou ponta) amino-terminal Extremidade carboxila-terminal

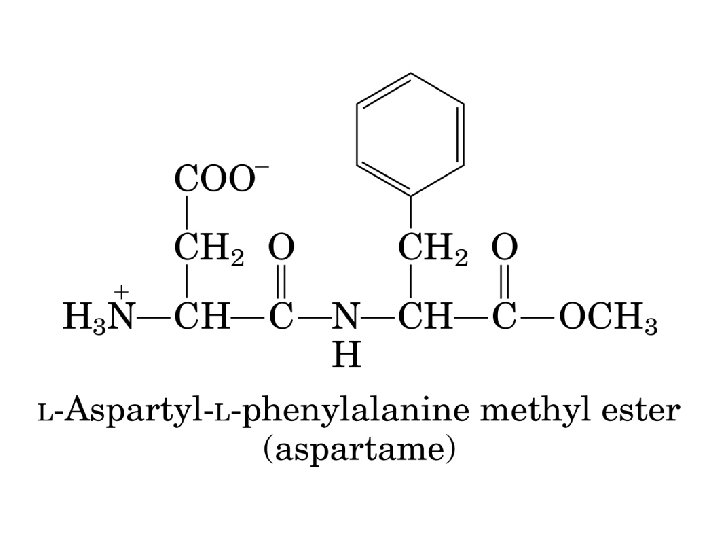

Peptídeos: ü Aspartame: adoçante; 2 resíduos de aa ü Ocitocina: 9 resíduos de aa; estimula contração uterina ü Bradicinina: ü Insulina: 9 resíduos de aa; inibe inflamação 2 cadeias polipeptídicas (30 e 21 aa); ü Glucagon: 29 aa

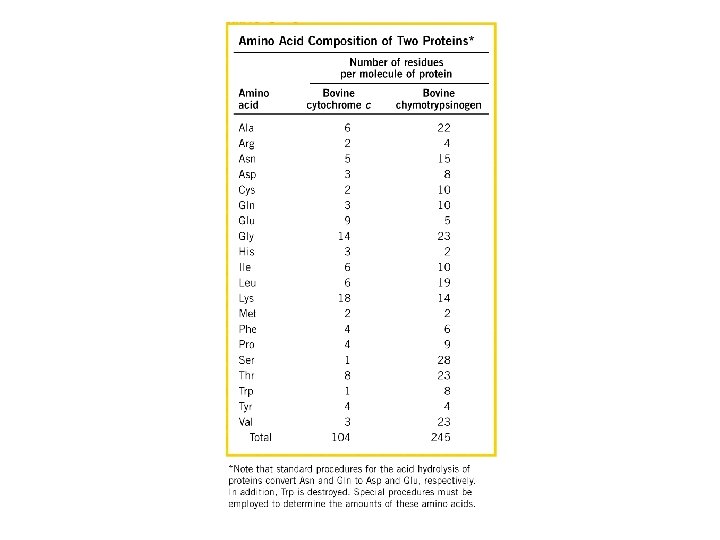
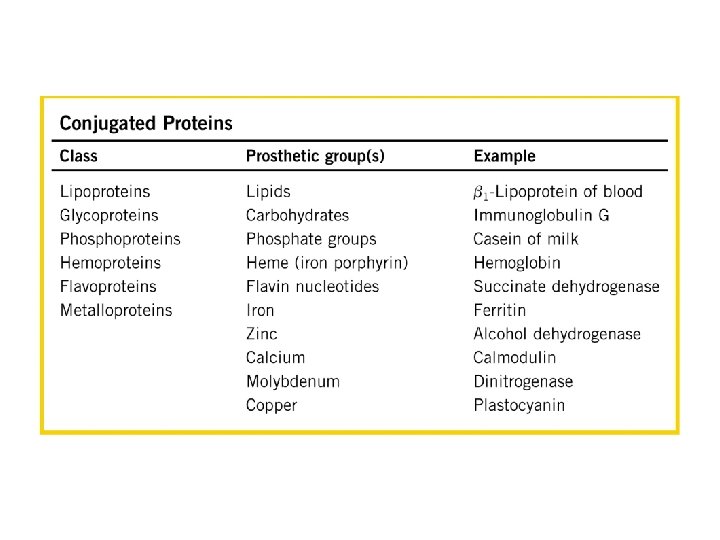

Estrutura primária Resíduos de aminoácidos Está relacionada com todas as ligações covalentes (principalmente ligações peptídicas e pontes dissulfeto) ligando os resíduos de aminoácidos em uma cadeia polipeptídica.
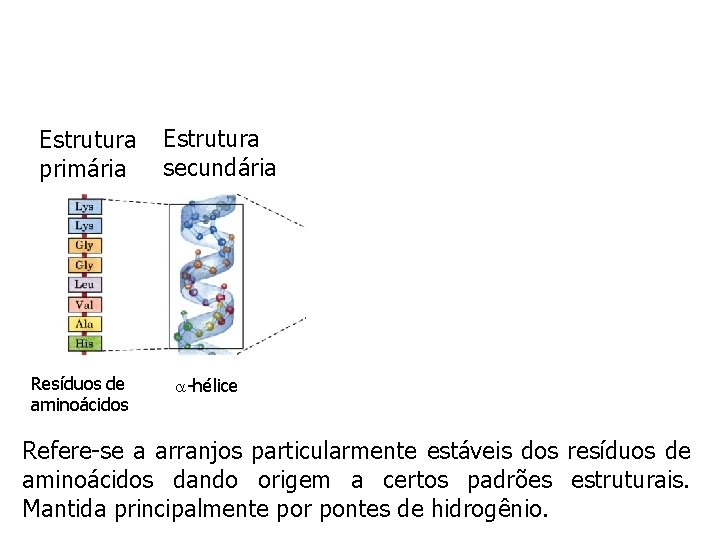
Estrutura primária Resíduos de aminoácidos Estrutura secundária -hélice Refere-se a arranjos particularmente estáveis dos resíduos de aminoácidos dando origem a certos padrões estruturais. Mantida principalmente por pontes de hidrogênio.
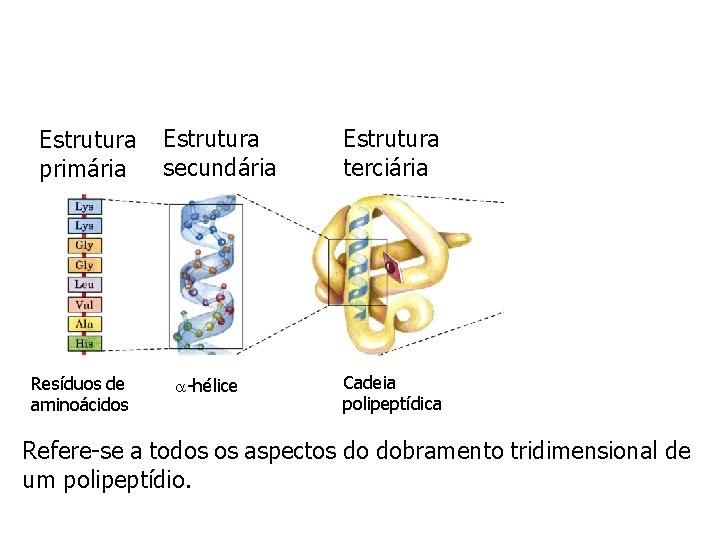
Estrutura primária Resíduos de aminoácidos Estrutura secundária -hélice Estrutura terciária Cadeia polipeptídica Refere-se a todos os aspectos do dobramento tridimensional de um polipeptídio.
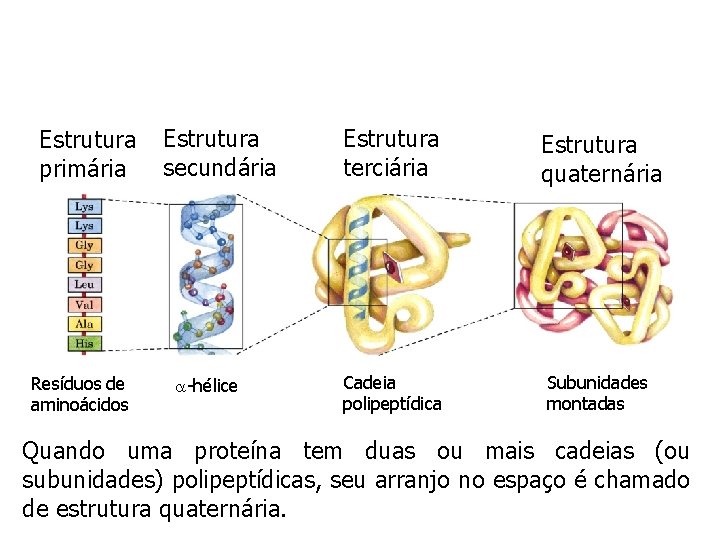
Estrutura primária Resíduos de aminoácidos Estrutura secundária -hélice Estrutura terciária Estrutura quaternária Cadeia polipeptídica Subunidades montadas Quando uma proteína tem duas ou mais cadeias (ou subunidades) polipeptídicas, seu arranjo no espaço é chamado de estrutura quaternária.
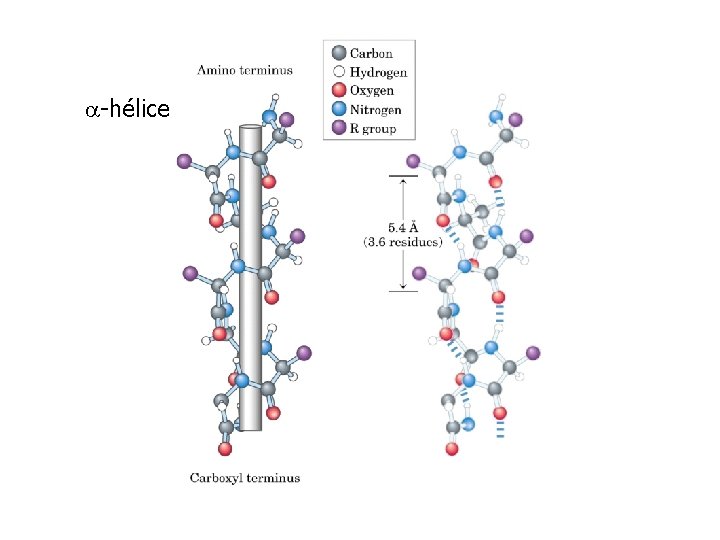
-hélice
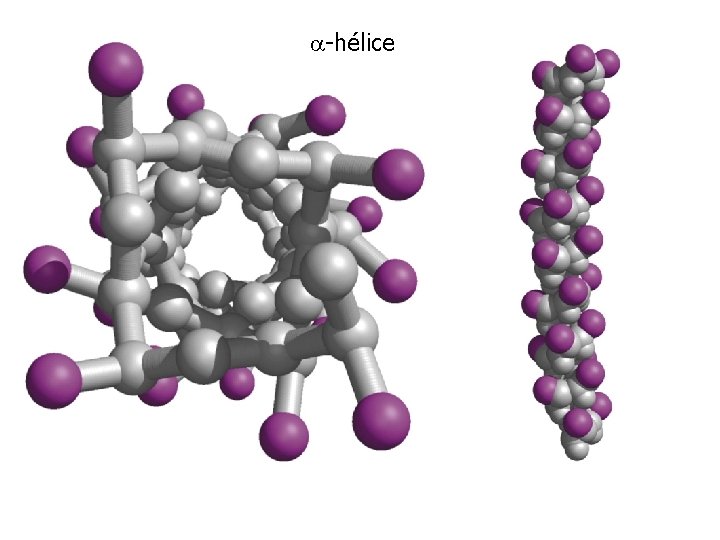
-hélice
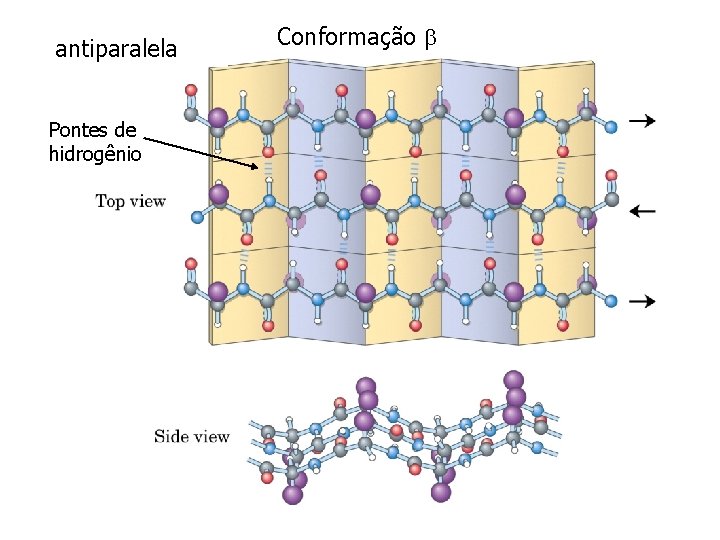
antiparalela Pontes de hidrogênio Conformação
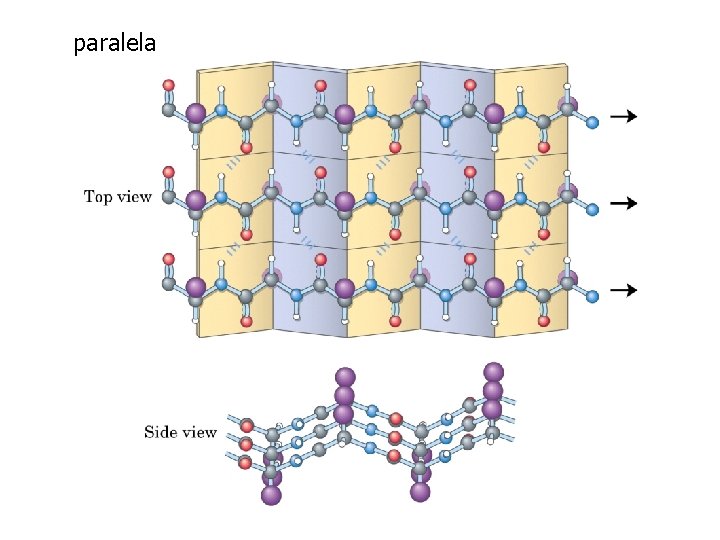
paralela


Albumina sérica humama: 585 resíduos de aa em uma única cadeia

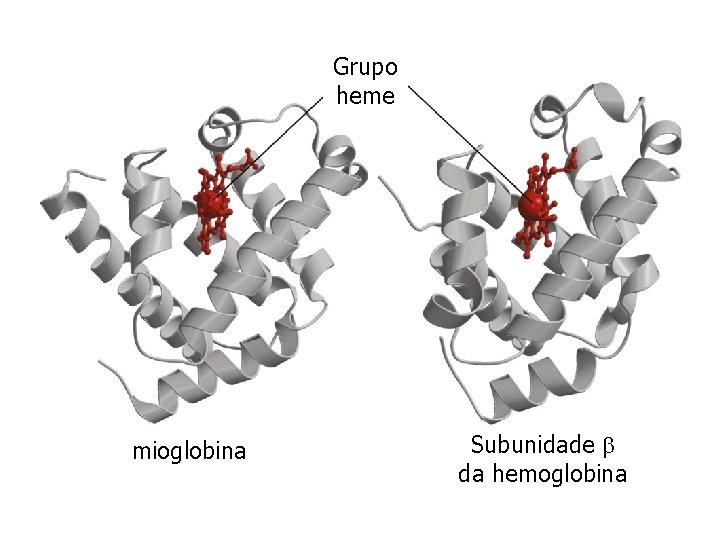
Grupo heme mioglobina Subunidade da hemoglobina


Colágeno ü Qual a sua função? ü Quais são os aminoácidos encontrados nesta proteína? ü Como está organizada secundária? a não-padrões sua estrutura ü E a terciária e quaternária? ü Qual a relação entre ausência de vitamina C e síntese defeituosa do colágeno?

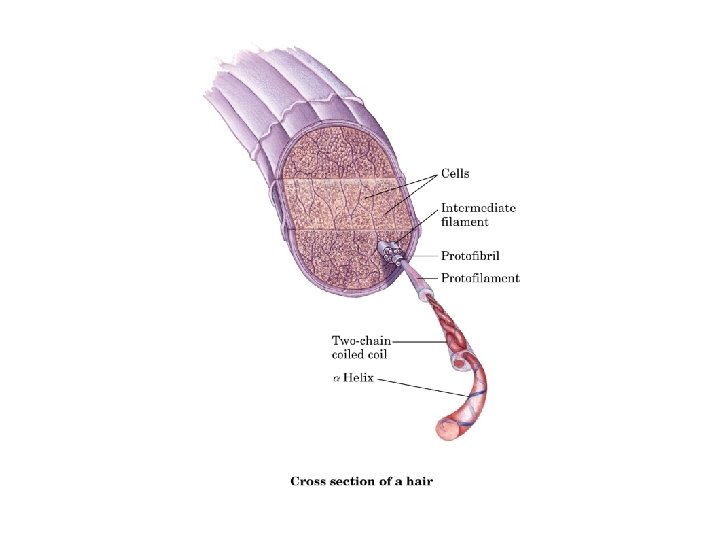
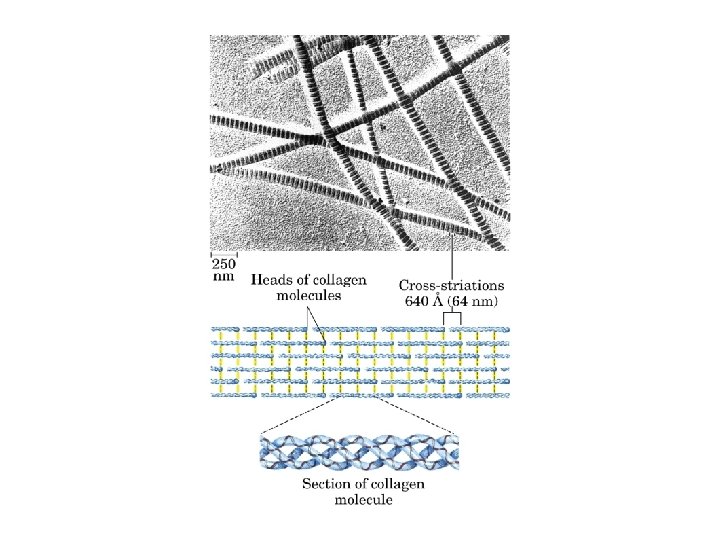
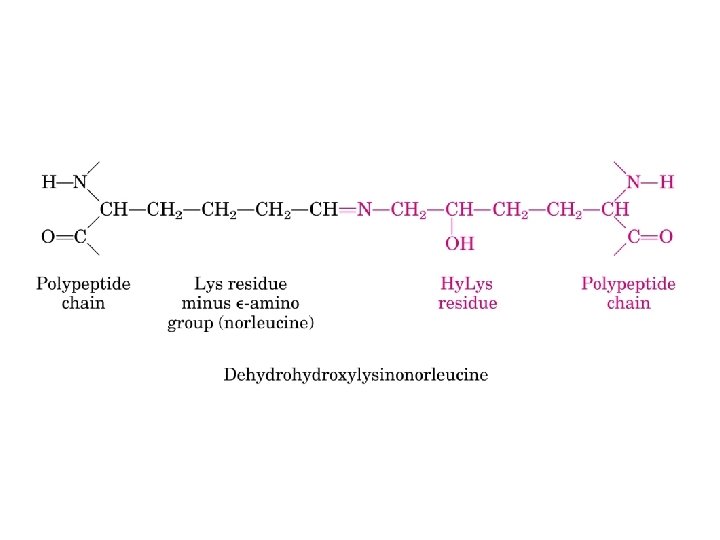
Colágeno ü Função: dar força, encontrado em tecidos conectivos, tais como, tendão, cartilagem, matriz orgânica do osso. ü aminoácidos não-padrões: 4 -hidroxiprolina e 5 -hidroxilisina ü estrutura secundária: hélice voltada para e esquerda. ü Terciária e Quaternária: 3 polipeptídeos separados estão superenrolados.
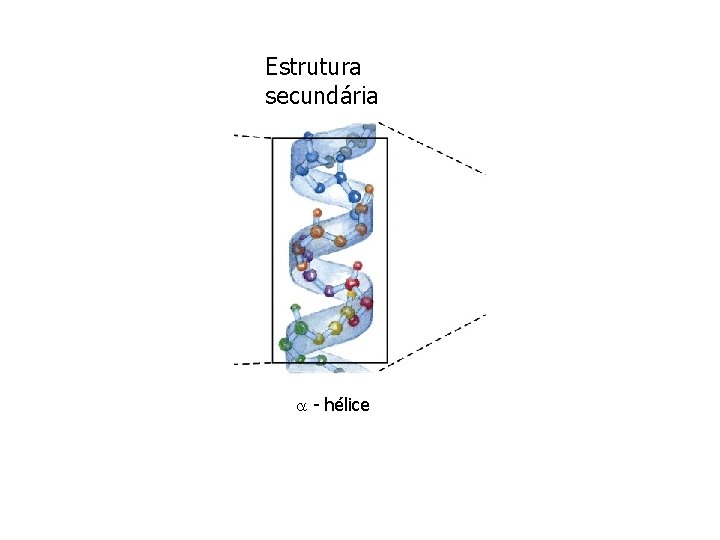
Estrutura secundária - hélice
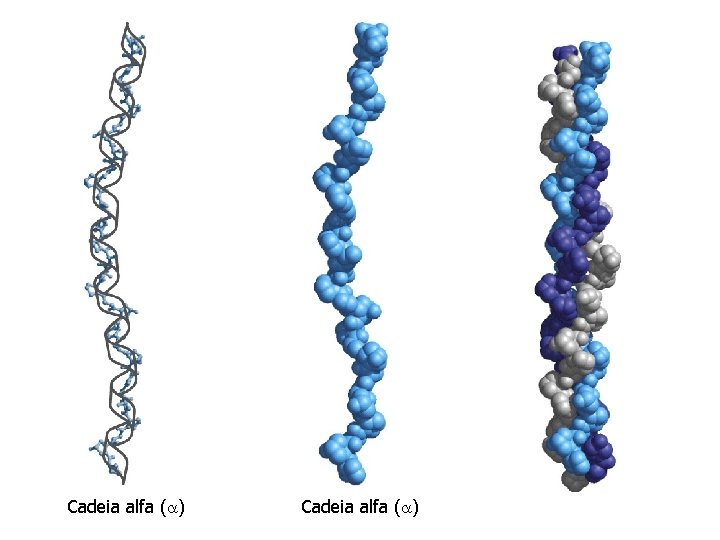
Cadeia alfa ( )

- Slides: 48