Biologisch wichtige organische Verbindungen II M Kresken 1

Biologisch wichtige organische Verbindungen II M. Kresken 1

Proteine M. Kresken 2

Peptide, Proteine • Die Carboxylgruppe einer Aminosäure kann mit einer Aminogruppe einer Aminosäure unter Wasserabspaltung reagieren (Kondensation). • Die Aminosäuren sind durch Carbonsäureamid. Bindungen zwischen -Carboxy- und -Amino. Gruppe verknüpft. • Die Bindung wird als Peptidbindung bezeichnet, in der alle Atome in einer Ebene liegen, d. h. es entstehen Kettenmoleküle. M. Kresken 3
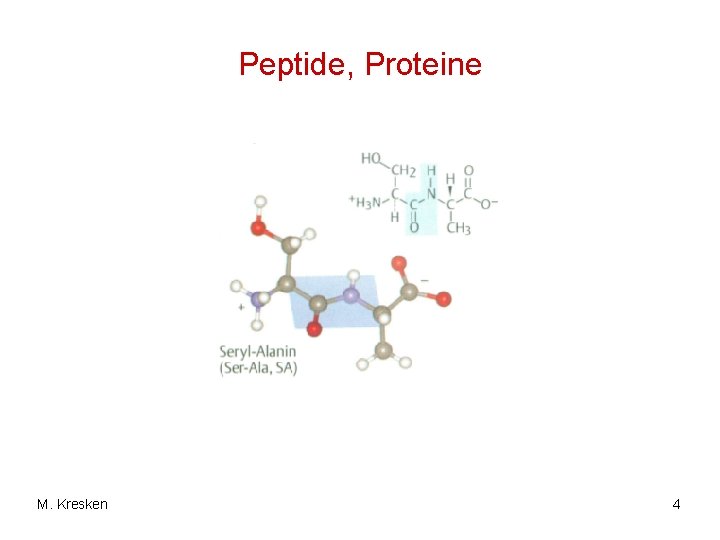
Peptide, Proteine M. Kresken 4
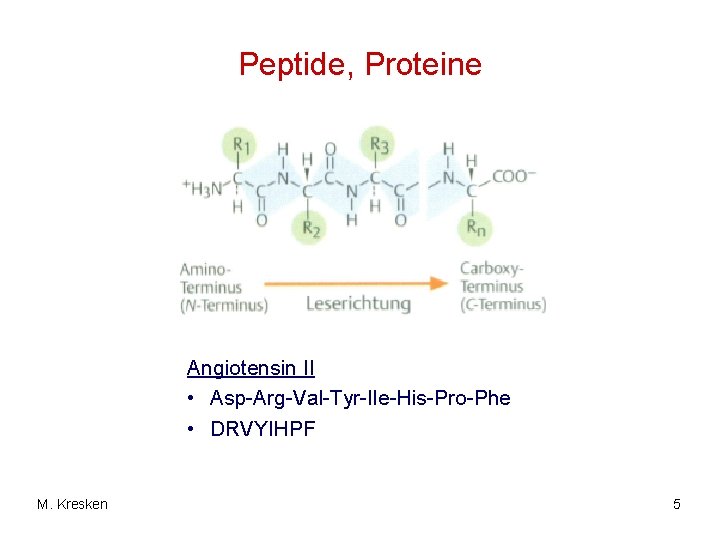
Peptide, Proteine Angiotensin II • Asp-Arg-Val-Tyr-Ile-His-Pro-Phe • DRVYIHPF M. Kresken 5
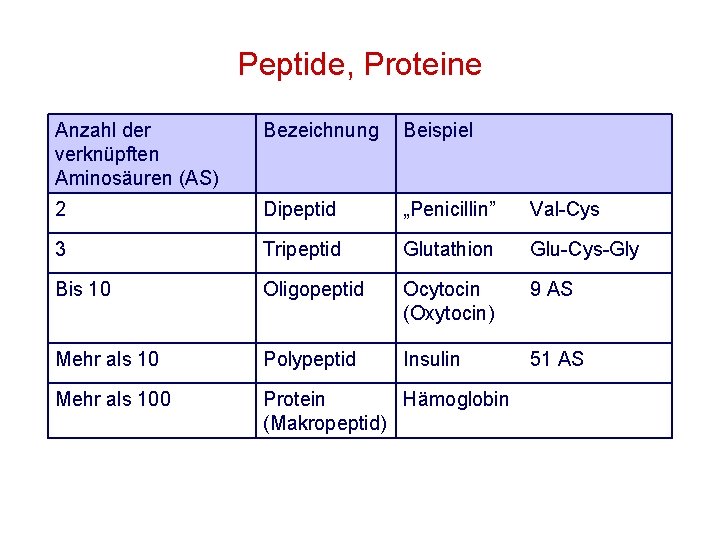
Peptide, Proteine Anzahl der verknüpften Aminosäuren (AS) Bezeichnung Beispiel 2 Dipeptid „Penicillin” Val-Cys 3 Tripeptid Glutathion Glu-Cys-Gly Bis 10 Oligopeptid Ocytocin (Oxytocin) 9 AS Mehr als 10 Polypeptid Insulin 51 AS Mehr als 100 Protein Hämoglobin (Makropeptid)

Struktur der Peptide / Proteine • Proteine sind Moleküle, deren Molekulargewicht 10. 000 bis mehrere Millionen u beträgt. • Da sie sehr spezifische Aufgaben (z. B. als Enzyme) haben, liegen Proteine nicht einfach als Ketten vor. M. Kresken 7

Struktur der Proteine 1. Primärstruktur: • Hierunter versteht man die Aminosäuresequenz -Ala-Gln-Val-Lys-Gly-His-Gly. Lys-Val-Ala-Asp-Ala-Leu. Thr-Asn-Ala-Val-Ala-His-Val. Aminsäurereste 53 -74 der -Untereinheit des Hämoglobins M. Kresken 8

Struktur der Proteine 2. Sekundärstruktur: • Sind durch Wasserstoffbrückenbindungen (H-Brücken) stabilisierte Bereiche der Peptidkette mit definierter Konformation. • Die Teilsequenz ist zu einer α-Helix gefaltet. • Die Peptidkette ist hier schraubenförmig gewunden. • α-Helices werden durch Wasserstoffbrückenbindungen zwischen den NH- und CO-Gruppen von Resten, die in der Sequenz jeweils um 4 Positionen voneinander entfernt sind, stabilisiert. M. Kresken 9
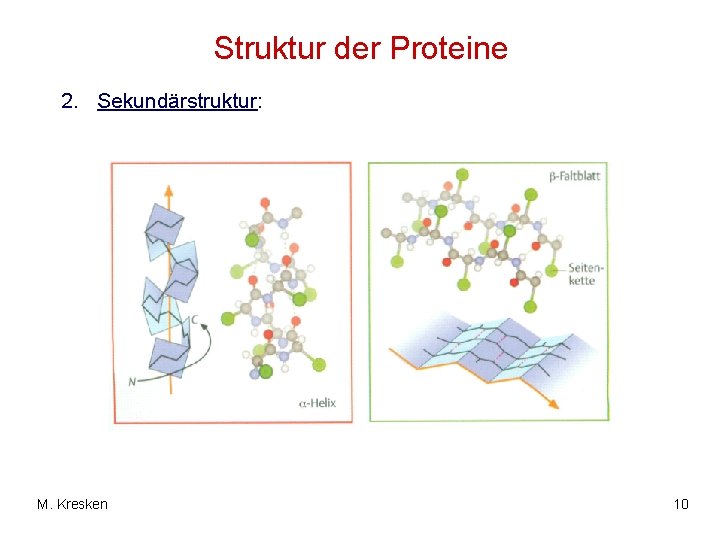
Struktur der Proteine 2. Sekundärstruktur: M. Kresken 10
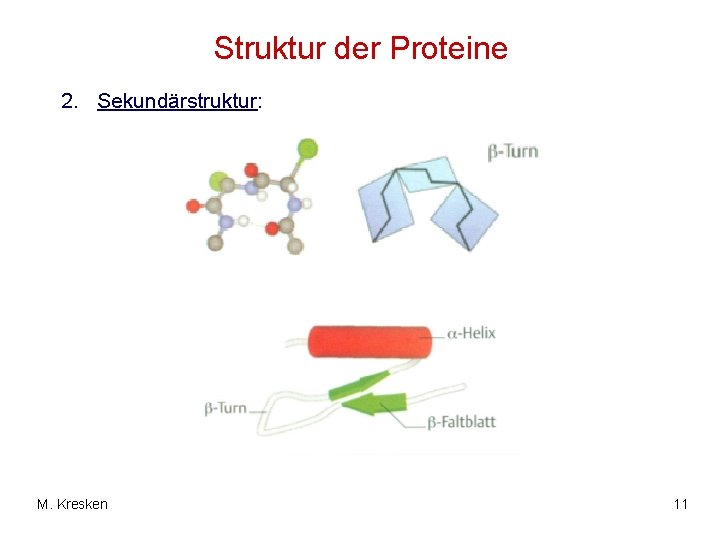
Struktur der Proteine 2. Sekundärstruktur: M. Kresken 11

Struktur der Proteine 3. Tertiärstruktur: • Als Tertiärstruktur bezeichnet man die aus Sekundärstruktur-Elementen und ungeordneten Bereichen aufgebaute, dreidimensionale Konformation eines Proteins. M. Kresken 12

Struktur der Proteine 4. Quartärstruktur: • Viele Proteine lagern sich aufgrund nichtkovalenter Wechselwirkungen zu symmetrischen Komplexen (Oligomeren) zusammen. Die Komponenten oligomerer Proteine (meist 2 -12) bezeichnet man als Untereinheiten oder Monomere. • Im Hämoglobin bilden zwei - (braun) und zwei Untereinheiten (grün) ein Tetramer. M. Kresken 13

Proteine • Man unterscheidet: - Strukturproteine - Lösliche Proteine M. Kresken 14

Strukturproteine • Faserförmige (fibrilläre) Proteine • Verleihen extrazellulären Strukturen mechanische Festigkeit • Sind am Aufbau des Cytoskeletts* beteiligt M. Kresken *Das Cytoskelett dient u. a. dazu, die Form der Zellen aufrecht zu erhalten. 15
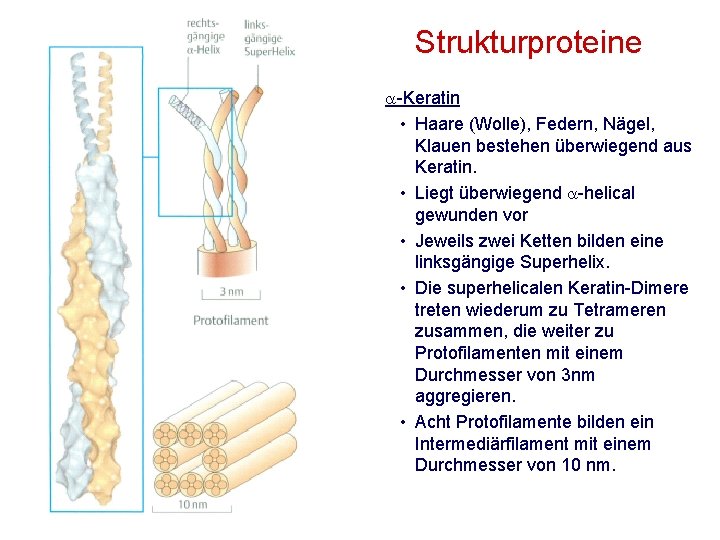
Strukturproteine -Keratin • Haare (Wolle), Federn, Nägel, Klauen bestehen überwiegend aus Keratin. • Liegt überwiegend -helical gewunden vor • Jeweils zwei Ketten bilden eine linksgängige Superhelix. • Die superhelicalen Keratin-Dimere treten wiederum zu Tetrameren zusammen, die weiter zu Protofilamenten mit einem Durchmesser von 3 nm aggregieren. • Acht Protofilamente bilden ein Intermediärfilament mit einem Durchmesser von 10 nm.
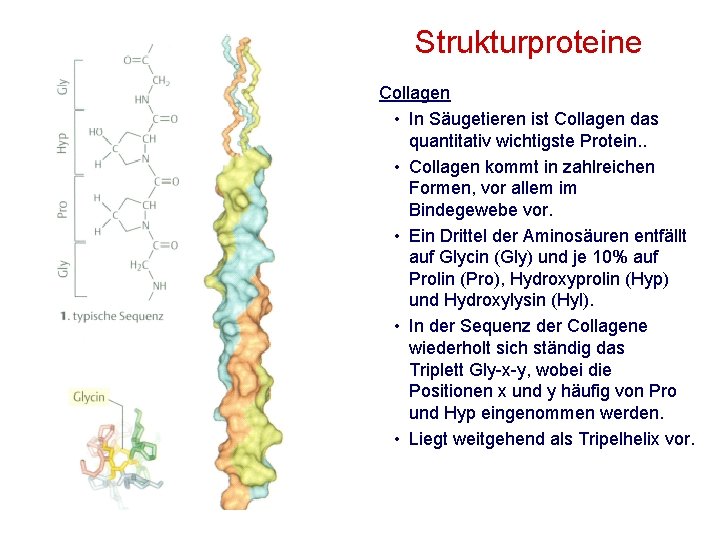
Strukturproteine Collagen • In Säugetieren ist Collagen das quantitativ wichtigste Protein. . • Collagen kommt in zahlreichen Formen, vor allem im Bindegewebe vor. • Ein Drittel der Aminosäuren entfällt auf Glycin (Gly) und je 10% auf Prolin (Pro), Hydroxyprolin (Hyp) und Hydroxylysin (Hyl). • In der Sequenz der Collagene wiederholt sich ständig das Triplett Gly-x-y, wobei die Positionen x und y häufig von Pro und Hyp eingenommen werden. • Liegt weitgehend als Tripelhelix vor.
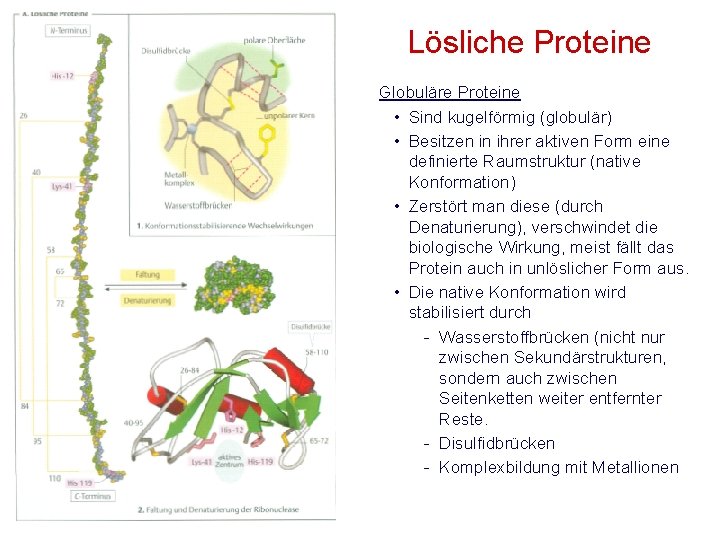
Lösliche Proteine Globuläre Proteine • Sind kugelförmig (globulär) • Besitzen in ihrer aktiven Form eine definierte Raumstruktur (native Konformation) • Zerstört man diese (durch Denaturierung), verschwindet die biologische Wirkung, meist fällt das Protein auch in unlöslicher Form aus. • Die native Konformation wird stabilisiert durch - Wasserstoffbrücken (nicht nur zwischen Sekundärstrukturen, sondern auch zwischen Seitenketten weiter entfernter Reste. - Disulfidbrücken - Komplexbildung mit Metallionen

Lösliche Proteine Globuläre Proteine II • Besonders wichtig für die Proteinstabilität ist der hydrophobe Effekt • In der nativen Form sind die meisten hydrophoben Aminosäurereste im Inneren der Struktur angeordnet, während die Mehrzahl der polaren Aminosäuren in Kontakt mit dem umgebenden Wasser auf der Oberfläche liegt. • Zur Denaturierung kommt es bei extremen p. H-Werten, hohen Temperaturen, oder Einwirkung von organischen Lösungen, Detergenzien u. a. Substanzen, z. B. Harnstoff. • Rückkehr zur nativen Form möglich (Bsp. Ribunuclease)
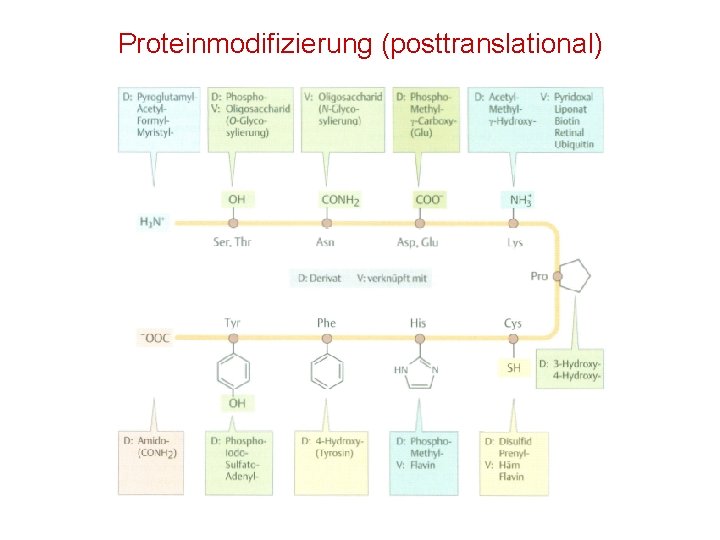
Proteinmodifizierung (posttranslational)

Proteinmodifizierung (posttranslational) • Findet meist im Endoplasmatschen Retikulum statt • Man schätzt, dass im tierischen Organismus 80% aller Proteine Nterminal acyliert werden, wobei lösliche Proteine meist acetyliert sind. • Glykolisiert werden vor allem extrazelluläre Proteine (z. B. Plasmaproteine [außer Albumin]). • Bei Plasmaproteinen dient die Glykolisierung der Erkennung durch Rezeptoren in der Leber, bei Mucinen (Schleimstoffen) erhöht sie die Wasserbindungsfähigkeit. • Die Phosphorylierung (und Dephosphorylierung) spielt bei der Regulation von Stoffwechsel, Zellproliferation und Zelldifferenzierung eine Rolle. • Die Acetylierung der -Aminogruppe des Lysins ist ein wichtiger Mechanismus zur Kontrolle der Genaktivität. • Auch viele Coenzyme und Cofaktoren sind kovalent mit Lysin verbunden. M. Kresken 21

Funktionen der Proteine • Strukturproteine sind für Form und Stabilität von Zellen verantwortlich. • Transportproteine - Hämoglobin der Erythrozyten (Transport von Sauerstoff und Kohlendioxid zwischen Lunge und den Geweben) - Albumine im Blutplasma transportieren körpereigene und körperfremde Substanzen. - Ionenkanäle und andere integrale Membranproteine vermitteln den Transport von Ionen und Metaboliten durch Membranen. • Abwehrproteine (Immunglobuline, Antikörper) unterstützen die spezifische Immunabwehr. M. Kresken 22

Funktionen der Proteine • Regulatorische Proteine wirken als Signalstoffe (Hormone) oder Rezeptoren. • Katalytische Proteine (Enzyme) - > 2. 000 bekannte Vertreter - Massen von 10 -15 k. Da bis > 500 k. Da • Motorproteine - das Zusammenspiel von Actin und Myosin ist für die Muskelkontraktion verantwortlich. • Speicherproteine – 6 kg Muskelprotein können in Hungerphasen als Nährstoffreserve zur Verfügung gestellt werden. M. Kresken 23
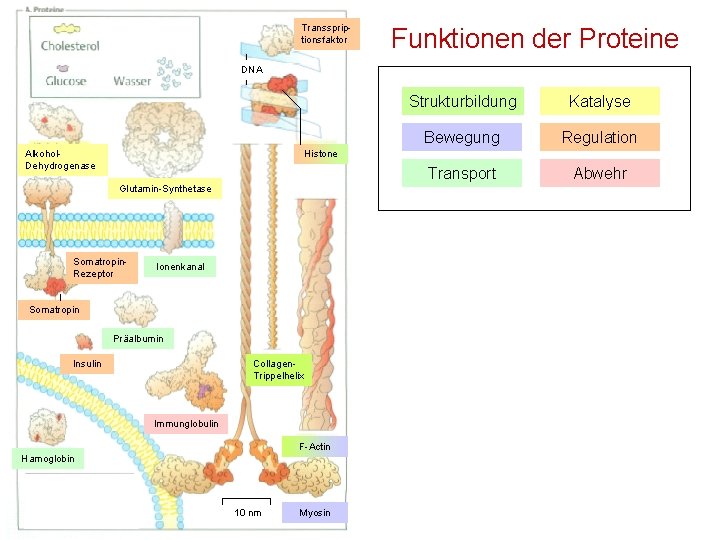
Transspriptionsfaktor Funktionen der Proteine DNA Alkohol. Dehydrogenase Strukturbildung Katalyse Bewegung Regulation Transport Abwehr Histone Glutamin-Synthetase Somatropin. Rezeptor Ionenkanal Somatropin Präalbumin Insulin Collagen. Trippelhelix Immunglobulin F-Actin Hamoglobin 10 nm Myosin

Zusammengesetzte Proteine • Mit Zucker - Glycoproteine • Mit Lipiden - Lipoproteine • Häm - Hämoglobin M. Kresken 25

Glykoproteine • Proteine an der Oberfläche der Plasmamembran sind meist, cytoplasmatische Proteine selten glycosyliert. • Können mehr als 70% Kohlenhydrat enthalten M. Kresken 26
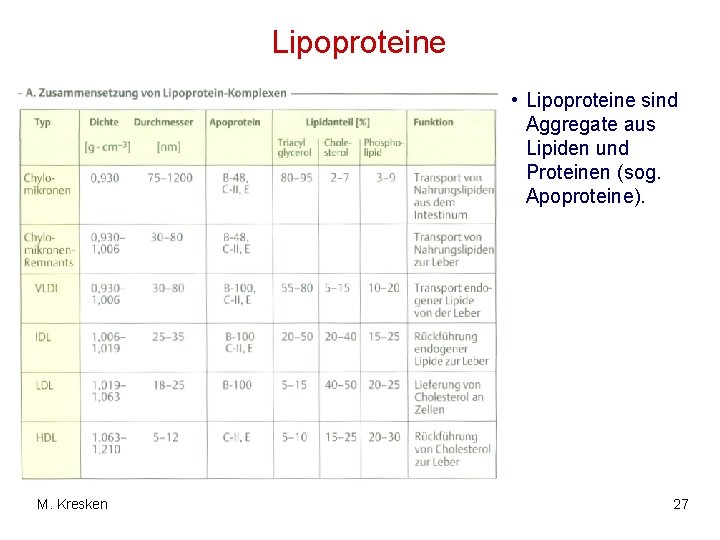
Lipoproteine • Lipoproteine sind Aggregate aus Lipiden und Proteinen (sog. Apoproteine). M. Kresken 27
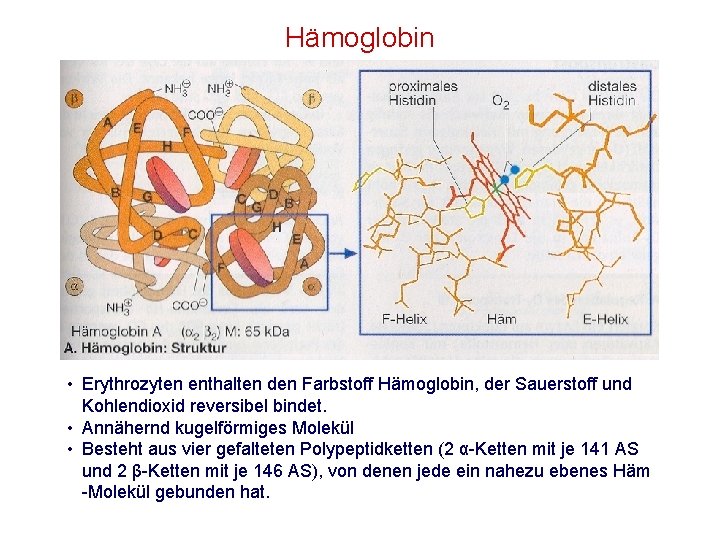
Hämoglobin • Erythrozyten enthalten den Farbstoff Hämoglobin, der Sauerstoff und Kohlendioxid reversibel bindet. • Annähernd kugelförmiges Molekül • Besteht aus vier gefalteten Polypeptidketten (2 α-Ketten mit je 141 AS und 2 β-Ketten mit je 146 AS), von denen jede ein nahezu ebenes Häm -Molekül gebunden hat.

Enzyme • Enzyme sind Biokatalysatoren, die chemische Reaktionen beschleunigen. - Es gibt auch Biokatalysatoren, die keine Enzyme sind (Ribozyme, katalytisch aktive RNA) • Jede Zelle verfügt über eine eigenetisch festgelegte Enzymausstattung, über die koordinierte Reaktionsfolgen entstehen (Stoffwechselwege). • Enzyme sind auch an Regulationsmechanismen beteiligt, die auf diese Weise den Stoffwechsel an veränderte Bedingungen anpassen. M. Kresken 29

Spezifität der Enzyme • Die Wirkung der meisten Enzyme ist hochspezifisch. • Dies bezieht sich auf den Typ der katalysierten Reaktion (Wirkungsspezifität) wie auch auf die Art der Verbindungen, die sie katalysieren (Substratspezifität). • Außerdem sind die meisten Enzyme in der Lage zwischen Stereoisomeren zu unterscheiden (Stereospezifität). M. Kresken 30
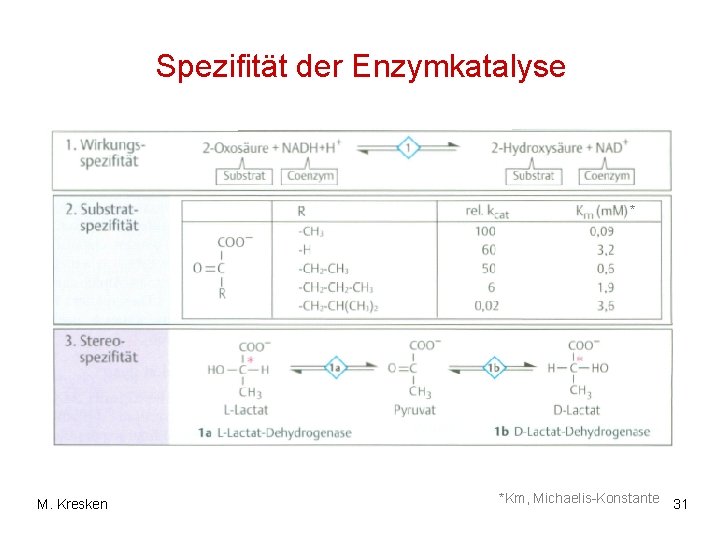
Spezifität der Enzymkatalyse * M. Kresken *Km, Michaelis-Konstante 31

Klassifizierung der Enzyme • Sechs Hauptklassen, Unterklassen • EC-Nummer • Lactatreductase (1. 1. 1. 27) • Klasse 1: Oxidreduktasen • 1. 1. CH – OH-Gruppe als Elektronendonator • 1. 1. 1. NAD(P)+ als Akzeptor M. Kresken 32

Klassifizierung der Enzyme • Der Name eines Enzyms setzt sich aus drei Teilen zusammen: - Name des umgesetzten Substrats - Art der katalysierten Reaktion - Silbe -ase als Endung Þ Lactat-Dehydrogenase M. Kresken 33

Klassifizierung der Enzyme • Oxidreduktasen (Klasse 1) katalysieren Redox-Reaktionen; Übertragung von Elektronen • Transferasen (Klasse 2) übertragen Gruppen, z. B. Amino-Gruppen, Phosphat-Reste - Enzyme der Klassen 1 und 2 benötigen stets Coenzyme • Hydrolasen (Klasse 3) übertragen Gruppen; Akzeptor ist kein Coenzym, sondern ein Wassermolekül • Lyasen (Klasse 4) (je nach bevorzugter Reaktionsrichtung auch als „Synthasen“ bezeichnet) katalysieren die Spaltung oder Bildung chemischer Bindungen. Dabei können Doppelbindungen entstehen oder verschwinden. • Isomerasen (Klasse 5) verschieben Gruppen innerhalb eines Moleküls; keine Änderung der Summenformel • Ligasen (Klasse 6, „Synthetasen“) katalysieren Verknüpfungsreaktionen; sind energetisch an die Spaltung von Nucleosidtriphosphaten (meist ATP) gekoppelt M. Kresken 34
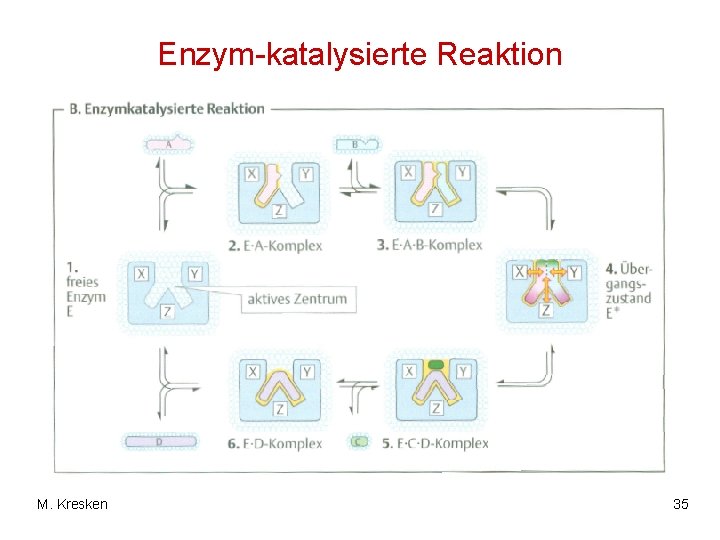
Enzym-katalysierte Reaktion M. Kresken 35

Coenzyme, Cofaktoren • Enzyme, die Gruppenübertragungsreaktionen katalysieren, benötigen in der Regel Coenzyme • Da Coenzyme selbst nicht katalytisch aktiv sind, ist der weniger gebräuchliche Begriff „Cosubstrate“ zutreffender. - Lösliche Coenzyme werden während der Reaktion wie Substrate gebunden, chemisch verändert und wieder frei gesetzt. - Als prosthetische Gruppen bezeichnet man dagegen Coenzyme, die fest an ein Enzym gebunden sind und dieses während der Reaktion nicht verlassen. • Viele Coenzyme sind aromatische Verbindungen, die von tierischen Zellen nicht von Grund auf synthetisiert werden. Ihre Vorstufen müssen daher als Vitamine mit der Nahrung zugeführt werden. • Auch Metall-Ionen können als Cofaktoren von Enzymen dienen. Manche stabilisieren die native Konformation des akiven Zentrums, andere beteiligen sich an Redox-Reaktionen (Spurenelemente). M. Kresken 36

Coenzyme (Auswahl) • Redox-Coenzyme - NAD(P)+/NADH(P) (übertragen Hydrid-Ionen – 2 e- und 1 H+) - Flavine (2 e- / 2 H+), Ubichinon – Coenzym Q (2 e- / 2 H+), Ascorbinsäure – Vitamin C (2 e- / 2 H+), Liponamid (2 e- / 2 H+), Häm (1 e-) • Gruppen-übertragende Coenzyme - Nucleosidphoshate - Übertragung von Phosphatresten (Phosphorilierung) - Coenzym A (enthält Pantothenat) – Übertragung von Acylresten - Tetrahydrofolat – Übertragung von C 1 -Gruppen M. Kresken 37
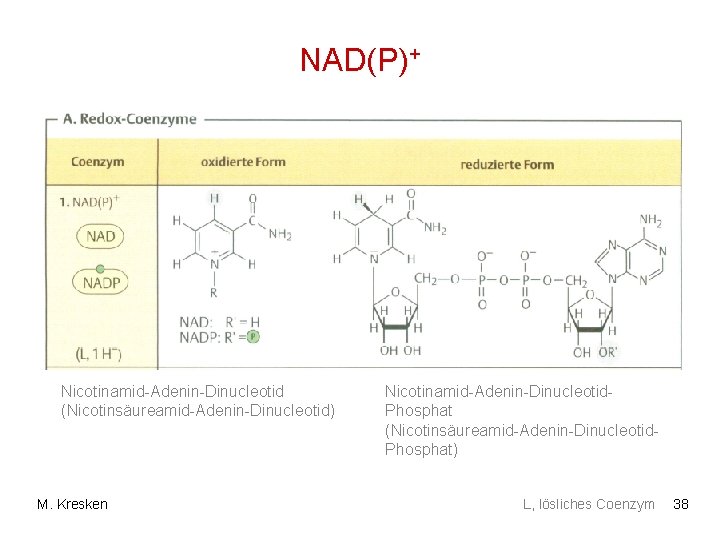
NAD(P)+ Nicotinamid-Adenin-Dinucleotid (Nicotinsäureamid-Adenin-Dinucleotid) M. Kresken Nicotinamid-Adenin-Dinucleotid. Phosphat (Nicotinsäureamid-Adenin-Dinucleotid. Phosphat) L, lösliches Coenzym 38
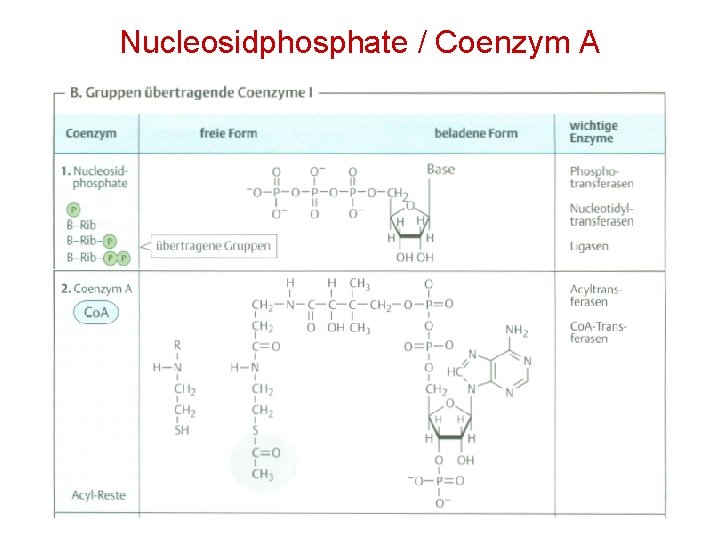
Nucleosidphosphate / Coenzym A
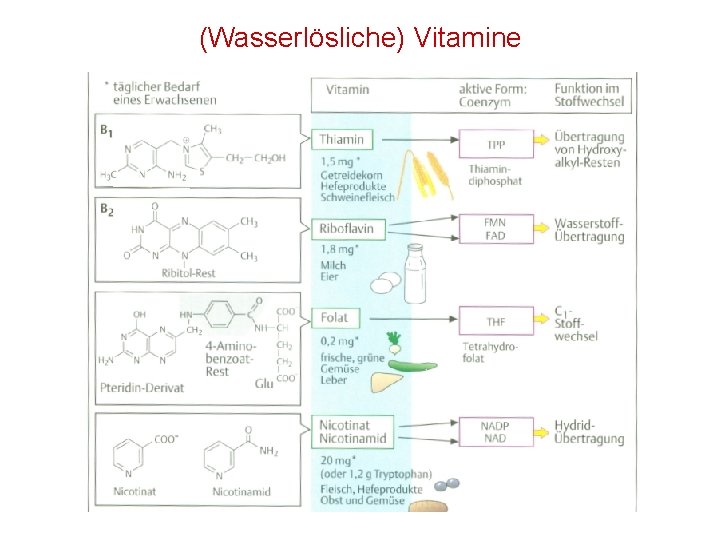
(Wasserlösliche) Vitamine
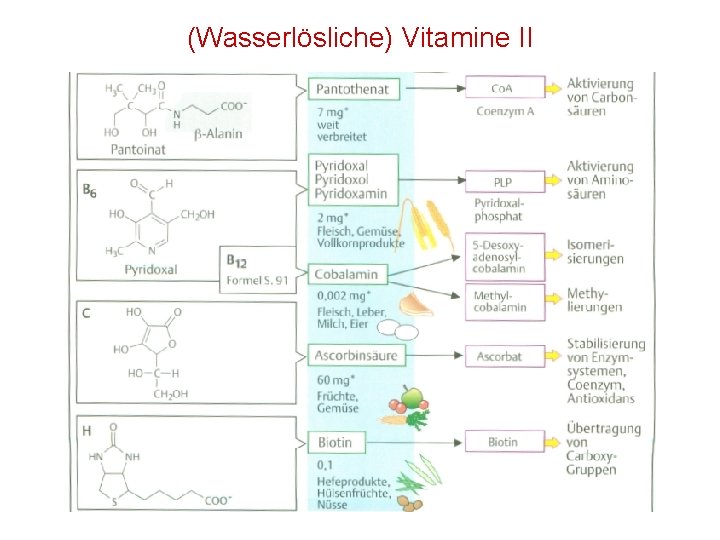
(Wasserlösliche) Vitamine II
- Slides: 41