Lezione 3 Proteine Livelli strutturali delle proteine 06032019




























- Slides: 53

Lezione 3 Proteine Livelli strutturali delle proteine 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 0

Capitolo 3 Amminoacidi, peptidi e proteine

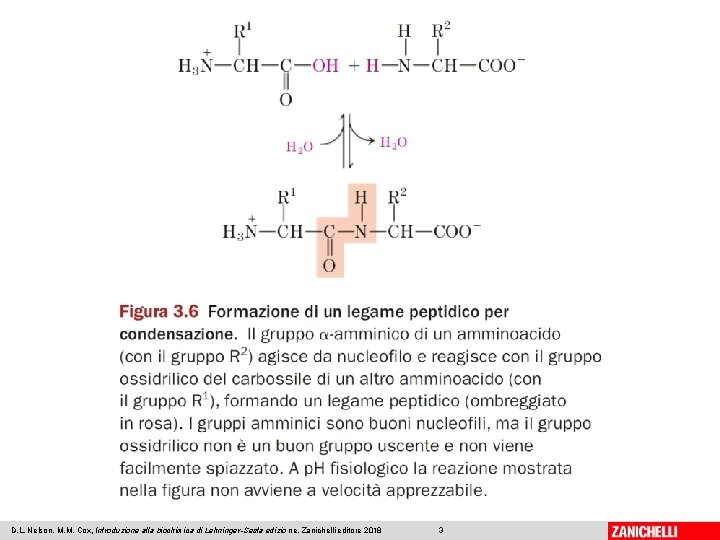
I polimeri degli amminoacidi • peptidi – dipeptidi, tripeptidi, tetrapeptidi, … oligopeptidi • polipeptidi o proteine – decine, centinaia, migliaia di amminoacidi • Due o più amminoacidi formano un legame peptidico, mediante una reazione di CONDENSAZIONE (e quindi uscita di una molecola d’acqua) 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 2

D. L. Nelson, M. M. Cox, Introduzione alla biochimica di Lehninger-Sesta edizio ne, Zanichelli editore 2018 3

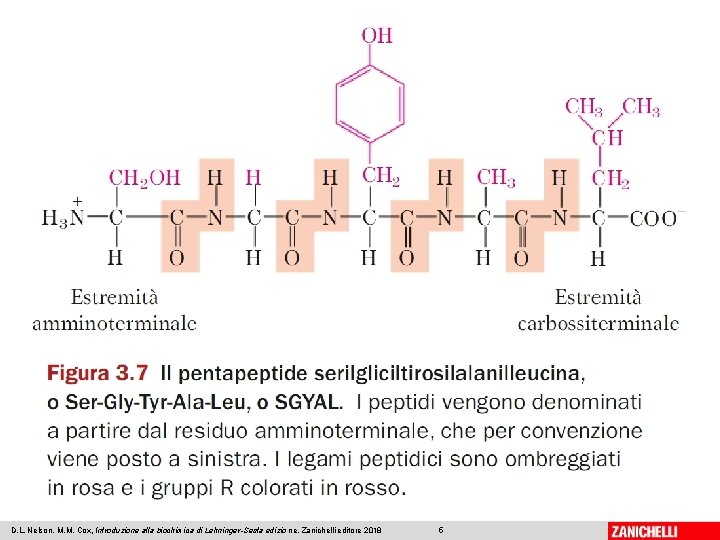
I nomi dei peptidi • Per convenzione l’amminoacido n. 1 è quello ammino-terminale • I nomi degli amminoacidi dei polipeptidi hanno il suffisso –ile (-il) al posto dell’ultima sillaba – – glicina glicil, glutammatao glutammil, aspartato aspartil, tirosina tirosil • L’amminoacido carbossiterminale mantiene il suo nome 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 4

D. L. Nelson, M. M. Cox, Introduzione alla biochimica di Lehninger-Sesta edizio ne, Zanichelli editore 2018 5

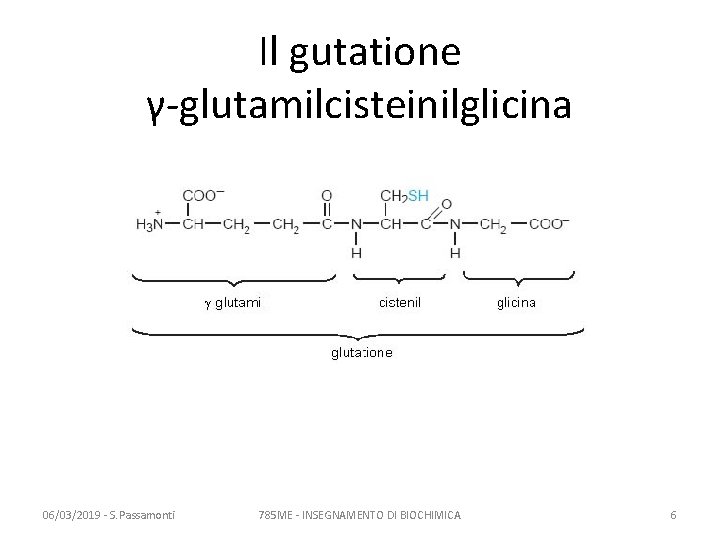
Il gutatione γ-glutamilcisteinilglicina 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 6

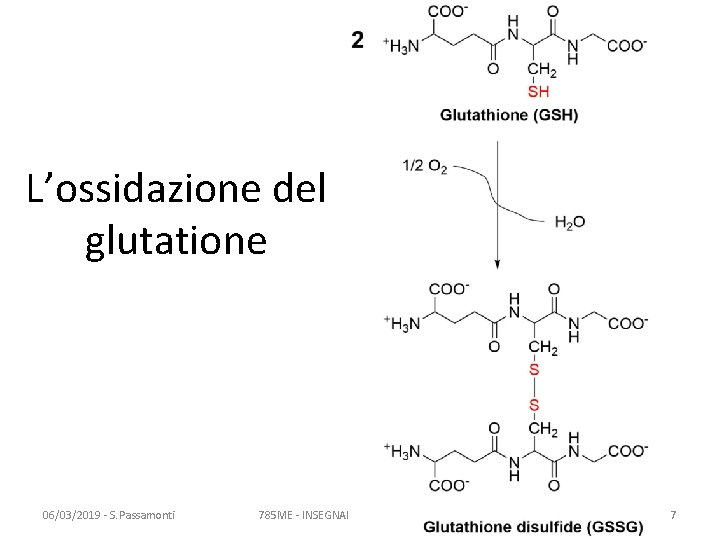
L’ossidazione del glutatione 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 7

Importanti caratteristiche dei (poli)peptidi • I legami peptidici sono stabili – vita media (t 1/2) = 7 anni – Le proteine sono però danneggiate dalle specie radicaliche • Possono ionizzarsi solo i gruppi ammino- e carbossiterminale – i gruppi impegnati nei legami peptici non ionizzano • I gruppi R degli amminoacidi peptidici possono ionizzarsi • La lunghezza dei polipeptidi è molto variabile – in genere circa 2000 amminoacidi 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 8

Le proteine si possono associare Gli assortimenti nelle proteine • singolo polipeptide • due, tre, quattro polipeptidi (o sub-unità) uguali – omodimero, omotrimero, omotetramero • due, tre, quattro polipeptidi (o sub-unità) diversi – eterodimero, eterotrimero, eterotetramero 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 9

Le proteine coniugate Alcune proteine legano dei GRUPPI PROSTETICI: ioni, gruppi chimici o molecole non proteiche 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 10

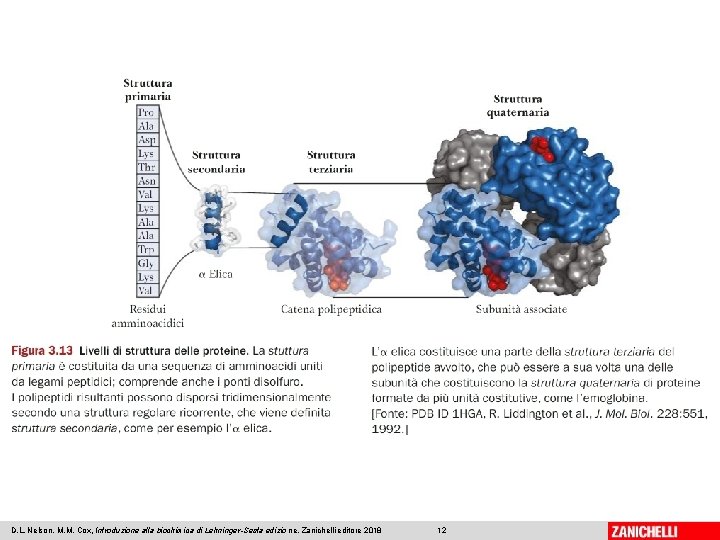
I livelli strutturali delle proteine • Struttura primaria – sequenza degli amminoacidi, legati mediante legame peptidico • Struttura secondaria – moduli strutturali ricorrenti (α-elica, foglietto β, …) che interessano solo alcune brevi sequenze all’interno del polipeptide • Struttura terziaria – struttura tridimensionale di tutto il polipeptide • Struttura quaternaria – struttura multimerica (aggregazione di sub-unità proteiche) 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 11

D. L. Nelson, M. M. Cox, Introduzione alla biochimica di Lehninger-Sesta edizio ne, Zanichelli editore 2018 12

Cosa si può dedurre dalla struttura primaria? • Le sequenze amminoacidiche sono depositate nelle banche dati – es. : ww. uniprot. org • Le sequenze si possono confrontare, per allineamento, grazie agli strumenti della Bioinformatica • Il grado di omologia (identità di sequenza) tra proteine diverse suggerisce relazioni genomiche o funzionali 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 13

Le proteine sono codificate da geni • La struttura primaria delle proteine corrisponde alla struttura primaria del DNA – ad una sequenza amminoacidica corrisponde una sequenza nucleotidica – il codice genetico consente di tradurre una sequenza nucleotidica in sequenza amminoacidica • Il genoma umano contiene circa 20. 000 geni che codificano almeno 20. 000 proteine – il proteoma (l’insieme delle proteine) umano non è ancora del tutto noto, per limiti analitici. 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 14

Le famiglie proteiche • Comprendono proteine che hanno: – omologie di sequenza amminoacidica – stessa o simile funzione TERMINOLOGIA Proteine omologhe = Omologhi • Famiglie proteiche possono essere presenti in molte specie diverse – Paraloghi = omologhi espressi nella stessa specie – Ortologhi = omologhi espressi in specie diverse 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 15

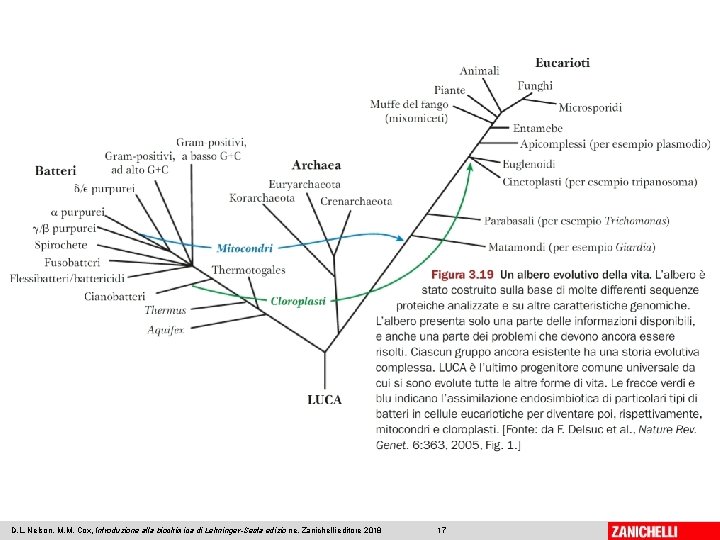
L’evoluzione molecolare • I geni che esprimono le proteine possono mutare da una generazione all’altra • L’evoluzione delle specie viventi ha portato ad avere genomi diversi • Si può immaginare un antenato comune 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 16

D. L. Nelson, M. M. Cox, Introduzione alla biochimica di Lehninger-Sesta edizio ne, Zanichelli editore 2018 17

La classificazione delle proteine • Le proteine si possono aggregare in gruppi in funzione dell’omologia di sequenza e similitudine di funzione • I gruppi sono: – FAMIGLIE – DOMINI – SEQUENZE 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 18

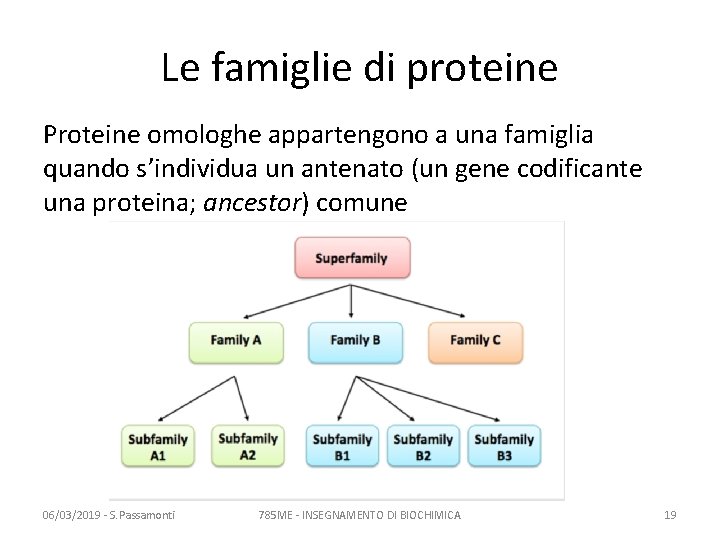
Le famiglie di proteine Proteine omologhe appartengono a una famiglia quando s’individua un antenato (un gene codificante una proteina; ancestor) comune 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 19

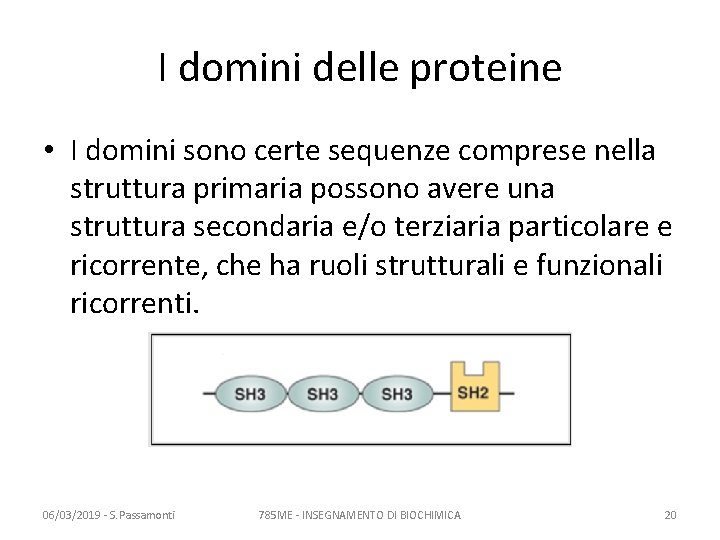
I domini delle proteine • I domini sono certe sequenze comprese nella struttura primaria possono avere una struttura secondaria e/o terziaria particolare e ricorrente, che ha ruoli strutturali e funzionali ricorrenti. 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 20

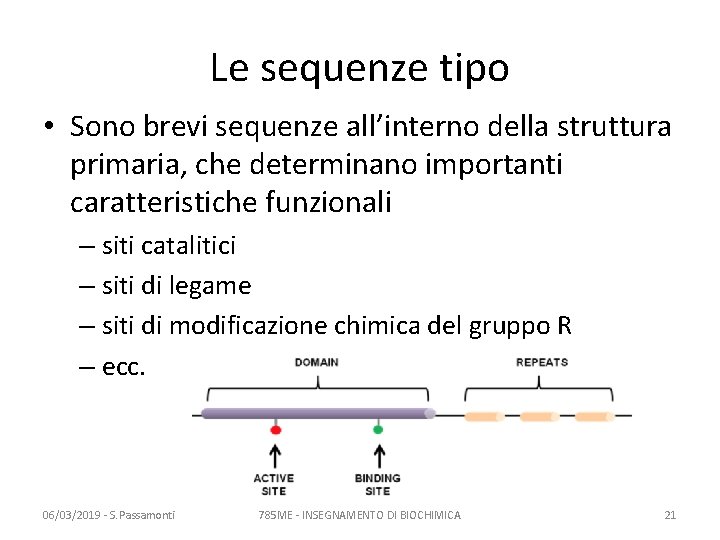
Le sequenze tipo • Sono brevi sequenze all’interno della struttura primaria, che determinano importanti caratteristiche funzionali – siti catalitici – siti di legame – siti di modificazione chimica del gruppo R – ecc. 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 21

Capitolo 4 Struttura tridimensionale delle proteine

La conformazione delle proteine • La conformazione è la struttura tridimensionale di una proteina – Un polipeptide è un filamento flessibile e può assumere (“disegnare”) teoricamente un numero enorme di forme (conformazioni) – ciò è possibile grazie alla rotazione degli atomi intorno ai legami • Le conformazioni più probabili (possibili) sono caratterizzate dalla minor energia libera di Gibbs, G, (en. potenziale, che può compiere lavoro) 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 23

Le conformazioni ripiegate sono più stabili • Le conformazioni lineari sono quelle associate alla maggior energia libera, a causa del massimo numero di interazioni possibili con l’acqua (entropia). • Quando un polipeptide si ripiega e si formano legami deboli intra-molecolari, questi sostituiscono i legami H con l’acqua, diminuisce l’entropia e così l’energia libera • Anche i legami disolfuro tra gruppi R delle cisteine contribuiscono a questa stabilizzazione conformazionale 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 24

Le forze del ripiegamento dei polipeptidi (cont. ) • I gruppi R apolari (Leu, Ile, Val, Phe, Trp) interagiscono tra di loro per effetto idrofobico e guidano il ripiegamento • Si forma un nucleo centrale apolare, da cui l’acqua è esclusa – diminuisce l’entropia • In questo nucleo apolare, gli atomi possono interagire grazie alle forze di van der Waals, e ciò stabilizza la conformazione 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 25

(cont. ) Le forze del ripiegamento dei polipeptidi • I gruppi R polari interagiscono con legami idrogeno • I gruppi R carichi interagiscono con legami elttrostatici • La superficie del polipeptide ripiegato interagisce con l’acqua mediante legami idorgeno 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 26

I limiti al ripiegamento dei polipeptidi • Il polipeptide ha una catena principale, costituita da gruppi peptidici che si ripetono -Cα-C-N-Cα-C-N-Cα • Gli atomi della catena principale dei polipeptidi NON sono completamente liberi di ruotare • Perché? vedi schema successivo 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 27

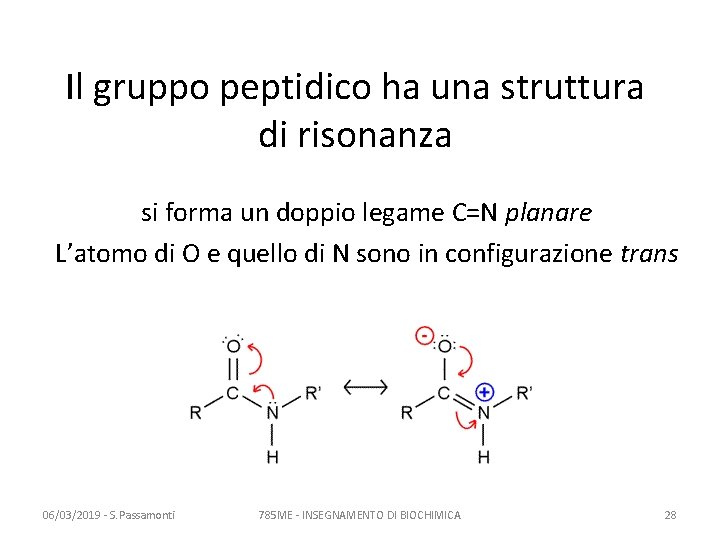
Il gruppo peptidico ha una struttura di risonanza si forma un doppio legame C=N planare L’atomo di O e quello di N sono in configurazione trans 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 28

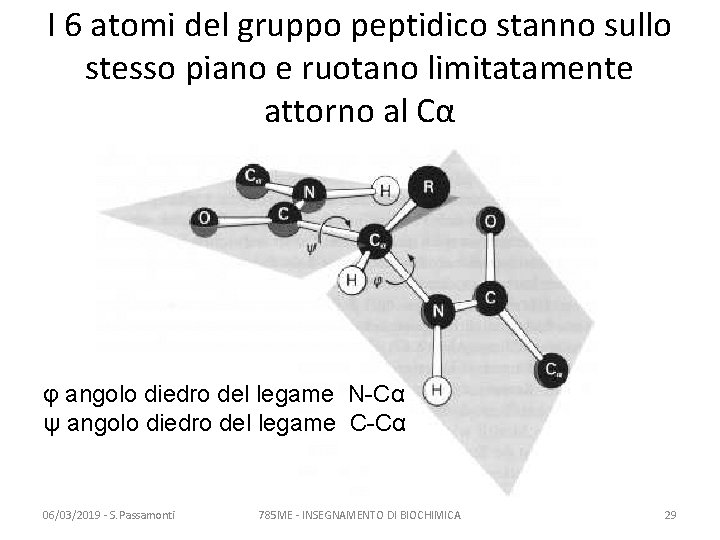
I 6 atomi del gruppo peptidico stanno sullo stesso piano e ruotano limitatamente attorno al Cα φ angolo diedro del legame N-Cα ψ angolo diedro del legame C-Cα 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 29

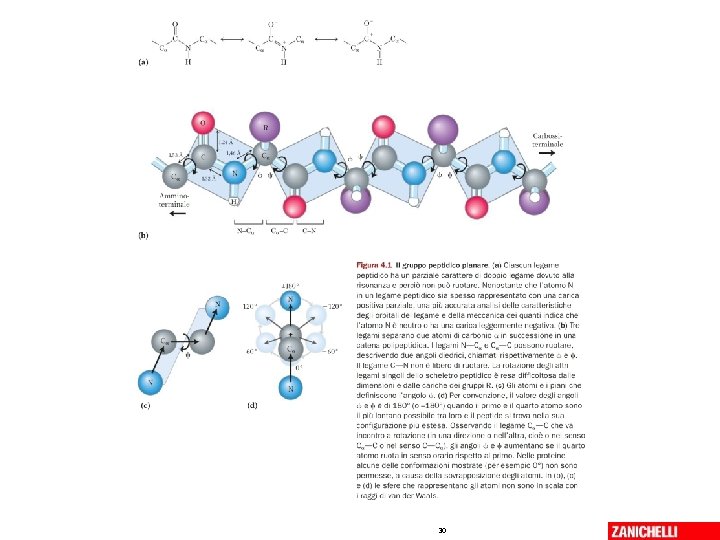
30

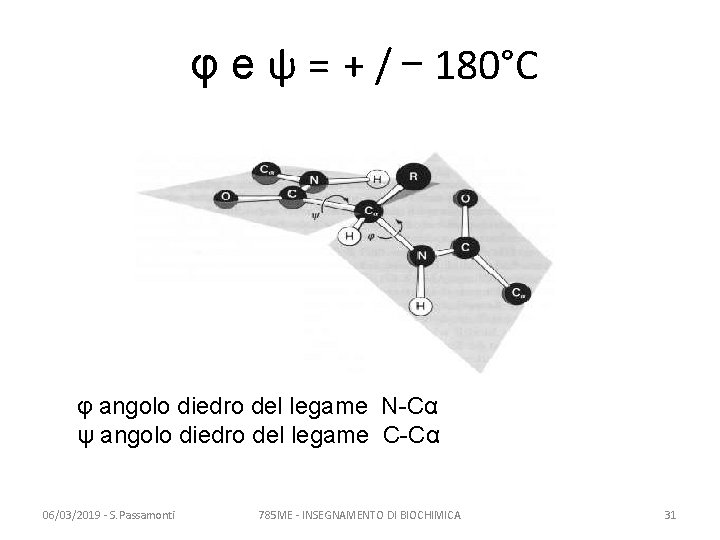
φ e ψ = + / – 180°C φ angolo diedro del legame N-Cα ψ angolo diedro del legame C-Cα 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 31

La struttura secondaria • Si riferisce solo alla catena principale • Si una struttura secondaria quando un segmento del polipeptide presenta angoli diedrici φ e ψ invariati • Le due principali strutture secondarie sono: α elica Il foglietto β • In assenza di struttura secondaria, la conformazione polipeptidica si definisce random coil 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 32

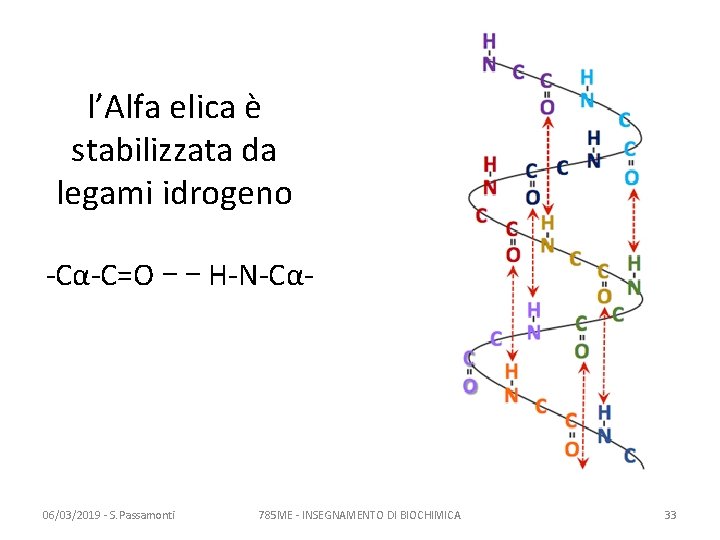
l’Alfa elica è stabilizzata da legami idrogeno -Cα-C=O - - H-N-Cα- 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 33

34

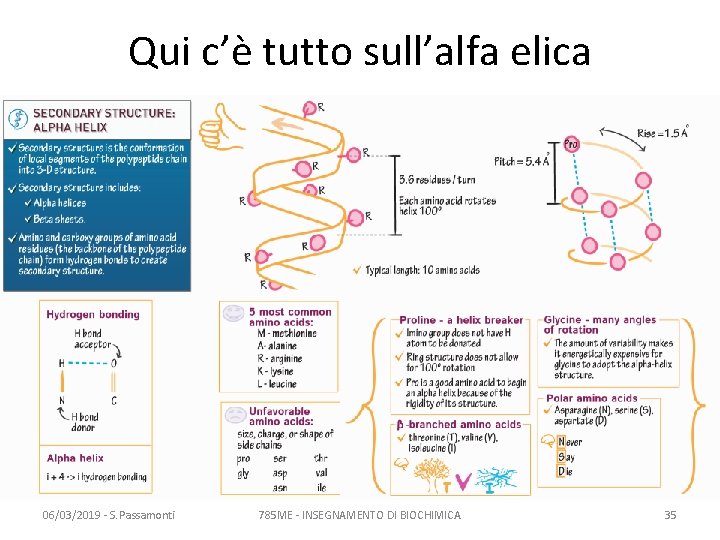
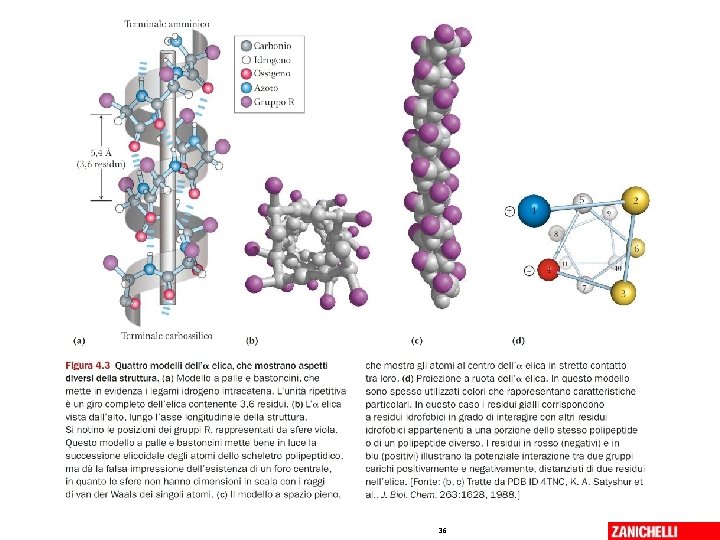
Qui c’è tutto sull’alfa elica 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 35

36

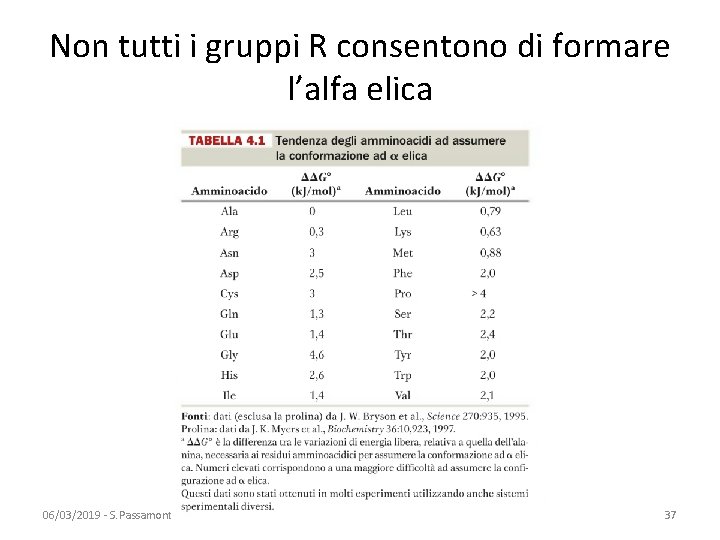
Non tutti i gruppi R consentono di formare l’alfa elica 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 37

Fattori limitanti la formazione di alfa-elica • Caratteristiche intrinseche dei gruppi R • Sequenze ricche di gruppi R carichi – repulsione o attrazione tra R influenzano gli angoli diedrici • La prolina (non ha un H per il legame H con O) • La glicina (il suo gruppo R=H le conferisce molta mobilità=entropia=delta G negativo) 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 38

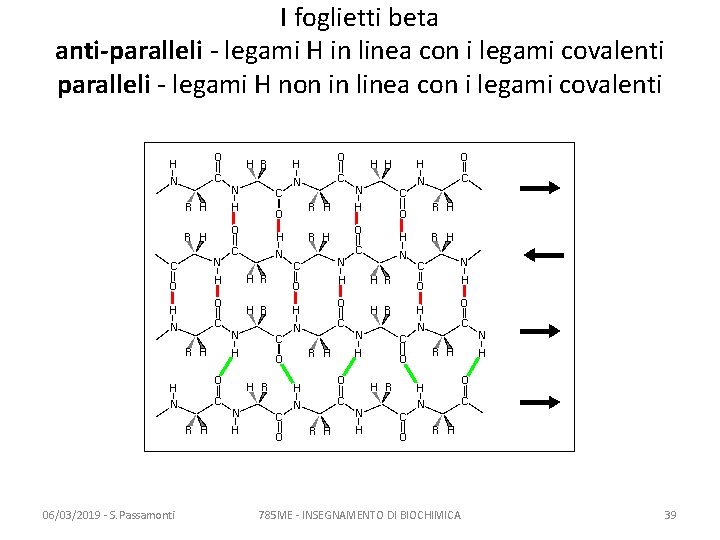
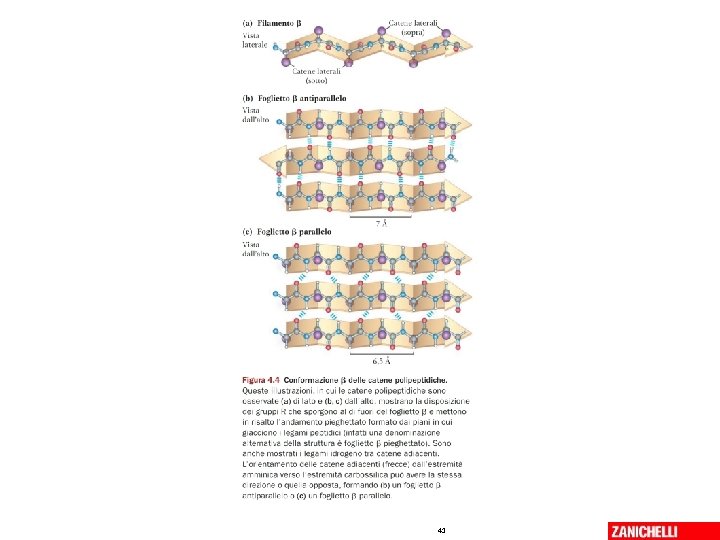
I foglietti beta anti-paralleli - legami H in linea con i legami covalenti paralleli - legami H non in linea con i legami covalenti 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 39

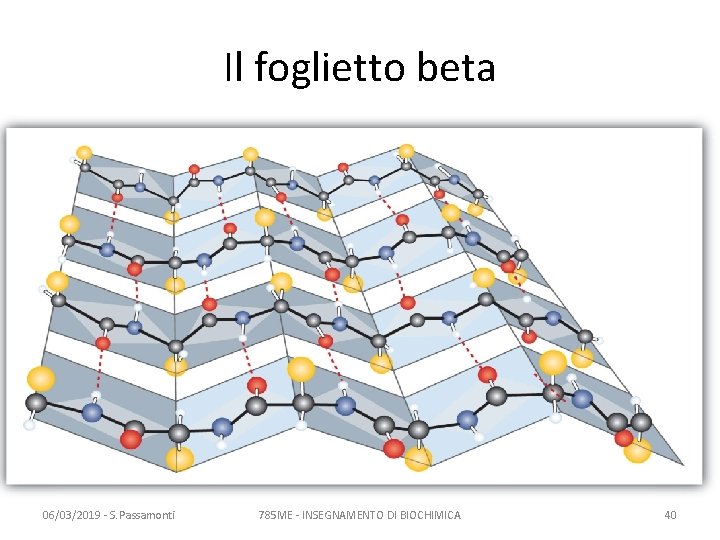
Il foglietto beta 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 40

41

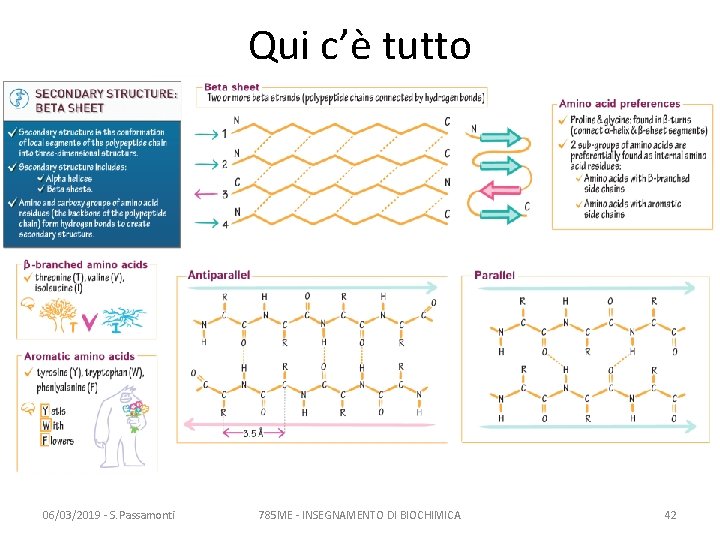
Qui c’è tutto 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 42

I fattori favorenti la formazione del foglietto beta • sequenze ricche di amminoacidi apolari, detti anche beta-ramificati: Thr, Val, Ile • sequenze ricche di amminoacidi aromatici: Tyr, Trp, Phe • Obbligatoria la possibilità di fare il ripiegamento beta del polipeptide, grazie a Gly e Pro – ripiegamento beta: vedi schema successivo 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 43

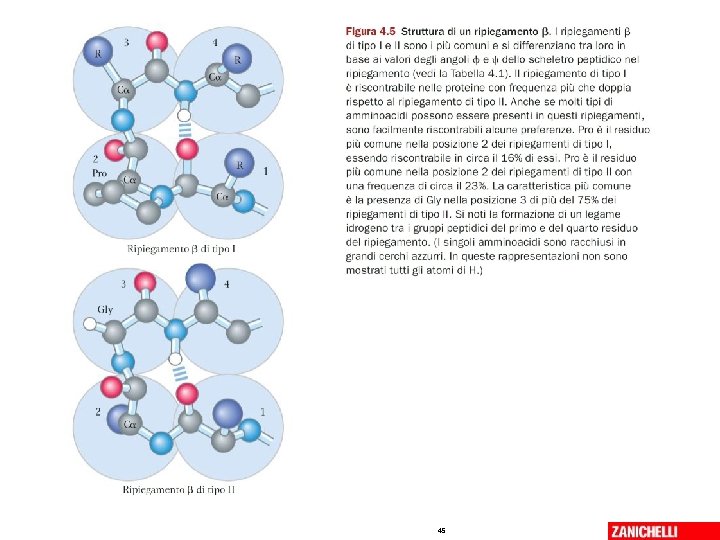
Il ripiegamento beta • La catena polipeptidica può formare delle anse strette: – ripiegamento di 180° – riguarda una sequenza di 4 amminoacidi – il gruppo C=O si lega con legame idrogeno all’atomo di H legato all’atomo di N del quarto amminoacido – I gruppi peptidici dei due amminoacidi centrali sono spesso esposti in superficie, e interagiscono con l’acqua 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 44

45

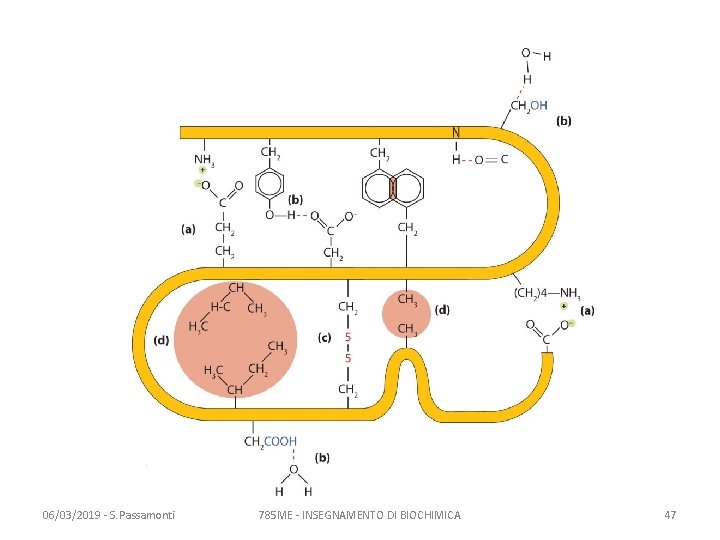
La struttura terziaria e quaternaria • Il polipeptide si avvolge su sé stesso, coinvolgendo gli eventuali domini aventi strutture secondarie, e assume una conformazione stabile (e caratteristica) • Le forze che determinano il ripiegamento finale sono i legami deboli tra atomi di amminoacidi anche molto distanti nella sequenza – MEMO: i legami deboli sono di 4 tipi 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 46

06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 47

La struttura quaternaria • Due o più polipeptidi (sub-unità) aventi una definita struttura terziaria si associano a formale una proteina multimerica • Le forze che determinano la struttura quaternaria sono i legami deboli tra atomi di amminoacidi di sub-unità diverse • MEMO: i legami deboli sono di 4 tipi 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 48

Due tipi di conformazioni • Proteine fibrose – ruoli strutturali • Proteine globulari – ruoli strutturali – ruoli catalitici – ruoli regolatori – ecc 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 49

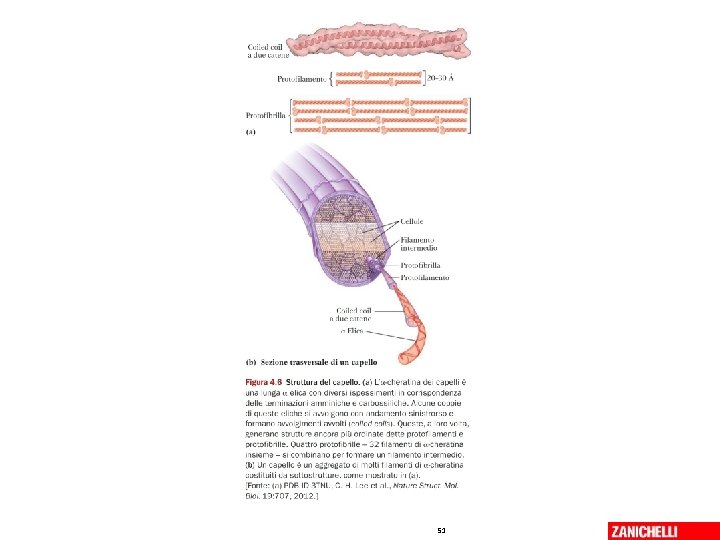
Proteine fibrose • alfa-cheratina • collegene • fibroina della seta 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 50

51

Fine A domani • Collagene • Proteine globulari 06/03/2019 - S. Passamonti 785 ME - INSEGNAMENTO DI BIOCHIMICA 52