I 20 aminoacidi delle proteine Modificazioni covalenti delle



- Slides: 39

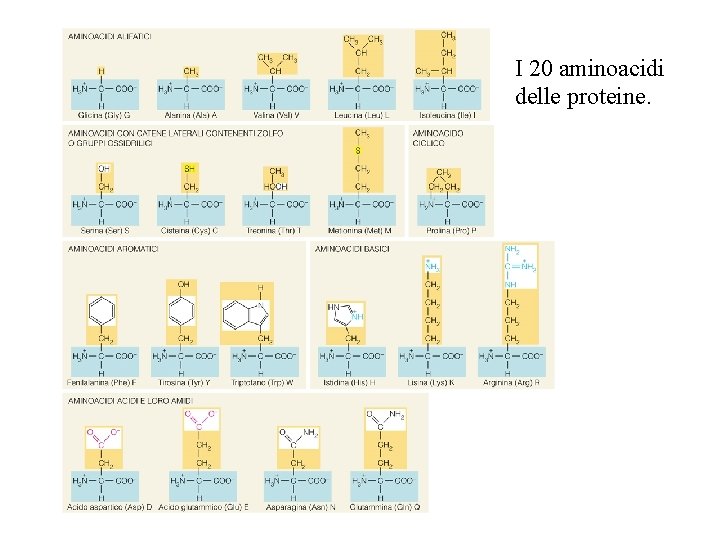
I 20 aminoacidi delle proteine.

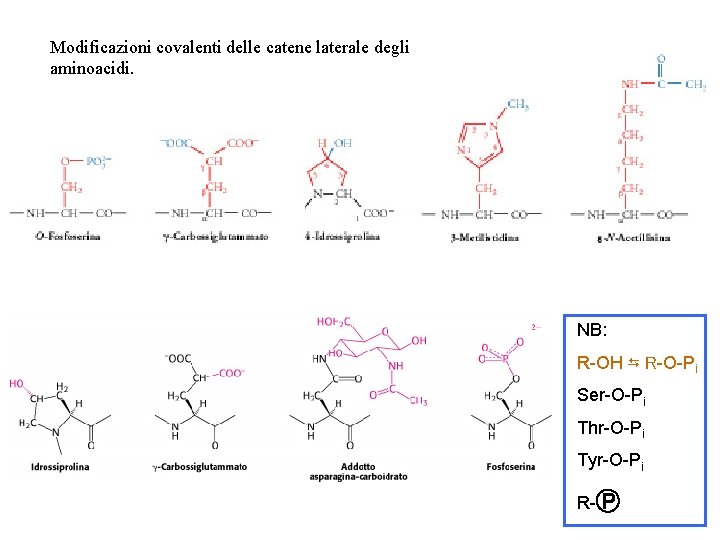
Modificazioni covalenti delle catene laterale degli aminoacidi. NB: R-OH ⇆ R-O-Pi Ser-O-Pi Thr-O-Pi Tyr-O-Pi R-Ⓟ

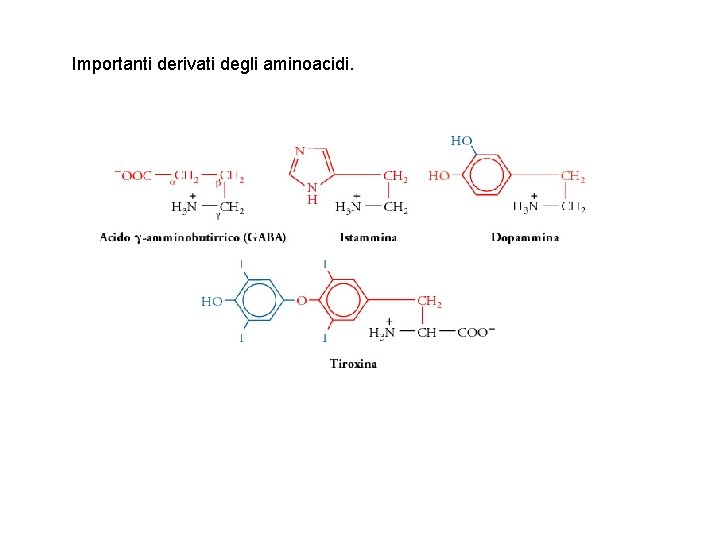
Importanti derivati degli aminoacidi.

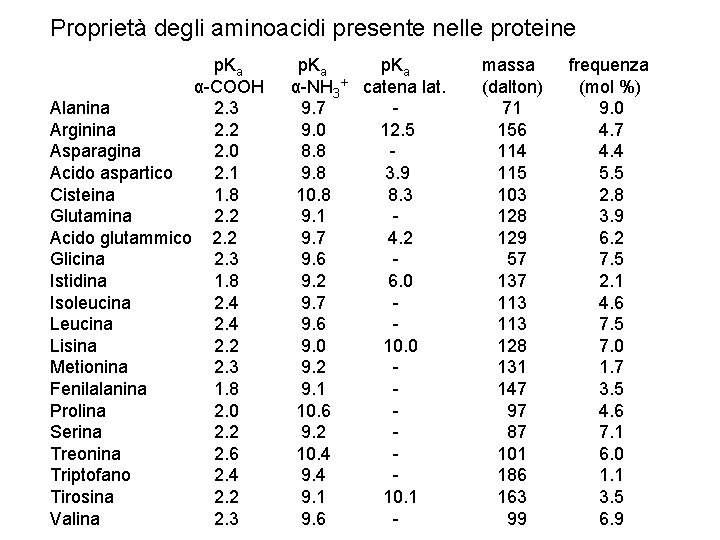
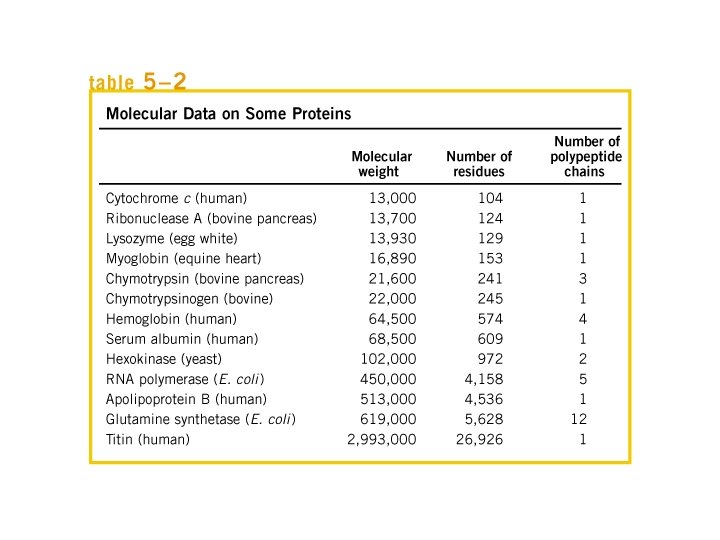
Proprietà degli aminoacidi presente nelle proteine p. Ka α-COOH Alanina 2. 3 Arginina 2. 2 Asparagina 2. 0 Acido aspartico 2. 1 Cisteina 1. 8 Glutamina 2. 2 Acido glutammico 2. 2 Glicina 2. 3 Istidina 1. 8 Isoleucina 2. 4 Lisina 2. 2 Metionina 2. 3 Fenilalanina 1. 8 Prolina 2. 0 Serina 2. 2 Treonina 2. 6 Triptofano 2. 4 Tirosina 2. 2 Valina 2. 3 p. Ka α-NH 3+ catena lat. 9. 7 9. 0 12. 5 8. 8 9. 8 3. 9 10. 8 8. 3 9. 1 9. 7 4. 2 9. 6 9. 2 6. 0 9. 7 9. 6 9. 0 10. 0 9. 2 9. 1 10. 6 9. 2 10. 4 9. 1 10. 1 9. 6 - massa (dalton) 71 156 114 115 103 128 129 57 137 113 128 131 147 97 87 101 186 163 99 frequenza (mol %) 9. 0 4. 7 4. 4 5. 5 2. 8 3. 9 6. 2 7. 5 2. 1 4. 6 7. 5 7. 0 1. 7 3. 5 4. 6 7. 1 6. 0 1. 1 3. 5 6. 9

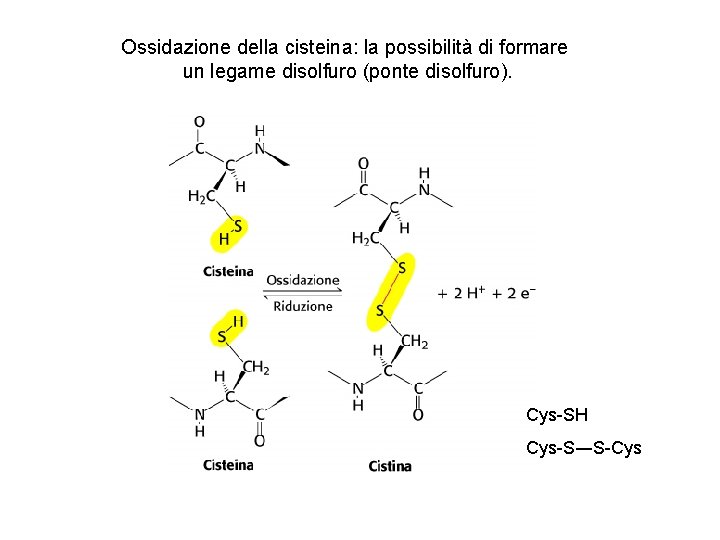
Ossidazione della cisteina: la possibilità di formare un legame disolfuro (ponte disolfuro). Cys-SH Cys-S―S-Cys

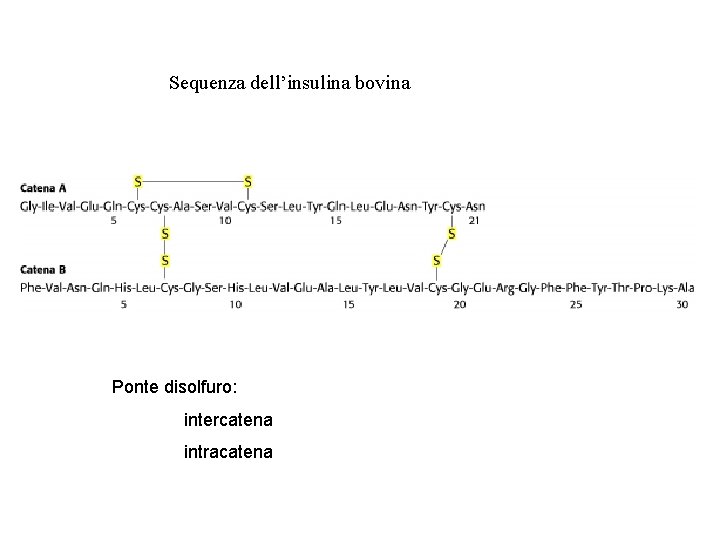
Sequenza dell’insulina bovina Ponte disolfuro: intercatena intracatena


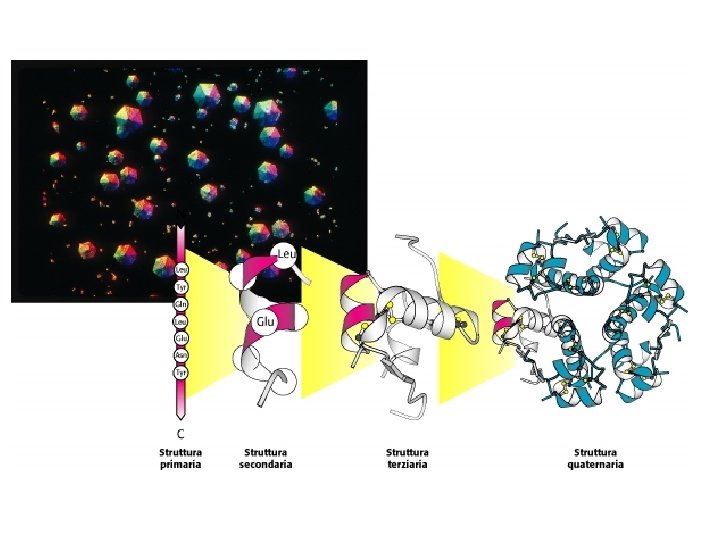
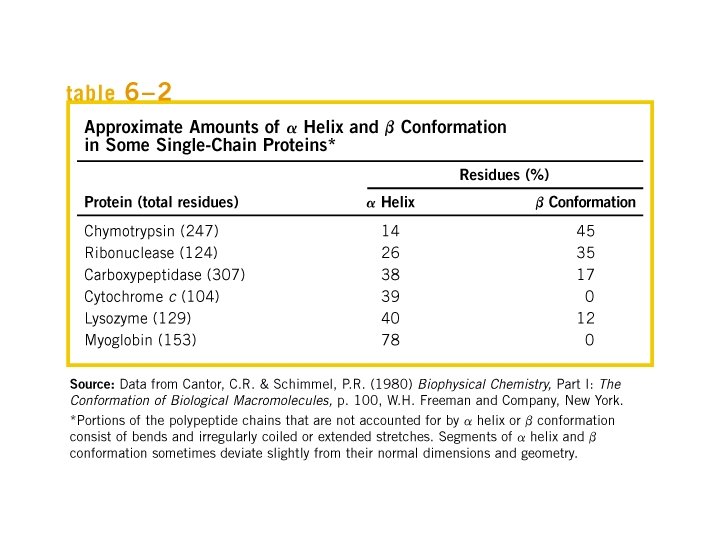
Struttura delle proteine: I quattro livelli. La struttura Primaria: la sequenza degli aminoacidi (della catena lineare) Ogni proteina ha una sequenza unica e precisamente definita La struttura Secondaria: schemi regolari di ripiegamento della catena α-elica, foglietto β, etc. La struttura Terziaria: la struttura tridimensionale di un intero polipeptide Proteine composte da due o più polipeptidi (subunità): La struttura Quaternaria: la disposizione spaziale delle subunità

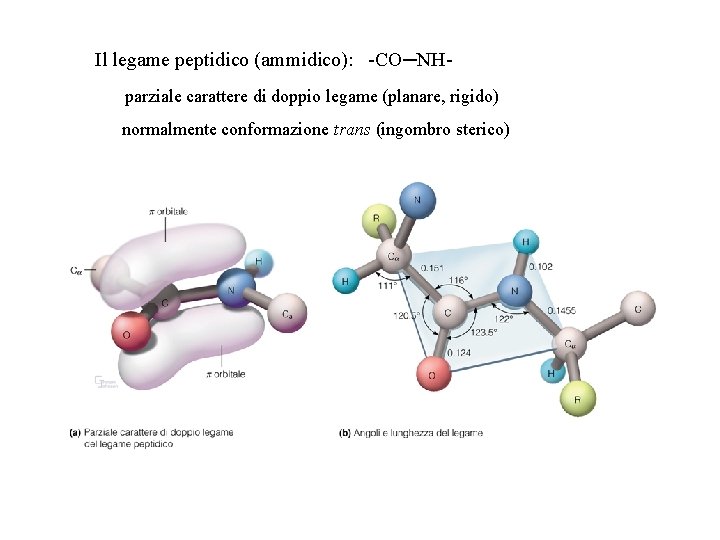
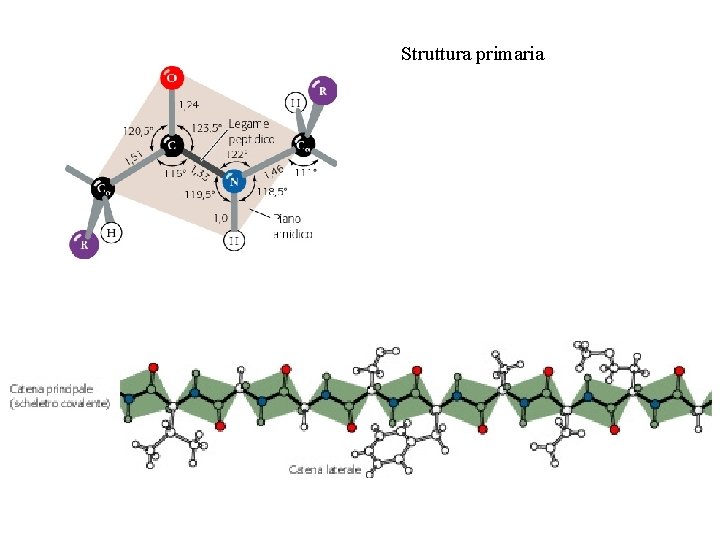
Il legame peptidico (ammidico): -CO─NHparziale carattere di doppio legame (planare, rigido) normalmente conformazione trans (ingombro sterico)

Struttura primaria

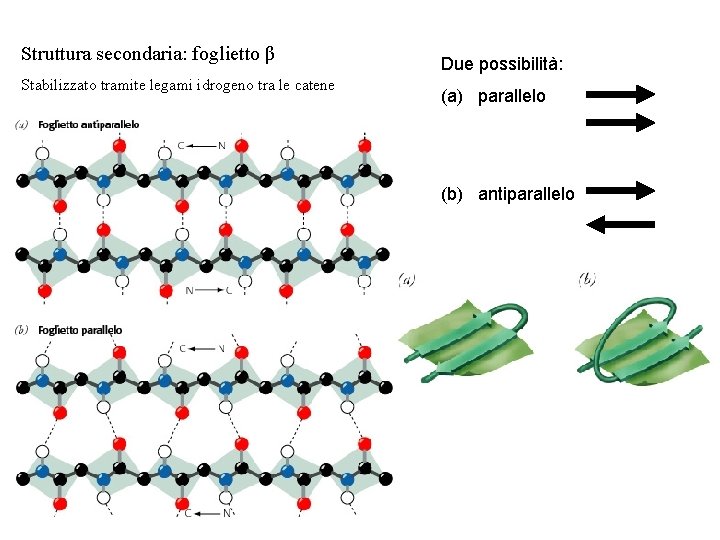
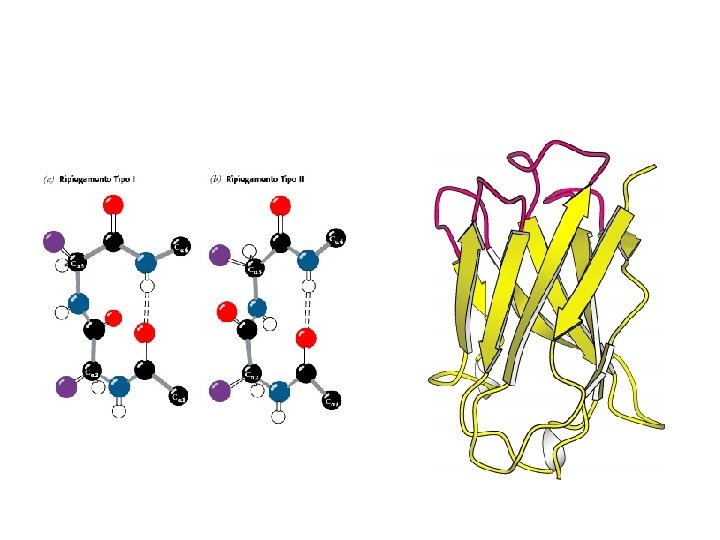
Struttura secondaria: foglietto β Stabilizzato tramite legami idrogeno tra le catene Due possibilità: (a) parallelo (b) antiparallelo

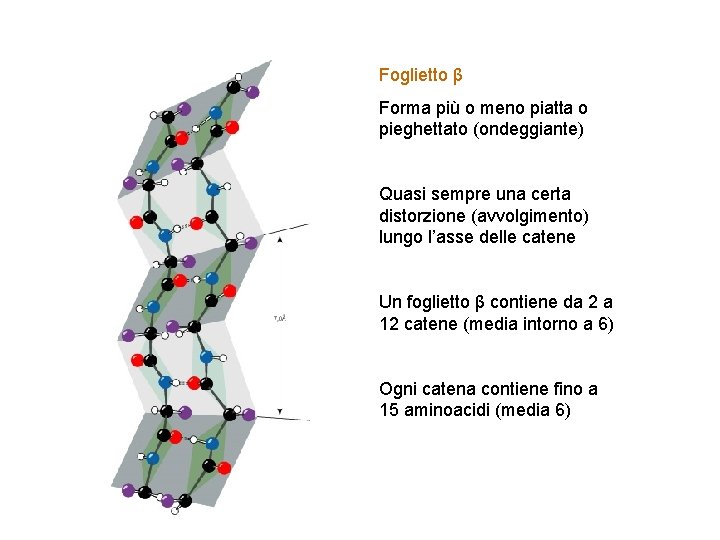
Foglietto β Forma più o meno piatta o pieghettato (ondeggiante) Quasi sempre una certa distorzione (avvolgimento) lungo l’asse delle catene Un foglietto β contiene da 2 a 12 catene (media intorno a 6) Ogni catena contiene fino a 15 aminoacidi (media 6)

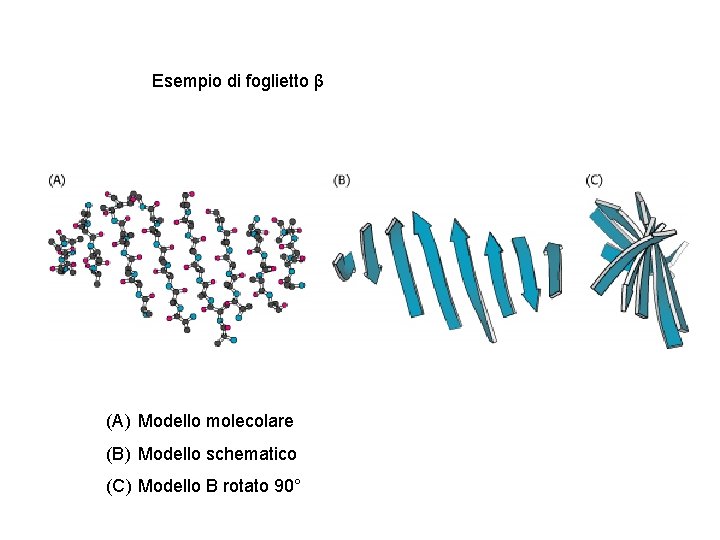
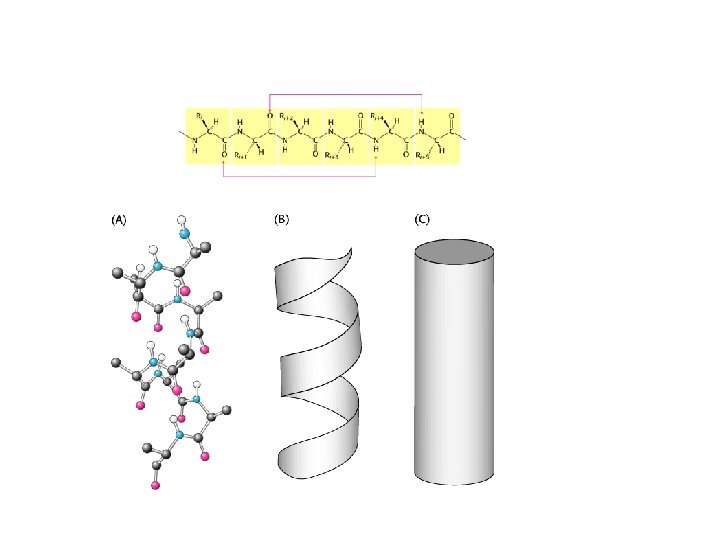
Esempio di foglietto β (A) Modello molecolare (B) Modello schematico (C) Modello B rotato 90°

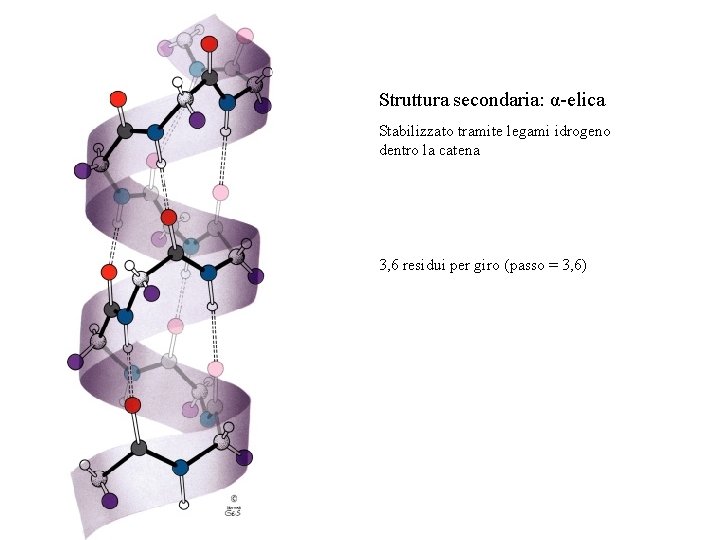
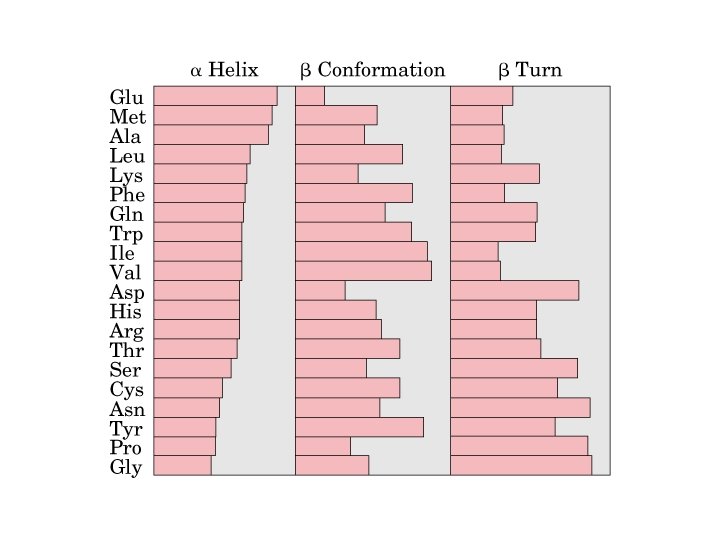
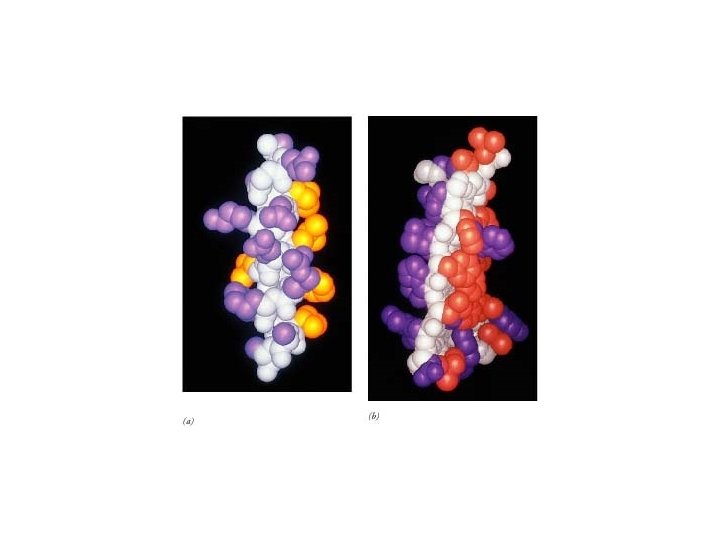
Struttura secondaria: α-elica Stabilizzato tramite legami idrogeno dentro la catena 3, 6 residui per giro (passo = 3, 6)

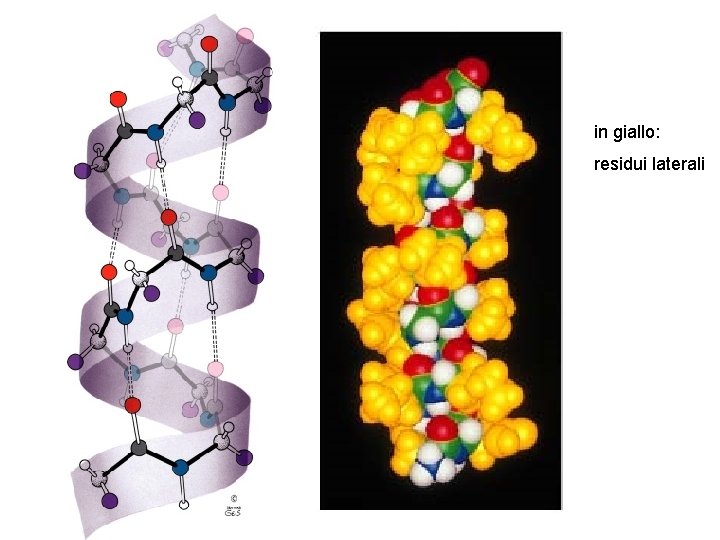
in giallo: residui laterali




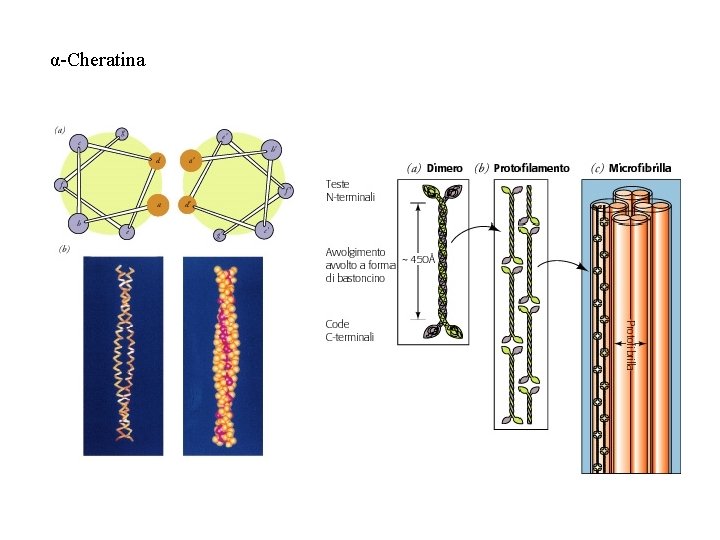
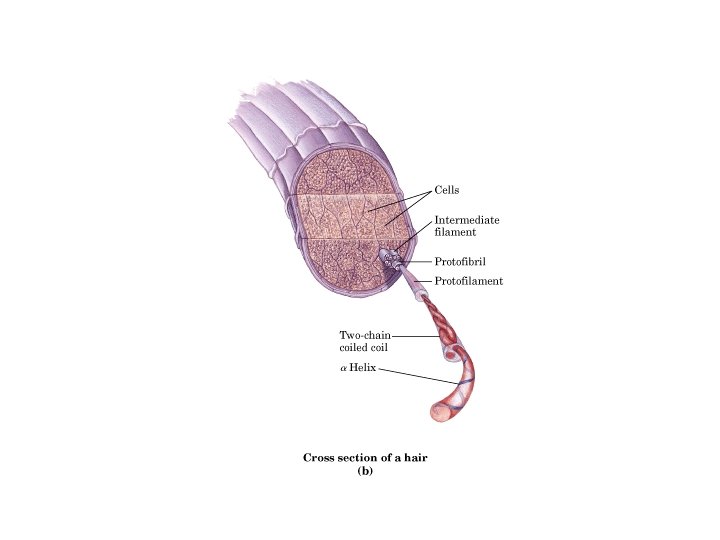
Proteine fibrose: ruoli strutturali in cellule e tessuti animali miosina (muscoli) fibrina (coaguli di sangue) α-cheratina (capelli) collageno (tendine, tessuto connettivo, cartilagine) β-cheratina (piume, scaglie) fibroina (seta) elastina (tessuto estensibile, legamenti, vasi sanguigni) α-Eliche avvolte (superavvolte). La lunghezza può superare 100 nm (0. 1 µm)

α-Cheratina


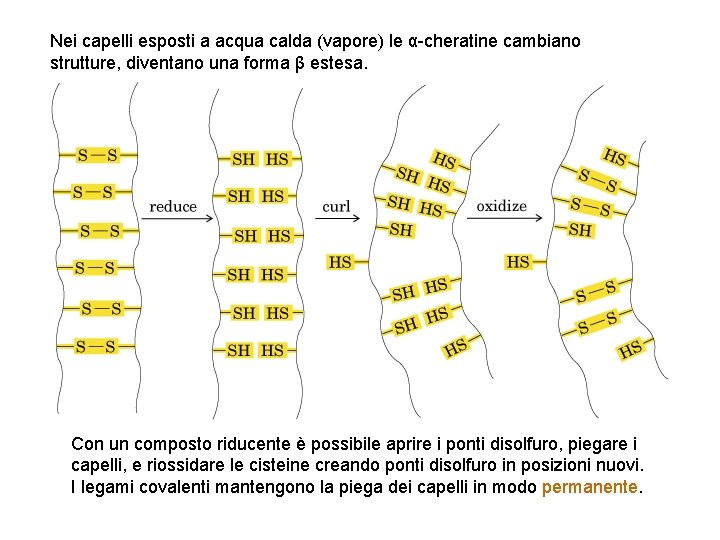
Nei capelli esposti a acqua calda (vapore) le α-cheratine cambiano strutture, diventano una forma β estesa. Con un composto riducente è possibile aprire i ponti disolfuro, piegare i capelli, e riossidare le cisteine creando ponti disolfuro in posizioni nuovi. I legami covalenti mantengono la piega dei capelli in modo permanente.

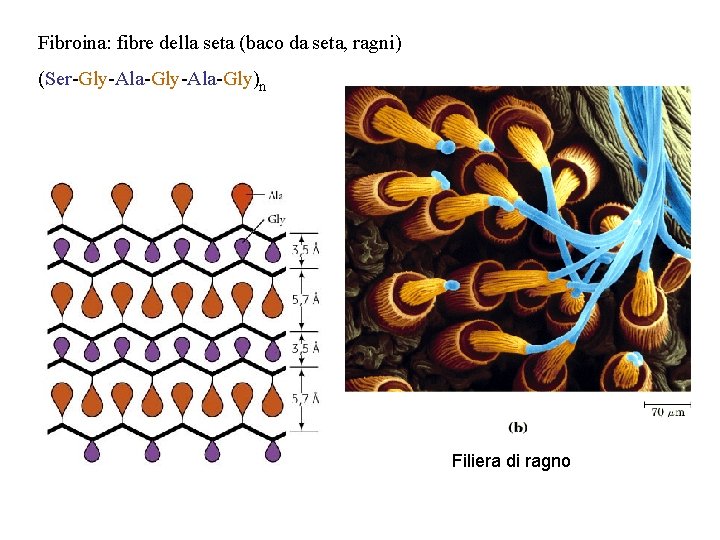
Fibroina: fibre della seta (baco da seta, ragni) (Ser-Gly-Ala-Gly)n Filiera di ragno

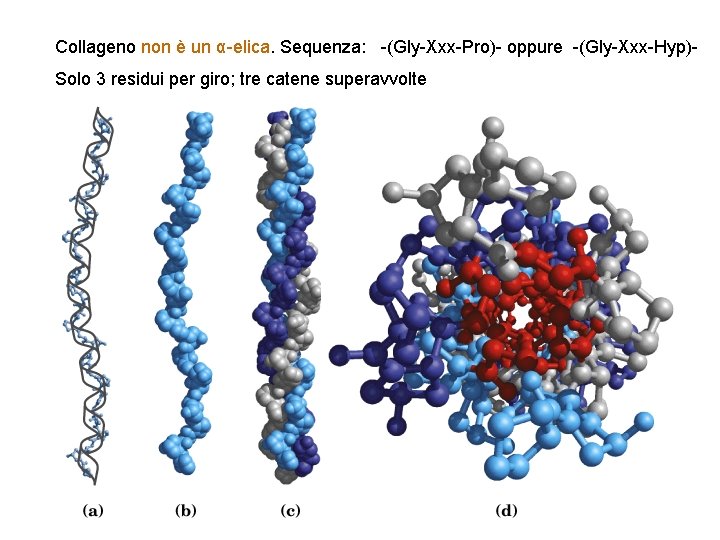
Collageno non è un α-elica. Sequenza: -(Gly-Xxx-Pro)- oppure -(Gly-Xxx-Hyp)Solo 3 residui per giro; tre catene superavvolte

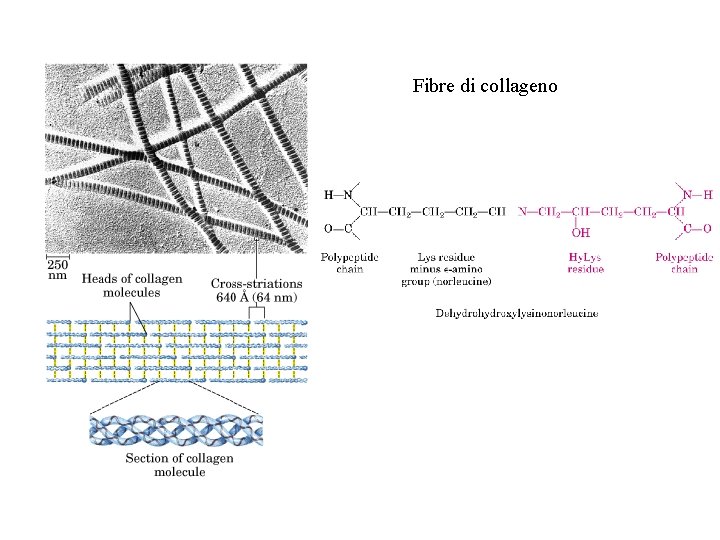
Fibre di collageno

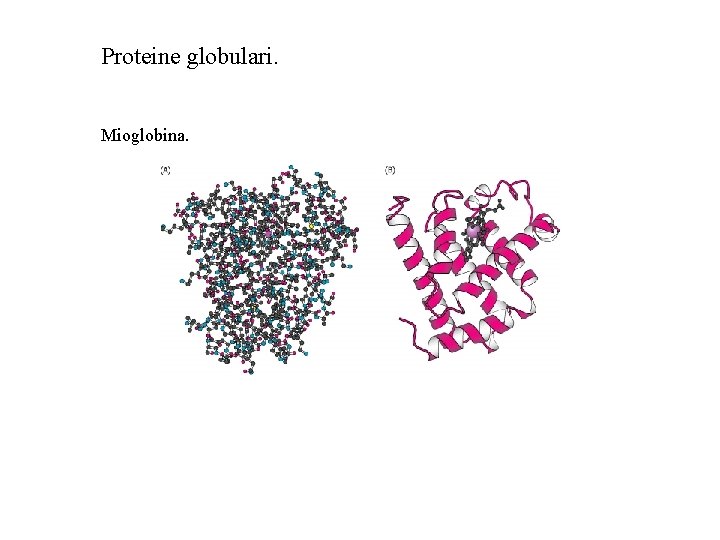
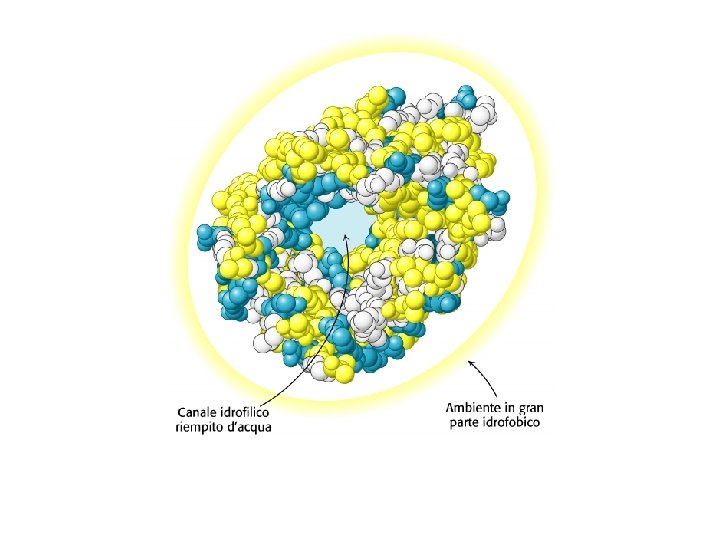
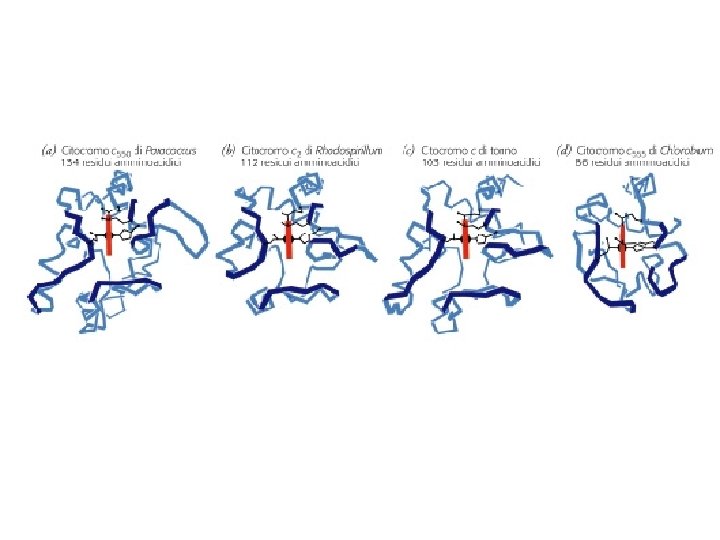
Proteine globulari. Mioglobina.

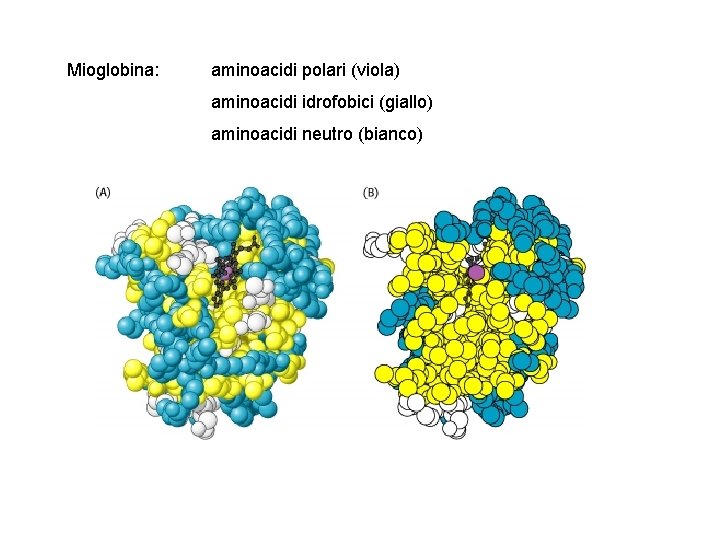
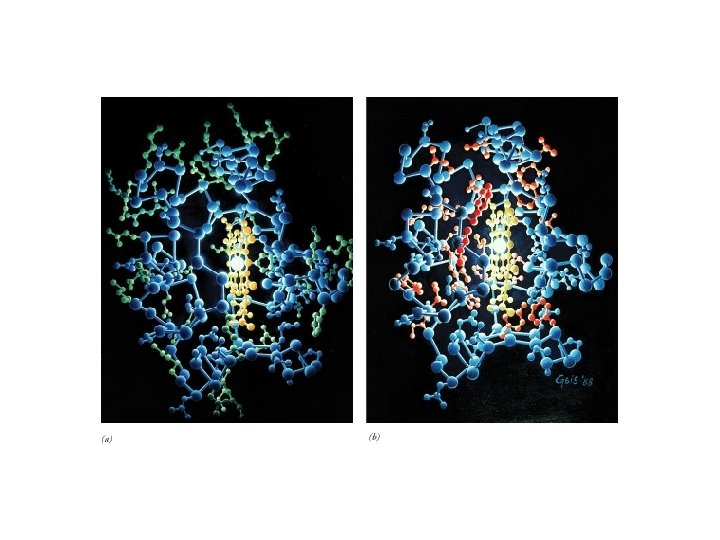
Mioglobina: aminoacidi polari (viola) aminoacidi idrofobici (giallo) aminoacidi neutro (bianco)




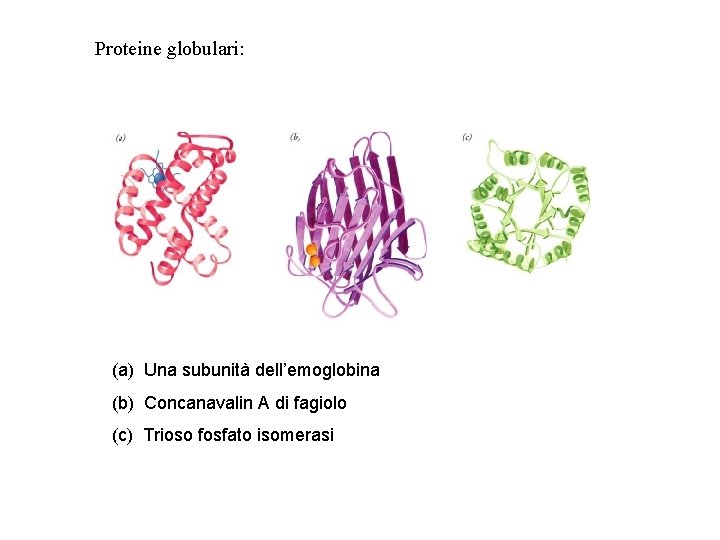
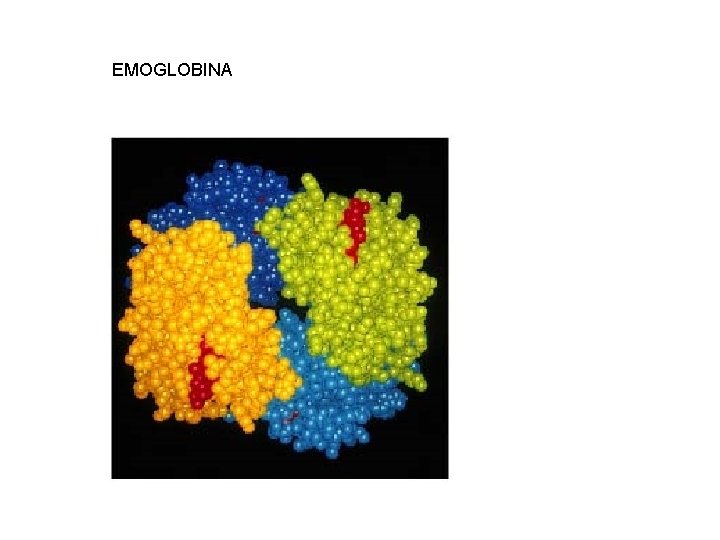
Proteine globulari: (a) Una subunità dell’emoglobina (b) Concanavalin A di fagiolo (c) Trioso fosfato isomerasi

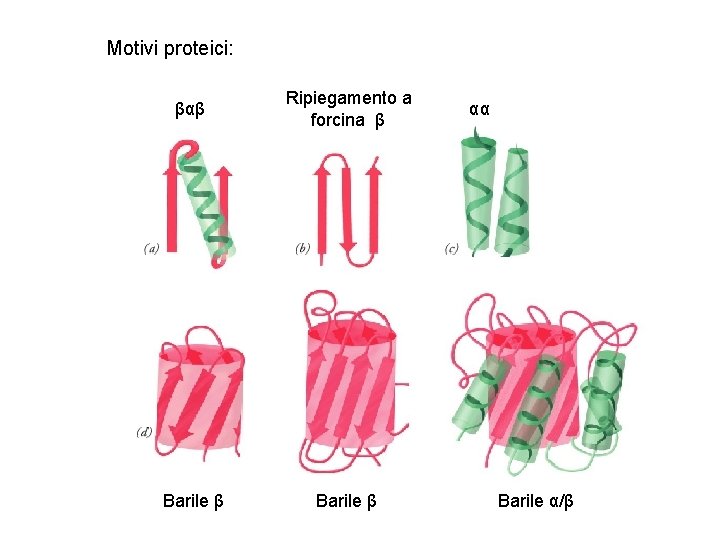
Motivi proteici: βαβ Ripiegamento a forcina β Barile β αα Barile α/β

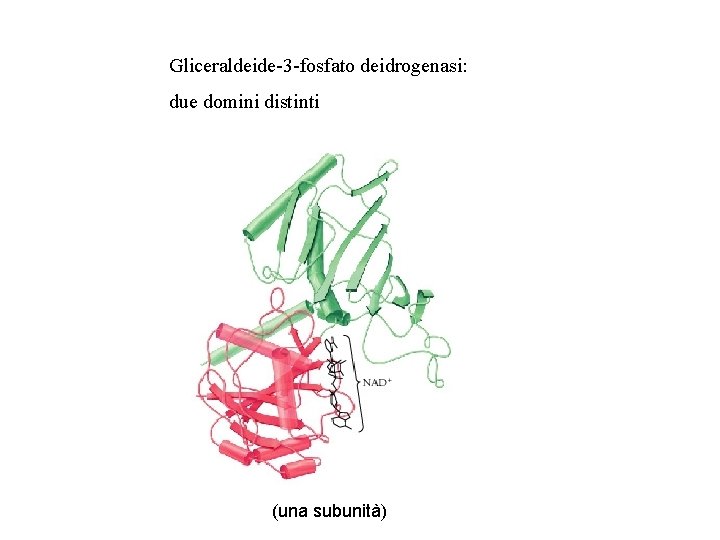
Gliceraldeide-3 -fosfato deidrogenasi: due domini distinti (una subunità)

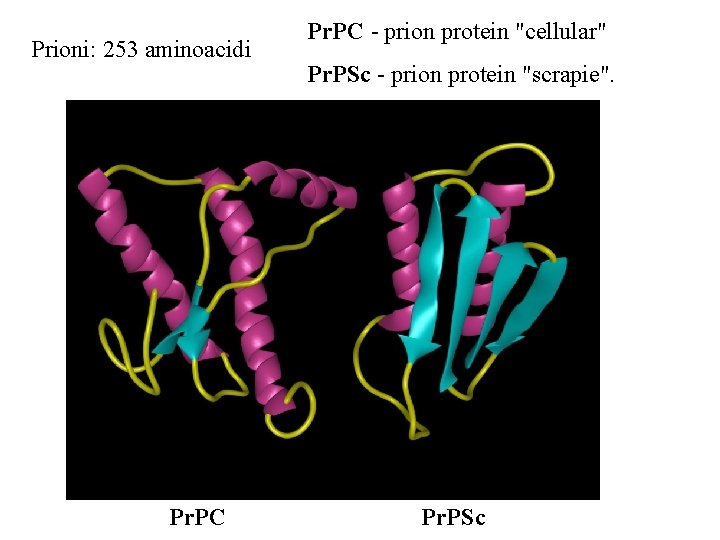
Prioni: 253 aminoacidi Pr. PC - prion protein "cellular" Pr. PSc - prion protein "scrapie". Pr. PSc

Animal forms: Scrapie BSE Transmissible mink encephalopathy (TME) chronic wasting disease Feline spongiform encephalopathy (FSE) Human forms: kuru Creutzfeldt-Jakob disease (CJD) Gerstmann-Straussler syndrome (GSS) fatal familial insomnia (FFI)




EMOGLOBINA