3 Das chemische Gleichgewicht 3 6 Die Geschwindigkeit




















































































































- Slides: 140

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Beispiele zweier Reaktionen mit negativer DG und sehr unterschiedlicher Geschwindigkeit

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Beispiele zweier Reaktionen mit negativer DG und sehr unterschiedlicher Geschwindigkeit 1. ) H 2 + F 2 2 HF Sehr schnelle Reaktion

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Beispiele zweier Reaktionen mit negativer DG und sehr unterschiedlicher Geschwindigkeit 1. ) H 2 + F 2 2 HF Sehr schnelle Reaktion 2. ) H 2 + Cl 2 2 HCl Bei NB keine meßbare Rkn.

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Beispiele zweier Reaktionen mit negativer DG und sehr unterschiedlicher Geschwindigkeit 1. ) H 2 + F 2 2 HF Sehr schnelle Reaktion 2. ) H 2 + Cl 2 2 HCl Bei NB keine meßbare Rkn. Die Gleichgewichtslage hat keinen Einfluß auf die Reaktionsgeschwindigkeit

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Beispiele zweier Reaktionen mit negativer DG und sehr unterschiedlicher Geschwindigkeit 1. ) H 2 + F 2 2 HF Sehr schnelle Reaktion 2. ) H 2 + Cl 2 2 HCl Bei NB keine meßbare Rkn. Die Gleichgewichtslage hat keinen Einfluß auf die Reaktionsgeschwindigkeit Welche Parameter haben Einfluß auf die Reaktionsgeschwindigkeit?

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Welche Parameter haben Einfluß auf die Reaktionsgeschwindigkeit? + Temperatur

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Welche Parameter haben Einfluß auf die Reaktionsgeschwindigkeit? + Temperatur + Konzentration der Reaktionsteilnehmer

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Welche Parameter haben Einfluß auf die Reaktionsgeschwindigkeit? + Temperatur + Konzentration der Reaktionsteilnehmer (Faustregel: 10 K Erhöhung steigert die Reaktionsgeschwindigkeit um das 2 -4 fache. )

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Welche Parameter haben Einfluß auf die Reaktionsgeschwindigkeit? + Temperatur + Konzentration der Reaktionsteilnehmer (Faustregel: 10 K Erhöhung steigert die Reaktionsgeschwindigkeit um das 2 -4 fache. ) + Katalyse

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Welche Parameter haben Einfluß auf die Reaktionsgeschwindigkeit? + Temperatur + Konzentration der Reaktionsteilnehmer (Faustregel: 10 K Erhöhung steigert die Reaktionsgeschwindigkeit um das 2 -4 fache. + Katalyse (Veränderung des Reaktionsweges!)

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Welche Parameter haben Einfluß auf die Reaktionsgeschwindigkeit? + Temperatur + Konzentration der Reaktionsteilnehmer (Faustregel: 10 K Erhöhung steigert die Reaktionsgeschwindigkeit um das 2 -4 fache. ) + Katalyse (Veränderung des Reaktionsweges!) Mit der Geschwindigkeit und den Mechanismen chemischer Reaktionen befaßt sich die Chemische Kinetik.

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit Für die Reaktion 2 N 2 O O 2 + 2 N 2

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit Für die Reaktion 2 N 2 O O 2 + 2 N 2 gilt die Geschwindigkeitsgleichung

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit Die Konzentration tritt mit dem Exponenten 1 auf; solche Reaktionen heißen Reaktionen erster Ordnung.

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit Die Konzentration tritt mit dem Exponenten 1 auf; solche Reaktionen heißen Reaktionen erster Ordnung. k wird als Geschwindigkeitskonstante bezeichnet.

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit Der Zerfall von Iodwasserstoff in die Elemente folgt der Gleichung 2 HI I 2 + H 2 Hierfür wird die folgende Geschwindigkeitsgleichung gefunden:

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit Der Zerfall von Iodwasserstoff in die Elemente folgt der Gleichung 2 HI I 2 + H 2 Hierfür wird die folgende Geschwindigkeitsgleichung gefunden:

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit Der Zerfall von Iodwasserstoff in die Elemente folgt der Gleichung 2 HI I 2 + H 2 Hierfür wird die folgende Geschwindigkeitsgleichung gefunden: Die Konzentration tritt mit dem Exponenten 2 auf; solche Reaktionen heißen Reaktionen zweiter Ordnung.

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit Chemische Bruttogleichungen informieren über + Edukte und Produkte

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit Chemische Bruttogleichungen informieren über + Edukte und Produkte und nicht über den molekularen Ablauf; den Reaktionsmechanismus.

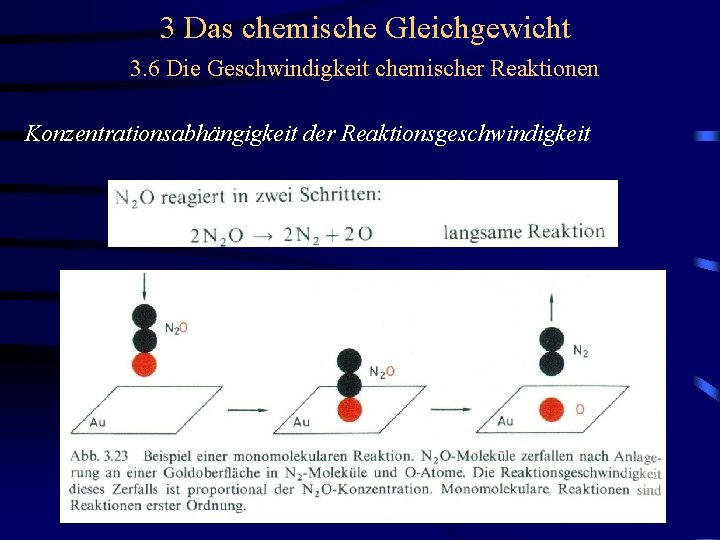
3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit zum Beispiel zerfällt N 2 O in zwei Schritten:

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit Liegt eine Folge von Reaktionsschritten vor, bestimmt der langsamste Reaktionsschritt die Geschwindigkeit der Gesamtreaktion.

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit Im obigen Fall ist die erste Rkn. geschwindigkeitsbestimmend. Da hier nur ein Molekül beteiligt ist, nennt man solche Zerfallsreaktionen monomolekulare Reaktionen.

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit Im obigen Fall ist die erste Rkn. geschwindigkeitsbestimmend. Da hier nur ein Molekül beteiligt ist, nennt man solche Zerfallsreaktionen monomolekulare Reaktionen. Monomolekulare Reaktionen sind immer erster Ordnung.

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit HI zerfällt nach einem Zeitgesetz zweiter Ordnung

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit HI zerfällt nach einem Zeitgesetz zweiter Ordnung es liegt ein anderer Reaktionsmechanismus vor:

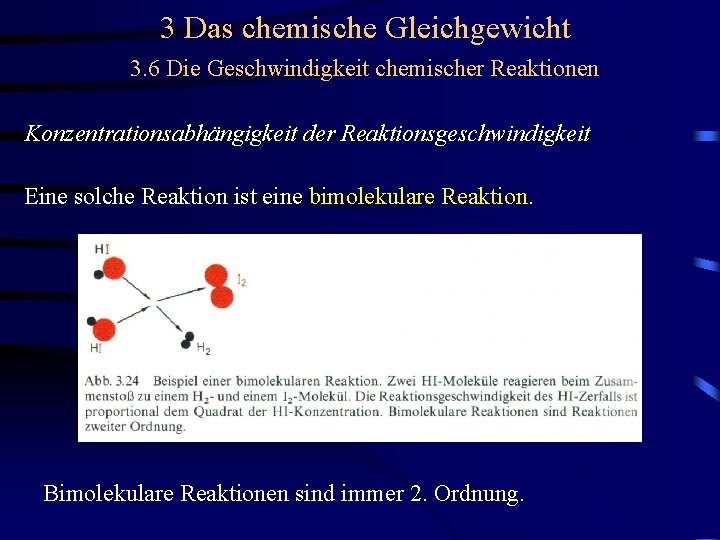
3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit HI zerfällt nach einem Zeitgesetz zweiter Ordnung es liegt ein anderer Reaktionsmechanismus vor: Geschwindigkeitsbestimmender Schritt ist ein Zusammenstoß zweier HI - Moleküle: HI + HI H 2 + I 2

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit HI zerfällt nach einem Zeitgesetz zweiter Ordnung es liegt ein anderer Reaktionsmechanismus vor: Geschwindigkeitsbestimmender Schritt ist ein Zusammenstoß zweier HI - Moleküle: HI + HI H 2 + I 2 Eine solche Reaktion ist eine bimolekulare Reaktion.

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit HI zerfällt nach einem Zeitgesetz zweiter Ordnung es liegt ein anderer Reaktionsmechanismus vor: Geschwindigkeitsbestimmender Schritt ist ein Zusammenstoß zweier HI - Moleküle: HI + HI H 2 + I 2 Eine solche Reaktion ist eine bimolekulare Reaktion.

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit Eine solche Reaktion ist eine bimolekulare Reaktion.

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit Eine solche Reaktion ist eine bimolekulare Reaktion. Bimolekulare Reaktionen sind immer 2. Ordnung.

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit Bei einer trimolekularen Reaktion müssen drei Teilchen gleichzeitig zusammenstoßen.

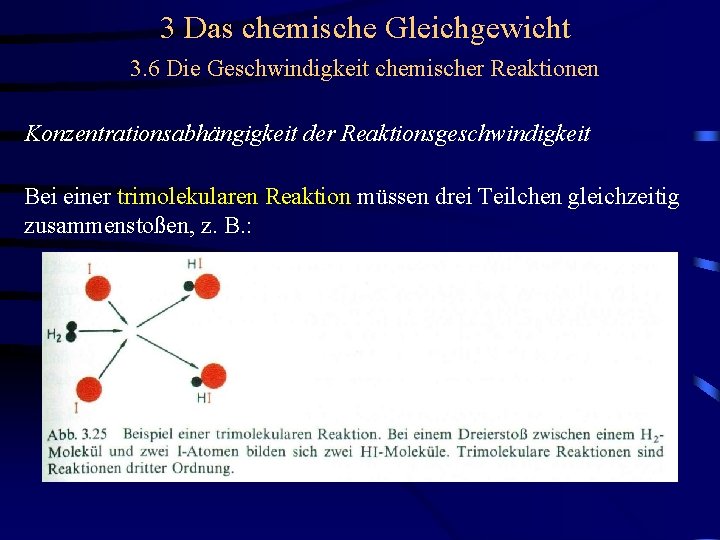
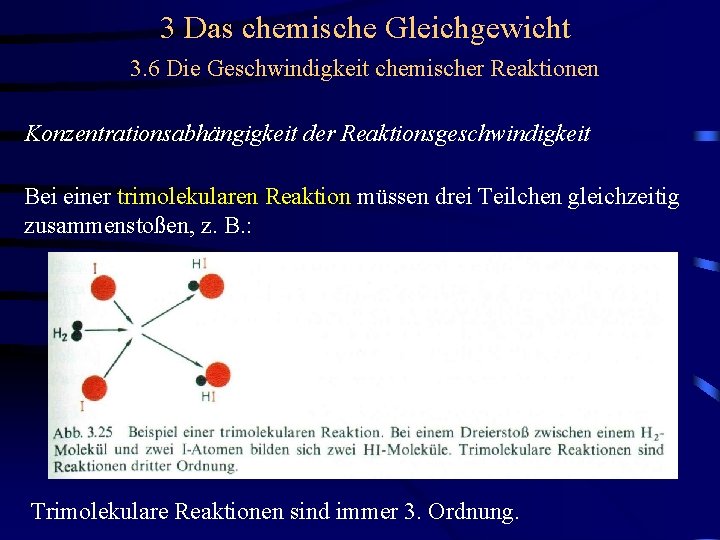
3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit Bei einer trimolekularen Reaktion müssen drei Teilchen gleichzeitig zusammenstoßen, z. B. :

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit Bei einer trimolekularen Reaktion müssen drei Teilchen gleichzeitig zusammenstoßen, z. B. : Trimolekulare Reaktionen sind immer 3. Ordnung.

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit Aus der Molekularität einer Reaktion ergibt sich also die Reaktionsordnung.

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit Aus der Molekularität einer Reaktion ergibt sich also die Reaktionsordnung. Umgekehrt kann aus der Reaktionsordnung nicht zwingend auf den Reaktionsmechanismus geschlossen werden.

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit Aus der Molekularität einer Reaktion ergibt sich also die Reaktionsordnung. Umgekehrt kann aus der Reaktionsordnung nicht zwingend auf den Reaktionsmechanismus geschlossen werden, wie im Folgenden gezeigt: Für die HI - Bildung aus den Elementen findet man eine (Gesamt)eaktion 2. Ordnung.

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit Aus der Molekularität einer Reaktion ergibt sich also die Reaktionsordnung. Umgekehrt kann aus der Reaktionsordnung nicht zwingend auf den Reaktionsmechanismus geschlossen werden, wie im Folgenden gezeigt: Für die HI - Bildung aus den Elementen findet man eine (Gesamt)eaktion 2. Ordnung. Möglich wäre demnach: H 2 + I 2 2 HI

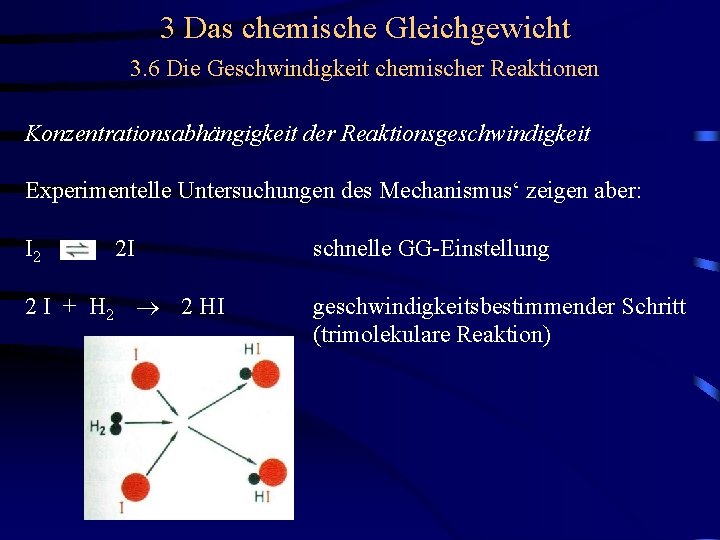
3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit Experimentelle Untersuchungen des Mechanismus‘ zeigen aber: I 2 2 I 2 I + H 2 2 HI schnelle GG-Einstellung geschwindigkeitsbestimmender Schritt

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit Experimentelle Untersuchungen des Mechanismus‘ zeigen aber: I 2 2 I 2 I + H 2 2 HI schnelle GG-Einstellung geschwindigkeitsbestimmender Schritt (trimolekulare Reaktion)

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit Experimentelle Untersuchungen des Mechanismus‘ zeigen aber: I 2 2 I 2 I + H 2 2 HI schnelle GG-Einstellung geschwindigkeitsbestimmender Schritt (trimolekulare Reaktion)

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit I 2 2 I 2 I + H 2 2 HI schnelle GG-Einstellung geschwindigkeitsbestimmender Schritt (trimolekulare Reaktion) Die Konzentration der Iodatome ist gegeben durch das MWG:

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit I 2 2 I 2 I + H 2 2 HI schnelle GG-Einstellung geschwindigkeitsbestimmender Schritt (trimolekulare Reaktion) Die Konzentration der Iodatome ist gegeben durch das MWG:

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit 2 I + H 2 2 HI Geschwindigkeitsgesetz: geschwindigkeitsbestimmender Schritt (trimolekulare Reaktion)

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit 2 I + H 2 2 HI geschwindigkeitsbestimmender Schritt (trimolekulare Reaktion) Geschwindigkeitsgesetz: zusammen mit folgt:

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Konzentrationsabhängigkeit der Reaktionsgeschwindigkeit 2 I + H 2 2 HI geschwindigkeitsbestimmender Schritt (trimolekulare Reaktion) Geschwindigkeitsgesetz: zusammen mit folgt:

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Temperaturabhängigkeit der Reaktionsgeschwindigkeit wird beschrieben durch die Arrhenius-Gleichung:

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Temperaturabhängigkeit der Reaktionsgeschwindigkeit wird beschrieben durch die Arrhenius-Gleichung: 1859 - 1927 schwedischer Physikochemiker

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Temperaturabhängigkeit der Reaktionsgeschwindigkeit wird beschrieben durch die Arrhenius-Gleichung:

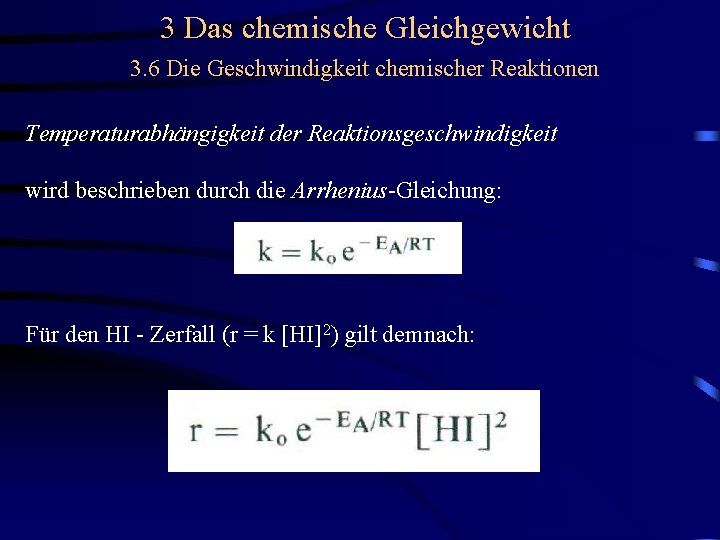
3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Temperaturabhängigkeit der Reaktionsgeschwindigkeit wird beschrieben durch die Arrhenius-Gleichung: Für den HI - Zerfall (r = k [HI]2) gilt demnach:

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Temperaturabhängigkeit der Reaktionsgeschwindigkeit wird beschrieben durch die Arrhenius-Gleichung: Für den HI - Zerfall (r = k [HI]2) gilt demnach:

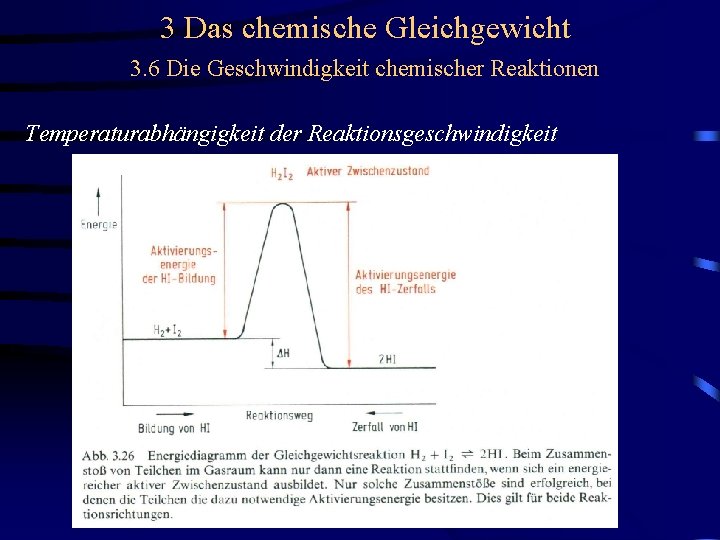
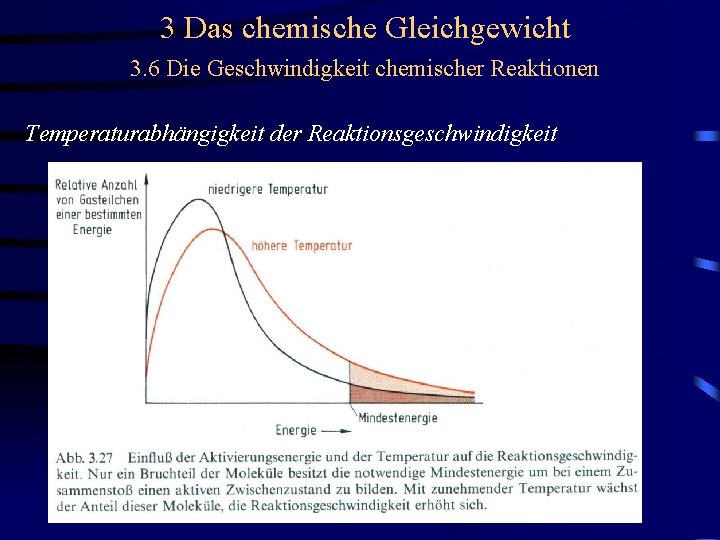
3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Temperaturabhängigkeit der Reaktionsgeschwindigkeit

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Temperaturabhängigkeit der Reaktionsgeschwindigkeit

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Temperaturabhängigkeit der Reaktionsgeschwindigkeit

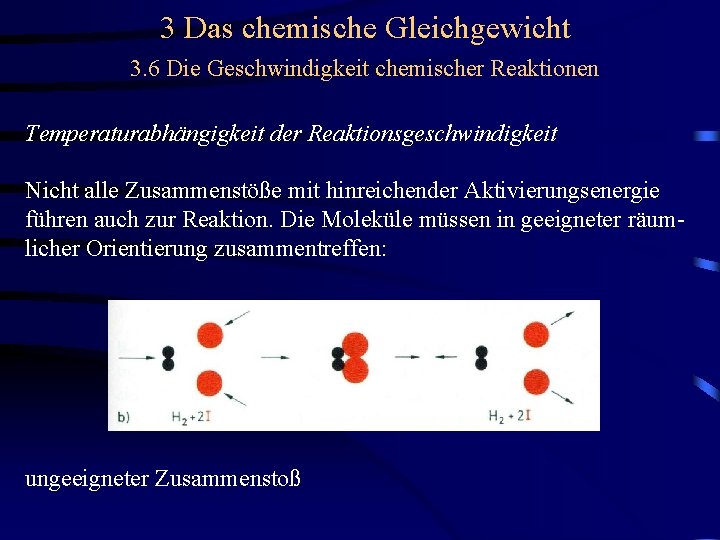
3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Temperaturabhängigkeit der Reaktionsgeschwindigkeit Nicht alle Zusammenstöße mit hinreichender Aktivierungsenergie führen auch zur Reaktion. Die Moleküle müssen in geeigneter räumlicher Orientierung zusammentreffen:

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Temperaturabhängigkeit der Reaktionsgeschwindigkeit Nicht alle Zusammenstöße mit hinreichender Aktivierungsenergie führen auch zur Reaktion. Die Moleküle müssen in geeigneter räumlicher Orientierung zusammentreffen: ungeeigneter Zusammenstoß

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Temperaturabhängigkeit der Reaktionsgeschwindigkeit Nicht alle Zusammenstöße mit hinreichender Aktivierungsenergie führen auch zur Reaktion. Die Moleküle müssen in geeigneter räumlicher Orientierung zusammentreffen: geeigneter Zusammenstoß

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Reaktionsgeschwindigkeit und chemisches Gleichgewicht Für die Gleichgewichtsreaktion

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Reaktionsgeschwindigkeit und chemisches Gleichgewicht Für die Gleichgewichtsreaktion

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Reaktionsgeschwindigkeit und chemisches Gleichgewicht Für die Gleichgewichtsreaktion

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Reaktionsgeschwindigkeit und chemisches Gleichgewicht Für die Gleichgewichtsreaktion

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Reaktionsgeschwindigkeit und chemisches Gleichgewicht Für die Gleichgewichtsreaktion

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Metastabile Systeme Bei hinreichend großer Aktivierungsenergie EA kann bei Normaltemperatur die Reaktionsgeschwindigkeit nahezu null werden.

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Metastabile Systeme Bei hinreichend großer Aktivierungsenergie EA kann bei Normaltemperatur die Reaktionsgeschwindigkeit nahezu null werden. H 2 + Cl 2 H 2 + 0. 5 O 2 2 HCl H 2 O

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Metastabile Systeme Bei hinreichend großer Aktivierungsenergie EA kann bei Normaltemperatur die Reaktionsgeschwindigkeit nahezu null werden. H 2 + Cl 2 H 2 + 0. 5 O 2 2 HCl H 2 O Trotzdem für beide Rkn. das GG weit rechts liegt, sind Mischungen aus Wasserstoff /Chlor oder Wasserstoff/Sauerstoff bei Normaltemperatur stabil.

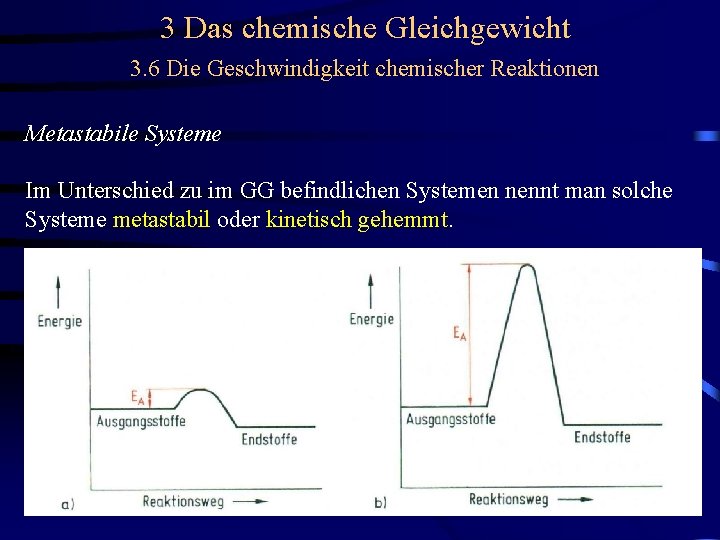
3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Metastabile Systeme Bei hinreichend großer Aktivierungsenergie EA kann bei Normaltemperatur die Reaktionsgeschwindigkeit nahezu null werden. H 2 + Cl 2 H 2 + 0. 5 O 2 2 HCl H 2 O Trotzdem für beide Rkn. das GG weit rechts liegt, sind Mischungen aus Wasserstoff /Chlor oder Wasserstoff/Sauerstoff bei Normaltemperatur stabil. Im Unterschied zu im GG befindlichen Systemen nennt man solche Systeme metastabil oder kinetisch gehemmt.

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Metastabile Systeme Im Unterschied zu im GG befindlichen Systemen nennt man solche Systeme metastabil oder kinetisch gehemmt.

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Metastabile Systeme Im Unterschied zu im GG befindlichen Systemen nennt man solche Systeme metastabil oder kinetisch gehemmt. Eine Aufhebung der Hemmung (Aktivierung) kann durch + Zuführung von Energie (DT oder hn)

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Metastabile Systeme Im Unterschied zu im GG befindlichen Systemen nennt man solche Systeme metastabil oder kinetisch gehemmt. Eine Aufhebung der Hemmung (Aktivierung) kann durch + + Zuführung von Energie (DT oder hn) oder durch Katalysatoren erfolgen.

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Metastabile Systeme Im Unterschied zu im GG befindlichen Systemen nennt man solche Systeme metastabil oder kinetisch gehemmt. Eine Aufhebung der Hemmung (Aktivierung) kann durch + + Zuführung von Energie (DT oder hn) oder durch Katalysatoren erfolgen. Bei Knallgas- oder Chlorknallgasgemischen Zündung durch Flamme, Lichtquanten oder Platinkontakt.

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Metastabile Systeme Bei Knallgas- oder Chlorknallgasgemischen Zündung durch Flamme, Lichtquanten oder Platinkontakt.

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Metastabile Systeme Bei Knallgas- oder Chlorknallgasgemischen Zündung durch Flamme, Lichtquanten oder Platinkontakt.

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Metastabile Systeme Bei Knallgas- oder Chlorknallgasgemischen Zündung durch Flamme, Lichtquanten oder Platinkontakt.

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Metastabile Systeme Bei Knallgas- oder Chlorknallgasgemischen Zündung durch Flamme, Lichtquanten oder Platinkontakt. Für Brom verläuft die Rkn. analog; für Iod beginnt die radikalische HIBildung erst oberhalb 500 °C, da die b. ) Rkn. stark endotherm ist.

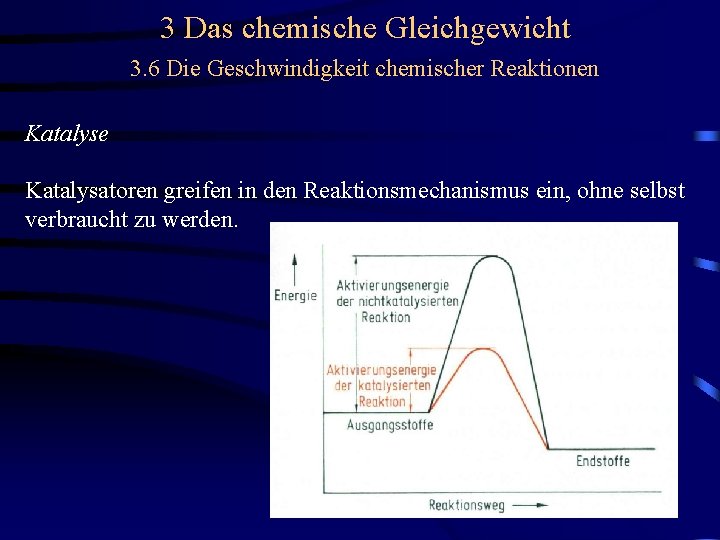
3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Katalyse Katalysatoren greifen in den Reaktionsmechanismus ein, ohne selbst verbraucht zu werden.

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Katalyse Katalysatoren greifen in den Reaktionsmechanismus ein, ohne selbst verbraucht zu werden.

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Katalyse Beispiel: hohe Aktivierungsenergie

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Katalyse Beispiel: hohe Aktivierungsenergie niedrige Aktivierungsenergie

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Katalyse Beispiel: hohe Aktivierungsenergie niedrige Aktivierungsenergie Diese Prozesse spielen bei der früher vorherrschenden Schwefelsäureerzeugung nach dem Bleikammerverfahren eine bedeutende Rolle.

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Katalyse unterschieden werden: homogene Katalyse und heterogene Katalyse (auch „Kontakt“; oft aufgebracht auf Trägermaterial. Erhöhung der Aktivität durch Promotoren. )

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Katalyse unterschieden werden: homogene Katalyse und heterogene Katalyse (auch „Kontakt“; oft aufgebracht auf Trägermaterial. Erhöhung der Aktivität durch Promotoren. ) Fremdstoffmengen können Katalysatoren unbrauchbar machen.

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Katalyse unterschieden werden: homogene Katalyse und heterogene Katalyse (auch „Kontakt“; oft aufgebracht auf Trägermaterial. Erhöhung der Aktivität durch Promotoren. ) Fremdstoffmengen können Katalysatoren unbrauchbar machen. (Kontaktgifte; z. B. : H 2 S, As, Pb, Hg)

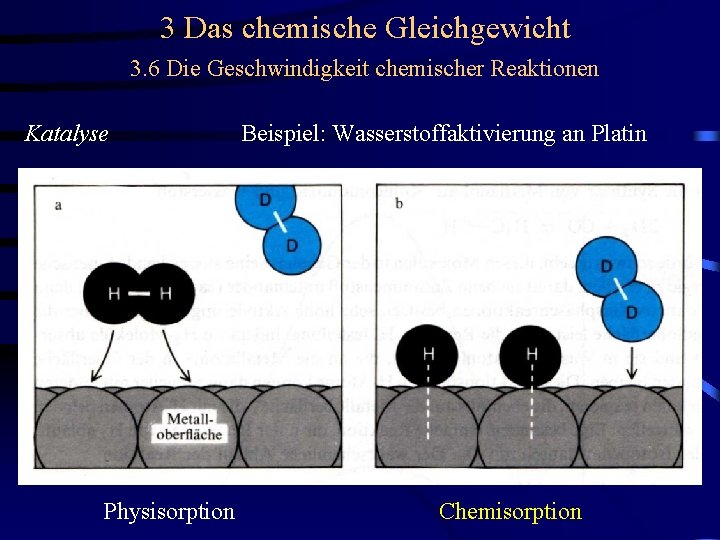
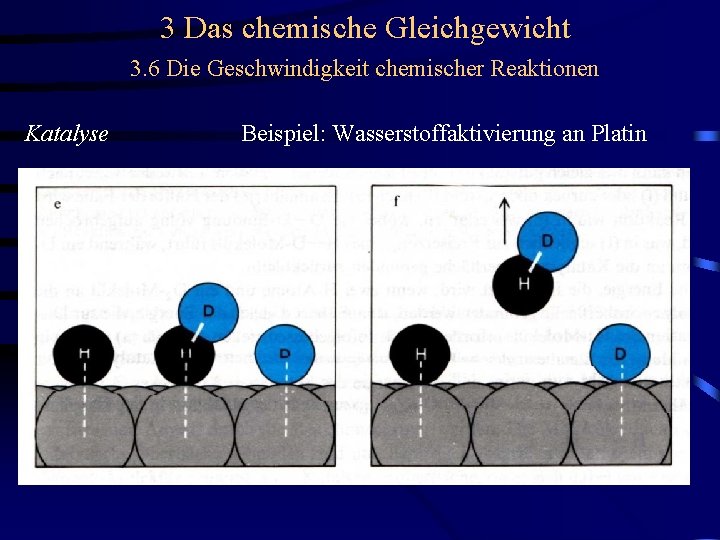
3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Katalyse Beispiel: Wasserstoffaktivierung an Platin Johann Döbereiner (1780 - 1849), Prof. in Jena und Freund Goethes

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Katalyse Beispiel: Wasserstoffaktivierung an Platin Döbereinersches Feuerzeug (ab 1823)

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Katalyse Beispiel: Wasserstoffaktivierung an Platin Döbereinersches Feuerzeug (ab 1823)

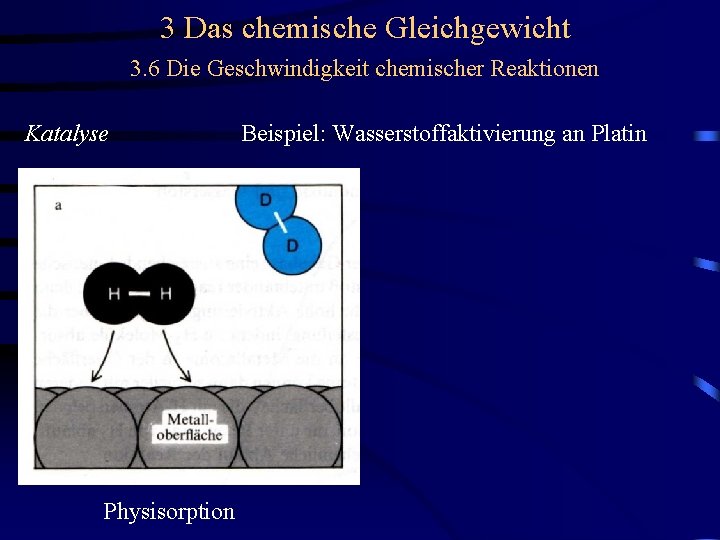
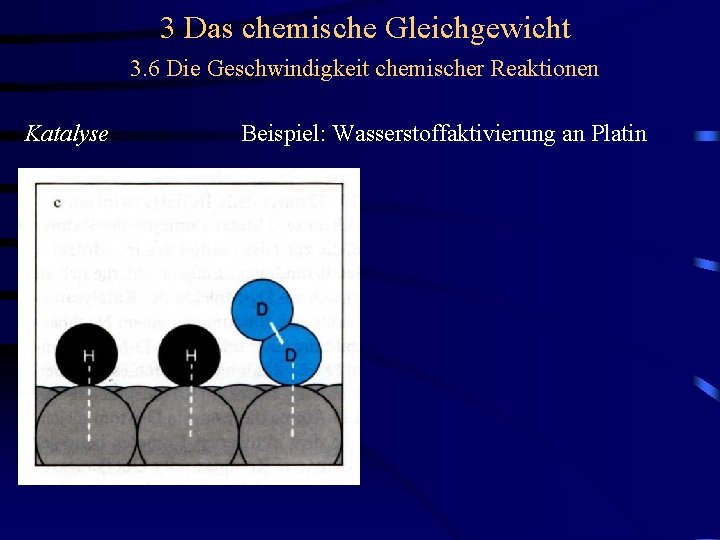
3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Katalyse Physisorption Beispiel: Wasserstoffaktivierung an Platin

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Katalyse Physisorption Beispiel: Wasserstoffaktivierung an Platin Chemisorption

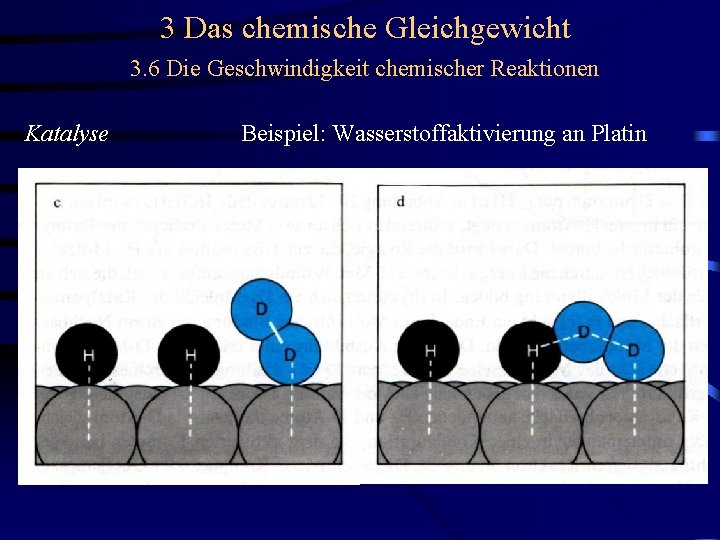
3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Katalyse Beispiel: Wasserstoffaktivierung an Platin

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Katalyse Beispiel: Wasserstoffaktivierung an Platin

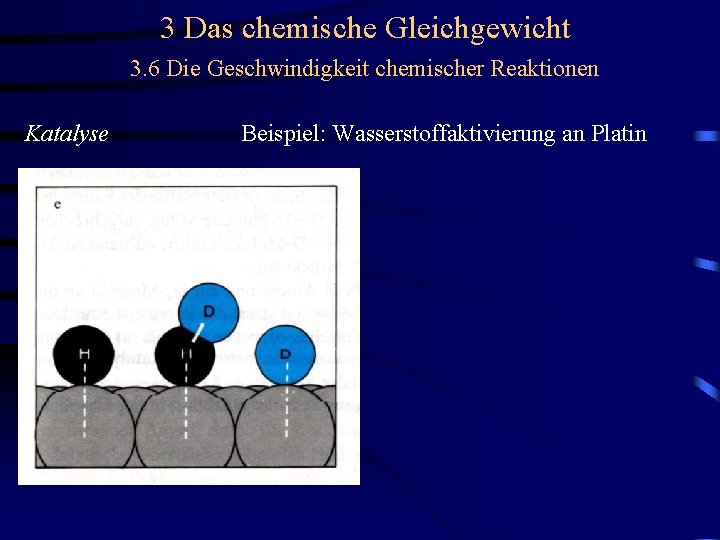
3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Katalyse Beispiel: Wasserstoffaktivierung an Platin

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Katalyse Beispiel: Wasserstoffaktivierung an Platin

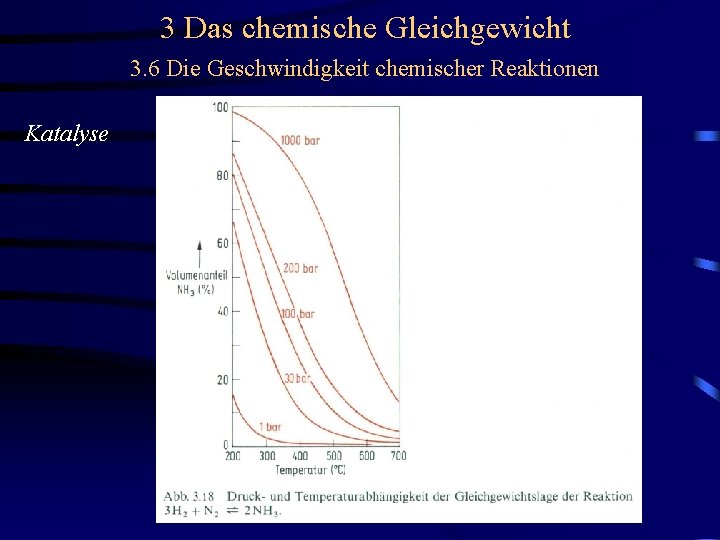
3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Katalyse Beispiel: Ammoniaksythese

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Katalyse Beispiel: Ammoniaksythese Katalysator: a-Fe Trägermaterial: Aluminium-, Calcium- und Kaliumoxid wirken gleichzeitig als Promotoren (Strukturpromot. )

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Katalyse Beispiel: Ammoniaksythese Katalysator: a-Fe Trägermaterial: Aluminium-, Calcium- und Kaliumoxid wirken gleichzeitig als Promotoren (Strukturpromot. ) Bedingungen: ca. 500 °C, 250 - 1000 bar

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Katalyse Beispiel: Ammoniaksythese

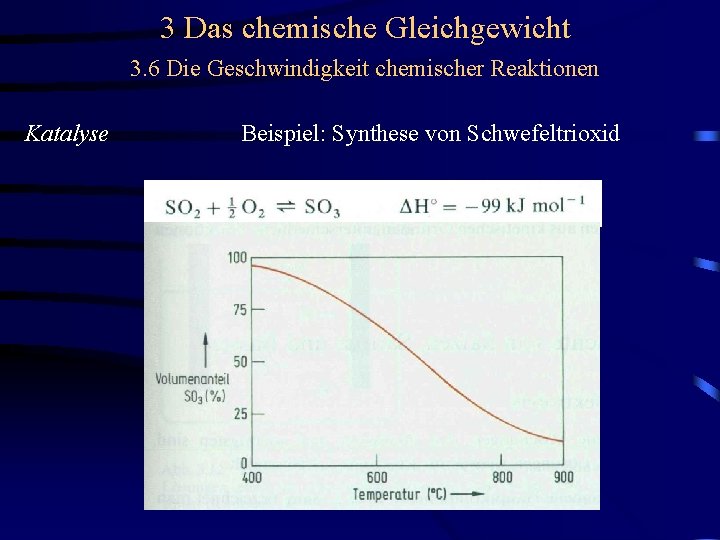
3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Katalyse Beispiel: Synthese von Schwefeltrioxid

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Katalyse Beispiel: Synthese von Schwefeltrioxid

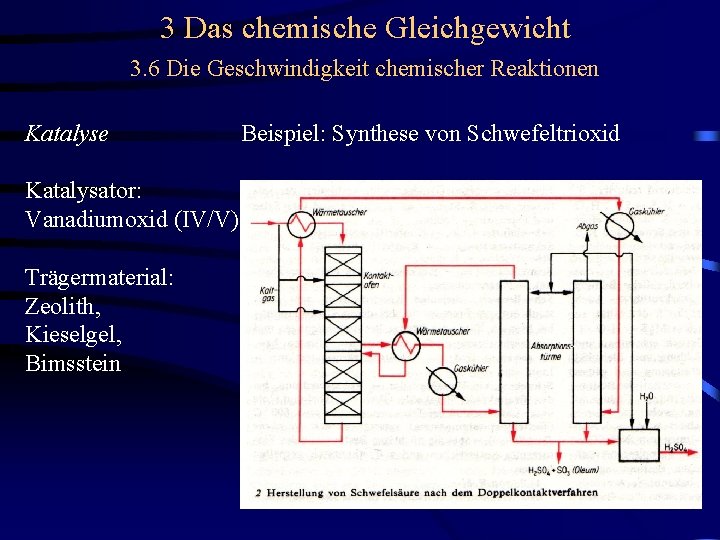
3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Katalyse Beispiel: Synthese von Schwefeltrioxid Katalysator: Vanadiumoxid (IV/V) Trägermaterial: Zeolith, Kieselgel, Bimsstein

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Katalyse Katalysator: Vanadiumoxid (IV/V) Trägermaterial: Zeolith, Kieselgel, Bimsstein Beispiel: Synthese von Schwefeltrioxid

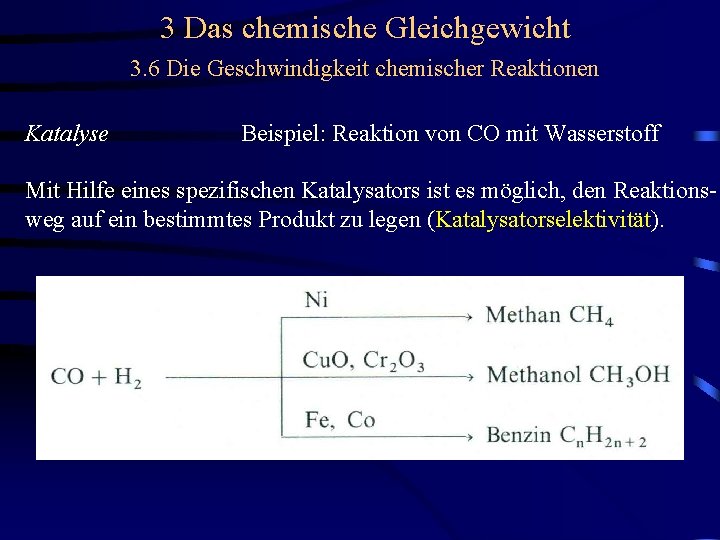
3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Katalyse Beispiel: Reaktion von CO mit Wasserstoff

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Katalyse Beispiel: Reaktion von CO mit Wasserstoff Mit Hilfe eines spezifischen Katalysators ist es möglich, den Reaktionsweg auf ein bestimmtes Produkt zu legen (Katalysatorselektivität).

3 Das chemische Gleichgewicht 3. 6 Die Geschwindigkeit chemischer Reaktionen Katalyse Beispiel: Reaktion von CO mit Wasserstoff Mit Hilfe eines spezifischen Katalysators ist es möglich, den Reaktionsweg auf ein bestimmtes Produkt zu legen (Katalysatorselektivität).

3 Das chemische Gleichgewicht 3. 7 Gleichgewichte von Salzen, Säuren und Basen Lösungen, Elekrolyte Lösungen sind homogene Mischungen. Nach Aggregatzustand kann man unterscheiden: + Gasmischungen

3 Das chemische Gleichgewicht 3. 7 Gleichgewichte von Salzen, Säuren und Basen Lösungen, Elekrolyte Lösungen sind homogene Mischungen. Nach Aggregatzustand kann man unterscheiden: + Gasmischungen + flüssige Lösungen

3 Das chemische Gleichgewicht 3. 7 Gleichgewichte von Salzen, Säuren und Basen Lösungen, Elekrolyte Lösungen sind homogene Mischungen. Nach Aggregatzustand kann man unterscheiden: + Gasmischungen + flüssige Lösungen + feste Lösungen (z. B. : Legierungen)

3 Das chemische Gleichgewicht 3. 7 Gleichgewichte von Salzen, Säuren und Basen Lösungen, Elekrolyte Lösung Hauptkomponente Lösungsmittel Nebenkomponenten gelöste Stoffe

3 Das chemische Gleichgewicht 3. 7 Gleichgewichte von Salzen, Säuren und Basen Lösungen, Elekrolyte

3 Das chemische Gleichgewicht 3. 7 Gleichgewichte von Salzen, Säuren und Basen Lösungen, Elekrolyte

3 Das chemische Gleichgewicht 3. 7 Gleichgewichte von Salzen, Säuren und Basen Lösungen, Elekrolyte

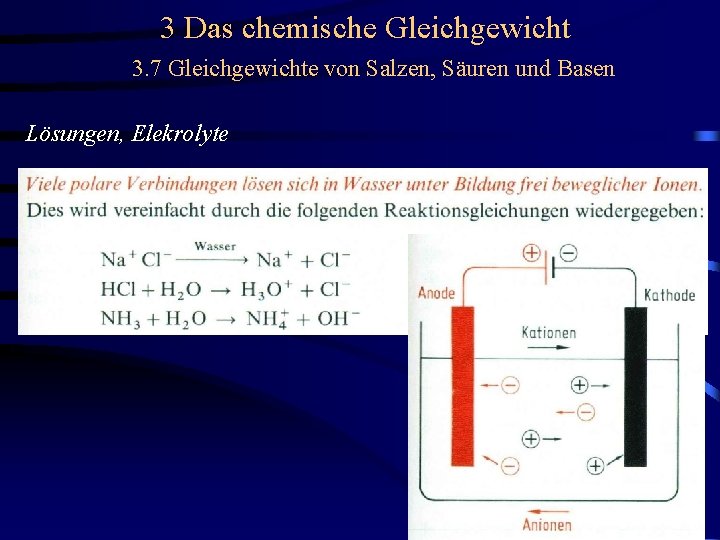
3 Das chemische Gleichgewicht 3. 7 Gleichgewichte von Salzen, Säuren und Basen Lösungen, Elekrolyte Stoffe, die unter Bildung von Ionen in Lösung gehen, nennt man Elektrolyte.

3 Das chemische Gleichgewicht 3. 7 Gleichgewichte von Salzen, Säuren und Basen Lösungen, Elekrolyte

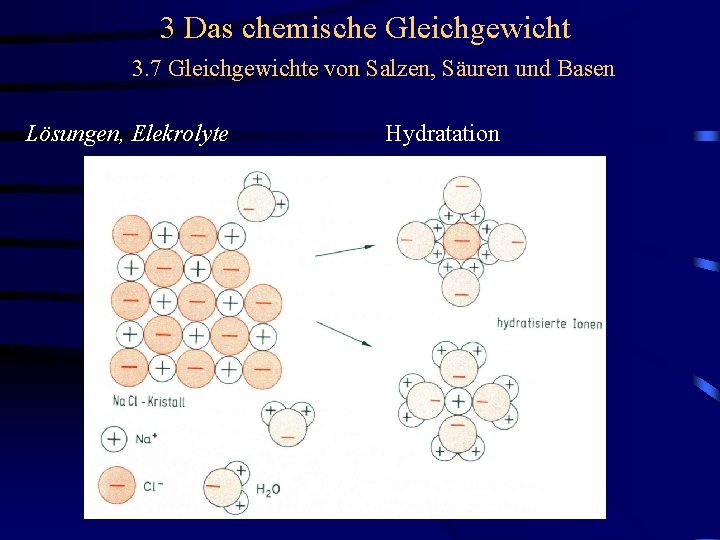
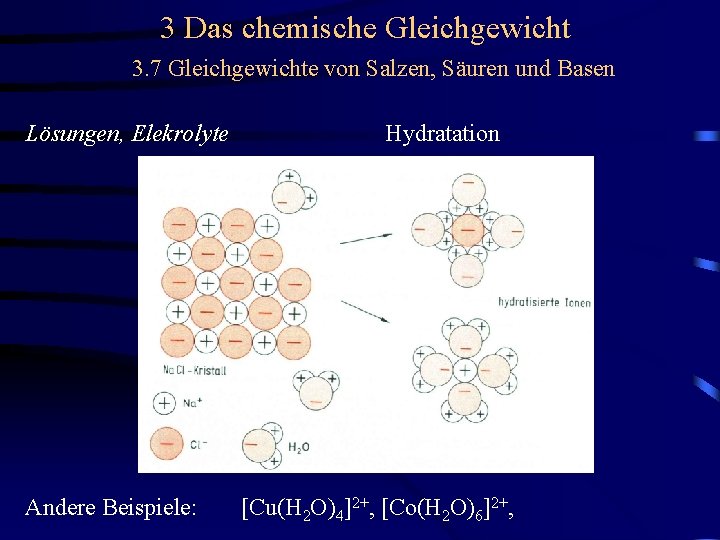
3 Das chemische Gleichgewicht 3. 7 Gleichgewichte von Salzen, Säuren und Basen Lösungen, Elekrolyte Hydratation

3 Das chemische Gleichgewicht 3. 7 Gleichgewichte von Salzen, Säuren und Basen Lösungen, Elekrolyte Andere Beispiele: Hydratation [Cu(H 2 O)4]2+, [Co(H 2 O)6]2+,

3 Das chemische Gleichgewicht 3. 7 Gleichgewichte von Salzen, Säuren und Basen Lösungen, Elekrolyte Hydratation Die Hydratationsenthalpie ist umso größer, je kleiner das Ion und je höher die Ionenladung ist.

3 Das chemische Gleichgewicht 3. 7 Gleichgewichte von Salzen, Säuren und Basen Lösungen, Elekrolyte In Elektrolytlösungen ablaufende Rkn. sind Ionenreaktionen. Die hohen Geschwindigkeiten von Ionenreaktionen führen zu praktisch sofortiger GG-Einstellung.

3 Das chemische Gleichgewicht 3. 7 Gleichgewichte von Salzen, Säuren und Basen Lösungen, Elekrolyte In Elektrolytlösungen ablaufende Rkn. sind Ionenreaktionen. Die hohen Geschwindigkeiten von Ionenreaktionen führen zu praktisch sofortiger GG-Einstellung. Bei sehr kleiner Ionenkonzentration spricht man von idealen Lösungen.

3 Das chemische Gleichgewicht 3. 7 Gleichgewichte von Salzen, Säuren und Basen Lösungen, Elekrolyte In Elektrolytlösungen ablaufende Rkn. sind Ionenreaktionen. Die hohen Geschwindigkeiten von Ionenreaktionen führen zu praktisch sofortiger GG-Einstellung. Bei sehr kleiner Ionenkonzentration spricht man von idealen Lösungen. Bei höheren Ionenkonzentrationen müssen WW zwischen den Ionen berücksichtigt werden. Dies führt zu einer kleineren als der wirklichen Konzentration, der sog. „wirksamen Konzentration“.

3 Das chemische Gleichgewicht 3. 7 Gleichgewichte von Salzen, Säuren und Basen Lösungen, Elekrolyte Bei sehr kleiner Ionenkonzentration spricht man von idealen Lösungen. Bei höheren Ionenkonzentrationen müssen WW zwischen den Ionen berücksichtigt werden. Dies führt zu einer kleineren als der wirklichen Konzentration, der sog. „wirksamen Konzentration“. man definiert auch die Aktivität a: a = f. c/co

3 Das chemische Gleichgewicht 3. 7 Gleichgewichte von Salzen, Säuren und Basen Lösungen, Elekrolyte Bei sehr kleiner Ionenkonzentration spricht man von idealen Lösungen. Bei höheren Ionenkonzentrationen müssen WW zwischen den Ionen berücksichtigt werden. Dies führt zu einer kleineren als der wirklichen Konzentration, der sog. „wirksamen Konzentration“. man definiert auch die Aktivität a: a = f. c/co Für ideale L. ist a = 1.

3 Das chemische Gleichgewicht 3. 7 Gleichgewichte von Salzen, Säuren und Basen Löslichkeit, Löslichkeitsprodukt, Nernstsches Verteilungsgesetz + gesättigte Lösung

3 Das chemische Gleichgewicht 3. 7 Gleichgewichte von Salzen, Säuren und Basen Löslichkeit, Löslichkeitsprodukt, Nernstsches Verteilungsgesetz + gesättigte Lösung

3 Das chemische Gleichgewicht 3. 7 Gleichgewichte von Salzen, Säuren und Basen Löslichkeit, Löslichkeitsprodukt, Nernstsches Verteilungsgesetz + gesättigte Lösung das Löslichkeitsprodukt LAB

3 Das chemische Gleichgewicht 3. 7 Gleichgewichte von Salzen, Säuren und Basen Löslichkeit, Löslichkeitsprodukt, Nernstsches Verteilungsgesetz + gesättigte Lösung

3 Das chemische Gleichgewicht 3. 7 Gleichgewichte von Salzen, Säuren und Basen Löslichkeit, Löslichkeitsprodukt, Nernstsches Verteilungsgesetz + gesättigte Lösung

3 Das chemische Gleichgewicht 3. 7 Gleichgewichte von Salzen, Säuren und Basen Löslichkeit, Löslichkeitsprodukt, Nernstsches Verteilungsgesetz + übersättigte Lösung

3 Das chemische Gleichgewicht 3. 7 Gleichgewichte von Salzen, Säuren und Basen Löslichkeit, Löslichkeitsprodukt, Nernstsches Verteilungsgesetz + übersättigte Lösung

3 Das chemische Gleichgewicht 3. 7 Gleichgewichte von Salzen, Säuren und Basen Löslichkeit, Löslichkeitsprodukt, Nernstsches Verteilungsgesetz Löslichkeitsprodukte für Salze vom Typ AB 2

3 Das chemische Gleichgewicht 3. 7 Gleichgewichte von Salzen, Säuren und Basen Löslichkeit, Löslichkeitsprodukt, Nernstsches Verteilungsgesetz Löslichkeitsprodukte für Salze vom Typ AB 2 und A 2 B 3

3 Das chemische Gleichgewicht 3. 7 Gleichgewichte von Salzen, Säuren und Basen Löslichkeit, Löslichkeitsprodukt, Nernstsches Verteilungsgesetz Löslichkeitsprodukte

3 Das chemische Gleichgewicht 3. 7 Gleichgewichte von Salzen, Säuren und Basen Löslichkeit, Löslichkeitsprodukt, Nernstsches Verteilungsgesetz Fällungsreaktionen

3 Das chemische Gleichgewicht 3. 7 Gleichgewichte von Salzen, Säuren und Basen Löslichkeit, Löslichkeitsprodukt, Nernstsches Verteilungsgesetz Das Verteilungsgesetz von Nernst

3 Das chemische Gleichgewicht 3. 7 Gleichgewichte von Salzen, Säuren und Basen Löslichkeit, Löslichkeitsprodukt, Nernstsches Verteilungsgesetz Das Verteilungsgesetz von Nernst Beispiel; Verteilung von Iod zwischen Chloroform und Wasser

3 Das chemische Gleichgewicht 3. 7 Gleichgewichte von Salzen, Säuren und Basen Löslichkeit, Löslichkeitsprodukt, Nernstsches Verteilungsgesetz Das Verteilungsgesetz von Nernst Beispiel; Verteilung von Iod zwischen Chloroform und Wasser