Zuren en basen Zure stoffen kennen we allemaal

Zuren en basen Zure stoffen kennen we allemaal: azijn of citroen Wanneer is een stof nu zuur of basisch ? ?

Indicatoren (Tabel 52 A)
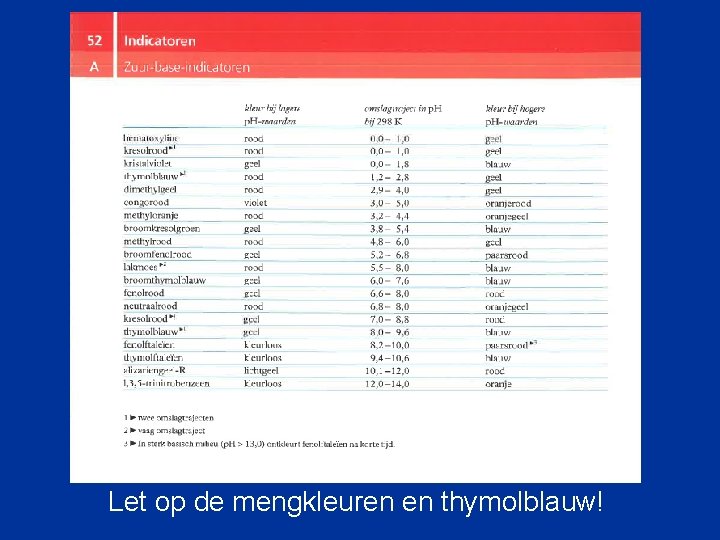
Let op de mengkleuren en thymolblauw!

Universeel Indicatorpapier Lakmoespapier

Zuren en basen Zuur: kan H+ afstaan Base: kan H+ opnemen Vaak negatief geladen of bevat N atoom Hoe weet je of een stof zuur of basisch is ? ? ? In BINAS T 49 staan een groot aantal van de zuren en basen die veel gebruikt worden vermeld. Linker kolom de zuren en rechterkolom de basen
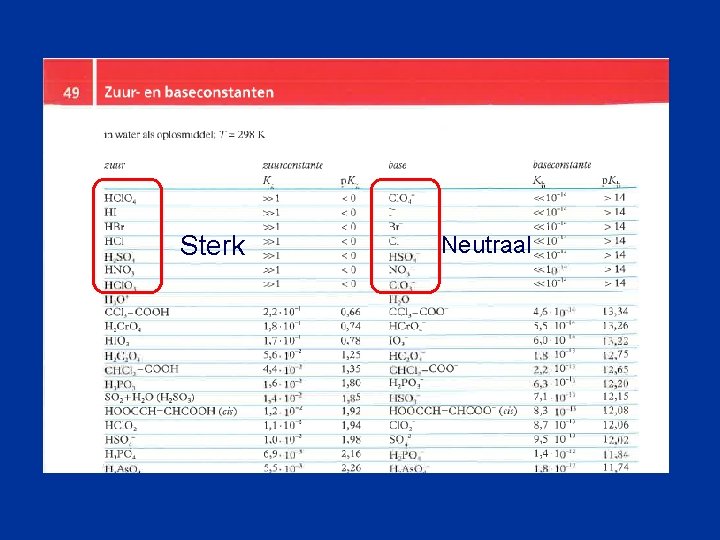
Sterk Neutraal

Sterke zuren: (staan water alle H+ af) • • • HCl HBr HI HNO 3 H 2 SO 4 waterstofchloride waterstofbromide waterstofjodide salpeterzuur zwavelzuur (tweewaardig sterk zuur)

Oplossen van een sterk zuur Alle zuurdeeltjes staan H+ af, ze splitsen volledig. Bv: oplossen salpeterzuur in water HNO 3 + H 2 O H 3 O+ + NO 3 oxonium- ion Zure oplossingen kunnen stroom geleiden.

LET OP! • zoutzuur is een oplossing van HCl Notatie: H 3 O + + Cl-

Zwakke zuren • • • (staan bijna geen H+ aan water af) (evenwicht) HF waterstoffluoride CH 3 COOH (HAC) azijnzuur H 2 C 2 O 4 oxaalzuur H 2 S waterstofsulfide H 3 PO 4 fosforzuur H 2 CO 3 koolzuur

Oplossen van een zwak zuur Bv: oplossen ammoniumnitraat in water Stap 1: aq NH 4 NO 3 NH 4+ + NO 3 Stap 2: NH 4+ + H 2 O NH 3 + H 3 O+ Niet alle zuurdeeltjes staan H + af er is evenwicht

Wat staat er op een etiket? • Sterk zure oplossing (altijd gesplitst): H 3 O+(aq) + …. . (aq) • Zwak zure oplossingen (nooit gesplitst): HCN (aq)

8. 4 Formules en namen van zuren • Organische zuren Bevatten C, H en O • Anorganische zuren Bevatten geen koolstofskelet Bijvoorbeeld: HCl, koolzuur • Ionen Bijvoorbeeld: ammonium, Fe(H 2 O)63+
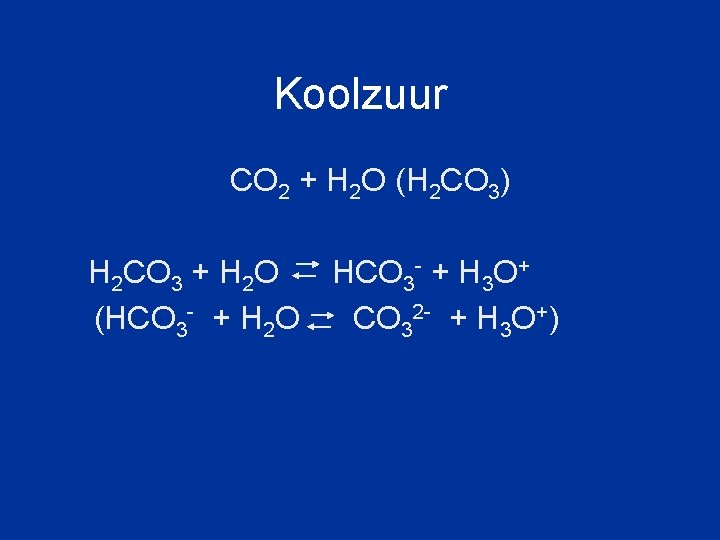
Koolzuur CO 2 + H 2 O (H 2 CO 3) H 2 CO 3 + H 2 O (HCO 3 - + H 2 O HCO 3 - + H 3 O+ CO 32 - + H 3 O+)
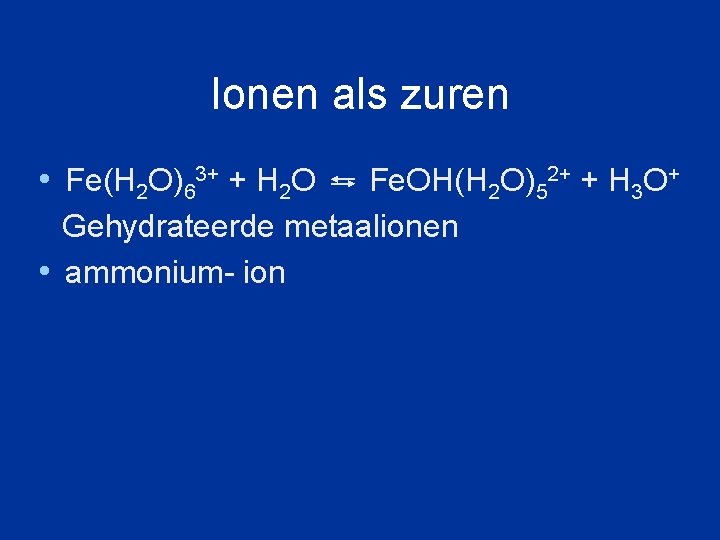
Ionen als zuren • Fe(H 2 O)63+ + H 2 O Fe. OH(H 2 O)52+ + H 3 O+ Gehydrateerde metaalionen • ammonium- ion
![8. 5 PH- berekeningen Welke relatie kan je afleiden tussen [H+] en p. H? 8. 5 PH- berekeningen Welke relatie kan je afleiden tussen [H+] en p. H?](http://slidetodoc.com/presentation_image_h/cc1ba2d1dd2a36f7330605e3bf38577d/image-17.jpg)
8. 5 PH- berekeningen Welke relatie kan je afleiden tussen [H+] en p. H?
![Zuren en basen: [H 3 O+] vs p. H = - log [H 3 Zuren en basen: [H 3 O+] vs p. H = - log [H 3](http://slidetodoc.com/presentation_image_h/cc1ba2d1dd2a36f7330605e3bf38577d/image-18.jpg)
Zuren en basen: [H 3 O+] vs p. H = - log [H 3 O+] = 10 -p. H

Zwavelzuur • Splitst twee H+ af en geeft dus 2 H 3 O+ • Bereken de p. H van 0, 01 M zwavelzuuroplossing • Significantie wordt bepaald door het aantal decimalen van de gegeven p. H.

p. H oplossing zwak zuur • • • Kz= zuurconstante Hoe lager de Kz hoe zwakker het zuur. Alleen afhankelijk van de temperatuur [H 2 O]= constant = 1 Evenwichtsconstante:

Zwak zuur berekening B ∆ E HZ (aq) + H 2 O Z- (aq) + H 3 O+ (aq) 0, 10 0 0 -x +x +x 0, 10 -x x x • Kz =[Z- ]. [H 3 O+] [HZ] • Kz = x 2 (0, 10 – x) abc- formule gebruiken

Zwak zuur berekening • p. H van 0, 10 M HNO 2 -oplossing berekenen • HNO 2 niet 100% geïoniseerd, dus met zuurconstante • • berekenen. HNO 2(aq) + H 2 O(l) NO 2 - (aq)+ B 0, 10 0 ∆ -x +x E 0, 10 -x x - ]. [H O+] = 5, 6. 10 -4 = [NO 2 3 • Kz [HNO 2] • x = [H 3 O+] ? H 3 O+(aq) 0 +x x

x 2 = 5, 6. 10 -4 0, 10 - x Hieruit volgt: x 2 + 5, 6. 10 -4 x - 5, 6. 10 -5 = 0 a= 1; b= 5, 6. 10 -4; c= -5. 6. 10 -5 Invullen in: x=7, 2 E-3 p. H= 2, 14
- Slides: 23