3 Das chemische Gleichgewicht 3 8 Redoxvorgnge Elektrolyse





















































- Slides: 60

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrolyse

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrolyse

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrolyse

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrolyse

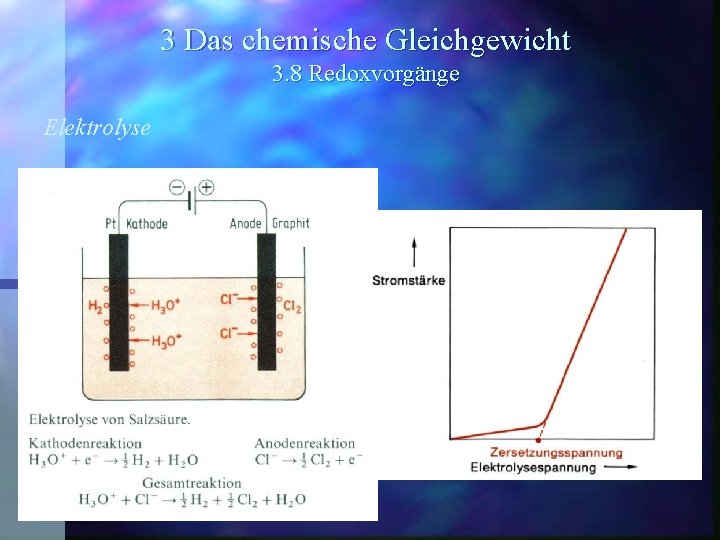
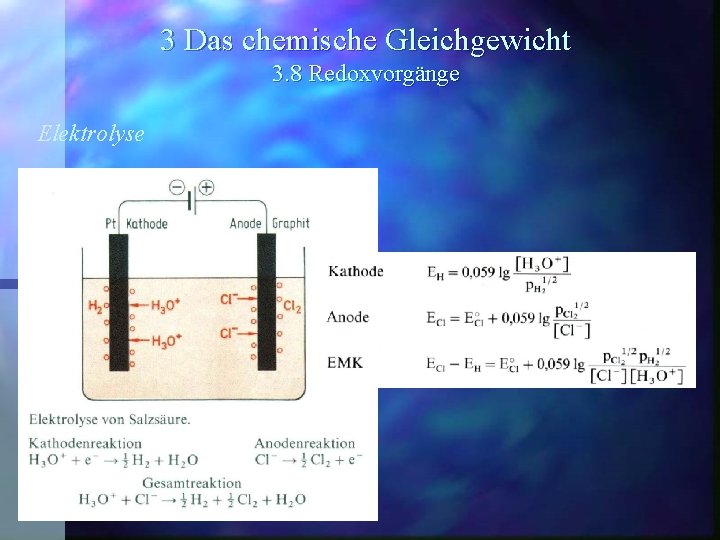
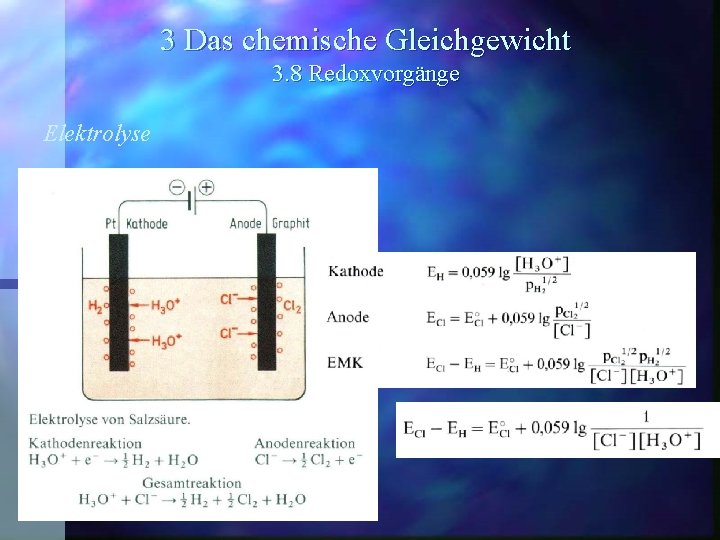
3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrolysiert man eine wäßrige Lösung , die verschiedene Ionensorten enthält, so scheiden sich mit wachsender Spannung die einzelnen Ionensorten nacheinander ab.

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrolysiert man eine wäßrige Lösung , die verschiedene Ionensorten enthält, so scheiden sich mit wachsender Spannung die einzelnen Ionensorten nacheinander ab. An der Kathode wird zuerst die Kationensorte mit dem positivsten Potential entladen. Je edler ein Metall ist, umso leichter sind seine Ionen reduzierbar.

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrolysiert man eine wäßrige Lösung , die verschiedene Ionensorten enthält, so scheiden sich mit wachsender Spannung die einzelnen Ionensorten nacheinander ab. An der Kathode wird zuerst die Kationensorte mit dem positivsten Potential entladen. Je edler ein Metall ist, umso leichter sind seine Ionen reduzierbar. An der Anode werden zuerst diejenigen Ionen oxidiert, die negativsten Redoxpotentiale haben.

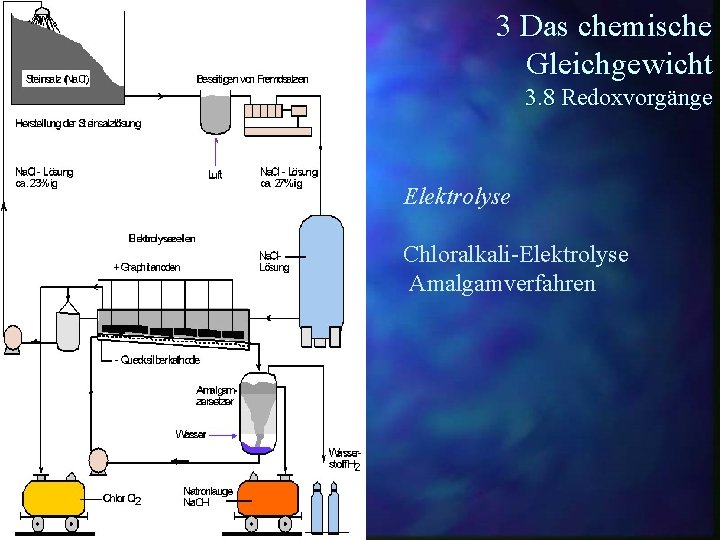
3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrolyse Chloralkali-Elektrolyse

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrolyse Chloralkali-Elektrolyse

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrolyse Chloralkali-Elektrolyse

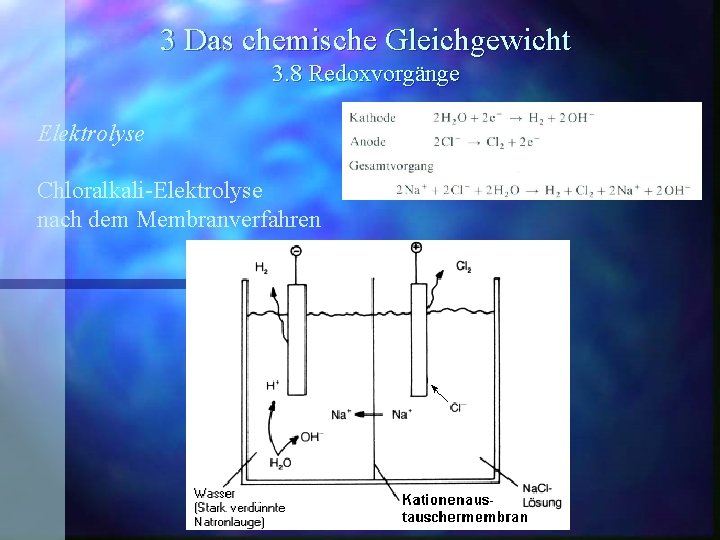
3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrolyse Chloralkali-Elektrolyse nach dem Membranverfahren

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrolyse Chloralkali-Elektrolyse Amalgamverfahren

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrolyse Chloralkali-Elektrolyse Amalgamverfahren

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrolyse Chloralkali-Elektrolyse Amalgamverfahren

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrolyse Äquivalent Ein Äquivalent ist der Bruchteil 1/z* eines Teilchens X. z* wird Äquivalentzahl genannt.

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrolyse Äquivalent Ein Äquivalent ist der Bruchteil 1/z* eines Teilchens X. z* wird Äquivalentzahl genannt. Beispiel Neutralisationsäquivalent (Säure-Base-Äquivalent) 1/2 H 2 SO 4, 1/2 Ba(OH)2, 1/3 H 3 PO 4

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrolyse Äquivalent Ein Äquivalent ist der Bruchteil 1/z* eines Teilchens X. z* wird Äquivalentzahl genannt. Beispiel Redoxäquivalent (Aufnahme oder Abgabe eines Elektrons) 1/5 KMn. O 4, 1/6 K 2 Cr 2 O 7

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrolyse Äquivalent Ein Äquivalent ist der Bruchteil 1/z* eines Teilchens X. z* wird Äquivalentzahl genannt. Beispiel Ionenäquivalent (Bruchrteils eines Ions, das eine Elementarladung trägt. 1/3 Fe 3+, 1/2 Mg 2+, 1/2 SO 42 -

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrolyse Äquivalent Die Stoffmenge von Äquivalenten ist gleich dem Produkt aus der Äquivalentzahl z* und der Stoffmenge n, bezogen auf die Teilchen X.

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrolyse Äquivalent Die Stoffmenge von Äquivalenten ist gleich dem Produkt aus der Äquivalentzahl z* und der Stoffmenge n, bezogen auf die Teilchen X.

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrolyse Äquivalent

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrolyse Äquivalent

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrolyse Faraday-Gesetz

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrolyse Faraday-Gesetz Durch die Ladungsmenge von 1 F werden 1 mol Ionenäquivalente abgeschieden. Durch 1 F werden also gerade 1 mol Me+-Ionen (Na+, Ag+), 1/2 mol Me 2+-Ionen (Cu 2+, Zn 2+) und 1/3 mol Me 3+-Ionen (Al 3+, Fe 3+) abgeschieden.

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Man unterscheidet Primärelemente und Sekundärelemente

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Man unterscheidet Primärelemente und Sekundärelemente

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Bleiakkumulator

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Bleiakkumulator Besteht aus einer Bleielektrode und einer Bleidioxidelektrode; als Elektrolyt wird ca. 20%ige Schwefelsäure verwendet.

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Bleiakkumulator Besteht aus einer Bleielektrode und einer Bleidioxidelektrode; als Elektrolyt wird ca. 20%ige Schwefelsäure verwendet.

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Bleiakkumulator Besteht aus einer Bleielektrode und einer Bleidioxidelektrode; als Elektrolyt wird ca. 20%ige Schwefelsäure verwendet.

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Bleiakkumulator

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Bleiakkumulator

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Natrium-Schwefel-Akkumulator

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Natrium-Schwefel-Akkumulator Besteht aus bei der Betriebstemperatur von 300 - 350 °C flüssigen Elektroden aus Natrium und Schwefel.

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Natrium-Schwefel-Akkumulator Besteht aus bei der Betriebstemperatur von 300 - 350 °C flüssigen Elektroden aus Natrium und Schwefel. Beide Elektroden sind durch einen für Na+ - Ionen durchlässigen Festelektrolyten voneinander getrennt.

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Natrium-Schwefel-Akkumulator Besteht aus bei der Betriebstemperatur von 300 - 350 °C flüssigen Elektroden aus Natrium und Schwefel. Beide Elektroden sind durch einen für Na+ - Ionen durchlässigen Festelektrolyten voneinander getrennt. Betriebsspannung 2, 08 V

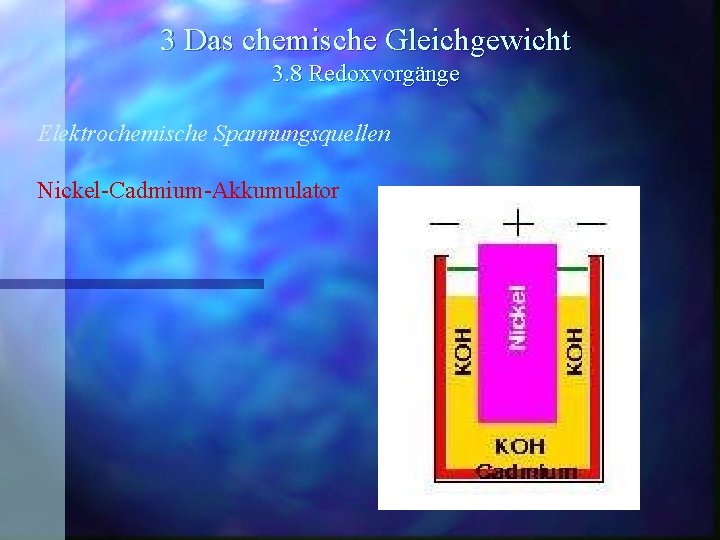
3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Nickel-Cadmium-Akkumulator

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Nickel-Cadmium-Akkumulator

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Nickel-Cadmium-Akkumulator

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Nickel-Cadmium-Akkumulator

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Leclanché-Element

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Leclanché-Element

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Leclanché-Element

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Leclanché-Element

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Leclanché-Element

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Leclanché-Element

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Leclanché-Element

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Leclanché-Element

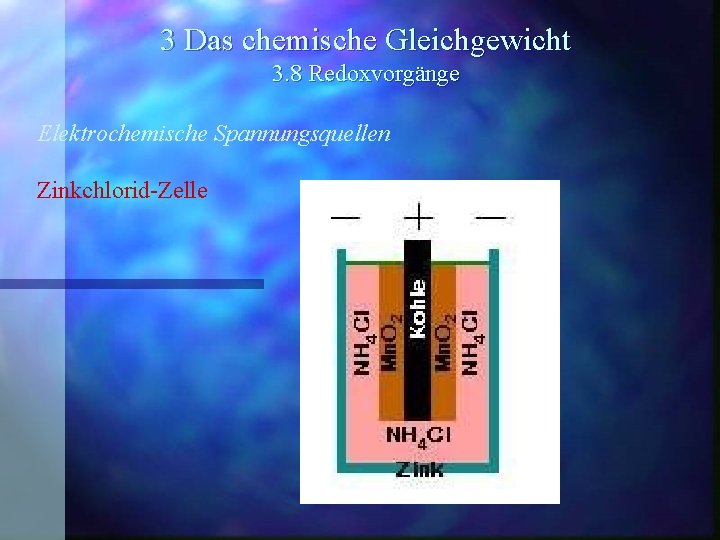
3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Zinkchlorid-Zelle

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Zinkchlorid-Zelle

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Zinkchlorid-Zelle gute Auslaufsicherheit, da Wasser verbraucht wird.

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Zinkchlorid-Zelle

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Alkali-Mangan-Zelle

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Alkali-Mangan-Zelle

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Alkali-Mangan-Zelle Betrieb bis -35 °C.

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Alkali-Mangan-Zelle

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Silber-Zink-Zelle

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Silber-Zink-Zelle

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Silber-Zink-Zelle Betriebsspannung 1, 5 V

3 Das chemische Gleichgewicht 3. 8 Redoxvorgänge Elektrochemische Spannungsquellen Brennstoffzelle