Chemische reacties algemeen kenmerk Bij scheikunde bestuderen we

Chemische reacties: algemeen kenmerk Bij scheikunde bestuderen we stoffen en de eigenschappen van stoffen. Hierbij worden experimenten gedaan waarbij (begin)stoffen verdwijnen en (eind)stoffen hiervoor in de plaats komen Een belangrijk kenmerk van chemische reacties: 1 of meer stoffen verdwijnen en 1 of meer stoffen komen hiervoor in de plaats mlavd@BCEC 1

Chemische reacties en energie Als er thuis gekookt wordt op gas weet je dat bij de verbranding van aardgas energie (in dit geval warmte) vrij komt. In de scheikunde noemen we zo’n reactie dan EXOTHERM - Een exotherme reactie is een reactie waarbij energie (warmte, licht, stroom, etc) vrij komt. - Een exotherme reactie kan zichzelf op gang houden. mlavd@BCEC 2

Chemische reacties en energie De verbranding van gas gebeurt niet spontaan. Je moet er eerst een vlammetje of vonkje bijhouden om de reactie op gang te brengen. In de scheikunde noemen we dit dat de stoffen eerst op reactietemperatuur moeten komen voor ze reageren. - Elke reactie heeft zijn eigen reactietemperatuur. - De energie die nodig is om de reactie op gang te brengen (activeren) noemen we activeringenergie mlavd@BCEC 3

Chemische reacties en energie Het tegengestelde van een reactie waarbij energie vrij komt is een reactie die continu energie nodig heeft om te kunnen verlopen. In de scheikunde noemen we zo’n reactie dan ENDOTHERM - Een endotherme reacties is een reactie waarbij energie verbruikt wordt. - Een endotherme reactie heeft continu energie nodig om te kunnen verlopen. mlavd@BCEC 4

Chemische reacties en energie We kunnen een grafiek maken van de energie die bij een reactie vrij komt of verbruikt wordt. Zo’n grafiek noemen we een ENERGIEDIAGRAM - In een energiediagram wordt aangegeven hoeveel energie er vrijkomt of verbruikt wordt bij een reactie = reactieenergie. - In een energiediagram wordt aangegeven hoeveel energie het kost om de reactie op gang te brengen = activeringsenergie mlavd@BCEC 5
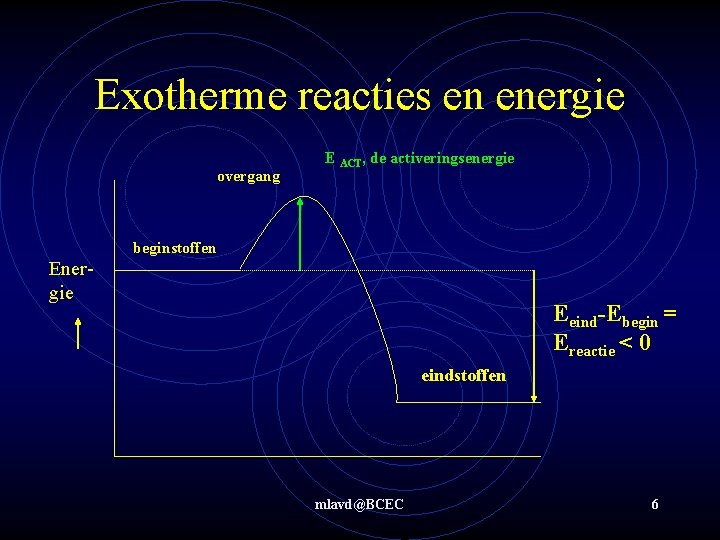
Exotherme reacties en energie overgang E ACT, de activeringsenergie beginstoffen Energie Eeind-Ebegin = Ereactie < 0 eindstoffen mlavd@BCEC 6
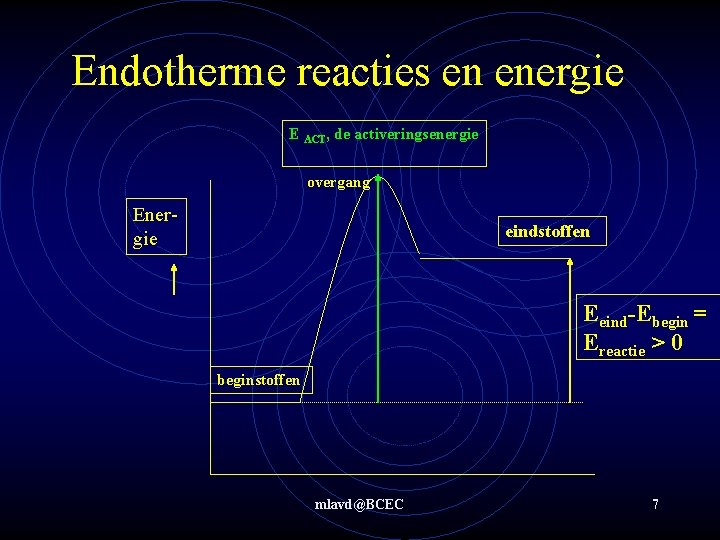
Endotherme reacties en energie E ACT, de activeringsenergie overgang Energie eindstoffen Eeind-Ebegin = Ereactie > 0 beginstoffen mlavd@BCEC 7
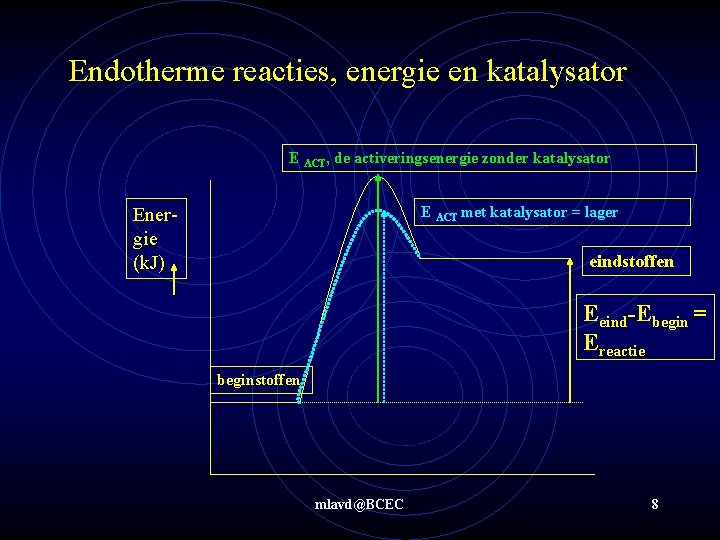
Endotherme reacties, energie en katalysator E ACT, de activeringsenergie zonder katalysator E ACT met katalysator = lager Energie (k. J) eindstoffen Eeind-Ebegin = Ereactie beginstoffen mlavd@BCEC 8
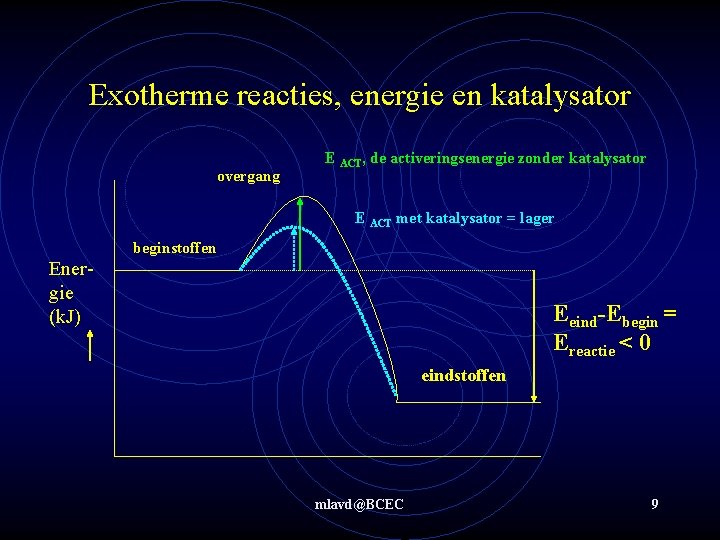
Exotherme reacties, energie en katalysator overgang E ACT, de activeringsenergie zonder katalysator E ACT met katalysator = lager beginstoffen Energie (k. J) Eeind-Ebegin = Ereactie < 0 eindstoffen mlavd@BCEC 9

reacties en energie Opdracht A: Bereken hoeveel energie vrij komt bij de verbranding als door de verbranding van CH 4 100 g water opwarmt van 20 naar 25 ºC. Benodigde Soortelijke warmte van de energie stof die opgewarmd wordt Q = m * C w * ΔT Massa van de stof die opgewarmd wordt Temperatuursverandering van de stof die opgewarmd wordt mlavd@BCEC 10

reacties en energie Q = m * C w * ΔT Q = 100 g * 4, 18 J/(g*°C) * 5 °C = 2090 J Exotherme reactie want ΔT > 0 Q < 0 - 2090 J Opdracht B: bereken hoeveel gram CH 4 verbrand is (gebruik Binas T 56) mlavd@BCEC 11

reacties en energie Opdracht B: bereken hoeveel gram CH 4 verbrand is (gebruik Binas T 56) Q = 2090 J Binas T 56: verbrandingswarmte CH 4 = - 8, 9*105 J/mol Q = 2090 J 2090 J/(8, 9*105 J/mol) = 2, 34*10 -3 mol * 16 g/mol = 0, 0376 g = 3, 76*10 -2 g mlavd@BCEC 12

Verbrandingsreactie = Oxydatie-reactie Wat heb je nodig om een verbrandingsreactie te laten verlopen ? O 2 brand Temperatuur Brandstof mlavd@BCEC 13

Oxydatie-reacties Bij een verbrandings- of oxydatiereactie worden oxiden gevormd, dit zijn verbindingen van het element met zuurstof. Volledige verbranding C + O 2 CO 2 S + O 2 SO 2 2 S + 3 O 2 2 SO 3 2 H 2 + O 2 2 H 2 O Onvolledige verbranding 2 C +O 2 CO mlavd@BCEC 14

Factoren die snelheid bepalen Factoren: - Soort stof - Verdelingsgraad van de stof - Concentratie van de reagerende stoffen - Temperatuur - Katalysator sim 1 / sim 2 mlavd@BCEC 15

Factoren die snelheid bepalen -Animatie: http: //www. chem. iastate. edu/group/Green bowe/sections/projectfolder/flashfiles/kine tics 2/iodine_clock. html -Animatie: http: //www. chem. iastate. edu/group/Green bowe/sections/projectfolder/flashfiles/kine tics 2/kinetics. html mlavd@BCEC 16

Formule van snelheid Bij Na wordt snelheid uitgedrukt in m/s Bij Sk wordt snelheid uitgedrukt in mol/(L*s) Om te voorkomen dat bij het meten van de snelheid verschillende resultaten verkregen worden is een handige formule noodzakelijk. mlavd@BCEC 17

Formule van snelheid A + 2 B 3 C + 0 sec 0, 1 mol 0, 1 mol 0, 0 mol Δ - 0, 05 mol - 0, 1 mol + 0, 15 mol 120 sec 0, 05 mol 0, 0 mol s = - 0, 05/120 mol/L*s 0, 15 mol 4 D 0, 0 mol + 0, 2 mol 0, 2 mol s = + 0, 15/120 mol/L*s s = - 0, 1/120 mol/L*s mlavd@BCEC s = + 0, 2/120 mol/L*s 18

Formule van snelheid A + 2 B 3 C + 4 D s = - 0, 05/120 mol/L*s s = + 0, 15/120 mol/L*s s = - 0, 1/120 mol/L*s s = + 0, 2/120 mol/L*s Bij 1 reactie 4* verschillende snelheid kan niet formule aanpassen voor reactant (A, B) of product (C, D) en reactieverhouding s = -1/1*(-0, 05/120 mol/L*s) = 0, 05/120 mol/L*s s = 1/3*(0, 15/120 mol/L*s) = 0, 05/120 mol/L*s s = -1/2*(-0, 1/120 mol/L*s) = 0, 05/120 mol/L*s mlavd@BCEC s = 1/4*(0, 2/120 mol/L*s) = 0, 05/120 mol/L*s 19

Formule van gemiddelde snelheid sgem is nu voor elke stof: 0, 05/120 mol/L*s Algemene formule voor sgem - reactant: sgem = 1/coefficient*Δ[ ]/Δt (mol/L*s) product: sgem = 1/coefficient*Δ[ ]/Δt (mol/L*s) mlavd@BCEC 20

gemiddelde snelheid Bepaal de gemiddelde snelheid (uitgedrukt in mol A/L*s, mol B/L*s en mol C/L*s voor de volgende reactie: 4 A + 5 B 3 C als gegeven is dat je op t 0 begint met 1, 00 mol A, 4, 00 mol B en je na 10 minuten 0, 50 mol C gevormd hebt in een reactievat van 100 L. to 4 A 1, 0 + 5 B 4, 00 3 C 0, 00 -0, 5*5/3 +0, 5. Δ -0, 5*4/3 Te 0, 33 0, 50 3, 17 Sa= ¼ * (0, 67/100)/600 = 2, 79*10 -6 mol/L*s Sb= 1/5 * (0, 83/100)/600 = 2, 77*10 -6 mol/L*s Sc= 1/3 * (0, 5/100)/600 = 2, 78*10 -6 mol/L*s mlavd@BCEC 21

Botsende deeltjesmodel en factoren die snelheid bepalen Een chemische reactie kan je zien als 2 deeltjes die op de juiste manier met de juiste snelheid botsen en dan van eigenschap veranderen. Dit noemen we een effectieve botsing Als de deeltjes wel botsen maar niet op de juiste manier of met de juiste snelheid botsen treedt er geen reactie op. Dit noemen we een effectieve botsing mlavd@BCEC 22

Botsende deeltjesmodel en snelheidsfactoren - Soort stof: andere stoffen andere effectieve botsing (want andere Eact) - Concentratie van de reagerende stoffen: hoe meer deeltjes in dezelfde ruimte hoe meer botsingen kans op effectieve botsing = reactie neemt toe - Verdelingsgraad van de stof (bij heterogeen systeem): botsing (=reactie) bij vaste stof alleen aan oppervlak Kleinere deeltjes hebben groter oppervlak snellere reactie - Temperatuur: T hoger meer en snellere beweging meer en ‘hardere’ botsingen meer effectieve botsingen snelheid wordt hoger (elke 10 ºC ongeveer 2 tot 2, 5 keer) mlavd@BCEC 23
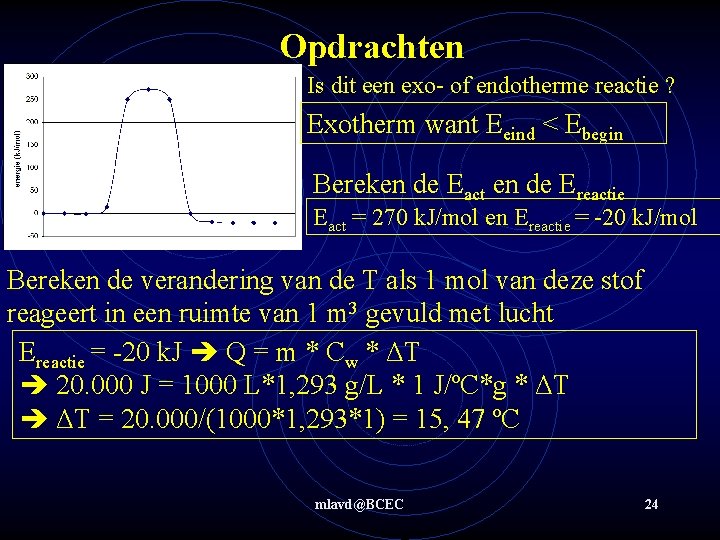
Opdrachten Is dit een exo- of endotherme reactie ? Exotherm want Eeind < Ebegin Bereken de Eact en de Ereactie Eact = 270 k. J/mol en Ereactie = -20 k. J/mol Bereken de verandering van de T als 1 mol van deze stof reageert in een ruimte van 1 m 3 gevuld met lucht Ereactie = -20 k. J Q = m * Cw * ΔT 20. 000 J = 1000 L*1, 293 g/L * 1 J/ºC*g * ΔT = 20. 000/(1000*1, 293*1) = 15, 47 ºC mlavd@BCEC 24

2 N 2 O 5 4 NO 2 + O 2 Opdrachten Geef de formule van de gemiddelde snelheid uitgedrukt in N 2 O 5 , NO 2 en O 2 Sgem N 2 O 5 = -1/2 * d[N 2 O 5]/d. T Sgem NO 2 = 1/4 * d[NO 2]/d. T Sgem O 2 = 1/1 * d[O 2]/d. T Bereken de gemiddelde snelheid tussen 0 en 300 s Sgem NO 2 = 1/4 * 2/300 = 1, 67*10 -3 mol/L*s Bereken de gemiddelde snelheid tussen 1500 en 2000 s Sgem NO 2 = 1/4 * 1/300 = 8, 33*10 -4 mol/L*s Leg het verschil in de berekende snelheden uit Hoe langer de reactie duurt hoe minder deeltjes er kunnen reageren hoe langzamermlavd@BCEC de reactie zal verlopen. 25
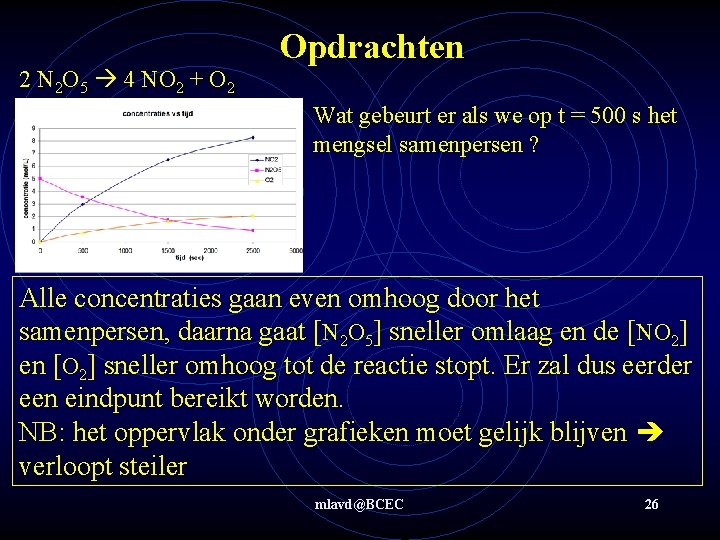
2 N 2 O 5 4 NO 2 + O 2 Opdrachten Wat gebeurt er als we op t = 500 s het mengsel samenpersen ? Alle concentraties gaan even omhoog door het samenpersen, daarna gaat [N 2 O 5] sneller omlaag en de [NO 2] en [O 2] sneller omhoog tot de reactie stopt. Er zal dus eerder een eindpunt bereikt worden. NB: het oppervlak onder grafieken moet gelijk blijven verloopt steiler mlavd@BCEC 26

Informatie halen uit raaklijn Bestudeer de volgende simulatie en bepaal mbv een raaklijn de snelheid op t 0: http: //www. chm. davidson. edu/Chemistry. Applets/kinetics/Reaction. Rates. html Bepaal in de de volgende simulatie mbv een raaklijn de snelheid op t 0, t 4 en t 7 http: //www. chm. davidson. edu/Chemistry. Applets/kinetics/Rate. Of. Reaction. html mlavd@BCEC 27
- Slides: 27