Bestimmung der Elementarladung durch Elektrolyse von Kupfer in

Bestimmung der Elementarladung durch Elektrolyse von Kupfer in einer Kupfersulfatlösung unter Verwendung der Loschmidtschen Zahl im Schülerversuch Mag. Franz Langsam AG – Physik 16. 11. 2006 Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Bestimmung der Elementarladung • Vorteile • Historischer Überblick (Millikan) • Grundlagen für das Verständnis (Atomistische Deutung der Faraday Gesetze nach Helmholz) • Molbegriff und Loschmidtsche Zahl • Gemeinsame Durchführung des Experiments • Hints, Geräte + Zeitaufwand Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Vorteile • Kaum Probleme beim Verständnis • Lehrplanbezug el. Strom, Faraday, Elektrolyse, Elementarladung, Molbegriff. . • sehr zeitökonomisch, materialschonend, billig, äußerst genau Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Historischer Überblick • Millikan´sche Methode: Öltröpfchenversuch 1906 - 1913 (Nobelpreis 1923) • Robert A. Millikan 1868 – 1953 Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Historischer Überblick • Apparatur Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Historischer Überblick • Millikan/Aufwärtsbewegung: Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Historischer Überblick • Millikan/Fallbewegung: Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Historischer Überblick • Millikan/Formel: Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Bestimmung von e durch Elektrolyse Theorie • Eigenschaft der bewegten Ladung : Strom Q=I*t • Annahme: jedes Ion eines einwertigen Stoffes trägt eine Elementarladung (=Ladung eines Elektrons, Protons…) • Notwendigkeit: Bestimmung der Zahl der wandernden Teilchen bei der Elektrolyse Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Bestimmung von e durch Elektrolyse Theorie • Loschmidt hat 1865 die Zahl der Teilchen eines Mol bestimmt 1 Mol = 6, 022 *10²³ Teilchen • Wird ein Mol eines Stoffes elektrolysiert, so fließen 1 Mol (das sind 6, 022*10²³) Elementarladungen Q = e * NA Mag. Franz Langsam => Bestimmung der Elementarladung e = Q / NA 16. 11. 2006 AG - Physik

Bestimmung von e durch Elektrolyse Theorie Das Mol • 1 Mol = 6, 022 * 10²³ Teilchen • So viele Teilchen, wie in 12 g 12 C • Früher : Bezug auf Wasserstoff, dann auf Sauerstoff • Allg. : 1 Mol = rel. Atom– bzw. Molekülmasse in Gramm Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Bestimmung von e durch Elektrolyse Theorie Vernetzung nach Pietschmann • 1 Mol ist ca. eine Quadrillion Teilchen (1024) • 1 Mol 18 g Wasser (= 1 Eprouvette fast voll) • 207 g Blei • 22, 4 l irgendeines Gases bei 0° C und normalem Druck (Luftballon d=46 cm) Mag. Franz Langsam oder 63, 6 g Kupfer Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Bestimmung von e durch Elektrolyse Theorie • 1024 Teilchen in 1 m Abstand aufgereiht NASA Mikrowellenhintergrund Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Bestimmung von e durch Elektrolyse Theorie Aus wie vielen Teilchen besteht ein Mensch 70 kg? 65%O (43 kg) = 43000 g 43000 /16 = 2700 Mol 18%C (16 kg) = 16000 g 16000 /12 = 1300 Mol 10%H (7 kg) = 7000 g 7000/1 = 7000 Mol => 11000 Mol = 6, 6 *1027 Teilchen Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Bestimmung von e durch Elektrolyse Theorie • Sonne: 1030 kg H = 1033 g 1033 Mol = 6*1056 Teilchen Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Bestimmung von e durch Elektrolyse Theorie • Universum: 1011 Sonnen pro Galaxie 1011 Galaxien pro Universum => 6*1078 Teilchen Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Praxis • Praxisbeispiel aus den Laborübungen: Bestimmung der Elementarladung durch Elektrolyse von Kupfer in einer Kupfersulfatlösung: Zwei Kupferelektroden sind auf 1/1000 g genau abzuwiegen und dann einer Elektrolyse zu unterziehen. Bei einer Stromstärke von 0, 5 Ampere soll das Experiment 20 min andauern. Die Zeit ist auf die Sekunde genau zu messen, die Stromstärke muss kontrolliert werden. Vor dem Einschalten ist die Schaltung der Aufsicht zu zeigen. Es ist anzugeben: • • • Reaktionsgleichung für Anoden- und Kathodenreaktion der jeweilige Reaktionstyp Massenzunahme und Massenabnahme Anzahl der aufgelösten und abgeschiedenen Mole Cu Berechnung der Elementarladung aus Anodenreaktion und aus Kathodenreaktion Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Praxis Durchführung: Reinigung der Elektroden Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Praxis Durchführung: Abwiegen der Elektroden Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Praxis Durchführung: Vorbereitung der Elektrolyse Kupfersulfatlösung und Cu - Elektroden Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Praxis Durchführung: Durchführung der Elektrolyse Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Praxis Durchführung: Abspülen der Elektroden Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Praxis Durchführung: Trocknen der Elektroden Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Praxis Durchführung: Nochmaliges Abwiegen der Elektroden Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Rechnung • Eigene Messung: Kathode Anode vorher m(Cu): nachher : 22, 51 g 22, 71 g ------0, 20 g 17, 45 g 17, 24 g -----0, 21 g • Stromfluss: • Zeit: I = 1, 0 A t = 10 min 40 s • bewegte Ladung: Mag. Franz Langsam C = 640 A*s Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Berechnung der Elementarladung aus den Messwerten • Abscheidung an der Kathode: m = 0, 20 g => 0, 20/63, 5 = 3, 159*10 -3 Mol • n = 3, 159*10 -3 *6, 022 *1023 = 1, 902*1021 Teilchen • Ladung pro Teilchen (zweiwertig!!) : Q/n = 640 / 1, 902*1021 = 3, 36*10 -19 C • e = 3, 36*10 -19/2 = 1, 68*10 -19 C Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Anhang Bestimmung der Loschmidtschen Zahl Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Anhang Bestimmung der Loschmidtschen Zahl • Prinzip: Ein Tropfen Ölsäure breitet sich auf Wasser so aus, dass sich ein monomolekularer Film bildet. • Näherungsweise wird angenommen, dass ein Ölsäuremolekül das Volumen d³ einnimmt. • Bei bekanntem Volumen kann aus der Fläche des Ölfilms die Ausdehnung eines Moleküls bestimmt werden, daraus das Volumen und bei Umrechnung auf 1 Mol die Avogadro- Konstante. Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik
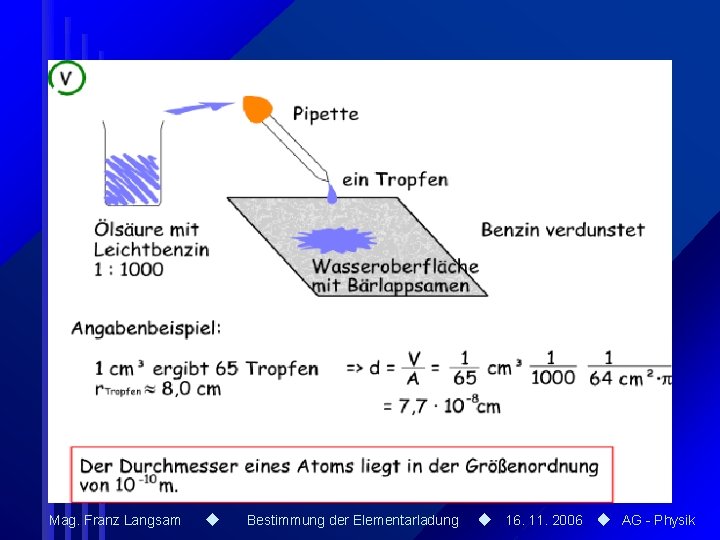
Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Erste Bestimmung durch Josef Loschmidt 1865 Loschmidt's method was based on the kinetic theory of gases, which had been developed with great success largely by the efforts of his contemporaries, Maxwell and Clausius. The movements of individual particles are governed solely by chance, and from these assumptions Maxwell was able to deduce that the viscosity of a gas is given by the relation : Where rho is the density of the gas, v is the average velocity of the molecules, and l is the mean free path, or average distance between two impacts. Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Erste Bestimmung durch Josef Loschmidt 1865 • He was also able to show that if each molecule is a sphere of diameter , then : where N is Loschmidt's number, and V is the gram-molecular volume. Loschmidt assumed that if a gas were condensed, its molecules would be very closely packed so that volumes of the molecules in a gram-molecule could be regarded as approximately equal to the volume of the liquid formed on condensation. This gave third equation for finding N. The most reliable data give, for mercury, N > 4, 4 x 1023. Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Bestimmung der Loschmidtschen Zahl durch die Brown‘sche Bewegung Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Bestimmung der Loschmidtschen Zahl durch die Radioaktivität Boltwood and Rutherford: N = 6, 6 x 1023 Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Bestimmung der Loschmidtschen Zahl über die Faraday‘sche Konstante durch Millikan * Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Bestimmung der Loschmidtschen Zahl durch Röntgenbeugung Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik

Literatur Science Progress, v 27, 1933, pp 634 – 649 Loschmidts Number By S. E. VIRGO, M. Sc. Physics Department, University Sheffield Mag. Franz Langsam Bestimmung der Elementarladung 16. 11. 2006 AG - Physik
- Slides: 37