ZEL ORGANK KMYA Organik kimya yapsnda C H

























































- Slides: 108

ÖZEL ORGANİK KİMYA

§ Organik kimya yapısında C, H, N ve O elementleri bulunduran maddeleri inceler. Kısaca “karbon kimyası” olarak bilinir. § İnorganik kimya, organik olmayan yani karbon-hidrojen bağı içermeyen bileşiklerin özelliklerini ve kimyasal davranışlarını inceleyen kimya dalıdır. Elementleri ve onların bileşiklerini inceler. § İnsan ve hayvan organizmasında varlığı tespit edilebilen çok sayıda elementten yaklaşık 24’ü hayat için önemlidir. § Bunlardan dördü (C, H, O ve N) temel elementler olup canlı organizmaların kuruluşuna iştirak ederler ve mineral madde olarak dikkate alınmazlar. § Kalsiyum, fosfor, sodyum, potasyum, klor, magnezyum ve kükürt makroelementler olarak adlandırılır ve C, H, O ve N ile birlikte canlı organizmaların % 99 undan fazlasını oluştururlar. § Demir, iyot, bakır, mangan, çinko, kobalt, molibden, selenyum ise mikroelementler (yada iz elementler) olarak sınıflandırılır. Bu gün bunlara F, B, Cr, Si, Sn, V eklenmiştir.

• Organik bileşiklerin hemen tamamında C ve H atomu vardır. • Bu nedenle CO 2, CO, CS gibi bileşikler ve karbonat (CO 3 -) içeren bileşikler organik bileşik sınıfına dahil edilmezler. Canlıların Temel Bileşenleri İnorganik Bileşikler Su Mineraller Asitler Bazlar Tuzlar Organik Bileşikler Karbonhidratlar Yağlar Proteinler Vitaminler Nükleik asitler

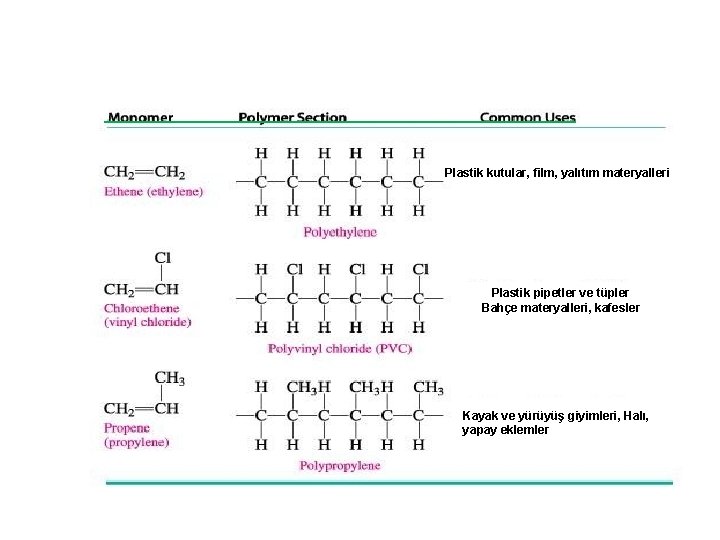
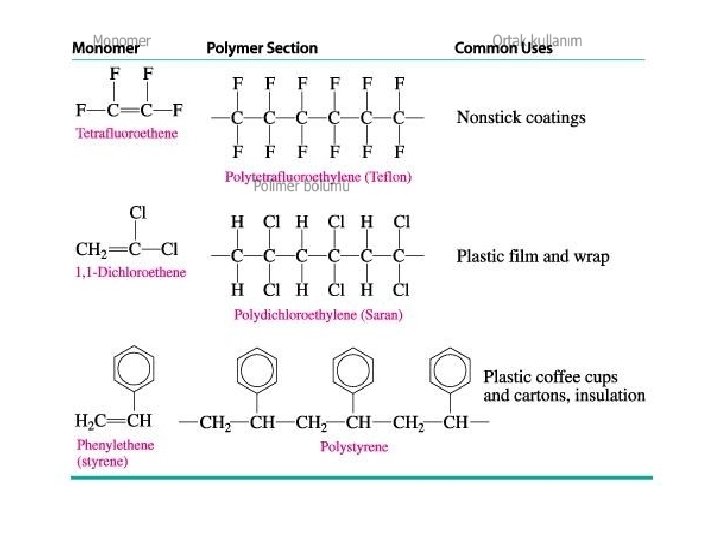
• Çok sayıda atomun (monomer) birbirine bağlanarak oluşturdukları çok büyük moleküllere polimer denir. Örnek: Etilen bir monomer, polietilen ise bir polimerdir • Polietilen en çok kullanılan plastiklerin başında gelir. • Plastikler sentetik polimerlerdir, doğada hazır bulunmazlar. • İnsan müdahalesi ile elde edilirler. • Çok yaygın şekilde kullanılmaktadır.


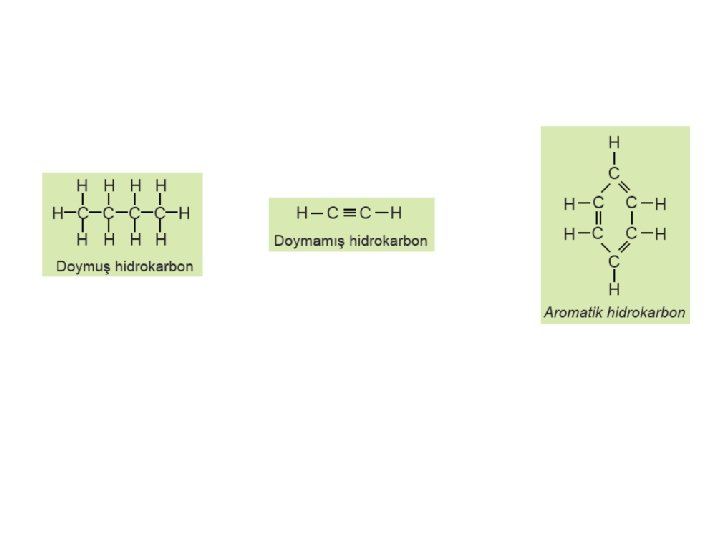
HİDROKARBONLAR 1. Alifatikler (Zincir yada halkalı) a- Doymuş: Alkanlar b- Doymamış: Alkenler, Alkinler 2. Aromatikler Benzen ve türevleri, nitro ve amino bileşikleri

• Günlük yaşamda etrafta görülen her üç nesneden ikisi plastiktir. Plastik polimer ile çoğu kere benzer anlamda kullanılmaktadır. Plastik karbonun metal olmayan elementlerle (H, O, Cl, N) meydana getirdiği büyük moleküllü organik bileşiklerdir. Otomotiv, beyaz eşya, ambalaj sektörleri başta gelmek üzere bir çok sektör tarafından tercih edilmektedir. Araç lastikleri, plastik maddeler, ayakkabı, bisiklet, tenis raketi ve topu, PVC, teflon tava v. b. birçok malzeme sentetik polimerden üretilmiştir.

Plastik kutular, film, yalıtım materyalleri Plastik pipetler ve tüpler Bahçe materyalleri, kafesler Kayak ve yürüyüş giyimleri, Halı, yapay eklemler


Polimerlerin Özellikleri Küçük moleküllü maddeler genellikle gaz veya sıvı haldedir, polimerler ise büyük moleküllü oldukları için katı ve genellikle serttir. § Polimer zincirler kolayca katlanmaya ve esnekliğe meyillidir. § Küçük moleküllü bileşikler genellikle çözücülerde kolay çözünür, polimerler ise hem zor çözünür, hem de çözünme şekilleri küçük moleküllü bileşiklerden tamamen farklıdır § Küçük moleküllü bileşiklerin çözeltileri şeffaf olduğu halde, yüksek moleküllü bileşiklerin çözeltilerinde ışığın dağılması gözlenir. § Küçük moleküllü bileşiklerin çözeltilerinin kristalleşmesi genellikle kolay ve belli bir sıcaklıkta olduğu halde, yüksek moleküllü birleşmeler için kristalleşme olayı çok zor ve geniş bir sıcaklık aralığında olur. Zincirlerin kristal uyumu sert bir polimer yapar. Kristalleşme derecesi; polimerin kimyasal yapısı ve zincir uzunluğu ile belirlenir.

Temel Yapılar 1. Alifatik hidrokarbonlar a. Doymuş bileşikler b. Doymamış bileşikler 2. Sikloalifatik hidrokarbonlar a. Monosiklik bileşikler b. Bisiklik ve polisiklik bileşikler c. Spiro bileşikler 3. Aromatik hidrokarbonlar a. Monosiklik aromatik bileşikler b. Polisiklik aromatik bileşikler c. Hidrojenlenmiş polisiklik aromatik bileşikler d. Köprülü polisiklik aromatik bileşikler 4. Heterosiklik bileşikler a. Monosiklik bileşikler b. Polisiklik bileşikler c. Heterosiklik köprülü bileşikler d. Heterosiklik spiro bileşikler

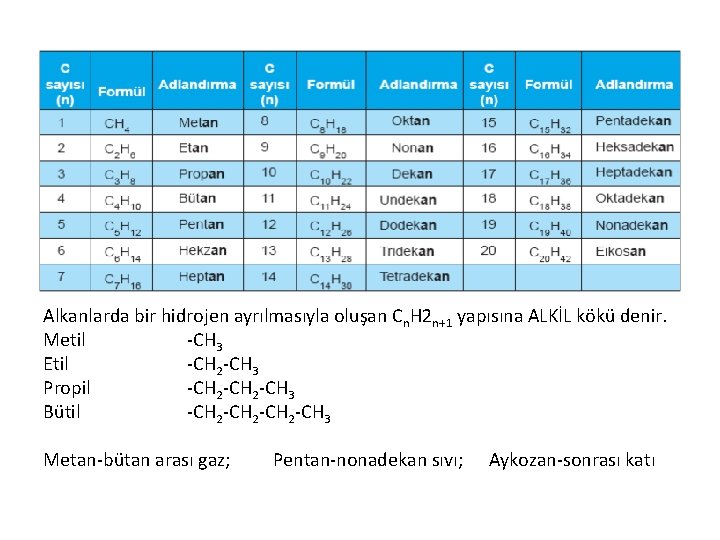
1. Alifatik Hidrokarbonlar Doymuş bileşikler: Genel formülü Cn. H 2 n+2’dir. Düz zincirli doymuş hidrokarbonlara alkanlar veya parafinler de denir. Alkanların ilk dört üyesinin adı IUPAC’ın kabul ettiği özel adlardır. Bunlar metan, propan ve bütandır. Dört karbonlu alkanlardan sonra gelen düz zincirli alkanlar adlandırılırken karbon atomu sayısını belirtmek için IUPAC‘ın kabul ettiği önekler kullanılır. 1 Mono 2 Di 3 Tri 4 Tetra 5 Penta 6 Heksa 7 Hepta 8 Okta 9 Nona 10 Deka 11 Undeka 12 Dodeka 13 Trideka 14 Tetradeka 15 Pentadeka 16 Heksadeka 17 Heptadeka 18 Oktadeka 19 Nonadeka 20 Eikosa

Alkanlarda bir hidrojen ayrılmasıyla oluşan Cn. H 2 n+1 yapısına ALKİL kökü denir. Metil -CH 3 Etil -CH 2 -CH 3 Propil -CH 2 -CH 3 Bütil -CH 2 -CH 3 Metan-bütan arası gaz; Pentan-nonadekan sıvı; Aykozan-sonrası katı

• IUPAC kurallarına göre : • Doymuş yapılarda en uzun karbon zinciri seçilir. Bu zincirin adı temel ad olarak alınır. Ancak molekülde doymamışlık varsa, bunları içeren zincir kısa da olsa temel zincir olarak alınır. • Temel zincire bağlı diğer zincirler alkil grubu olarak alınır. • Temel zincirin numaralanmasına doymamışlığın, dallanmanın ve sübstitüentin bağlı olduğu en yakın taraftan başlanır. • Temel zincir üzerinde aynı cinsten birden fazla sübstitüent varsa, di, tri, tetra vb. gibi ekler kullanılarak sayıları belirtilir. • Sayılar birbirinden virgül, harflerden tire ile ayrılırlar. • Molekülde üçlü bağ varsa, üçlü bağın yakın olduğu uçtan numaralandırmaya başlanır. Üçlü bağ yoksa, ikili bağa dikkat edilir. • İskelet üzerinde bir tane üçlü bağ varsa kökten sonra –in eki getirilir. Üçlü bağ uçta değilse hangi numaralı karbondan sonra geliyorsa o rakam kökten önce yazılır. İskelette iki yerde üçlü bağ varsa hangi numaralı karbondan sonra geldikleri kökten önce yazılır. Kökten sonra ise –di in son eki getirilir. • Karbon iskeletinde üçlü bağ yok, fakat çift bağ varsa, eğer bir yerde ise –en veya –ilen eki getirilir. Çift bağ başta değil ise, hangi numaralı karbondan sonra geliyorsa, o rakam kökten önce yazılır. İskelette birden fazla çiftbağ varsa yerleri kökten önce belirtilir. Kök heceden sonra ise dien, trien. . . gibi uygun son ek getirilir.

ALKANLAR Alkanların genel formülleri Cn. H 2 n+2 dir. Halkalı olanlarına siklo alkanlar denir ve siklo alkanların genel formülü Cn. H 2 n dir. Doymuş hidrokarbonlardır. Moleküldeki tüm karbon atomları arasında tek bağ vardır. Yani pi bağı içermezler. Moleküldeki tüm atomlar sp 3 hibritleşmesi yapmıştır.

ALKANLARIN GENEL ÖZELLİKLERİ • • • Alkanların ilk dört üyesi gaz, 5 -17 karbon içerenler sıvı, diğerleri katıdır. Apolar olduklarından suda çözünmezler. Moleküller arasında sadece London etkileşimi vardır. Karbon sayısı arttıkça kaynama noktaları yükselir. Alkanlar katılma tepkimesi vermezler. Ancak halojenlerle yer değiştirme (sübstitüsyon) tepkimesi verirler. Aynı C sayılılarda dallanma artıkça erime ve kaynama noktası düşer.

ALKANLARDA ADLANDIRMA Önce en uzun karbon zinciri seçilir. (ana zincir) Ana zincire bağlı gruplara (dallanma) en küçük numara gelecek şekilde numaralandırma yapılır. Dallanmanın bağlı olduğu karbonun numarası yazılır ve tire (-) konur. Tireden sonra dallanmanın adı belirtilir. • Dallanmalar alfabetik sıraya göre belirlenir.

• Aynı cinsten birden fazla dallanma varsa grekçesayısı di, tri, tetra… belirtilir. • En uzun karbon zincirine karşılık gelen alkanın adı yazılır. 2, 3 -dimetil pentan

Alkanlarda İzomeri

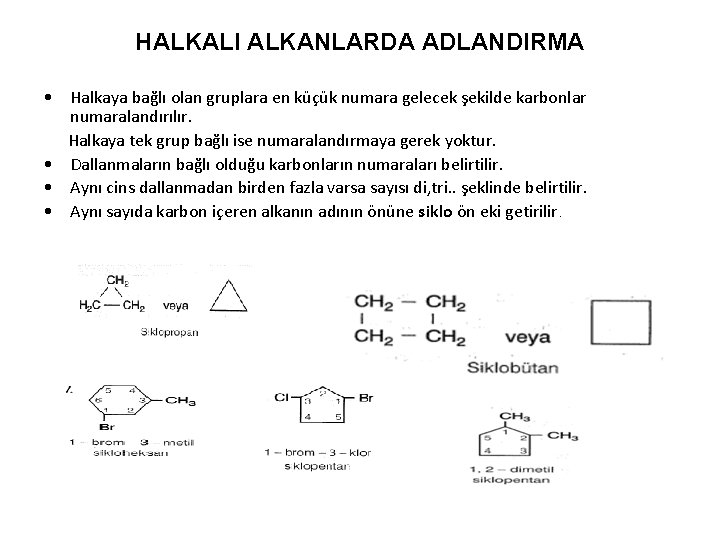
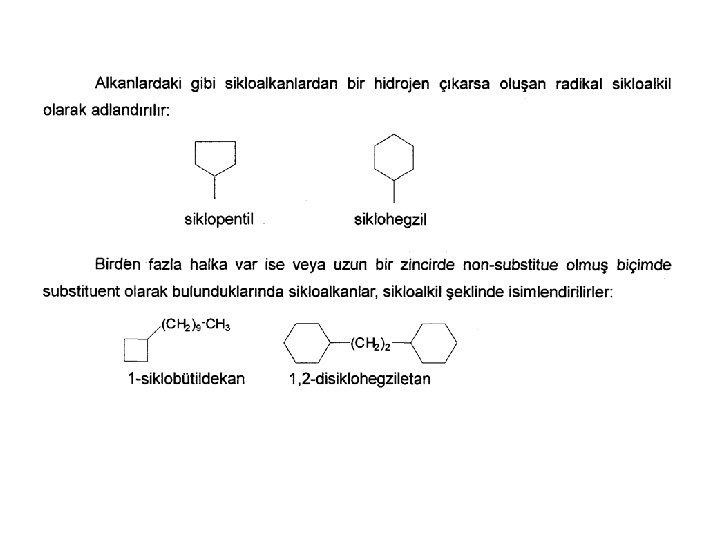
HALKALI ALKANLARDA ADLANDIRMA • Halkaya bağlı olan gruplara en küçük numara gelecek şekilde karbonlar numaralandırılır. Halkaya tek grup bağlı ise numaralandırmaya gerek yoktur. • Dallanmaların bağlı olduğu karbonların numaraları belirtilir. • Aynı cins dallanmadan birden fazla varsa sayısı di, tri. . şeklinde belirtilir. • Aynı sayıda karbon içeren alkanın adının önüne siklo ön eki getirilir.

ALKENLER • Alkenler karbon atomları arasında en az bir tane ikili bağ taşıyan ve genel formülleri Cn. H 2 n şeklinde olan doymamış hidrokarbonlardır. • İkili bağa sahip karbon atomları sp 2 hibritleşmesi yapmıştır. • İlk üyesi etendir.

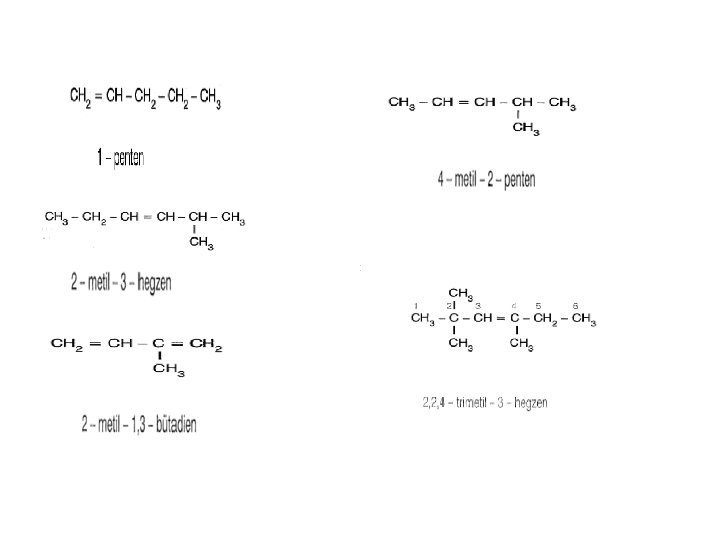
ADLANDIRMA • Alkenler adlandırılırken aynı karbon sayılı alkan isminin sonundaki –an eki yerine –en ya da –ilen eki getirilir • Üzerinde ikili bağın bulunduğu en uzun karbon zinciri seçilir. • Numaralandırma ikili bağ en küçük numarayı alacak şekilde yapılmalıdır. • İkili bağ iki uca eşit uzaklıkta ise dallanmış grup en küçük numarayı alacak şekilde numaralandırılır. • Numaraları ile beraber önce dallanmış grupların isimleri belirtilir.


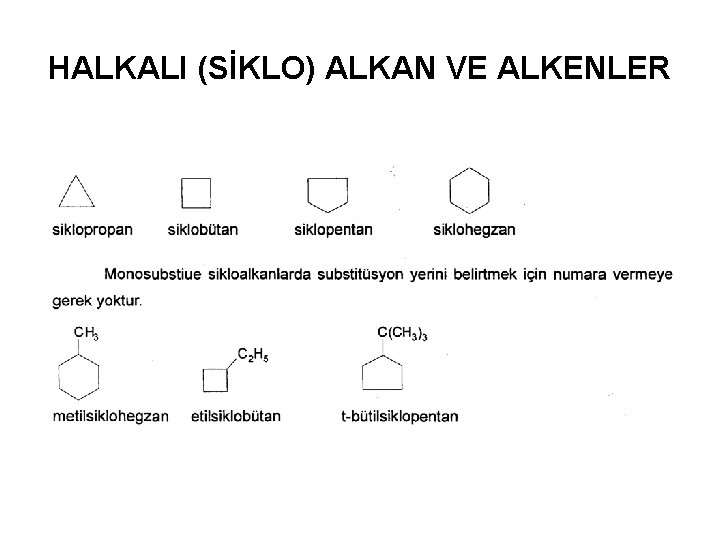
HALKALI (SİKLO) ALKAN VE ALKENLER

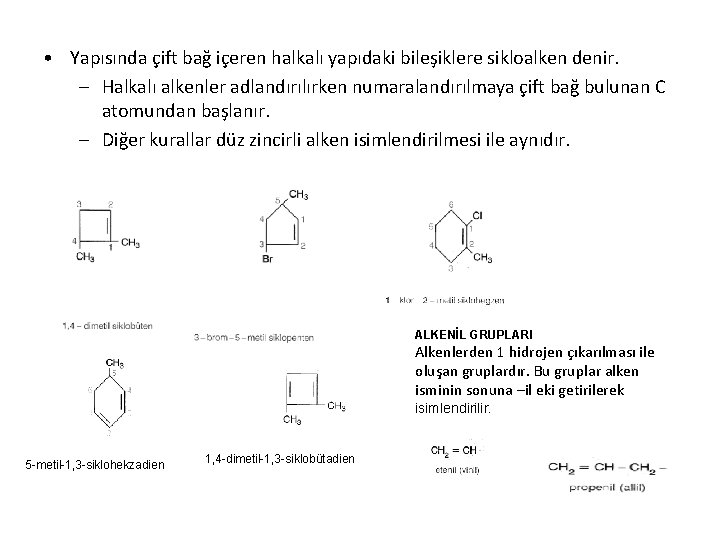
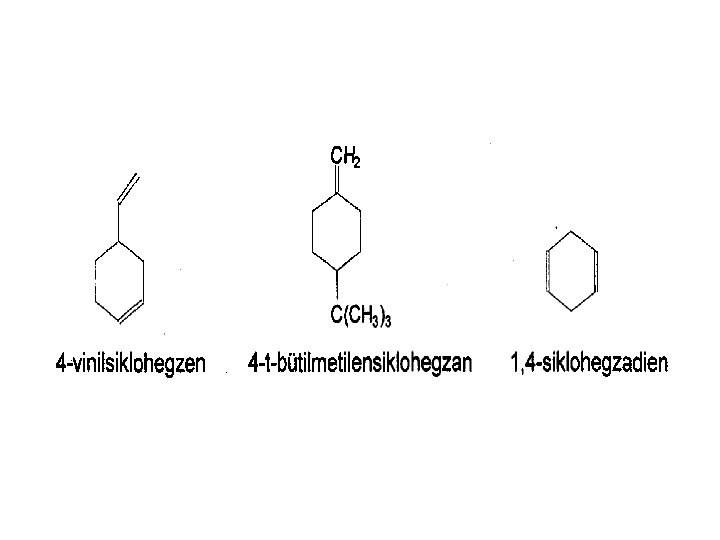
• Yapısında çift bağ içeren halkalı yapıdaki bileşiklere sikloalken denir. – Halkalı alkenler adlandırılırken numaralandırılmaya çift bağ bulunan C atomundan başlanır. – Diğer kurallar düz zincirli alken isimlendirilmesi ile aynıdır. ALKENİL GRUPLARI Alkenlerden 1 hidrojen çıkarılması ile oluşan gruplardır. Bu gruplar alken isminin sonuna –il eki getirilerek isimlendirilir. 5 -metil-1, 3 -siklohekzadien 1, 4 -dimetil-1, 3 -siklobütadien

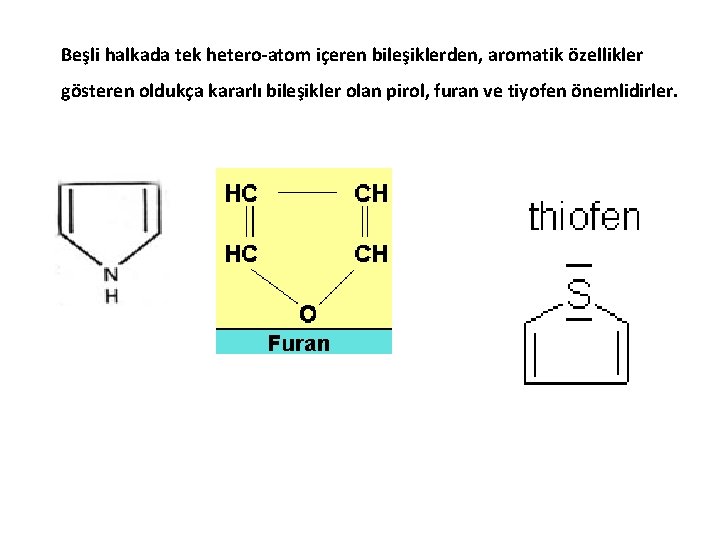
Beşli halkada tek hetero-atom içeren bileşiklerden, aromatik özellikler gösteren oldukça kararlı bileşikler olan pirol, furan ve tiyofen önemlidirler.

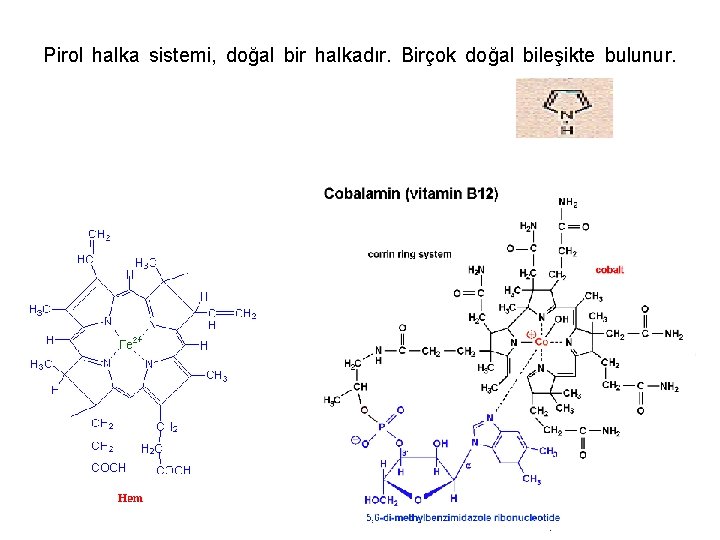
Pirol halka sistemi, doğal bir halkadır. Birçok doğal bileşikte bulunur.

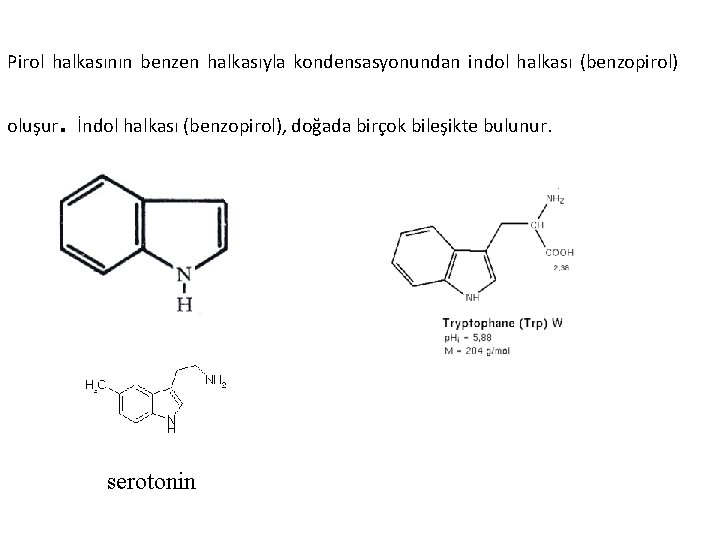
Pirol halkasının benzen halkasıyla kondensasyonundan indol halkası (benzopirol) . oluşur İndol halkası (benzopirol), doğada birçok bileşikte bulunur. serotonin

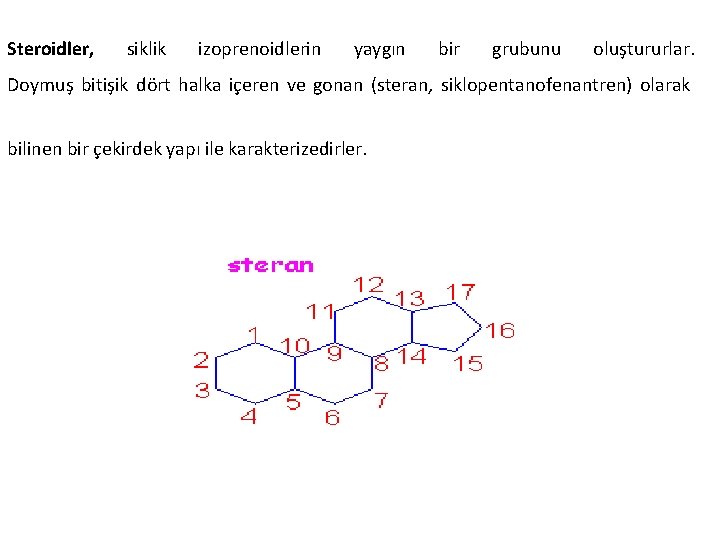
Steroidler, siklik izoprenoidlerin yaygın bir grubunu oluştururlar. Doymuş bitişik dört halka içeren ve gonan (steran, siklopentanofenantren) olarak bilinen bir çekirdek yapı ile karakterizedirler.

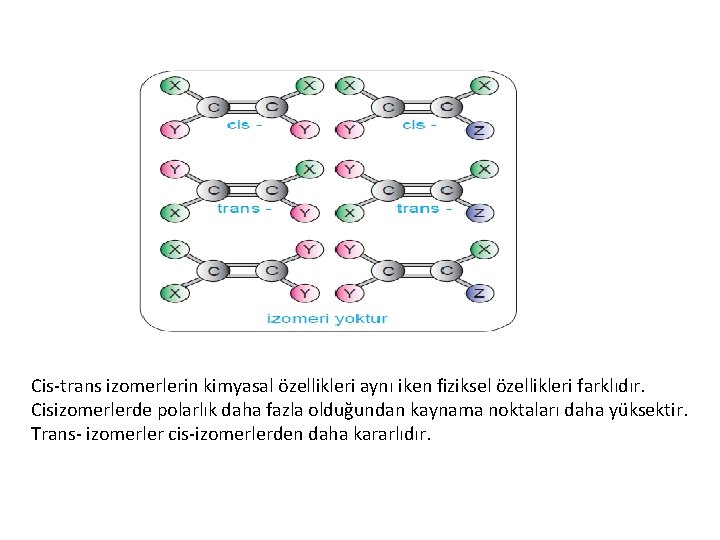
ALKENLERDE İZOMERİ Alkenlerde yapı ve geometrik izomeri görülür. • Geometrik izomeri (Cis-Trans izomeri) • Alkenlerde çift bağlı C atomlarına bağlı grupların yönelimlerine göre Cis-trans izomerler oluşur • Cis-trans izomerlerin kimyasal özellikleri aynı, fiziksel özellikleri farklıdır. • Cis izomerlerde polarlık daha fazla olduğundan kaynama noktaları daha yüksektir. • Trans izomerler cis izomerlerden daha kararlıdır.

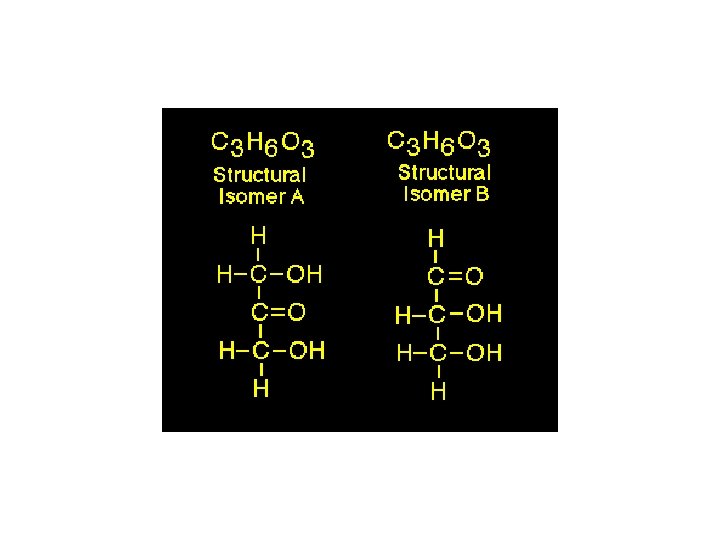
• Fonksiyonel izomerlik: Atomların farklı dizilişleri farklı fonksiyonel grupların oluşmasına neden olur. • Bazı eterlerle alkoller CH 3 -O-CH 3 dimetileter ile C 2 H 5 OH etil alkol izomer(C 2 H 6 O) • Bazı aldehitlerle ketonlar CH 3 -CH 2 -CHO propiyonaldehit ile CH 3 -CO-CH 3 aseton (C 3 H 6 O) • Bazı esterlerle karboksilik asitler CH 3 -COOCH 3 metilasetat ile CH 3 -CH 2 -COOH propiyonikasit (C 3 H 6 O 2) izomerlerdir.

Yukardaki örneklerde sadece ikili bağ yerleri farklı olduğundan yapı izomeridirler. Aynı karbon sayılı alkenler ile sikloalkanlar yapı izomeridirler. Geometrik izomeri (Cis-Trans izomeri) Alkenlerdeçift bağlı C atomlarına bağlı grupların yönelimlerine göre Cis-trans izomerler oluşur Cis-1, 2 -diklor eten Trans-1, 2 -diklor eten


Cis-trans izomerlerin kimyasal özellikleri aynı iken fiziksel özellikleri farklıdır. Cisizomerlerde polarlık daha fazla olduğundan kaynama noktaları daha yüksektir. Trans- izomerler cis-izomerlerden daha kararlıdır.

ALKENLERİN GENEL ÖZELLİKLERİ Alkenler apolar moleküllerdir. C sayısı arttıkça kaynama noktası artar. • Oda koşullarında ilk dört üyesi gaz 5 -15 karbonlu üyeleri sıvıdır. • Homolog sıra oluştururlar. • Yanma tepkimesi verirler. Katılma tepkimesi verirler. (Elektrofilik katılma) B) Hidrojen Katılması A) Halojen Katılması C) Hidrojen Halojenür Katılması

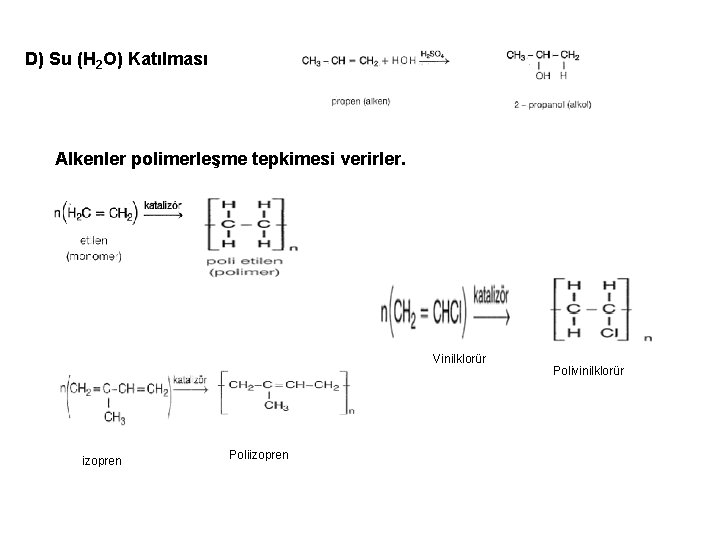
D) Su (H 2 O) Katılması Alkenler polimerleşme tepkimesi verirler. Vinilklorür izopren Polivinilklorür

– Alkenler apolar moleküllerdir. C sayısı arttıkça kaynama noktası artar. – Oda koşullarında ilk dört üyesi gaz 5 -15 karbonlu üyeleri sıvıdır. – Homolog sıra oluştururlar. – Yanma tepkimesi verirler. – Katılma tepkimesi verirler. (Elektrofilik katılma) 1. Halojen Katılması 2. Hidrojen Katılması 3. Hidrojen Halojenür Katılması 4. H 2 O Katılması

• Yükseltgenme tepkimesi verirler • Polimerleşme tepkimesi veririler GENEL ELDE EDİLME YOLLARI 1. Alkollerden su çekilmesi 2. Alkil halojenürden hidrojen halojen çekilmesi 3. Alkanlardan H 2 çekilmesi 4. Dihalojenürlerden halojen çekilmesi 5. Alkinlerin kısmi doyrulması

ALKİNLER • Genel formülleri Cn. H 2 n-2 şeklinde olan ve C atomları arasında en az bir tane 3 lü bağ bulunan bileşiklerdir. • Bu bileşiklere, moleküllerindeki üçlü bağ içermeleri ve sadece karbon ve hidrojenden oluşmalarından ötürü doymamış hidrokarbon da denir • Bazı tepkimeleri alkenlerinkine benzer: Katılma ve yükseltgenme • Bazı tepkimeler ise alkinlere özeldir. • En küçük üyesi 2 karbonludur: • C≡C • Etin C 2 H 2 • Propin C 3 H 4 • Butin C 4 H 6 C 2 H 2 Etin (Asetilen)

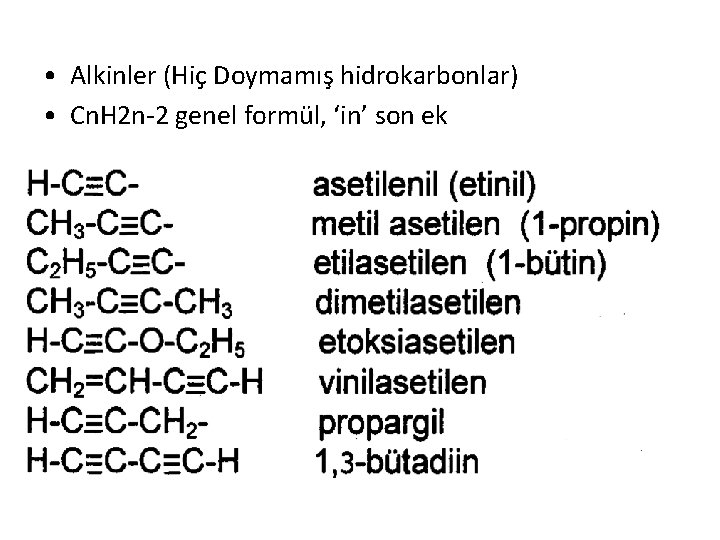
• Alkinler (Hiç Doymamış hidrokarbonlar) • Cn. H 2 n-2 genel formül, ‘in’ son ek

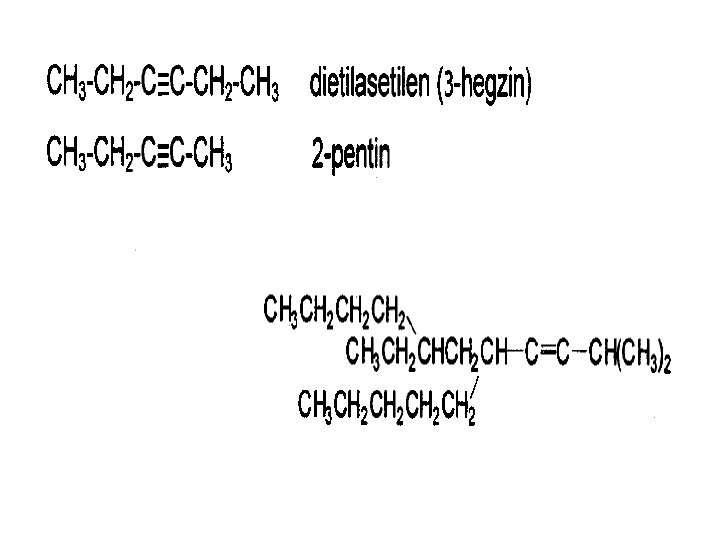
Alkinlerin Adlandırılması • • H-C≡C-H H-C≡C-CH 3 H-C≡C-CH 2 -CH 3 -C≡C-CH (CH 3)2 H-C≡C-H CH 2=CH-C≡C-H C 6 H 5 -C≡C-C 6 H 5 Etin Asetilen Propin Metilasetilen 1 -Bütin Etilasetilen 2 -Bütin Dimetilasetilen 4 -Metil-2 -Pentin (Metilizopropilasetilen) 2, 3 -Bütadin Diasetilen 1 -Büten-3 -in Vinilasetilen Difeniletin Difenilasetilen


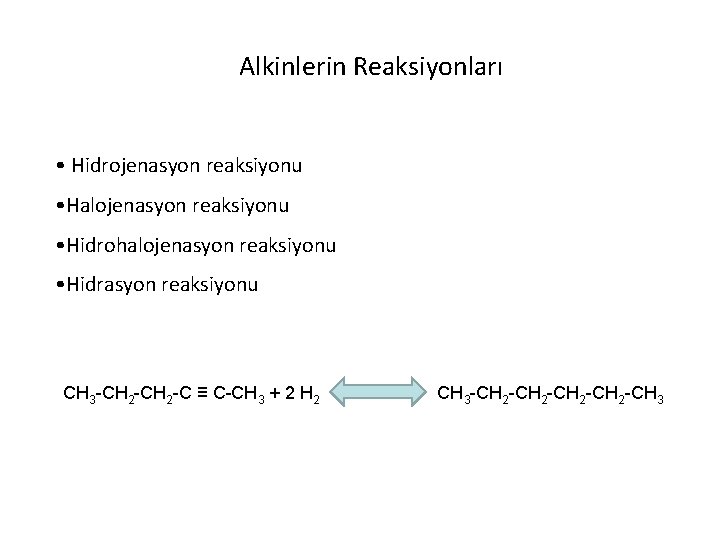
Alkinlerin Reaksiyonları • Hidrojenasyon reaksiyonu • Halojenasyon reaksiyonu • Hidrohalojenasyon reaksiyonu • Hidrasyon reaksiyonu CH 3 -CH 2 -C ≡ C-CH 3 + 2 H 2 CH 3 -CH 2 -CH 3

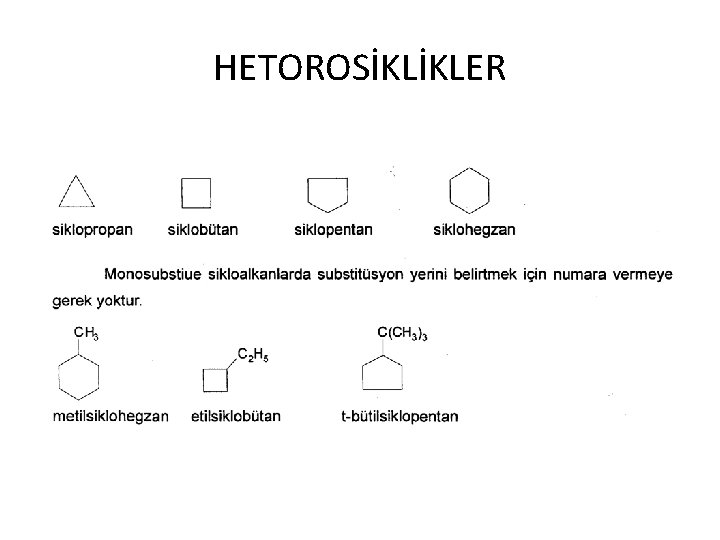
AROMATİK SİSTEMLER Aromatik bileşikler halkalı (siklik) yapıda olan düzlemsel (veya yaklaşık düzlemsel olan) moleküllerdir. Aromatik halkalar genellikle beş, altı ya da yedi üyeden oluşmuşlardır.

HETOROSİKLİKLER


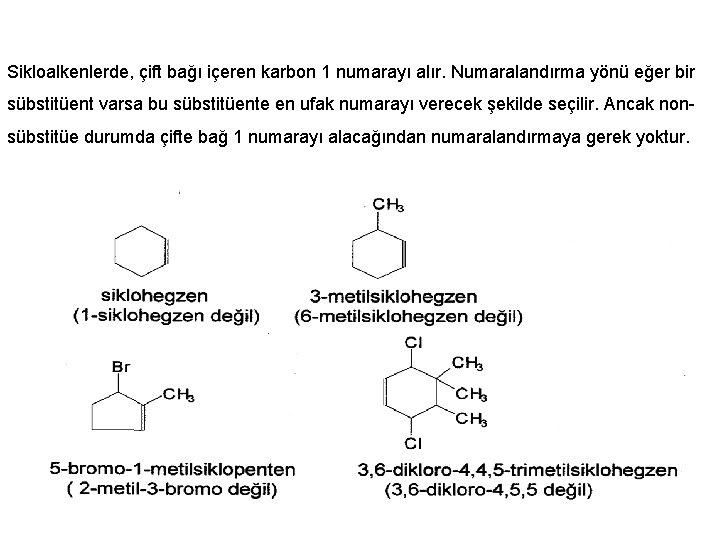
Sikloalkenlerde, çift bağı içeren karbon 1 numarayı alır. Numaralandırma yönü eğer bir sübstitüent varsa bu sübstitüente en ufak numarayı verecek şekilde seçilir. Ancak nonsübstitüe durumda çifte bağ 1 numarayı alacağından numaralandırmaya gerek yoktur.


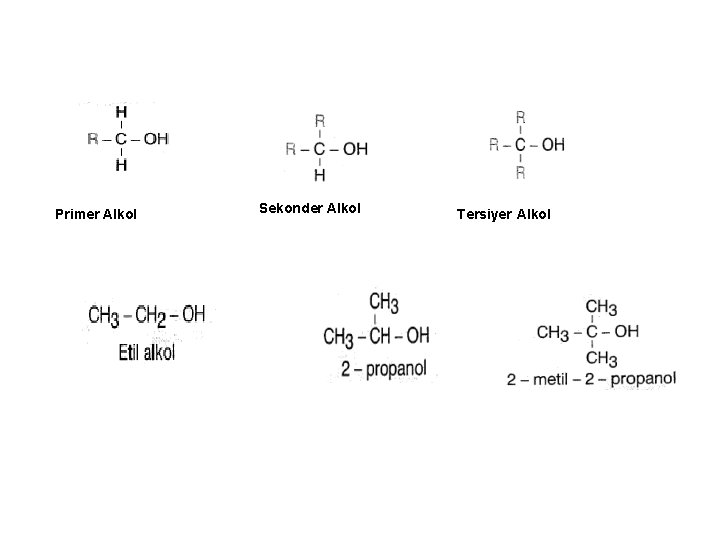
ALKOLLER • Alkoller, alkillenmiş su veya hidroksillenmiş hidrokarbon olarak düşünülebilir Alkoller, hidrokarbon iskeletinde bir veya birden fazla hidroksil (OH) grubu bulunduran bileşiklerdir. • Alkoller, moleküllerindeki –OH grubu taşıyan karbon atomuna bağlı alkil gruplarının sayısına göre primer, sekonder ve tersiyer olmak üzere 3 gruba ayrılır.

Primer Alkol Sekonder Alkol Tersiyer Alkol

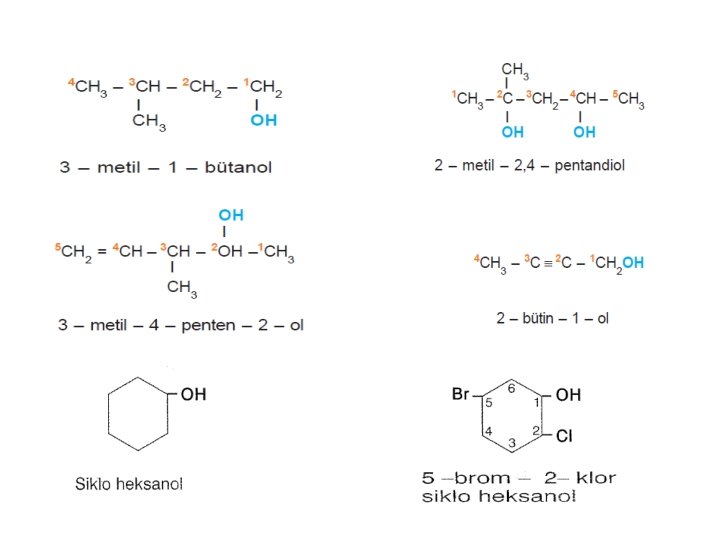
• • Alkollerin IUPAC sistemik adlandırılmasında, hidrokarbonun adının sonuna “ol” eki getirilir. Ayrıca hidroksil grubunun bağlı olduğu karbonu da belirtmek gerekir. CH 3 -OH metanol (metil alkol) C 2 H 5 -OH etanol (etil alkol) C 3 H 7 -OH propanol (propil alkol) C 4 H 9 -OH butanol (butil alkol) Dört karbonlu bir alkol primer, sekonder veya tersiyer olabilir. Farkı belirtebilmek için ol-ekinden önce -OH grubunun bağlı olduğu karbonun numarası söylenmelidir: CH 3 -CH 2 -CH 2 -OH Butan-l-ol (primer) CH 3 -CH 2 -CHOH-CH 3 Butan-2 -ol (sekonder)

• 1. IUPAC‘a göre adlandırma • • • -OH grubunun bulunduğu en uzun C zinciri belirlenir ve numaralandırma - OH’ın yakın olduğu uçtan yapılır. - OH grubu dışındaki atomların ve grupların zincirdeki yerleri belirlenir. OH’ın yeri belirtilir. Ana zincirle aynı sayıda C içeren alkan isminin sonundaki -an eki erine -ol eki getirilir.


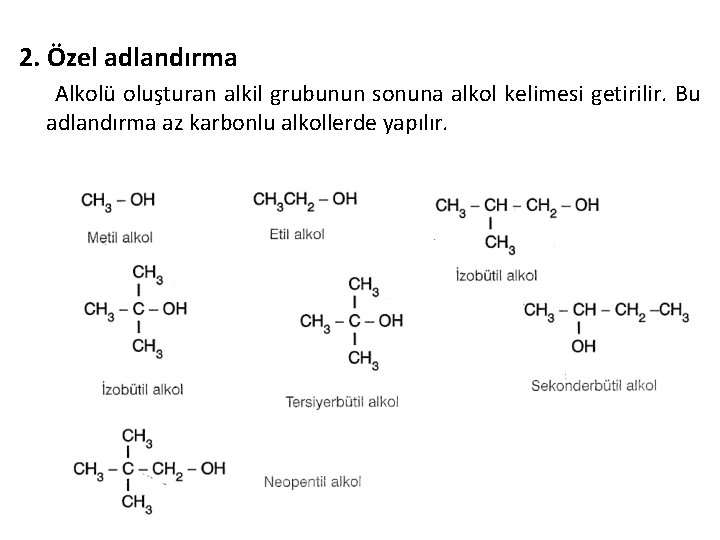
2. Özel adlandırma Alkolü oluşturan alkil grubunun sonuna alkol kelimesi getirilir. Bu adlandırma az karbonlu alkollerde yapılır.

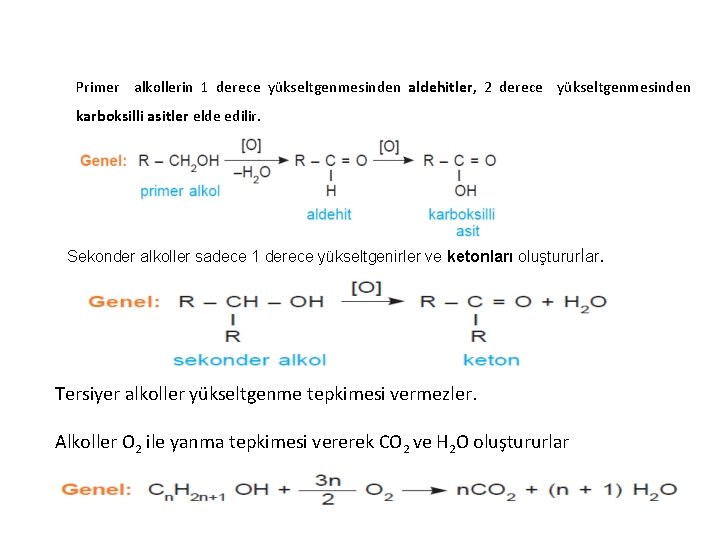
Primer alkollerin 1 derece yükseltgenmesinden aldehitler, 2 derece yükseltgenmesinden karboksilli asitler elde edilir. Sekonder alkoller sadece 1 derece yükseltgenirler ve ketonları oluştururlar. Tersiyer alkoller yükseltgenme tepkimesi vermezler. Alkoller O 2 ile yanma tepkimesi vererek CO 2 ve H 2 O oluştururlar

• Metanol, bilinen en basit alkoldür. • Alkoller, moleküllerindeki hidroksil sayısına göre, mono ve polihidrik olmak üzere de sınıflandırılabilirler. • Polihidrik alkoller içerdikleri hidroksil sayısına göre dihidrik, trihidrik, tetrahidrik olarak isimlendirilirler: - Monohidrik alkol R-CH 2 -OH – Dihidrik alkol HO-CH 2 -OH (etilen glikol) – Trihidrik alkol HO-CH 2 -CH(OH)-CH 2 -OH (gliserin) – Tetrahidrik alkol HO-CH 2 -CH(OH)-CH 2 -OH (eritritol)

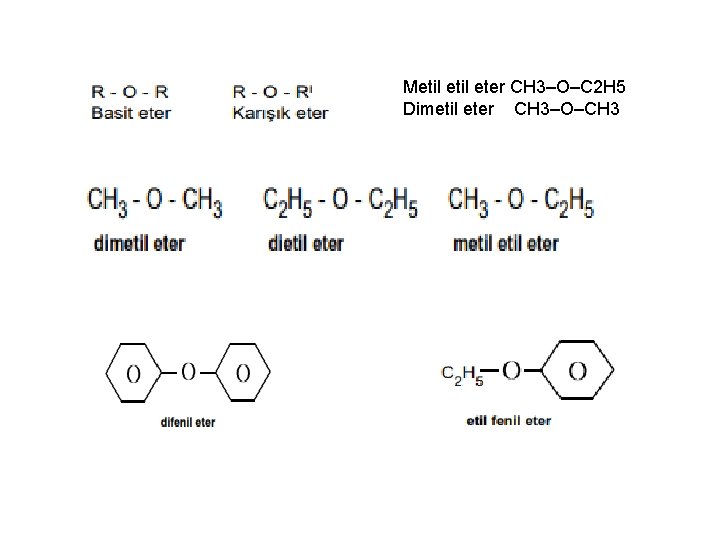
ETERLER Ø Genel formülleri R-O-R olan eterler, alkillenmiş alkol veya iki kez alkillenmiş su şeklinde düşünülebilir. Ø Su molekülünden bir H çıkıp, yerine alkil kökü bağlandığında oluşan bileşiklere alkol adı verilirken, sudaki iki hidrojenin de çıkıp, yerine iki alkil kökünün gelmesi ile oluşan bileşiklere de eter adı verilir. Ø H-O-H : Su R-O-H : Alkillenmiş su (alkol) R-O-R : Eter Ø Eterler karanlıkta ve kapalı şişelerde saklanmalıdır. Aksi takdirde eterler ışığın katalitik etkisiyle, havanın oksijeni ile yavaş, radikalik bir reaksiyona girerek, peroksitlere dönüşür. Bu peroksitler, şiddetle patlayan, oldukça tehlikeli bileşiklerdir. Ø Alkoller ve eterler birbirlerinin izomerleri olduklarından genel formülleri aynıdır (Cn. H 2 n+2 O)

Metil eter CH 3–O–C 2 H 5 Dimetil eter CH 3–O–CH 3

Eterlerin Adlandırılması Eterler iki şekilde adlandırılabilir. İlki özel adlandırma ikincisi ise IUPAC sistemine göre adlandırmadır. Özel Adlandırma; Özel adlandırmada alkil gruplarının adı ve sonuna da eter kelimesi getirilir. Mesela aşağıdaki dimetil eter’de gördüğünüz gibi sırayla alkil grubumuzu ilk yazdık en son da eter kelimesini ekledik. Eterlerin isimlendirilmesi, eter molekülünde bulunan alkil gruplarından küçük olanın isminin sonuna diğer alkil grubunun ismi ve eter kelimesi eklenir. IUPAC Sistemine Göre Adlandırma; IUPAC sistemine göre adlandırılmada ise alkil gruplarından karbon (C) sayısı en fazla olanı ana zincir olarak kabul etmeliyiz. Diğer alkil grubu ise oksijenle birlikte alkoksi grubu olarak adlandırılırmaktadır. Örnek olarak aşağıdaki etoksi propan’a bakabilirsiniz.

Ø Eterlerin Eldesi 1. ) İki mol mono alkolden bir mol su çekilmesiyle elde edilir. 2 -) Williamson Senteziyle (Alkolatlardan) elde edilir.

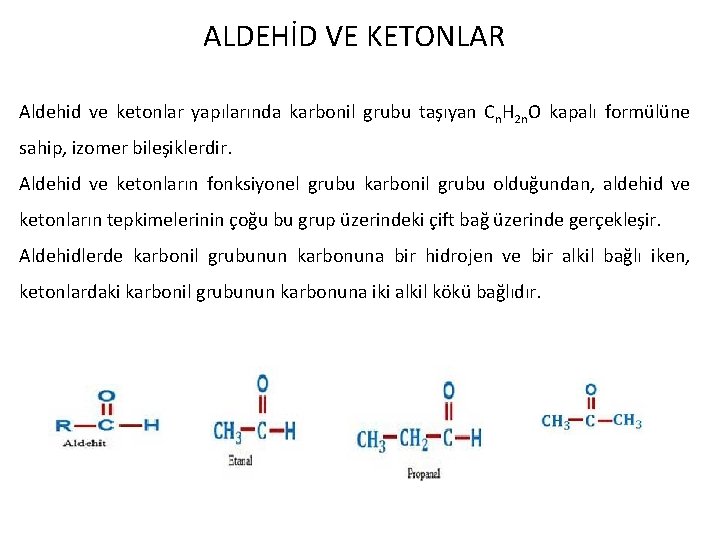
ALDEHİD VE KETONLAR Aldehid ve ketonlar yapılarında karbonil grubu taşıyan Cn. H 2 n. O kapalı formülüne sahip, izomer bileşiklerdir. Aldehid ve ketonların fonksiyonel grubu karbonil grubu olduğundan, aldehid ve ketonların tepkimelerinin çoğu bu grup üzerindeki çift bağ üzerinde gerçekleşir. Aldehidlerde karbonil grubunun karbonuna bir hidrojen ve bir alkil bağlı iken, ketonlardaki karbonil grubunun karbonuna iki alkil kökü bağlıdır.

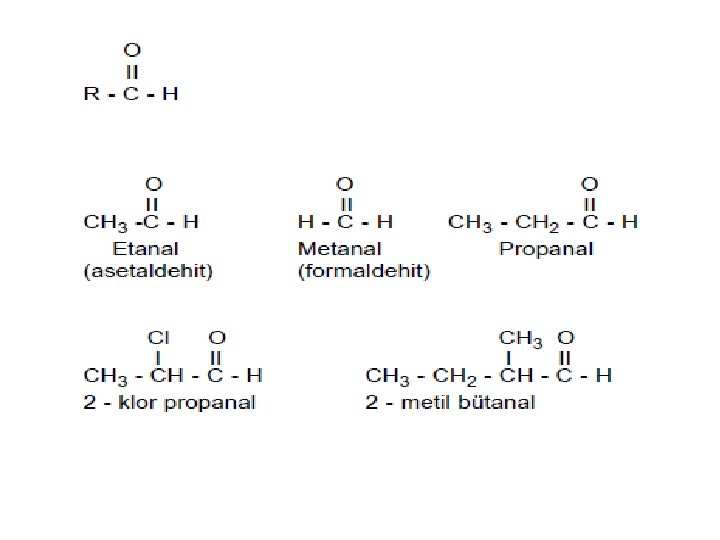
ALDEHİDLER Ø Karbonil grubunun karbon atomuna bir alkil grubu ile bir hidrojen atomu bağlanmış olan bileşiklerdir. Aldehidin kelime anlamı dehidrojene edilmiş alkol demektir. Ø Aynı C sayılı alkanların sistematik adının sonuna -al eki getirilerek adlandırılırlar. OHHC Formaldehid O H CH 3 C Asetaldehid O H C 2 H 5 C Propiyonaldehit Ø C atomunun O ile çift bağ yaptığı, diğer iki element ile tek bağ yaptığı fonksiyonel grup karbonil grubu olarak adlandırılır. Karbonil grubunda C atomunun bir tarafına H atomu diğer tarafına bir alkil grubu bağlanmasıyla meydana gelen bileşiklere "Aldehit" denir. Aldehitlerin en küçük üyesi metanal olarak adlandırılır. Metanal bileşiğinde C atomunun her iki tarafında birer H atomu bulunmaktadır. Yani metanal de alkil grubu bulunmaz, diğer tüm aldehitlerde alkil grubu bulunur.

• Aldehitlerin fonksiyonel grubu formildir. • Formil grubu, karbonil grubu da içerir. • Karbonil grubuna bir tane hidrojen atomu bağlanmışsa formil grubu olur. • Aldehit ve ketonlar yapılarında karbonil grubu bulunduran bileşiklerdir. • Ketonların fonksiyonel grubu karbonildir.

ALDEHİTLERİN GENEL ÖZELLİKLERİ 1) Küçük moleküllü üyeleri sıvıdır. Hidrojen bağı içermediklerinden aynı sayıda karbon taşıyan alkollerden ve karboksilli asitlerden daha düşük sıcaklıkta kaynarlar. Dört karbonluya kadar olanlar dışında suda çözünmezler. Küçük moleküllü olanların keskin ve tahriş edici kokuları vardır. Büyük moleküllü olanlar güzel kokuludur. Karbonil grubunun özelliğinden dolayı polar yapılı maddelerdir. 2) Homolog sıra oluştururlar. 3) Aldehitler bir derece yükseltgenerek karboksilli asitleri oluştururlar. 4) Aldehitler indirgendirler. NH 3’lü Ag. NO 3 çözeltisinden (Tollens ayıracı) Ag +1’li metalik Ag’ye indirgerler (Gümüş aynası). Bu tepkime aldehitlerin ayıracıdır. 5) Fehling çözeltisinden Cu +2’ yi Cu+1 e indirgerler. Bu tepkimede aldehitlerin ayıracıdır. 6) Yanma ürünleri CO 2 ve H 2 O’dur. 7) Yapılarında çift bağ bulunduğu için katılma tepkimesi verirler (H 2, NH 3, HCN, Na. HSO 3 ve H 2 O ile katılma tepkimesi verirler. Genelde bu katılma ürünleri kararsızdır.


ALDHİTLERİN ELDESİ 1) Primer (birincil) alkollerin bir derece yükseltgenmesinden aldehitler elde edilir. 2) Uçtaki karbonda iki halojen taşıyan alkanlar (alkildihalojenürler) H 2 O ile tepkimeye sokulursa aldehit elde edilir. 3) Karboksilli asitlerin indirgenmesinden aldehit elde edilir. 4) Birincil alkollerin dehidrojenasyonu ile aldehit elde edilir. 5) Asit klorürlerden aldehit elde edilir.

FORMALDEHİT • Kimya laboratuvarlarında deneylerde kullanılır. • Laboratuvarda anatomi, nekropsi gibi doku muhafazasında çözeltisi kullanılır. Bu çözelti formol ya da formalin adıyla bilinir. Formaldehit aynı zamanda dezenfektandır. • Yapay reçine çözeltisi, formaldehit içerir. Yapay reçine çözeltisinin kullanıldığı başlıca yer laminantlardır. • Ürotropin, idrar yolları enfeksiyonlarında kullanılan bir idrar yolları antiseptiğidir. Ayrıca diüretik (idrar söktürücü) etkisi de vardır. Formaldehit bebe şampuanlarının, birçok kişisel bakım ürününün, banyo köpüklerinin ve bazı taşların terkibine girer.

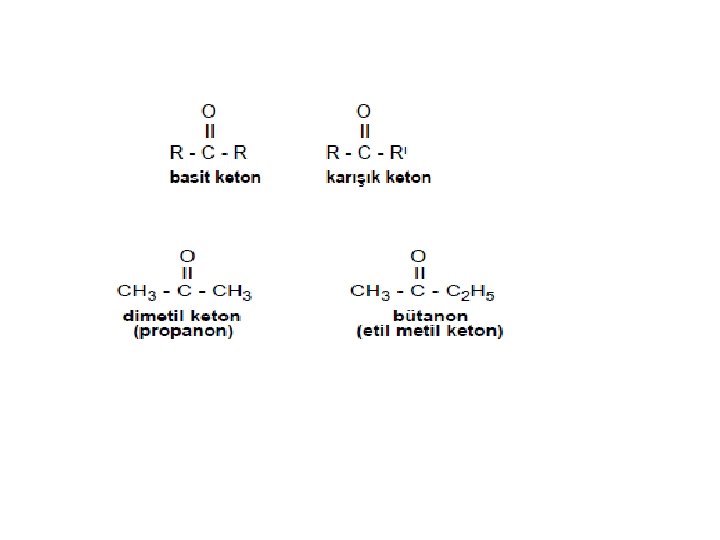
KETONLARIN ADLANDIRILMALARI § Aynı sayıda karbon taşıyan alkanların sistematik adının sonuna -on eki getirilir (sistematik adlandırma). § Ya da alkil grupları okunduktan sonra sonuna keton kelimesi getirilir (özel adlandırma). KETONLARIN GENEL ÖZELLİKLERİ 1) Polar yapıda olduklarından küçük moleküllüleri suda çok çözünür. Molekül büyüdükçe çözünürlük azalır. Hidrojen bağı içermediklerinden kaynama noktaları aynı sayıda karbon içeren alkol ve karboksilli asitlerden düşüktür. 2) Homolog sıra oluştururlar. 3) Ketonlar yükseltgenmez. 4) Ketonların aldehitlerden en önemli farkı indirgen olmamalarıdır. Bundan dolayı NH 3’lü Ag. NO 3 çözeltisinden Ag metalini açığa çıkartamadıkları gibi, Fehling çözeltisinden Cu +2’ yi de indirgeyemezler.

5)Ketonlar bir derece indirgenirse sekonder alkolleri oluştururlar. 6) Çift bağ taşıdıklarından katılma tepkimesi verirler. Aldehitlerdeki katılma tepkimeleri ketonlar için de geçerlidir. Ayrıca alkollerle de katılma tepkimesi verirler. 7) Aynı sayıda karbon taşıyan ketonlar aldehitlerle izomerdirler. En küçük keton 3 karbonlu olduğundan metanal ve etanalın izomeri olan keton yoktur. 8) Ketonların yanma ürünleri CO 2 ve H 2 O bileşikleridir. 9)Aseton kondenzasyon reaksiyonu verir. Kondenzasyon reaksiyonu küçük moleküllerin birleşerek büyük bir molekül ve yanında daha küçük bir molekül oluşturmasıdır. 10) Ketonlar organik maddeleri çözmede kullanılırlar.


KETONLARIN ELDE EDİLMELERİ 1)Sekonder alkollerin bir derece yükseltgenmesinden ketonlar elde edilir. 2) Molekül yapısında ortada bulunan karbonda iki halojen taşıyan alkanlar (alkil dihalojenürler) ile Na. OH çözeltisi karşılaştırılırsa keton hidrat verir. Bu keton hidrattan H 2 O çıkarılırsa keton elde edilir. 3) Alkinlere H 2 O katılması ile keton elde edilir. 4) Organik asitlerin metal tuzlarının ısıtılması sonucu keton elde edilir. Yan ürün olarak kireç taşı açığa çıkar.

Karboksilli Asitler Ø Aldehitlerin oksidasyon ürünü olan karboksilli asitler –COOH grubu içerirler. Ø Biyokimyasal açıdan önemli olanlar; • Formikasit HCOOH formiat • Asetik asit CH 3 COOH asetat • Propiyonik asit CH 3 CH 2 COOH propiyonat • Butirik asit CH 3 CH 2 COOH bütirat • Stearikasit C 17 H 35 COOH stearat • Palmitikasit C 15 H 31 COOH palmitat

ESTERLER Bir karboksilli asit molekülü ile bir alkol molekülünden, bir mol su çekilmesi ile oluşan maddeye ester, bu olaya da esterleşme denir. Esterlerin genel formülleri Cn. H 2 n. O 2’dir. Esterler aynı sayıda karbon atomu içeren monokarboksilli asitlerle izomerdir. Esterleşme olayı bir denge tepkimesi şeklinde yürür. Esterlerin fonksiyonel grubu olan ─ C ─ O ─ , benzer veya farklı iki alkil grubuna bağlıdır.

Adlandırılmaları • Esterler adlandırılırken önce oksijene bağlı alkil grubundan sonra asit grubunun adı söylenir. Asit grubu okunurken -ik asit yerine -at eki getirilerek adlandırılma yapılabilir. Aşağıdaki örneklerde IUPAC ve özel adlandırmalar verilmiştir. 1. Esterler su ile tepkimeye girdiğinde karboksilli asitler ve alkollere dönüşür. 2. Esterler kuvvetli bazlarla tepkimeye girerek karboksilli asit tuzu ve alkol oluştururlar. Oluşan tuza sabun, bu olaya da sabunlaşma denir.

3. Esterler NH 3 ile tepkimeye girdiğinde amit ve alkol oluşur. 4. Esterler Cu, Cr 2 O 3 ve Li. Al. H 4 katalizörlüğünde H 2 ile indirgenirse alkolleri oluştururlar.

AMİNLER • Aminler, amonyağın alkillenmiş türevleridir. Bir amin’in fonksiyonel grubu, amino grubu (NH 2)’dur CH 3 -NH 2 Metiamin CH 3 -N-CH 3 H Dietilamin CH 3 -NCH 3 -CH 3 Trietilamin Aminler, alifatik ya da aromatik aminler olarak adlandırılır. Alifatik aminler de azot, sadece alkil gruplarına veya hidrojenlere bağlıdır. Aromatik aminler de azot, bir veya daha fazla aromatik halkaya bağlıdır.

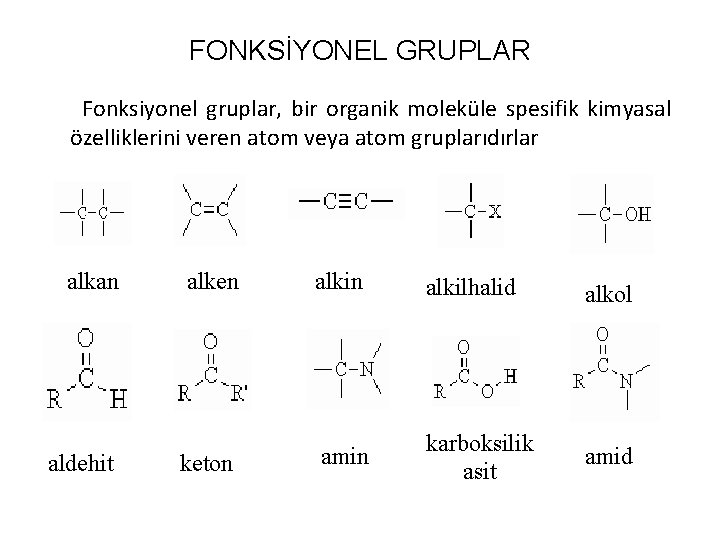
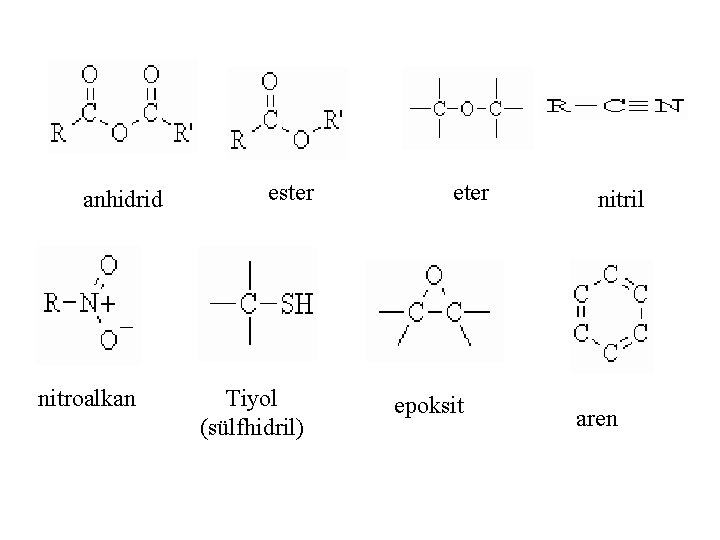
FONKSİYONEL GRUPLAR Fonksiyonel gruplar, bir organik moleküle spesifik kimyasal özelliklerini veren atom veya atom gruplarıdırlar alkan aldehit alken keton alkilhalid alkol amin karboksilik asit amid

anhidrid nitroalkan ester Tiyol (sülfhidril) eter epoksit nitril aren

ASİTLER • ASİTLER Proton vericiler • Kuvvetli bir asitin dissosiyasyonu tamamen iyonlarına ayrışır HCl H+ + Cl. Dolayısıyla: [H+] = [HCl]

BAZLAR • Proton alıcılar, Kuvvetli bir bazın dissosiyasyonu tamamen iyonlarına ayrışır. Na. OH Na+ + OHDolayısıyla: [OH-] = [Na. OH]

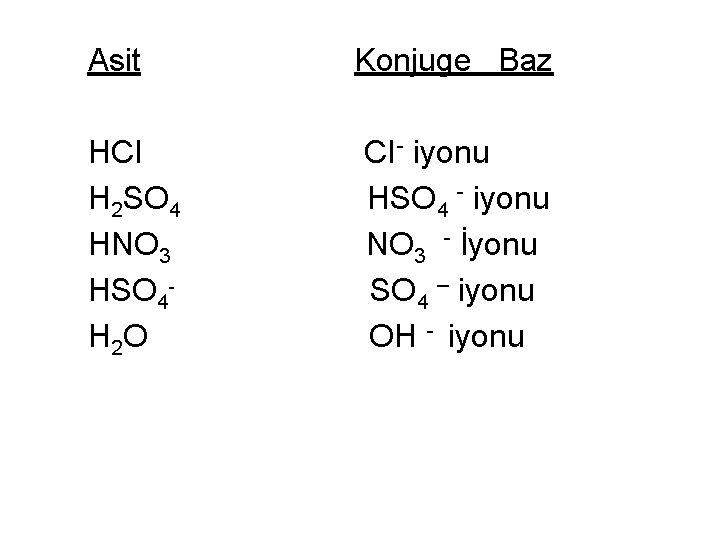
Biyokimyadaki asit ve bazların çoğu ZAYIF ASİT veya ZAYIF BAZ formundadır. Zayıf asitlerde, asit ile konjuge bazı (tekrar asit oluşturmak için proton kabul eden iyon) arasında sabit bir denge vardır. CH 3 COOH + H 2 O Asit 1 Baz 2 H 30+ + CH 3 COOKonjj. asit 2 Konj baz 2 NH 3 + H 2 O Baz 1 Asit 1 NH 4+ Konj. asit 1 + OHKonj. baz 2 Konjuge asit, bir bazın proton alışı, konjuge baz ise asitin proton verdikten sonra oluşan halidir. Konjuge bazların –OH içermesi gerekmez. Bu maddeler sudaki H+’ları bağlayarak OH- konsantrasyonunu artırırlar. Bir asit ne kadar kuvvetliyse, konjuge bazı o kadar zayıftır. Yani, bir asit proton vermeye ne kadar eğilimli ise, onun konjuge bazı proton alıp yeniden asit oluşturmaya o denli az eğilimlidir.

Asit HCI H 2 SO 4 HNO 3 HSO 4 H 2 O Konjuge Baz CI- iyonu HSO 4 - iyonu NO 3 - İyonu SO 4 – iyonu OH - iyonu

Baz NH 3 F – iyonu Konjuge Asit NH 4 + iyonu HF

KARBONHİDRATLAR • KHD lar biyokimyanın konusu olmakla birlikte yalıtımlar, kimyasal reaksiyonları ve üretimleri bakımından organik kimyanın ve endüstriyel kimyanın da konusunu oluştururlar. • Glukoz ve bir miktar frukoz canlılarda enerji kaynağı olarak kullanılırken, sellüloz, pektin, kitin gibi yapısal biyopolimerler olarak doğada bulunurlar.

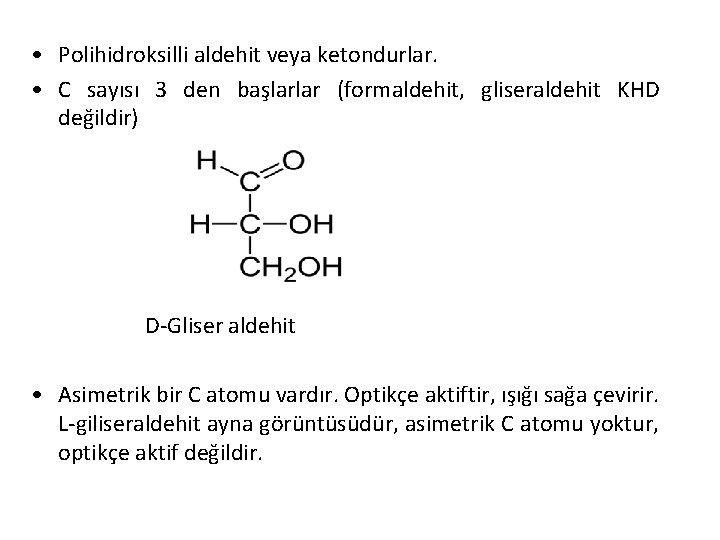
• Polihidroksilli aldehit veya ketondurlar. • C sayısı 3 den başlarlar (formaldehit, gliseraldehit KHD değildir) D-Gliser aldehit • Asimetrik bir C atomu vardır. Optikçe aktiftir, ışığı sağa çevirir. L-giliseraldehit ayna görüntüsüdür, asimetrik C atomu yoktur, optikçe aktif değildir.

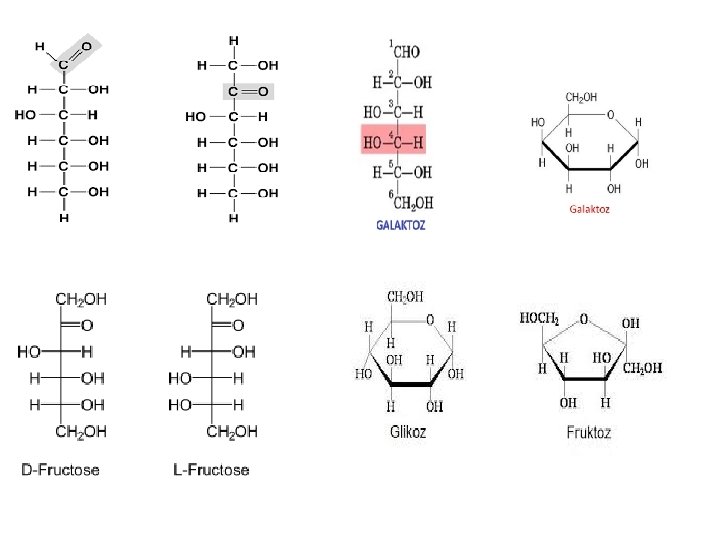
Konfigürasyon Formülleri : C atomlarının taşıdıkları H ve OH grubunun uzaydaki konumlarını gösterir. 6 C’lu monosakkatit Heksozar, KHD’ların en küçük yapıtaşlarıdır, früktoz, glukoz, galaktoz birbirinin izomeridir. Kapalı formülleri; C 6 H 12 O 6

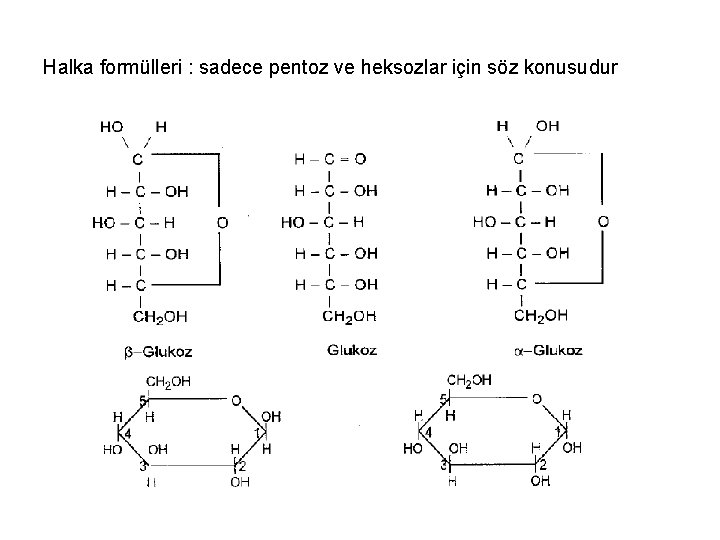
Halka formülleri : sadece pentoz ve heksozlar için söz konusudur


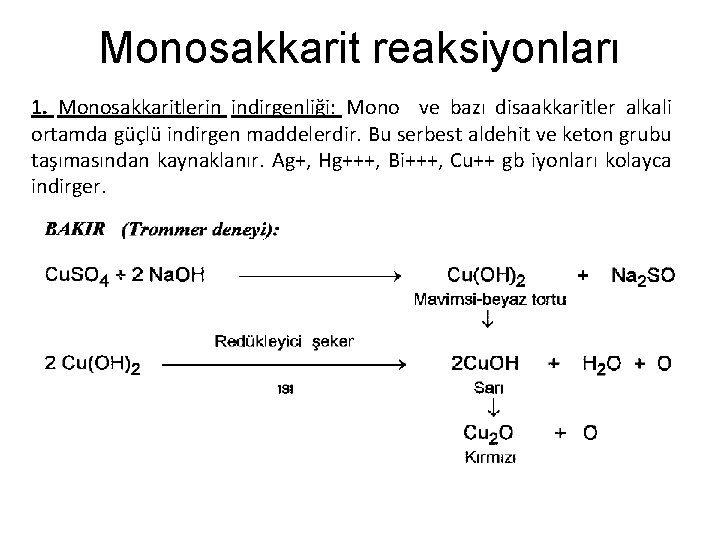
Monosakkarit reaksiyonları 1. Monosakkaritlerin indirgenliği: Mono ve bazı disaakkaritler alkali ortamda güçlü indirgen maddelerdir. Bu serbest aldehit ve keton grubu taşımasından kaynaklanır. Ag+, Hg+++, Bi+++, Cu++ gb iyonları kolayca indirger.

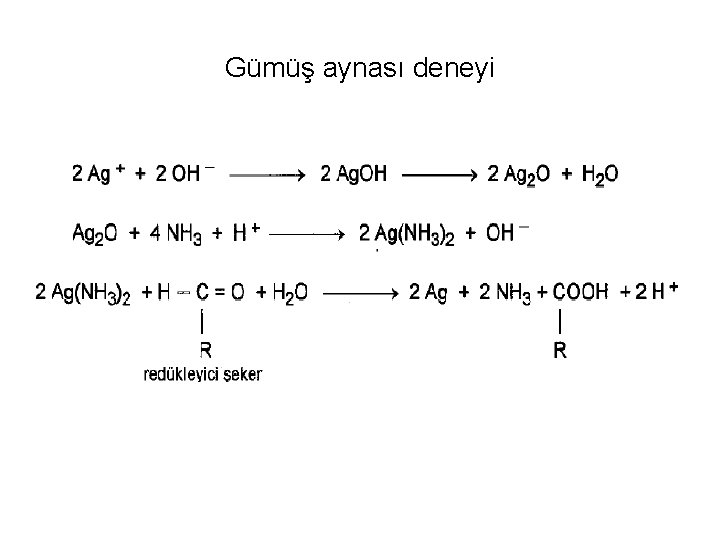
Gümüş aynası deneyi

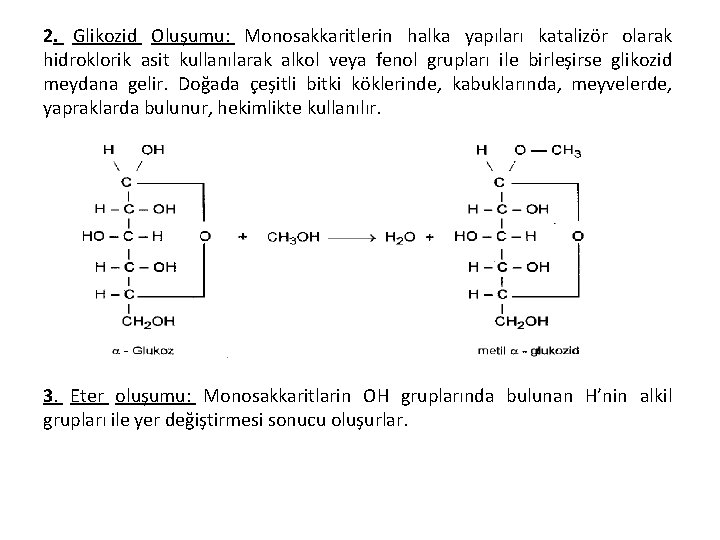
2. Glikozid Oluşumu: Monosakkaritlerin halka yapıları katalizör olarak hidroklorik asit kullanılarak alkol veya fenol grupları ile birleşirse glikozid meydana gelir. Doğada çeşitli bitki köklerinde, kabuklarında, meyvelerde, yapraklarda bulunur, hekimlikte kullanılır. 3. Eter oluşumu: Monosakkaritlarin OH gruplarında bulunan H’nin alkil grupları ile yer değiştirmesi sonucu oluşurlar.

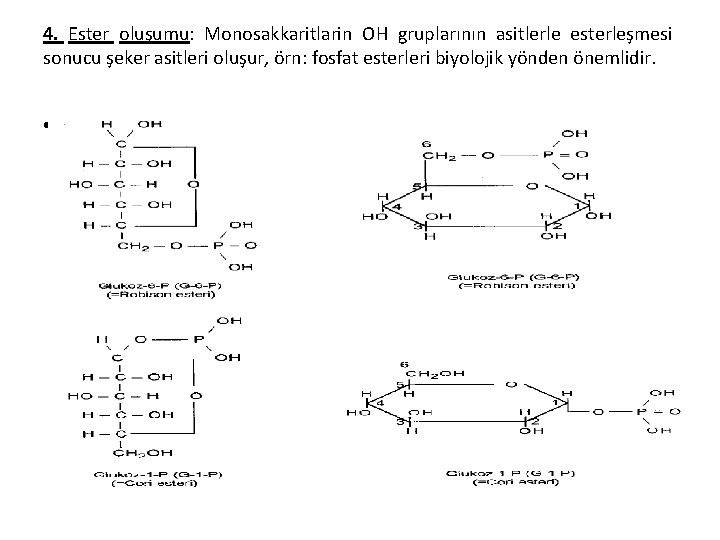
4. Ester oluşumu: Monosakkaritlarin OH gruplarının asitlerle esterleşmesi sonucu şeker asitleri oluşur, örn: fosfat esterleri biyolojik yönden önemlidir. •

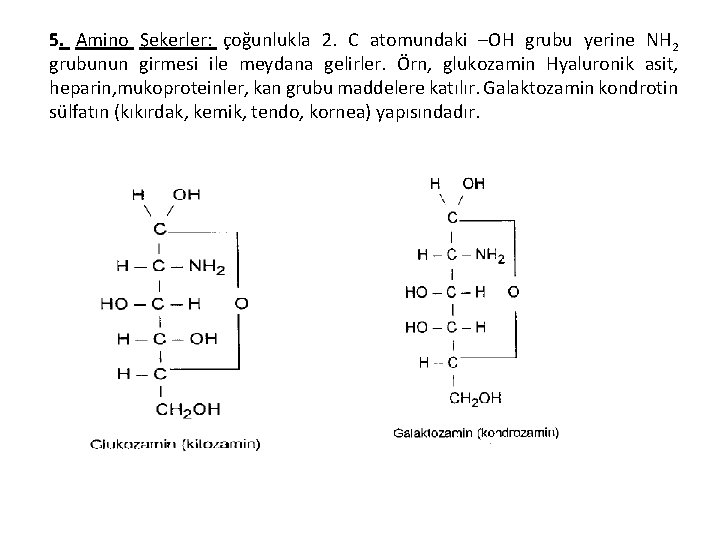
5. Amino Şekerler: çoğunlukla 2. C atomundaki –OH grubu yerine NH 2 grubunun girmesi ile meydana gelirler. Örn, glukozamin Hyaluronik asit, heparin, mukoproteinler, kan grubu maddelere katılır. Galaktozamin kondrotin sülfatın (kıkırdak, kemik, tendo, kornea) yapısındadır.

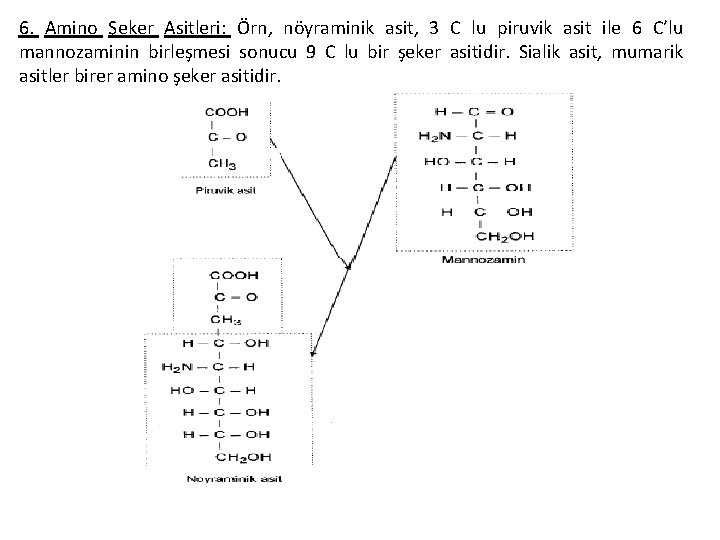
6. Amino Şeker Asitleri: Örn, nöyraminik asit, 3 C lu piruvik asit ile 6 C’lu mannozaminin birleşmesi sonucu 9 C lu bir şeker asitidir. Sialik asit, mumarik asitler birer amino şeker asitidir.

7. Deoksi Şekerler: 2. veya 6. C atomunda O bulundurmayan şekerlerdir. Deoksiriboz nükleik asitlerde bulunur.

8. Şeker Alkolleri: Monosakkaritlerdeki aldehit veya keton gruplarının alkol grubuna indirgenmesi ile oluşuyor. Sorbitol glukozdan, mannitol mannozdan, dulsitol galaktozdan, gliserol gliser aldehitden oluşan bir şeker alkolüdür.

9. Şeker Asitleri: Monosakkaritlerin oksidasyon ürünleridir. C atomlarına göre 3 çeşit meydana gelir. 1. C atomunda aldehitin oksitlenmesi ile –COOH oluşarak glukozdan glukuronik asit meydana gelir. Galaktozdan galaktonik asit vs 2. Sakkarik asitler (dikarboksilik asitler) Aldozların 1. C daki aldehit grubu ile 6. C daki birincil alkolün oksitlenmesi ile COOH’e değişmesi ile oluşur. 3. Üronik asitler, 1. C atomundaki alkol grubunun oksitlenmesi ile oluşur. Glukuronik asit: Mukopolisakkaritler, Kondroitin sülfat, Heparin, Hyaluronik asit yapısında bulunur

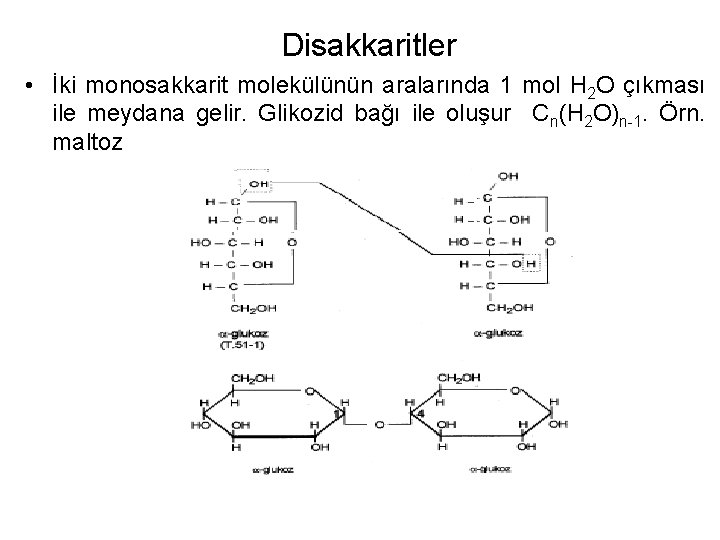
Disakkaritler • İki monosakkarit molekülünün aralarında 1 mol H 2 O çıkması ile meydana gelir. Glikozid bağı ile oluşur Cn(H 2 O)n-1. Örn. maltoz

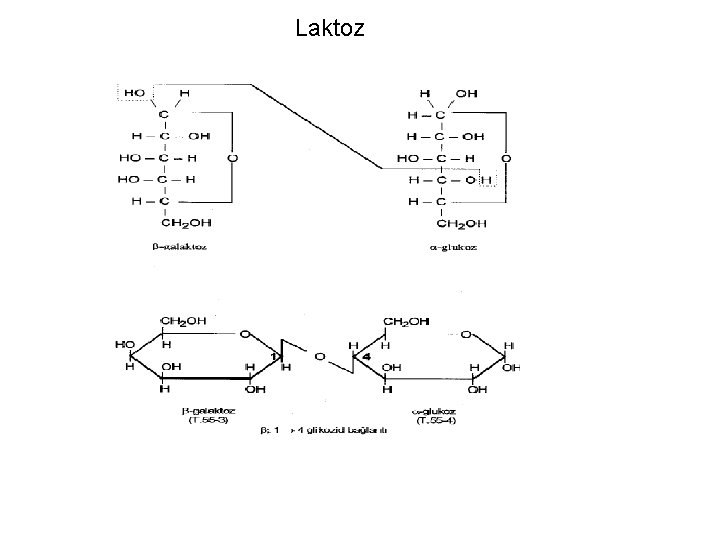
Laktoz

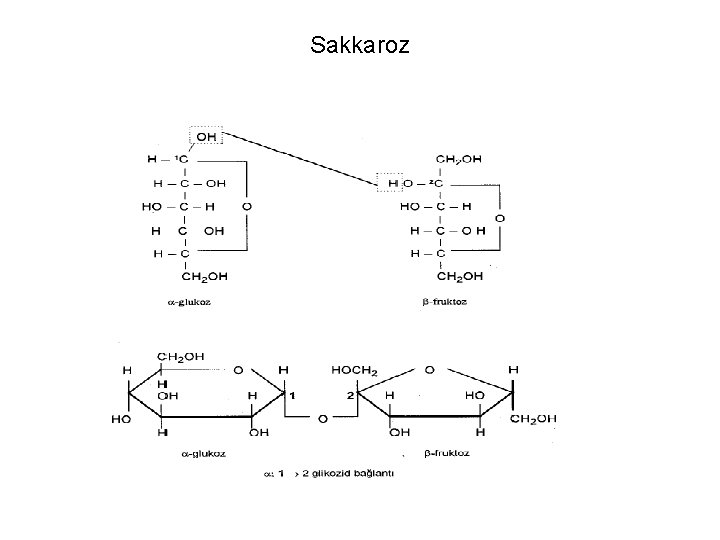
Sakkaroz

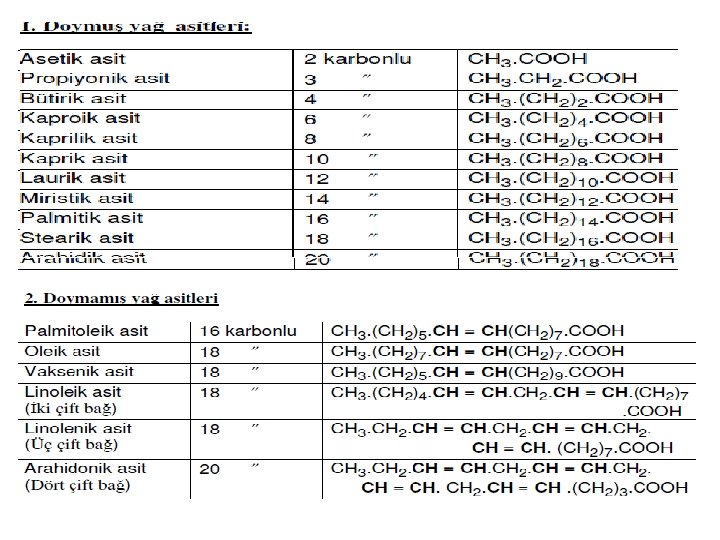
LİPİDLER Lipidler için ortak nokta yağ asidi olmakla birlikte ya taşımayan lipidlerde bulunur ama lipid sınıfından kabul edilmeleri için en azından yağ asitleri ile esterleşirler. Suda erimezler, eter kloroform, benzen, aseton gibi organik maddelerde çözünürler. y. a= R- COOH CH 3 -COOH asetik asit Doğada en çok bulunan ya 18 C’lu oleik asit Doymamış ya. leri Linoleik asit 18 C lu Linolenik asit 18 C lu Arahidonik asit 20 C lu 2 çift bağ 3 çift bağ 4 çift bağ


KİMYASAL ÖZELLİKLERİ 1. Tuz oluşumu: 6 C dan büyük ya nin metallerle (Na, K) yaptığı tuzlara sabun denir. 2. Deterjan oluşumu: ya nin yüksek alkollerinin sülfürik asit esterlerinin metal tuzlarıdır. 3. Çift Bağa ait özellikler: a) Hidrojenlenme, doymuş ya oluşur. b) Oksitlenme, ya nin çift bağlarının oksitlenmesi c) Halojenlenme, Çift bağın F, CI, I, Br gb halojen ile doyurulması

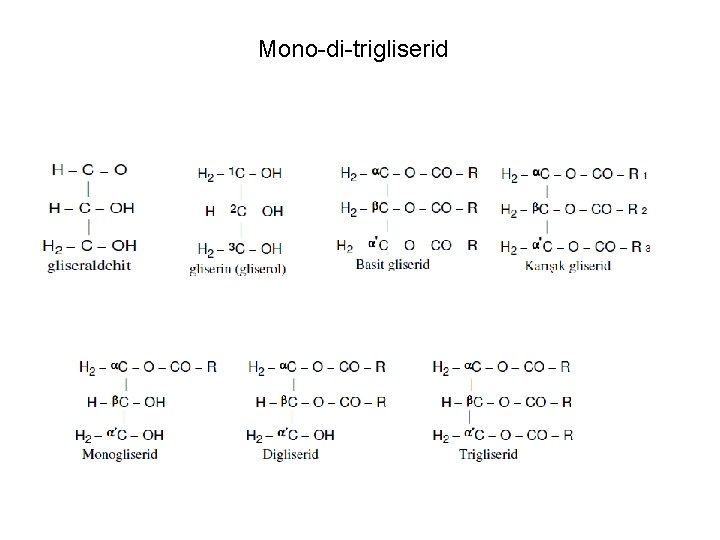
Mono-di-trigliserid

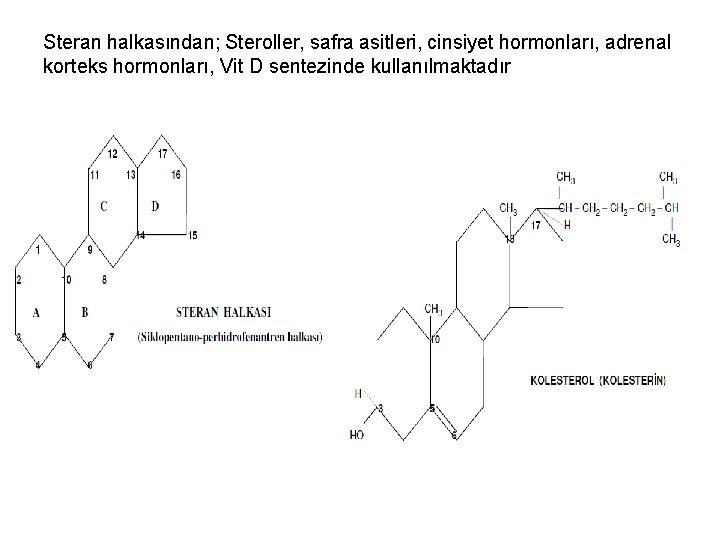
Steran halkasından; Steroller, safra asitleri, cinsiyet hormonları, adrenal korteks hormonları, Vit D sentezinde kullanılmaktadır

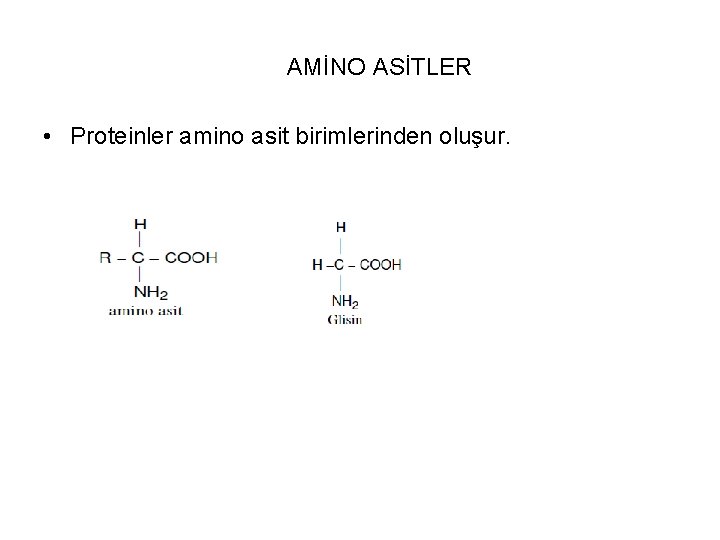
AMİNO ASİTLER • Proteinler amino asit birimlerinden oluşur.

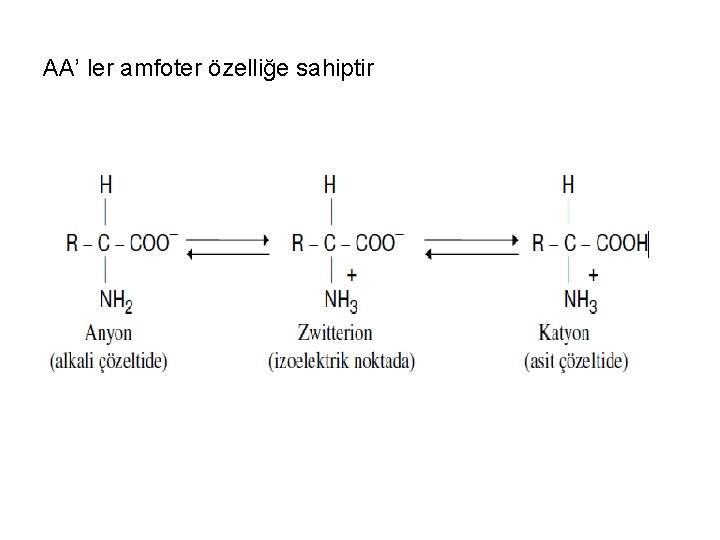
AA’ ler amfoter özelliğe sahiptir

Peptid Bağı: bir aa in karboksil grubu ile diğer aa din amino grubu arasında 1 mol H 20 açığa çıkararak aralında oluşturdukları bağdır.