ORGANK KMYA l Karbon bileiklerinin kimyas olarakta isimlendirilirler
ORGANİK KİMYA

l “Karbon bileşiklerinin kimyası” olarakta isimlendirilirler. l Karbon bileşikleri C ve H’den oluşur. l Bağ türü ve molekül yapılarına göre ya Doymuş (alkanlar, parafinler, alifatikler) l Doymamış (alkenler, alkinler, olefinler) l Ya da l Düz zincirli (asiklik) l Halkalı (siklik) bileşikler olarak gruplandırılırlar. l

l Kovalent bağlı karbon omurgalı moleküller organik bileşikler olarak isimlendirilirler. l Biyomoleküllerin çoğunluğu organik bileşiktir. l Gerek bitkisel gerekse hayvansal organizmaların yapı ve hayatlarını sürdürebilmeleri için gerekli olan klorofil, vitamin, hormon, enzim, koenzim, protein, yağ asidi ve karbonhidrat gibi pek çok bileşik organik yapıdadır.

l Organik kimyanın bir bilim dalı olarak 1780’lerde gelişimi ile birlikte; l Canlı organizmadan elde edilen bileşikler organik, cansız kaynaklardan elde edilen ise inorganik bileşikler olarak tanımlanmıştır.

Scheele l Üzümden = Tartarik asit l Elmadan = Malik asit l Limondan = Sitrik asit l Sütten = Laktik asit l İdrardan = Ürik asit elde etti.

l Molekül formülleri aynı kimyasal özellikleri farklı olan bileşiklere İZOMER denir. l Liebig-Wöhler: İzomer moleküllerin varlığını göstererek izomeri kavramını tanımladılar.

l Organik bileşikler ile inorganik bileşikler arasında farklar vardır. l Bu farklılıklar karbonun periyodik cetveldeki yerinden kaynaklanır.

l Organik bileşikler genellikle l değildir. yanıcıdır. l Organik bileşiklerin erime l (3000 C den düşüktür). Organik bileşikler l Organik bileşiklerde izomerizm büyük rol oynar. İnorganik bileşiklerin çoğu suda çözünürler. l İnorganik bileşikler iyonik yapıdadır. Organik bileşiklerin çoğunun yapısı iyonik değildir. l l genellikle suda çözünmezler. İnorganik bileşiklerin erime noktaları genellikle yüksektir. noktaları genellikle düşüktür l İnorganik bileşikler yanıcı l İnorganik bileşiklerde izomerizm yoktur.

l Organik bileşiklerin oluşumunda katalizörlerin rolü büyüktür. Farklı katalizörler kullanılarak aynı maddelerden farklı bileşikler oluşturulabilir. l Organik bileşiklerle yapılan reaksiyonlar fazla ısı ve zaman gerektirir. l Organik bileşiklerin dansitesi genellikle düşüktür. l Organik bileşiklerin reaksiyonları kantitatif değildir. l İnorganik bileşiklerin reaksiyonları daha hızlıdır.

Orbitaller ve Kovalent Bağlanma l Hidrojen Bağlanma: Hidrojen (H 2) en basit moleküldür. l Hidrojen atomu 1 s orbitalinde bir elektron taşır. l İki hidrojen atomu arasında bir moleküler orbital oluşur ve kovalent bağ meydana gelir. Bu moleküler orbitale sigma (σ) moleküler orbitali, oluşan bağa sigma bağı denir.

Karbonun melez orbitalleri l Karbon 1 s orbitalinde 2 elektron taşır ve dolu olan bu orbital bağ yapımında kullanılmaz. l Karbonun değerlik eletronları ikinci ana enerji düzeyindeki 4 elektronudur. l İkinci ana enerji düzeyinde 2 s ve üç 2 p olmak üzere 4 orbital vardır. l Karbon bağ yaparken bu dört orbitali bu durumlarıyla kullanmaz onları melezleştirir.

Üç şekilde melezleştirilir l 1 - sp 3 melezleşmesi, karbon 4 tekli bağ yaptığında kullanılır. l 2 - sp 2 melezleşmesi, karbon çift bağ yaptığında kullanılır. l 3 - sp melezleşmesi, karbon üçlü bağ veya bitişik (kümüle) çift bağ yaptığında kullanılır.

l Karbon atomu, melez orbitaller daha iyi örtüştükleri, daha düşük enerjili, daha kararlı moleküller oluşturdukları için melezleşmiş orbitallerle bağ yapar.

sp 3 Melezleşmesi l Metanda C atomu 4 H’ine 4 eşdeğer bağ ile bağlanmıştır. CH bağları arasındaki bağ açısı 109, 50 dir. Bu dört eşdeğer bağ dört atomik orbitalin bir 2 s ve üç 2 p orbitallerinin karışmasıyla sp 3 melez orbitalleri oluşur.

l Karbon çekirdeğinin etrafında dört sp 3 melez orbitali, negatif yüklerin birbirini itmesi nedeniyle olabildiğince uzak, birbirlerinden bir yüzlünün (tetrahedron) yönlenmiş durumda düzgün dört köşelerine bulunurlar. sp 3 melezleşmesi yapmış C atomuna düzgün dört yüzlü C atomu da denir.

l Herhangi bir molekülde, bir C atomu dört başka atoma bağlanmışsa sp 3 melezleşmesi yapmıştır ve bağın dördü de sigma bağıdır. Eğer bir engel yoksa bağ açıları 109, 50 dir.

sp 2 Melezleşmesi l Karbon atomu, başka bir atoma iki bağ ile bağlanmışsa sp 2 melezleşmesi yapmıştır. l Karbon, sp 2 bağlayıcı orbitallerini oluşturmak için 2 s orbitali ile 2 p orbitallerinden ikisini melezleştirir. l Melezleşme için üç atomik orbital kullanıldığından üç tane sp 2 melez orbitali oluşur.

l Karbon çekirdeği etrafındaki üç sp 2 melez orbitali birbirinden olabildiğince uzak olacak şekilde yerleşirler. Aralarındaki açı 1200 dir. l sp 2 melezleşmesi yapmış karbon atomuna eşkenar karbon denir.

l Etilen’de karbon atomları birer sp 2 melez orbitallerinin örtüşmesiyle kendi aralarında bir sigma bağı oluştururlar. Sigma bağı çift bağları oluşturan bağlardan biridir. l Karbon atomlarının geriye kalan ikişer sp 2 melez orbitalleri H atomlarıyla bağ yapar. Ayrıca her bir C atomu melezleşmemiş bir p atomik orbitali taşır. Geriye kalan bu p orbitalleri, biri sigma bağları düzleminin altında, diğeri ise üstünde olan iki loba sahiptirler ve birer elektron taşırlar.

l Eğer bu p elektronları, bağlayıcı bir moleküler orbitalde ortaklaşırlarsa sistemin enerjisi azalır. P bulunduklarından orbitalleri yan yana örtüşürler. Yandan örtüşme ile oluşan bu bağa pi (π) bağı denir ve çift bağı oluşturan diğer bağdır.

l Başka 3 atoma bağlanmış C atomu sp 2 melezleşmesi yapmıştır. l Kararlı bileşiklerde sp 2 melezleşmesi yapmış C atomunun p orbitali komşu bir atomun p orbitali ile örtüşür. Bu komşu atom karbon olabileceği gibi başka bir elementin atomu da olabilir.

l İki p orbitalinden oluşan pi bağı sigma bağına göre daha az kararlıdır. l Pi elektronları daha yüksek enerjili oldukları için dış etkilere karşı sigma bağı elektronlarından daha duyarlıdırlar, daha kolay polarlanırlar ve yüksek enerjili bir orbitale daha kolay atlarlar. l Dışarıdaki bir atom veya molekül pi bağına daha kolay saldırır (etkin bölge).

l Pi bağı, çift bağlı C atomlarını sıkıya tutar, ayrıca bu C atomlarına bağlı diğer atomları da sabit tutar. l Çift bağlı karbon atomlarının ve bunlara bağlı grupların çift bağ ekseni etrafında dönebilmeleri için pi bağının kopması gerekir.

sp Melezleşmesi l Bir C atomu yalnızca iki başka atoma bağlanmışsa sp melezleşmesi yapmıştır. l sp melezleşmesi bir 2 s orbitali ile bir 2 p orbitalinin karışımından oluşur. l Herbiri tek elektron taşıyan iki 2 p orbitali melezleşme dışı kalır.

l P orbitaller hem birbirine, hem de sp orbitaline diktir. Orbitalleri arasında 1800’lik açı bulunmaktadır. l Asetilen’de iki C atomu sp-sp sigma bağlarıyla bağlanmıştır. Ayrıca her C bir H atomuna sp-s sigma bağıyla bağlıdır. l Bir C’daki iki p orbitali de iki pi-bağı yapmak üzere diğer C’un iki p orbitali ile örtüşür. Yani sp melezleşmesinde 1 sigma ve 2 pi bağı bulunur.

Fonksiyonel (işlevsel) Gruplar l Molekülün kimyasal etkinliğe sahip bölgesine işlevsel grup denir. l Bir organik molekülde kimyasal tepkimenin meydana gelmesini sağlayan pi bağı ya da elektronegatif (veya elektropozitif) bir atom bir işlevsel grup ve ya işlevsel grubun parçası olabilir.

l Aynı işlevsel grubu taşıyan bileşikler benzer kimyasal tepkimeleri verme eğilimindedirler. l Örneğin: hidroksil grubu taşıyan moleküller benzer kimyasal tepkimeler verirler ve alkol sınıfına girerler. l Aynı işlevsel grubu taşıyan bileşiklerin kimyasal özellikleri benzer olduğu için bunları bir genel formül ile göstermek mümkündür.
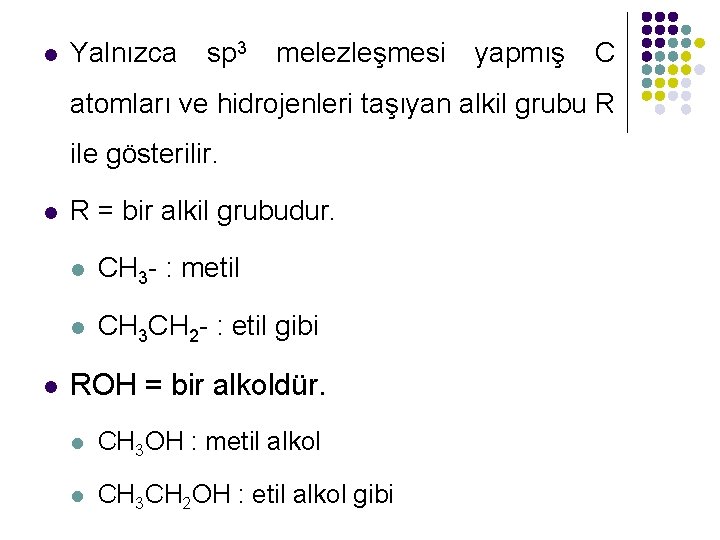
l Yalnızca sp 3 melezleşmesi yapmış C atomları ve hidrojenleri taşıyan alkil grubu R ile gösterilir. l l R = bir alkil grubudur. l CH 3 - : metil l CH 3 CH 2 - : etil gibi ROH = bir alkoldür. l CH 3 OH : metil alkol l CH 3 CH 2 OH : etil alkol gibi

Karbonil grubu l Karbonil grubu (C=O), çeşitli işlevsel grupların bir bölümüdür. l Bileşiklerin işlevsel grubu ve sınıfı, karbonil grubuna bağlı diğer atomlar tarafından tayin edilir.

l Eğer bu karbonil grubuna, l Bir H bağlanırsa aldehit meydana gelir. l İki C bağlanırsa keton oluşur. l OH grubu bağlanırsa karboksilli asitler oluşur.

Konjuge çift bağlar l Organik moleküllerde çift bağlar başlıca iki konumda bulunabilirler. l Çift bağlar arasında birer tek bağ varsa bunlara konjuge çift bağlar denir. l Çift bağlar arasında birden fazla tek bağ varsa bunlara ayrık (izole) ya da konjuge olmayan çift bağlar denir (yani çift bağlardaki karbon atomları komşu değildir).

Aromatik Sistemler l Benzen halkalı bir bileşiktir. l Her C sp 2 melezleşmesi yapmış 6 C’dan oluşur. l Her bir C, bir H’e bağlıdır.

Organik Bileşiklerde İzomeri l Sadece C ve H içeren bir bileşik hidrokarbon adını alır. l Metan, Etilen, Benzen gibi Yalnız sp 3 melezleşmesi yapmış karbon atomlu hidrokarbonlara alkan denir. Eğer bunların C atomları halka biçiminde birleşmişse sikloalkanlar adı verilir.

l Alkan ve sikloalkanlara doymuş hidrokarbonlar adı verilir. l Bu bileşikler H ile reaksiyon vermezler. l Pi bağı içeren bileşiklere doymamış bileşikler denir. Bu bileşikler H ile tepkimeye girerek doymuş ürünler verir. l Aynı molekül formülü ile gösterilen iki yada daha fazla sayıda farklı bileşiğe izomer denir.

İzomerlerin Sınıflandırılması Yapı (konstitüsyon) İzomeri: Aynı yapıtaşlarının farklı sıralanması - İskelet izomeri - Pozisyon izomeri - Fonksiyonel izomeri Konfigürasyon (stereo) izomeri: Şiralite Cis-Trans İzomeri Konformasyon izomeri: Serbest dönmenin sonucu

Yapı İzomerleri l Organik bileşiklerin yapılarındaki çeşitlilik l Molekülde bulunan farklı sayıdaki atom tiplerinden l Bir moleküldeki atomların birbirine bağlanma düzeninden kaynaklanabilir. l Aynı molekül formülü ile gösterildiği halde atomların bağlanma düzenleri farklı olan bileşiklere yapı izomeri denir.

l İskelet izomeri: Temel iskeletteki C atomlarının farklı dizilimleri Örnek: n-hekzan, 2 -metil pentan Üç yada daha az sayıda C içeren atomların izomeri yoktur. Dört C’lu alkanda karbon atomları düz ve dallanmış zincirli olmak üzere iki farklı şekilde düzenlenebilir. Bir işlevsel grubun bir molekülde farklı durumlarda bulunması da yapı izomerisine neden olur.

Pozisyon izomeri: Primer (I) C atomu: Komşu C atomuna tek valansları ile bağlanmışlardır. Zincir başında ve sonunda yer alır. Sekonder (II) C atomu: Zincir içinde yer alırlar, komşu C atomuna iki valansları üzerinden bağlanırlar.

Tersiyer (III) C atomu: Komşu 3 C atomuna 3 valansları üzerinden bağlanırlar. Zincirdeki dallanma noktasında yer alırlar. Quarter C atomu: Komşu 4 C atomuna 4 valansları üzerinden bağlanırlar. Zincirde her iki yana dallanma olan bölgede yer alır.

l Fonksiyonel İzomeri: Fonksiyonel grupların farklı pozisyonlarda yer alması. Örneğin C 2 H 6 O molekül formülü için iki farklı yapı molekülü yazılabilir. § CH 3 OCH 3 (dimetileter): oda sıcaklığında gaz olup, soğutucu ve itici gaz olarak kullanılır. § CH 3 CH 2 OH (etilalkol): oda sıcaklığında sıvıdır. Hem çözücü hemde alkollü içeceklerin yapımında kullanılır.

Konfigürasyon izomeri l Cis-Trans İzomeri: Halka sistemindeki ve çift bağlardaki substitüentlerin farklı dizilişi ile oluşur. Bir alkenin yapısını yazarken sp 2 melezleşmesi yapmış C atomlarını ve bunlara bağlı diğer atomları bütünüyle bir düzlem içindeymiş gibi gösteririz. l Benzer iki grup l Çift bağın iki yanındaysa molekül cis, l Çift bağın karşıt yanlarında ise molekül trans yapıdadır.

l Cis ve trans 1, 2 -dikloreten farklı fiziksel özelliklere sahiptir. l Bunlar değişik bileşiklerdir. Ancak bunlar yapı izomerleri değildirler. l Çünkü, cis ve trans izomerlerde atomların sırası ve çift bağın yeri her iki bileşikte aynıdır.

l Cis ve trans 1, 2 -dikloreten bileşikleri birbirinin steroizomeridir. l Yani, bunlar sadece atomlarını uzaydaki dizilişleri farklı olan, aynı yapıya sahip değişik bileşiklerdir. l Bunlar geometrik izomerlerin özel bir grubunu oluşturur. Bunlara cis-trans izomerlerde denir.

l Şiralite (Molekül asimetrisi, Optik izomeri): Asimetrik C atomundaki farklı dizilim. l Kiral (asimetrik) karbon atomu: Dört farklı gruba bağlanmış C atomuna kiral karbon atomu veya asimetrik karbon atomu denir. Aslında kiral olan C atomu değil moleküldür. l Kiral bir molekülün en önemli yapısal özelliği C atomunun sp 3 melezleşmesi yapmış olmasıdır. l İki enantiomeri vardır (L – D).

l Üst üste çakışmazlık (kirallik) dışında enantiomerlerin yapıları aynıdır. Bu nedenle hemen tüm fiziksel ve kimyasal özellikleri aynıdır. l Ancak, iki özelliği farklıdır; l Diğer asimetrik bileşiklerle etkileşimi l Polarlanmış ışık ile etkileşimi Adi ışık, çeşitli düzlemlerde dalga boylarında hareket eden ve çeşitli dalgalardan oluşmuştur. Dalga hareketi, ışığın yayılma doğrultusuna diktir.

l Polarize ışığın yayılma düzlemini sağa çeviren enantiomere destrorotatori yada sağa çeviren denir. l Bunun ayna görüntüsü polarize ışığın yayılma düzlemini sola çevirir ve buna levorotator yada sola çeviren adı verilir. l Adlandırmada sağa çeviren (+), sola çeviren (-) işaretiyle belirtilir

l Bir bileşiğin optik izomerlerinin maksimum sayısı 2 n’dir. l n: kiral karbonların sayısıdır. l 2 asimetrik karbonu varsa 4 stereoizomeri olabilir. l 3 asimetrik karbonu varsa 8 stereoizomeri olabilir.

Konformasyon İzomeri l Konformasyonları göstermede üç çeşit formül kullanılır; l 1) Üç boyutlu formüller l 2) Top ve çubuk formülü l 3) Newman iz düşümleri l Top ve çubuk formülü ile üç boyutlu formül bir bileşiğin moleküler modelinin üç boyutlu gösterilişidir. l Newman izdüşümünde molekülün, yalnızca iki C atomu arkaya getirilmiştir. Öndeki C’un taşıdığı bağlar yuvarlağa kadardır.
- Slides: 48