Sulu Faz Atmosfer Kimyas Sulu Faz Atmosfer Kimyas















![Sulu Faz Sülfür Kimyası-4 0=[H+]3+(Kw+HSO 2+K 1 p. SO 2)[H+]-2 HSO 2 K 1 Sulu Faz Sülfür Kimyası-4 0=[H+]3+(Kw+HSO 2+K 1 p. SO 2)[H+]-2 HSO 2 K 1](https://slidetodoc.com/presentation_image_h/ecee8647148fd9ebc1abd78a3c1e7e6b/image-22.jpg)




















![• Elektronötralite Eşitliği: [H+] + [NH 4+] = [OH-] + [HO 2 -] • Elektronötralite Eşitliği: [H+] + [NH 4+] = [OH-] + [HO 2 -]](https://slidetodoc.com/presentation_image_h/ecee8647148fd9ebc1abd78a3c1e7e6b/image-45.jpg)






![• [SO 2. H 2 O] = HSO 2. PSO 2 ----------(1) • • [SO 2. H 2 O] = HSO 2. PSO 2 ----------(1) •](https://slidetodoc.com/presentation_image_h/ecee8647148fd9ebc1abd78a3c1e7e6b/image-53.jpg)
- Slides: 53

Sulu Faz Atmosfer Kimyası

Sulu Faz Atmosfer Kimyası • Sulu çözeltilerde oluşan kimyasal tepkimeleri içeren heterojen kimyanın önemli bir bölümünü oluşturur. • Tepkime asıltı tanecik, sis damlacığı veya bulut damlacığı yüzeyinde ya da içinde olur • Ozonun stratosferde bahar ayında görülen kaybı, SO 2 ve NOx gibi gazların asitli bileşiklere yükseltgenip asit yağmuru halinde yağması, atmosferdeki partikül maddenin atmosfere bırakılan gazların dönüşümüyle partikül maddenin miktarının ve içeriğinin değişerek çevreye olan etkileri farklı fazlarda gerçekleşen kimyasal tepkimelerin (Heterojen kimya) bir sonucudur. • SO 2’nin %70’i sulu faz tepkimelerle SO 24 haline dönüşür.

Önemli Noktalar • Asıltı taneciklerde olan tepkimeler laboratuardaki sulu çözeltilerdeki tepkimelerden iki yönden ayrılır: • 1. Bulut ve sis damlacıkları dışındaki atmosferdeki asıltılar yoğun tuz çözeltileridir. Yüksek iyonik kuvvet nedeniyle denge ve hız sabitleri seyreltik çözeltilerden çok farklıdır. Birçok laboratuar verisi seyreltik çözeltiler için olduğundan, asıltı tanecik kimyasında kullanılmaları sonuçlardaki belirsizlik kaynaklarından biridir.

Önemli Noktalar • 2. Laboratuardaki çözeltilerde madde konsantrasyonu, çözeltiye konulan madde miktarı ile hesaplanır. Atmosferdeki taneciklerde ise madde dış ortamla sürekli bir alışveriş halindedir. Bu nedenle hem maddenin fazlar arasındaki dengesi, hem de maddenin fazlar arasındaki transfer hızının bilinmesi gerekir.

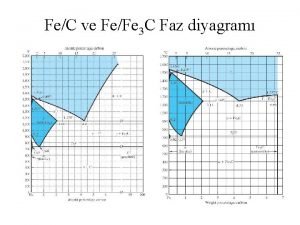
Sulu Faz Kimya Aşamaları 2. Türün çözünmesi (gas-sıvı arası geçiş 1. Yüzeye difüzyon 3. Sulu fazda difüzyon A B 4. Kimyasal tepkime veya iyonlaşma Su Damlacığı

2. Türün Çözünmesi: Bir maddenin su içinde emildiğinde sulu fazdaki konsantrasyonu dışarıdaki gaz konsantrasyonu ile dengeye erişecektir. Bir gazı bir sıvı içerisindeki çözünebilirlik dengesi aşağıdaki tepime ile gösterilir. A(g) A(aq) A(g) + H 2 O AH 2 O Gazın suda çözünebilirliği Henry Kanunu ile Her litre verilir: çözeltideki mol Henry Kanunu Sabiti = (mol/l) / atm cinsinden A miktarı (molarite) Gaz fazında A’nın kısmi basıncı (atm)

2. Türün Çözünmesi: Henri Sabiti büyükse gazın çözünmesi daha çoktur Kısmi basıncı ideal gaz kanunu kullanarak mol/L cinsinden yazarak Birimsiz Henry Sabiti elde edilir. Sıcaklık (K) Gas Sabiti = 0. 082 Latm/(mol K)

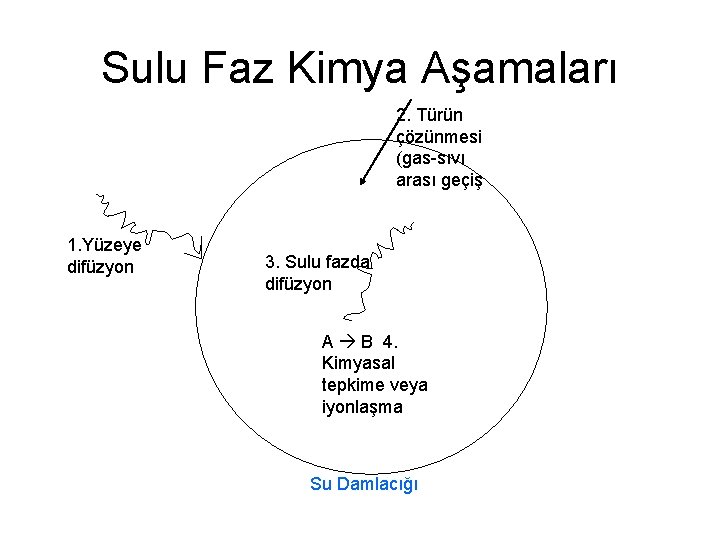
Tür HA (298 K), mol/L atm HA -∆H/R, K SO 2 1. 23 30. 05 3120 H 2 O 2 7. 45 E 4 1. 81 E 6 6620 HNO 3 2. 1 E 5 5. 1 E 6 HNO 2 49 1195 4780 O 3 1. 13 E-2 25. 3 E-2 2300 O 2 1. 3 E-3 29. 1 E-3 NO 2 1. 0 E-2 22. 4 E-2 2500 NO 1. 9 E-3 42. 6 E-3 1480 CO 2 3. 4 E-2 76. 2 E-2 2420 NH 3 75 1680 3400 CH 3 C(O)O 2 NO 2 2. 9 65. 0 5910 HCl 727 16. 3 E 3 2020 HCHO 6. 3 E 3 1. 4 E 5 6460 NO 3 2. 1 E 5 47 E 5 8700 OH. 25 560 5280 HO 2. 0 E 3 4. 5 E 4 6640 Birimsiz Tablo 1: Su içerisinde çözünen gazların Henry Kanunu Sabitleri. (Pandis ve Seinfeld, 1989) HA diğer denge sabitleri gibi sıcaklığa bağlı olarak değişir. Sıcaklık azaldıkça sıvı içerisinde çözünürlük artar. Van’t Hoff eşitliği ile farklı sıcaklıklardaki HA lar hesaplanabilir. Küçük sıcaklık aralıkları üzerinde bu eşitlik kullanılır. Tablo 1

Atmosferdeki Su Miktarı • Dünyadaki toplam suyun sadece %0. 001’iatmosferde bulunur. (%97 okyanuslar, %2. 1 kutup buzulları, %0. 6 akuifer) • Sıcaklık arttıkça havanın taşıyabileceği maksimum su buharı miktarı da artar. • Hava 30°’de 30. 3 g/m 3 su taşıyabilir, 0’de bu miktar sadece 4. 8 g/cm 3 tür.

Atmosferdeki Su Miktarı 1 kg hava, 20 C 10 C 0 C 7 gr H 2 O buharı 3. 5 gr su 20 C’de kapasite: 14 gr H 2 O buhar içeriği: 7 gr Bağıl nem: 7/14 = 50% 10 C’de kapasite: 7 gr 0 C’de kapasite: 3. 5 gr H 2 O buhar içeriği: 7 gr H 2 O buhar içeriği: 3. 5 gr Bağıl nem: 7/7 = 100% Bağıl nem: 3, 5/3, 5 = 100%

Atmosferdeki Su Miktarının İfadesi • L = atmosferin sıvı fazda su miktarı cm 3 su/cm 3 hava • Sıvı su miktarı türlerin gaz ve sulu fazdaki yer alma yüzdelerini etkiler. • Her çözünebilir bir madde için sulu faza geçen gaz miktarı var olan sıvı su miktarına bağlıdır, ya da aynı şekilde sulu fazdaki madde konsantrasyonu var olan çözülebilir gaz miktarıyla kontrol edilir.

Çap(mm) L p. H Pus 0. 05 -0. 5 10 -5 – 10 -4 1 -8 Bulut 10 0. 1 -1 3 -6 Sis 10 0. 05 -0. 5 2 -6 Yağmur 500 -5000 0. 1 -1 4 -5 Hangi türlerin çözündüğüne bağlı olarak değişir.

Gaz ve Sıvı Faz Arasındaki Bölüşme • Birimsiz nicelik olarak HART su miktarı ile çarpıldığında = her litre havada sulu çözeltide bulunan A’nın mol sayısı/ her litre havada bulunan A’nın mol sayısı • Eğer HAL = 1 => A her fazda eşit miktarda • Eğer HAL << 1 => A daha çok gaz fazda • Eğer HAL >> 1 => A daha çok sulu fazda

Örnek • Tablo 1’de verilen maddelerden L = 10 -6 için hangisi gaz fazında olacaktır? • ĤAL = 1 => HARTL =1 HA = 4 x 104 M/atm Eğer HA>4 x 104 ise sulu fazda Eğer HA<4 x 104 ise gaz fazda. Tablodan görüldüğü gibi çoğu bileşik daha çok gaz fazında (HNO 3, NO 3 , HO 2, HCHO ve H 2 O 2 dışında).

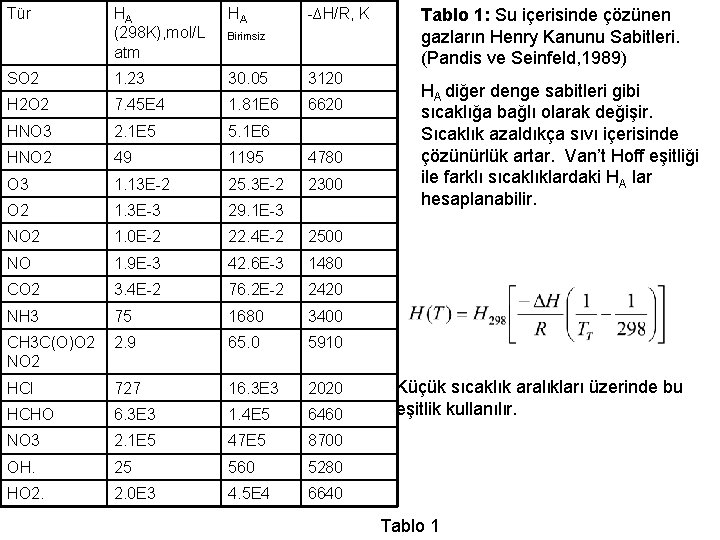
Uyarı • Henry kanunu bulunabilecek A miktarına bir sınır tanımadığından Henry kanunu herhangi bir tür için uygulandığında sulu fazdaki konsantrasyon olduğundan daha fazla hesaplar. O neden bu değer bir Amax değer tarafından kontrol edilmelidir. • Henry sabiti sadece sis ve yağmur damlalarına uygulanmalıdır. Pusta bulunan asıltı taneciklerde yüksek derişim söz konusu olduğundan formüldeki konsantrasyon yerine maddelerin etkinliği(a) kullanılmalıdır. Gaz fazdaki tüm A’nın çözeltiye gittiğini varsayarak hesaplanan [A]’nın sulu fazdaki konsantrasyonu Etkinlik hesabı

Sülfür Oksitler • SO 2 hem gaz hem de sulu fazdaki süreçlerle tepkimeye girer. Kuru ve yaş çökelme ile çıkar. Gaz Fazdaki Sülfürlü Bileşiklerin Kimyası • 2 SO 2 + O 2 2 SO 3 k çok düşük, o nedenle atmosferdeki SO 3’ün kaynağı değildir. • Gaz fazda OH. İle tepkime birinci sırada yer alır. SO 2 + OH. + M HOSO 2. + O 2 HO 2. + SO 3 + H 2 O + M H 2 SO 4 + M

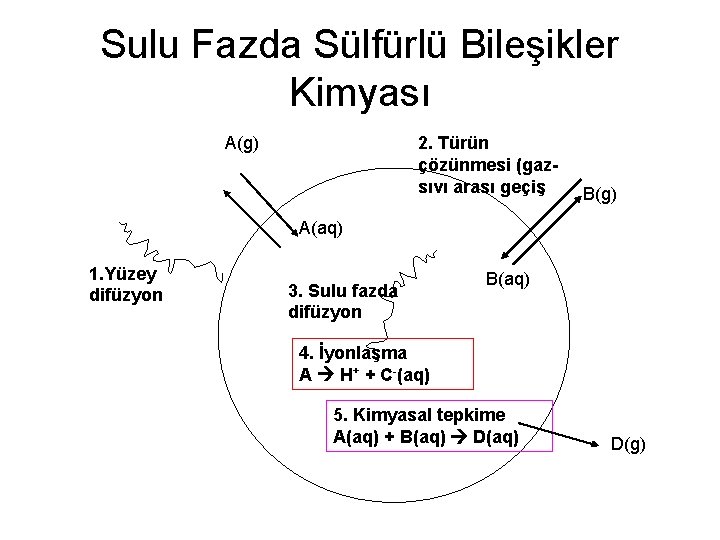
Sulu Fazda Sülfürlü Bileşikler Kimyası A(g) 2. Türün çözünmesi (gazsıvı arası geçiş B(g) A(aq) 1. Yüzey difüzyon 3. Sulu fazda difüzyon B(aq) 4. İyonlaşma A H+ + C-(aq) 5. Kimyasal tepkime A(aq) + B(aq) D(aq) D(g)

Sulu Fazda Sülfürlü Bileşikler Kimyası • Maddenin iki faz (gaz ve tanecik içindeki sulu faz) arasındaki taşınma hızının damlacık içindeki kimyasal tepkimelerden daha hızlı olduğu varsayımı yapılırsa ilgileneceğimiz süreçler 2, 4 ve 5 olacaktır. • Çok büyük bulut damlacıkları gibi damlacıklar dışında tanecik içindeki difüzyon (3) gaz-tanecik tepkimelerinin hızını etkilemez.

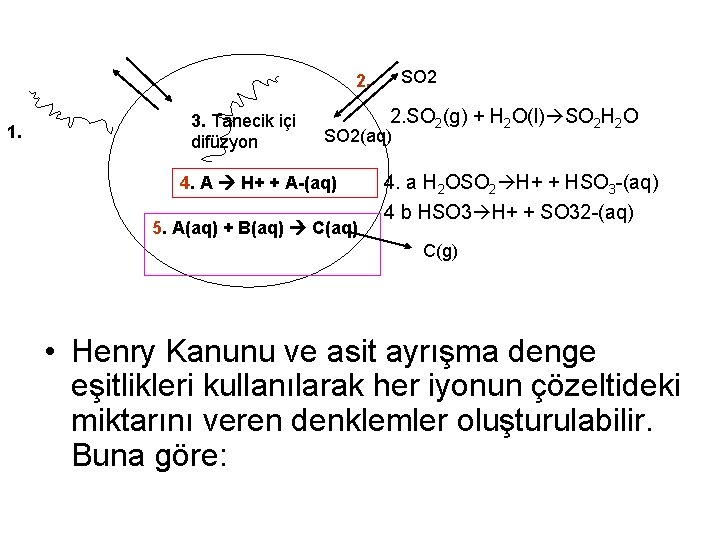
SO 2 2. 1. 3. Tanecik içi difüzyon 2. SO 2(g) + H 2 O(l) SO 2 H 2 O SO 2(aq) 4. A H+ + A-(aq) 5. A(aq) + B(aq) C(aq) 4. a H 2 OSO 2 H+ + HSO 3 -(aq) 4 b HSO 3 H+ + SO 32 -(aq) C(g) • Henry Kanunu ve asit ayrışma denge eşitlikleri kullanılarak her iyonun çözeltideki miktarını veren denklemler oluşturulabilir. Buna göre:

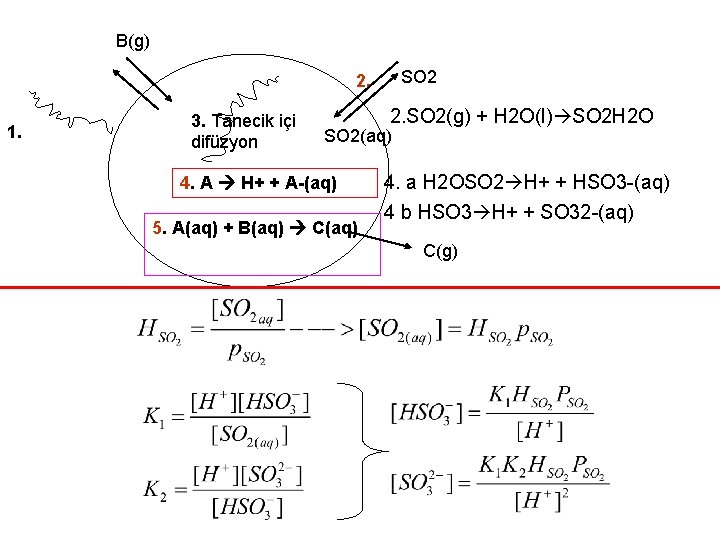
B(g) SO 2 2. 1. 3. Tanecik içi difüzyon 2. SO 2(g) + H 2 O(l) SO 2 H 2 O SO 2(aq) 4. A H+ + A-(aq) 5. A(aq) + B(aq) C(aq) 4. a H 2 OSO 2 H+ + HSO 3 -(aq) 4 b HSO 3 H+ + SO 32 -(aq) C(g)

Sulu Faz Sülfür Kimyası-4 • Bu denge eşitlikleri, elektron nötralite eşitliği(6) ve suyun iyonlaşma eşitliği(7) ile birlikte çözüldüğünde çözeltinin p. H’sı ve buna bağlı olarak türlerin konsantrasyonları bulunur. [H+]=[OH-]+[HSO 3 -]+2[SO 32 -] (6) Kw = [H+][OH-] (7) Tüm bu denklemleri 6’da yerine koyarsak: 0=[H+]3+(Kw+HSO 2+K 1 p. SO 2)[H+]-2 HSO 2 K 1 K 2 PSO 2 (8) Sıcaklık ve SO 2(g)’in kısmi basıncı bilinirse, p. H ve onar bağlı olarak iyon konsantrasyonları bulunur.
![Sulu Faz Sülfür Kimyası4 0H3KwHSO 2K 1 p SO 2H2 HSO 2 K 1 Sulu Faz Sülfür Kimyası-4 0=[H+]3+(Kw+HSO 2+K 1 p. SO 2)[H+]-2 HSO 2 K 1](https://slidetodoc.com/presentation_image_h/ecee8647148fd9ebc1abd78a3c1e7e6b/image-22.jpg)
Sulu Faz Sülfür Kimyası-4 0=[H+]3+(Kw+HSO 2+K 1 p. SO 2)[H+]-2 HSO 2 K 1 K 2 PSO 2 (8) p. SO 2 = 1 ppb ise p. H = 5. 4 p. SO 2 = 1 ppt ise p. H = 6. 7

Sulu Faz Sülfür Kimyası -4 • (SO 2, HSO 3 -, SO 32 -) dengeleri çok hızlı kurulduğundan, oksidasyon nosu 4 olan bu türler S(IV) olarak gösterilir. S(IV) = SO 2(aq)+HSO 3 - + SO 32 Normal atmosferik şartlarda (p. H 2 -6 arası HSO 3 - iyonu olarak bulunur) p. H toplam çözünen S(IV) miktarını etkiler. p. H arttıkça S(IV) miktarı da artar.

Tanecik İçinde Kimyasal Tepkime-5 • S(IV) türleri sulu fazda ayrışma gösterdikleri gibi, tanecik içindeki diğer oksidantlarla kimyasal tepkimelerle yükseltgenerek S(VI) (+6 oksidasyon nolu bileşikler) haline gelirler. S(IV) S(VI) Bu yükseltgenme için O 2(aq), O 3(aq) ve H 2 O 2(aq) düşünülebilir.

O 2(aq) • O 2(aq) H 298 = 1. 3 x 10 -3 • HSO 3 -+1/2 O 2 H+ + SO 42 • Ancak O 2 ile S(IV)’den S(VI)’ya yükseltgenme, başlarda önemli olacağı düşünülse de fazla etkili olmadığı görülmüştür.

O 2(aq) • S(IV)’ün O 2 ile tepkimesi yavaş olmasına karşın çeşitli metallerin (Demir ve manganez gibi) varlığıyla tepkime hızlanır. Mn 2+, Fe 3+ S(IV) + ½ O 2 --- S(VI) • Ayrıca çözünmüş HNO 2 ve karbon da sülfat oluşumunda kataliz görevi görürler.

O 3(aq) • SO 32 -+O 3(aq) SO 42 -(aq) + O 2(aq) (1) ya da • HSO 3 - + O 3 H+ + SO 42 - + O 2 (2) 1’e göre S(VI)’nın oluşum hızını yazarsak: (3 a) (4) (5)

O 3(aq) • HSO 3 - + O 3 H+ + SO 42 - + O 2 (2) 2’ye göre S(VI)’nın oluşum hızını yazarsak: (3 b) (4) (6)

O 3(aq) 3 a ve 3 b’de yazıldığı şekilde sistem p. H’ya bağlı görülmez. Ancak p. H’nın S(IV) üzerindeki etkisi göze alındığında 5 ve 6 nolu eşitliklerde görüldüğü gibi önemi belli olur. SO 32 - okside oldukça gaz fazdan çözünen SO 2 onun yerini alır. Tepkime ilerledikçe p. H ve oksidasyon tepkimesinin hızı azalır. Yani tepkime kendini sınırlar. Hız ihmal edilebilir hale gelene kadar sadece çok küçük bir miktar sülfat oluşabilir.

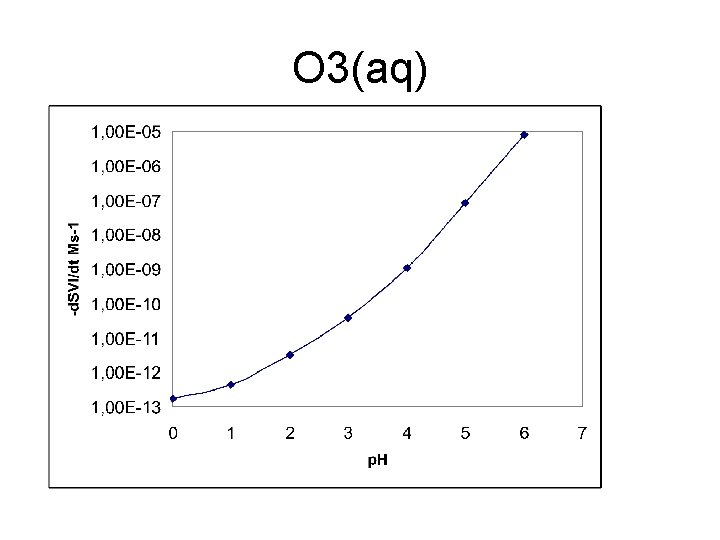
O 3(aq) Deneysel çalışmalar ve onlara uydurulan eğilim çizgilerine göre S(IV)’ün ozon tarafından S(VI)’ya çevrilmesi seyreltik bir çözelti için aşağıdaki ifadeyle verilir.

O 3(aq)

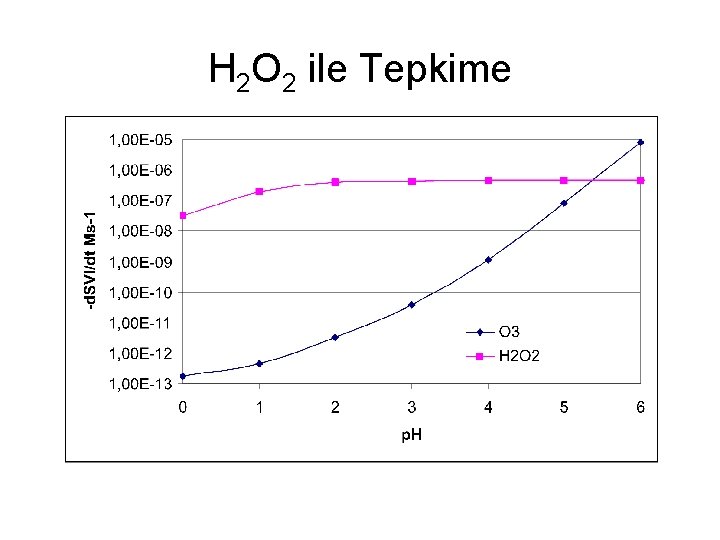
Sülfürlü Bileşikler, H 2 O 2 ile tepkime • Hidrojen peroksit ise p. H’dan bağımsız olarak S(IV) yükseltgemesini gerçekleştirir. Ortamda H 2 SO 4’un oluşumuyla asitlik artsa bile tepkime yavaşlamaz. • HSO 3 - + H 2 O 2(aq) + H+ SO 42 - +H 2 O+2 H+ p. H’dan bağımsız p. H düşük olduğu değerlerde bile S(IV) oksidasyonu devam eder.

H 2 O 2 ile Tepkime • Hoffmann ve Calvert (1985) H 2 O 2’nin S(IV) ile tepkimesi için aşağıdaki hız ifadesini deneysel olarak bulmuşlardır: p. H>2 için 1 + K[H] =1 ve [H+][HSO 3 -] = HSO 3 K 1 PSO 2 olduğundan oluşum hızının p. H’dan bağımsız olduğu söylenebilir.

H 2 O 2 ile Tepkime

OH ile Tepkime • Aşağıdaki tepkimelerin OH ile sülfürlü bileşiklerin sulu faz kimyasında etkili olduğu düşünülmektedir: • HSO 3 - + OH SO 3 - (persulfit anyon) + H 2 O • SO 32 - + OH SO 3 - + OH • Hızlı SO 3 - + O 2 SO 5 - (peroxymonosulfat kökü) • Yavaş SO 5 - + HSO 3 HSO 5 - + SO 3 • Veya • yavaş SO 5 - + SO 32 - HSO 5 - + SO 3 - +OH Ancak ana kaybolma tepkimesi kendisiyle olan tepkime: • SO 5 - + SO 5 - 2 SO 4 - + O 2 • SO 5 - + SO 5 - S 2 O 82 - + O 2 • SO 4 - + HSO 3 - + H+ + SO 42 -

S(IV) S(VI) Notlar • Ozon, H 2 O 2 ve metallerin katalistliğindeki S(IV) oksidasyonunun yanı sıra OH, organik peroksitler ve nitrojen oksitler de sulu fazda S(IV) S(VI) oksidasyonunu gerçekleştirirler. • p. H’dan neredeyse bağımsız olan H 2 O 2 tepkimesi en hızlı S(VI) oluşumuna neden olur.

S(IV) S(VI) Notlar • Sülfat oluşum hızları, sıvı fazdaki birim hacim başınadır. Gaz fazdaki SO 2’nin ne kadar hızla tüketildiğini bulmak için toplam sıvı su içeriği ile çarpmak gerekir. Bu nedenle özellikle bulutlardaki su içeriği düşünüldüğünde sülfat oluşumunda bulutların önemi daha iyi anlaşılır. • NOT. S(IV) yükseltgenmelerindeki tepkimeye giren bileşikler her zaman atmosferden gaz olarak sağlanmaz. Örneğin HO 2 radikal gaz fazda üretilip sonrasında tanecik içinde H 2 O 2’ye çevrilir. HO 2(aq) + Cu 2+ H+(aq) + O 2 + Cu+(aq) HO 2(aq) + Cu+ (aq) HO 2 -(aq) + CU 2+(aq) HO 2 - (aq) + H+(aq) H 2 O 2

Sulu Faz Nitrit ve Nitrat Kimyası • Nitrik asitin sanayide oluşum mekanizması (su içinde NO 2(aq) + NO 2(aq) NO 2 - + NO 3 - +2 H+ gibi) atmosfer şartlarında çok yavaş olduğu için nitrik asit oluşumu nitrojen radikallerinin yer aldığı tepkimelerle gerçekleşir. • NO 3 radikali (doğrudan kendisi veya N 2 O 5 olarak) geceleri sulu faz kimyada yer alan en tepkin azotlu bileşiktir

Sulu Faz Nitrit ve Nitrat Kimyası NO 3 ve N 2 O 5 suda kolayca çözünürler ve NO 3 için Henry sabiti 2, 1 E 5 M/atm ve N 2 O 5’in de dengede tamamen sulu faza geçtiği varsayılır. • N 2 O 5(aq) + H 2 O 2 H+ + 2 NO 3 • NO 3 +Cl- NO 3 - + Cl(aq) Klorid iyonunun az olduğu durumlarda ise NO 3 HSO 3 - ile tepkimeye girip SO 3 radikalini oluşturur.

Sulu-faz Kimya Modelleri • En basit modeller belli bir su içeriği (g/m 3 bulut veya sis suyu) varsayıp suda çözünebilen bileşiklerin gaz ve sıvı faz arasında termodinamik bir dengeye sahip olduğunu öngörürler. (Henry Kanunu) • Daha detaylı modellerde ise termodinamik denge yerine taneciğin sürekli dış ortamla kütle transferi halinde olduğu düşünülerek iki faz arasındaki madde geçişi modellenir. • En karmaşık modellerde bulut veya sis damlalarının da zamanla değişimi dikkate alınır. (Boyut dağılımı dikkate alınır)

Çoklu Faz Kimya • Sulu Faz Kimyanın Dinamiğinin Modellemesi – Sulu faz kimya hızının hesaplanmasında hem damlacığın içine söz konusu türün alınması hem de tepkime hızı göz önüne alınır. Genelde sulu faza geçme ve ayrışma dengesinin kimyasal tepkimenin süresine oranla çok daha kısa sürede kurulduğu varsayılır. (Bu varsayım her zaman geçerli olmaz. Örneğin çapları daha büyük olan bulut damlacığı için gaz fazdaki difüzyon hız limitleyen adım olabilirken, suda çözünemeyen türler için kütle transferi asıl sorun olabilir. )

Sulu Faz Kimyanın Dinamiğinin Modellemesi • Eğer gaz fazın damlacıkla dengede olduğunu varsayarsak gaz fazı iki şekilde ele alabiliriz. • Açık Sistem Yaklaşımı: Gaz fazdaki türlerin kısmi basınçları sabit kabul edilir. Diğer bir deyişle, gaz türü damla tarafından tüketildikçe aynı hızda yeni gelen bir hava kitlesiyle veya o gazı üreten kimyasal bir tepkime ile sürekli yenilenmekte • Kapalı Sistem Yaklaşımı: damlacığın bulunduğu hacim içersinde başta belli miktarda gaz var. Bu gaz sıvı faza geçtikçe ortamdaki gaz miktarı azalmakta. Gerçekte her iki yaklaşımda gerçek bir bulutu modellerken en uç sınırlayıcı vakaya karşılık gelir. Atmosferde mutlaka karışma olacağından kapalı sistem yaklaşımı pek gerçekçi olmazken, açık sistem de tepkime ve damlacık içine alınan gazın miktarını olduğundan fazla tahmin edecektir.

Açık ve Kapalı Sistem Örneği • Başlangıçta saf bir su damlası (p. H = 7), L = 10 -6 m 3 su/m 3 hava t=0 zamanında aşağıdaki başlangıç gaz konsantrasyonlarına sahip bir havaya maruz kalıyor. Gaz t = 0 (ppb) Dengede (ppb) SO 2 5 3. 03 NH 3 5 1. 87 H 2 O 2 1 0. 465 O 3 5 5 HNO 3 1 10 -8

• p. H ve konsantrasyon değerleri Henry kanunu, ayrışma dengesi, elektronötralite ve kütle dengesi eşitliklerin çözerek bulunur. • 1. Türlerin sulu fazdaki başlangıç konsantrasyonlarını Henry Kanunu ve Kütle Eşitliği denklemlerinden bulabiliriz. – O 3 için yazarsak: [O 3]T = 5 ppb = [O 3]aq + [O 3]g HO 3 = [O 3]aq [O 3]g + [O 3]aq
![Elektronötralite Eşitliği H NH 4 OH HO 2 • Elektronötralite Eşitliği: [H+] + [NH 4+] = [OH-] + [HO 2 -]](https://slidetodoc.com/presentation_image_h/ecee8647148fd9ebc1abd78a3c1e7e6b/image-45.jpg)
• Elektronötralite Eşitliği: [H+] + [NH 4+] = [OH-] + [HO 2 -] +[HSO 3 -] + 2[SO 3 -2] + [NO 3 -] Yüksüz olaraksa çözeltide SO 2(aq), NH 3(aq), H 2 O 2(aq), O 3(aq), HNO 3(aq), bulunur. Kimyasal tepkimeler oluşmaya başlayınca S(IV) türleri S(VI)’ya dönüşecektir. Bir zaman adımı alıp ilk önce SIV türlerin dmalacıktaki konsantrasyonları [S(IV)] = H*SO 2 p. SO 2 ile etkili Henry Kanunu sabiti biliniyorsa hesaplanabilir. Ancak H* p. H’ya bağlı olarak değiştiğinden her adımda p. H’da değişecektir. Ayrıca diğer türler NH 3 gibi damlacık içine girerek bazı asitleri nötralize ederek p. H’nın değişmesine neden olurlar.

• Bu durumda her bir zaman adımında elektronötralite Eşitliği yeniden yazılacaktır. S(VI) oluştuğunda EN eşitliği: [H+] + [NH 4+] = [OH-] + [HO 2 -] +[HSO 3 -] + 2[SO 3 -2] + [NO 3 -] +2[SO 4 -2] + [HSO 4 -] Gene aynı şekilde eşitlik denge sabitleri, kısmi basınçlar ve [H+] cinsinden yazılıp, p. H belirlenip sonra da tüm iyonların konsantrasyonları belirlenir. Eğer sistem kapalı sistemse, Pi değeri zamanla sürekli değişeceğinden eşitlikte bu göz önüne alınmalıdır. Bu şekilde kimyasal hız eşitlikleri integre edilip anlık denge hali varsayımıyla zamanla konsantrasyonların nasıl değiştiği hesaplanır.

Sayfa 385 -391

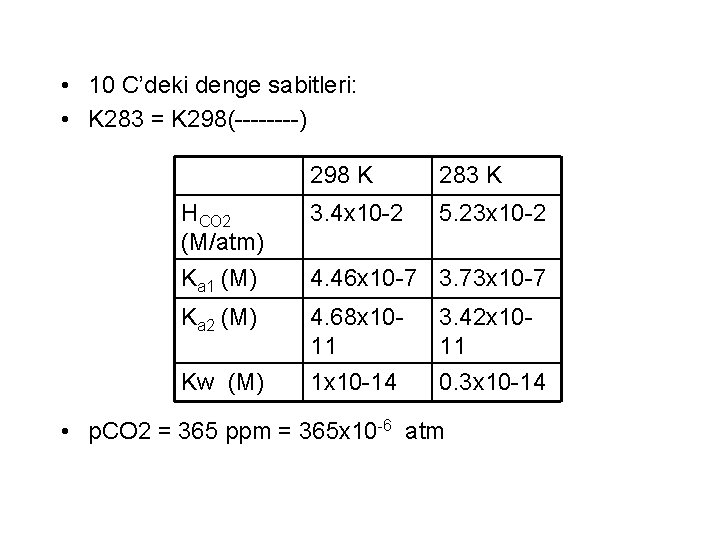
Örnek • 10 C’de 365 ppm CO 2 konsantrasyonu ile dengede olan bir bulut damlasının p. H’sını hesaplayın

• Henry Kanunu CO 2 (g) –CO 2 (aq) Ayrışma Eşitlikleri CO 2 (aq)—HCO 3 - + H+ HCO 3—CO 32 -+H+ Su Dengesi Kw = [H+] [OH-] EN: [H+] = [OH-] +[HCO 3 -]+2[CO 32 -]

• 10 C’deki denge sabitleri: • K 283 = K 298(----) 298 K 283 K HCO 2 (M/atm) 3. 4 x 10 -2 5. 23 x 10 -2 Ka 1 (M) 4. 46 x 10 -7 3. 73 x 10 -7 Ka 2 (M) 4. 68 x 1011 1 x 10 -14 Kw (M) 3. 42 x 1011 0. 3 x 10 -14 • p. CO 2 = 365 ppm = 365 x 10 -6 atm


ÖRNEK 2 • Aşağıdaki iki durumda her bir oksidasyon mekanizması için H 2 SO 4’ün oluşma hızını hesaplayın A (kirli bulut) PSO 2, ppb T, K L g/m 3 p. H p. O 3, ppb [H 2 O 2], M [Mn 2+], M [Fe 3+], M 50 298 0. 1 3. 5 -4. 5 100 4. 7 x 10 -5 10 -6 B (karasal arkaplan) 5 298 1 4. 5 -6. 0 40 5. 9 x 10 -6 2 x 10 -9 3. 3 x 10 -9
![SO 2 H 2 O HSO 2 PSO 2 1 • [SO 2. H 2 O] = HSO 2. PSO 2 ----------(1) •](https://slidetodoc.com/presentation_image_h/ecee8647148fd9ebc1abd78a3c1e7e6b/image-53.jpg)
• [SO 2. H 2 O] = HSO 2. PSO 2 ----------(1) • [HSO 3 -] = Ka 1 HSO 2. PSO 2/[H+]-------(2) • [SO 3”] = Ka 2 Ka 1 HSO 2. PSO 2/[H+]2 -----(3)
 Atmosfer berasal dari bahasa yunani yang berarti
Atmosfer berasal dari bahasa yunani yang berarti Ainda bem que agora encontrei
Ainda bem que agora encontrei Bitkinin yaşam döngüsü
Bitkinin yaşam döngüsü Sulu boya teknikleri
Sulu boya teknikleri Crackers captain underpants
Crackers captain underpants Sulu çözeltilerde denge
Sulu çözeltilerde denge Hoje faz uma semana
Hoje faz uma semana Sulu yol verici
Sulu yol verici Suda çözündüğünde oh- iyonu veren maddelere ne denir
Suda çözündüğünde oh- iyonu veren maddelere ne denir Ozonsfer
Ozonsfer Atmosfer berasal dari
Atmosfer berasal dari Hujan frontal
Hujan frontal Sirkulasi musiman
Sirkulasi musiman Ilmu yang mempelajari keadaan cuaca
Ilmu yang mempelajari keadaan cuaca Atmosfer nedir
Atmosfer nedir Stratofer
Stratofer Segala macam bentuk
Segala macam bentuk Dngler
Dngler Rumus temperatur efektif bintang
Rumus temperatur efektif bintang Rumus teori braak
Rumus teori braak Ilmu yang mempelajari bumi secara keseluruhan adalah.... *
Ilmu yang mempelajari bumi secara keseluruhan adalah.... * Restoran atmosfer bileşenleri
Restoran atmosfer bileşenleri Atmosfer bileşimi
Atmosfer bileşimi Atmosfer berasal dari kata
Atmosfer berasal dari kata Peta konsep struktur bumi
Peta konsep struktur bumi Komposisi atmosfer
Komposisi atmosfer Ksenobiyotik örnekleri
Ksenobiyotik örnekleri Diferença entre sonho e projeto
Diferença entre sonho e projeto Obrigada pela atençao
Obrigada pela atençao Jovem desperta faz te pronto numero
Jovem desperta faz te pronto numero Suyun faz diyagramı
Suyun faz diyagramı Pornografia faz mal?
Pornografia faz mal? Ovaryumdan salınan kadın cinsiyet hormonu
Ovaryumdan salınan kadın cinsiyet hormonu Negatif akut faz reaktanları
Negatif akut faz reaktanları A charge faz referência
A charge faz referência Nutrologo o que faz
Nutrologo o que faz Atitude é uma pequena coisa que faz uma grande diferença
Atitude é uma pequena coisa que faz uma grande diferença Peritektik dönüşüm
Peritektik dönüşüm Efekt krioskopowy
Efekt krioskopowy Faz 1 reaksiyonları
Faz 1 reaksiyonları Işaretli katı faz yöntemleri
Işaretli katı faz yöntemleri O kakashi se fazer teatro de objetos
O kakashi se fazer teatro de objetos Gastrointestinal sistem hormonları
Gastrointestinal sistem hormonları Cinco pedreiros fazem um muro em 10 horas
Cinco pedreiros fazem um muro em 10 horas Fe c diyagramı
Fe c diyagramı Ven espiritu santo y llena los corazones
Ven espiritu santo y llena los corazones Pedagogia social
Pedagogia social Negatif akut faz reaktanları
Negatif akut faz reaktanları Como colocar o elefante na geladeira
Como colocar o elefante na geladeira Pra que saber meu nome saber do meu passado gian e giovani
Pra que saber meu nome saber do meu passado gian e giovani Ministerio zoe aquieta minha alma
Ministerio zoe aquieta minha alma Suyun faz diyagramı
Suyun faz diyagramı Negatif akut faz reaktanları
Negatif akut faz reaktanları Um exemplo de texto narrativo
Um exemplo de texto narrativo