STRUKTUR SENYAWA KARBON Penggambaran 3 D Penggambaran 2
STRUKTUR SENYAWA KARBON Penggambaran 3 D Penggambaran 2 D

Senyawa Karbon Adalah senyawa yang molekulnya mengandung atom -atom karbon dan atom-atom unsur lain seperti hidrogen, oksigen, nitrogen, belerang, dan halogen. Reaksi Senyawa Karbon - Reaksi Subtitusi -- Reaksi Adisi Eliminasi

Reaksi Subtitusi Adalah reaksi penggantian suatu atom atau gugus atom oleh atom lain yang terdapat dalam suatu molekul. Contoh Reaksi Subtitusi : Pada Pembuatan alkil Halida dari alkana, atom H diganti oleh atom Halogen CH 3 CH 2 CH 3 + Cl 2 CH 3 CH 2 Cl + HCl

Reaksi Adisi Adalah reaksi yang terjadi karena pengubahan ikatan tak jenuh menjadi jenuh, atau ikatan rangkap menjadi ikatan tunggal. Contoh Reaksi Subtitusi : Adisi hidrogen terhadap alkuna H 3 C – C CH + H 2 H 3 C – CH = CH 2 + H 2 H 3 C – CH 2 – CH 3

Reaksi Eliminasi adalah penyingkiran atau penghilangan beberapa atom yang terjadi pada suatu senyawa. Contoh Reaksi Eliminasi : Eliminasi Hidrogen dari alkana (dehidrogenasi)

ALKIL HALIDA : Tinjauan reaksi subtitusi nukleofilik Kimia Organik Universitas Islam Negri Sunan Gunung Djati Bandung
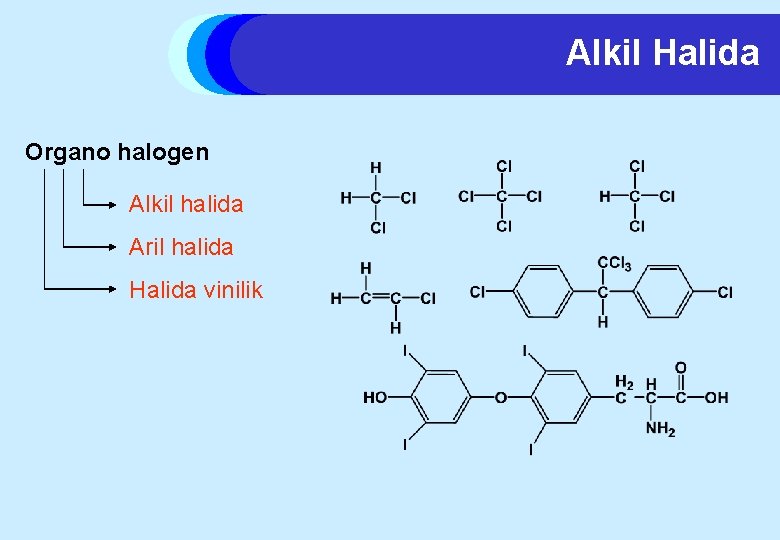
Alkil Halida Organo halogen Alkil halida Aril halida Halida vinilik

Pembahasan 1. Pembuatan alkil halida : reaksi radikal bebas 2. Reaksi alkil halida : Reaksi subtitusi : SN 1 dan SN 2 Reaksi eliminasi : E 1 dan E 2
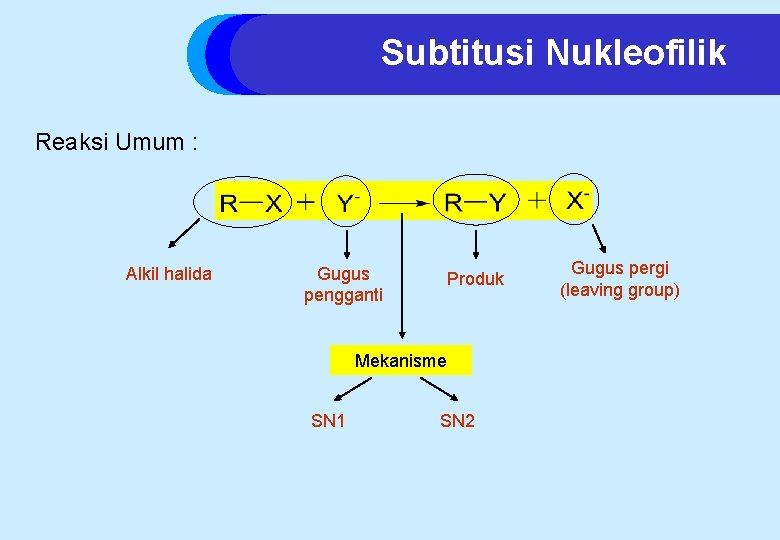
Subtitusi Nukleofilik Reaksi Umum : Alkil halida Gugus pengganti Produk Mekanisme SN 1 SN 2 Gugus pergi (leaving group)
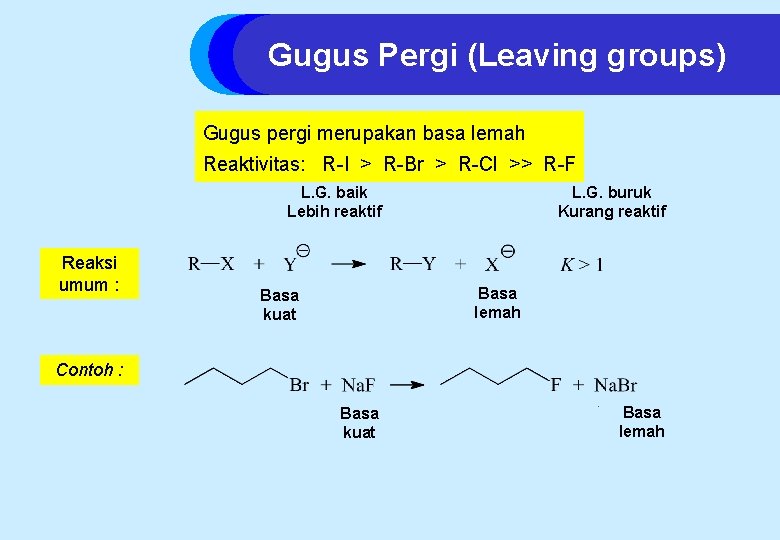
Gugus Pergi (Leaving groups) Gugus pergi merupakan basa lemah Reaktivitas: R-I > R-Br > R-Cl >> R-F L. G. buruk Kurang reaktif L. G. baik Lebih reaktif Reaksi umum : Basa lemah Basa kuat Contoh : Basa kuat Basa lemah
![Mekanisme SN Rumus umum laju reaksi : V = k 1[RX] + k 2[RX][Y–] Mekanisme SN Rumus umum laju reaksi : V = k 1[RX] + k 2[RX][Y–]](http://slidetodoc.com/presentation_image/4a65c634b66dfb8fdfd5e9b63bbfceb5/image-11.jpg)
Mekanisme SN Rumus umum laju reaksi : V = k 1[RX] + k 2[RX][Y–] k 1 meningkat RX = CH 3 X 1º 2º 3º k 2 meningkat k 1 ~ 0 k 2 ~ 0 V = k 2[RX][Y–] (bimolekular) V = k 1[RX] (unimolekular) SN 2 SN 1
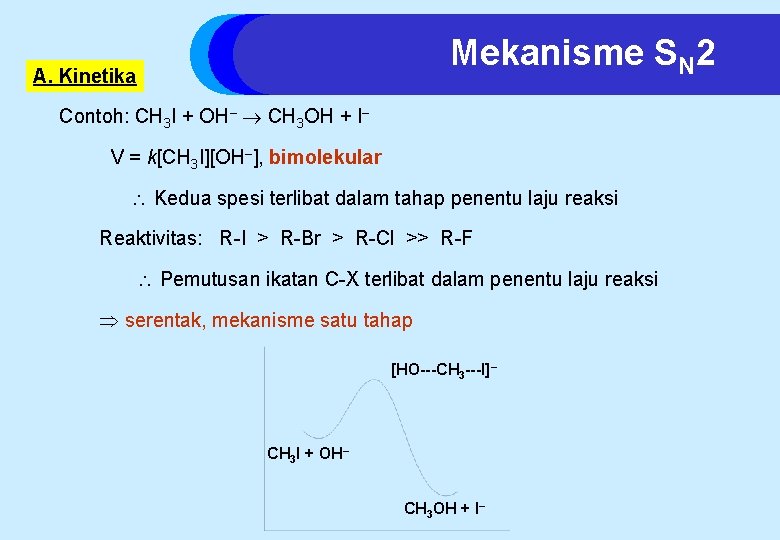
Mekanisme SN 2 A. Kinetika Contoh: CH 3 I + OH– CH 3 OH + I– V = k[CH 3 I][OH–], bimolekular Kedua spesi terlibat dalam tahap penentu laju reaksi Reaktivitas: R-I > R-Br > R-Cl >> R-F Pemutusan ikatan C-X terlibat dalam penentu laju reaksi serentak, mekanisme satu tahap [HO---CH 3 ---I]– CH 3 I + OH– CH 3 OH + I–
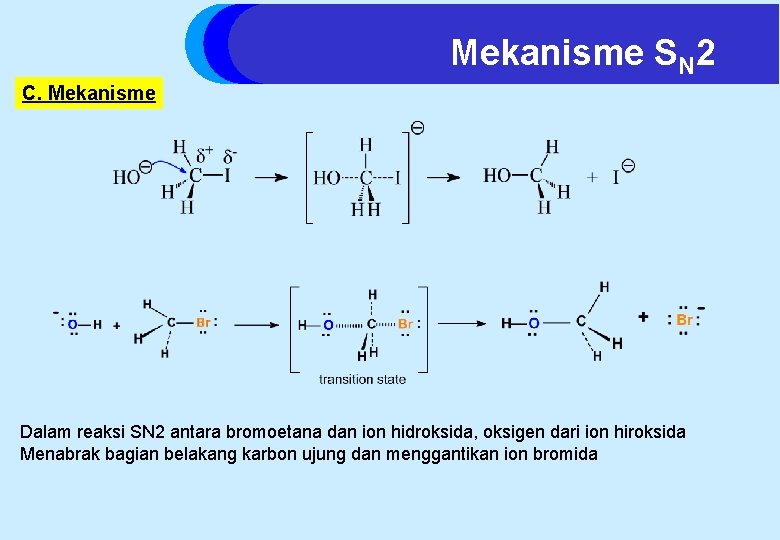
Mekanisme SN 2 C. Mekanisme Dalam reaksi SN 2 antara bromoetana dan ion hidroksida, oksigen dari ion hiroksida Menabrak bagian belakang karbon ujung dan menggantikan ion bromida
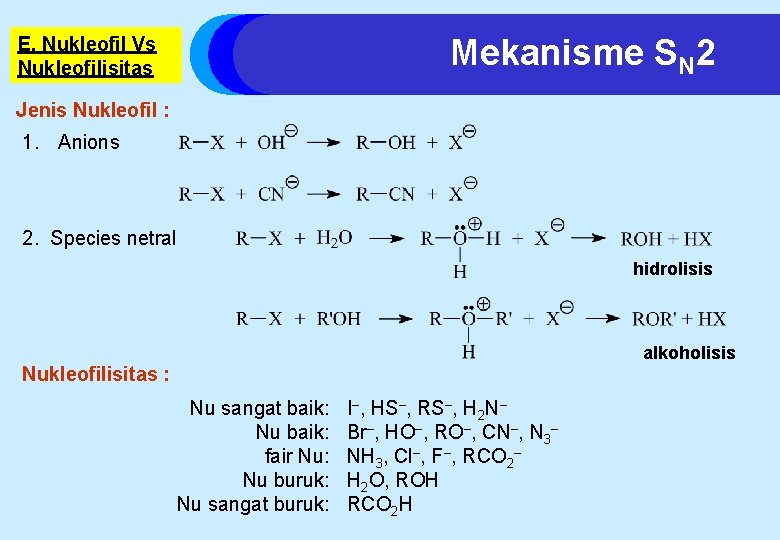
Mekanisme SN 2 E. Nukleofil Vs Nukleofilisitas Jenis Nukleofil : 1. Anions 2. Species netral hidrolisis alkoholisis Nukleofilisitas : Nu sangat baik: Nu baik: fair Nu: Nu buruk: Nu sangat buruk: I–, HS–, RS–, H 2 N– Br–, HO–, RO–, CN–, N 3– NH 3, Cl–, F–, RCO 2– H 2 O, ROH RCO 2 H
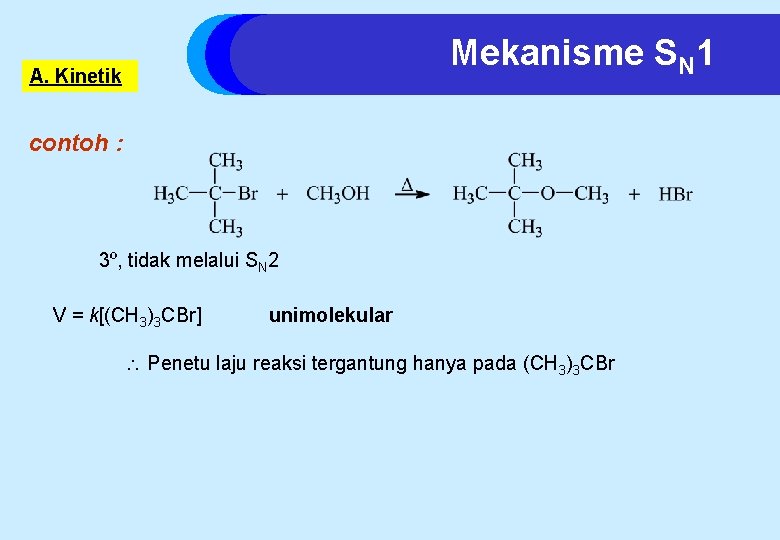
Mekanisme SN 1 A. Kinetik contoh : 3º, tidak melalui SN 2 V = k[(CH 3)3 CBr] unimolekular Penetu laju reaksi tergantung hanya pada (CH 3)3 CBr
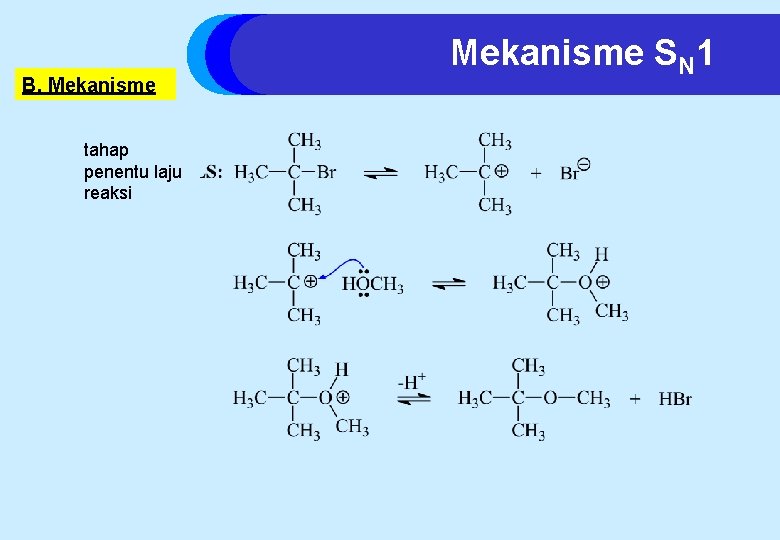
B. Mekanisme tahap penentu laju reaksi Mekanisme SN 1
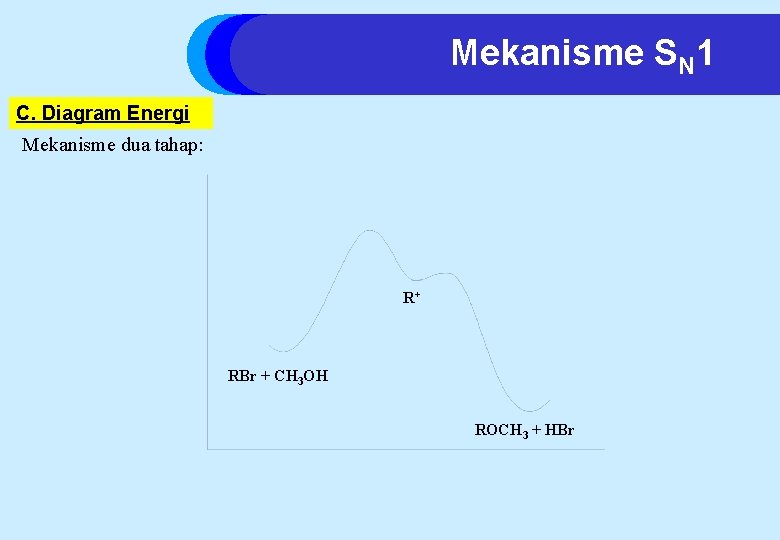
Mekanisme SN 1 C. Diagram Energi Mekanisme dua tahap: R+ RBr + CH 3 OH ROCH 3 + HBr
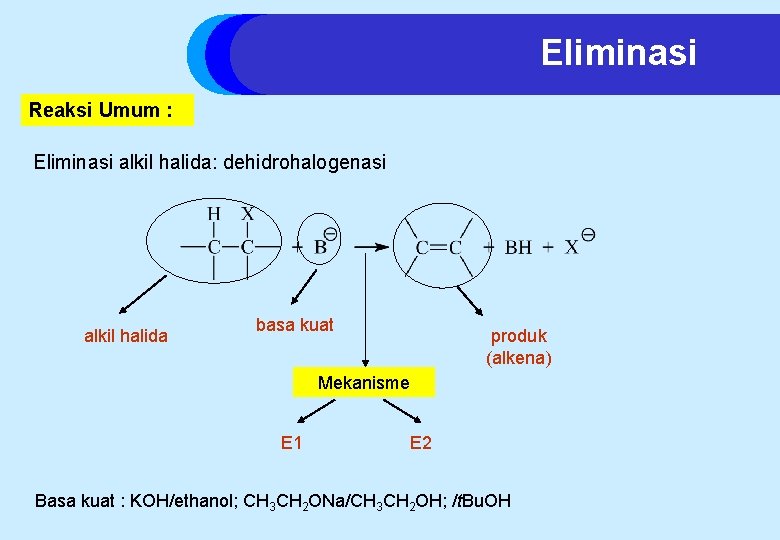
Eliminasi Reaksi Umum : Eliminasi alkil halida: dehidrohalogenasi alkil halida basa kuat produk (alkena) Mekanisme E 1 E 2 Basa kuat : KOH/ethanol; CH 3 CH 2 ONa/CH 3 CH 2 OH; /t. Bu. OH
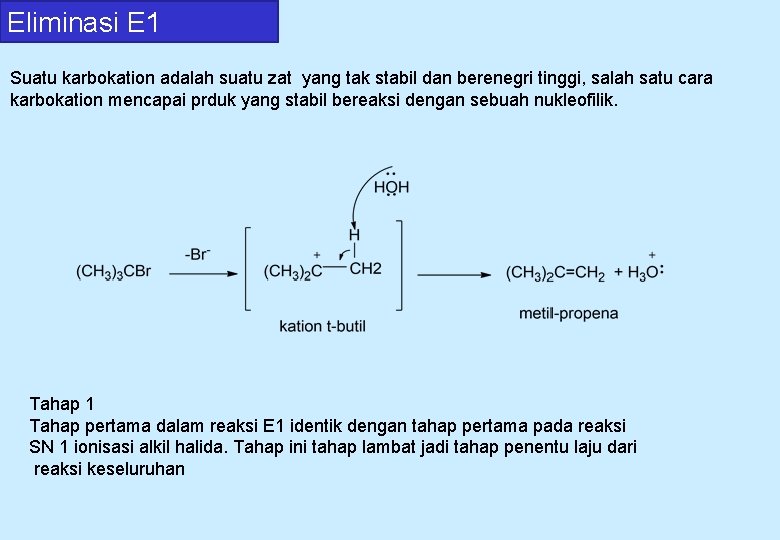
Eliminasi E 1 Suatu karbokation adalah suatu zat yang tak stabil dan berenegri tinggi, salah satu cara karbokation mencapai prduk yang stabil bereaksi dengan sebuah nukleofilik. Tahap 1 Tahap pertama dalam reaksi E 1 identik dengan tahap pertama pada reaksi SN 1 ionisasi alkil halida. Tahap ini tahap lambat jadi tahap penentu laju dari reaksi keseluruhan
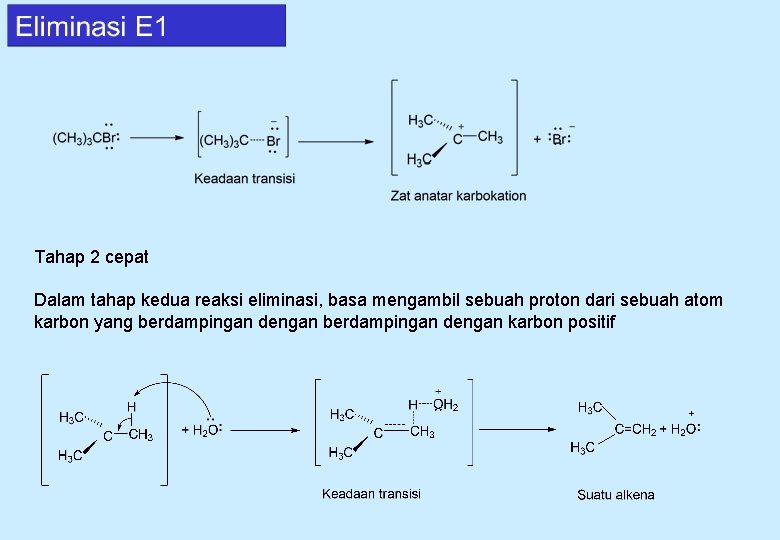
Tahap 2 cepat Dalam tahap kedua reaksi eliminasi, basa mengambil sebuah proton dari sebuah atom karbon yang berdampingan dengan karbon positif
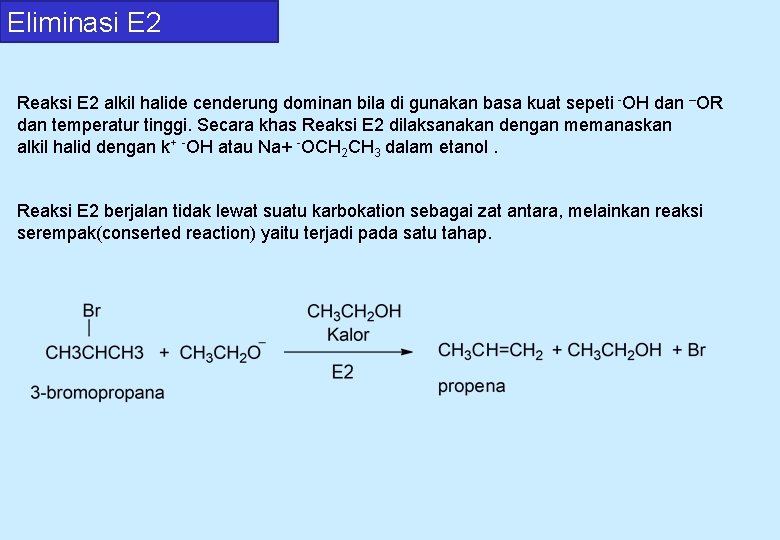
Eliminasi E 2 Reaksi E 2 alkil halide cenderung dominan bila di gunakan basa kuat sepeti -OH dan –OR dan temperatur tinggi. Secara khas Reaksi E 2 dilaksanakan dengan memanaskan alkil halid dengan k+ -OH atau Na+ -OCH 2 CH 3 dalam etanol. Reaksi E 2 berjalan tidak lewat suatu karbokation sebagai zat antara, melainkan reaksi serempak(conserted reaction) yaitu terjadi pada satu tahap.
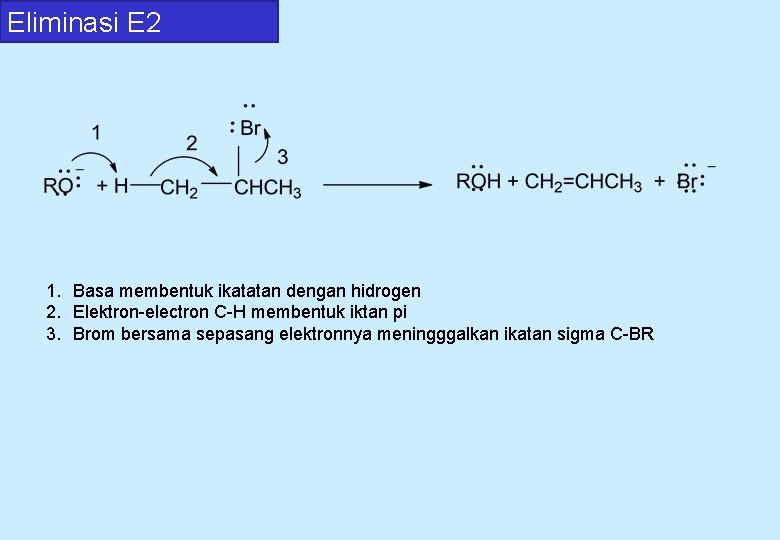
Eliminasi E 2 1. Basa membentuk ikatatan dengan hidrogen 2. Elektron-electron C-H membentuk iktan pi 3. Brom bersama sepasang elektronnya meningggalkan ikatan sigma C-BR

Mekanisme E 2 : eliminasi bimolekuler • Reaksi adalah bimolekul, V tergantung pada konsentrasi RX dan B– V = k[RX][B–] Tahap penentu laju reaksi melibatkan konsentrasi B– • reactivity: RI > RBr > RCl > RF kekuatan ikatan R—X meningkat Tahap penentu laju reaksi melibatkan pemutusan ikatan R—X (Reaksi tidak tergantung pada jenis RX apakah 1º, 2º, atau 3º)
- Slides: 23