Ozbekiston Respublikasi Oliy va Orta Maxsus Talim Vazirligi

O’zbekiston Respublikasi Oliy va O’rta Maxsus Ta’lim Vazirligi Guliston Davlat Universiteti “Umumiy kimyo va kimyoviy texnologiya’ kafedirasi’ Organik kimyo fanidan O’qituvchi: Yettiboyeva L. A.

MAVZU: “Organik kimyo fani va uning ahamiyati“ mavzusi yuzasidan tayyorlagan

ORGANIK KIMYОNING NAZARIY ASOSLARI Organik kimyo- uglerod birikmalari kimyosidir. Organik kimyo- uglevodorodlar va ularning hosilalari kimyosi deb ta‘rif berish ham mumkin. Organik kimyo mustaqil fan sifatida X 1 X asr boshlarida ajralib chiqdi. Bunga asosiy sabablar: 1. Uglerod birikmalari, ya‘ni organik birikmalar sonini ko’pligi (7 milliondan ortiq) Vaholanki, uglerod elementidan tashari 107 element birikmalari 1 millionga yaqin. Hozirda bir yilda 200 mingdan ortiq yangi organik modda sintez qilinmoqda. Organik birikmalarning ko’p bo’lishligiga sababni, uglerod atomi o’zaro bir-biri bilan birikib uzun zanjir hosil qilishi, izomeriya xodisasi, hamda tirik tabiat bilan bog’liqligi bilan tushuntiriladi.

ORGANIK KIMYO FANI VA UNING AHAMIYATI Organik moddalar kishilarga juda qadimdan ma‘lum bo’lgan. Ular qadim zamondan beri shakar va moy olishni, yog’larni qaynatib sovun olishni bilganlar. Hindiston va Misrda organik kimyo fani fan sifatida shakllanmagan bo’lsada, kishilar organik bo’yoqlardan foydalanib, buyash san‘atini rivojlantirgan edi. Sof holdagi organik moddalar dastlab 900 yillarda arab alkimyogarlari tomonidan hosil qilingan edi. Umuman moddalar to’g’risidagi tushunchalar dastlab Aristotelning filosofik qarashlarida ma‘lum bo’lgan edi. Ya‘ni hamma moddalar 4 ta «element» dan iborat – yer, suv, havo va olov. Kimyoviy bilimlar 16 asrdan boshlab rivojlana boshlandi. O’sha paytda nazariy asosda bo’lmasada lekin moddalar to’g’risida juda ko’p tajribalar to’plangan edi. Amma moddalar hali organik va anorganik moddalarga bo’linmagan edi. XIX asrda «Flogiston» nazariyasi davrida asta-sekin organik va anorganik moddalarni sinflarga bo’linishi boshlandi.

1807 yilda Shved olimi Ya. Bertselius tirik organizmdan olingan moddalarni organik moddalar deb atashni taklif qildi va tez orada bunday moddalardan sun‘iy yo’l bilan yangi organik moddalar hosil qilindi. Shunday qilib, organik kimyo o’simlik va hayvonlardan olinadigan moddalar kimyosi sifatida shakllana boshladi. 1824 yilda Bertseliusning shogirdi nemis kimyogari F. Vyoler laboratoriya sharoitida ditsiandan o’simlik organizmida uchraydigan oksalat kislotani, 1828 yilda esa oddiy organik tuz – ammoniy tsianatdan hayvon organizmida hosil bo’ladigan mochevina (karbamid) ni sintez qildi. Dastlab kaliy tsianidni oksidlab kaliy tsianat hosil qilinadi. KCN + [O] KNCO

Bu modda ammoniy sulfat ta‘sirida parchalanib, ammoniy tsianat NH 4 NCO ni hosil qiladi. NH 4 NCO esa yuqori harorat ta‘sirida mochevinaga aylanadi. KNCO + (NH 4)2 SO 4 2 NH 4 NCO + (NH 4)2 CO (аммоний цианат) ёки ditsian. 1842 yilda rus olimi N. N. Zininning nitrobenzoldan anilinni olishi. 1845 yilda nemis olimi Kolbening sirka kislotani sintez qilishi. 1861 yili rus olimi A. M. Butlerovning paraformaldegiddan shakarsimon moddani sintez qilib olishi organik kimyo fanining rivojlanishiga katta yo’l ochdi.

Organik kimyo fani uglevodorodlar va ularning hosilalarini o’rganuvchi fandir. Kimyo fani tabiatni o’rganuvchi fanlardan biridir. Tabiat bizga yog’och, tuz, toshko’mir, neft, tabiiy gaz va boshqa xom ashyo materiallarini beradi. Organik kimyo fani biologiya va tibbiyot bilan uzviy bog’liq holda o’rganiladi. O’simliklardan, hayvonlardan va boshqa tabiiy manbalardan olinadigan barcha moddalar kimyosi, biologik faollikka ega bo’lgan modda kimyosi, olingan moddalar farmakologiyasi hamma-hammasi uzviy bog’liqdir. Organik kimyo fani yutuqlariga tayangan holda yuqori sifatli sintetik kauchuklar, plastmassalar, sun‘iy tolalar, organik o’g’itlar, motor yoqilg’ilari, dori-darmon preparatlari, bo’yoqlar va xalq xo’jaligi uchun zarur bo’lgan boshqa mahsulotlar ishlab chiqarilmoqda. Hozirgi kunda organik kimyoning yangi zamonaviy soxalari - tabiiy fiziologik faol moddalar kimyosi, biorganik kimyo, polimer kimyosi, peptid va oqsillar kimyosi jadal rivojlanib bormoqda. Organik kimyoni va uning yangi sohalarini rivojlanishida o’zbek olimlarining hissasi kattadir.

Dunyoga mashhur akademiklar S. Yunusov, O. S. Sodiqovlarning tabiiy birikmalar kimyosi, akademik X. U. Usmonovning polimerlar kimyosi soxasidagi ulkan ilmiy - tadqiqot ishlari ustida to’xtalib o’tish lozim. O’simlik moddalari kimyosi, jumladan alkaloidlar kimyosi bo’yicha S. Yunusov yaratgan maktabning butun dunyo tan olgan. Buning isboti sifatida, dunyoda topilgan alkaloidlarning har uchtadan biri S. Yunusov va uning shogirdlari tomonidan topilganligini aytish mumkin. Organik kimyoning rivojlanishida professorlar A. R. Abdurasulova, A. Abdusamatov, S. R. Rashidova va hokazolarning xizmatlari katta. Respublikamiz ulkan uglevodorodlarning tabiiy manbalariga ega.

Respublikamizda ulkan neftni qayta ishlaydigan zavod (Farg’ona va Oltiariq), hamda gazni qayta ishlaydigan (SHo’rtan va Muborak) zavodlari ishlab turibdi. Ulardan xilma-xil neft va gaz maxsulotlari ishlab chiqarilmoqda. Chirchiq, Farg’ona va Navoiydagi ulkan kimyo kombinatlar haqida ma‘lumotlarni tariflab o’tish mumkin. Organik birikmalarning tuzilish nazariyasi E. Frankland, Sh. F. Jerar, F. Kekule va boshqa olimlar bilan bog’liq. Bu nazariyani xal qilishda ulug’ rus olimi A. M. Butlerovning xizmati katta. U 1861 yilda o’zining kimyoviy tuzilish nazariyasining asosiy qoidalarini bayon qildi. Molekulada atomlar bir-biri bilan valentliklariga muvofiq ma‘lum izchillikda birikadi. Atomlarning bunday bog’lanish tartibi kimyoviy tuzilishi deyiladi.

Moddalarning xossalari molekulaning tarkibi va ularning tuzilishiga bog’liq. Moddalarning tarkibi va molekulyar ogirligi bir hil, lekin tuzilishi, hamda xossalari turlicha bo’lgan moddalar izomerlar deyiladi. Moddalarni xossasiga ko’ra uning tuzilishini aniqlash, modda molekulasining tuzilishi asosida moddalarning xossalarini oldindan aytish mumkin. Modda molekulasidagi atom va atomlar guruhi o’zaro bir-biriga ta‘sir etadi. Kimyoviy reaktsiyada modda molekulasini tashkil etgan barcha atomlar emas balki, ayrim atomlar yoki atomlar guruhi ishtirok etadi. Organik birikmalarda uglerod doimo to’rt valentli bo’lib, o’zaro birikib to’g’ri, tarmoqlangan, xalqasimon zanjirlarni hosil qila ola

D. I. Mendeleevning elementlar davriy sistemasi yangi elementlar borligini oldindan aytishga imkon bergan bo’lsa, Butlerovning kimyoviy tuzilish nazariyasi orqali hali topilmagan moddalar mavjudligi, ularning tuzilishini oldin aytib, sintez usulda olishga imkoniyat yaratildi. Organik kimyoni mukammal egallash uchun birinchi navbatda uning nazariy asoslari organik birikmalarning elektron tabiati, kimyoviy reaktsiyalarni boshqaruvchi qonunlarini o’rganish lozim. Lekin, moddalarning xossalarini o’rganishdan oldin uning tozaligi, sifat va miqdor tarkibi so’ngra tuzilishi aniqlanadi. Organik moddalarning toza holda ajratish va tozalashning usullari: haydash, ekstraktsiya, qayta kristallash, sublimatsiya va zamonaviy xromatografiya usullarini bilish lozim.

Toza organik moddalarni tuzilishini aniqlash uchun, dastlab ularning fizik konstantalari suyuq. t, qayn. t, sindirish ko’rsatgichi, optik solishtirma buruvchanligi, eruvchanligi aniqlanadi. So’ngra, mumtoz, hamda hozirgi zamon spektrial UB, IQ, PMR va massspektroskopiya usullar yordamida tuzilishlari aniqlanadi

KIMYOVIY TUZILISH NAZARIYАSI XIX asrning boshlari minglab organik moddalarning kashf etilishi va sintez qilinishi davri bo’ldi. Ammo moddalardagi kimyoviy o’zgarishlarni va qonuniyatlarni asoslab beruvchi nazariyaning yo’qligi organik kimyoning yanada rivojlanishiga to’sqinlik qildi. Nemis kimyogari Yu. Libix bodom mag’zidan benzoy aldegid O С 6 Н 5 -С benzoy kislota S 6 N 5 SOON H dan benzoil xlorid

О С 6 Н 5 -С olishga muvaffaq bo’ldi va Cl ularning tarkibida o’zgarmaydigan S 6 N 5 -SO gruppaning borligini aniqladi. Ko’pchilik kimyogarlar organik moddalar reaktsiyaga kirishish jarayonida boshqa moddalarga aylanganida, ularning molekulalaridagi ma‘lum bir atomlar gruppalarining o’zgarmasligini kuzatadilar. Masalan: [О] О СН 3 -СН 2 ОН СН 3 -С etil spirti sirka aldegidi Н sirka kislota ОН reaktsiyada “СН 3” gruppa o’zgarmay qoladi. Bunday atomlar gruppasi “radikallar”

deyilib, organik moddalar radikallardan tashkil topgan degan fikr paydo bo’ldi. Shu tufayli, o’z kuzatishlariga asoslangan xolda 1815 yilda L. Gey. Lyussak, 1823 yilda F. Vyoler va 1832 yilda Yu. Libix organik moddalarni bir sistemaga solish maqsadida “radikallar nazariyasini” ilgari surdilar. Bu nazariyaga ko’ra radikallar organik moddalarda atom vazifasini bajarib, Xech qanday kimyoviy o’zgarishlarga uchramaydi. ¤sha vaqtda organik birikmalarning radikallarga qarab gruppalarga ajratilishi kimyoning bir oz bo’lsada rivojlanishiga yo’l ochib berdi. Ammo radikallar nazariyasi uzoqqa bormadi, chunki uning tarafdorlari molekulaning

tuzilishidagi tutgan o’rnini isbotlay olmadilar, keyinchalik radikallardagi vodorod atomlarining reaktsiyaga kirishishi mumkinligi isbotlangandan so’ng, bu nazariya o’z kuchini yo’qotdi. Organik kimyoning rivojlanishi bilan 1840 1854 yillarda radikallar nazariyasining o’rniga tiplar nazariyasi vujudga keldi. Bu nazariyaning tarafdorlari J. Dyuma, Sh. Jerar, A. Kekule va boshqalar organik moddalarning tuzilishini tajriba yo’li bilan aniqlab bo’lmaydi, ularni faqat molekulalarning reaktsiya natijasida o’zgaradigan qismiga qarab tiplarga bo’lish mumkin, - degan fikrni ilgari surdilar. Tiplar nazariyasiga ko’ra organik moddalarning tuzilishi va xossalari anorganik birikmalarnikiga o’xshash bo’lib, ulardagi faqat bir yoki bir necha vodorod atomining o’rniga radikallarning almashinishi natijasida yangi organik moddalar xosil bo’ladi.















MAVZU: Alkadiyenlar tuzilishi, xossalari va izomeriyasi. Uglerod zanjirida ikkita qoshbog boladigan uglevadarodlar diyen uglevadarodlar deyiladi ularni asetilen uglevadarodlarining izomeri deyish mumkin diyen uglevodarodlar malekulasida vadarod atomlarini umumiy soni tegishli toyingan uglevadaroddagidan 4 ta kam boladi shu sababli diolefenlarning tarkibi umumiy Cn H 2 n-2 formula bilan ifodalanadi.

Ø Diyen uglevodorodlar molikulasida qo’shbog’larning joylashgan o’rniga qarab 3 grupaga bo’linadi: agar ikkala qo’shbog’bitta uglerod atomiga tutashgan bo’lsa, ular kamulatsiyalangan, agar ikkalaqo’shbog’ uglerod atomi bitta oddiy bog’ bilanbirikan bo’lsa, u holda ular konyugarlangan, agar ikkala qo’shbog’uglerot atomlariga 2 -3 oddiy bog’ bilan bog’langan bo’lsa ajratilgan qo’shbog’li uglevodorotlar deyiladi

• OLINISH USULLARI 1 -3 butadiyen, yani divinil CH 2 - CH-CH=CH 2 sahoatda sintetik kauchik olish uchun muhim hom ashyo bo’lganligi sababli, uning turli hil olinishi ussularini ishlab chiqilgan. neft mahsulotlari va toshko’mir piroliz qilinganda ham oz miqdorda divinil hosil bo’ladi. sanoat miqyosida divinil olish usulini S. V. Lebedev ishlab chiqqan bo’lib, bu usullga ko’ra, etil spirti tempiraturada(400500’C)bug’ga aylantiriladi katalizator ustidan o’tkaziladi.

Reaksiya natijasida divinil suv va vodarod hosil bo’ladi: Ø katalizator Ø C 2 H 5 OH ─────→CH 2=CH-CH=CH 2 +2 H 2 O +H 2 Divinil asitelindan hamolish ham mumkin buni uchunasitelinga avolo, simob tuzi katalizatorligi suv biriktiriladi. bu reaksiya Kucherov reaksiya deyiladi Ø CH≡CH + H 2 O → CH 3 -CH=O

Hosi. L sirka aldegidi o’yuvchi ishqorishtirogida aldol konsentirlanish reaksiyasiga uchratiladi: 2 CH 3 -CH=0 -CH 3 -CH(OH)-CH 2 -CH=0 Aldod qaytarilganda ikki atomli spirt-1. 3 butadiol hosil bo’ladi, so’ngra bu modda fosfat kislata katalizatorligida digedratlanadi va divinil hosil bo’ladi Ø CH 3 -CH(OH)-CH 2 -CHO +H 2 → CH 3 -CH(OH)-CH 2 -CH 2 OH → CH 2=CH-CH=CH 2 +2 H 2 O Ø 1, 3 -butandiol divinil Ø

FIZIK HOSSALARI Divinil oddiy sharoitda-gaz qaynash tempuratusi-45˚ C, suyuqlanish tempuraturasi 108, 9˚ C. izopropin dimetilbutadiyen, xloproren va boshqa diyen uglevadarotlarni normal sharoitdasuyiqlik. diyen uglevadarotlarda ham fizik hossalari to’yinga va to’yinmagan uglevadarotlarning gomollogik qatori kabitartibda ma’lum tartibda ozgaradi’

Izopropen suyuqlik, qaynash tempiraturasi -34. 1˚ C, suyuqlanish tempuraturasiesa 146. ˚ C. dimetbutadiyen suyuqlik ham suyuqlik qaynash tempuraturasi – 68, 8˚C suyuqlanish tempuraturasi 76˚C ga teng bo’ladi.

KIMYOVIY XOSSALARI Konyugrlangan qo’shbog’li uglivodorodlar boshqa diyen uglivodarodlarga qaraganda reaksiya oson kirishadi undan tashqari ular biriksh reaksiyaga uchratilganda o’ziga hos xususiyatlarini nomoyon qiladi. Masalan, divinilgabrom tasir ettirilsa, brom olifenlar yoki kumushlangan va ajratilgan qo’shbo’li diyenlardagidan farqlii o’laroqzanjir uchidagi uglevadarotlarga birikadi
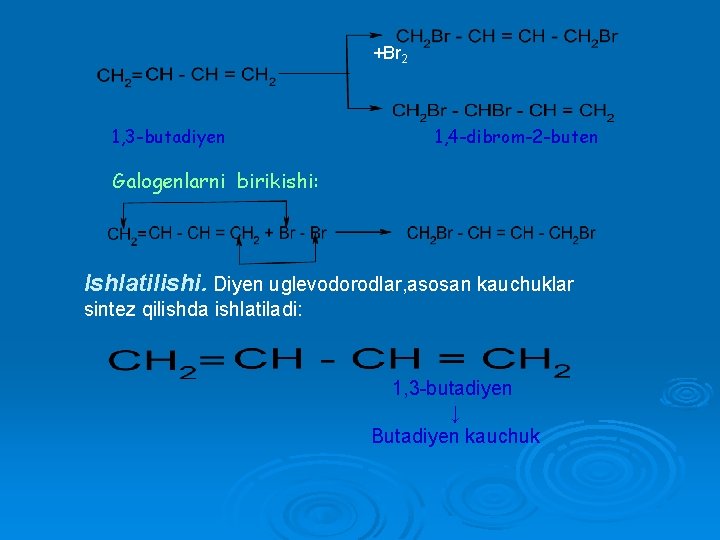
+Br 2 1, 3 -butadiyen 1, 4 -dibrom-2 -buten Galogenlarni birikishi: Ishlatilishi. Diyen uglevodorodlar, asosan kauchuklar sintez qilishda ishlatiladi: 1, 3 -butadiyen ↓ Butadiyen kauchuk
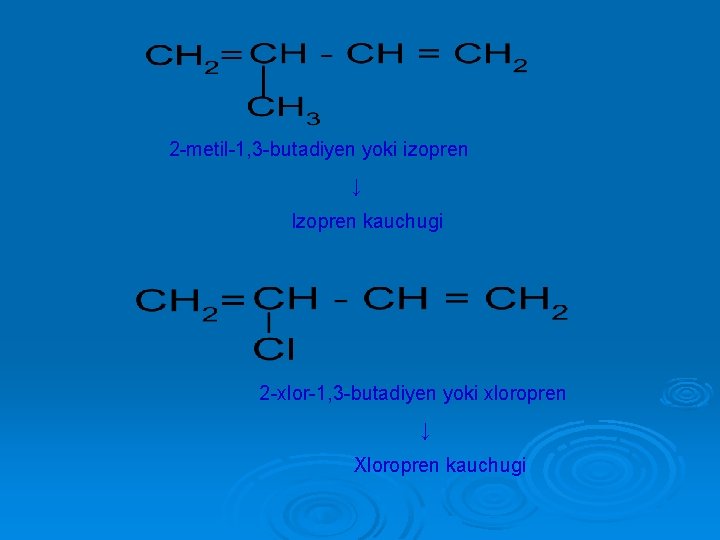
2 -metil-1, 3 -butadiyen yoki izopren ↓ Izopren kauchugi 2 -xlor-1, 3 -butadiyen yoki xloropren ↓ Xloropren kauchugi

NAZORAT SAVOLLARI 1. Diyen uglevodlar deb nimaga aytiladi? 2. Diyen uglevodlar molekulasidagi qo’shbog’ joylashishiga qarab nechaga bo’linadi? 3. Konyugierlangan qo’shbog’ deb nimaga aytiladi? 4. Kucherov reaksiyasi deb nimaga aytiladi? 5. Diyen uglevodorodni fizik va kimyoviy xossalari haqida.

MAVZU: BIR VA KO’P ASOSLI KARBON KISLOTALAR HAMDA ULARNING HOSILALARI l Ma’ruza rejasi: l Tuzilishi, sinflanishi, izomeriyasi, nomenklaturasi l Olinish usullari, fizik va kimyoviy xossalari l Karbon kislotalarning galogenli hosilalari l Ayrim vakillari

Tuzilishida - karboksil guruhi bo’lgan organik birikmalarga karbon kislotalar deyiladi. l Karboksil guruhining soniga qarab ular bir va ko’p asosli kislotalarga bo’linadilar. Karboksil guruhi to’yingan uglevodorod qoldig’i bilan bog’langan bo’lsa to’yingan kislotalar, agar karboksil guruhi to’yinmagan uglevodorod qoldig’i bilan bog’langan bo’lsa to’yinmagan kislotalar deyiladi. l

To’yingan bir asosli karbon kislotalar. l l To’yingan bir asosli karbon kislotalar Cn. H 2 n+1 COOH yoki R-COOH umumiy formulalar bilan ifodalanadi. R-COOH formulada R=-H: - CH 3; -C 2 H 5 va boshqa radikallar bo’lishi mumkin. Izomeriyasi va nomlanishi. Karbon kislotalarning gomologik qatori chumoli kislota H-COOH dan boshlanadi. Ularning dastlabki 3 vakilini izomerlari yo’q. To’rtinchi vakilidan boshlab izomeriya hodisasi kuzatiladi
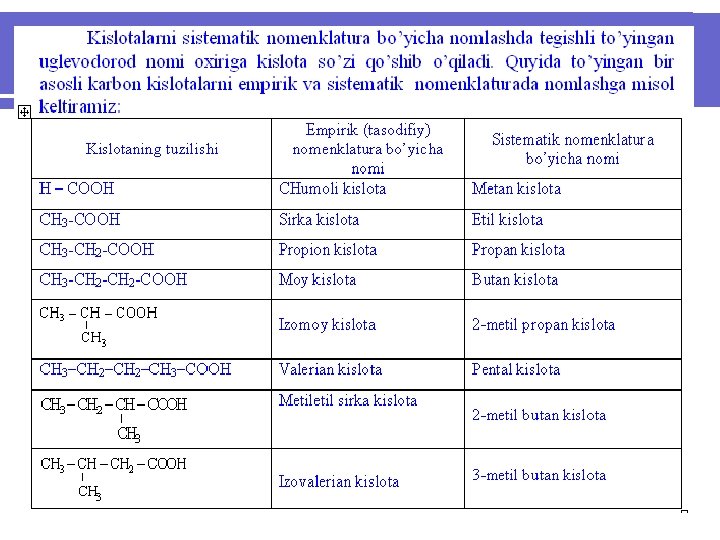



Karbon kislotalarning xossalari. l. Tuzilishida uchtagacha uglerod bo’lgan kislotalar rangsiz suyuqlik bo’lib, o’ziga xos o’tkir xidga ega; suv bilan istalgan nisbatda aralashadi. Tuzilishida to’rttadan to’qqiztagacha uglerod bo’lgan kislotalar moysimon suyuqlik bo’lib, yoqimsiz hidga ega, suvda yomon eriydi. Yuqori kislotalar qattiq moddalar bo’lib, suvda erimaydilar. Chumoli va sirka kislotalarining zichligi birdan katta, qolganlariniki esa birdan kichikdir. Tarkibida teng uglerod atomi saqlangan to’g’ri zanjir hosil qilib tuzilgan kislotalar yuqori haroratda, tarmoqlangan tuzilishga ega bo’lganlari esa nisbatan past haroratda qaynaydilar. Juft sonli uglerod atomi saqlovchi kislotalar yuqori haroratda, toq sonli uglerod atomi saqlovchi kislotalar esa past haroratda suyuqlanadilar. Masalan, kapril kislota C 7 H 15 -COOH ning suyuqlanish harorati 15, 20 C, enant– C 6 H 13 COOH va felargon kislota C 8 H 17 -COOH niki esa– 10, 50 C va 12, 50 C ga tengdir. Kislotalar tegishli spirtlarga qaraganda yuqori haroratda qaynaydilar. Buning asosiy sababi ular molekulalarining assotsiyalangan holatda bo’lishligi hisoblanadi.
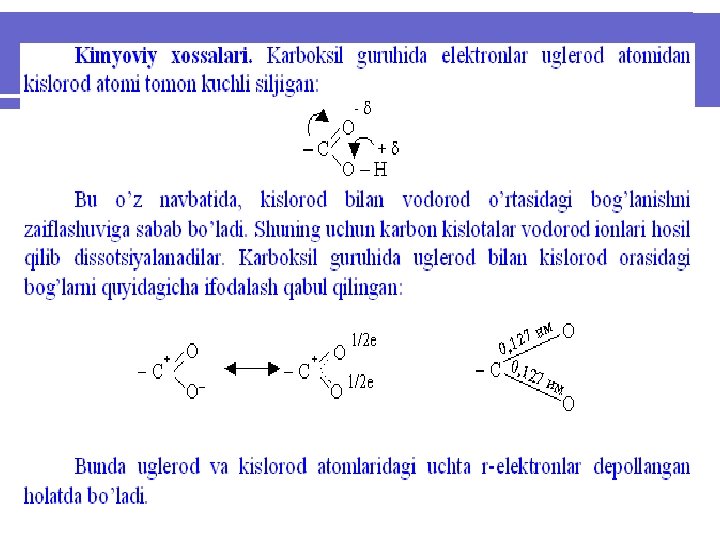




Fizik-kimyoviy xususiyatlari. Ikki asosli to’yingan karbon kislotalar suvda yaxshi eriydigan kristall moddalar bo’lib, ularni kislotalik doimiyligi tegishli bir asosli kislotalarnikiga qaraganda yuqori. Ular bosqichli dissotsionaladilar: Kimyoviy xossalari jihatidan ikki asosli kislotalar to’yingan bir asosli kislotalarning barcha xossalarini takrorlaydilar, ya’ni ular metall va metall oksidlari, gidrooksidlari bilan tuz hosil qiladilar, murakkab efir, kislota angidridi, galoid angidrid va boshqalar hosil qiladilar. Faqat ularda reaksiya bosqichli borib, o’rta va nordon tuz, mono- va diefir va boshqalarni hosil qilishlari mumkin. Shuning bilan birga bir asosli kislotalardan farq qiladigan reaksiyalarga ham kirisha oladilar.

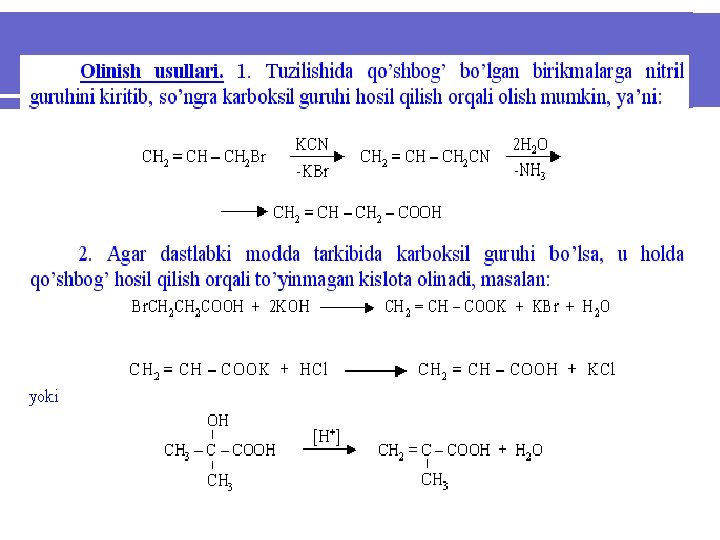

Fizik va kimyoviy xossalari. To’yinmagan kislotalar to’yingan kislotalarga qaraganda zichligining va kislotalik konstantasining kattaligi bilan farq qiladilar. l Ular ikki xil xususiyatni namoyon qiladilar, ya’ni kislotalar kabi tuzlar, angidridlar, amidlar, murakkab efirlarni hosil qilsalar, qo’shboshning hisobidan biriktirib olish, polimerlanish kabi reaksiyaga kirisha oladilar. l Agar qo’shbog’ karboksil guruhiga nisbatan - yoki holatda joyilashgan bo’lsa, bunday kislotalarga turli reagentlarning birikishi Markovnikov qoidasiga teskari boradi. l Akril, metakril kislota va ularning efirlari etilen uglevodorodlariga qaraganda oson polimerlanadilar: l


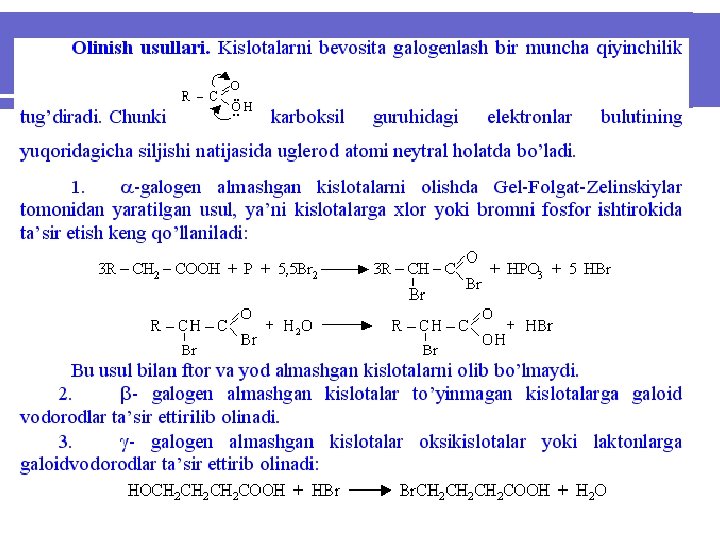




6. 6. Aromatik karbon kislotalarning tuzilishida aromatik halqa bilan birga bir necha karboksil guruhi mavjud bo’ladi. Karboksil guruhi benzol halqasi bilan bevosita bog’langan yoki yon zanjirda bo’lishi mumkin. Karboksil guruhi yon zanjirda joylashgan kislotalar alkil – aromatik karbon kislotalar deb qaraladi. Aromatik kislotalar karboksil guruhining soniga qarab bir va ko’p asosli kislotalarga bo’linadilar. Agar karboksil guruhi aromatik halqa bilan bevosita bog’langan bo’lsa ularning nomi aromatik uglevodorod nomidan hosil qilinadi, agar karboksil guruhi yon zanjirda joylashgan bo’lsa, bunday kislotalarning nomi tegishli yog’ qator kislotasining nomidan olinadi, masalan:
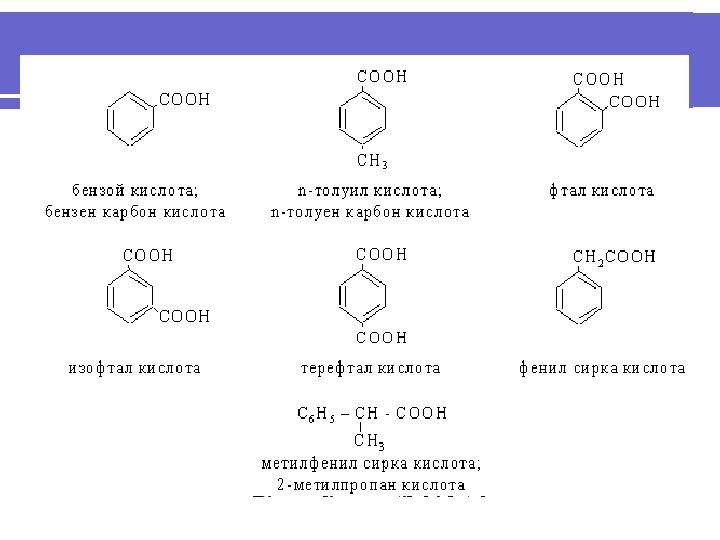
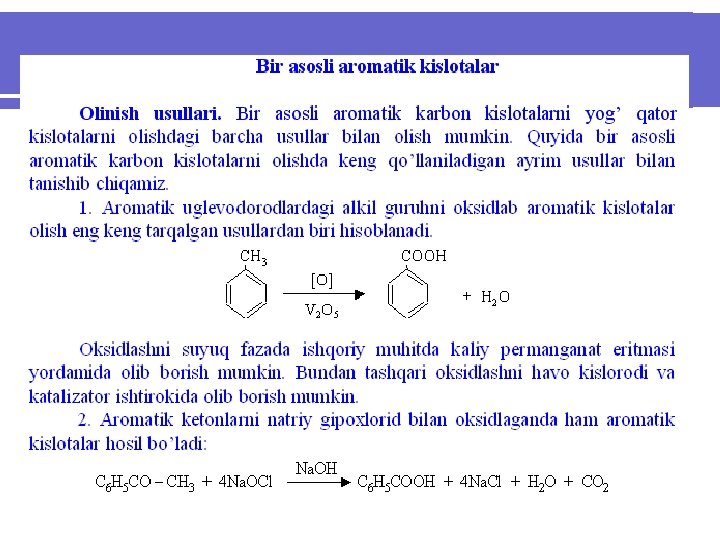


Fizikaviy va kimyoviy xossalari. Benzol qator aromatik monokarbonkislotalari 1000 C dan yuqori haroratda suyuqlanadigan rangsiz kristall moddalardir. Agar karboksil guruhiga nisbatan para-holatda o’rinbosar bo’lsa, bunday kislotalar yuqori haroratda suyuqlanadilar. Aromatik karbon kislotalar teng uglerod sonli yog’ qator kislotalariga qaraganda yuqori haroratda suyuqlanadilar va qaynaydilar. Aromatik monokarbonkislotalar sovuq suvda yomon, issiq suvda yaxshi eriydilar. l Monokarbonkislotalarning suvli eritmalarida ular yaxshi dissotsiyalangan bo’ladilar va ularning kislotalik doimiyligi yog’ qator kislotalarnikiga nisbatan katta, masalan, sirka kislotaning dissotsiyalash doimiysi 1, 8. 10 -5 ga, benzol kislotaniki esa 6, 6. 10 -5 ga teng. l



Alohida vakillari va ularning qo’llanilishi. Benzoy kislota sof holda benzoy qatroni (smolasi) tarkibida uchraydi. Benzoy efiri ko’rinishida ayrim balzamlar tarkibiga kiradi. Glutar kislota ko’rinishida esa, u ayrim xayvonlarning peshobida uchraydi. Sanoatda toluolni oksidlab olinadi. Benzoy kislota 121, 50 C da suyuqlanadigan rangsiz iproqlar ko’rinishiga ega. l Suv bilan hosil qilgan kristall gidrati 900 C da suyuqlanadi. Bo’yoqlar va yoqimli hid beruvchi vositalar konservantlar ishlab chiqarishda qo’llaniladi. Benzoy kislotaning muhim hosilalaridan biri benzoil xlorid bo’lib, u o’ziga xos hidga ega. Turli molekulalar tarkibiga benzoil guruhini kiritishda foydalaniladi. l Fenilsirka kislota C 6 H 5 CH 2 COOH -760 C da suyuqlanadigan kristall modda. Benzilxloriddan nitril va magniy organik birikma orqali olinadi: l

Nazorat savollari l l l l l Karbon kislotalar deb qanday birikmalarga aytiladi? Atsil radikali nima? Yog’ kislotalari deb qanday moddalarga aytiladi? Palmitin va stearin kislotalar qayerlarda uchraydi? Qanday birikmalarga qattiq va suyuq sovun deyiladi? Benzoy kislota va uning Na li tuzi oziq-ovqat sanoatining, qaysi sohasida va nima uchun ishlatiladi? Benzoil peroksid oziq-ovqat sanoatining qaysi sohasida ishlatiladi? U qanday xususiyatga ega? Fenil sirka kislota qayerlarda ishlatiladi? Nima sababli galogenli karbon kislotalar kuchliroq kislota hisoblanadi? Karbon kislota angidridlari deb qanday moddalarga aytiladi?










- Slides: 94