BAB 8 Hidrokarbon Perkembangan Kimia Karbon Senyawa karbon

BAB 8 Hidrokarbon

Perkembangan Kimia Karbon Senyawa karbon yang tersusun atas atom karbon (C) dan atom hidrogen (H), dikenal dengan hidrokarbon, merupakan senyawa karbon yang susunan (strukturnya) paling sederhana. Elpiji mengandung senyawa hidrokarbon, seperti propana, etana, dan butana. Komponen utama elpiji adalah propana (90%) yang merupakan hidrokarbon alifatik jenuh (ikatan rantai karbonnya terdiri atas ikatan tunggal). Nyala api pada kompor gas dapat menghasilkan sejumlah energi yang dapat dimanfaatkan untuk memasak.

Perkembangan Kimia Karbon Senyawa karbon merupakan senyawa yang molekulnya mengandung atom karbon. Semula orang beranggapan bahwa senyawa karbon hanya dapat diperoleh dari makhluk hidup. Frederick Wohler, seorang ahli kimia dari Jerman dapat menyintensis urea (CO(NH 2)2) dengan cara memanaskan amonium sianat (NH 4 CNO). Urea merupakan senyawa organik yang berasal dari luar makhluk hidup. Sejak penemuan Wohler tersebut, penggolongan senyawa karbon menjadi senyawa organik dan anorganik tidak didasarkanpada asalnya, tetapi didasarkan pada sifatnya.

Perkembangan Kimia Karbon Uji Keberadaan Unsur C, H, dan O dalam Senyawa Karbon Selain mengandung atom karbon (C), senyawa organik dapat mengandung atom lain, seperti hidrogen (H), oksigen (O), nitrogen (N), belerang (S), fosfor (P). Oleh karena itu, senyawa organik disebut juga senyawa karbon. Senyawa organik titik didih dan titik leleh nya relatif rendah, mudah larut dalam air pelarut nonpolar, kurang reaktif (sukar bereaksi), tidak stabil terhadap pemanasan. Adapun senyawa anorganik titik didih dan titik lelehnya ada yang sangat tinggi, tetapi ada yang sangat rendah, mudah larut dalam pelarut polar, reaktif, dan stabil terhadap pemanasan. Senyawa karbon berasal dari tumbuhan, hewan karbohidrat, protein, lemak, hormon, yang merupakan hasil biosintesis dalam tubuh atau sel tumbuhan dan hewan ( batu bara, gas alam, dan minyak bumi) hasil untuk kosmetik, pupuk, peralatan rumah tangga, dan lain-lain.
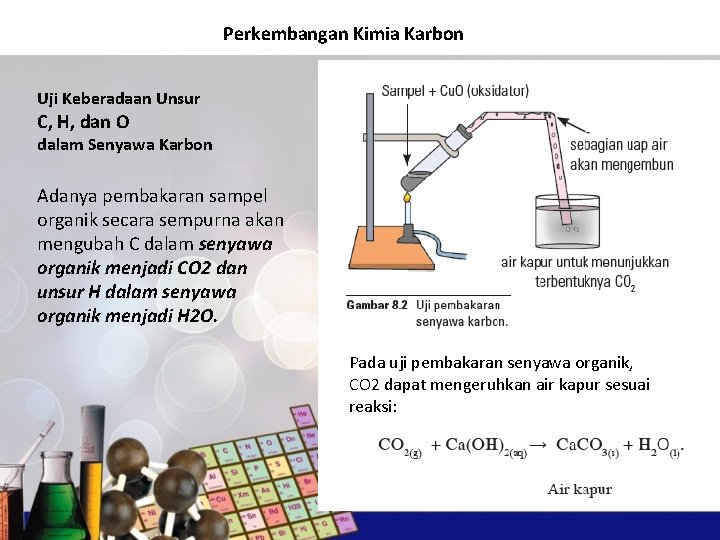
Perkembangan Kimia Karbon Uji Keberadaan Unsur C, H, dan O dalam Senyawa Karbon Adanya pembakaran sampel organik secara sempurna akan mengubah C dalam senyawa organik menjadi CO 2 dan unsur H dalam senyawa organik menjadi H 2 O. Pada uji pembakaran senyawa organik, CO 2 dapat mengeruhkan air kapur sesuai reaksi:

Uji Keberadaan Unsur C, H, dan O dalam Senyawa Karbon Kekhasan Atom Karbon Posisi atom karbon tersebut mengakibatkan atom karbon mempunyai sifat yang khas dibandingkan atom lainnya. Atom karbon mempunyai elektron valensi 4 sehingga untuk mencapai kestabilan akan membentuk ikatan kovalen yang digambarkan sebagai 4 tangan ikatan Atom karbon dapat membentuk rantai karbon dengan berbagai kemungkinan. Atom karbon relatif kecil, daripada atom karbon dengan nomor atom 6, berarti mempunyai 2 kulit sehingga jari-jari atom kecil. Hal ini mengakibatkan ikatan kovalen yang dibentuk relatif kuat.

Kekhasan Atom Karbon Posisi atom karbon dalam rantai karbon meliputi atom C primer yaitu atom C yang mengikat 1 atom C yang lain atom C tersier yaitu atom C yang mengikat 3 atom C yang lain atom C sekunder yaitu atom C yang mengikat 2 atom Cyang lain atom C kuarterner yaitu atom C yang mengikat 4 atom C yang lain

Penggolongan Hidrokarbon Alifatik Jenuh Alifatik jenuh adalah senyawa alifatik yang ikatan rantai karbonnya terdiri atas ikatan tunggal. Hidrokarbon alifatik adalah senyawa karbon yang ikatan rantai karbonnya terbuka.

Penggolongan Hidrokarbon Alifatik Hidrokarbon alifatik adalah senyawa karbon yang ikatan rantai karbonnya terbuka. Alifatik Tak Jenuh Alifatik tak jenuh adalah senyawa alifatik yang ikatan rantai Karbon nya terdapat ikatan rangkap (rangkap 2 atau rangkap 3). Hidrokarbon Siklik Hidrokarbon siklik adalah senyawa karbon yang rantai karbonnya tertutup atau melingkar. Hidrokarbon siklik dibedakan menjadi dua, yaitu sebagai berikut. Senyawa Karbosiklik Senyawa Heterosiklik

Penggolongan Hidrokarbon Senyawa Karbosiklik Senyawa karbosiklik adalah senyawa siklik yang rantai lingkarannya terdiri atas atom karbon. Senyawa karbosiklik dapat dibedakan menjadi dua: Senyawa Aromatik Senyawa aromatik adalah senyawa siklik yang rantai lingkarannya tunggal dan rangkap berselang-seling.

Penggolongan Hidrokarbon Senyawa Karbosiklik Senyawa alisiklik adalah senyawa alifatik yang rantai karbonnya tertutup. Senyawa Heterosiklik Senyawa heterosiklik adalah senyawa siklik yang rantai lingkarannya terdapat atom lain selain atom karbon.

Alkana merupakan hidrokarbon alifatik jenuh, yaitu hidrokarbon dengan rantai terbuka dan semua ikatan karbon merupakan ikatan tunggal ( C-C). Deret Homolog Suatu kelompok senyawa karbon dengan rumus umum yang sama dan sifat yang bermiripan disebut deret homolog (deret sepancaran). Rumus Umum Alkana Keterangan n : jumlah atom C

Tata Nama Alkana Jika rantai C tidak bercabang Nama alkana sesuai dengan jumlah atom C dan diberi awalan n (n: normal/tidak bercabang) jika rantai karbon terdiri atas 4 atom C atau lebih. Jika rantai C bercabang Menentukan rantai C terpanjang (rantai induk) yang menjadi nama alkananya Atom-atom C yang tidak terletak pada rantai terpanjang merupakan cabang Cabang diberi nama alkil, yaitu nama alkana yang sesuai dengan mengganti akhiran -ana menjadi -il. Gugus alkil mempunyai rumus umum:

Nama gugus alkil dan strukturnya

Penulisan Rumus Struktur Senyawa Alkana 1) Menuliskan rantai induk senyawa alkana. 2) Menuliskan cabang (gugus alkil) pada rantai induk. 3) Menambahkan atom H yang terikat pada atom C. Pada prinsipnya, penulisan struktur senyawa alkana adalah atom C mempunyai 4 tangan ikatan Alkena (Olefin: Pembentukan Minyak) Rumus Umum Alkena Keterangan: n : jumlah atom C
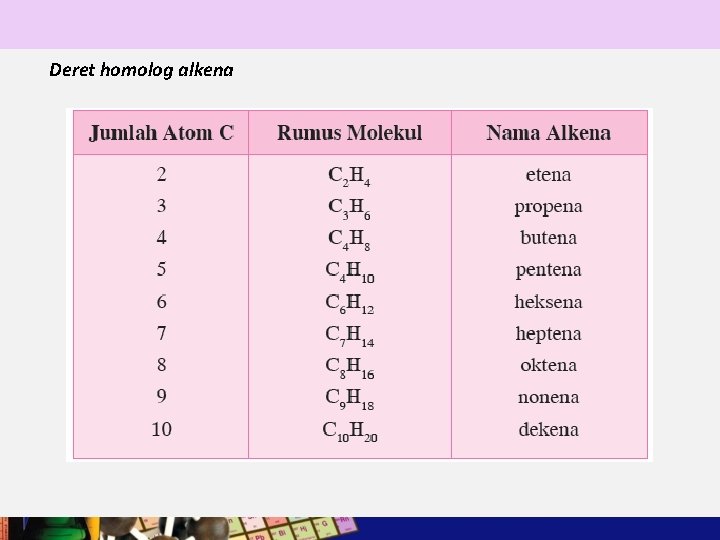
Deret homolog alkena
- Slides: 16