Mavzu Karbon kislotalar Toyingan bir asosli karbon kislotalar

Mavzu: Karbon kislotalar. To`yingan bir asosli karbon kislotalar olinishi, kimyoviy, fizikaviy xossalari. Agar sen o’zing uchun harakat qilmasang, intilmasang, yuzta o’qituvchini senga biriktirib, qo’yilganida ham bundan xech qanday natija chiqmaydi. !!! (Aristotel)

Reja 1. Karbon kislotalarning umumiy tavsifi, tabiatda tarqalishi. 2. Karbon kislotalarni olinish va xossalari. 3. karbon kislotani ishlatilishi.

Molekulasida funksional karboksil gruppasi saqlaydigan organik birikmalarga karbon kislotalar deyiladi. Karboksil degan nom karbonil va gidroksid so‘zlaridan kelib chiqqan. Karbon kislotalar molekulasidagi karboksil gruppaning soniga ko‘ra bir asosli, ikki asosli va ko‘p asosliga, radikalning tabiatiga ko‘ra to‘yingan, to‘yinmagan va aromatik xillariga farqlanadi. Bir asosli to‘yingan karbon kislotalarga shunday ta’rif berish mumkin: molekulalarida to‘yingan uglevodorod radikali yoki vodorod atomi bilan birikkan bitta karboksil gruppasi bo‘lgan organik moddalar bir asosli to‘yingan karbon kislotalari deb ataladi.

Ularni umumiy holda formula bilan ifodalash mumkin (chumoli kislota bundan Nomenklaturasi. Ko‘pincha kislotalarning tarixiy trivial nomlari ishlatiladi: H—COOH—chumoli kislota; CH 3—COOH—sirka kislota; CH 3—CH 2—COOH—propion kislota; CH 3—CH 2—COOH —moy kislota; CH 3—CH 2—CH 2—COOH—valerian kislota. СН 3 — (СН 2)4 — СООН — kapron kislota СН 3 — (СН 2)5 — СООН — enant kislota СН 3 — (СН 2)14 — СООН — palmitin kislota СН 3 — (СН 2)|6 — СООН — stearin kislota

Ratsional nomenklaturaga muvofiq bir asosli karbon kislotalarni nomlashda karboksil gruppa bilan birikkan radikalga mos keladigan uglevodorod nomiga “karbon kislota“ so‘zlari qo‘shiladi. Masalan: sirka kislota CH 3 COOH— metan karbon kislota; propion kislota CH 3 CH 2 COOH—etan karbon kislota; moy kislota CH 3 CH 2 COOH—propan karbon kislota, deb ataladi. Karbon kislotalarda gidroksil gruppa ta’sirida karboksil gruppaga qo'shni bo'lgan uglerod atomidagi vodorod atomlarining harakatchanligi ortadi. Shu sababli ularning o'rnini xlor yoki brom atomlari oson egallashi mumkin: CH 3 COOH + Cl 2 → CH 2 Cl. COOH + HCI 2 -xloretan (xlorsirka) kislota СН 3 СH 2 СООН + Br 2 → CH 3 CHBr. COOH +HBr 2 -brompropan
![I. Karbon kislotalarni oksidlash reaksiyalari orqali olinishi 1. Spirtlarni oksidlab 2. Aldegidlarni oksidlab [O] I. Karbon kislotalarni oksidlash reaksiyalari orqali olinishi 1. Spirtlarni oksidlab 2. Aldegidlarni oksidlab [O]](http://slidetodoc.com/presentation_image_h2/600bbfaf53be243d79144a553590530e/image-6.jpg)
I. Karbon kislotalarni oksidlash reaksiyalari orqali olinishi 1. Spirtlarni oksidlab 2. Aldegidlarni oksidlab [O] – havo kislorodi va Co, Mn kat.

Tabiatda tarqalishi. Chumoli kislota HCOOH, o‘tkir hidli, rangsiz suyuqlik, 101 °C da qaynaydi. Suvda istalgan miqdorda eriydi. Terini kuydiradi. U chumoli bezlaridan ajralib chuqadigan suyuqlik tarkibida, shuningdek ba’zi o‘simliklarda, qichitqi o‘t (krapiva)da va ignabargli archada bo‘ladi. Qichitqi o‘tning kuydirishi — chumoli kislotaning yallig‘lantirish ta’sirining natijasidir. Moy kislota (propan kislota) achigan moy tarkibida, valerian (butan) kislota esa valerian o‘simligi ildizida bo‘ladi.

Chumoli kislota 16 asr – chumolilardan chiqadigan “achchiq bug’i o’simliklardan olingan bo’yoqlarning rangini qizil rangga o’zgartirishi aniqlangan Dj. Rey – chumolilardan chumoli kislotasini sintez qilgan va unga nom bergan
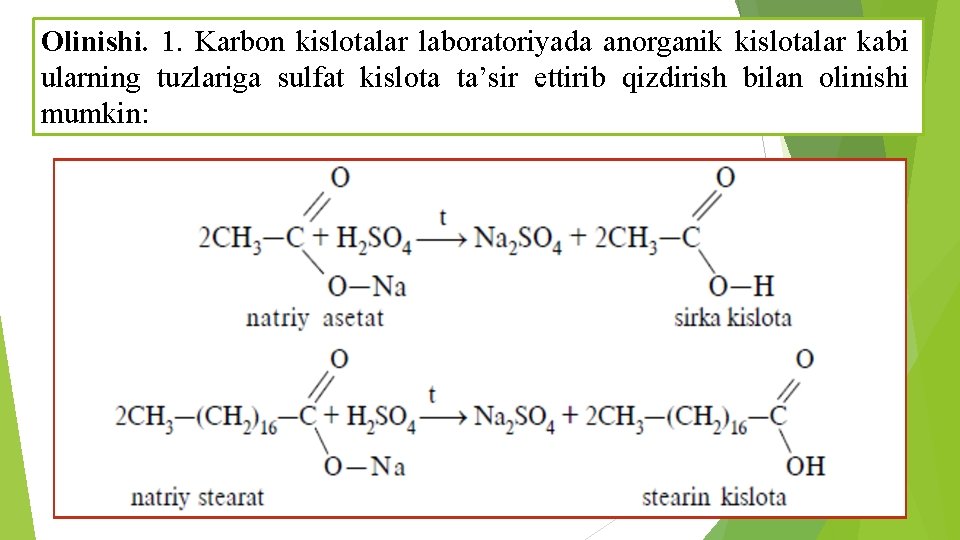
Olinishi. 1. Karbon kislotalar laboratoriyada anorganik kislotalar kabi ularning tuzlariga sulfat kislota ta’sir ettirib qizdirish bilan olinishi mumkin:

To‘yingan bir asosli karbon kislotalar, asosan, quyidagi usullar bilan olinadi: 1. Murakkab efirlarni gidrolizlash bilan olish mumkin: Bu usul amalda yuqori molekular yog‘ kislotalarini yog‘lardan va moylardan olishda qo‘llaniladi. 2. Birlamchi spirtlarni oksidlash yo‘li bilan olish. Bunda avval aldegid, so‘ngra esa kislota hosil bo‘ladi:

Karbon kislotalarni yana bir vakili sirka kislota bo`lib: Sirka kislota odatdagi temperaturada — o'ziga xos o'tkir hidli rangsiz suyuqlik. U +16, 6°Cdan past temperaturada muzga o'xshash kristallar holida qotadi, shu sababli m u z sirka kislota deyiladi. Sirka kislota suvda istalgan miqdorda eriydi, uning suvdagi 3 - 9 % li eritmasi sirka deyiladi va ovqatga qo'shish uchun ishlatiladi. 70 - 8 0 % li sirka kislota sirka essensiyasi deyiladi. Kimyoviy xossalari jihatidan sirka kislota mineral kislotalarga o'xshaydi. U suvdagi eritmada ionlarga dissotsilanadi: CH 3 COOH ↔ CHCOO- + H+
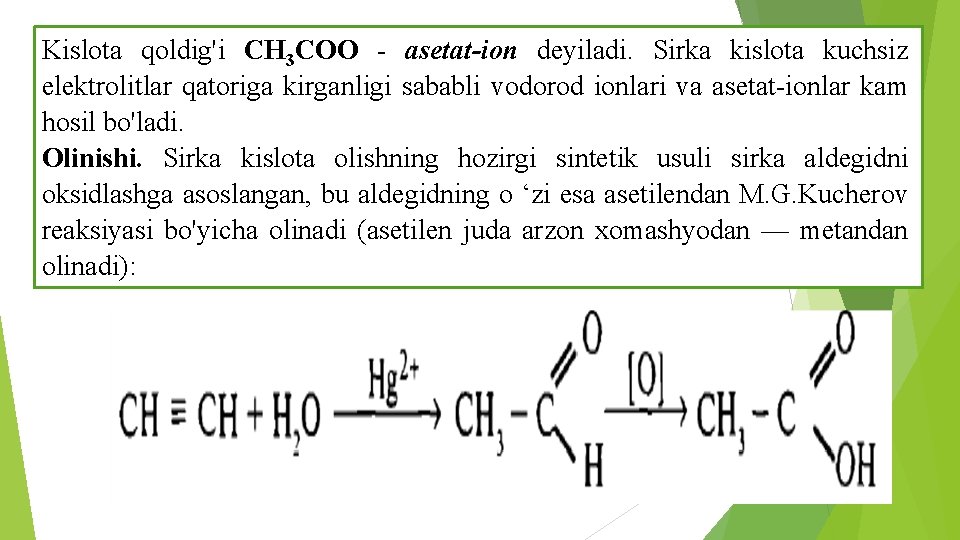
Kislota qoldig'i CH 3 COO - asetat-ion deyiladi. Sirka kislota kuchsiz elektrolitlar qatoriga kirganligi sababli vodorod ionlari va asetat-ionlar kam hosil bo'ladi. Olinishi. Sirka kislota olishning hozirgi sintetik usuli sirka aldegidni oksidlashga asoslangan, bu aldegidning o ‘zi esa asetilendan M. G. Kucherov reaksiyasi bo'yicha olinadi (asetilen juda arzon xomashyodan — metandan olinadi):

Kim birinchi bor kislotalarni olgan? Sirka kislota СН 3 СООН – 8 asrdan beri bizga ma’lum Suvsiz sirka kislotani – 1789 yili. , Toviy Yegorovich Lovits, aktiv ko’mirdan olgan t=16, 50 С da kristallanadi, muzni yodga soladi → «muzli kislota»

Sirka kislota olishning butanni oksidlashga asoslangan yangi usuli katta ahamiyat kasb etmoqda: Sirka kislotani metandan olish jarayoni ko‘p bosqichli b o‘lgan holda (metan → asetilen →sirka aldegid → sirka kislota) butanni oksidlab kislota olish bir bosqichlidir, bu esa katta iqtisodiy samara beradi. Ishlatilishi. Sirka kislota turli-tuman maqsadlarda ishlatiladi. Kimyo sanoatida undan plastik massalar, turli xil bo‘yoqlar, doridarmonlar, sun’iy tola(asetat ipak), yonmaydigan kinoplyonkava h. k. olish uchun foydalaniladi. Sirka kislotaning aluminiyli, xromli va temirli tuzlari gazlamalami bo'yashda, dorilash uchun ishlatiladi. Sirka kislotaning tuzlaridan qishloq xo'jaligi zararkunandalariga qarshi kurashda h a m foydalaniladi. Sirka kislota ovqatga solish, sabzavotlarni konservalash uchun ham ishlatiladi.

- Slides: 15