WEEK 8 9 10 Energi Perubahan Energi Binyamin

WEEK 8, 9 & 10 (Energi & Perubahan Energi) Binyamin Mechanical Engineering Muhammadiyah University Of Surakarta

Energi = Kemampuan untuk melakukan usaha Jenis Energi yang dimiliki oleh suatu benda Energi Kinetik ( EK ) = Benda bergerak Energi Potensial ( EP ) = Tersimpan akibat posisi Energi Radiasi = Energi Matahari Energi Kimia = Energi tersimpan oleh struktur zat kimia Energi Thermal = Energi terkait gerak atom Hukum kekekalan energi : “Energi tidak dapat diciptakan dan tidak dapat dimusnahkan melainkan hanya dapat diubah dari bentuk satu ke bentuk yang lain”. 2

PERUBAHAN ENERGI DALAM REAKSI KIMIA Satuan energi dalam ilmu Fisika adalah Joule, 1 Joule = 1 Kg m 2/s 2 = 1 Nm Energi panas memiliki satuan kalori (kal), 1 kal didefinisikan sebagai jumlah panas/kalor yang diperlukan untuk menaikkan temperatur sebesar 1 o. C dari 1 gram air dengan suhu asal 15 o. C. 1 kal = 4, 184 J 1 Kkal = 4184 J = 4, 184 KJ 3
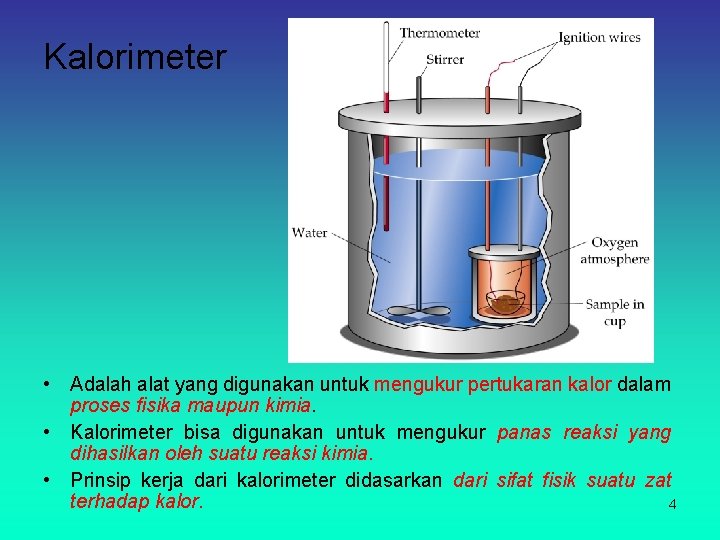
Kalorimeter • Adalah alat yang digunakan untuk mengukur pertukaran kalor dalam proses fisika maupun kimia. • Kalorimeter bisa digunakan untuk mengukur panas reaksi yang dihasilkan oleh suatu reaksi kimia. • Prinsip kerja dari kalorimeter didasarkan dari sifat fisik suatu zat terhadap kalor. 4

Kalorimeter (2) • Suatu zat memiliki sifat yang disebut sebagai kalor jenis (Specific heat) yaitu suatu sifat terkait dengan jumlah kalor yang di perlukan untuk menaikkan suhu sebesar 1 o. C dari 1 gram zat. Kalor jenis diberi simbol c dan Satuannya Joule/(gr o. C) • Jika suatu benda massa tertentu dipanaskan maka kalor yang dibutuhkan untuk menaikkan temperatur 1 derajat Celcius benda tersebut disebut sebagai kapasitas kalor/panas dimana; • Kapasitas panas (C) = massa x Kalor jenis dan satuan J/o. C 5

Kalorimeter (3) Contoh Persoalan Berapa kapasitas panas (KJ/0 C) dari 2, 00 Kg batang tembaga bila diketahui panas spesifik dari tembaga 0, 387 J g-1 0 C-1. Jawab : Kapasitas panas = kalor jenis x massa = (0, 387 J g-1 0 C-1) X 2000 g = 774 J/ 0 C = 0, 774 KJ/0 C Berapa Joule energi yang dibutuhkan untuk menaikkan suhu sebuah paku yang mempunyai massa 7, 05 g dari 25 o. C ke 1000 C, kalor jenis besi adalah 0, 452 J g-1 o. C-1. Penyelesaian : Energi = massa x kalor jenis x Δ suhu = 7, 05 g x 0, 452 J g-1 0 C-1 x (100 – 25 ) 0 C = 239 J 6
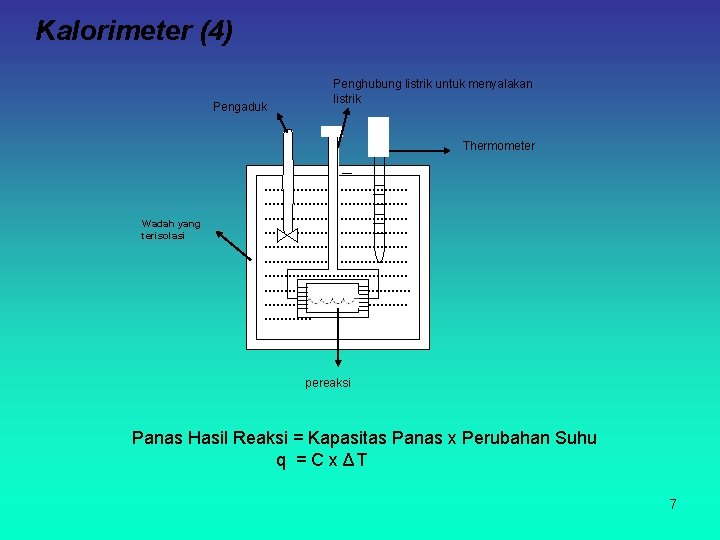
Kalorimeter (4) Pengaduk Penghubung listrik untuk menyalakan listrik Thermometer Wadah yang terisolasi ……………………………… ……………………………… …………………air……………… ………… pereaksi Panas Hasil Reaksi = Kapasitas Panas x Perubahan Suhu q = C x ΔT 7
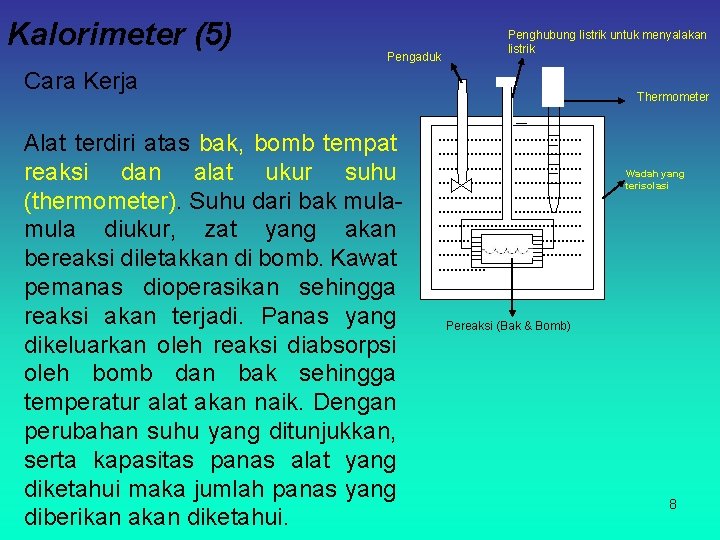
Kalorimeter (5) Pengaduk Penghubung listrik untuk menyalakan listrik Cara Kerja Alat terdiri atas bak, bomb tempat reaksi dan alat ukur suhu (thermometer). Suhu dari bak mula diukur, zat yang akan bereaksi diletakkan di bomb. Kawat pemanas dioperasikan sehingga reaksi akan terjadi. Panas yang dikeluarkan oleh reaksi diabsorpsi oleh bomb dan bak sehingga temperatur alat akan naik. Dengan perubahan suhu yang ditunjukkan, serta kapasitas panas alat yang diketahui maka jumlah panas yang diberikan akan diketahui. Thermometer ……………………………… ……………………………… …………………air……………… ………… Wadah yang terisolasi Pereaksi (Bak & Bomb) 8

Kalorimeter (6) Contoh Pada suatu percobaan, 0, 100 g H 2 dan 0, 800 g O 2 dimampatkan dalam bomb 1, 00 L yang kemudian ditempatkan dalam sebuah kalorimeter yang mempunyai kapasitas Panas 9, 08 x 104 J/0 C. Temperatur mula-mula dari kalorimeter diukur yaitu 250 C dan sesudah reaksi menjadi 25, 150 C. Hitung jumlah panas yang dikeluarkan oleh reaksi antara H 2 dan O 2 untuk membentuk H 2 O dalam : a) Kilo Joule dan b)Dalam Kilo Joule/mol H 2 O Penyelesaian : a). Jumlah panas = Kapasitas panas x perubahan suhu Jumlah panas = (9, 08 x 104 J/0 C) X (0, 150 C) = 1, 362 x 104 J = 13, 62 KJ. b). Reaksi antara H 2 dan O 2 untuk menghasilkan H 2 O 2 H 2 + O 2 2 H 2 O jumlah antara H 2 O yang terbentuk : 0, 100 g H 2 x = 0, 05 mol H 2 O sehingga jumlah panas yang dikeluarkan oleh reaksi untuk tiap mol H 2 O adalah = 13, 62 KJ / 0, 05 mol = 272, 4 KJ/mol H 2 O 9

TERMOKIMIA PENGERTIAN Termokimia adalah cabang dari ilmu kimia yang mempelajari hubungan antara reaksi kimia dengan panas yang menyertainya. HAL-HAL YANG DIPELAJARI • Perubahan energi yang menyertai reaksi kimia • Reaksi kimia yang berlangsung secara spontan • Reaksi kimia dalam kedudukan kesetimbangan. 10

REAKSI EKSOTERM DAN ENDOTERM 1. REAKSI EKSOTERM Adalah reaksi yang pada saat berlangsung disertai pelepasan/menghasilkan panas atau kalor. Panas reaksi ditulis dengan tanda positip. Contoh : N 2 (g) + 3 H 2 (g) 2 NH 3 (g) + 26, 78 Kkal 2. REAKSI ENDOTERM Adalah reaksi yang pada saat berlangsung membutuhkan panas. Panas reaksi ditulis de ngan tanda negatif Contoh : 2 NH 3 N 2 (g) + 3 H 2 (g) - 26, 78 Kkal 11

PERUBAHAN ENTALPI (ΔH) PENGERTIAN Perubahan entalpi adalah perubahan kalor dari reaksi pada temperatur dan tekanan yang tetap, yaitu selisih antara entalpi zatzat hasil dikurangi entalpi zat-zat reaktan. Rumus : ΔH = Hh - Hr ΔH : perubahan entalpi Hh : entalpi hasil reaksi Hr : entalpi zat reaktan. 12

PERUBAHAN ENTALPI (ΔH) 1. PADA REAKSI EKSOTERMAL P + Q R + x Kkal P dan Q = zat awal R = zat hasil reaksi x = besarnya panas reaksi Menurut hukum kekekalan energi : Isi panas (P + Q) = Isi panas R + x Kkal H (P + Q) = H ( R) + x Kkal H (R) - H (P + Q) = - x Kkal ΔH = - x Kkal 13

PERUBAHAN ENTALPI (ΔH) 2. PADA REAKSI ENDOTERMAL R P + Q – x Kkal Berlaku : H (P + Q) - H (R) = x Kkal ΔH = x Kkal Kesimpulan : Besarnya perubahan entalpi (ΔH) sama dengan besarnya panas reaksi, tetapi dengan tanda berlawanan. Contoh soal : Hitung entalpi perubahan CH 4 (g) menjadi CO 2 (g) dan H 2 O(g) Pada temperatur 298 K, bila diketahui pada temperatur tersebut : ΔH. CH 4 = -74, 873 KJ mol-1 ; ΔH. O 2 = 0, 00 KJ mol-1 14

PERUBAHAN ENTALPI (ΔH) ΔH. CO 2 = - 393, 522 KJ mol-1 dan ΔH. H 2 O = -241, 827 KJ mol-1 Jawab : CH 4 + 2 O 2 CO 2 + 2 H 2 O ΔH = H {CO 2 + (2 x H 2 O)} – H {CH 4 + (2 x O 2)} ΔH = {- 393, 522 + (2 x (- 241, 827)} – {- 74, 873 + (2 x 0, 000)} ΔH = - 802, 303 KJ mol-1 Tanda negatif menunjukkan bahwa reaksi di atas merupakan reaksi eksoterm (reaksi yang menghasilkan kalor). PENENTUAN PERUBAHAN ENTALPI Penentuan perubahan entalpi selalu dilakukan pada tekanan dan temperatur yang tetap. Untuk reaksi tertentu dapat ditentukan dengan kalorimeter. 15

PERUBAHAN ENTALPI (ΔH) Reaksi tertentu tersebut, antara lain : 1. Reaksi dalam larutan 2. Reaksi gas yang tidak mengalami perubahan koefisien antara sebelum dan sesudah reaksi. Contoh : Pada perubahan dari 12, 425 gram karbon menjadi CO 2 pada, suhu reaksi yang semula 30 o. C, terjadi kenaikan suhu sebesar 0, 484 o. C. Apabila kapasitas kalorimeter 200 Kkal/o. C. Berapa ΔH tiap mol karbon yang dibakar ? Jawab : C + O 2 CO 2 16

Contoh : Pada perubahan dari 12, 425 gram karbon menjadi CO 2 pada, suhu reaksi yang semula 30°C, terjadi kenaikan suhu sebesar 0, 484°C. Apabila kapasitas kalorimeter 200 Kkal/o. C. Berapa ΔH tiap mol karbon yang dibakar ? Jawab : C + O 2 CO 2 Kalor reaksi pada reaksi di atas = Kapasitas kalorimeter x Δt mol C 200 Kkal/°C x 0, 484 °C 12, 425 gr/12, 01 gr/mol = 93, 414 Kkal/mol Pada pembakaran 1 mol C dibebaskan/dihasilkan panas 93, 414 Kkal. Jadi ΔH = - 93, 414 Kkal (reaksi eksotermal) 17

HUKUM HESS Bunyi HUKUM HESS : “Kalor reaksi dari suatu reaksi tidak bergantung apakah reaksi tersebut berlangsung satu tahap atau beberapa tahap” KEPENTINGAN : Hukum Hess sangat penting dalam perhitungan kalor reaksi yang tidak dapat ditentukan secara eksperimen. Contoh reaksi : 1. Reaksi langsung A B ΔH 1 = x Kkal 2. Secara tidak langsung ΔH 2 = b Kkal a) lewat C A C C B ΔH 3 = c Kkal 18
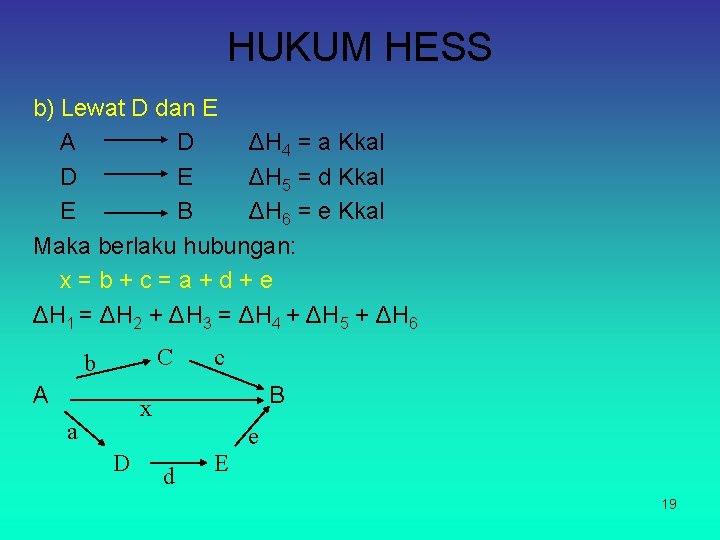
HUKUM HESS b) Lewat D dan E A D ΔH 4 = a Kkal D E ΔH 5 = d Kkal E B ΔH 6 = e Kkal Maka berlaku hubungan: x=b+c=a+d+e ΔH 1 = ΔH 2 + ΔH 3 = ΔH 4 + ΔH 5 + ΔH 6 C b A c B x a D d E e 19
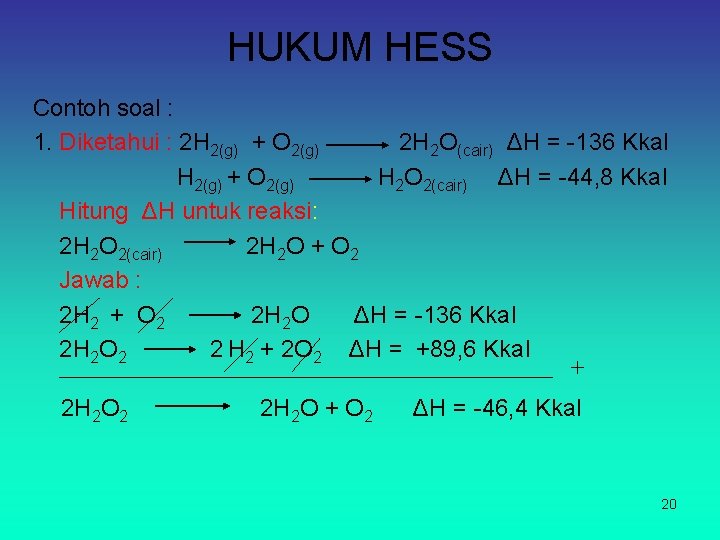
HUKUM HESS Contoh soal : 1. Diketahui : 2 H 2(g) + O 2(g) 2 H 2 O(cair) ΔH = -136 Kkal H 2(g) + O 2(g) H 2 O 2(cair) ΔH = -44, 8 Kkal Hitung ΔH untuk reaksi: 2 H 2 O 2(cair) 2 H 2 O + O 2 Jawab : 2 H 2 + O 2 2 H 2 O ΔH = -136 Kkal 2 H 2 O 2 2 H 2 + 2 O 2 ΔH = +89, 6 Kkal + 2 H 2 O 2 2 H 2 O + O 2 ΔH = -46, 4 Kkal 20

HUKUM HESS 2. Diketahui : I. C + O 2 II. H 2 + ½ O 2 III. 2 C + 3 H 2 CO 2 H 2 O C 2 H 6 ΔH = - 94 Kkal ΔH = - 68 Kkal ΔH = - 20 Kkal Ditanyakan : berapa x pada reaksi : C 2 H 6 + 7/2 O 2 2 CO 2 + 3 H 2 O ΔH = x Kkal Jawab : I. 2 C + 2 O 2 2 CO 2 ΔH = -188 Kkal II. 3 H 2+ 3/2 O 2 3 H 2 O ΔH = - 204 Kkal III. C 2 H 6 2 C + 3 H 2 ΔH = 20 Kkal C 2 H 6 + 7/2 O 2 2 CO 2 + 3 H 2 O ΔH = - 372 Kkal, maka x = -372 Kkal. + ΔH = -372 Kkal 21

HUKUM PERTAMA TERMODINAMIKA Hukum I Termodinamika : Hukum kekekalan massa dan energi, yaitu : energi tidak dapat diciptakan dimusnahkan hanya dapat diubah ke bentuk yang lain. Secara matematis dirumuskan sbb : 1. Bilamana dalam suatu sistim terjadi perubahan energi, maka besarnya perubahan energi ini ditentukan oleh dua faktor : a. energi panas yang diserap (q) b. usaha (kerja) yang dilakukan oleh sistim (w) Untuk sistim yang menyerap panas → q : positip (+) Untuk sistim yang mengeluarkan panas → q : negatif (-) 22

HUKUM PERTAMA TERMODINAMIKA Untuk sistim yang melakukan usaha (kerja) → w : positif Jika usaha dilakukan terhadap sistim → w : negatif Energi sistim akan naik apabila : q (+) dan w (-) Energi sistim akan berkurang apabila : q (-) dan w (+) Berlaku : ΔE = q – w ΔE q w = perubahan energi = energi panas yang diserap = usaha yang dilakukan oleh sistim 23

HUKUM PERTAMA TERMODINAMIKA - Suatu usaha dilakukan oleh sistim apabila terjadi perubahan volume pada tekanan tetap. w = P. ΔV Jadi ΔE = q - P. ΔV → P = tekanan ΔV = perubahan volume - Jika sistim berlangsung pada V dan P tetap/konstan, maka ΔV = 0 dan w = 0, maka ΔE = qv (pada P dan V tetap) 2. Hubungannya dengan entalpi (H) Definisi entalpi : H = E + P. V 24

HUKUM PERTAMA TERMODINAMIKA - Jika P konstan, maka ΔH : ΔH = H 2 - H 1 = (E 2 + P 2. V 2) – ( E 1 + P 1. V 1) = (E 2 - E 1) – (P 2. V 2 - P 1. V 1) = (E 2 - E 1) + P (V 2 – V 1) ΔH = ΔE + P. ΔV Karena ΔE = qp – P. ΔV, maka : ΔH = qp- P. ΔV + P. ΔV ΔH = qp Jadi perubahan entalpi = perubahan panas/kalor yang terjadi pada (P & T tetap) 25

HUKUM PERTAMA TERMODINAMIKA Jika V konstan (ΔV = 0), maka ΔH : ΔH = H 2 - H 1 =(E 2 + P 2. V 2) – ( E 1 + P 1. V 1) = (E 2 - E 1) – (P 2. V 2 - P 1. V 1) = (E 2 - E 1) + (P 2 – P 1) V ΔH = ΔE + ΔP. ΔV Karena : ΔE = qv dan ΔV = 0, maka ΔH = qv Jadi perubahan entalpi sama dengan perubahan panas yang terjadi pada (V & T tetap). 26

HUKUM PERTAMA TERMODINAMIKA 3. PENGUKURAN ΔH DAN ΔE a. Untuk reaksi-reaksi yang tidak ada perubahan volume berlaku ΔH = ΔE Reaksi-reaksi yang berlangsung tanpa perubahan volume, adalah : - Reaksi-reaksi gas yang tidak mengalami perubahan koefisien reaksi (koefisien sebelum = sesudah reaksi) Contoh : H 2(g) + Cl 2(g) → 2 HCl(g) - Reaksi – reaksi dalam larutan atau zat padat ( sebenarnya terjadi perubahan volume, tetapi sangat kecil dan diabaikan. 27

HUKUM PERTAMA TERMODINAMIKA b. Reaksi-reaksi gas yang mengalami perubahan jumlah molekul Dari persamaan gas ideal : PV = n. RT P. ΔV = Δn. RT Dari ΔH = ΔE + P. ΔV maka : ΔH = ΔE + Δn. RT Keterangan : ΔH = perubahan entalpi ΔE = perubahan energi Δn = perubahan jumlah molekul R = tetapan gas umum : 1, 987 kalori/mol. K 28

HUKUM PERTAMA TERMODINAMIKA Contoh : N 2 + 3 H 2 → 2 NH 3, maka Δn = 2 – (1 + 3) = -2 Contoh soal : 1. Pada reaksi : N 2 + 3 H 2 → 2 NH 3. Besarnya ΔE = -25, 4 Kkal/mol pada suhu 250 C. Ditanyakan : ΔH. Jawab : N 2 + 3 H 2 → 2 NH 3. Δn = 2 – (1 + 3) = -2 ΔH = ΔE + Δn. RT = -25, 4 Kkal/mol + (-2). (1, 987 kal/mol. K)(273 + 25)K = (-25. 400 – 1184, 252) kal/mol = -26. 584, 252 kal/mol = -26, 58 Kkal/mol 29

HUKUM PERTAMA TERMODINAMIKA 2. 1, 5 mol gas etilen (C 2 H 2) dibakar sempurna dalam kalorimeter pada suhu 250 C, energi panas yang dihasilkan 186 Kkal. Ditanyakan ΔH pada suhu tersebut. Jawab : C 2 H 2(g) + 5/2 O 2(g) → 2 CO 2(g) + H 2 O(cair) Δn = 2 – (1 + 5/2) = - 3/2 ΔE = - 186 Kkal /1, 5 mol = -124 Kkal/mol ΔH = ΔE + Δn. RT = -124. 000 kal/mol + (-3/2 x 1, 987 kal/mol. K x 298 K) = (-124. 000 – 1566, 078) kal/mol = - 125. 566, 078 kal/mol = -125, 566 Kkal/mol 30

HUKUM KEDUA TERMODINAMIKA HK. II. TERMODINAMIKA : • TIDAK DIRUMUSKAN SECARA MATEMATIS • DITERANGKAN BEBERAPA PERISTIWA YANG BERHUBUNGAN DENGAN HK KEDUA TERMODINAMIKA 1. Proses Spontan dan Tak Spontan Proses Spontan : proses yang dapat berlangsung dengan sendirinya dan tidak dapat balik tanpa pengaruh dari luar. Contoh : a. Panas, selalu mengalir dari temperatur tinggi ke tem peratur rendah. b. Gas mengalir dari tekanan tinggi ke tekanan rendah 31

HUKUM KEDUA TERMODINAMIKA c. Air mengalir dari tempat yang tinggi ke tempat yang rendah. Manfaat Proses Spontan : • Energi panas dapat menggerakkan mesin panas • Ekspansi gas dapat menggerakkan piston (motor bakar) • Air terjun untuk menggerakkan turbin listrik. Proses tak spontan : proses yang tidak dapat berlangsung tanpa pengaruh dari luar. Contoh : panas tak dapat mengalir dari suhu rendah ke suhu tinggi tanpa pengaruh dari luar. 32

HUKUM KEDUA TERMODINAMIKA • Semua proses spontan berlangsung dari energi potensial tinggi ke energi potensial yang lebih rendah • Reaksi kimia akan berlangsung secara spontan apabila reaksinya eksoterm. Jadi diikuti penurunan entalpi. Untuk hal ini entalpi sebagai energi potensial kimia. • Jika entalpi reaktan lebih tinggi dari entalpi zat hasil, sehingga ΔH negatif, maka reaksi bersifat spontan. • Reaksi endoterm dapat juga berlangsung spontan. Prosesnya berlangsung terus hingga tercapai keadaan setimbang. contoh : air menguap secara spontan ke atmosfer. Jumlah air yang menguap = uap yang kembali mengembun. 33

HUKUM KEDUA TERMODINAMIKA • Reaksi yang dapat balik juga dapat terjadi secara spontan. Contoh : H 2 bereaksi dengan Cl 2 membentuk HCl. Sebaliknya HCl akan terurai menjadi H 2 dan Cl 2 sampai terjadi keadaan setimbang. • Proses menuju ke keadaan setimbang juga merupakan proses spontan. • Kesimpulan : Semua perubahan spontan berlangsung dengan arah tertentu. ENTROPI (s) • Selain perubahan entalpi, perubahan kimia maupun fisika melibatkan perubahan dalam kekacaubalauan (disorder) relatif dari atom-atom, molekul-molekul ataupun ion-ion. Kekacaubalauan (ketidakteraturan) suatu sistim disebut ENTROPI. 34

HUKUM KEDUA TERMODINAMIKA Contoh : • Gas yang diwadahi dalam suatu labu 1 L memiliki entropi lebih besar daripada gas dengan kuantitas yang sama ditempatkan dalam labu 10 ml. • Natrium Klorida dalam bentuk ion-ion gas mempunyai entropi lebih tinggi daripada bentuk kristal padat. • Air (cair) pada suhu 0 o. C mempunyai entropi lebih tinggi dari pada es dengan temperatur yang sama. Jumlah entropi di alam semesta selalu meningkat Makin tidak teratur : S semakin meningkat. 35
- Slides: 35