ENZIM Enzim merupakan senyawa organik bermolekul besar yang
ENZIM

• Enzim merupakan senyawa organik bermolekul besar yang berfungsi untuk mempercepat jalannya reaksi metabolisme di dalam tubuh tumbuhan tanpa mempengaruhi keseimbangan reaksi • Enzim tidak ikut bereaksi, struktur enzim tidak berubah baik sebelum dan sesudah reaksi tetap • Enzim sebagai biokatalisator • Bagian enzim yang aktif adalah sisi aktif dari enzim

Tata nama enzim • Enzim diberi nama sesuai dengan nama substrat dan reaksi yang dikatalisis • Biasanya ditambah akhiran ase • Enzim dibagi ke dalam 7 golongan besar

Penamaan Enzim • Setiap enzim memiliki satu nama sistematik yang menunjukkan kelompok dan sub kelompok. Contoh laktat: NAD oksidoreduktase, mempunyai nomor sistematik 1. 1. 1. 27. Angka pertama menunjukkan bahwa enzim itu termasuk kelompok satu yaitu oksidoreduktase. Angka kedua menunjukkan sub kelompok yaitu gugus kimia yang diubah – CHOH. Angka ketiga menunjukkan sub-sub kelompoknya yang menunjukkan bahwa NAD atau NADP sebagai hidrogen akseptor.

Lanjutan Penamaan Enzim • Angka keempat menunjukkan enzim. • Selain nama sistematik, juga dikenal nama trivial yang lebih pendek dan lebih mudah dibanding nama sistematik, contoh enzim di atas lebih umum dikenal sebagai laktat dehidrogenase.

Kelas Tipe reaksi Oksidoreduktase (nitrat reduktase) memisahkan dan menambahkan elektron atau hidrogen Transferase (Kinase) memindahkan gugus senyawa kimia Hidrolase (protease, lipase, amilase) memutuskan ikatan kimia dengan penambahan air Liase (fumarase) membentuk ikatan rangkap dengan melepaskan satu gugus kimia Isomerase (epimerase) mengkatalisir perubahan isomer Ligase/sintetase (tiokinase) menggabungkan dua molekul yang disertai dengan hidrolisis ATP Polimerase (tiokinase) menggabungkan monomer-monomer sehingga terbentuk polimer

Golongan Enzim Utama 1. 2. 3. 4. 5. 6. 7. Oksidoreduktase, mengkatalisis reaksi reduksi oksidasi. Donor hidrogen atau donor elektron adalah satu substratnya. Transferase, mengkatalisis reaksi transfer (pemindahan) gugus. Dengan bentuk umum A - X + B, A + B -X Hidrolase, mengkatalisis reaksi hidrolisis. Pada C-C, C-N, C -O, dan ikatan lainnya. Lyase, pemutusan (bukan hidrolitik) Pada C-C, C-N, C-O, dan ikatan lainnya, menyisakan ikatan rangkap dua; atau, penambahan gugus pada ikatan rangkap dua. Isomerase, perubahan, susunan geometris (spasial) pada suatu molekul. Lygase, mengkatalisis reaksi penggabungan dua molekul. Polimerase, menggabungkan monomer-monomer

Susunan enzim • Komponen utama enzim adalah protein • Tidak semua protein bertindak sebagai enzim

Istilah • Penyusun utama suatu enzim adalah molekul protein yang disebut Apoenzim. Agar berfungsi sebagaimana mestinya, enzim memerlukan komponen lain yang disebut kofaktor. • Kofaktor adalah komponen nonprotein berupa ion atau molekul. Berdasarkan ikatannya, kofaktor dapat dibagi menjadi tiga kelompok, yaitu gugus prostetik, koenzim, dan ion-ion anorganik • Gugus prostetik merupakan tipe kofaktor yang terikat kuat pada enzim. berperan memberi kekuatan tambahan terhadap kerja enzim. Contohnya : heme, yaitu molekul berbentuk cincin pipih yang mengandung besi. Heme merupakan gugus prostetik sejumlah enzim, antara lain katalase, peroksidase, dan sitokrom oksidase. • Koenzim merupakan kofaktor yang terdiri atas molekul organik nonprotein yang terikat renggang dengan enzim. • Koenzim berfungsi untuk memindahkan gugus kimia, atom, atau elektron dari satu enzim ke enzim yang lain. Contohnya, tiamin pirofosfat, NADP+, dan asam tetrahidrofolat. • Ion-ion anorganik merupakan kofaktor yang terikat dengan enzim atau substrat kompleks sehingga fungsi enzim lebih efektif. Contohnya, amilase dalam ludah akan bekerja lebih baik dengan adanya ion klorida dan kalsium. • Bagian protein dari enzim dinamakan apoenzim, sedangkan enzim yang lengkap dinamakan holoenzim.

Contoh koenzim 1. 2. 3. 4. 5. 6. NAD (koenzim 1) NADP (koenzim 2) FMN dan FAD Cytokrom: cytokrom a, a 3, b, b 6, c, dan f Plastoquinon, plastosianin, feredoksin ATP: senyawa organik berenergi tinggi, mengandung 3 gugus P dan adenin ribose
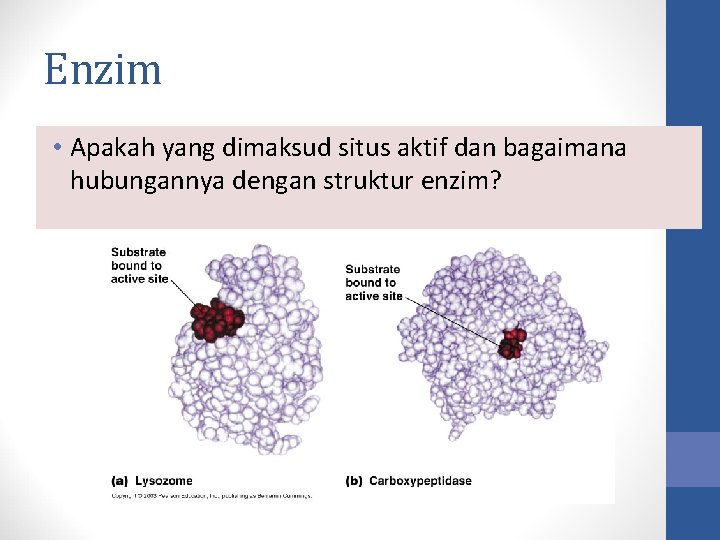
Enzim • Apakah yang dimaksud situs aktif dan bagaimana hubungannya dengan struktur enzim?
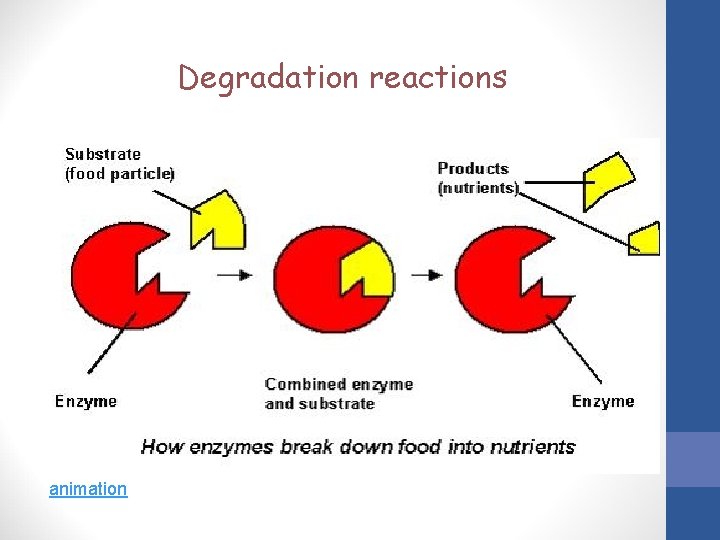
Degradation reactions animation

Degradation reactions Starch Maltose

Degradation reaction Substrate Enzyme Product Hydrogen Catalase peroxide Starch Amylase Oxygen and water Maltose Maltase Glucose Protein Pepsin Peptides Protease Amino acids Fats Lipase Fatty Acids and Glycerol
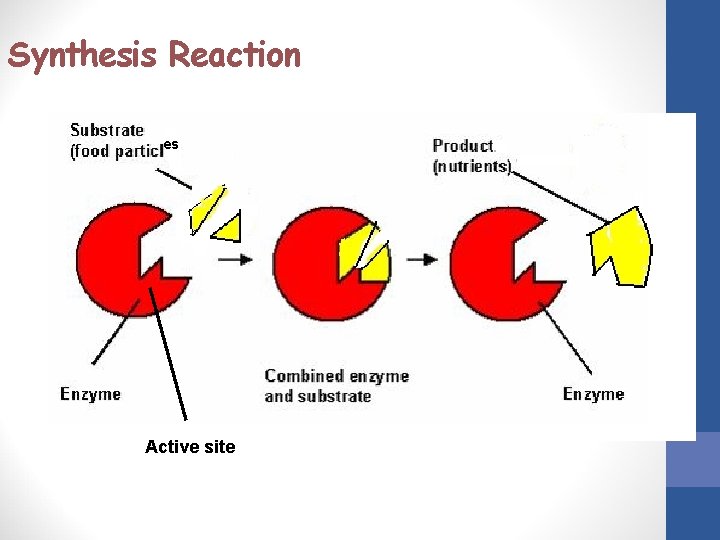
Synthesis Reaction es Active site
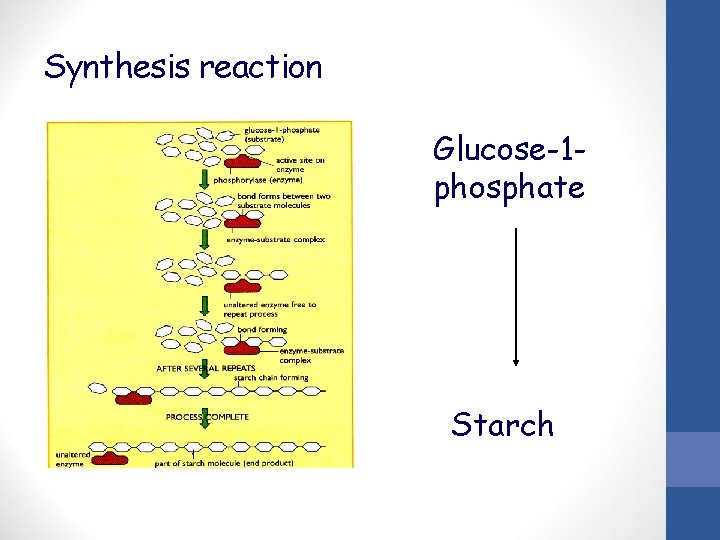
Synthesis reaction Glucose-1 phosphate Starch
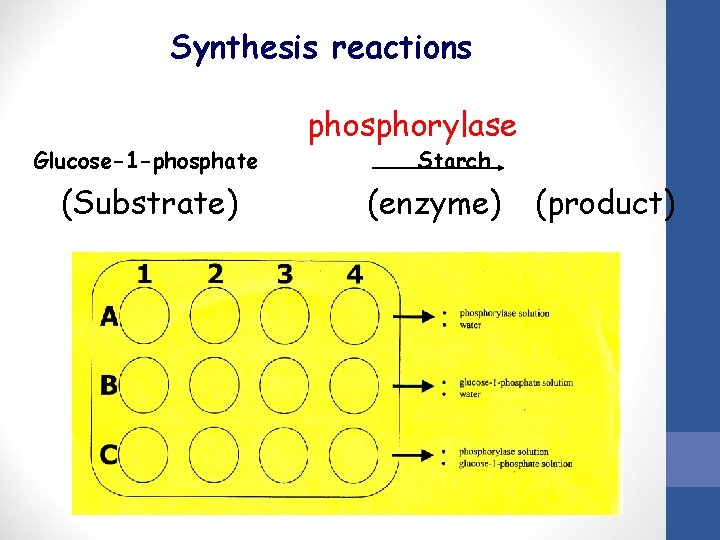
Synthesis reactions Glucose-1 -phosphate (Substrate) phosphorylase Starch (enzyme) (product)

Karakteristik Enzim • Enzim mempercepat reaksi kimia tetapi tidak mempengaruhi keseimbangan akhir. • Enzim hanya diperlukan dalam jumlah kecil untuk mengubah sejumlah besar molekul. • Enzim hanya akan berfungsi pada kondisi p. H, temperatur, konsentrasi substrat, kofaktor tertentu. • Enzim bersifat spesifik (khusus) artinya enzim hanya mengkatalisis reaksi dalam skala kecil atau dalam beberapa kasus hanya mengkatalis satu reaksi.
Faktor-Faktor yang Mempengaruhi Aktivitas Enzim Four Variables
Enzyme activity Enzyme Concentration Four Variables Substrate Concentration p. H Temperature

1. Pengaruh konsentrasi enzim Bila jumlah enzim dalam satu reaksi menjadi dua kali lipat maka jumlah substrat yang diubah menjadi produk (hasil) adalah dua kali lipat juga.
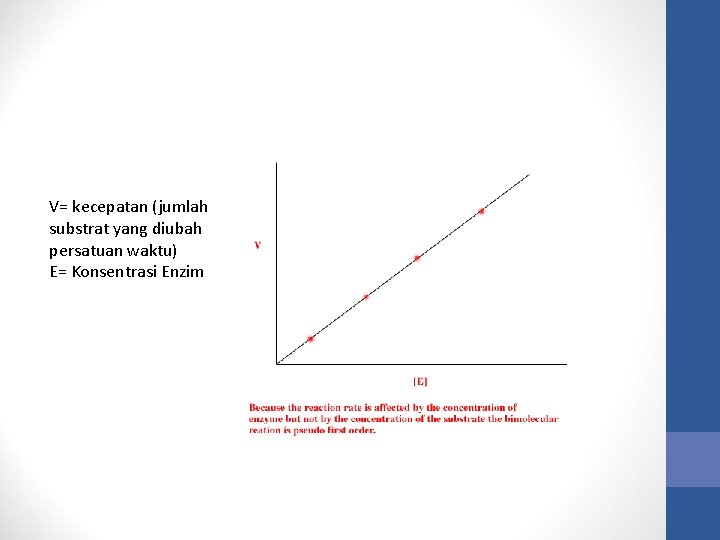
V= kecepatan (jumlah substrat yang diubah persatuan waktu) E= Konsentrasi Enzim

2. Pengaruh konsentrasi substrat Kecepatan sebanding dengan konsentrasi substrat. Jumlah substrat 2 kali lipat maka kecepatannya 2 kali lipat sampai waktu tertentu dengan catatan konsentrasi enzim tetap konstan.
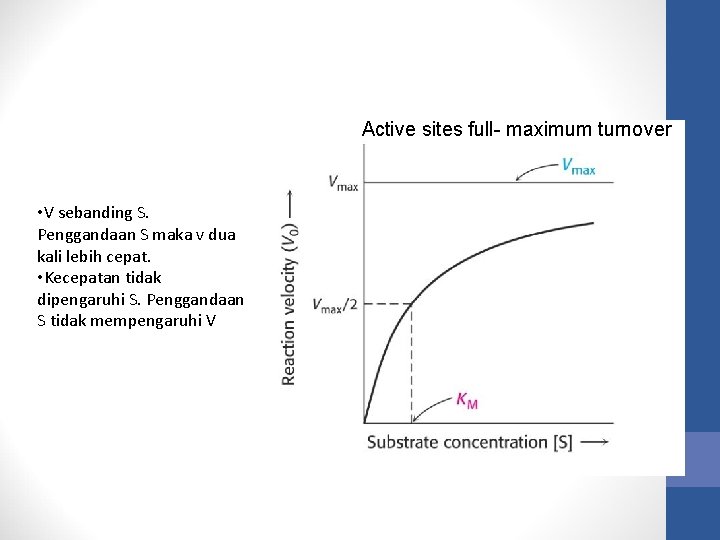
Active sites full- maximum turnover • V sebanding S. Penggandaan S maka v dua kali lebih cepat. • Kecepatan tidak dipengaruhi S. Penggandaan S tidak mempengaruhi V

Kompleks enzim substrat Aktivitas enzim tidak meningkat lagi pada konsentrasi substrat tertentu, Brown (1902) menduga bahwa enzim di dalam mengikat molekul substrat mempunyai kemampuan terbatas yaitu menjadi jenuh. Michaelis menten mengusulkan suatu persamaan yang didasarkan kepada asumsi sehingga memungkinkan diadakannya pengujian hipotesis. Salah satu asumsinya yaitu: E + S ↔ ES → E + P enzim + substrat ↔ Enzim substrat → Enzim + Produk

• Namun tidak semua reaksi enzim dapat dirumuskan seperti di atas. Pada beberapa peristiwa sering terdapat lebih dari satu kompleks ES (Enzim Substrat). Skema yang paling umum dituliskan sebagai berikut: E + S ↔ ES ‘↔ EP ↔ E + P Dimana ES adalah bahan antara yang tidak stabil, ES’ merupakan kompleks substrat yang diaktivasi dan EP merupakan kompleks Enzim Produk (hasil).

3. Pengaruh p. H • p. H ekstrim dapat mengakibatkan enzim mengalami denaturasi. Perubahan p. H yang tidak ekstrim mempengaruhi enzim secara temporer. Setiap enzim mempunyai p. H tertentu dimana enzim memiliki aktivitas maksimum p. H tersebut disebut p. H’ optimum untuk enzim tersebut
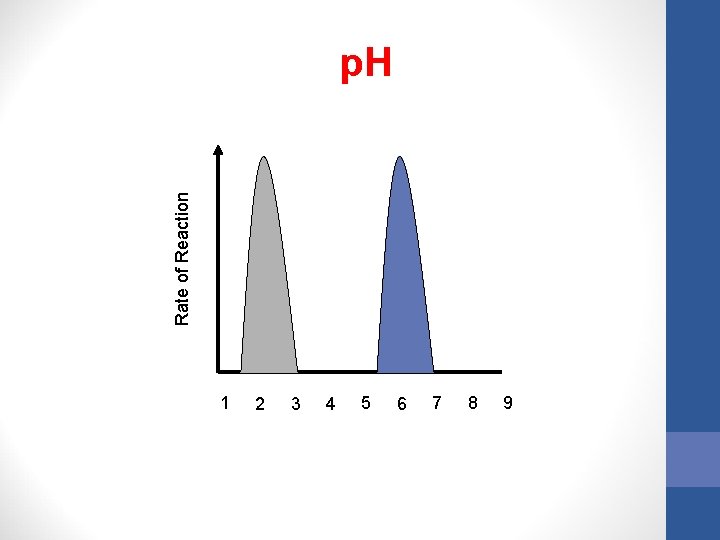
Rate of Reaction p. H 1 2 3 4 5 6 7 8 9
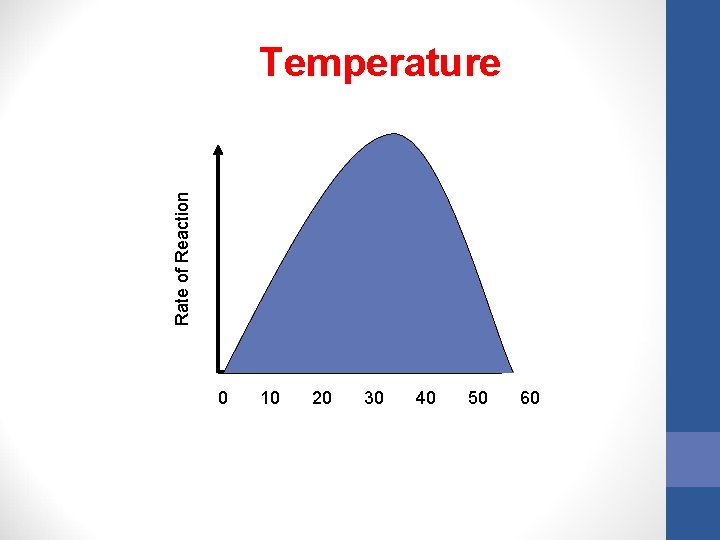
Rate of Reaction Temperature 0 10 20 30 40 50 60
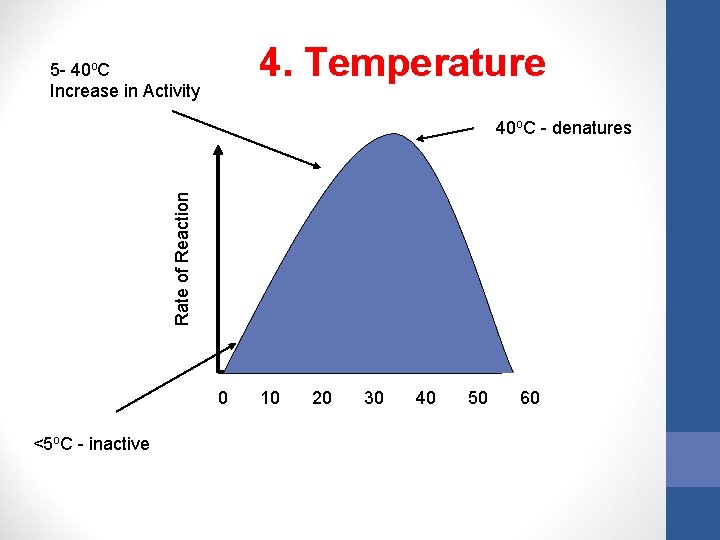
4. Temperature 5 - 40 o. C Increase in Activity Rate of Reaction 40 o. C - denatures 0 <5 o. C - inactive 10 20 30 40 50 60
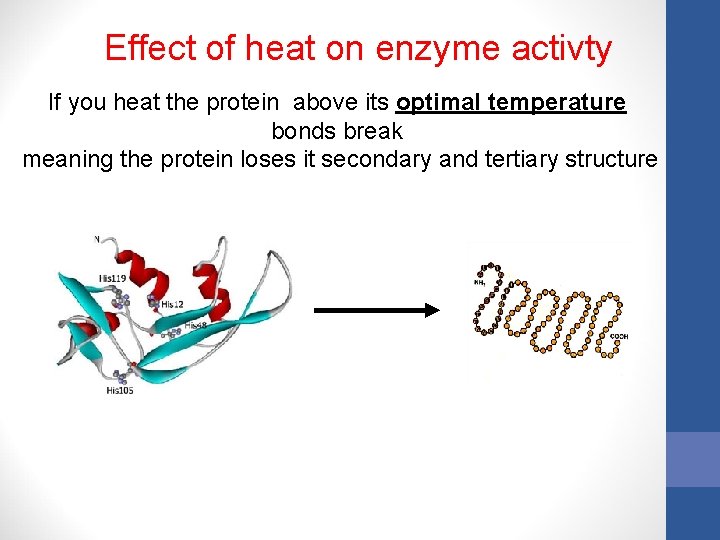
Effect of heat on enzyme activty If you heat the protein above its optimal temperature bonds break meaning the protein loses it secondary and tertiary structure
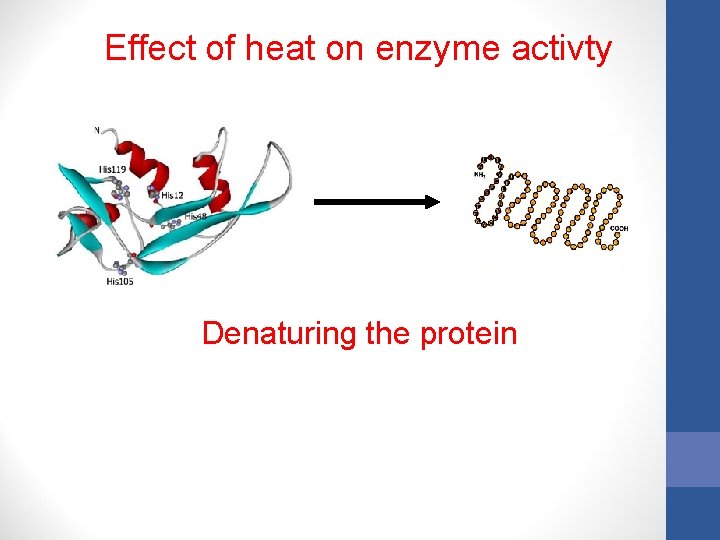
Effect of heat on enzyme activty Denaturing the protein

Effect of heat on enzyme activty Denaturing the protein ACTIVE SITE CHANGES SHAPE SO SUBSTRATE NO LONGER FITS Even if temperature lowered – enzyme can’t regain its correct shape
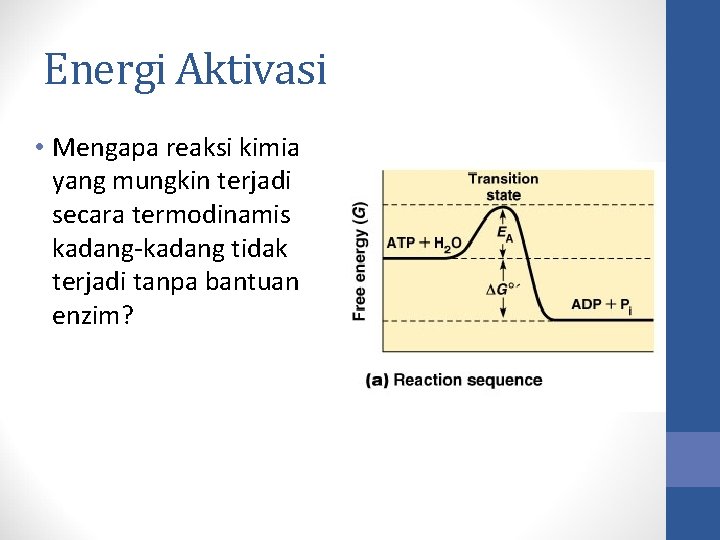
Energi Aktivasi • Mengapa reaksi kimia yang mungkin terjadi secara termodinamis kadang-kadang tidak terjadi tanpa bantuan enzim?

Energi Aktivasi • Bagaimana kecepatan reaksi dalam sel dapat ditingkatkan tanpa peningkatan suhu dan konsentrasi reaktan?
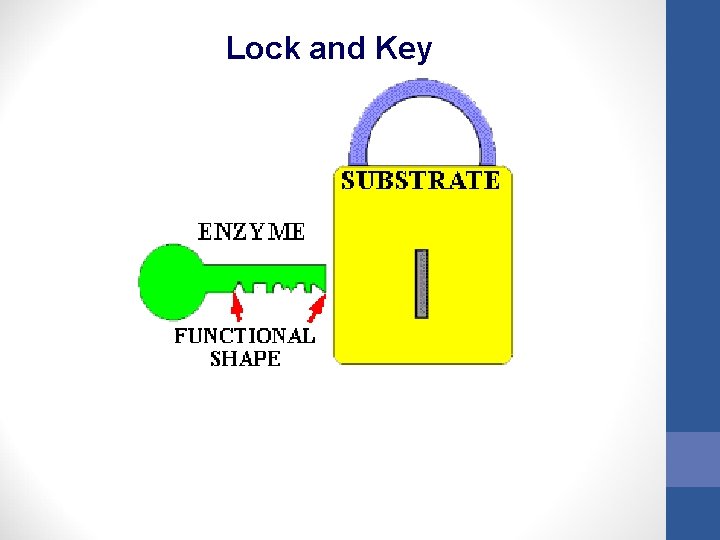
Lock and Key
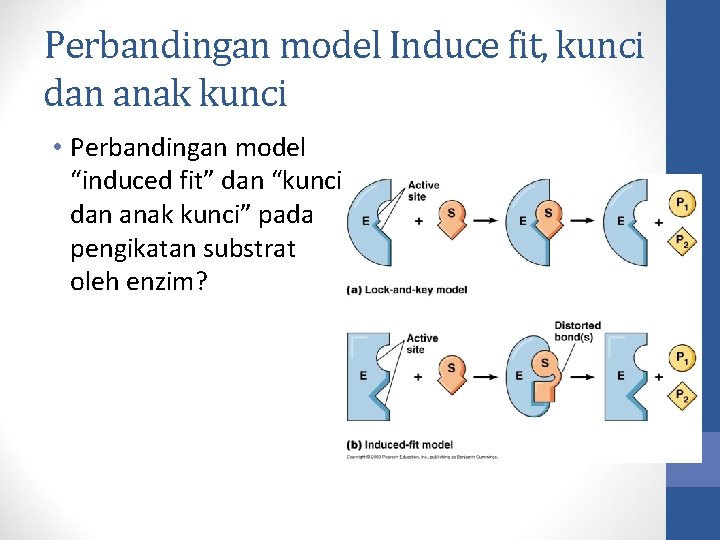
Perbandingan model Induce fit, kunci dan anak kunci • Perbandingan model “induced fit” dan “kunci dan anak kunci” pada pengikatan substrat oleh enzim?

Inhibitors • Inhibitor adalah bahan kimia yang mengurangi rata-rata reaksi enzim • Spesifik dan bekerja pada konsentrasi rendah • Memblok kerja enzim tp biasanya tidak merusak enzim • Banyak obat dan racun merupakan inhibitor

The effect of enzyme inhibition • Irreversible inhibitors: bergabung dengan kelompok asam amino di aktive site, tdk dapat balik Examples: nerve gases and pesticides, containing organophosphorus, combine with serine residues in the enzyme acetylcholine esterase

The effect of enzyme inhibition • Reversible inhibitors: dapat balik dengan cara dialisis There are two categories: 1) Competitive 2) Non Competitive
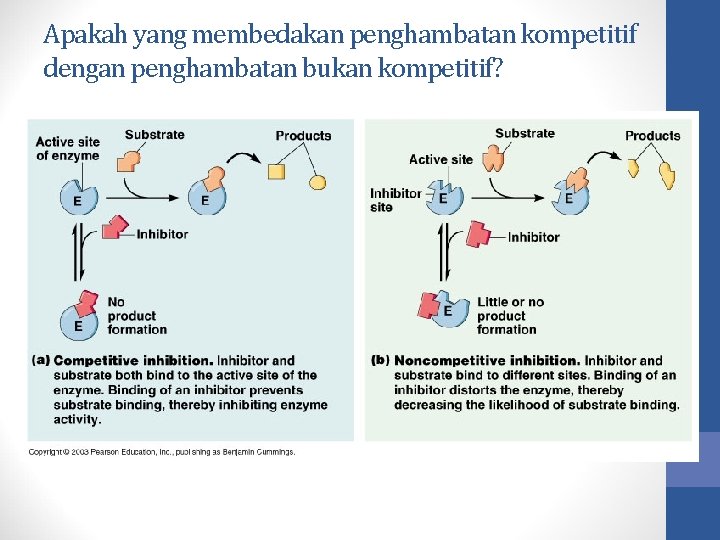
Apakah yang membedakan penghambatan kompetitif dengan penghambatan bukan kompetitif?

Aplikasi di TL • Mekanisme degradasi hidrokarbon aromatik Banyak senyawa ini digunakan sebagai donor elektron secara aerobik oleh bakteri Pseudomonas. Degradasi senyawa hidrokarbon aromatik disandikan dalam plasmid atau kromosom oleh gen xy/E. Gen ini berperan dalam produksi enzim katekol 2, 3 dioksigenase. Metabolisme senyawa ini oleh bakteri diawali dengan pembentukan protocatechuate atau catechol atau senyawa yang secara struktur berhubungan dengan senyawa ini. Kedua senyawa ini selanjutnya didegradasi oleh enzim katekol 2, 3 -dioksigenase menjadi senyawa yang dapat masuk ke dalam siklus Krebs (siklus asam sitrat), yaitu suksinat, asetil Ko. A, dan piruvat.

Aplikasi di TL • interaksi mikroba terhadap logam : 1. Mengikat ion logam yang ada di lingkungan eksternal pada permukaan sel serta membawanya ke dalam sel untuk berbagai fungsi sel. Contohnya : bakteri Thiobaccilus sp. Mampu menggunakan Fe dalam aktivasi enzim format dehidrogenase pada sitokrom. 2. Menggunakan logam sebagai donor atau akseptor elektron dalam metabolisme energi 3. Mengikat logam sebagai kation pada permukaan sel yang bermuatan negatif dalam proses yang disebut biosorpsi. Mikroba mengurangi bahaya pencemaran logam berat dapat dilakukan dengan cara detoksifikasi, dan bioakumulasi.
- Slides: 43