QUMICA ORGNICA Alcanos Acclicos Alquenos Alquinos Alifticos Alicclicos



























- Slides: 71

QUÍMICA ORGÁNICA

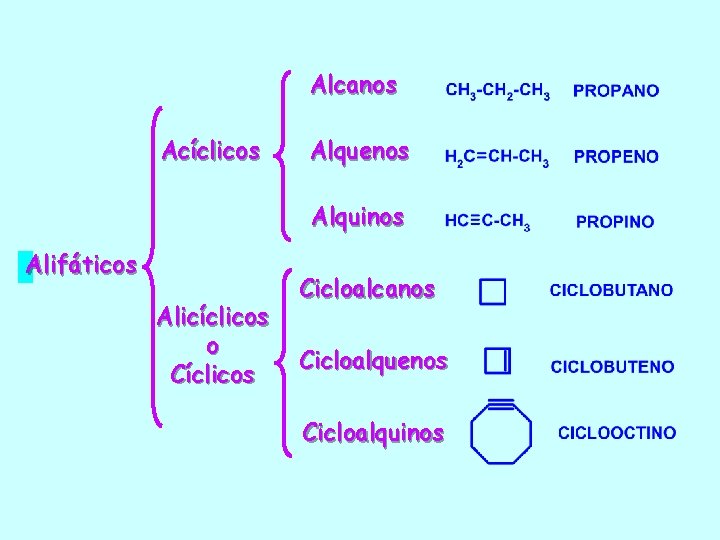
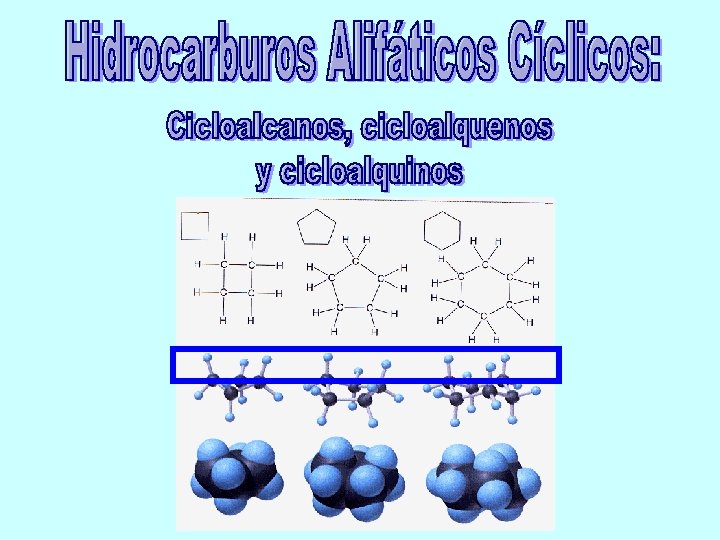
Alcanos Acíclicos Alquenos Alquinos Alifáticos Alicíclicos o Cíclicos Cicloalcanos Cicloalquenos Cicloalquinos

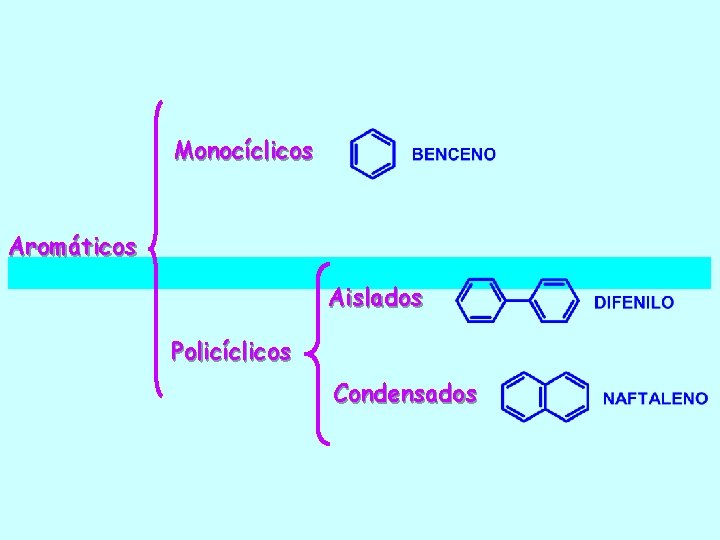
Monocíclicos Aromáticos Aislados Policíclicos Condensados

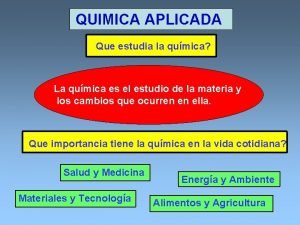
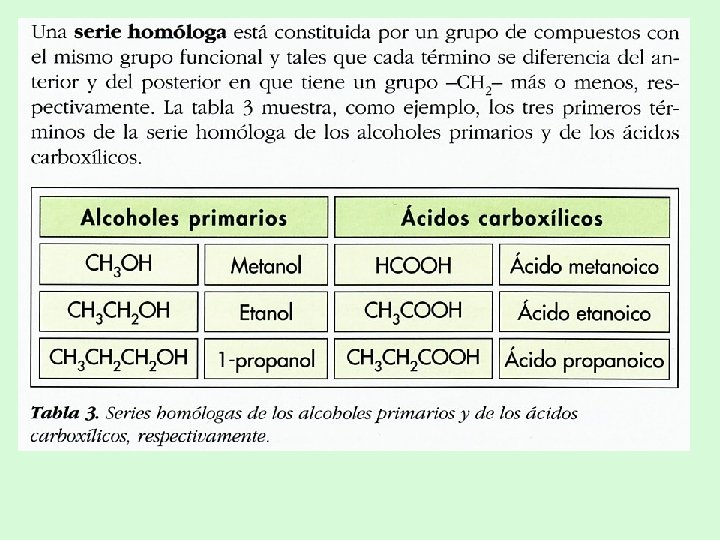
FORMULACIÓN ORGÁNICA Las sustancias orgánicas se clasifican en bloques que se caracterizan por tener un átomo o grupo atómico definido (grupo funcional) que le confiere a la molécula sus propiedades características. Al conjunto de sustancias que tienen el mismo grupo funcional se le llama función química. Una serie homóloga es el conjunto de compuestos orgánicos que tienen el mismo grupo funcional.


SUPER


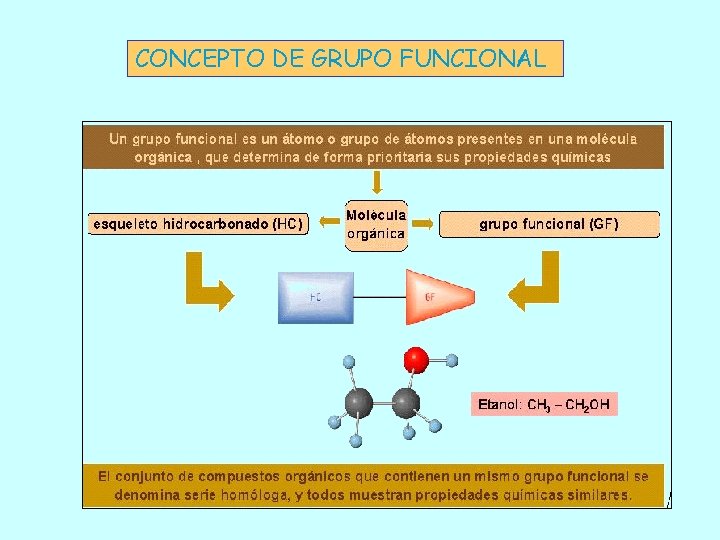
CONCEPTO DE GRUPO FUNCIONAL

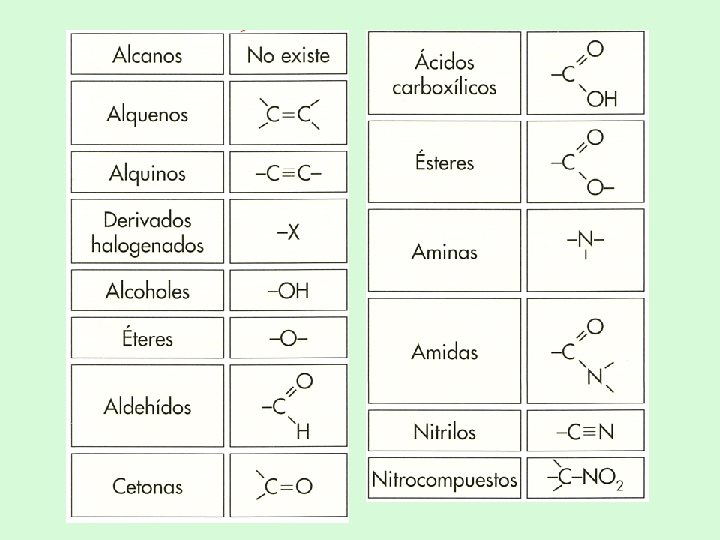
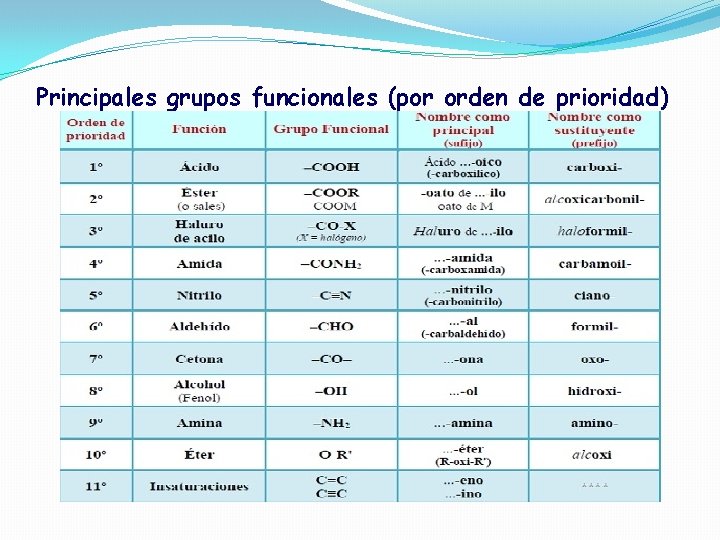
Principales grupos funcionales (por orden de prioridad)


Formulas

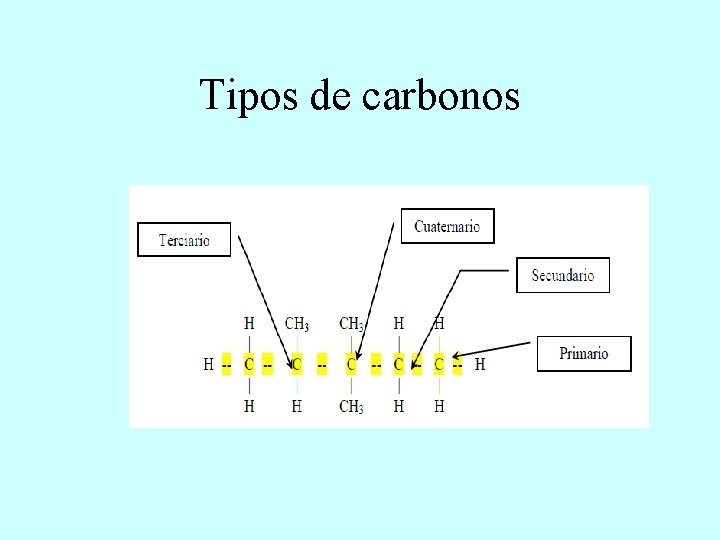
Tipos de carbonos

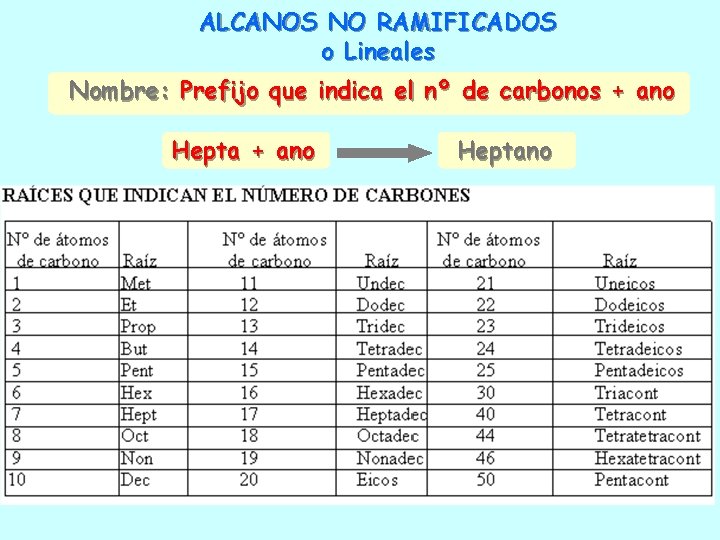
ALCANOS NO RAMIFICADOS o Lineales Nombre: Prefijo que indica el nº de carbonos + ano Heptano

ALCANOS NO RAMIFICADOS o Lineales Nombre: Prefijo que indica el nº de carbonos + ano Heptano

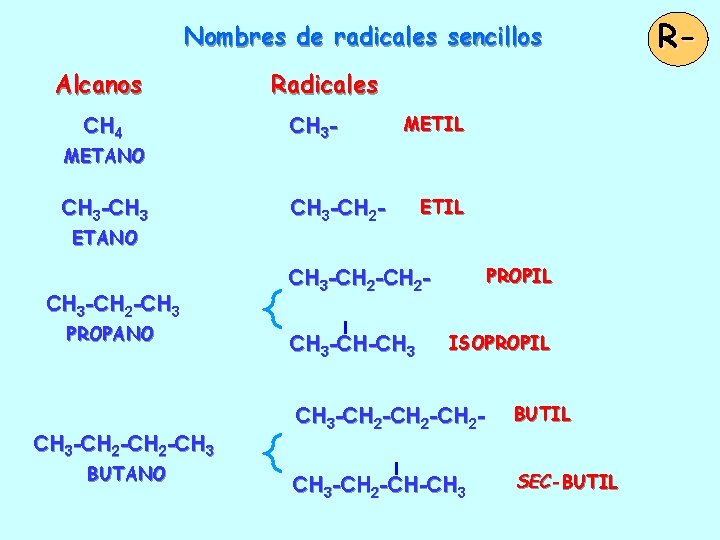
Nombres de radicales sencillos Alcanos CH 4 METANO CH 3 -CH 3 ETANO CH 3 -CH 2 -CH 3 PROPANO CH 3 -CH 2 -CH 3 BUTANO Radicales CH 3 - METIL CH 3 -CH 2 - ETIL PROPIL CH 3 -CH 2 CH 3 -CH-CH 3 ISOPROPIL CH 3 -CH 2 -CH 2 - BUTIL CH 3 -CH 2 -CH-CH 3 SEC-BUTIL R-

ISOMERÍA

Isomería estructural o plana. Las diferencias entre los isómeros se pueden ver en una representación plana. Isomería de cadena.

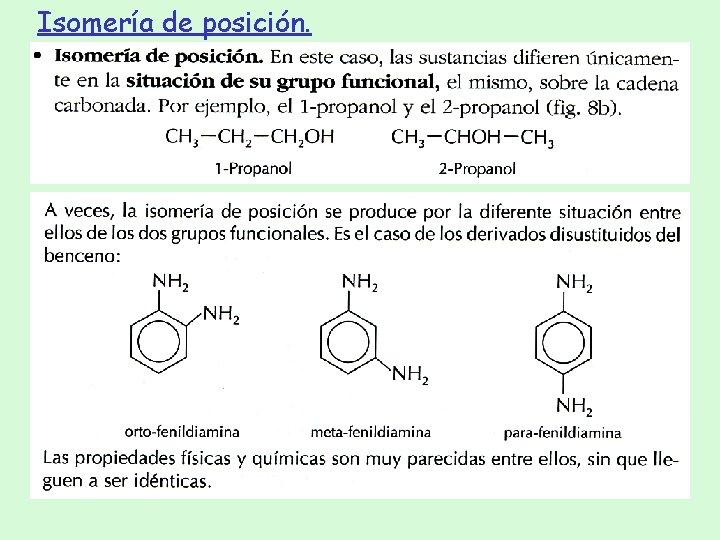
Isomería de posición.

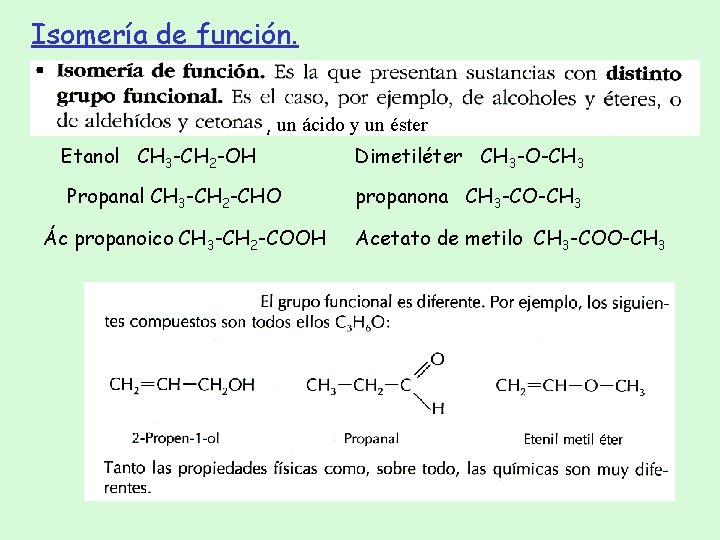
Isomería de función. , un ácido y un éster Etanol CH 3 -CH 2 -OH Dimetiléter CH 3 -O-CH 3 Propanal CH 3 -CH 2 -CHO propanona CH 3 -CO-CH 3 Ác propanoico CH 3 -CH 2 -COOH Acetato de metilo CH 3 -COO-CH 3

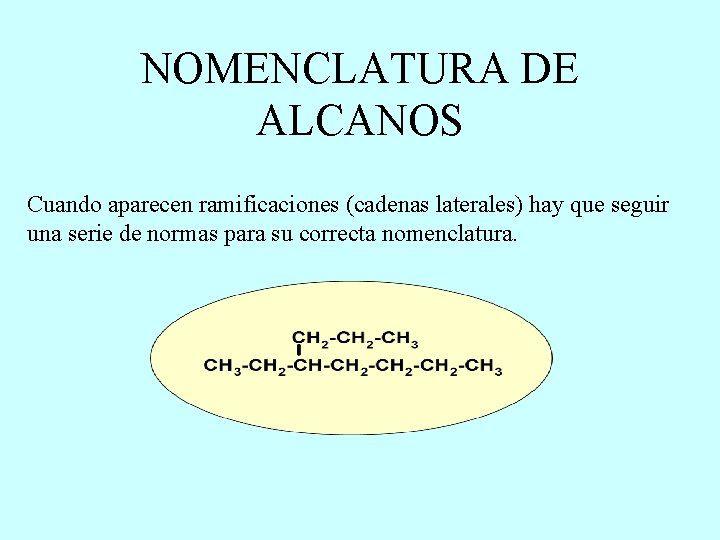
NOMENCLATURA DE ALCANOS Cuando aparecen ramificaciones (cadenas laterales) hay que seguir una serie de normas para su correcta nomenclatura.

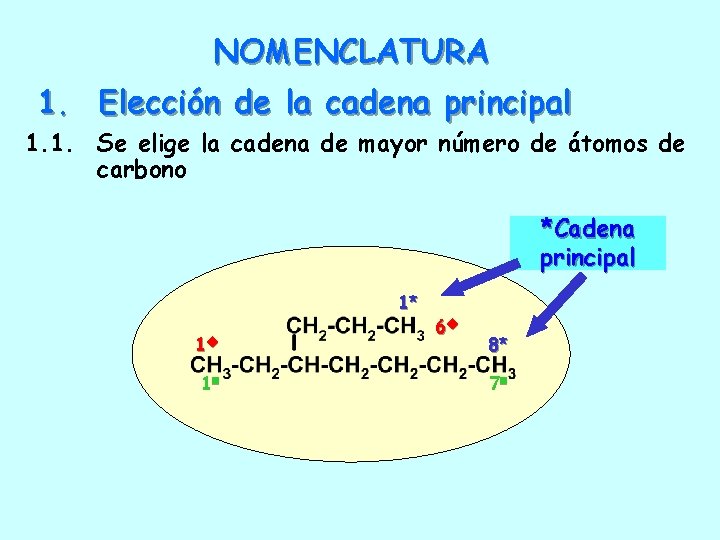
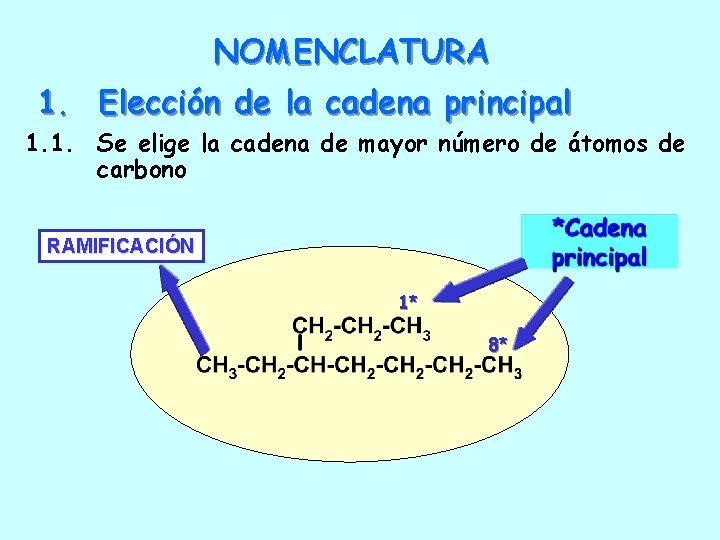
NOMENCLATURA 1. Elección de la cadena principal 1. 1. Se elige la cadena de mayor número de átomos de carbono *Cadena principal 1* 1 1 6 8* 7

NOMENCLATURA 1. Elección de la cadena principal 1. 1. Se elige la cadena de mayor número de átomos de carbono RAMIFICACIÓN 1* 8*

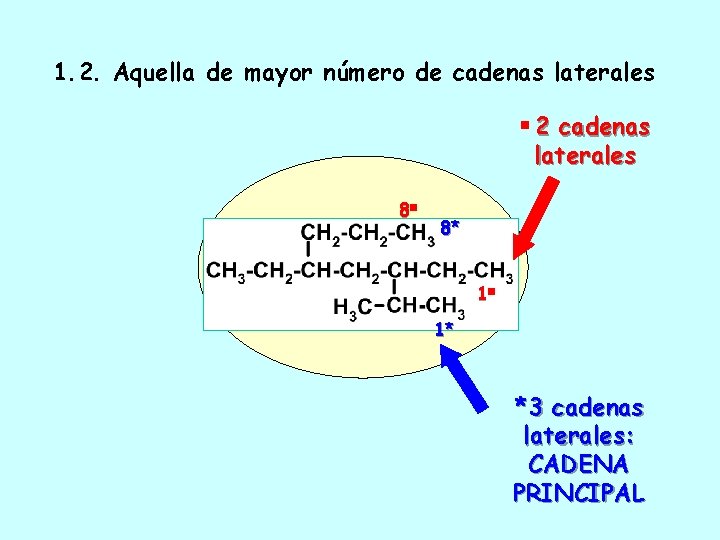
1. 2. Aquella de mayor número de cadenas laterales 8 2 cadenas laterales 8* 1 1* *3 cadenas laterales: CADENA PRINCIPAL

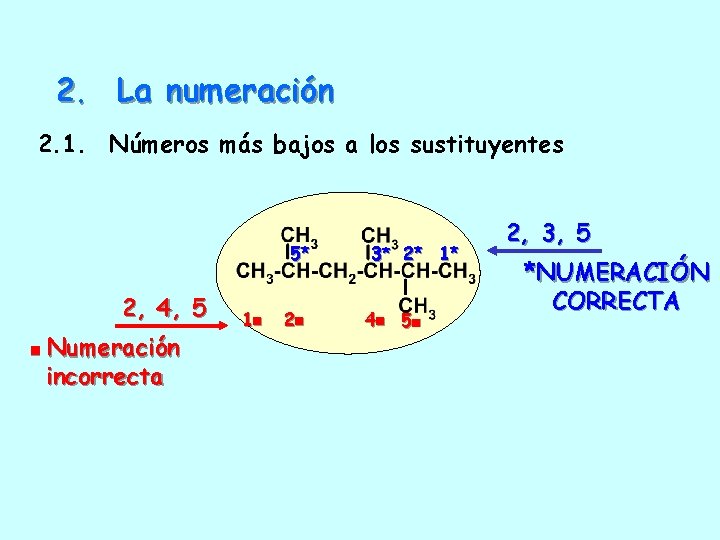
2. La numeración 2. 1. Números más bajos a los sustituyentes 5* 2, 4, 5 Numeración incorrecta 1 2 3* 2* 1* 4 5 2, 3, 5 *NUMERACIÓN CORRECTA

Si te dan la Formula

SI TE DAN EL NOMBRE

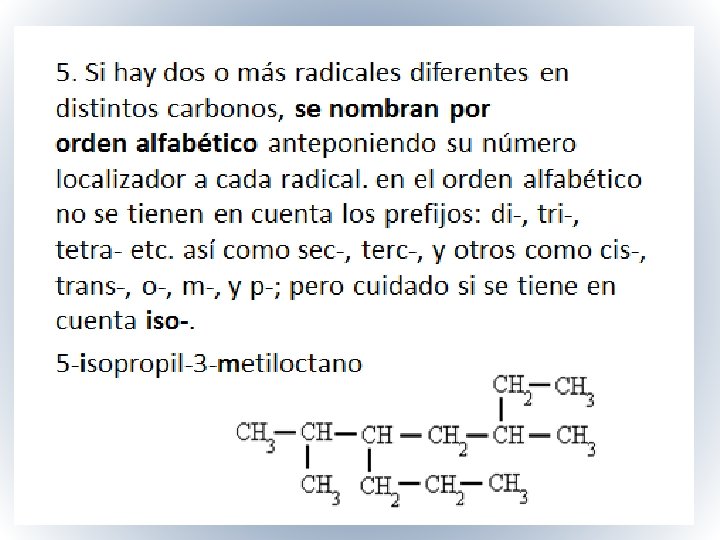
• Si un mismo átomo de carbono tiene dos radicales se pone el número localizador delante de cada radical y se ordenan por orden alfabético. • vhttp: //www. alonsoformula. com/organica/alca nos. htm


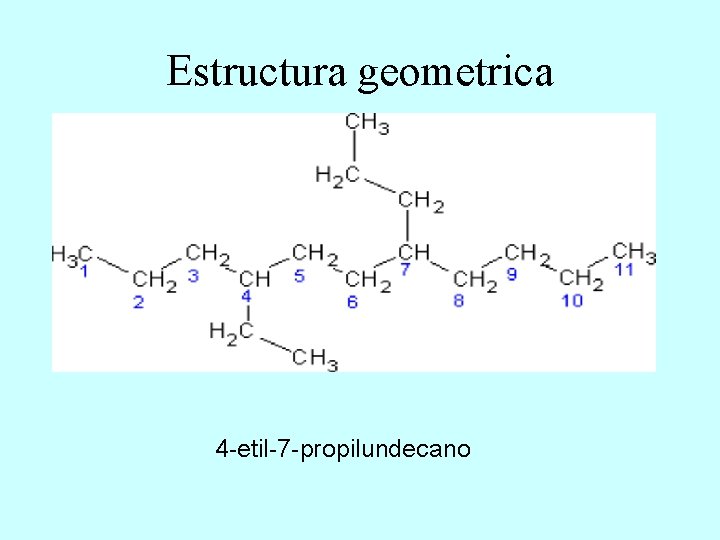
Estructura geometrica 4 -etil-7 -propilundecano

NOMENCLATURA DE HALOGENURO DE ALQUILO RX

SI TE DAN LA FORMULA

SI TE DAN EL NOMBRE


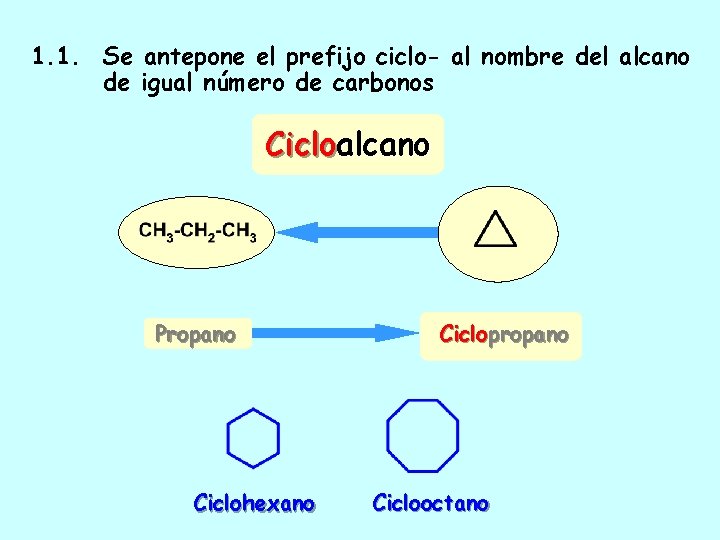
1. 1. Se antepone el prefijo ciclo- al nombre del alcano de igual número de carbonos Cicloalcano Propano Ciclohexano Ciclopropano Ciclooctano

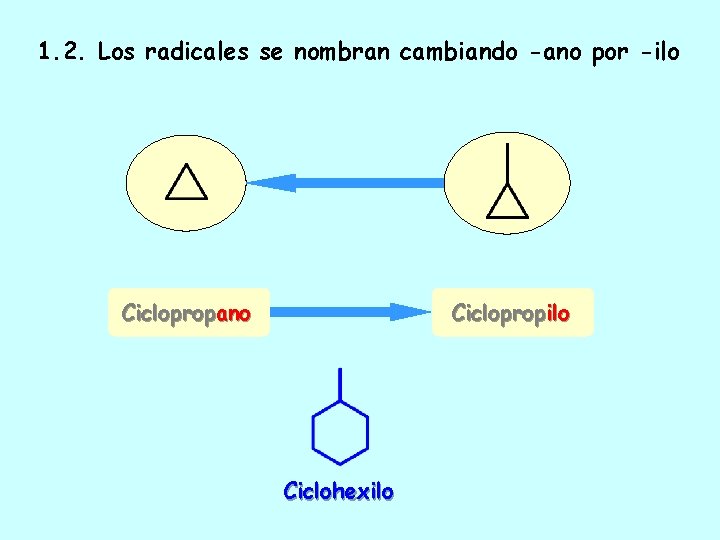
1. 2. Los radicales se nombran cambiando -ano por -ilo Ciclopropano Ciclopropilo Ciclohexilo

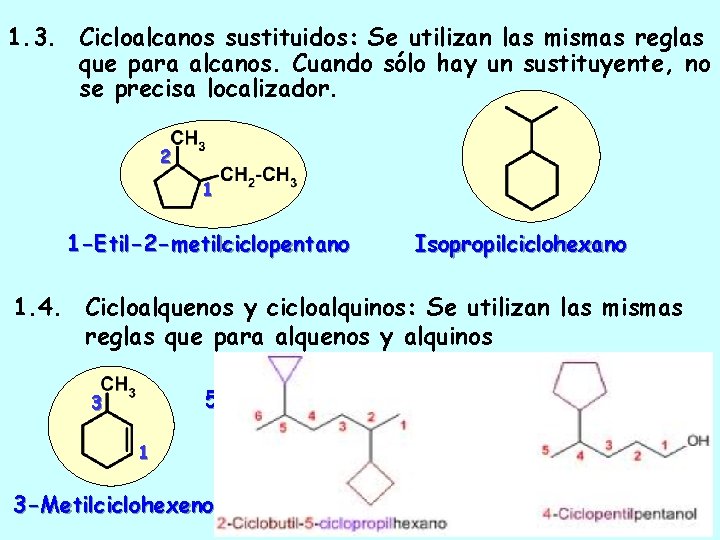
1. 3. Cicloalcanos sustituidos: Se utilizan las mismas reglas que para alcanos. Cuando sólo hay un sustituyente, no se precisa localizador. 2 1 1 -Etil-2 -metilciclopentano Isopropilciclohexano 1. 4. Cicloalquenos y cicloalquinos: Se utilizan las mismas reglas que para alquenos y alquinos 5 -Metilciclohe-1, 3 -dieno 3 3 1 3 -Metilciclohexeno 5 1 Metilideniclopentano

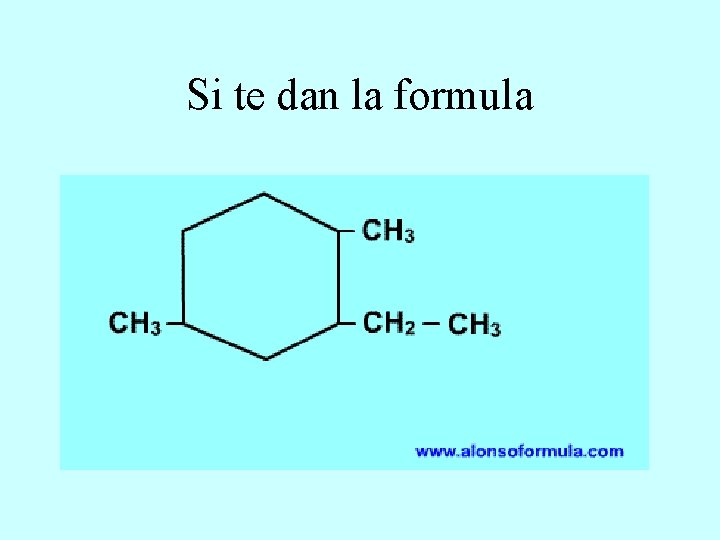
Si te dan la formula

Si te dan el Nombre

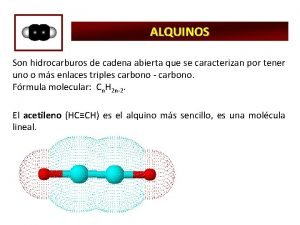
ALQUENOS Cn. H 2 n • Los alquenos son compuestos que contienen un doble enlace entre dos átomos de carbono (no saturado). Hibridación sp 2. • Propiedades físicas: Los alquenos, también llamados olefinas, sus propiedades son muy semejantes a las de los alcanos. Son insolubles en agua, solubles en disolventes no polares, son menos densos que el agua. Sus puntos de ebullición aumentan al aumentar el número de carbonos. A temperatura ambiente, C 1 A C 3 son gases, del alqueno C 4 A C 16 son líquidos, y del C 17 en adelante son sólidos.

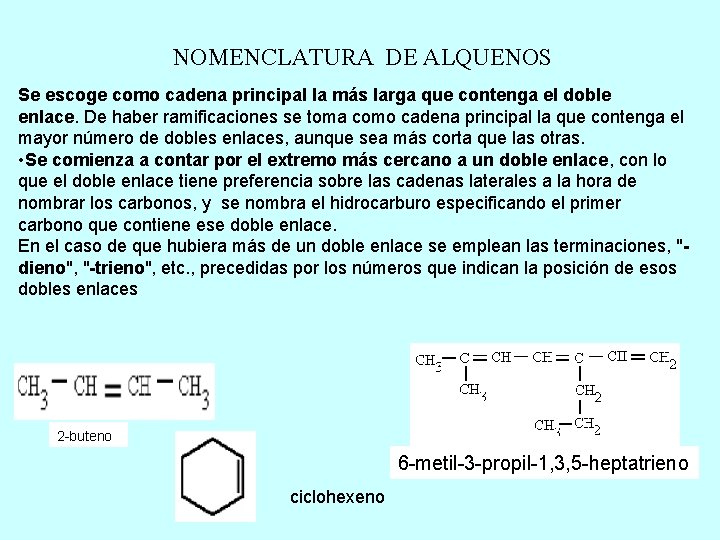
NOMENCLATURA DE ALQUENOS Se escoge como cadena principal la más larga que contenga el doble enlace. De haber ramificaciones se toma como cadena principal la que contenga el mayor número de dobles enlaces, aunque sea más corta que las otras. • Se comienza a contar por el extremo más cercano a un doble enlace, con lo que el doble enlace tiene preferencia sobre las cadenas laterales a la hora de nombrar los carbonos, y se nombra el hidrocarburo especificando el primer carbono que contiene ese doble enlace. En el caso de que hubiera más de un doble enlace se emplean las terminaciones, "dieno", "-trieno", etc. , precedidas por los números que indican la posición de esos dobles enlaces 2 -buteno 6 -metil-3 -propil-1, 3, 5 -heptatrieno ciclohexeno

Si nos dan la formula

Si nos dan el nombre

ALQUINOS Cn. H 2 n-2 • Compuestos que contienen un triple enlace entre dos átomos de carbono (no saturado). Hibridación sp. • Propiedades físicas: Son compuestos de baja polaridad, por lo que sus propiedades físicas son muy semejantes a la de los alquenos. Son insolubles en agua, solubles en disolventes no polares, son menos densos que el agua. Sus puntos de ebullición aumentan al aumentar el número de carbonos. A temperatura ambiente, los tres primeros términos son gases, los términos intermedios son líquidos y los superiores son sólidos

NOMENCLATURA DE ALQUINOS

Si te dan la formula

Si te dan el nombre

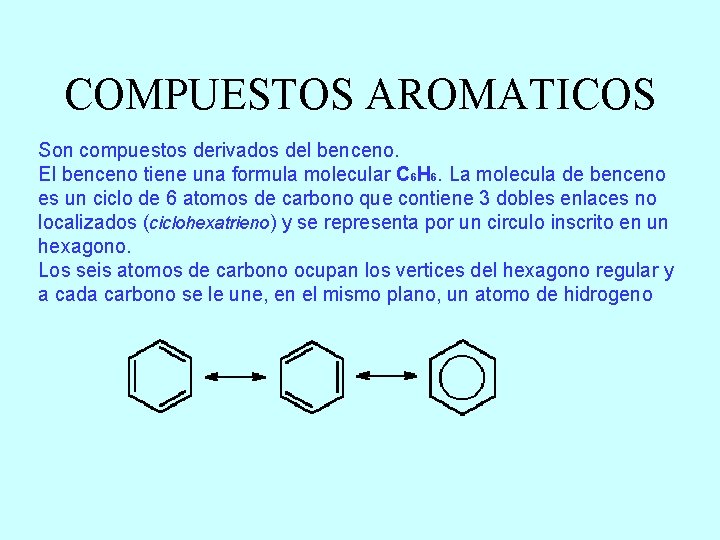
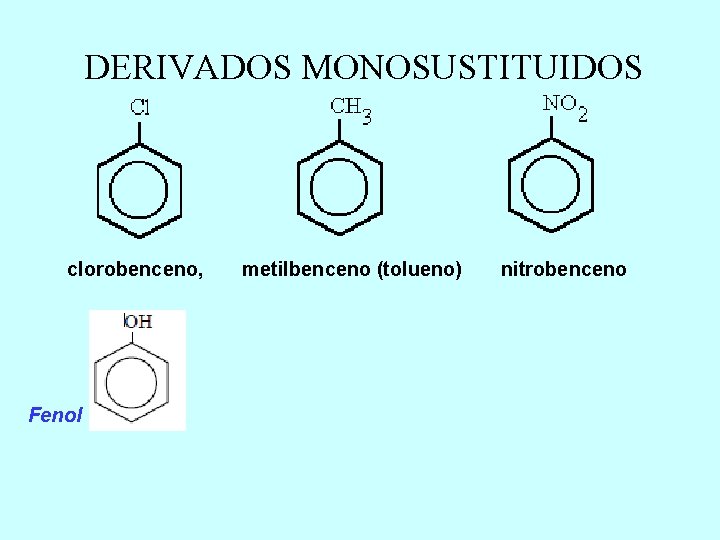
COMPUESTOS AROMATICOS Son compuestos derivados del benceno. El benceno tiene una formula molecular C 6 H 6. La molecula de benceno es un ciclo de 6 atomos de carbono que contiene 3 dobles enlaces no localizados (ciclohexatrieno) y se representa por un circulo inscrito en un hexagono. Los seis atomos de carbono ocupan los vertices del hexagono regular y a cada carbono se le une, en el mismo plano, un atomo de hidrogeno

DERIVADOS MONOSUSTITUIDOS clorobenceno, Fenol metilbenceno (tolueno) nitrobenceno

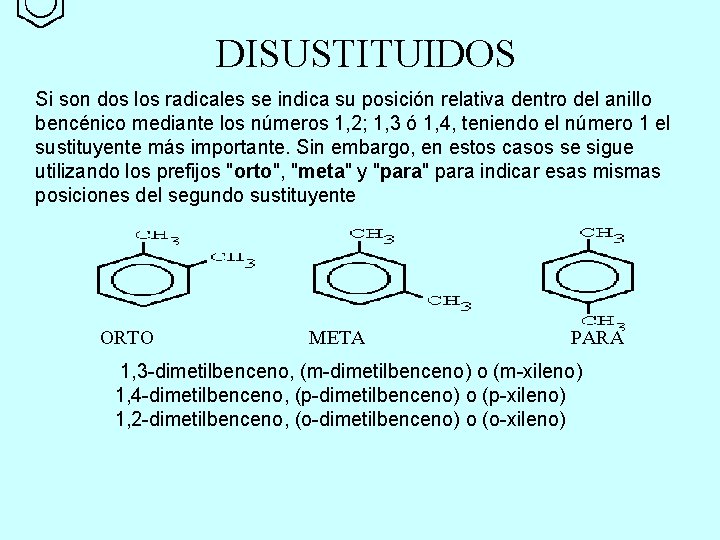
DISUSTITUIDOS Si son dos los radicales se indica su posición relativa dentro del anillo bencénico mediante los números 1, 2; 1, 3 ó 1, 4, teniendo el número 1 el sustituyente más importante. Sin embargo, en estos casos se sigue utilizando los prefijos "orto", "meta" y "para" para indicar esas mismas posiciones del segundo sustituyente ORTO META PARA 1, 3 -dimetilbenceno, (m-dimetilbenceno) o (m-xileno) 1, 4 -dimetilbenceno, (p-dimetilbenceno) o (p-xileno) 1, 2 -dimetilbenceno, (o-dimetilbenceno) o (o-xileno)

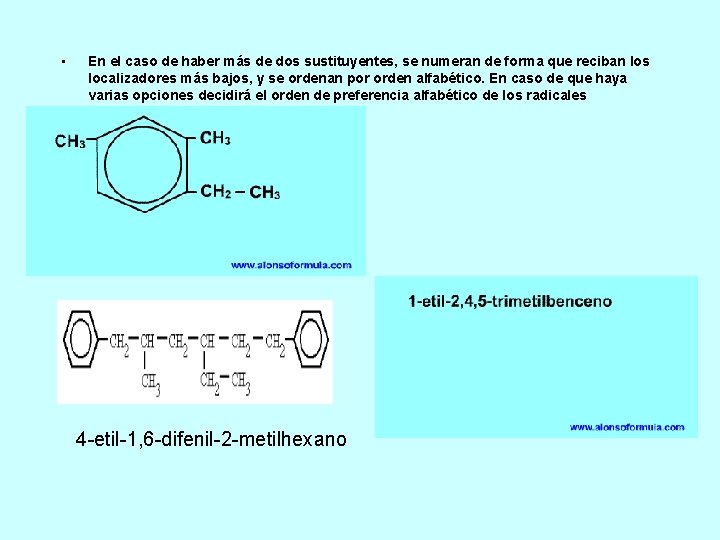
• En el caso de haber más de dos sustituyentes, se numeran de forma que reciban los localizadores más bajos, y se ordenan por orden alfabético. En caso de que haya varias opciones decidirá el orden de preferencia alfabético de los radicales 4 -etil-1, 6 -difenil-2 -metilhexano

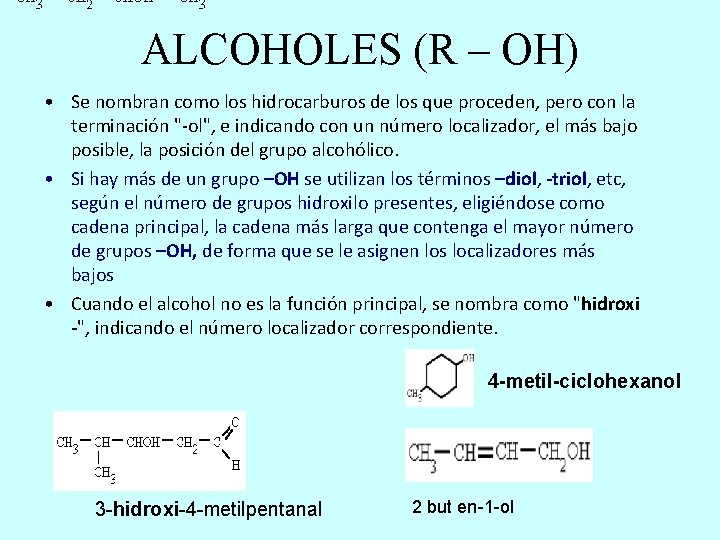
ALCOHOLES (R – OH) • Se nombran como los hidrocarburos de los que proceden, pero con la terminación "-ol", e indicando con un número localizador, el más bajo posible, la posición del grupo alcohólico. • Si hay más de un grupo –OH se utilizan los términos –diol, -triol, etc, según el número de grupos hidroxilo presentes, eligiéndose como cadena principal, la cadena más larga que contenga el mayor número de grupos –OH, de forma que se le asignen los localizadores más bajos • Cuando el alcohol no es la función principal, se nombra como "hidroxi -", indicando el número localizador correspondiente. 4 -metil-ciclohexanol 3 -hidroxi-4 -metilpentanal 2 but en-1 -ol

Si te dan la formula Si te dan el nombre

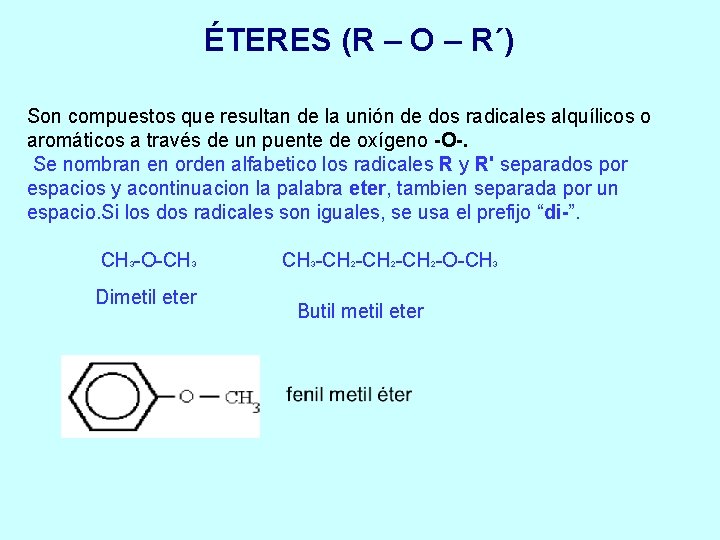
ÉTERES (R – O – R´) Son compuestos que resultan de la unión de dos radicales alquílicos o aromáticos a través de un puente de oxígeno -O-. Se nombran en orden alfabetico los radicales R y R' separados por espacios y acontinuacion la palabra eter, tambien separada por un espacio. Si los dos radicales son iguales, se usa el prefijo “di-”. CH -O-CH 3 3 Dimetil eter CH -CH -O-CH 3 2 2 Butil metil eter 2 3

Si te dan la formula Si te dan el nombre

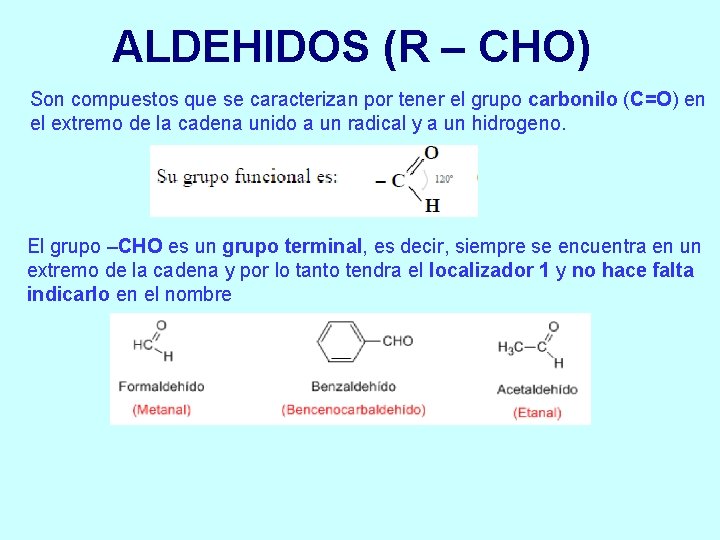
ALDEHIDOS (R – CHO) Son compuestos que se caracterizan por tener el grupo carbonilo (C=O) en el extremo de la cadena unido a un radical y a un hidrogeno. El grupo –CHO es un grupo terminal, es decir, siempre se encuentra en un extremo de la cadena y por lo tanto tendra el localizador 1 y no hace falta indicarlo en el nombre

Si te dan la formula Si te dan el nombre

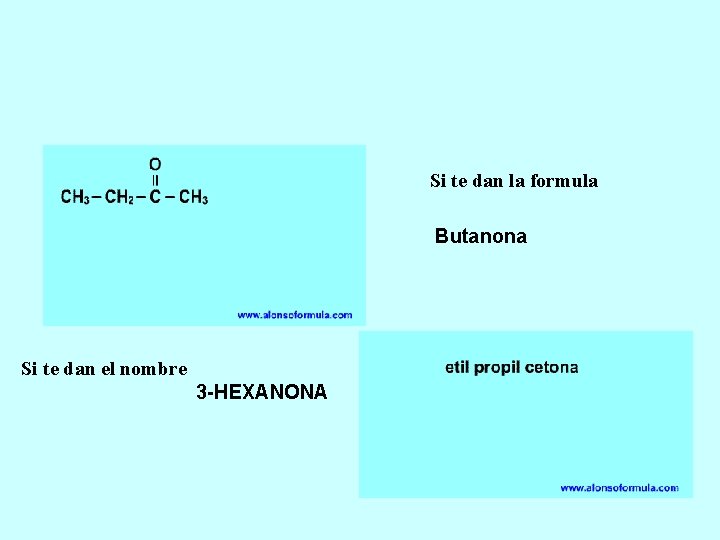
CETONAS (R – CO – R' ) Son compuestos que tambien tienen el grupo carbonilo (C=O), pero a diferencia de los aldehidos no es un grupo terminal y va unido a dos radicales, R – CO – R'. Se escribe generalmente de forma abreviada como –CO– -Se elige como cadena principal la mas larga que contenga al grupo carbonilo y se numera por el extremo que se le asigne al grupo –CO– el localizador mas bajo. -Se nombran, en orden alfabetico, los dos radicales (R y R') que van unido al grupo carbonilo seguido de la palabra “cetona” -En caso de que existan mas de un grupo carbonilo –CO–, se anaden los sufijos “-diona”, “-triona”, “-tetraona”. Cuando el grupo carbonilo, –CO–, se encuentra como sustituyente en una cadena y no es el grupo principal se nombra con el prefijo “oxo-”. CH -CO-CH 3 2 2 CH -CO-CH -CH 3 2 2, 4 -Hexanodiona 3 -Pentanona 3 2 3

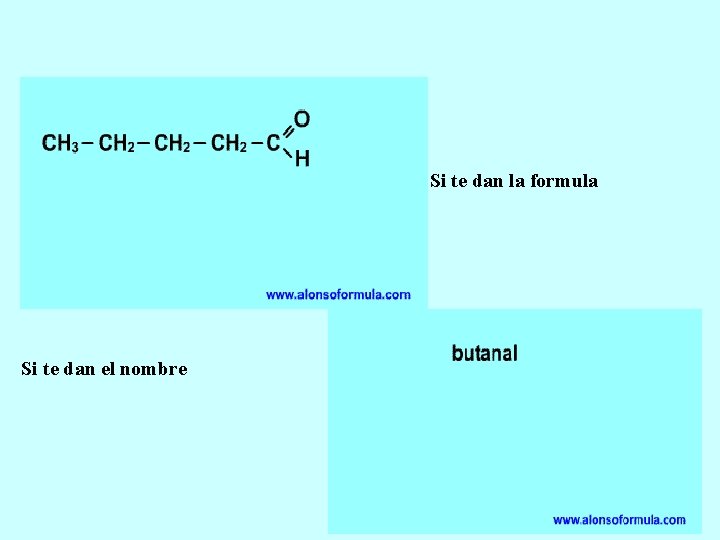
Si te dan la formula Butanona Si te dan el nombre 3 -HEXANONA

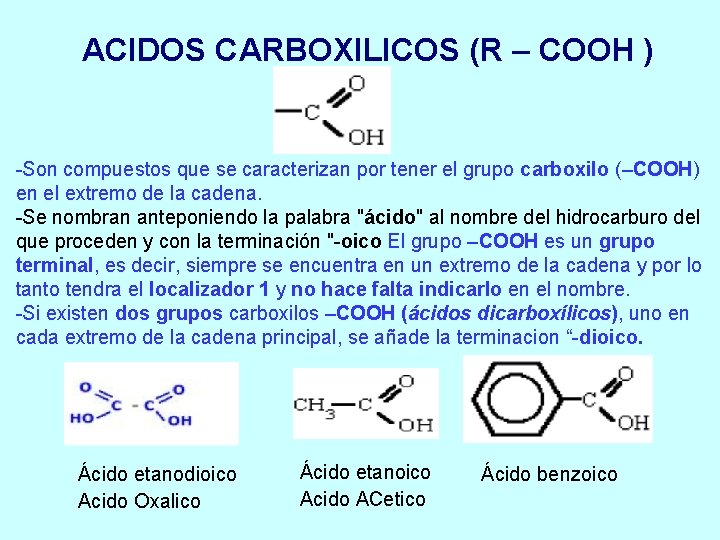
ACIDOS CARBOXILICOS (R – COOH ) -Son compuestos que se caracterizan por tener el grupo carboxilo (–COOH) en el extremo de la cadena. -Se nombran anteponiendo la palabra "ácido" al nombre del hidrocarburo del que proceden y con la terminación "-oico El grupo –COOH es un grupo terminal, es decir, siempre se encuentra en un extremo de la cadena y por lo tanto tendra el localizador 1 y no hace falta indicarlo en el nombre. -Si existen dos grupos carboxilos –COOH (ácidos dicarboxílicos), uno en cada extremo de la cadena principal, se añade la terminacion “-dioico. Ácido etanodioico Acido Oxalico Ácido etanoico Acido ACetico Ácido benzoico

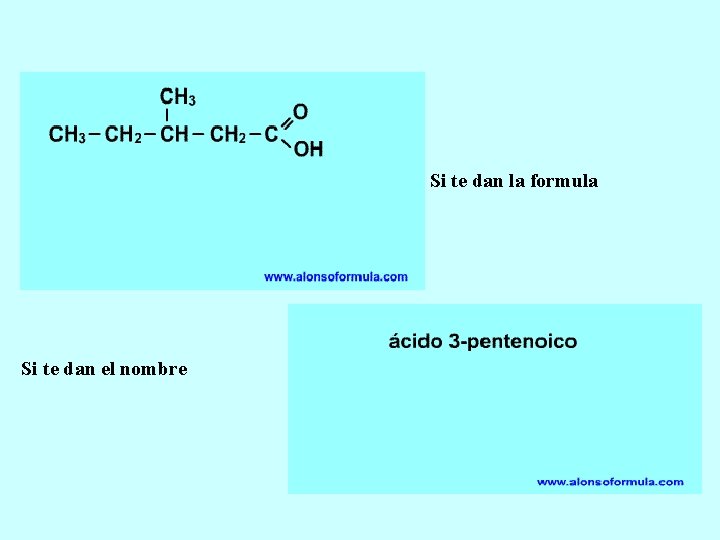
Si te dan la formula Si te dan el nombre

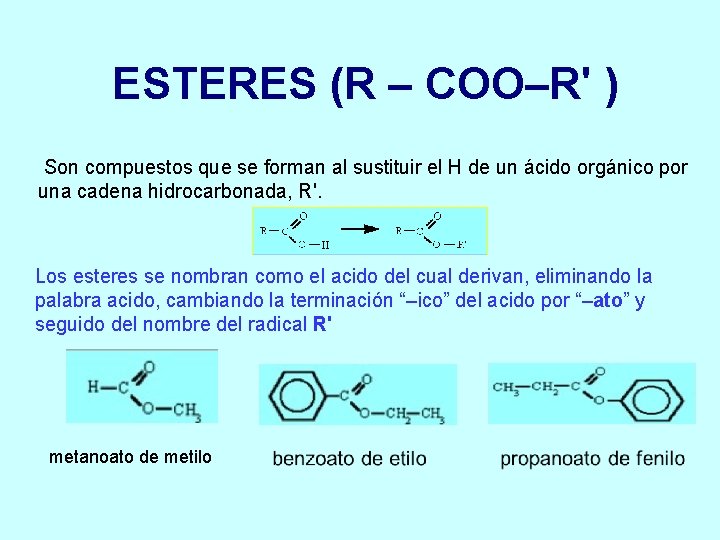
ESTERES (R – COO–R' ) Son compuestos que se forman al sustituir el H de un ácido orgánico por una cadena hidrocarbonada, R'. Los esteres se nombran como el acido del cual derivan, eliminando la palabra acido, cambiando la terminación “–ico” del acido por “–ato” y seguido del nombre del radical R' metanoato de metilo

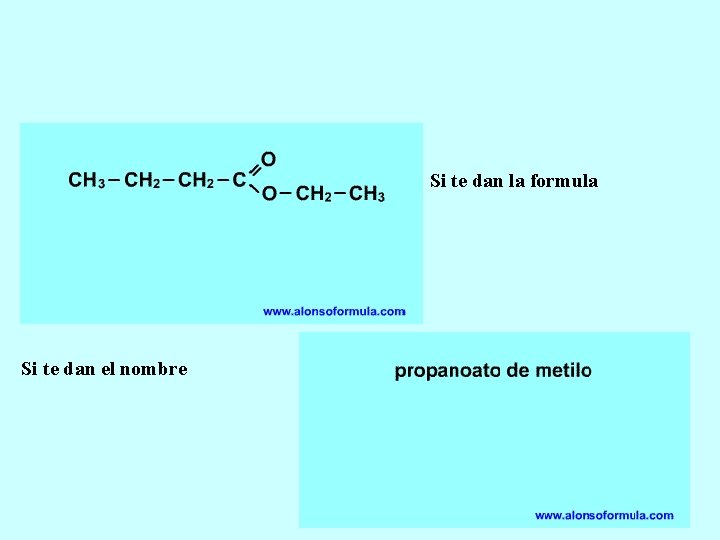
Si te dan la formula Si te dan el nombre

SALES ORGANICAS (R – COOMe ) Los ácidos carboxilicos, de igual forma que los acidos inorgánicos, forman sales por sustitucion del hidrogeno del grupo carboxilo –COOH por cationes metálicos o por el ion amonio, NH 4 , donde Me es un catión metálico o el ion amonio. Estas sales orgánicas se nombran (al igual que los esteres) como el acido del cual derivan, eliminando la palabra acido, cambiando la terminación “–ico” del acido por “–ato” y seguida del nombre del catión metálico que sustituye al hidrogeno del grupo carboxilo. HCOO‾ NH 4+ Etanoato de sodio (Acetato de sodio) Metanoato de amonio Benzoato de potasio

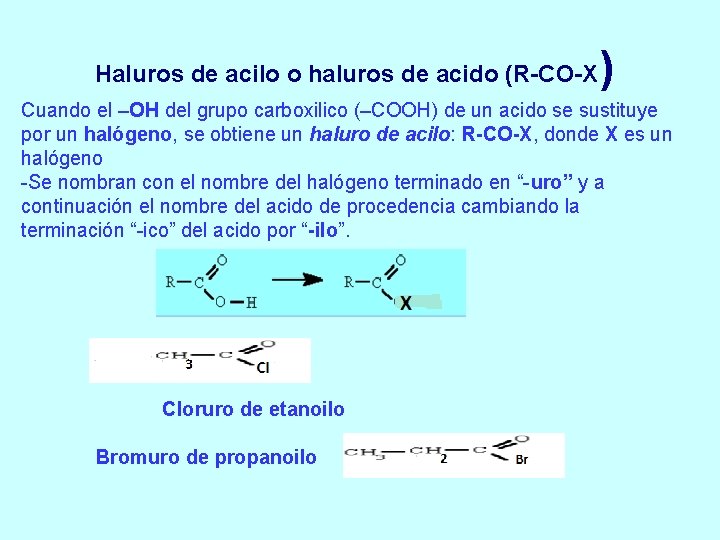
Haluros de acilo o haluros de acido (R-CO-X ) Cuando el –OH del grupo carboxilico (–COOH) de un acido se sustituye por un halógeno, se obtiene un haluro de acilo: R-CO-X, donde X es un halógeno -Se nombran con el nombre del halógeno terminado en “-uro” y a continuación el nombre del acido de procedencia cambiando la terminación “-ico” del acido por “-ilo”. Cloruro de etanoilo Bromuro de propanoilo

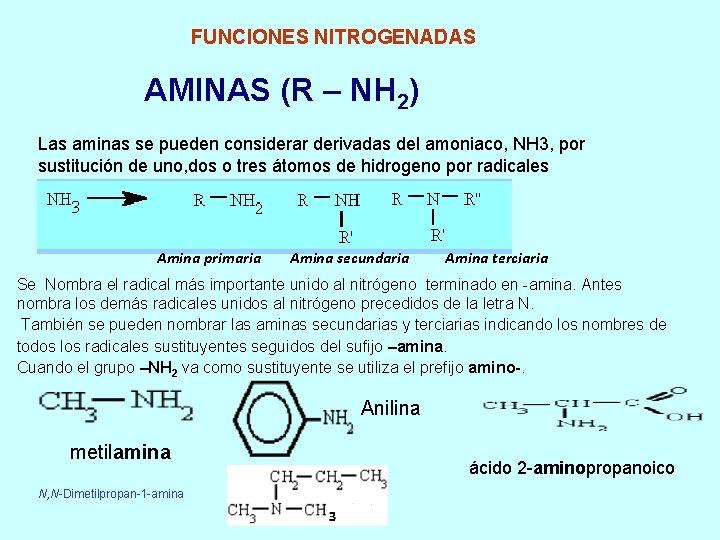
FUNCIONES NITROGENADAS AMINAS (R – NH 2) Las aminas se pueden considerar derivadas del amoniaco, NH 3, por sustitución de uno, dos o tres átomos de hidrogeno por radicales Amina primaria Amina secundaria Amina terciaria Se Nombra el radical más importante unido al nitrógeno terminado en -amina. Antes nombra los demás radicales unidos al nitrógeno precedidos de la letra N. También se pueden nombrar las aminas secundarias y terciarias indicando los nombres de todos los radicales sustituyentes seguidos del sufijo –amina. Cuando el grupo –NH 2 va como sustituyente se utiliza el prefijo amino-. Anilina metilamina N, N-Dimetilpropan-1 -amina ácido 2 -aminopropanoico

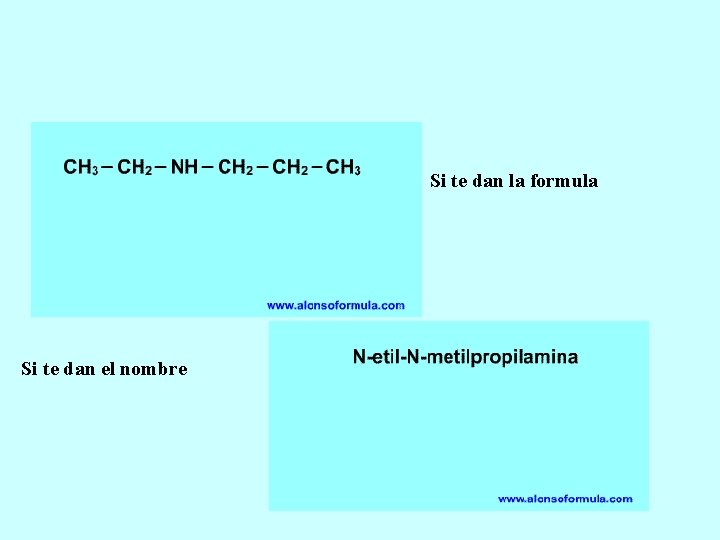
Si te dan la formula Si te dan el nombre

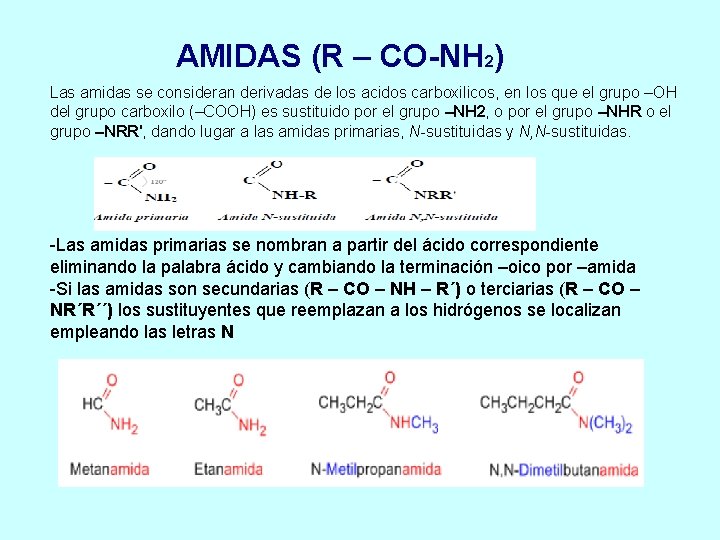
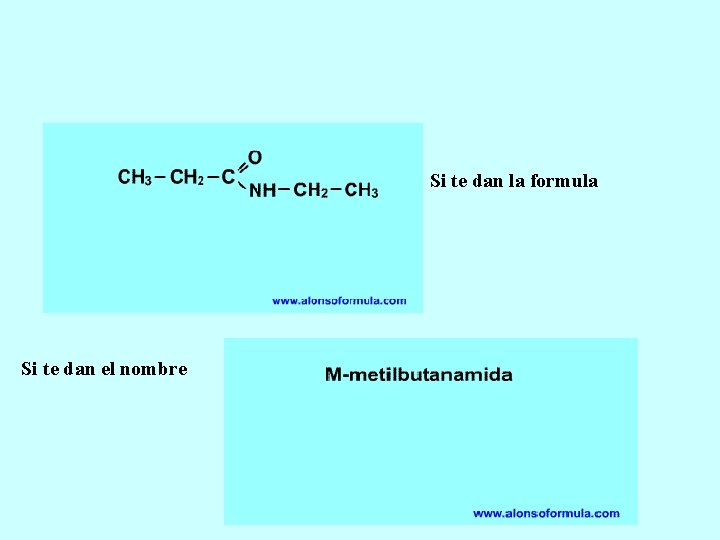
AMIDAS (R – CO-NH 2) Las amidas se consideran derivadas de los acidos carboxilicos, en los que el grupo –OH del grupo carboxilo (–COOH) es sustituido por el grupo –NH 2, o por el grupo –NHR o el grupo –NRR', dando lugar a las amidas primarias, N-sustituidas y N, N-sustituidas. -Las amidas primarias se nombran a partir del ácido correspondiente eliminando la palabra ácido y cambiando la terminación –oico por –amida -Si las amidas son secundarias (R – CO – NH – R´) o terciarias (R – CO – NR´R´´) los sustituyentes que reemplazan a los hidrógenos se localizan empleando las letras N

Si te dan la formula Si te dan el nombre

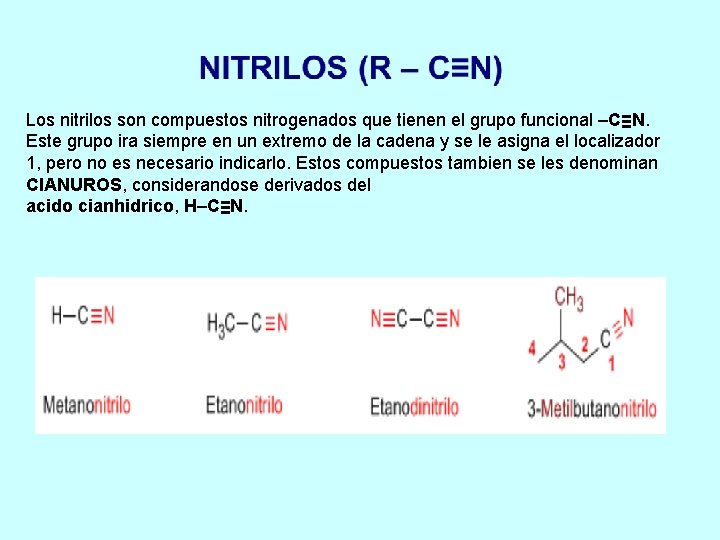
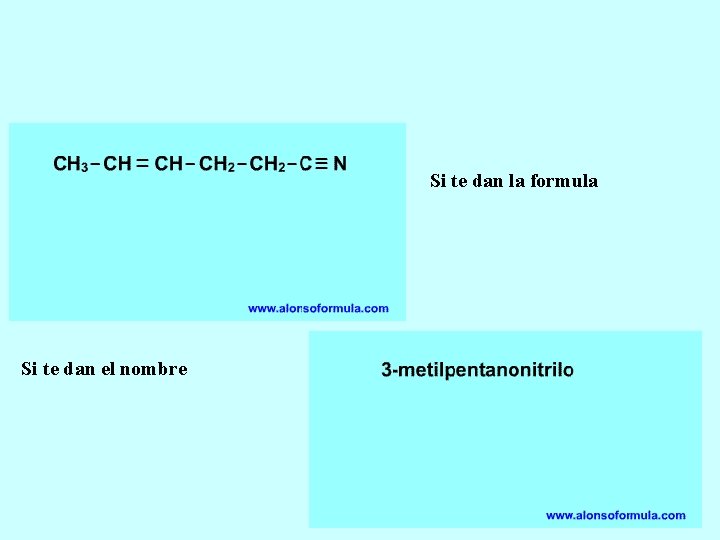
Los nitrilos son compuestos nitrogenados que tienen el grupo funcional –C≡N. Este grupo ira siempre en un extremo de la cadena y se le asigna el localizador 1, pero no es necesario indicarlo. Estos compuestos tambien se les denominan CIANUROS, considerandose derivados del acido cianhidrico, H–C≡N.

Si te dan la formula Si te dan el nombre

Anhídridos R -COOO¨-R ) ESTAS SUSTANCIAS Orgánicas PUEDEN SER CONSIDERADOS COMO EL RESULTADODE LA CONDENSACIÓN DE DOS moleculas DE ÁCIDO CARBOXÍLICO DESPUÉS DE PERDER UNA Molécula DE AGUA ENTRE AMBAS LOS ANHIDRIDOS DE ÁCIDO simétricos SE NOMBRAN SUSTITUYENDO LA PALABRA ÁCIDO POR anhídrido LOS ANHIDRIDOS DE ÁCIDO ASIMÉTRICOS SE NOMBRAN CON LA PALABRA anhídrido SEGUIDO DE CADA COMPONENTE DEL ÁCIDO CARBOXÍLICO ES Orden Alfabético (SIN LA PALABRA ÁCIDO).
 Metilidenciclopentano
Metilidenciclopentano Descomposición de alquinos
Descomposición de alquinos Alquenos
Alquenos Hidrocarburos insaturados alquenos y alquinos
Hidrocarburos insaturados alquenos y alquinos Nombre de los alquinos
Nombre de los alquinos Deshidrohalogenación de alquinos
Deshidrohalogenación de alquinos Cual es el grupo funcional de los alquinos
Cual es el grupo funcional de los alquinos Quimica organica
Quimica organica Cadena abierta ramificada
Cadena abierta ramificada Propiedades quimicas de los alquinos
Propiedades quimicas de los alquinos Interacciones moleculares
Interacciones moleculares Sec pentilo
Sec pentilo Nomenclatura grupos funcionales
Nomenclatura grupos funcionales Etino hibridacion sp
Etino hibridacion sp Propiedades quimica del carbono
Propiedades quimica del carbono Dimetil trimetil
Dimetil trimetil Cahg nomenclatura
Cahg nomenclatura Características de los alquinos
Características de los alquinos Hidratacion de alquinos
Hidratacion de alquinos Alcoximercuración-desmercuración
Alcoximercuración-desmercuración Isobutilen + hbr
Isobutilen + hbr Reactivo de swern
Reactivo de swern Ch2-ch3
Ch2-ch3 Reacciones de los alquenos
Reacciones de los alquenos Generalidades de los hidrocarburos
Generalidades de los hidrocarburos Producto saytzeff
Producto saytzeff Nomenclatura e z alquenos
Nomenclatura e z alquenos Usos de alquenos
Usos de alquenos Nomenclatura e z alquenos
Nomenclatura e z alquenos Caracteristicas dos seres vivos composição quimica
Caracteristicas dos seres vivos composição quimica Qumica
Qumica Clivagem oxidativa de alcenos
Clivagem oxidativa de alcenos Pilha de daniell
Pilha de daniell Ejemplos de epimeros
Ejemplos de epimeros Livresq
Livresq Materia extensiva
Materia extensiva Qumica
Qumica Qumica
Qumica Qumica
Qumica Cinetica molecular
Cinetica molecular Cintica
Cintica Qumica
Qumica Qumica
Qumica Enlace covalente coordinado
Enlace covalente coordinado Geometria trigonal plana
Geometria trigonal plana Fórmula bastão
Fórmula bastão Precipitado
Precipitado Nomenclatura das bases
Nomenclatura das bases Istopos
Istopos Que es el proyecto genoma humano
Que es el proyecto genoma humano Qumica
Qumica Qumica
Qumica Qumica
Qumica Energia en los enlaces quimicos
Energia en los enlaces quimicos Qumica
Qumica Mistura quimica
Mistura quimica Philippe spitaleri kaufmann
Philippe spitaleri kaufmann Qumica
Qumica Qumica
Qumica Notação de lewis
Notação de lewis Entalpia
Entalpia Qumica
Qumica Qumica
Qumica Qumica
Qumica Stoicheon
Stoicheon Qumica
Qumica Ciclenos
Ciclenos Entalpia de formação
Entalpia de formação Qumica
Qumica Qual a sentença verdadeira
Qual a sentença verdadeira Qumica
Qumica Gás carbônico e oxigênio
Gás carbônico e oxigênio