ESTRUCTURA DEL CARBONO HIBRIDACIN Estructura del Carbono El

ESTRUCTURA DEL CARBONO HIBRIDACIÓN

Estructura del Carbono • El carbono es un elemento con propiedades muy especiales que le permiten formar variadas familias de compuestos orgánicos, como los hidrocarburos, compuestos formados por átomos de carbono e hidrógeno únicamente, entre los que se encuentran los alcanos, alquenos y alquinos. • ¿Cómo es que el carbono puede formar variados compuestos?

Estructura del carbono • La respuesta la podemos encontrar en la estructura atómica del carbono. • Ya que su número atómico es seis, su configuración electrónica en el estado basal es: 1 s 2 2 p 2 • Y su representación gráfica: 1 s 2 s 2 px 2 py 2 pz

Estructura del carbono • Como puedes observar, el carbono tiene el orbital 2 pz vacío, en el estado basal. • Si el átomo de carbono gana energía (aplicando calor o electricidad), los electrones del orbital 2 s puede desaparearse y uno de ellos saltar hasta el orbital 2 pz: 1 s 2 s 2 px 2 py 2 pz

Estructura del carbono • De esta manera, el átomo de carbono ya tiene ocupados cuatro orbitales con un electrón cada uno. • El estado en el que un átomo gana energía y sus electrones pueden saltar a otros niveles de mayor energía, se le denomina excitado.

Estructura del carbono • El estado excitado del átomo de carbono puede estabilizarse mediante el mecanismo de hibridación, en el cual, orbitales puros se combinan entre sí y mediante un reacomodo energético producen orbitales híbridos de diferentes formas, tamaños y orientaciones. • El átomo de carbono puede presentar tres tipos de hibridación: sp, sp 2 , sp 3, con las que puede formar diferentes familias de hidrocarburos.
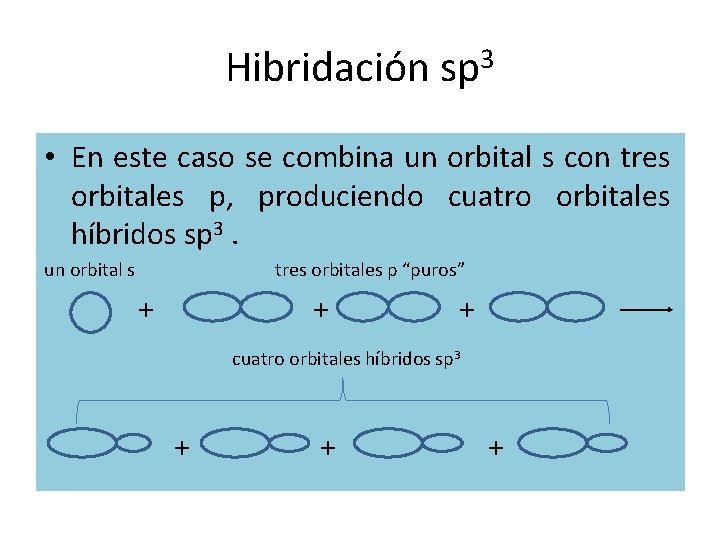
Hibridación sp 3 • En este caso se combina un orbital s con tres orbitales p, produciendo cuatro orbitales híbridos sp 3. un orbital s tres orbitales p “puros” + + + cuatro orbitales híbridos sp 3 + + +
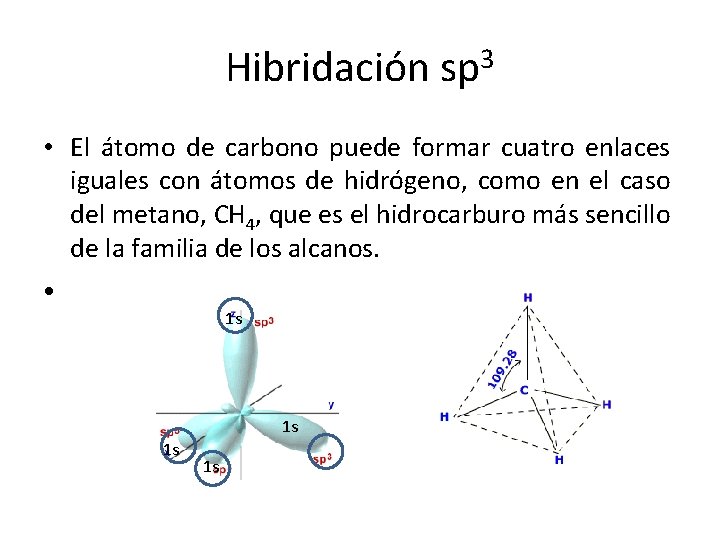
Hibridación sp 3 • El átomo de carbono puede formar cuatro enlaces iguales con átomos de hidrógeno, como en el caso del metano, CH 4, que es el hidrocarburo más sencillo de la familia de los alcanos. • 1 s 1 s

Hibridación sp 3 • En el metano, a cada uno de los enlaces que resultan de la superposición o traslapamiento de un orbital sp 3 del carbono con un orbital 1 s del hidrógeno se le denomina enlace sigma σ o sencillo y se forma a lo largo de la recta que une los centros de los átomos. El enlace sigma es además el eje de simetría del orbital molecular. • La hibridación sp 3 es característica para átomos de carbono, unidos por enlaces sencillos (enlaces sigma) a 4 átomos de cualquier elemento.

Hibridación sp 3 • Es la hibridación que se presenta en alcanos. • El ángulo entre cualquier par de orbitales sp 3 es de 109. 5°.

Hibridación sp 2 • El carbono también forma otra familia de hidrocarburos llamados alquenos, los cuales se caracterizan por la presencia de un doble enlace entre dos átomos de carbono. Como en el eteno o etileno CH 2 = CH 2. • ¿Cómo el carbono puede formar este tipo de compuestos?
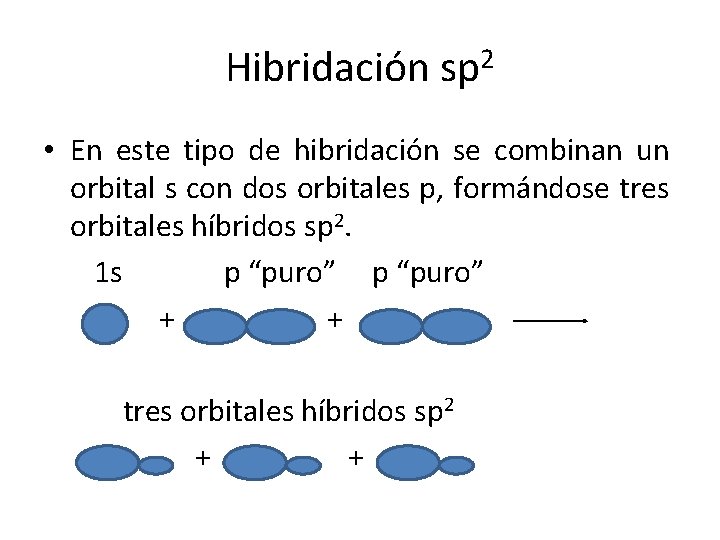
Hibridación sp 2 • En este tipo de hibridación se combinan un orbital s con dos orbitales p, formándose tres orbitales híbridos sp 2. 1 s p “puro” + + tres orbitales híbridos sp 2 + +

Hibridación sp 2 • El carbono para llegar a este tipo de hibridación debe pasar por: • Del estado basal o fundamental: 1 s 22 s 2 2 p 2 o 1 s 2 s 2 px 2 py 2 pz Al estado excitado: 1 s 2 s 2 px 2 py 2 pz

Hibridación sp 2 • Para estabilizarse, el átomo de carbono llegará al mecanismo de hibridación sp 2 en el que un orbital s se combina con dos orbitales p “puros”, formando tres orbitales híbridos sp 2 , quedando un orbital p “puro”. 1 s 2 sp 2 + 2 sp 2 2 pz

Hibridación sp 2 • El átomo de carbono con hibridación sp 2 puede formar tres enlaces sigma con otros átomos. Para formar el enlace adicional en alquenos, los orbitales p “puros” de dos átomos de carbono se traslapan, formando un enlace π pi. • La hibridación sp 2 es característica de los alquenos, da lugar a una geometría molecular de tipo trigonal. • El ángulo entre orbitales sp 2 es de 120°.
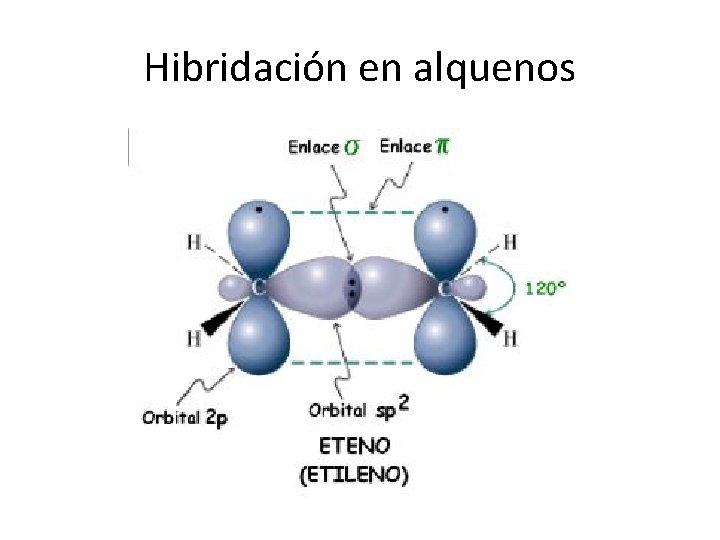
Hibridación en alquenos
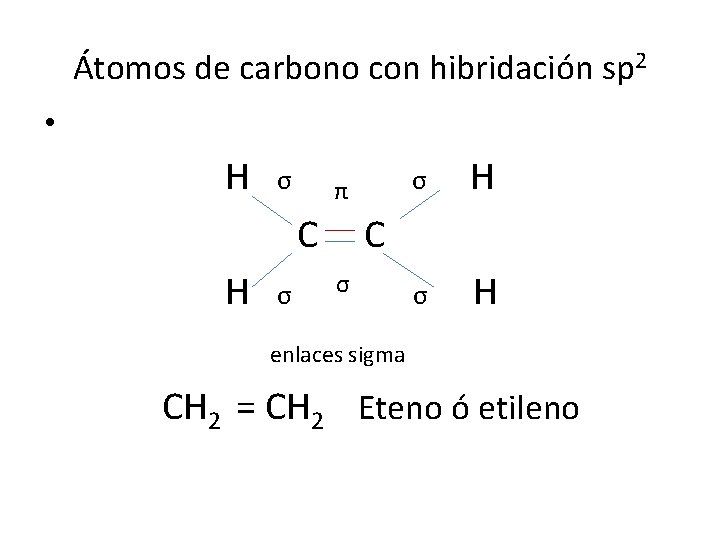
Átomos de carbono con hibridación sp 2 • H σ π C H σ σ H C σ enlaces sigma CH 2 = CH 2 Eteno ó etileno
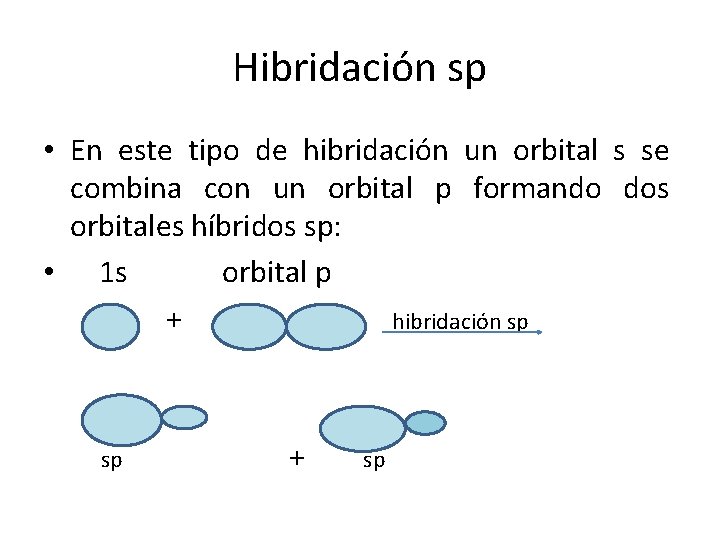
Hibridación sp • En este tipo de hibridación un orbital s se combina con un orbital p formando dos orbitales híbridos sp: • 1 s orbital p + hibridación sp sp + sp

Hibridación sp • Este tipo de hibridación se presenta en alquinos, para la formación del triple enlace carbono-carbono. Para ello el carbono pasa por: • Estado basal: 1 s 2 s 2 px 2 py 2 pz • Estado excitado: 1 s 2 s 2 px 2 py 2 pz

Hibridación sp • Mecanismo de hibridación sp: 1 s 2 sp 2 py 2 pz En el etino o acetileno cada átomo de carbono forma dos enlaces sencillos o sigma con los orbitales híbridos sp y los dos orbitales p “puros” los utilizan para formar dos enlaces adicionales para el triple enlace entre carbonos, característico de los alquinos.
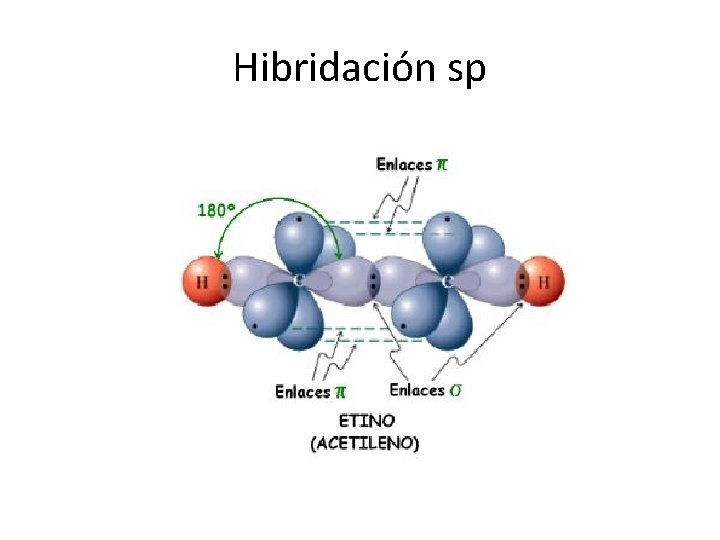
Hibridación sp

Hibridación • La hibridación sp es característica de los alquinos para la formación del triple enlace entre carbonos. • Da lugar a una geometría molecular de tipo lineal. • El ángulo entre orbitales híbridos es de 180°.
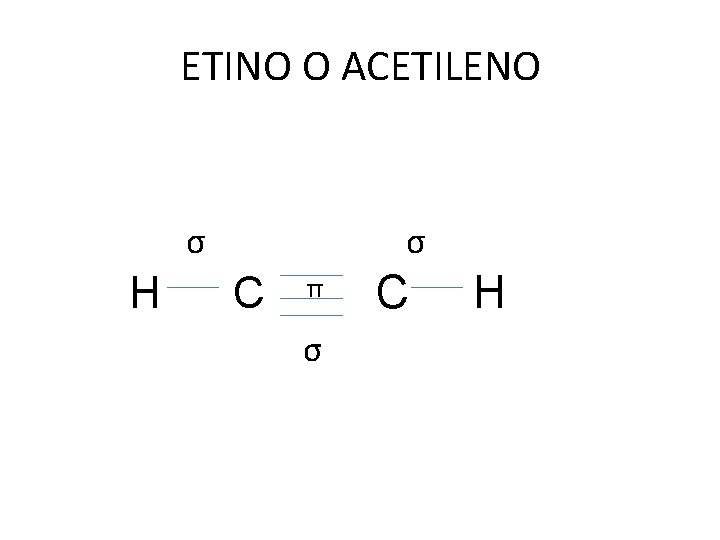
ETINO O ACETILENO σ H σ C π σ C H
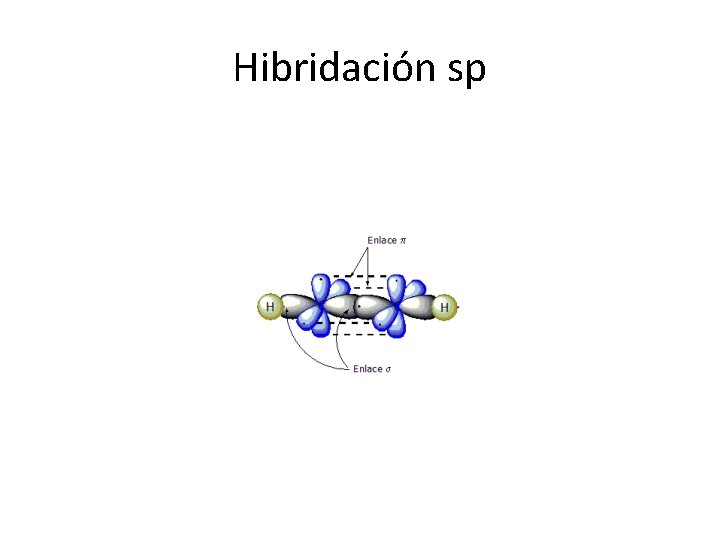
Hibridación sp

Actividad • Contesta las siguientes preguntas: 1. ¿Qué es hibridación? 2. ¿En qué consiste la hibridación sp 3 ? 3. ¿A qué tipo de compuestos da lugar? 4. ¿Qué geometría molecular presentan estos compuestos? 5. ¿Cuál es el ángulo de enlace entre orbitales híbridos?

Preguntas: 6. ¿Cómo se forma un enlace sigma? 7. ¿En qué consiste la hibridación sp 2? 8. ¿A qué tipo de compuestos da lugar? 9. ¿Qué geometría molecular se presenta en ellos? 10. ¿Cuál es el ángulo de enlace entre orbitales sp 2? 11. ¿Cómo se forma un enlace pi?

Preguntas • ¿Qué es la hibridación sp? • ¿De qué tipo de compuestos es característica? • ¿Qué geometría molecular presentan? En binas, contesten las preguntas. Comparen sus respuestas ante el grupo. Entreguen al profesor el cuestionario contestado para su portafolio de evidencias.

Actividad • Realicen búsqueda de información para determinar cómo influyen los enlaces sigma y pi en las propiedades de los hidrocarburos.
- Slides: 28