VO CHE 361 Spezielle Aspekte der Hauptgruppenelementchemie Teil






![Þ polysilanes exhibit pronounced substituent effects ( - -hyperconjugation) ionization energy [e. V] max Þ polysilanes exhibit pronounced substituent effects ( - -hyperconjugation) ionization energy [e. V] max](https://slidetodoc.com/presentation_image_h/838df3d7518284022ff2abfc01556c0b/image-86.jpg)




- Slides: 107

VO CHE. 361 Spezielle Aspekte der Hauptgruppenelementchemie Teil 1: Ao. -Univ. Prof. Dr. Ferdinand Belaj Teil 2: Ao. -Univ. Prof. Dr. Harald Stüger

Teil 1: Niedervalente Hauptgruppenelementverbindungen Diskussion am Beispiel der 4. Hauptgruppe: • höhere Carbenanaloge (Heterocarbene) R 2 Si: R 2 Ge: R 2 Sn: R 2 Pb: Silylen Germylen Stannylen Plumbylen • "nicht klassische" Mehrfachbindungssysteme R 2 Si=CR 2 R 2 Si=Si. R 2 RSi Si. R X=Si. R 2 Silene Disilyne Heterosilene • Polysilylene -(R 2 Si)n. Polysilane

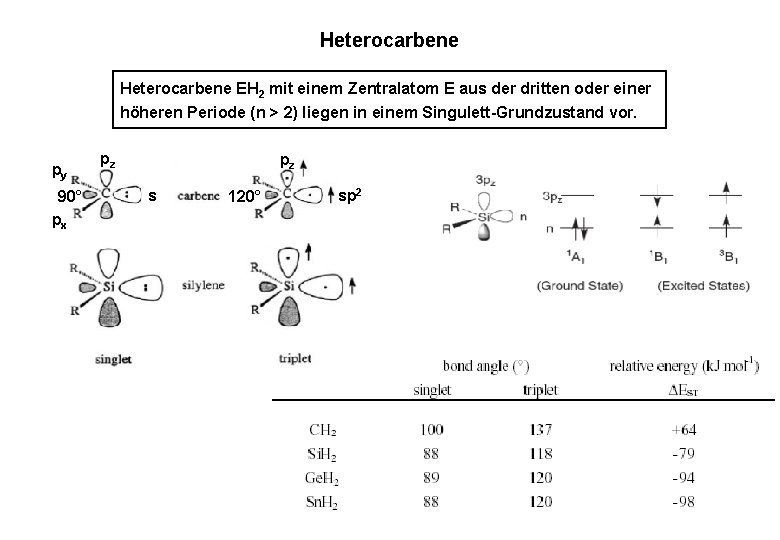
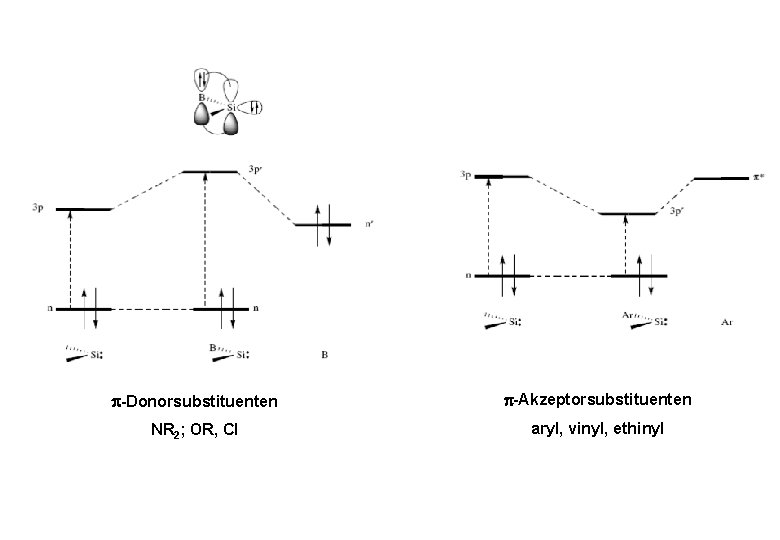
Heterocarbene EH 2 mit einem Zentralatom E aus der dritten oder einer höheren Periode (n > 2) liegen in einem Singulett-Grundzustand vor. py 90° px pz pz s 120° sp 2

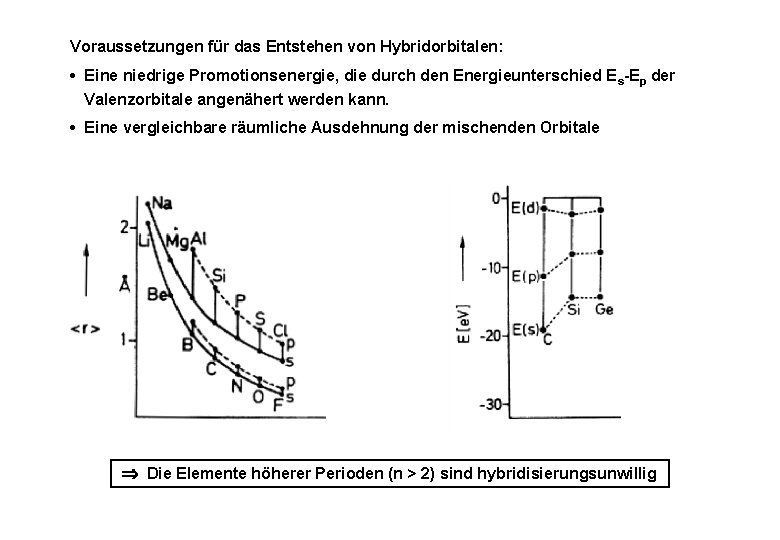
Voraussetzungen für das Entstehen von Hybridorbitalen: • Eine niedrige Promotionsenergie, die durch den Energieunterschied E s-Ep der Valenzorbitale angenähert werden kann. • Eine vergleichbare räumliche Ausdehnung der mischenden Orbitale Die Elemente höherer Perioden (n > 2) sind hybridisierungsunwillig


-Donorsubstituenten -Akzeptorsubstituenten NR 2; OR, Cl aryl, vinyl, ethinyl

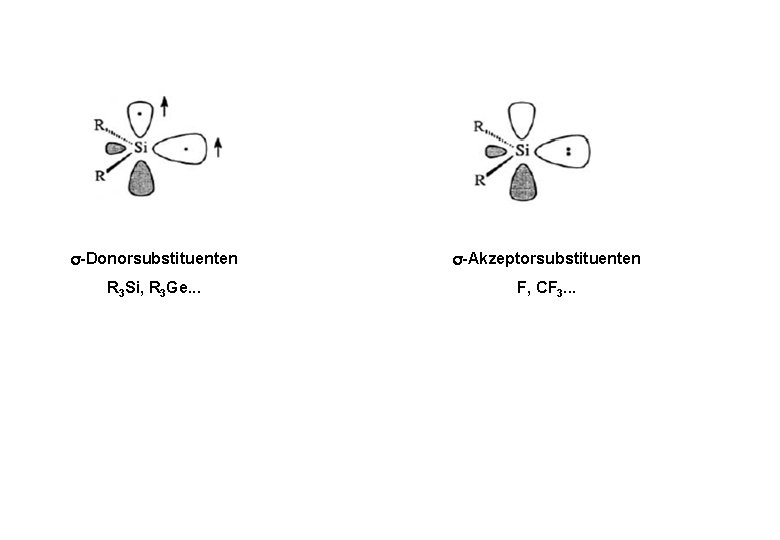
-Donorsubstituenten -Akzeptorsubstituenten R 3 Si, R 3 Ge. . . F, CF 3. . .

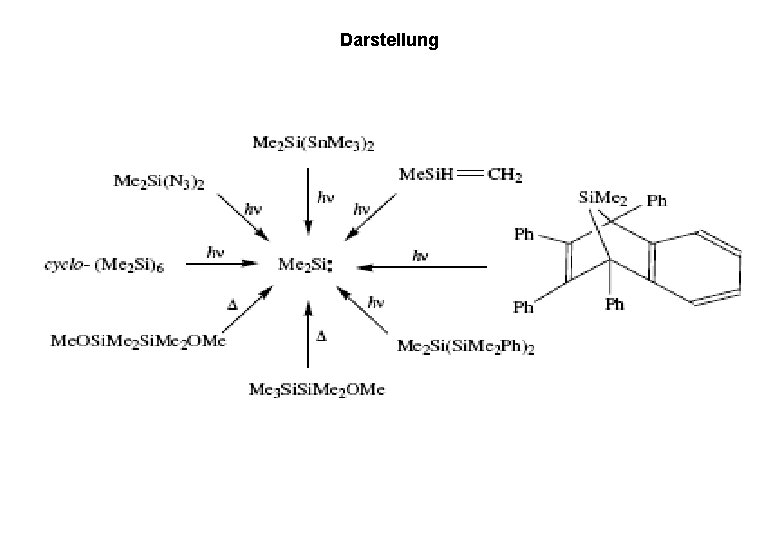
Darstellung

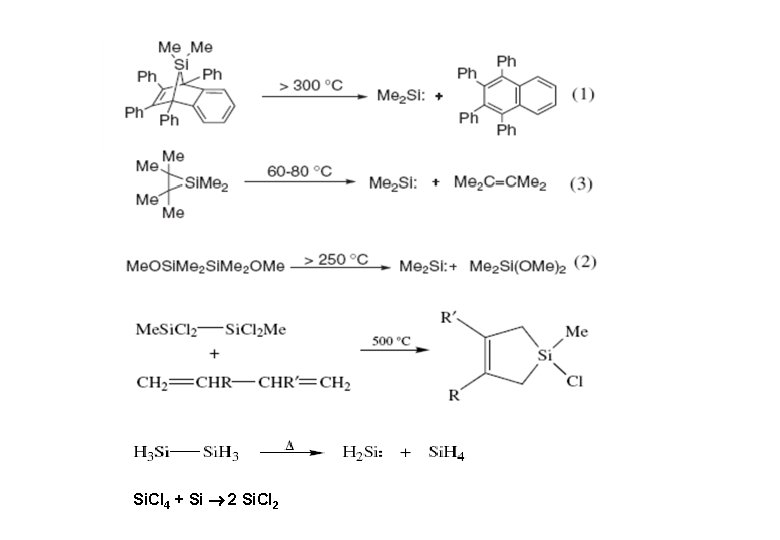
Si. Cl 4 + Si 2 Si. Cl 2



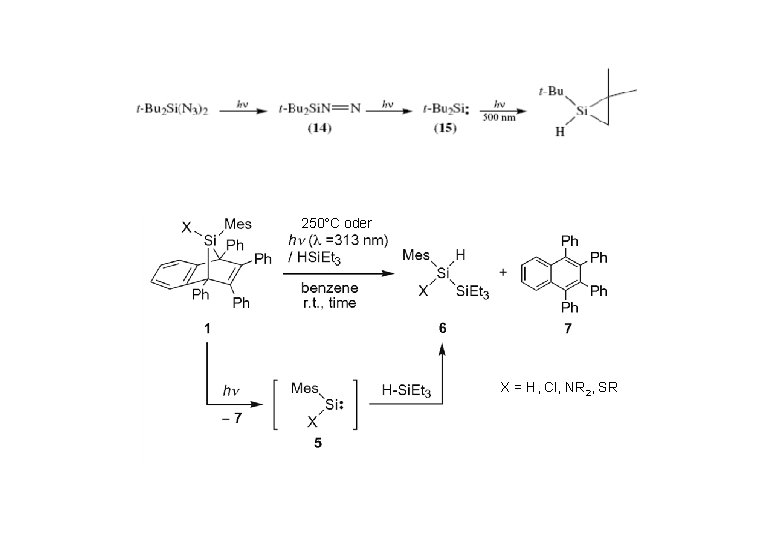
250°C oder X = H, Cl, NR 2, SR

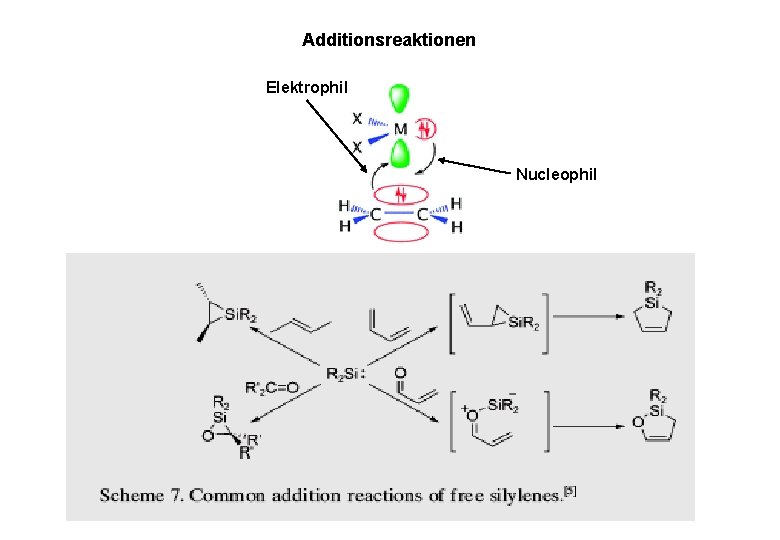
Additionsreaktionen Elektrophil Nucleophil

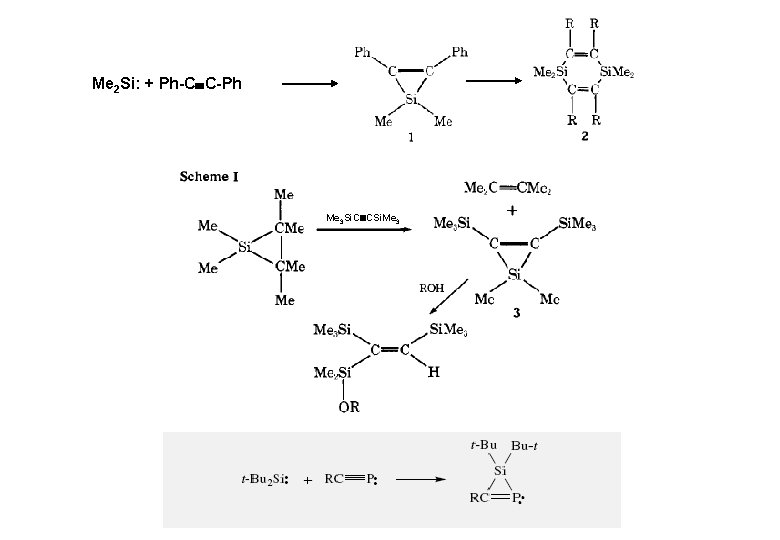
Me 2 Si: + Ph-C C-Ph Me 3 Si. C CSi. Me 3

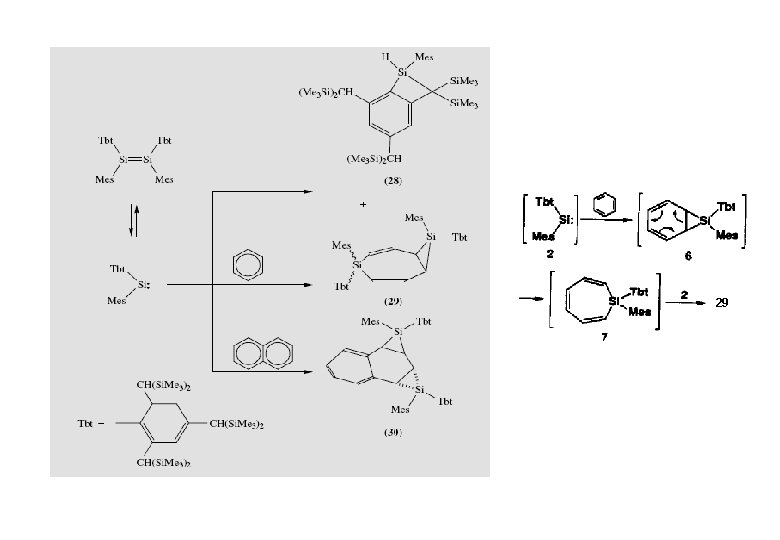
29

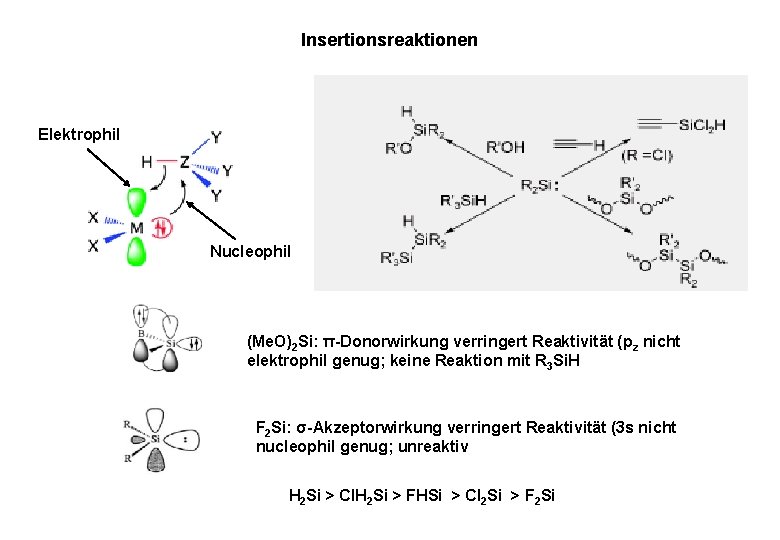
Insertionsreaktionen Elektrophil Nucleophil (Me. O)2 Si: π-Donorwirkung verringert Reaktivität (pz nicht elektrophil genug; keine Reaktion mit R 3 Si. H F 2 Si: σ-Akzeptorwirkung verringert Reaktivität (3 s nicht nucleophil genug; unreaktiv H 2 Si > Cl. H 2 Si > FHSi > Cl 2 Si > F 2 Si

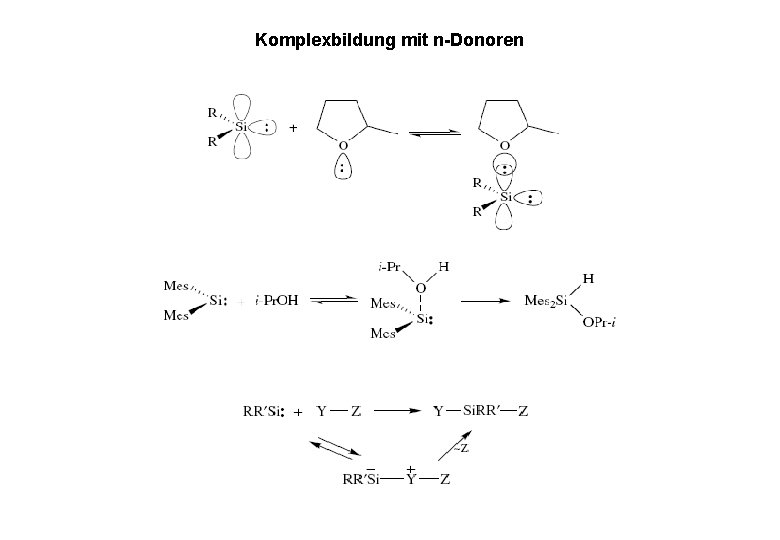
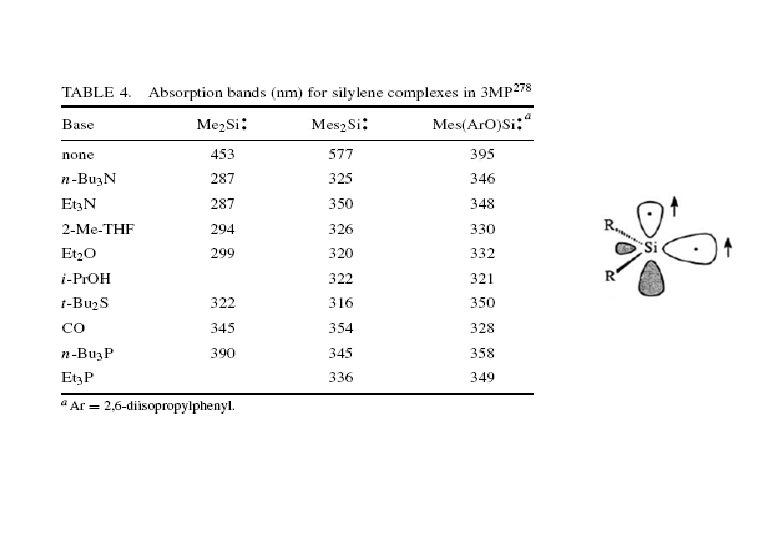
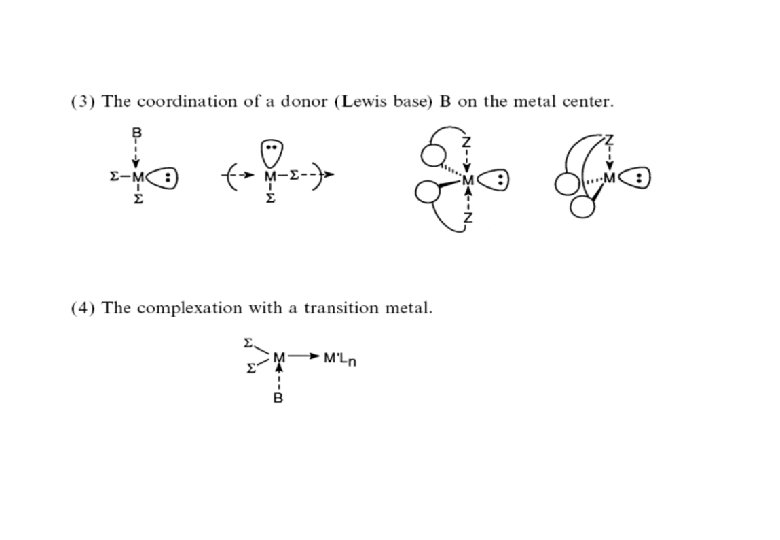
Komplexbildung mit n-Donoren


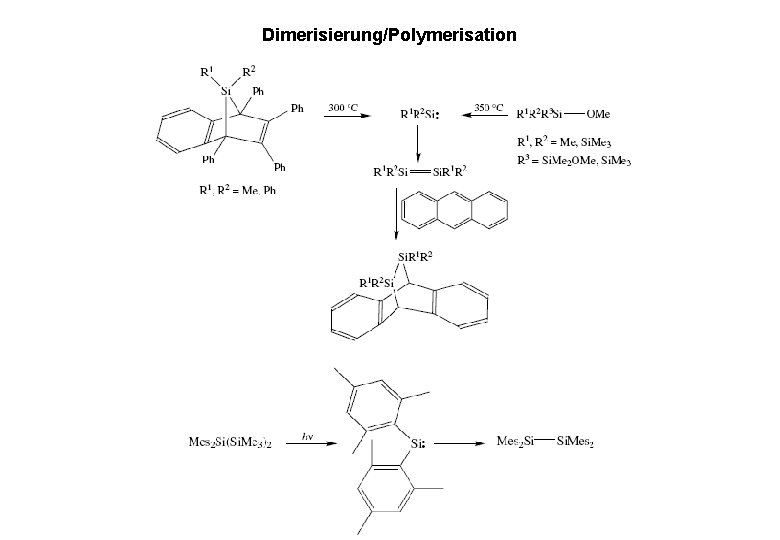
Dimerisierung/Polymerisation

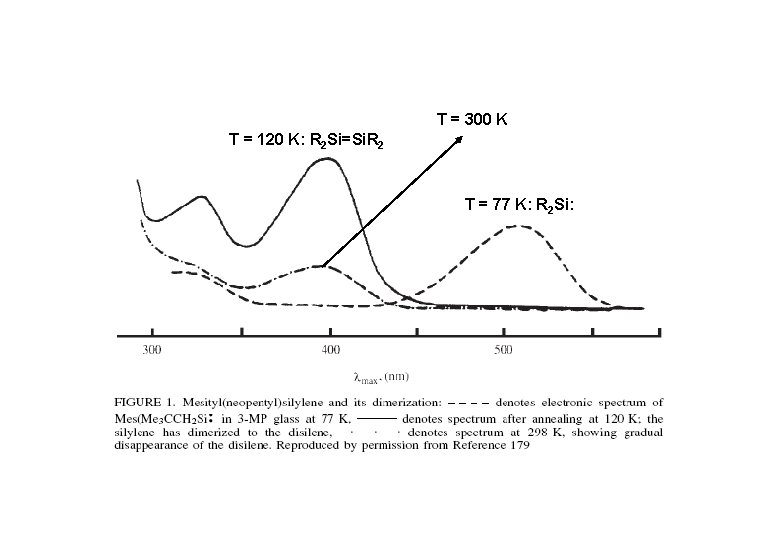
T = 300 K T = 120 K: R 2 Si=Si. R 2 T = 77 K: R 2 Si:


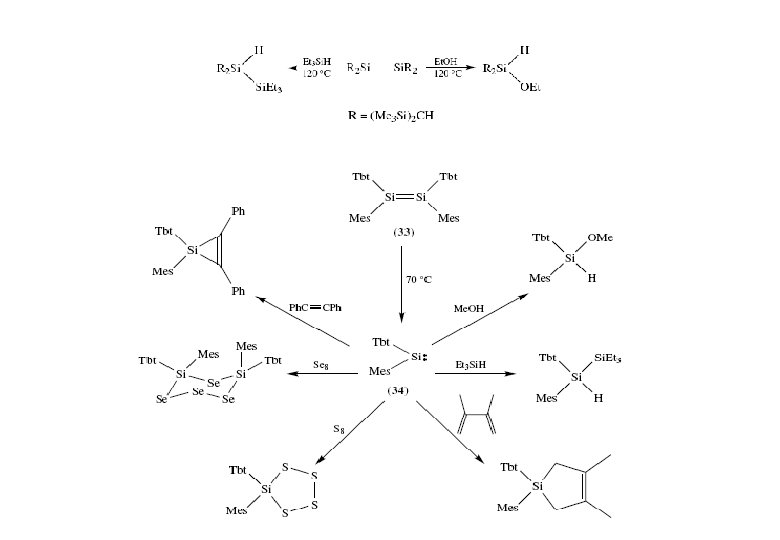
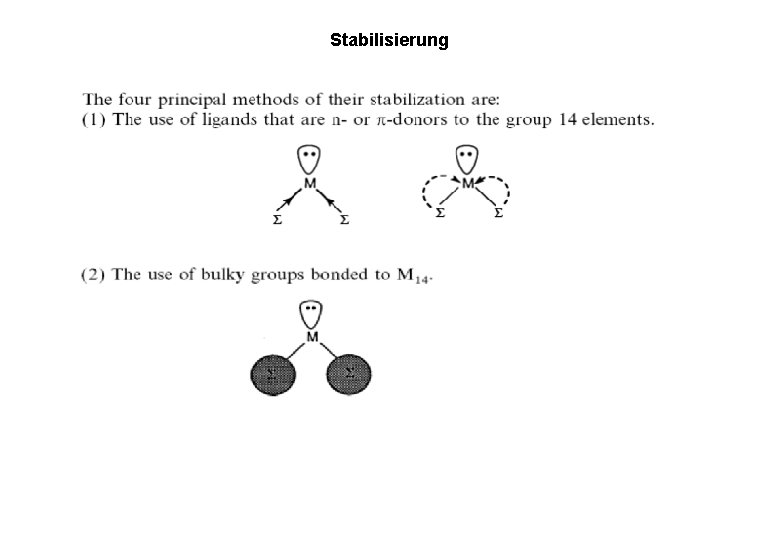
Stabilisierung

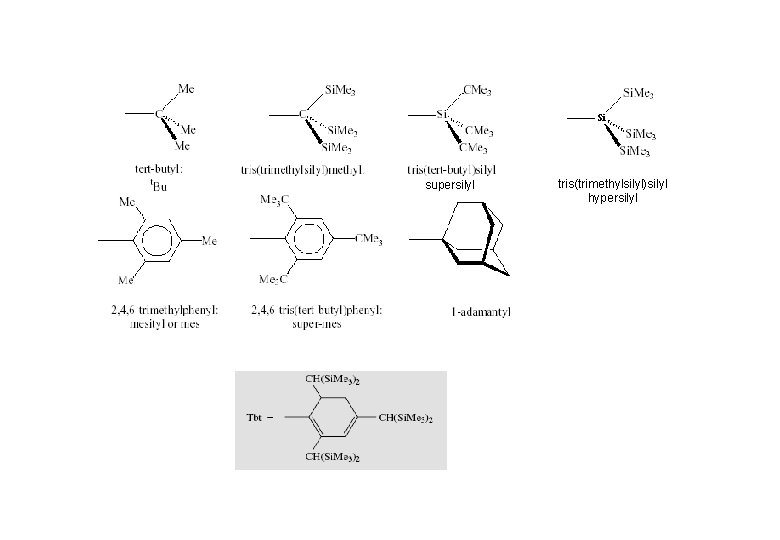
Si supersilyl tris(trimethylsilyl)silyl hypersilyl


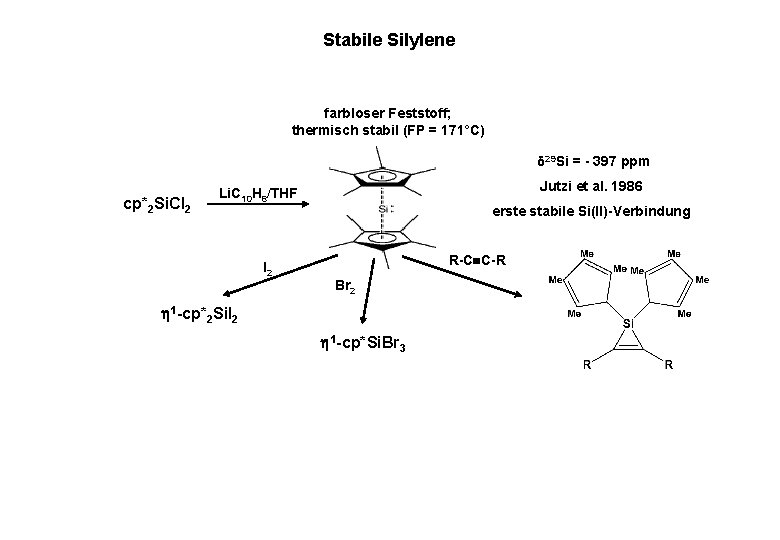
Stabile Silylene farbloser Feststoff; thermisch stabil (FP = 171°C) δ 29 Si = - 397 ppm cp*2 Si. Cl 2 Jutzi et al. 1986 Li. C 10 H 8/THF erste stabile Si(II)-Verbindung R-C C-R I 2 Br 2 1 -cp*2 Si. I 2 1 -cp*Si. Br 3

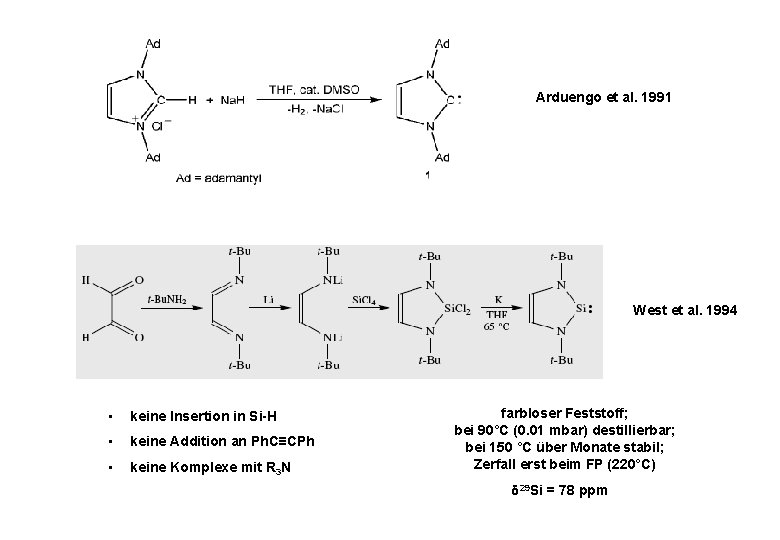
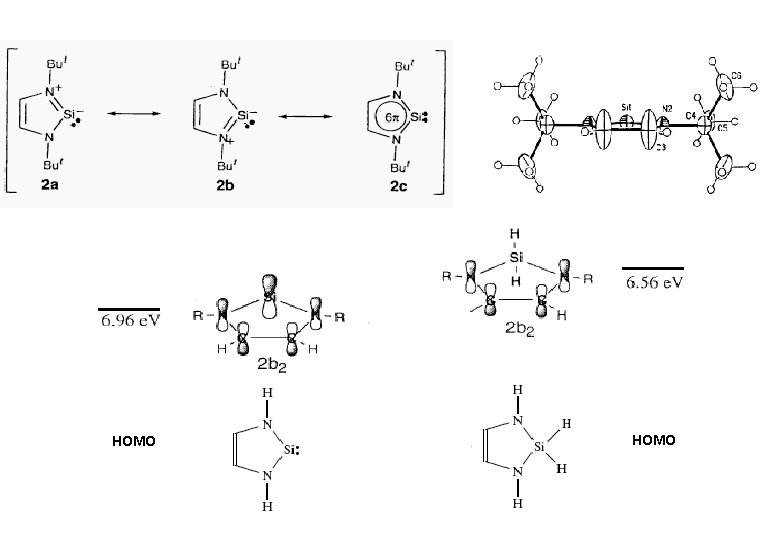
Arduengo et al. 1991 West et al. 1994 • keine Insertion in Si-H • keine Addition an Ph. C≡CPh • keine Komplexe mit R 3 N farbloser Feststoff; bei 90°C (0. 01 mbar) destillierbar; bei 150 °C über Monate stabil; Zerfall erst beim FP (220°C) δ 29 Si = 78 ppm

HOMO

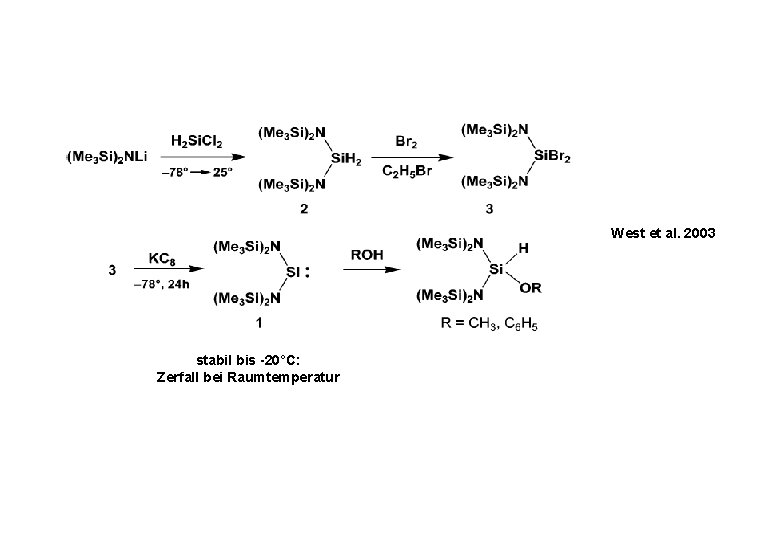
West et al. 2003 stabil bis -20°C: Zerfall bei Raumtemperatur

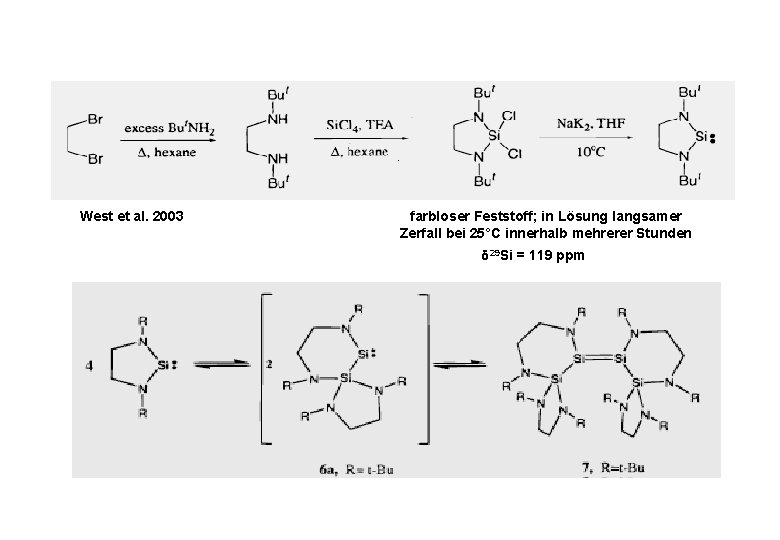
West et al. 2003 farbloser Feststoff; in Lösung langsamer Zerfall bei 25°C innerhalb mehrerer Stunden δ 29 Si = 119 ppm

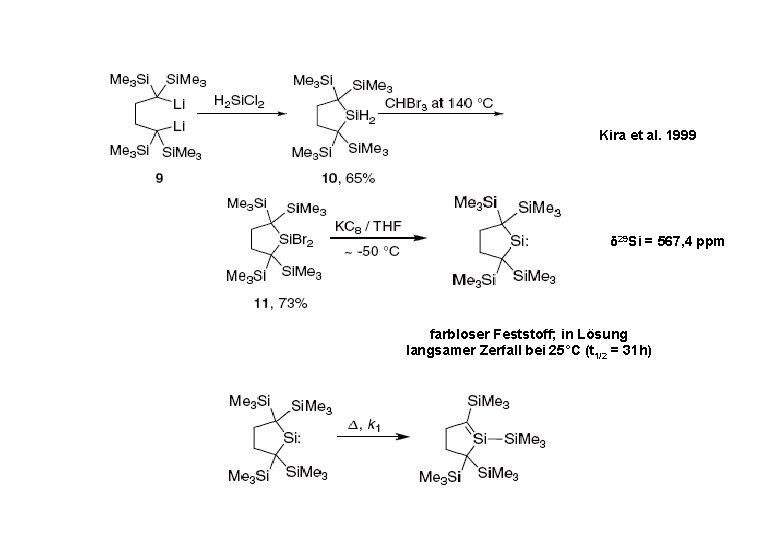
Kira et al. 1999 δ 29 Si = 567, 4 ppm farbloser Feststoff; in Lösung langsamer Zerfall bei 25°C (t 1/2 = 31 h)


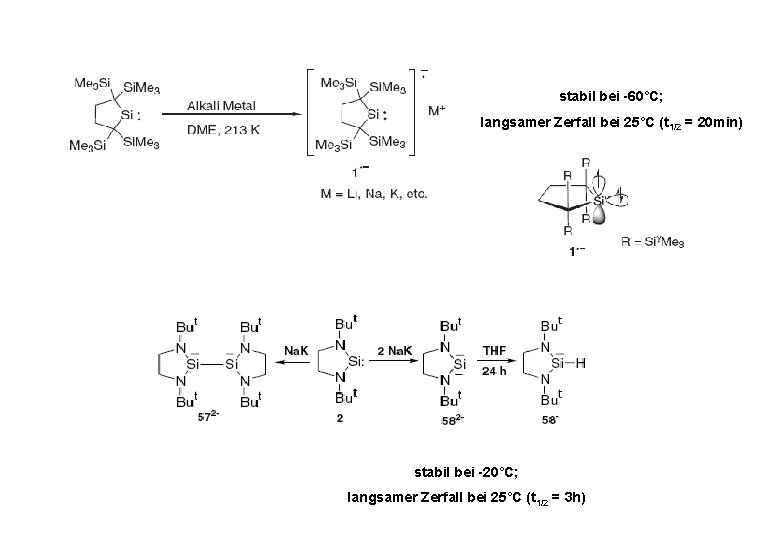
stabil bei -60°C; langsamer Zerfall bei 25°C (t 1/2 = 20 min) stabil bei -20°C; langsamer Zerfall bei 25°C (t 1/2 = 3 h)


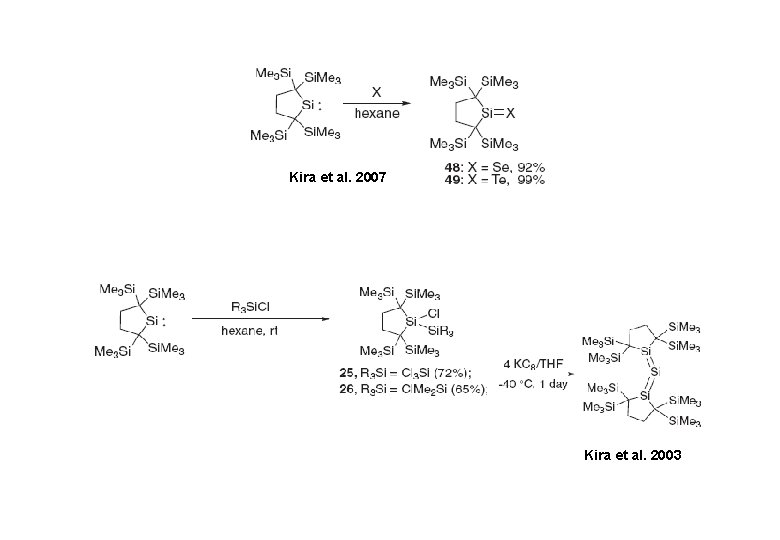
Kira et al. 2007 Kira et al. 2003

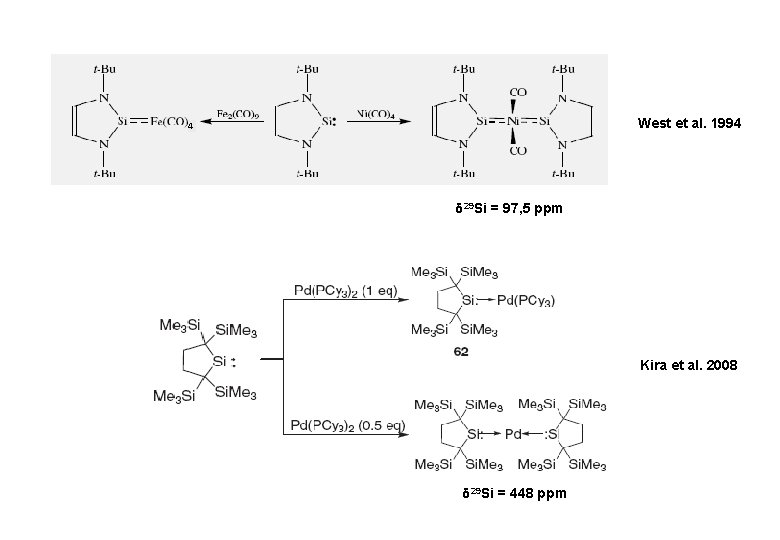
West et al. 1994 4 δ 29 Si = 97, 5 ppm Kira et al. 2008 δ 29 Si = 448 ppm

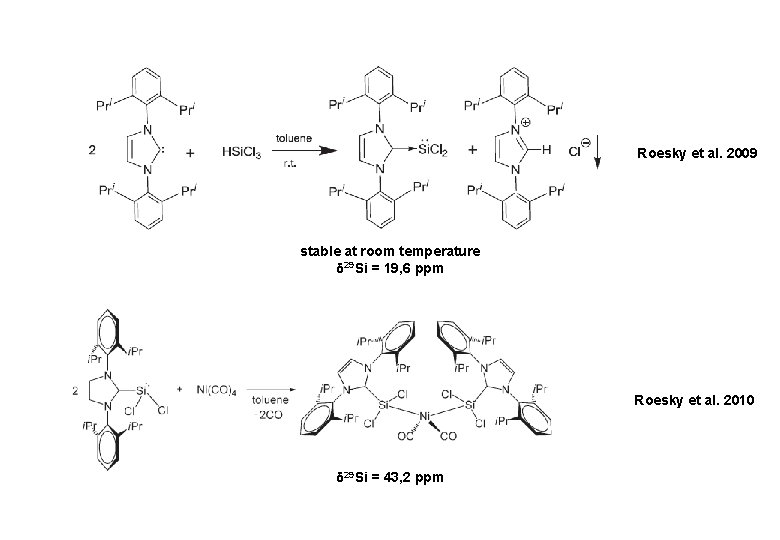
Roesky et al. 2009 stable at room temperature δ 29 Si = 19, 6 ppm Roesky et al. 2010 δ 29 Si = 43, 2 ppm

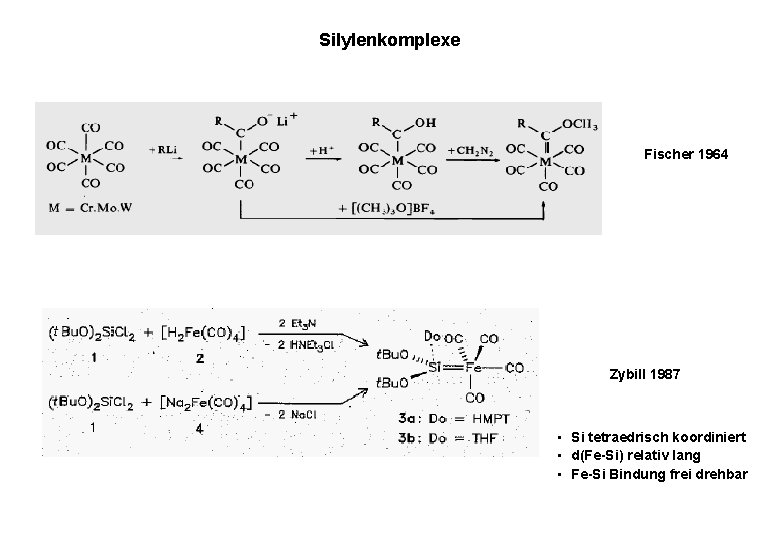
Silylenkomplexe Fischer 1964 Zybill 1987 • Si tetraedrisch koordiniert • d(Fe-Si) relativ lang • Fe-Si Bindung frei drehbar

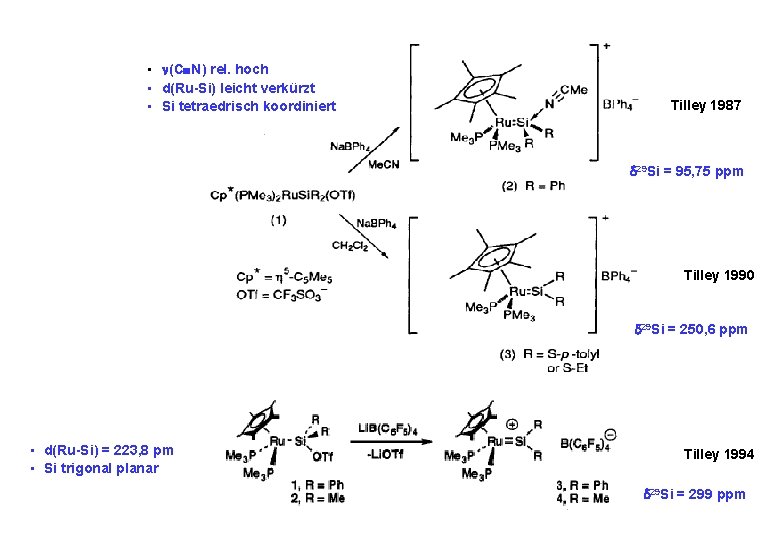
• (C N) rel. hoch • d(Ru-Si) leicht verkürzt • Si tetraedrisch koordiniert Tilley 1987 29 Si = 95, 75 ppm Tilley 1990 29 Si = 250, 6 ppm • d(Ru-Si) = 223, 8 pm • Si trigonal planar Tilley 1994 29 Si = 299 ppm

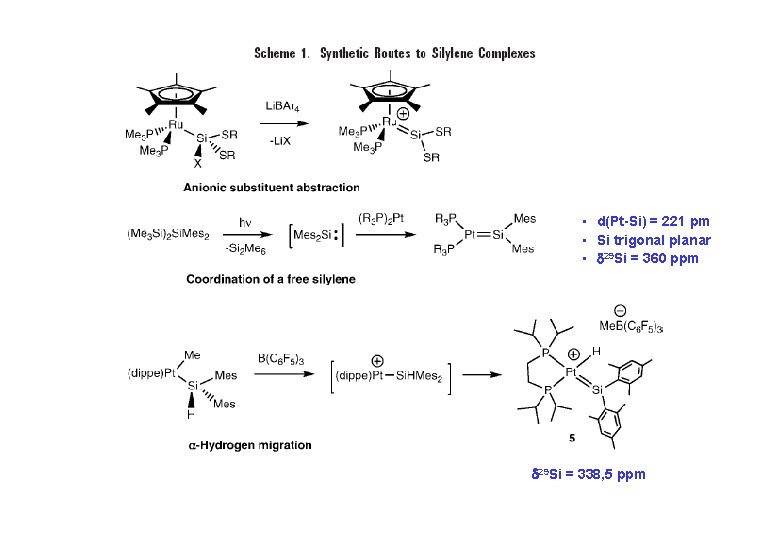
• d(Pt-Si) = 221 pm • Si trigonal planar • 29 Si = 360 ppm 29 Si = 338, 5 ppm


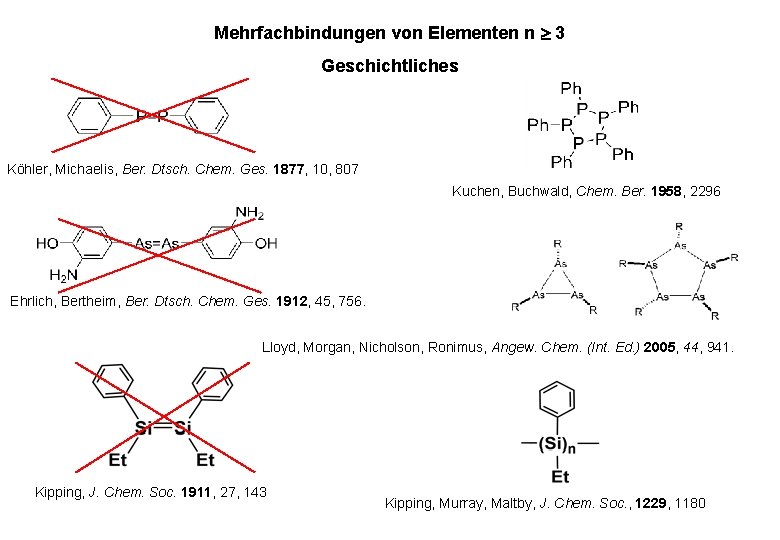
Mehrfachbindungen von Elementen n 3 Geschichtliches Köhler, Michaelis, Ber. Dtsch. Chem. Ges. 1877, 10, 807 Kuchen, Buchwald, Chem. Ber. 1958, 2296 Ehrlich, Bertheim, Ber. Dtsch. Chem. Ges. 1912, 45, 756. Lloyd, Morgan, Nicholson, Ronimus, Angew. Chem. (Int. Ed. ) 2005, 44, 941. Kipping, J. Chem. Soc. 1911, 27, 143 Kipping, Murray, Maltby, J. Chem. Soc. , 1229, 1180

Doppelbindungs Regel: Elemente jenseits der zweiten Periode des PSE bilden keine Mehrfachbindungen mit sich oder anderen Elementen. Becker 1976 Niecke 1973 Yoshifuji 1981 meanwhile. . . Brook, 1981 Bickelhaupt, 1984 Appel, 1983 West, 1981 Lappert, 1973/1986 Lappert, 1986 Cowley, 1983 Pietschnig, 2004 Sekiguchi, 2004 and many more. . .

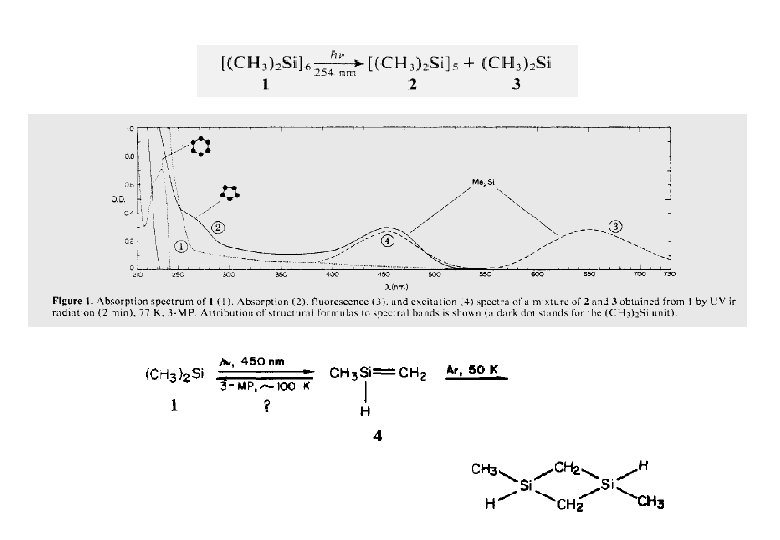
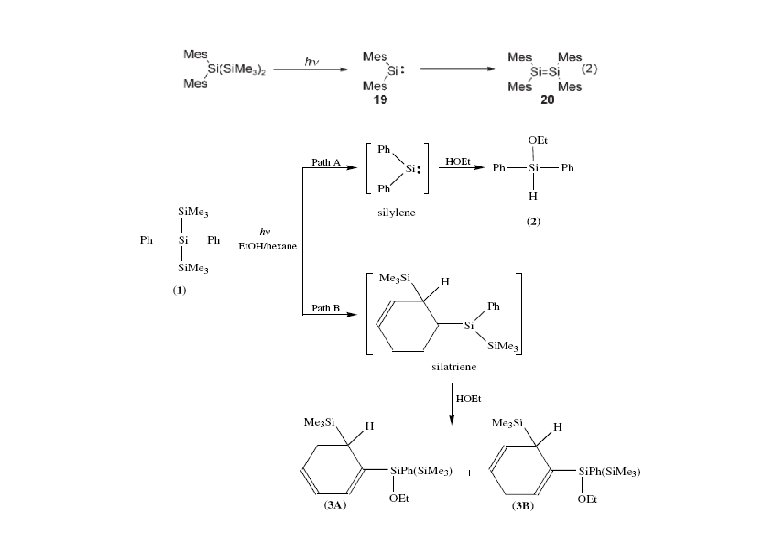
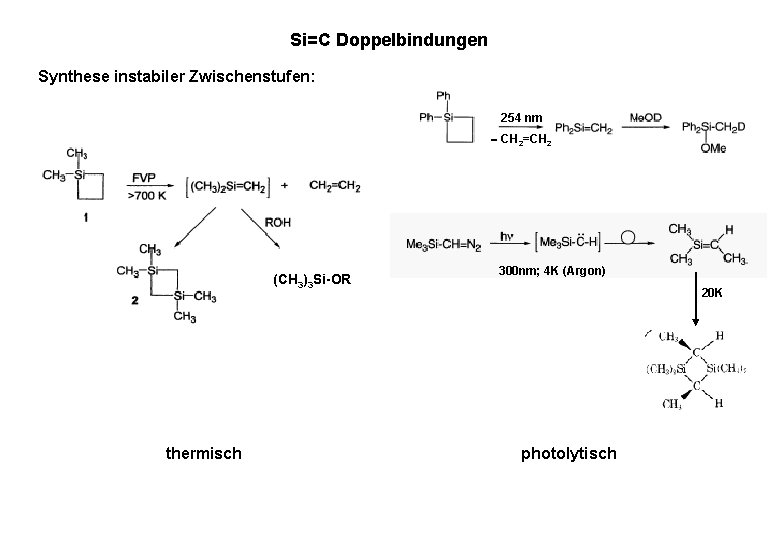
Si=C Doppelbindungen Synthese instabiler Zwischenstufen: 254 nm CH 2=CH 2 (CH 3)3 Si-OR thermisch 300 nm; 4 K (Argon) 20 K photolytisch

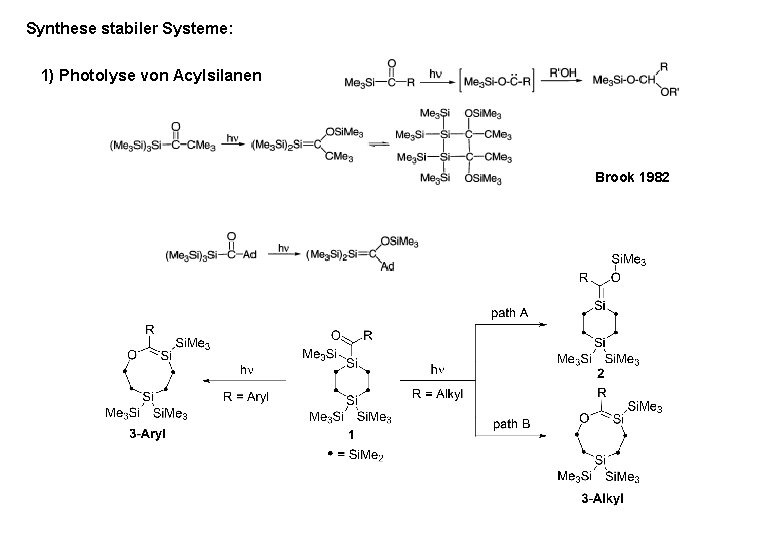
Synthese stabiler Systeme: 1) Photolyse von Acylsilanen Brook 1982

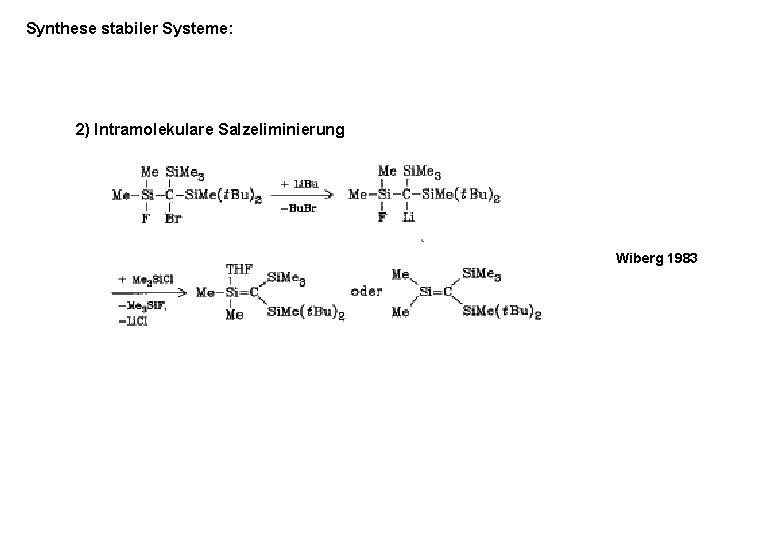
Synthese stabiler Systeme: 2) Intramolekulare Salzeliminierung Wiberg 1983

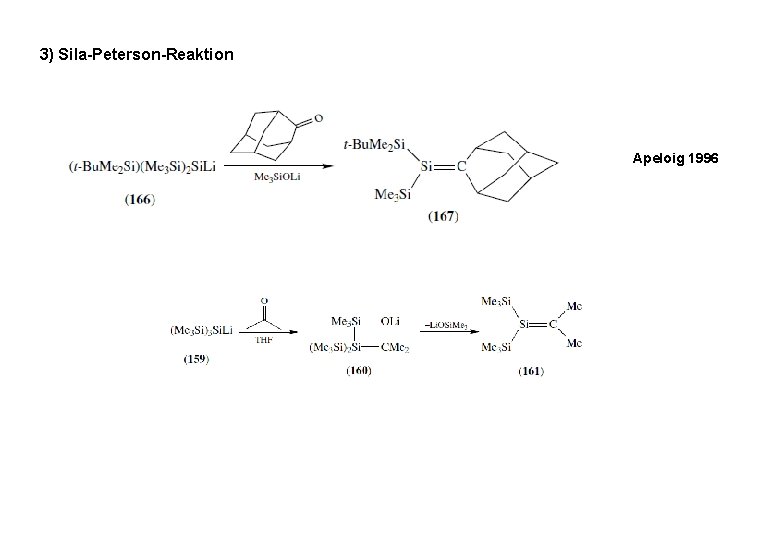
3) Sila-Peterson-Reaktion Apeloig 1996

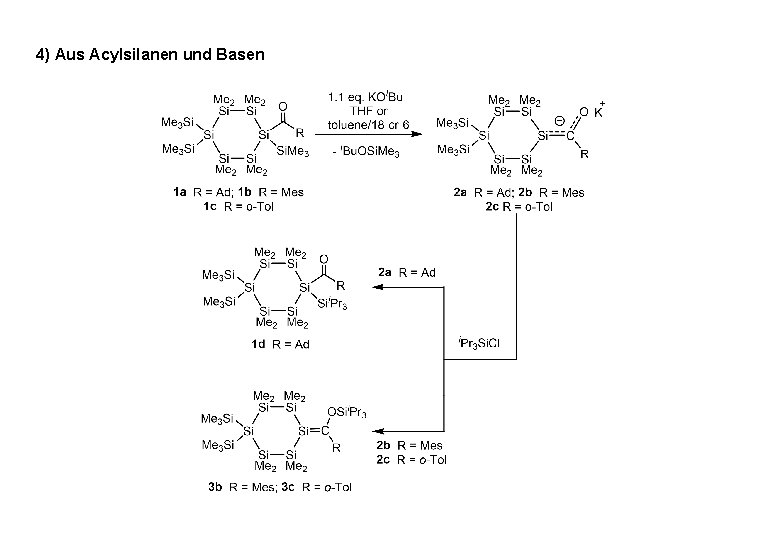
4) Aus Acylsilanen und Basen

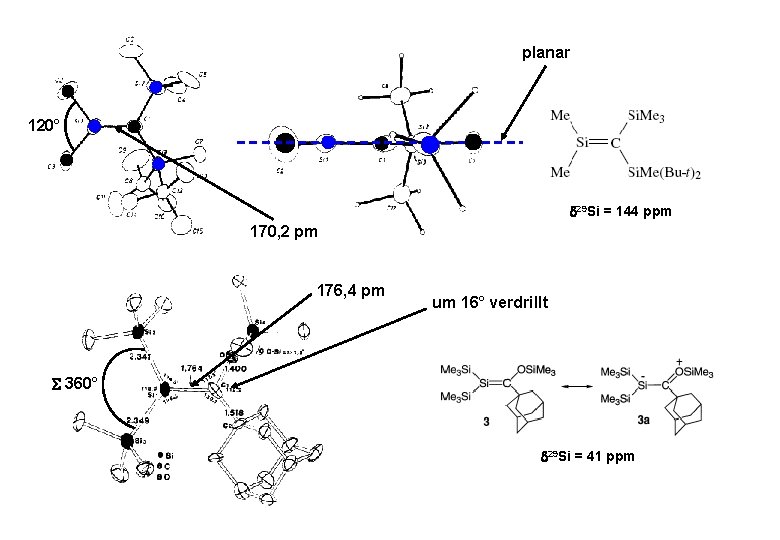
planar 120° 29 Si = 144 ppm 170, 2 pm 176, 4 pm um 16° verdrillt 360° 29 Si = 41 ppm

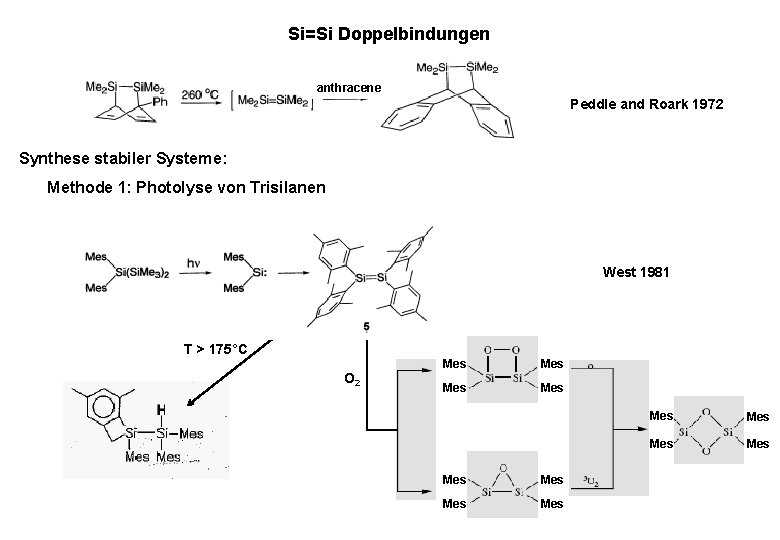
Si=Si Doppelbindungen anthracene Peddle and Roark 1972 Synthese stabiler Systeme: Methode 1: Photolyse von Trisilanen West 1981 T > 175°C O 2 Mes Mes Mes

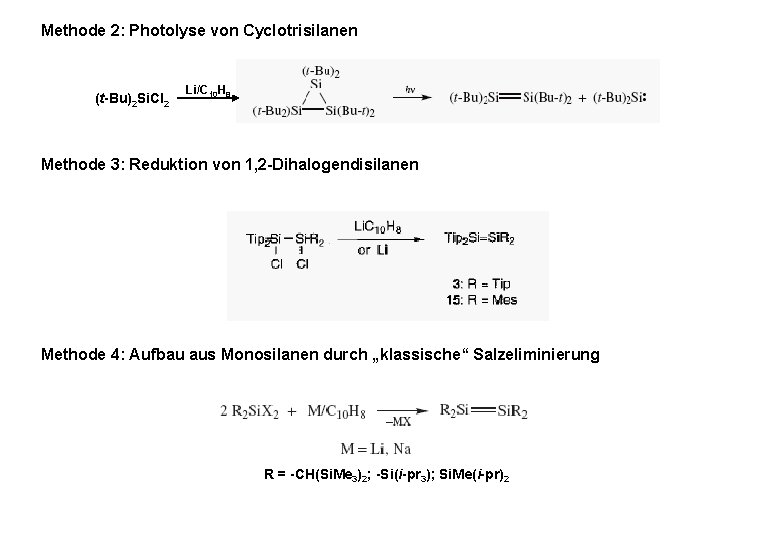
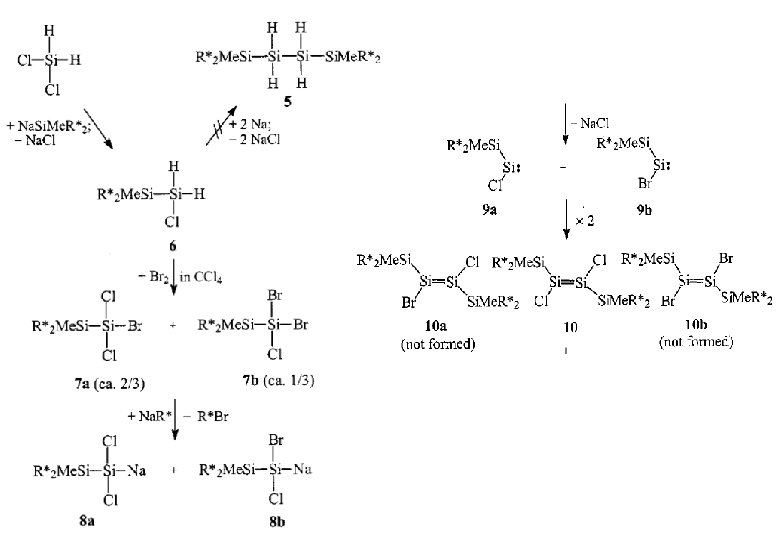
Methode 2: Photolyse von Cyclotrisilanen (t-Bu)2 Si. Cl 2 Li/C 10 H 8 Methode 3: Reduktion von 1, 2 -Dihalogendisilanen Methode 4: Aufbau aus Monosilanen durch „klassische“ Salzeliminierung R = -CH(Si. Me 3)2; -Si(i-pr 3); Si. Me(i-pr)2

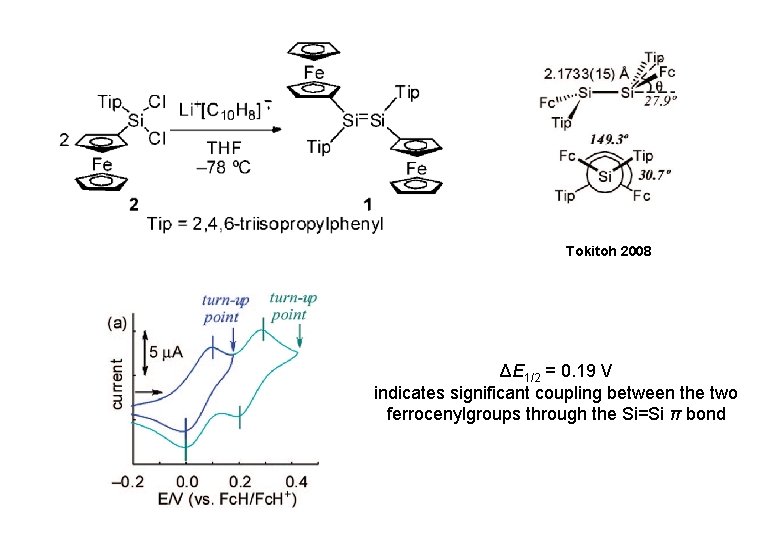
Tokitoh 2008 ΔE 1/2 = 0. 19 V indicates significant coupling between the two ferrocenylgroups through the Si=Si π bond

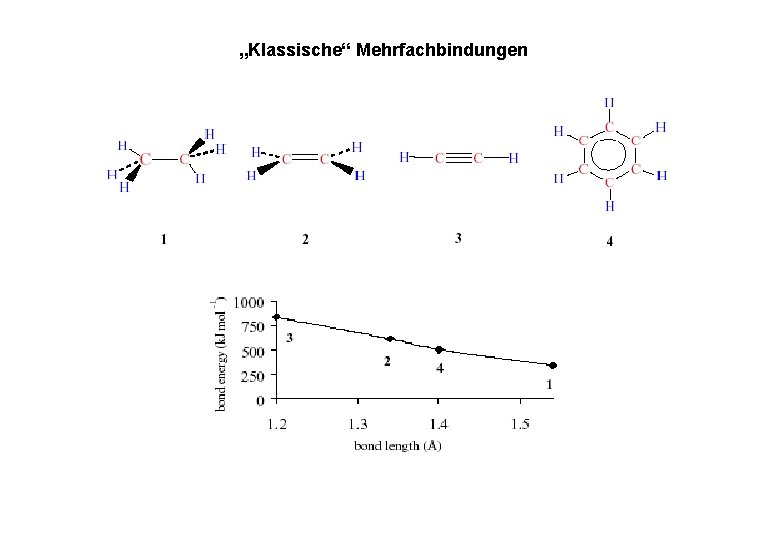
„Klassische“ Mehrfachbindungen

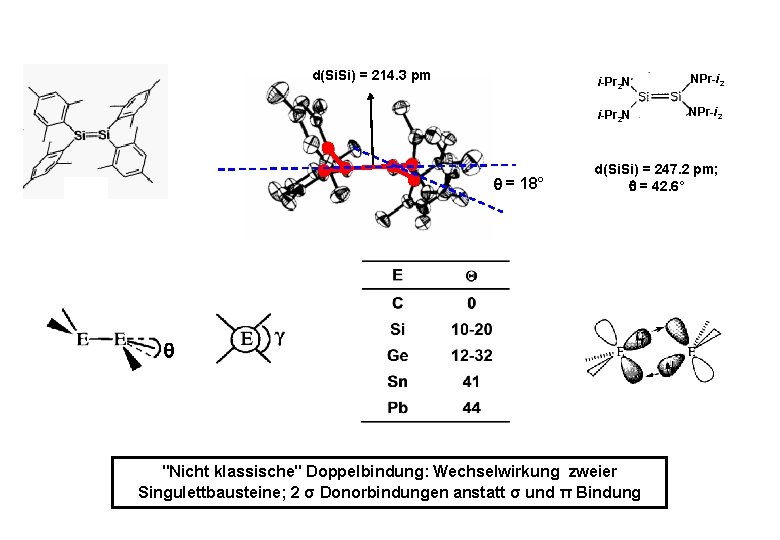
d(Si. Si) = 214. 3 pm = 18° i-Pr 2 N NPr-i 2 d(Si. Si) = 247. 2 pm; = 42. 6° "Nicht klassische" Doppelbindung: Wechselwirkung zweier Singulettbausteine; 2 σ Donorbindungen anstatt σ und π Bindung

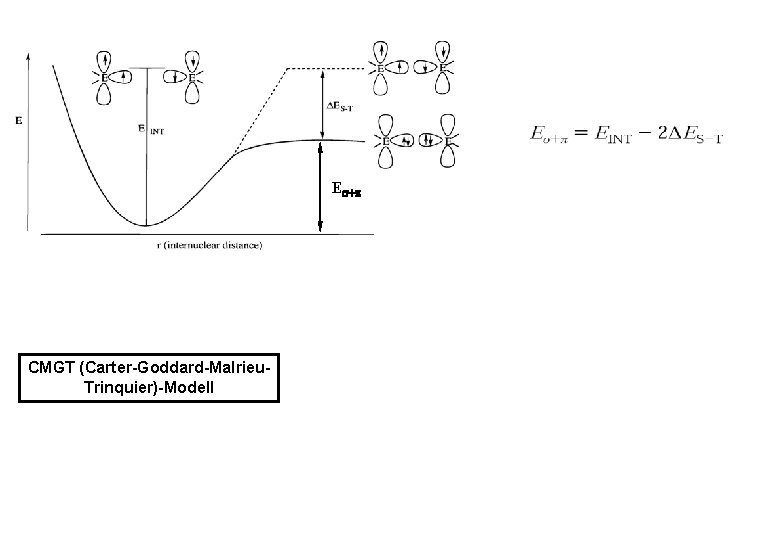
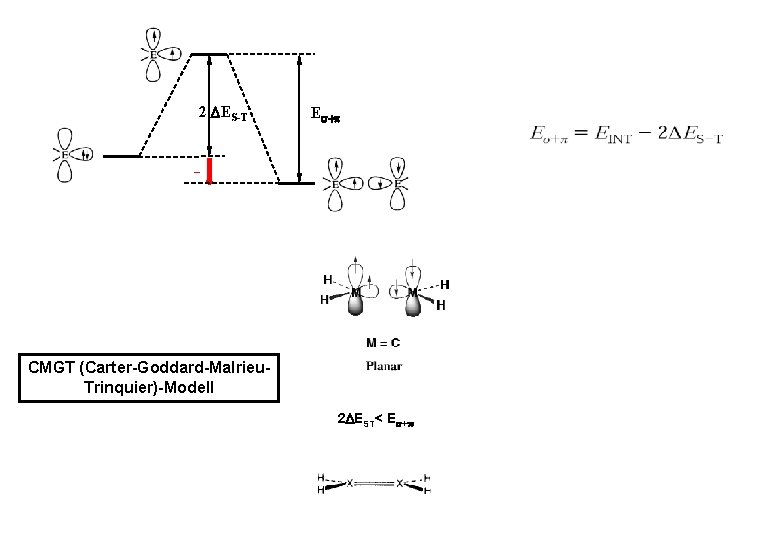
E + CMGT (Carter-Goddard-Malrieu. Trinquier)-Modell

2 ES-T E + - CMGT (Carter-Goddard-Malrieu. Trinquier)-Modell 2 EST< E +

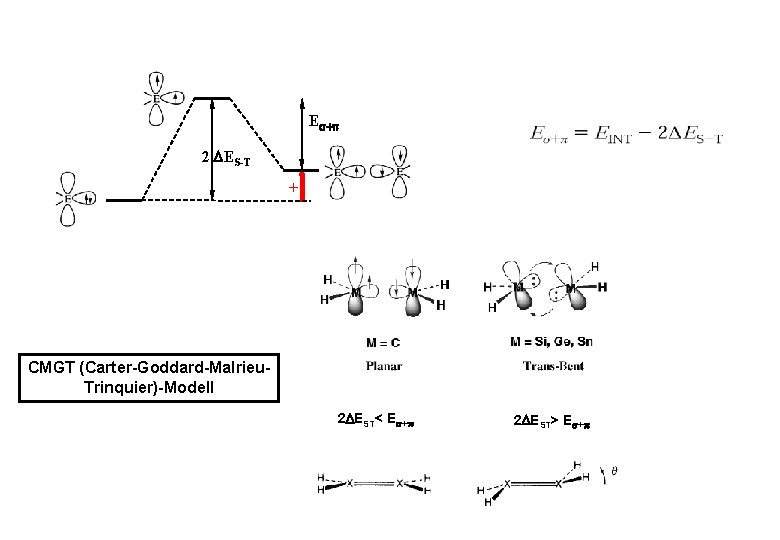
E + 2 ES-T + CMGT (Carter-Goddard-Malrieu. Trinquier)-Modell 2 EST< E + 2 EST> E +

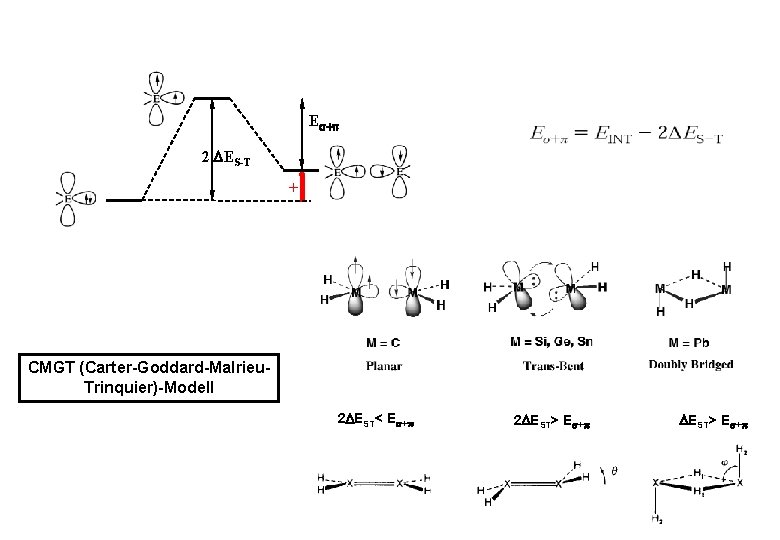
E + 2 ES-T + CMGT (Carter-Goddard-Malrieu. Trinquier)-Modell 2 EST< E + 2 EST> E +

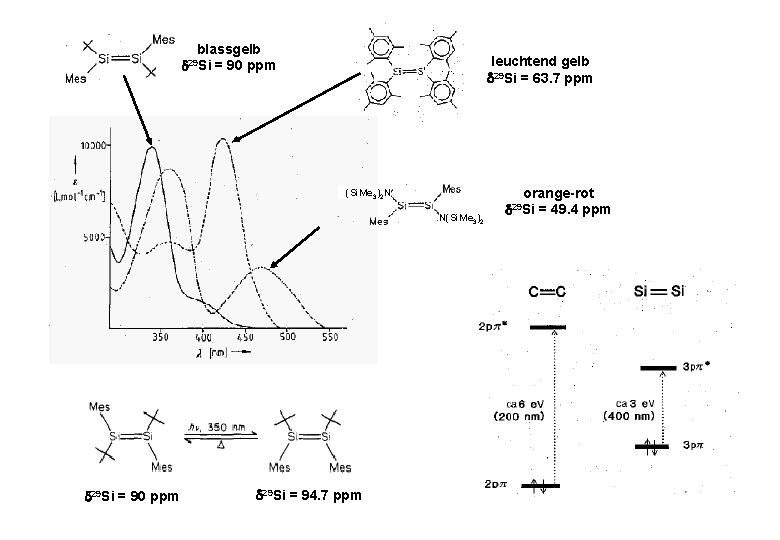
blassgelb leuchtend gelb 29 Si = 63. 7 ppm 29 Si = 90 ppm orange-rot (Si. Me 3)2 N N(Si. Me 3)2 29 Si = 90 ppm 29 Si = 94. 7 ppm 29 Si = 49. 4 ppm

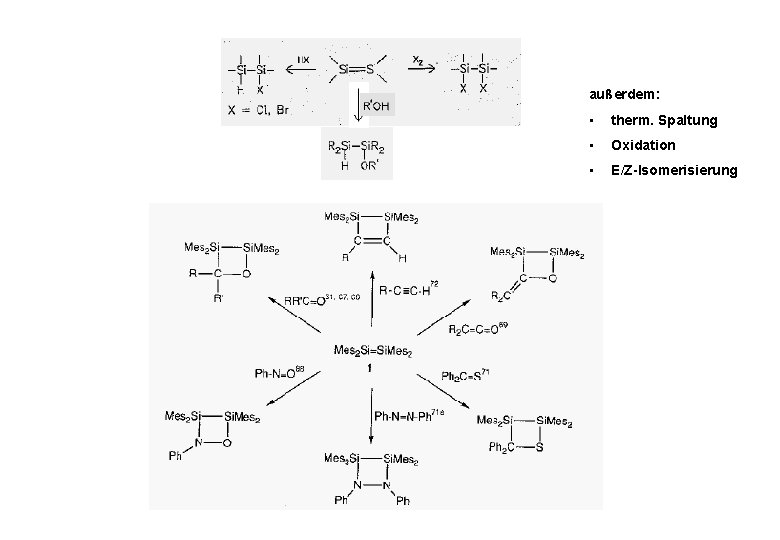
außerdem: • therm. Spaltung • Oxidation • E/Z-Isomerisierung

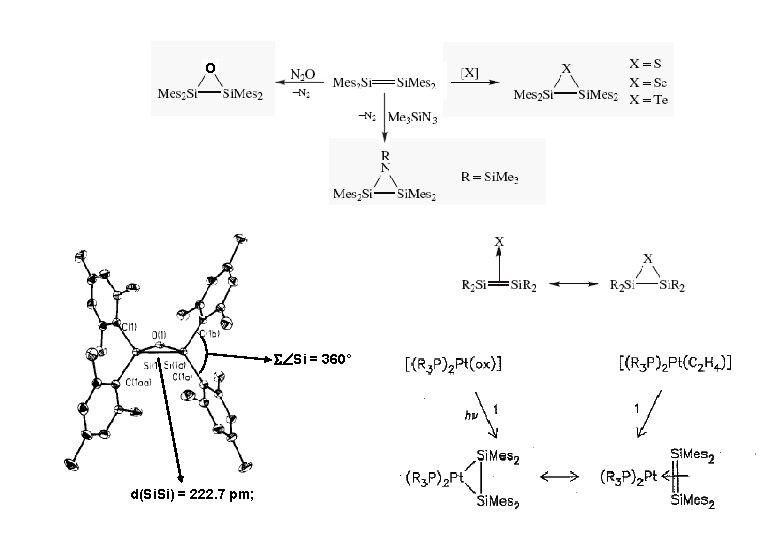
O Si = 360° d(Si. Si) = 222. 7 pm;

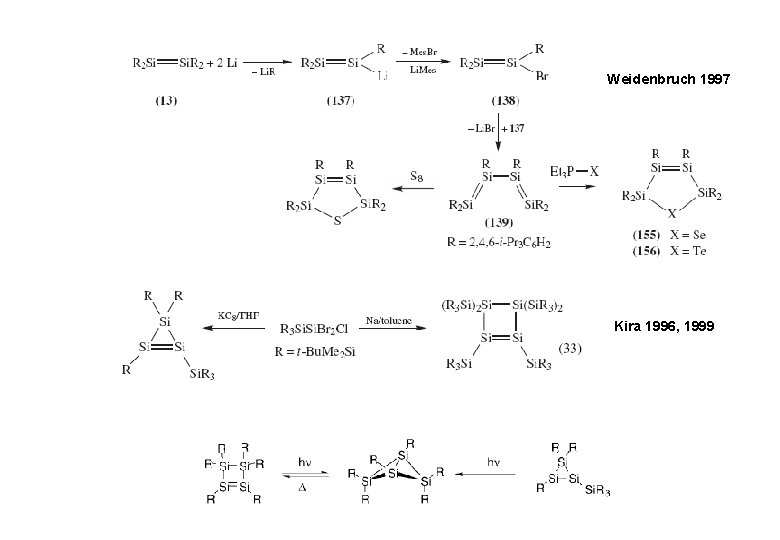
Weidenbruch 1997 Kira 1996, 1999

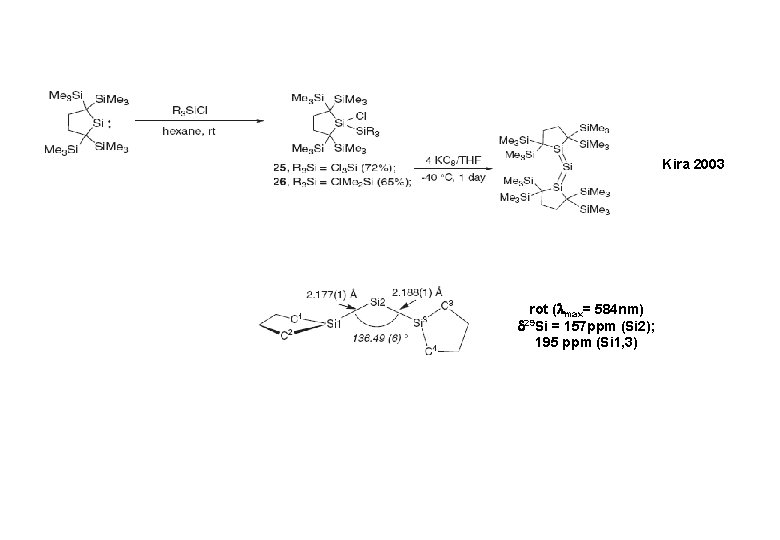
Kira 2003 rot ( max= 584 nm) 29 Si = 157 ppm (Si 2); 195 ppm (Si 1, 3)

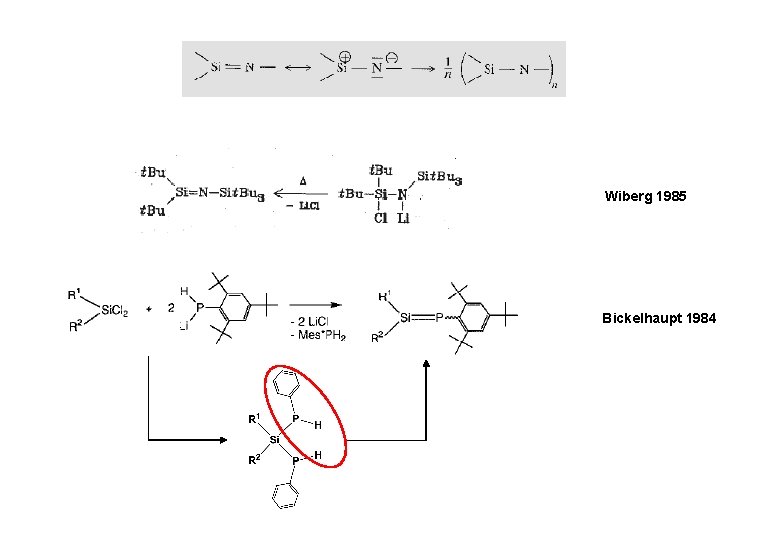
Wiberg 1985 Bickelhaupt 1984

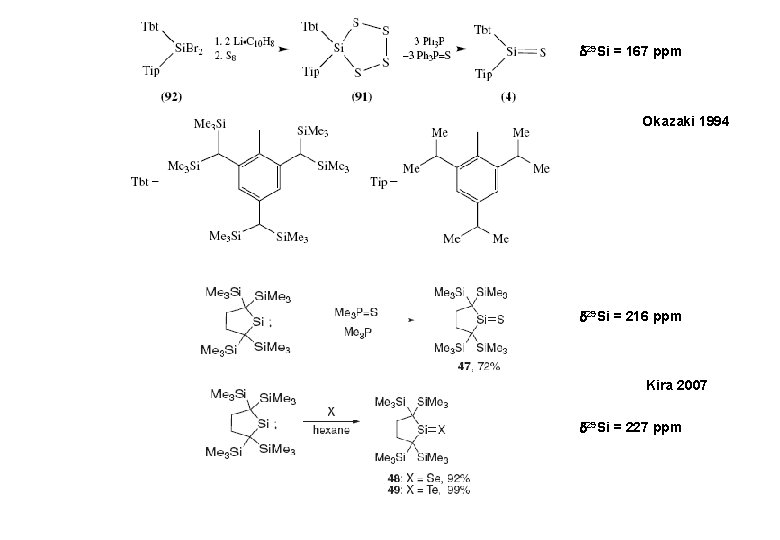
29 Si = 167 ppm Okazaki 1994 29 Si = 216 ppm Kira 2007 29 Si = 227 ppm

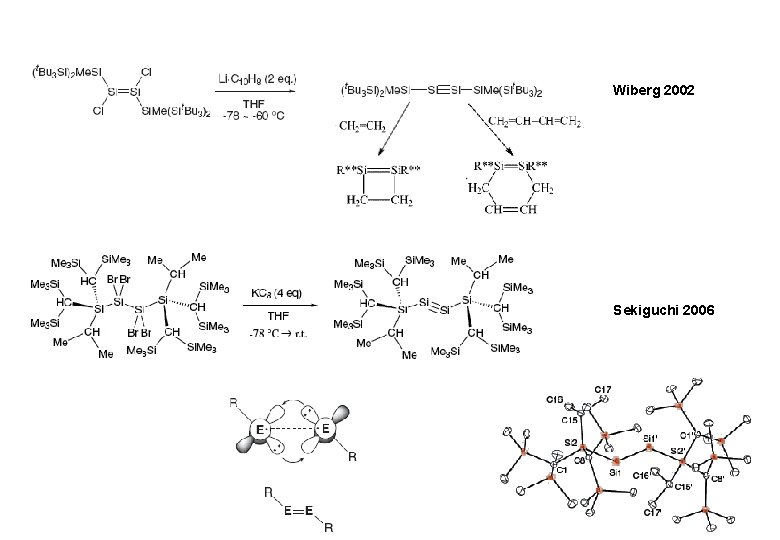
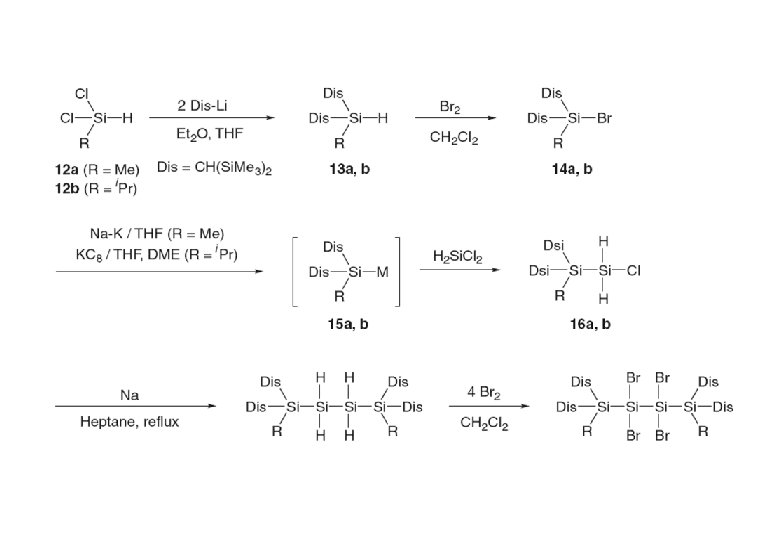
Wiberg 2002 Sekiguchi 2006



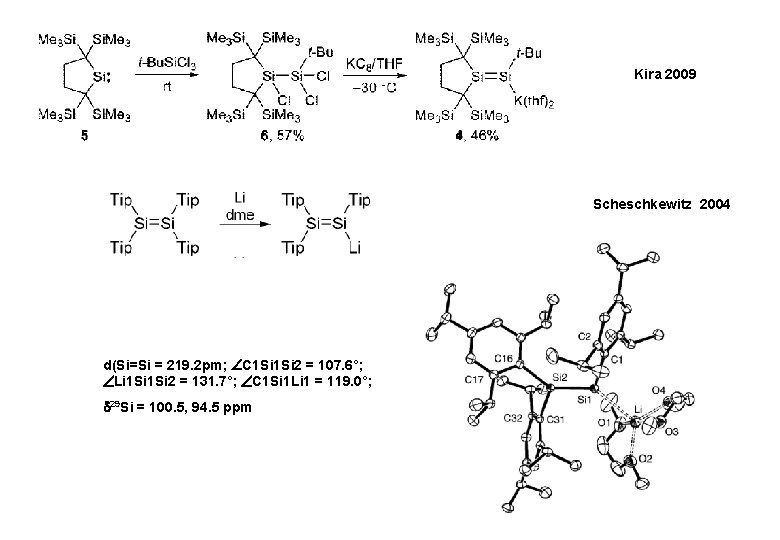
Kira 2009 Scheschkewitz 2004 d(Si=Si = 219. 2 pm; C 1 Si 2 = 107. 6°; Li 1 Si 2 = 131. 7°; C 1 Si 1 Li 1 = 119. 0°; 29 Si = 100. 5, 94. 5 ppm

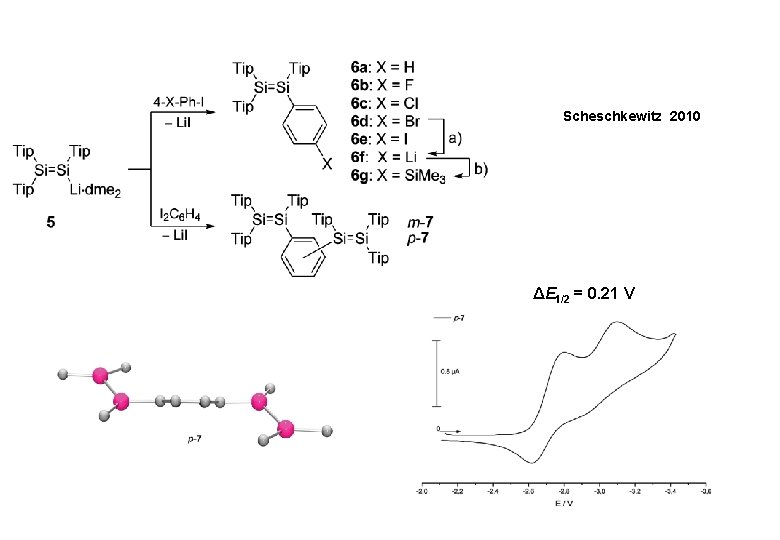
Scheschkewitz 2010 ΔE 1/2 = 0. 21 V

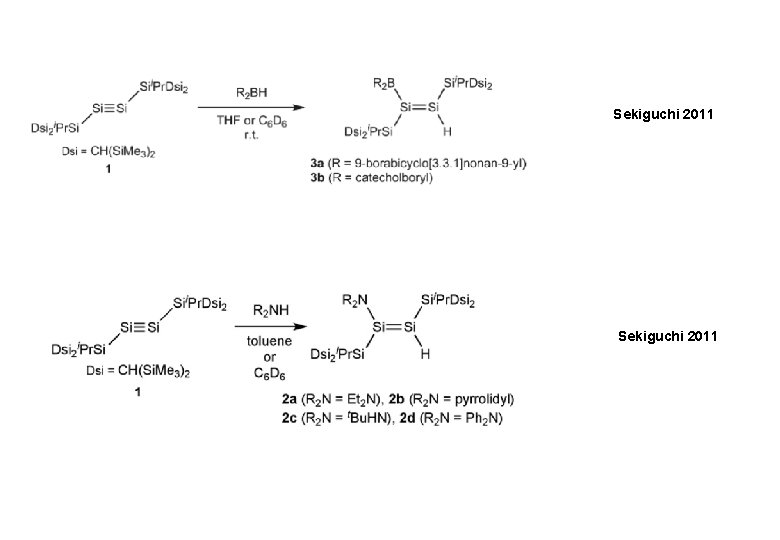
Sekiguchi 2011


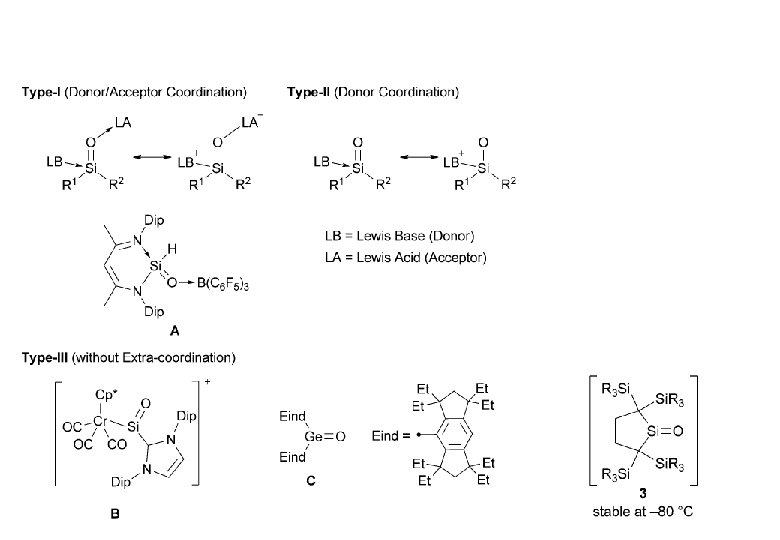
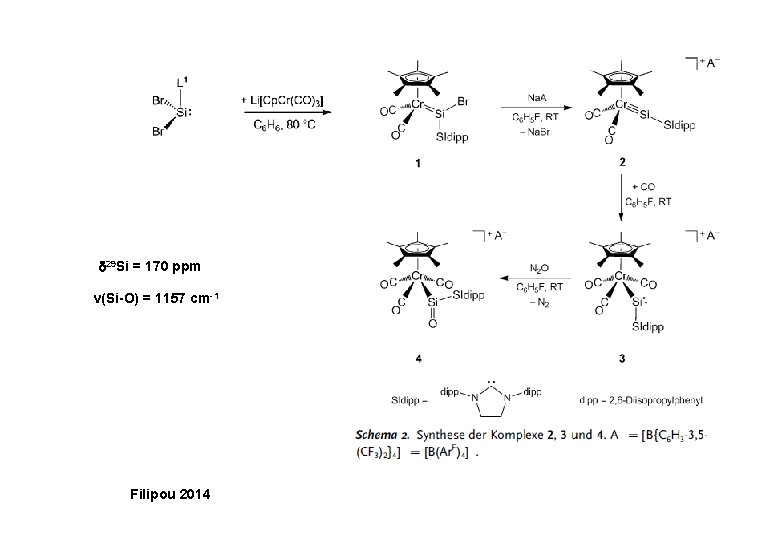
29 Si = 170 ppm ν(Si-O) = 1157 cm-1 Filipou 2014

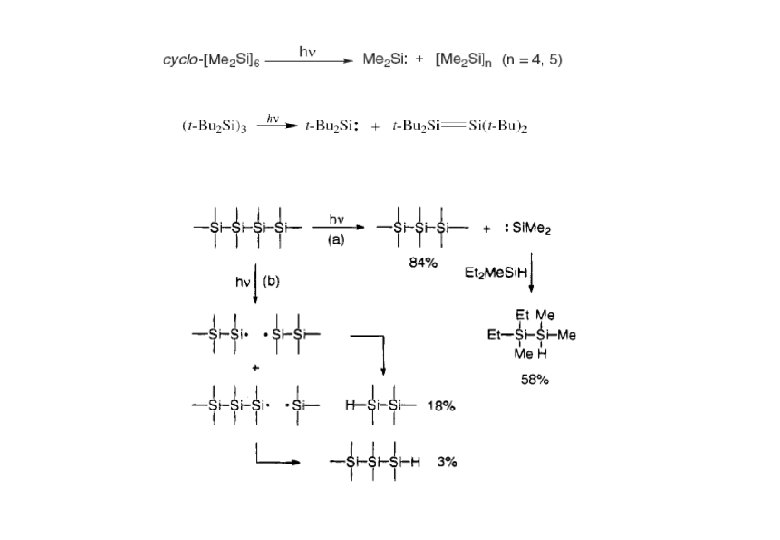
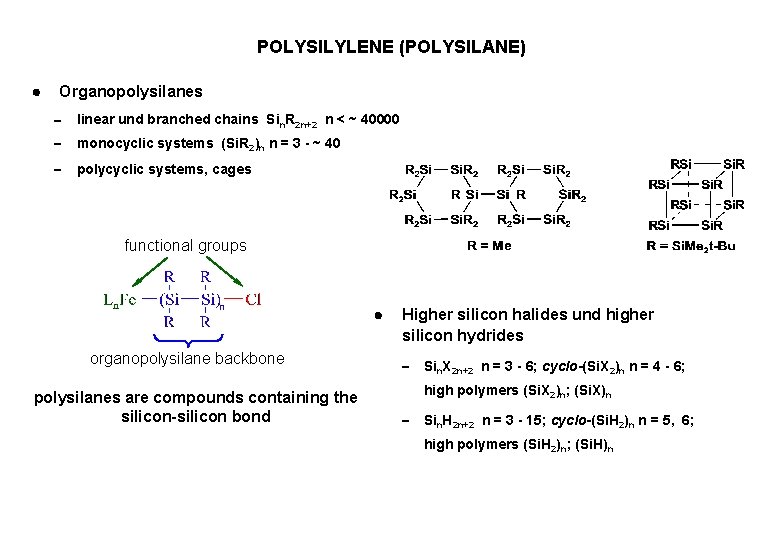
POLYSILYLENE (POLYSILANE) Organopolysilanes linear und branched chains Sin. R 2 n+2 n < ~ 40000 monocyclic systems (Si. R 2)n n = 3 - ~ 40 polycyclic systems, cages functional groups organopolysilane backbone polysilanes are compounds containing the silicon-silicon bond Higher silicon halides und higher silicon hydrides Sin. X 2 n+2 n = 3 - 6; cyclo-(Si. X 2)n n = 4 - 6; high polymers (Si. X 2)n; (Si. X)n Sin. H 2 n+2 n = 3 - 15; cyclo-(Si. H 2)n n = 5, 6; high polymers (Si. H 2)n; (Si. H)n

Metallorganische Chemie der 4. Hauptgruppe • Elektronegativitätsdifferenz E-C • energetisch passende leere Orbitale verfügbar

Si-C- Bindungsspaltung • Si-C-Bindungen sind nucleophil und elektrophil spaltbar • Reaktivität hängt vom Substrat und von den Substituenten am Si ab

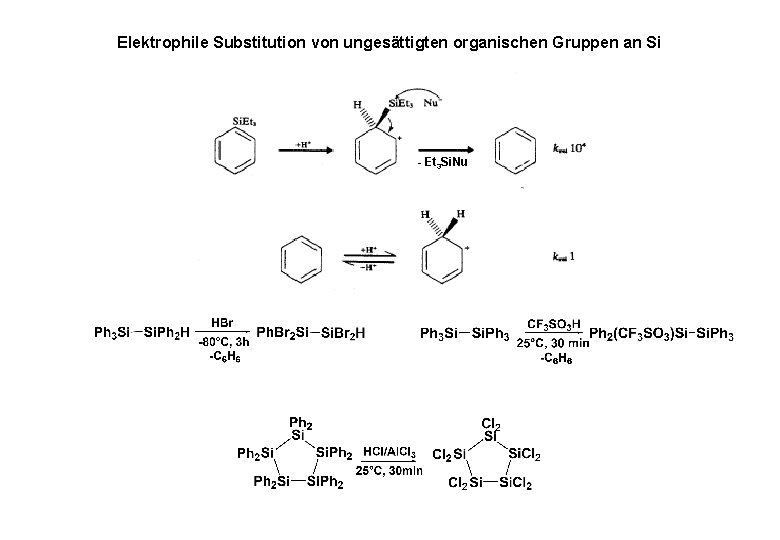
Elektrophile Substitution von ungesättigten organischen Gruppen an Si - Et 3 Si. Nu

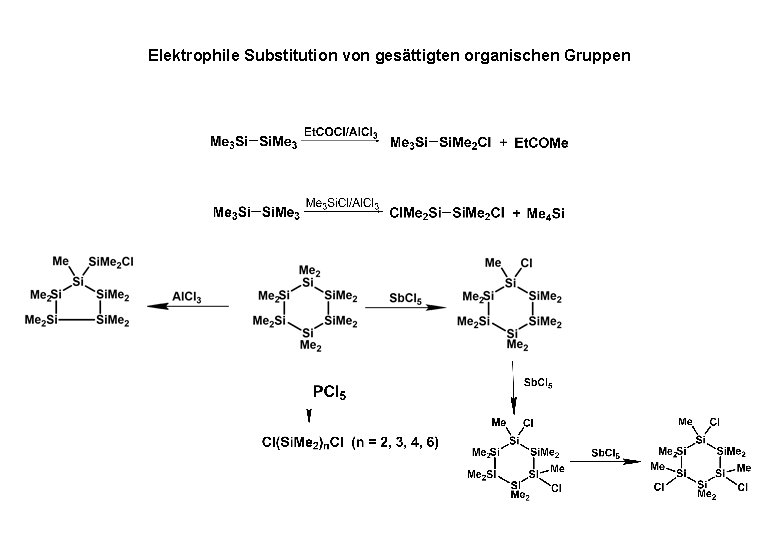
Elektrophile Substitution von gesättigten organischen Gruppen

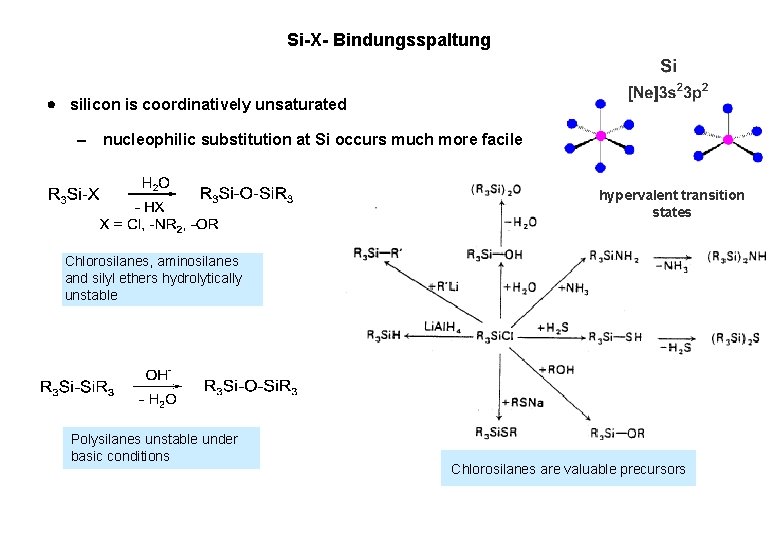
Si-X- Bindungsspaltung silicon is coordinatively unsaturated nucleophilic substitution at Si occurs much more facile hypervalent transition states Chlorosilanes, aminosilanes and silyl ethers hydrolytically unstable Polysilanes unstable under basic conditions Chlorosilanes are valuable precursors

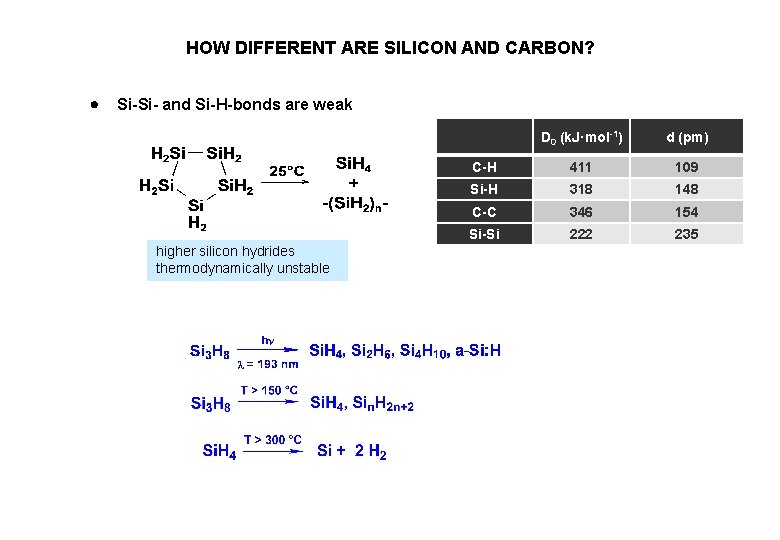
HOW DIFFERENT ARE SILICON AND CARBON? Si-Si- and Si-H-bonds are weak higher silicon hydrides thermodynamically unstable D 0 (k. J·mol-1) d (pm) C-H 411 109 Si-H 318 148 C-C 346 154 Si-Si 222 235

HOW DIFFERENT ARE SILICON AND CARBON? the polarity of the Si-H bond is reversed H is a good leaving group Electronegativity (Pauling) silicon hydrides are easily oxidized and often pyrophoric in air H 2. 2 C 2. 55 Si 1. 9 silanes react readily with H 2 O and O 2 silicon hydrides are pyrophoric in air and unstable upon storage in glass vessels

HOW DIFFERENT ARE SILICON AND CARBON? multiple bonds to silicon are weak, while certain single bonds Si-X (X = O, Cl, F. . . ) are unusually strong

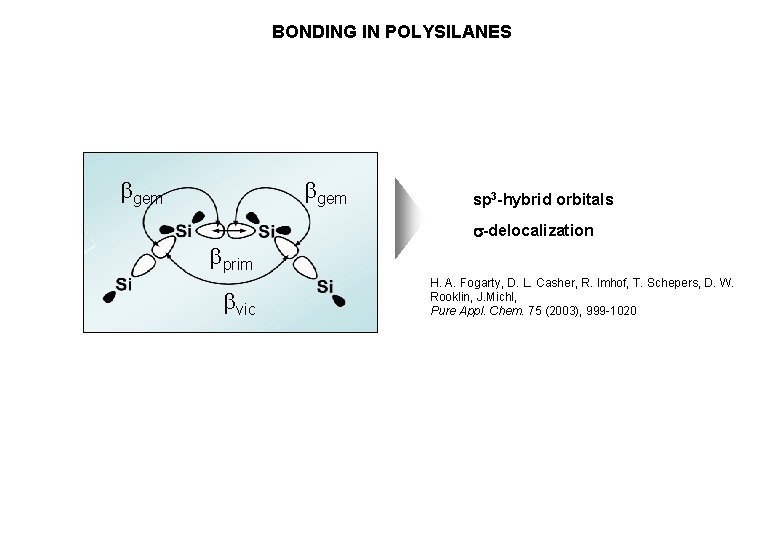
BONDING IN POLYSILANES gem prim vic sp 3 -hybrid orbitals -delocalization H. A. Fogarty, D. L. Casher, R. Imhof, T. Schepers, D. W. Rooklin, J. Michl, Pure Appl. Chem. 75 (2003), 999 -1020

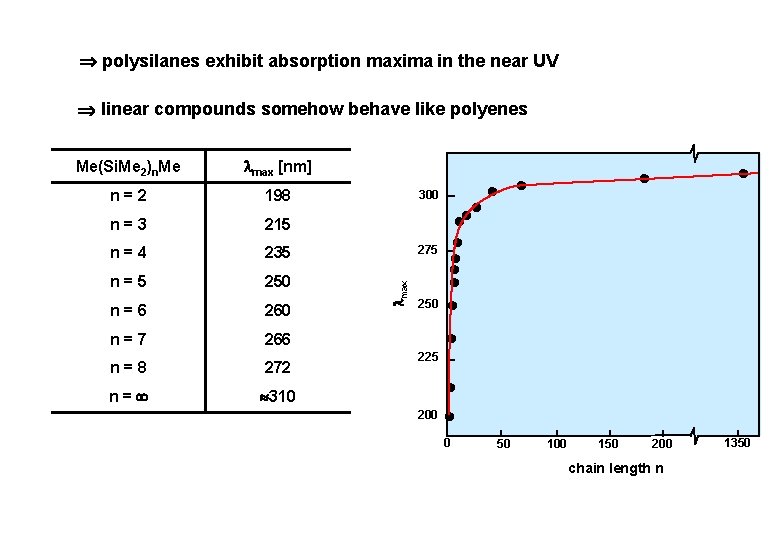
polysilanes exhibit absorption maxima in the near UV linear compounds somehow behave like polyenes max [nm] n = 2 198 n = 3 215 n = 4 235 n = 5 250 n = 6 260 n = 7 266 n = 8 272 n = 310 300 max Me(Si. Me 2)n. Me 275 250 225 200 0 50 100 150 200 chain length n 1350

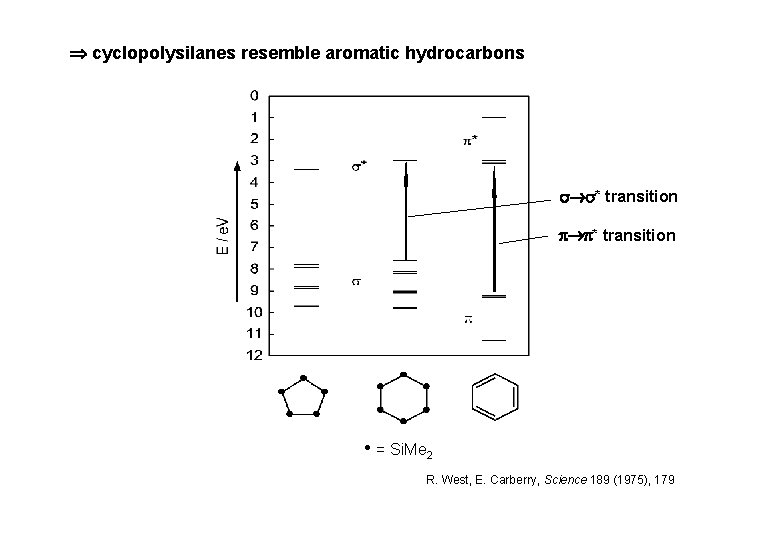
cyclopolysilanes resemble aromatic hydrocarbons * transition • = Si. Me 2 R. West, E. Carberry, Science 189 (1975), 179

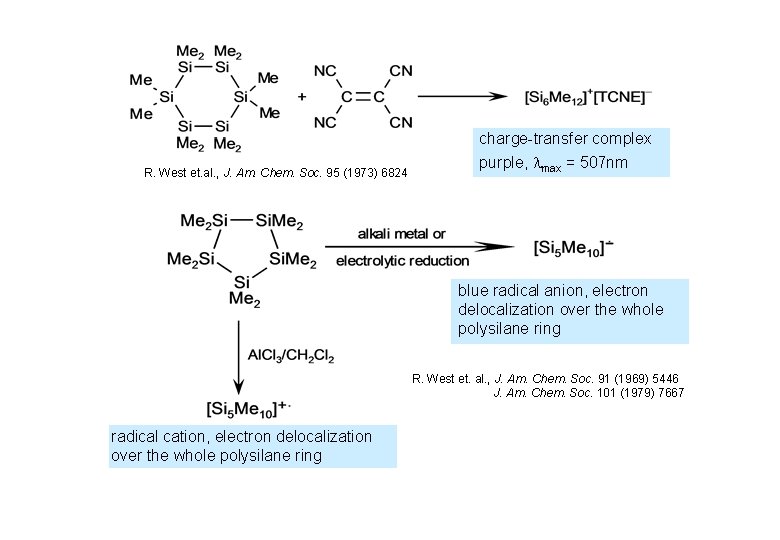
R. West et. al. , J. Am. Chem. Soc. 95 (1973) 6824 charge-transfer complex purple, max = 507 nm blue radical anion, electron delocalization over the whole polysilane ring R. West et. al. , J. Am. Chem. Soc. 91 (1969) 5446 J. Am. Chem. Soc. 101 (1979) 7667 radical cation, electron delocalization over the whole polysilane ring
![Þ polysilanes exhibit pronounced substituent effects hyperconjugation ionization energy e V max Þ polysilanes exhibit pronounced substituent effects ( - -hyperconjugation) ionization energy [e. V] max](https://slidetodoc.com/presentation_image_h/838df3d7518284022ff2abfc01556c0b/image-86.jpg)
Þ polysilanes exhibit pronounced substituent effects ( - -hyperconjugation) ionization energy [e. V] max [nm] ( ) 8. 35 s + (Si-Si) 9. 25 (e 1 g) 9. 07 as 8. 69 (Si-Si) Me 3 Si. Me 3 198 (8000) Ph. Me 2 Si. Me 3 231 (11000) Ph. Me 2 Si. Me 2 Ph 236 (18000) Ph 3 Si. Ph 3 246 (32000) Si. Me 3 Si. Me 2 10. 03 s - (Si-Si) - hyperconjugation X Si. Me 3 Si. Me 2 -n hyperconjugation

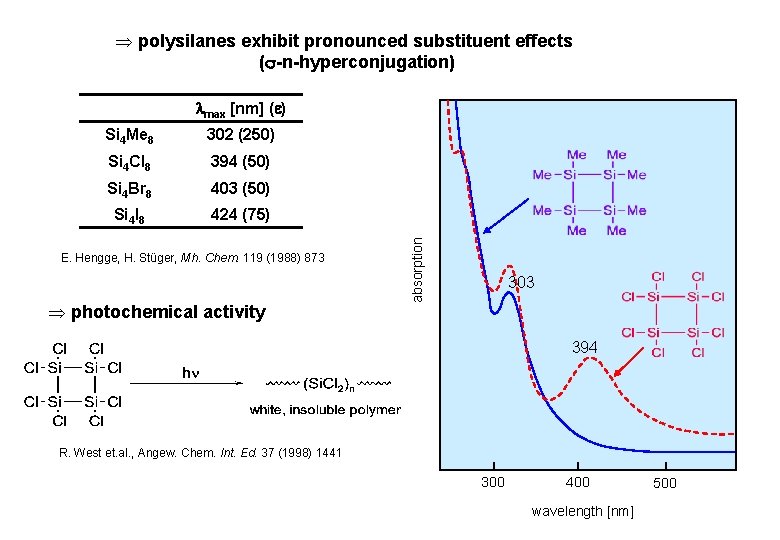
Þ polysilanes exhibit pronounced substituent effects ( -n-hyperconjugation) Si 4 Me 8 302 (250) Si 4 Cl 8 394 (50) Si 4 Br 8 403 (50) Si 4 I 8 424 (75) E. Hengge, H. Stüger, Mh. Chem. 119 (1988) 873 Þ photochemical activity absorption max [nm] ( ) 303 394 R. West et. al. , Angew. Chem. Int. Ed. 37 (1998) 1441 300 400 wavelength [nm] 500

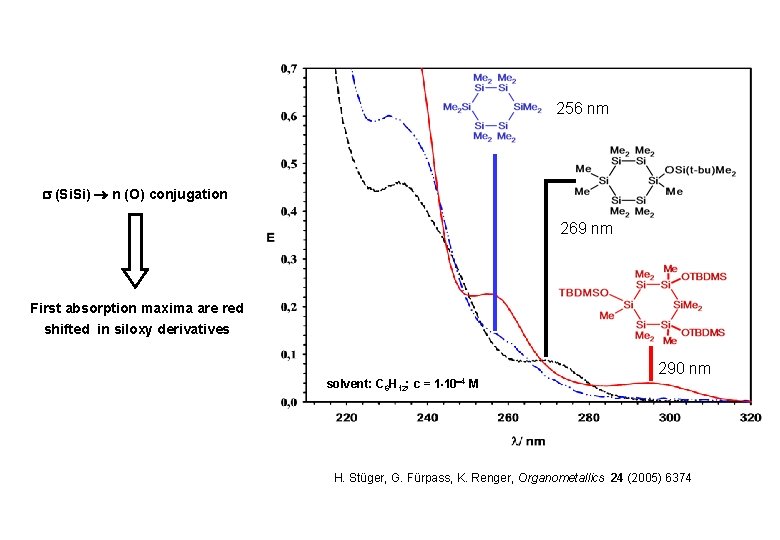
256 nm (Si. Si) n (O) conjugation 269 nm First absorption maxima are red shifted in siloxy derivatives solvent: C 6 H 12; c = 1 10 4 M 290 nm H. Stüger, G. Fürpass, K. Renger, Organometallics 24 (2005) 6374

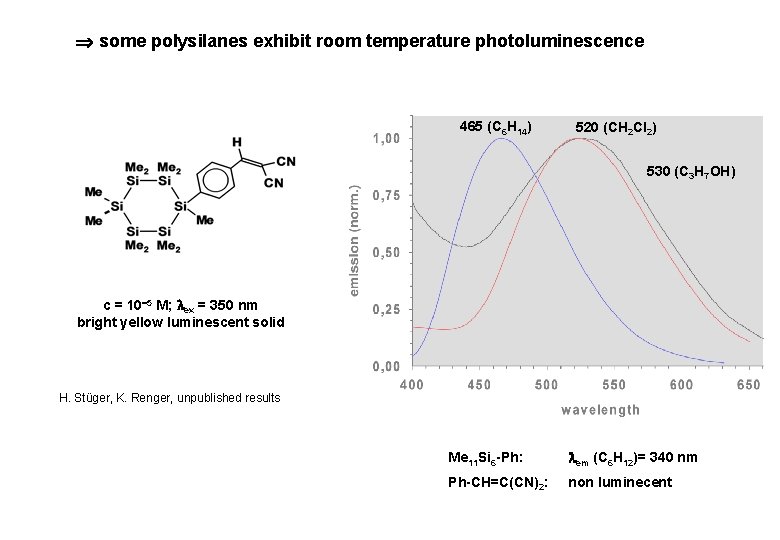
some polysilanes exhibit room temperature photoluminescence 465 (C 6 H 14) 520 (CH 2 Cl 2) 530 (C 3 H 7 OH) c = 10 5 M; ex = 350 nm bright yellow luminescent solid H. Stüger, K. Renger, unpublished results Me 11 Si 6 -Ph: em (C 6 H 12)= 340 nm Ph-CH=C(CN)2: non luminecent

polysilanes exhibit properties with technological potential starting materials for Si/N-, Si/C- or metal silicide ceramics or fibers; near UV photoresists; photo and charge conducting materials, emissive layers in integrated circuits etc. properties may be tuned by variation of backbone structure and/or substituents Yajima et. al. , (1976) -silicon carbide (Ph. Me. Si)n; (hexyl. Me. Si)n are soluble, meltable; can be used without prepyrolysis West et. al. , (1982)

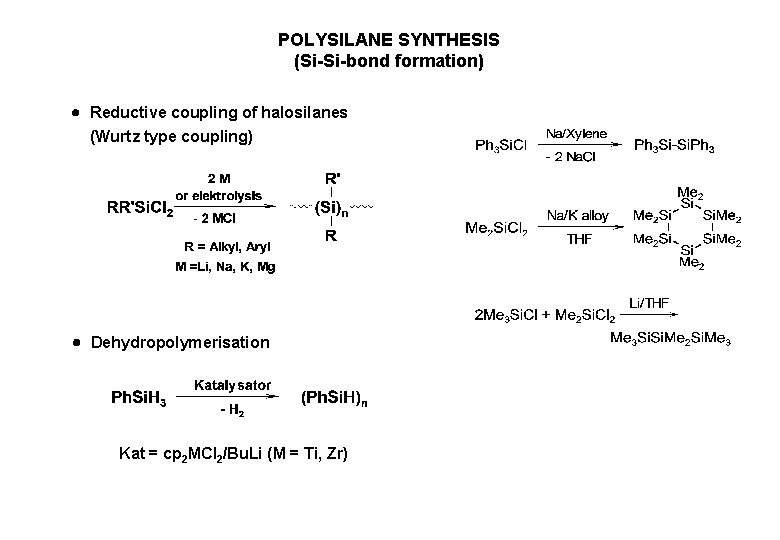
POLYSILANE SYNTHESIS (Si-Si-bond formation) Reductive coupling of halosilanes (Wurtz type coupling) Dehydropolymerisation Kat = cp 2 MCl 2/Bu. Li (M = Ti, Zr)

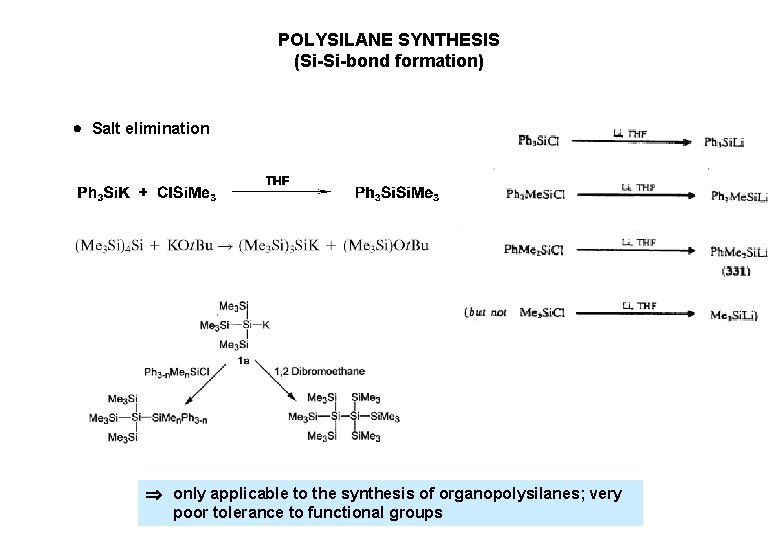
POLYSILANE SYNTHESIS (Si-Si-bond formation) Salt elimination only applicable to the synthesis of organopolysilanes; very poor tolerance to functional groups

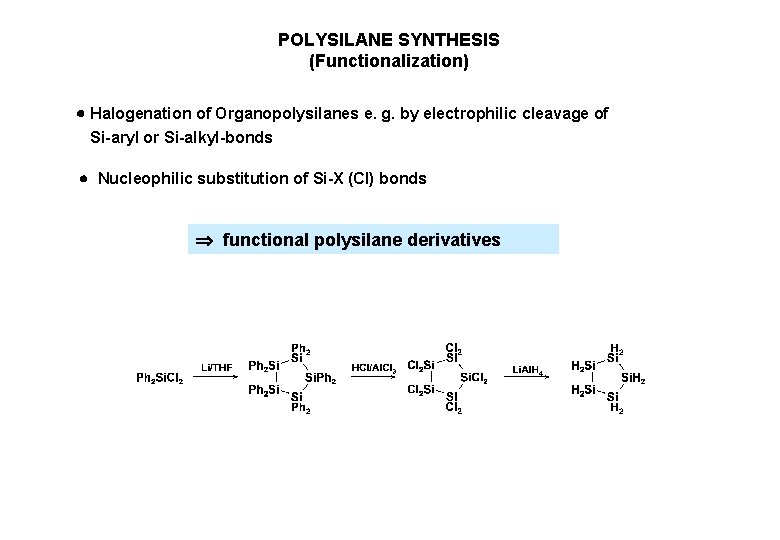
POLYSILANE SYNTHESIS (Functionalization) Halogenation of Organopolysilanes e. g. by electrophilic cleavage of Si-aryl or Si-alkyl-bonds Nucleophilic substitution of Si-X (Cl) bonds functional polysilane derivatives

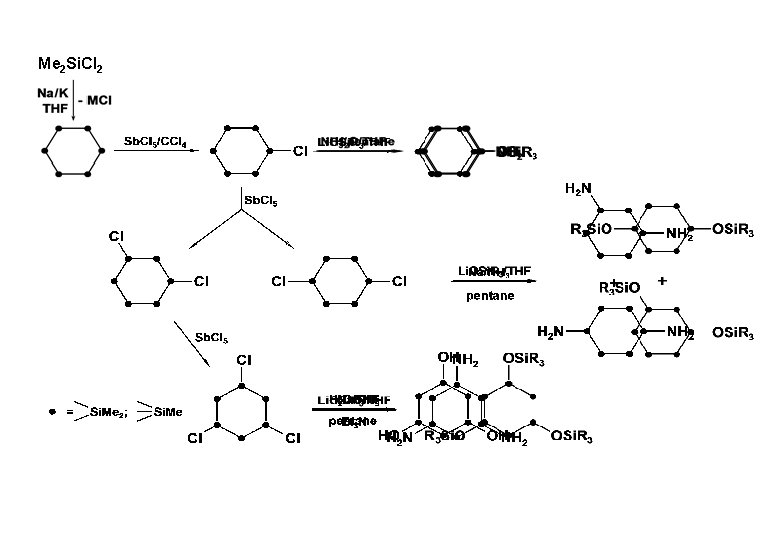
Me 2 Si. Cl 2 +

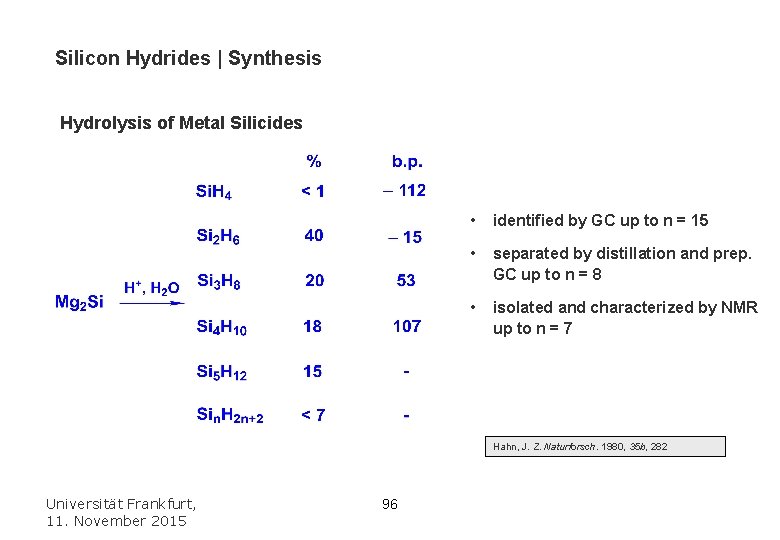
Higher Silicon Hydrides | Synthesis Hydrolysis of Metal Silicides • reasonable yield in a semi-technical scale (80 kg Mg 2 Si afford 2. 8 l crude silane / day) • large amounts of salt (200 kg Mg. Cl 2 from 80 kg Mg 2 Si) • complex product mixtures • tedious synthetic procedure Fehér, F. ; Schinkitz, F. D. ; Schaaf, J. Z. anorg. allgem. Chem. 1971, 383, 303 Universität Frankfurt, 11. November 2015 95

Silicon Hydrides | Synthesis Hydrolysis of Metal Silicides • identified by GC up to n = 15 • separated by distillation and prep. GC up to n = 8 • isolated and characterized by NMR up to n = 7 Hahn, J. Z. Naturforsch. 1980, 35 b, 282 Universität Frankfurt, 11. November 2015 96

Silicon Hydrides | Synthesis electrode from Monosilane gas in/out • technical production of di- and trisilane • problem: formation of considerable amounts of solid Sin. Hm Spanier, E. J. ; Mac. Diarmid, A. G. Inorg. Chem. 1962, 1, 432 Gokhale, S. D. ; Drake, J. E. ; Jolly, W. L. J. Inorg. Nucl. Chem. 1965, 27, 1911 Akhtar, M. Synth. React. Inorg. Metal-Org. Chem. 1986, 16, 729 cooling fluid electrode cooling fluid gas in/out Universität Frankfurt, 11. November 2015 97

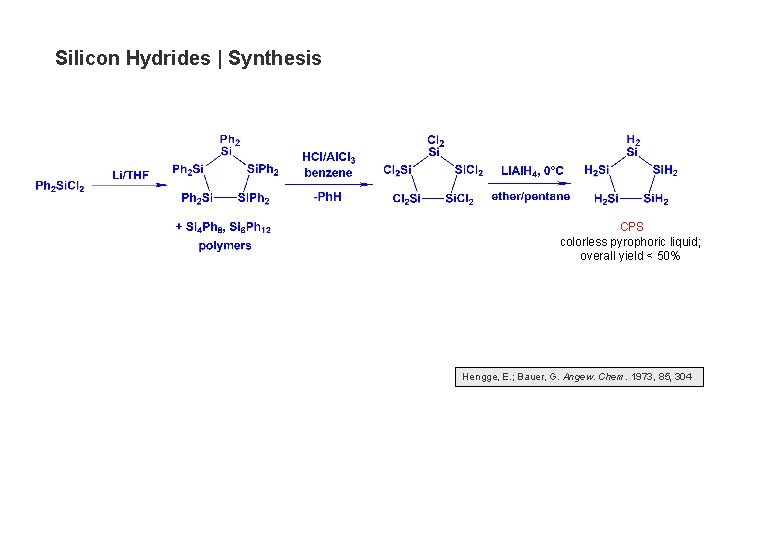
Silicon Hydrides | Synthesis CPS colorless pyrophoric liquid; overall yield < 50% Hengge, E. ; Bauer, G. Angew. Chem. 1973, 85, 304

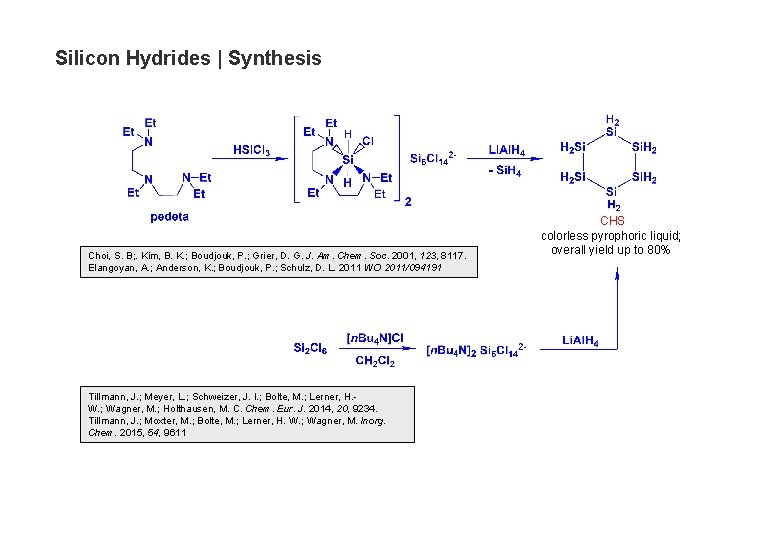
Silicon Hydrides | Synthesis Choi, S. B; . Kim, B. K. ; Boudjouk, P. ; Grier, D. G. J. Am. Chem. Soc. 2001, 123, 8117. Elangoyan, A. ; Anderson, K. ; Boudjouk, P. ; Schulz, D. L. 2011 WO 2011/094191 Tillmann, J. ; Meyer, L. ; Schweizer, J. I. ; Bolte, M. ; Lerner, H. W. ; Wagner, M. ; Holthausen, M. C. Chem. Eur. J. 2014, 20, 9234. Tillmann, J. ; Moxter, M. ; Bolte, M. ; Lerner, H. W. ; Wagner, M. Inorg. Chem. 2015, 54, 9611 CHS colorless pyrophoric liquid; overall yield up to 80%

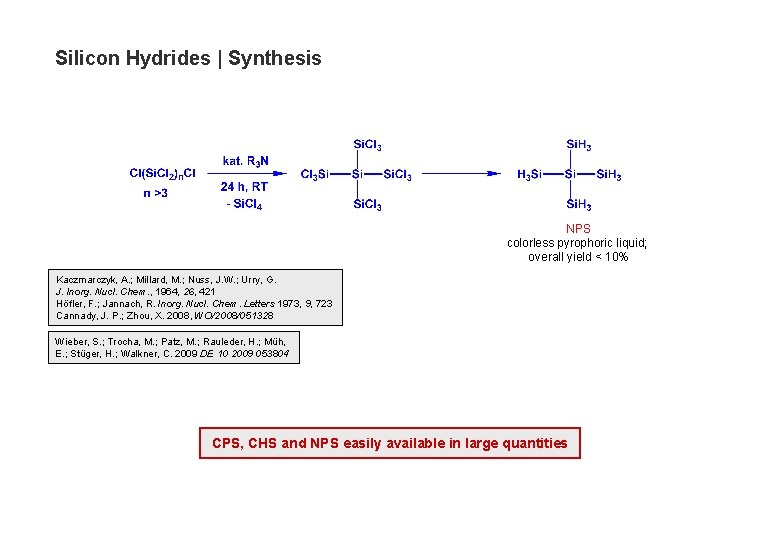
Silicon Hydrides | Synthesis NPS colorless pyrophoric liquid; overall yield < 10% Kaczmarczyk, A. ; Millard, M. ; Nuss, J. W. ; Urry, G. J. Inorg. Nucl. Chem. , 1964, 26, 421 Höfler, F. ; Jannach, R. Inorg. Nucl. Chem. Letters 1973, 9, 723 Cannady, J. P. ; Zhou, X. 2008, WO/2008/051328 Wieber, S. ; Trocha, M. ; Patz, M. ; Rauleder, H. ; Müh, E. ; Stüger, H. ; Walkner, C. 2009 DE 10 2009 053804 CPS, CHS and NPS easily available in large quantities

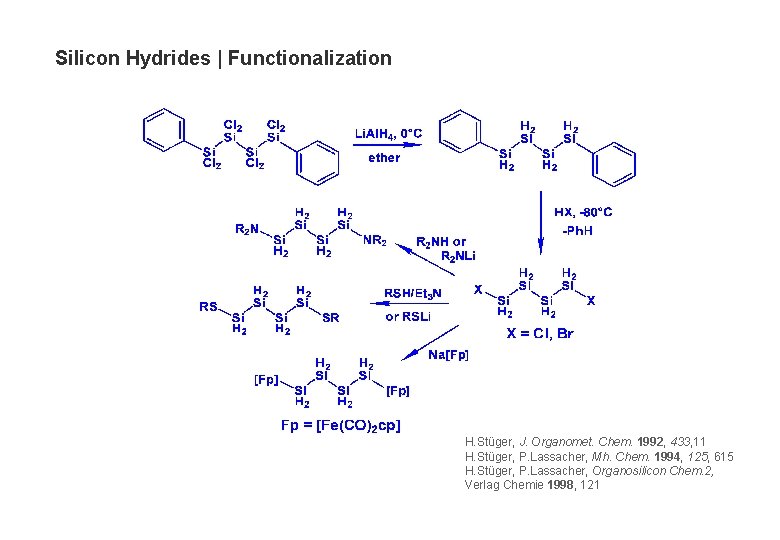
Silicon Hydrides | Functionalization H. Stüger, J. Organomet. Chem. 1992, 433, 11 H. Stüger, P. Lassacher, Mh. Chem. 1994, 125, 615 H. Stüger, P. Lassacher, Organosilicon Chem. 2, Verlag Chemie 1998, 121

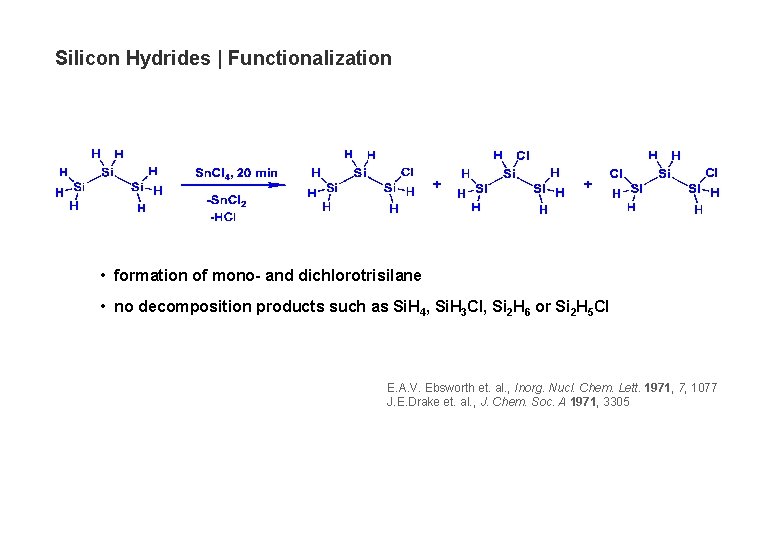
Silicon Hydrides | Functionalization • formation of mono- and dichlorotrisilane • no decomposition products such as Si. H 4, Si. H 3 CI, Si 2 H 6 or Si 2 H 5 CI E. A. V. Ebsworth et. al. , Inorg. Nucl. Chem. Lett. 1971, 7, 1077 J. E. Drake et. al. , J. Chem. Soc. A 1971, 3305

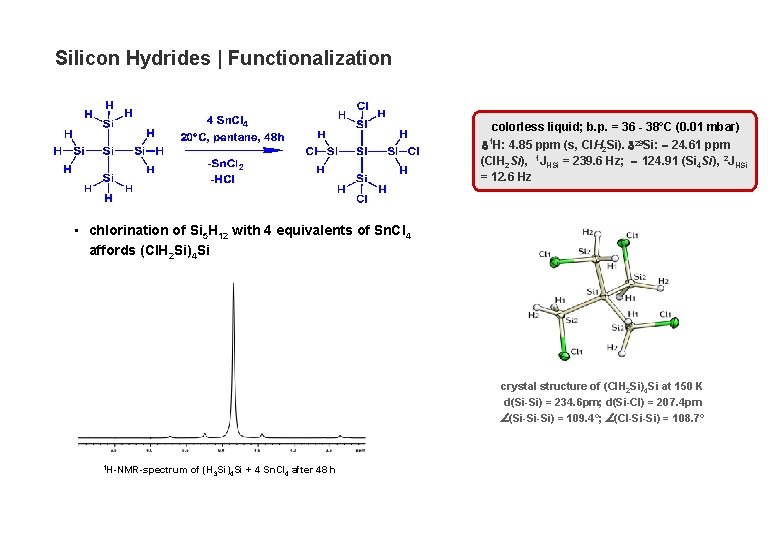
Silicon Hydrides | Functionalization colorless liquid; b. p. = 36 - 38°C (0. 01 mbar) 1 H: 4. 85 ppm (s, Cl. H 2 Si). 29 Si: 24. 61 ppm (Cl. H 2 Si), 1 JHSi = 239. 6 Hz; 124. 91 (Si 4 Si), 2 JHSi = 12. 6 Hz • chlorination of Si 5 H 12 with 4 equivalents of Sn. Cl 4 affords (Cl. H 2 Si)4 Si crystal structure of (Cl. H 2 Si)4 Si at 150 K d(Si-Si) = 234. 6 pm; d(Si-Cl) = 207. 4 pm (Si-Si-Si) = 109. 4°; (Cl-Si-Si) = 108. 7° 1 H-NMR-spectrum of (H 3 Si)4 Si + 4 Sn. Cl 4 after 48 h

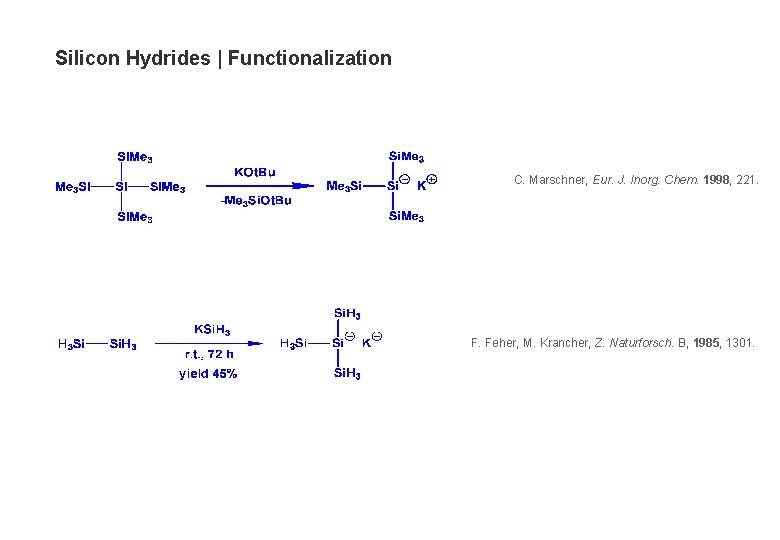
Silicon Hydrides | Functionalization C. Marschner, Eur. J. Inorg. Chem. 1998, 221. F. Feher, M. Krancher, Z. Naturforsch. B, 1985, 1301.

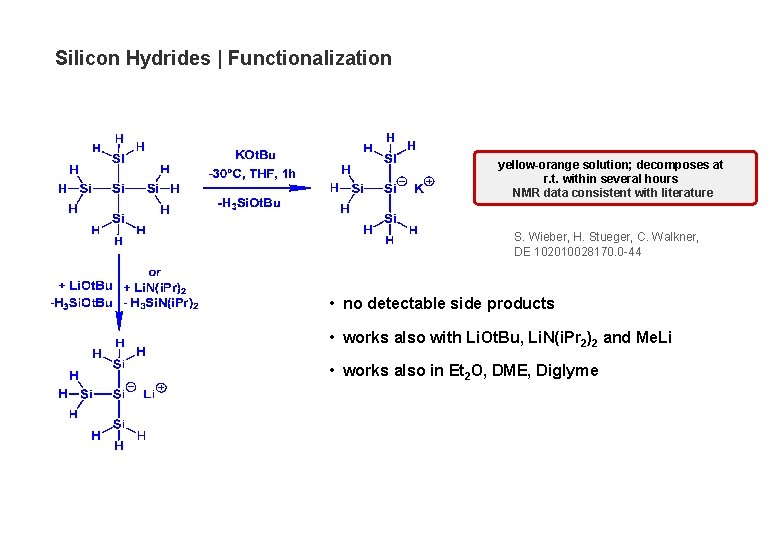
Silicon Hydrides | Functionalization yellow-orange solution; decomposes at r. t. within several hours NMR data consistent with literature S. Wieber, H. Stueger, C. Walkner, DE 102010028170. 0 -44 • no detectable side products • works also with Li. Ot. Bu, Li. N(i. Pr 2)2 and Me. Li • works also in Et 2 O, DME, Diglyme

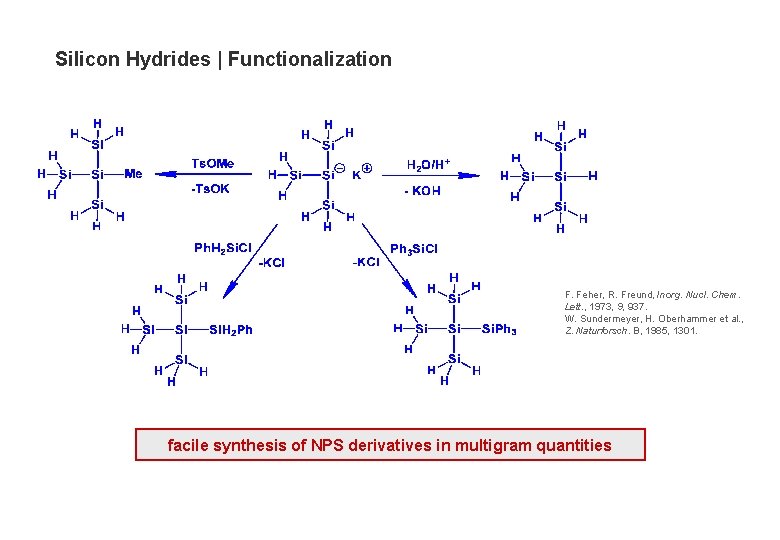
Silicon Hydrides | Functionalization F. Feher, R. Freund, Inorg. Nucl. Chem. Lett. , 1973, 9, 937. W. Sundermeyer, H. Oberhammer et al. , Z. Naturforsch. B, 1985, 1301. facile synthesis of NPS derivatives in multigram quantities

Silicon Hydrides | Application • application of higher silanes as precursor materials for liquid phase Si-film deposition in electronics industry ("printed electronics") (thin film transistor, flexible large area displays, photovoltaics etc. ) processing from liquid sources • Shimoda, T. ; Matsuki, Y. ; Furusawa, M. ; Aoki, T. ; Yudasaka, I. ; Tanaka, H. ; Iwasawa, H. ; Wang, D. ; Miyasaka, M. ; Takeuchi, Y. Nature 2006, 440, 783 desired property: Han, S. ; Dai, X. ; Loy, P. ; Lovaasen, J. ; Huether, J. ; Hoey, J. M. ; Wagner, A. ; Sandstrom, J. ; Bunzow, D. ; Swenson, O. F. ; Akhatov, I. S. ; Schulz, D. L. J. Non-Cryst. Solids 2008, 354, 2623. decomposition prior to evaporation Sontheimer, T. ; Amkreutz, D. ; Schulz, K. ; Wöbkenberg, P. H. ; Guenther, C. ; Bakumov, V. ; Erz, J. ; Mader, C. ; Traut, S. ; Ruske, F. ; Moshe Weizman, M. ; Schnegg, A. ; Patz, M. ; Trocha, M. ; Wunnicke, O. ; Rech, B. Adv. Mater. Interfaces 2014, 1300046.