HIVAids Epidemiologia e controle Gerusa Figueiredo Departamento de



































- Slides: 54

HIV/Aids Epidemiologia e controle Gerusa Figueiredo Departamento de Medicina Preventiva/ Instituto de Medicina Tropical/USP Universidade de São Paulo

Objetivos Descrever as características epidemiológicas da infecção pelo HIV/aids. Descrever a situação atual da epidemia no mundo e as perspectivas futuras dentro dos Objetivos do Desenvolvimento Sustentável. Descrever a situação atual da “epidemia” no Brasil com ênfase nas populações chave. Descrever medidas de prevenção e controle do HIV/aids.

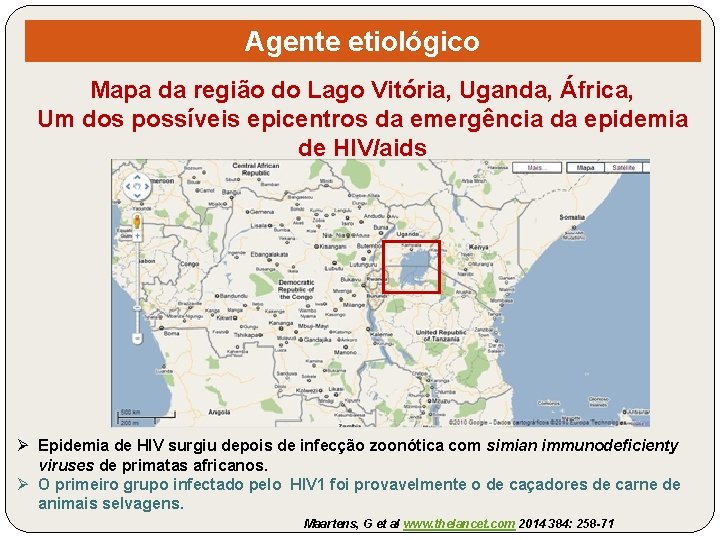
Agente etiológico Mapa da região do Lago Vitória, Uganda, África, Um dos possíveis epicentros da emergência da epidemia de HIV/aids Ø Epidemia de HIV surgiu depois de infecção zoonótica com simian immunodeficienty viruses de primatas africanos. Ø O primeiro grupo infectado pelo HIV 1 foi provavelmente o de caçadores de carne de animais selvagens. Maartens, G et al www. thelancet. com 2014 384: 258 -71

Agente etiológico Ø Existem 4 grupos de HIV 1: M, N, O e P § HIV-1 similar ao SIVcpz Ø M, N e O - transmissão de chimpanzés § HIV-2 similar ao SIVsm Ø P - de gorilas. Ø Grupo M teve início há cerca de 110 anos e é a causa da pandemia global. Ø Tem 9 subtipos =A-D, F-H, J e K Ø Subtipo C predomina na África e Índia. Ø Subtipo B predomina na Oeste da Europa, América e Austrália. Ø HIV 2 – confinado no oeste da África, quadro similar, mas progride Reservatório mais lentamente que o HIV 1 e é menos transmissível. Maartens, G et al www. thelancet. com 2014 384: 258 -71 Ø De importância na epidemia do HIV 1 – seres humanos

Modos de transmissão do HIV/Aids ü Sexual, parenteral, vertical, inclusive pelo leite materno. ü Período de transmissibilidade: ü O portador pode transmitir o agente etiológico durante todas as fases da infecção. ü A probabilidade de transmissão é proporcional à viremia e é maior na infecção aguda e na doença avançada (sem terapêutica). ü Outras Infecções Sexualmente Transmissíveis (IST), em especial as que cursam com lesões ulcerativas aumentam o risco de transmissão. ü Período de incubação: entre a exposição e a fase aguda, de 5 a 30 dias.



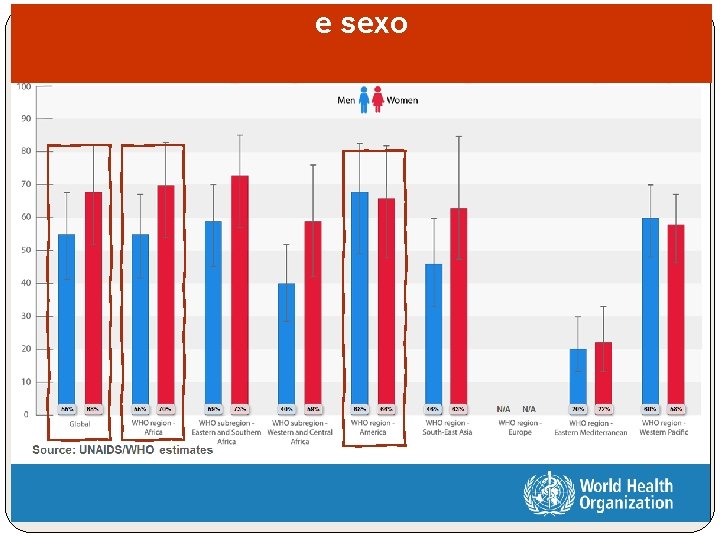
e sexo

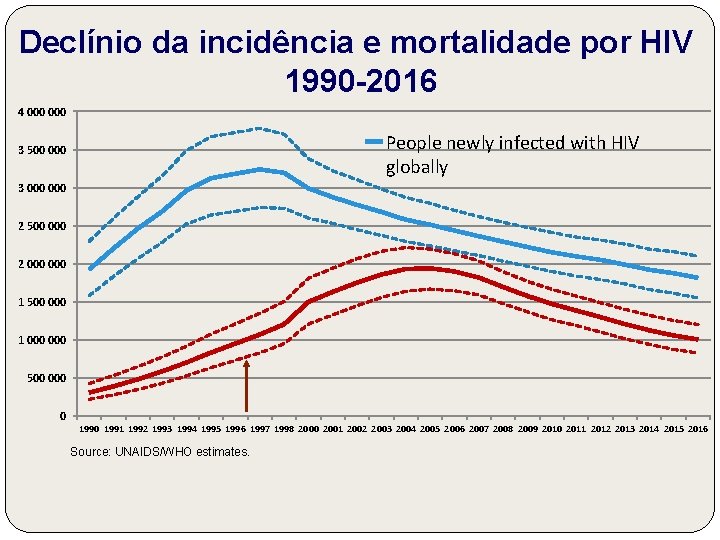
Declínio da incidência e mortalidade por HIV 1990 -2016 4 000 People newly infected with HIV globally 3 500 000 3 000 2 500 000 2 000 1 500 000 1 000 500 0 1990 1991 1992 1993 1994 1995 1996 1997 1998 2000 2001 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011 2012 2013 2014 2015 2016 Source: UNAIDS/WHO estimates.

Sucedendo os Objetivos do Milênio

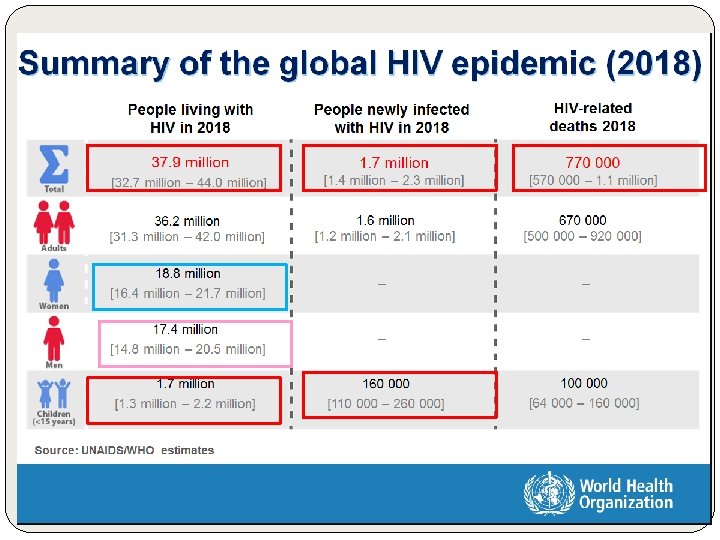
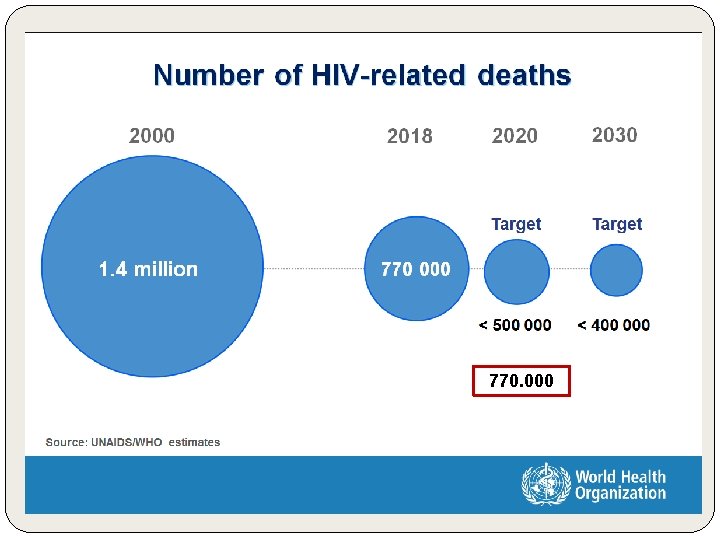
770. 000

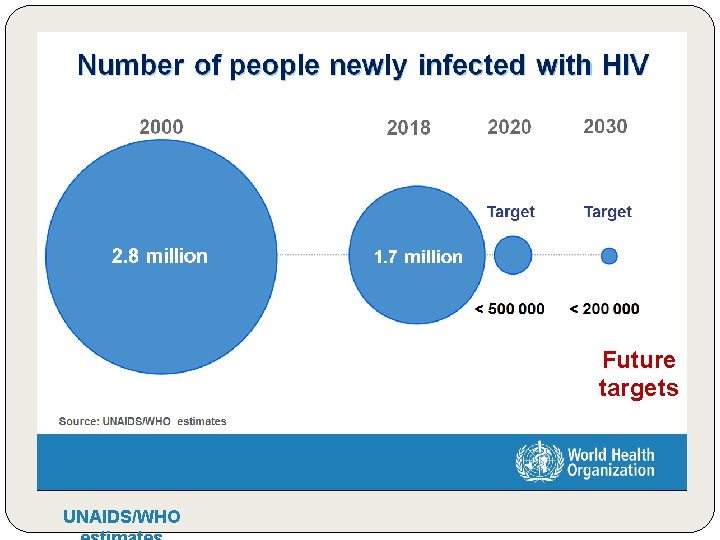
Future targets UNAIDS/WHO

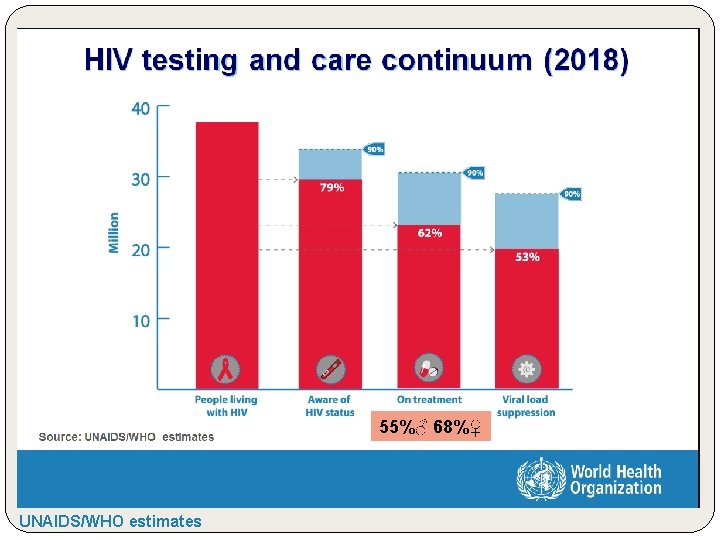
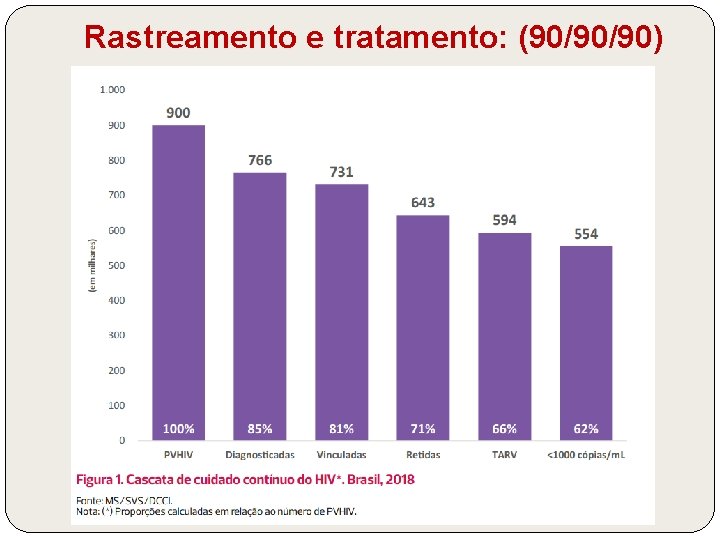
Metas até 2021 Ø Rastreamento e tratamento: (90/90/90) Ø garantir que 90% das pessoas vivendo com HIV saibam seu status sorológico; Ø garantir que 90% das pessoas diagnosticadas com HIV recebam terapia anti-retroviral; Ø garantir que 90% das pessoas vivendo com HIV, em tratamento, consigam a supressão da carga viral.

55%♂ 68%♀ UNAIDS/WHO estimates

Metas até 2021 (cont. ) Ø Mortes relacionadas ao HIV: Ø reduzir o número de mortes por HIV no mundo abaixo de 500 000; Ø reduzir as mortes por tuberculose entre as § 1/3 da mortes de aids devido pessoas que vivem com HIV em 75%; à TB § Pessoas com HIV tem 15 a 22 x + +chance de desenvolver TBC Ø reduzir as mortes por hepatite B e C entre as pessoas coinfectadas com HIV em 10%, em consonância com as metas de mortalidade das

Causas de morte em pessoas vivendo com aids Cerca de 50% de todas as mortes em pessoas usando HAART em países desenvolvidos não são devidas a aids. Estudo de coorte mostrou que a maior causa de morte foram cânceres não definidores de aids, doenças cardiovasculares e doenças hepáticas. Antiretroviral Therapy Cohort Collaboration. Causes of death in HIV-1 -infected patients treated with antiretroviral therapy, 1996– 2006: collaborative analysis of 13 HIV cohort studies. Clin Infect Dis 2010; 50: 1387– 96. Doença hepática é devida principalmente a coinfecção por hepatite C, a qual compartilha vias similares de transmissão com HIV. Joshi D, O’Grady J, Dieterich D, Gazzard B, Agarwal K. Increasing burden of liver disease in patients with HIV infection. Lancet 2011; 377: 1198– 209.

Metas até 2021 (cont. ) Ø Discriminação: Ø zerar leis, regulamentos e políticas discriminatórias relacionadas ao HIV; Ø zerar discriminação relacionada ao HIV em todos os equipamentos sociais, especialmente os de saúde; Ø que 90% das pessoas vivendo com HIV e populações-chave não relatem discriminação no setor da saúde.

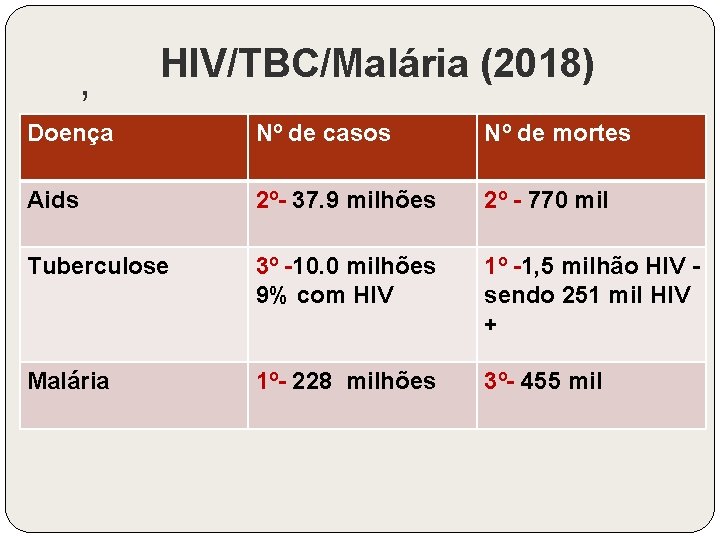
, HIV/TBC/Malária (2018) Doença Nº de casos Nº de mortes Aids 2º- 37. 9 milhões 2º - 770 mil Tuberculose 3º -10. 0 milhões 9% com HIV 1º -1, 5 milhão HIV sendo 251 mil HIV + Malária 1º- 228 milhões 3º- 455 mil

Objetivos Descrever as características epidemiológicas da infecção pelo HIV/aids. Descrever a situação atual da epidemia no mundo e as perspectivas futuras dentro dos Objetivos do Desenvolvimento Sustentável. Descrever a situação atual da epidemia no Brasil. Descrever as ações de vigilância e controle do HIV/aids.

HIV/aids Brasil § Prevalência de infecção por HIV = 0, 6% (15 – 49 anos) Depto DST/AIDS/IST/HV, Ministério da Saúde

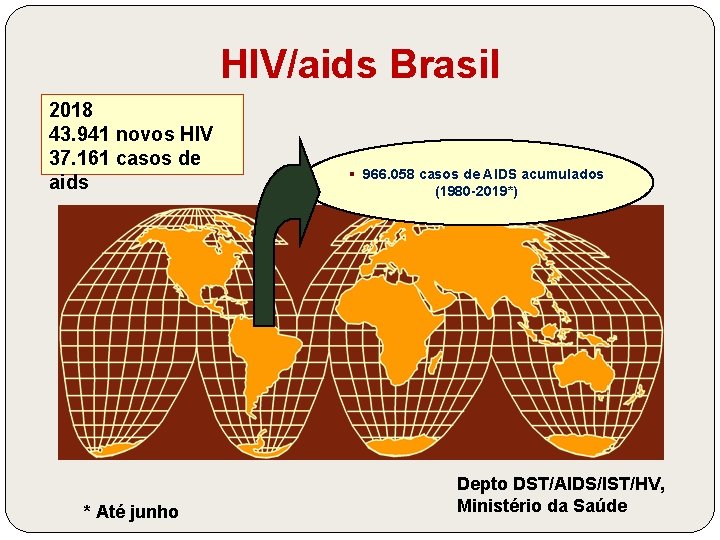
HIV/aids Brasil 2018 43. 941 novos HIV 37. 161 casos de aids * Até junho § 966. 058 casos de AIDS acumulados (1980 -2019*) Depto DST/AIDS/IST/HV, Ministério da Saúde

Taxa de detecção de aids (por 100 mil Brasil) por UF 2012 = 21, 4 casos por 100 mil; 2018= 17, 8 casos por 100 mil

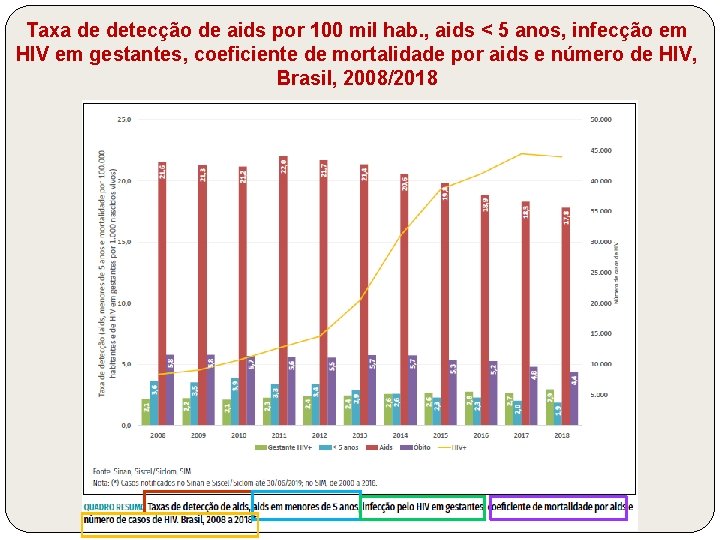
Taxa de detecção de aids por 100 mil hab. , aids < 5 anos, infecção em HIV em gestantes, coeficiente de mortalidade por aids e número de HIV, Brasil, 2008/2018

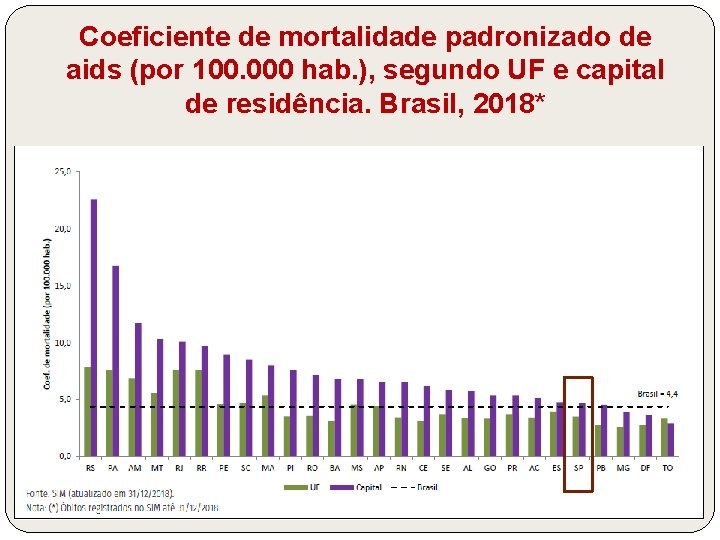
Coeficiente de mortalidade padronizado de aids (por 100. 000 hab. ), segundo UF e capital de residência. Brasil, 2018*

HIV/aids/Brasil < 1% população geral ≠ Em subgrupo populacional § § Epidemia concentrada Depto DST/AIDS/IST/HV, Ministério da Saúde

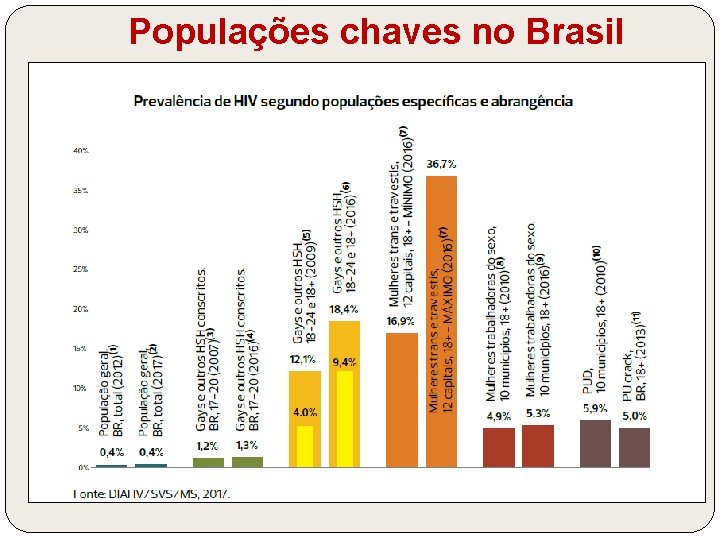
Populações chaves no Brasil

Populações chaves no Brasil

Populações chaves no Brasil BRASIL. Ministério da Saúde. Secretaria de Vigilância em Saúde. Departamento das IST, do HIV/Aids e das Hepatites Virais. Relatório de Monitoramento Clínico do HIV. Brasília: Ministério da Saúde, 2016 b; (2) PEREIRA, G. F. M. et al. Transitioning from antenatal surveillance surveys to routine HIV testing: a turning point in the mother-to-child transmission prevention programme for HIV surveillance in Brazil. BMC Infect Dis. , [S. l. ], v. 17, n. 1, p. 469, jul. 2017; (3) SZWARCWALD, C. L. et al. Práticas de risco relacionadas à infecção pelo HIV entre jovens brasileiros do sexo masculino, Brasil, 2007. Cad. Saúde Pública, [S. l. ], v. 27, supl. 1, p. s 19 -s 26, 2011; (4) SPERHACKE, R. C. Relatório Técnico Final. Rio Grande do Sul: Universidade Caxias do Sul, 2016. Produto 6. Projeto 914 BRZ 1138; (5) KERR, L. et al. HIV among MSM in a large middle-income country. AIDS, [S. l. ], v. 28/27, n. 3, p. 427 -35, jan. 2013; (6) KERR, L. Relatório Técnico Final. Brasília: Ministério da Saúde, 2017. Produto 6. Projeto 914 BRZ 1138; (6) KERR, L. HIV prevalence among men who have sex with men in Brazil: results of the 2 nd national survey using respondent-driven sampling. Kerr L. et al. Medicine (2018) 97: S 1(e 10573 (7) GRINSZTEJN, B. et al. Unveiling of HIV dynamics among transgender women: a respondent- driven sampling in Rio de Janeiro, Brazil. The Lancet HIV, [S. l. ], v. 4, n. 4, p. e 169 -e 176, abr. 2017; (8) DAMACENA, G. N. et al. Risk factors associated with HIV prevalence among female sex workers in 10 Brazilian cities. J. Acquir. Immune Defic. Syndr. , [S. l. ], v. 57, Supl. 3, p. S 144– 52, ago. 2011; (9) SZWARCWALD, C. L. Relatório Técnico Final. Brasília: Ministério da Saúde, 2016. Produto 6. Projeto 914 BRZ 1138; (10) BASTOS, F. I. Taxas de infecção de HIV e sífilis e inventário de conhecimento, atitudes e práticas de risco relacionadas às infecções sexualmente transmissíveis entre usuários de drogas em 10 municípios brasileiros. Relatório técnico entregue ao Departamento de DST, Aids e Hepatites

Estudos de soroprevalência no Brasil � Prevalência de HIV em HSH em 10 cidades brasileiras: � Amostra obtida pela técnica “RDS” (respondent driven sample). Estudo de campo realizado em 2009. � Amostra de 3. 859 HSH. � 49% nunca havia feito o teste para HIV. � 6, 6% sabia ser portadores do HIV. � Prevalência de 14, 2% (IC 95%: 12, 1 – 16, 6), variando entre 5, 2% (Recife) e 23, 7% (Brasília). Cidades participantes: Rio de Janeiro, Belo Horizonte, Recife, Manaus, Salvador, Campo Grande, Brasília, Itajaí, Santos e Curitiba. • Kerr LR et al. HIV infection among MSM in a large middle income country. AIDS 2013, 27(3): 427 -35

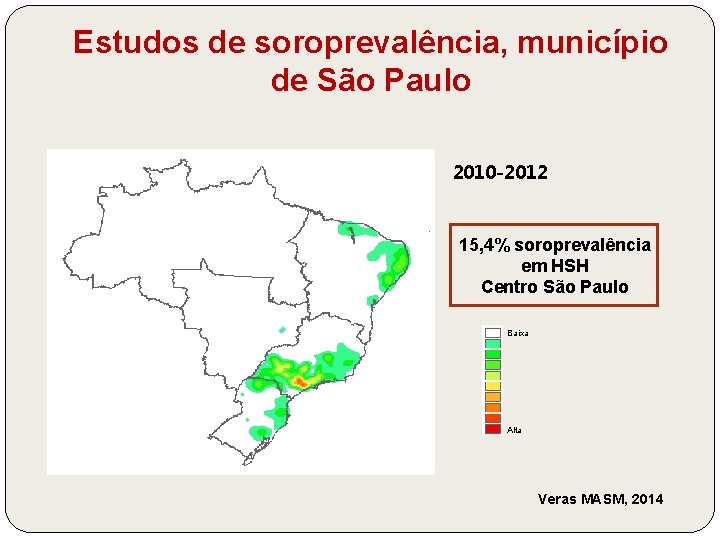
Estudos de soroprevalência, município de São Paulo 2010 -2012 15, 4% soroprevalência em HSH Centro São Paulo Baixa Alta Veras MASM, 2014

Estudos de soroprevalência no Brasil � Prevalência de HIV em HSH em 12 cidades brasileiras das 5 macroregiões: � Amostra obtida pela técnica “RDS” (respondent dr sample). � Estudo de campo realizado de junho a dezembro de 2 � Amostra de 3. 058. � Prevalência de 18, 4% (IC 95% 15, 4 a 21, 7). HIV prevalence among men who have sex with men in Brazil: results of the 2 nd national survey using respondentdriven sampling. Kerr L. et al. Medicine (2018) 97: S 1(e 10573)


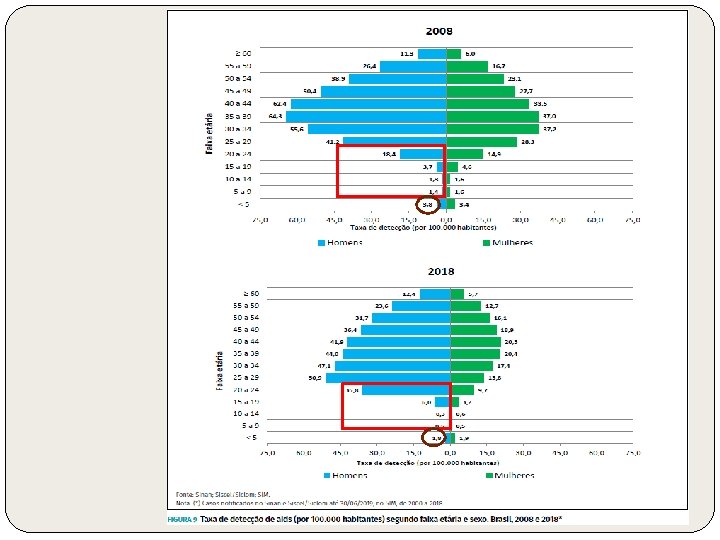
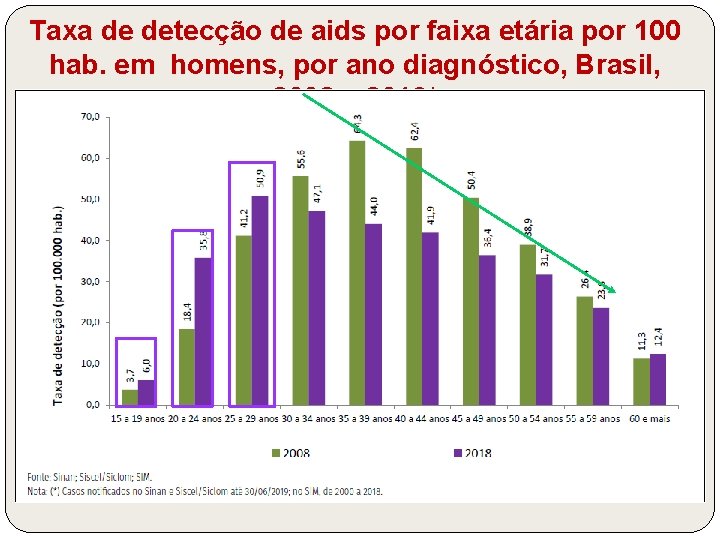
Taxa de detecção de aids por faixa etária por 100 hab. em homens, por ano diagnóstico, Brasil, 2008 – 2019*

Objetivos Descrever as características epidemiológicas da infecção pelo HIV/aids. Descrever a situação atual da epidemia no mundo e as perspectivas futuras dentro dos Objetivos do Desenvolvimento Sustentável. Descrever a situação atual da epidemia no Brasil. Descrever as ações de vigilância e controle do HIV/aids.

Vigilância Epidemiológica e Controle do HIV/Aids no Brasil � Aids foi incluída na lista de Doenças de Notificação Compulsória no Brasil em 1986 (1983 no Estado de São Paulo). � Continua na portaria 204 de 17/02/2016. � Portaria Nº 1. 271, de 6 de junho de 2014 acresceu Infecção pelo Vírus da Imunodeficiência Humana (HIV) positivo como de notificação.


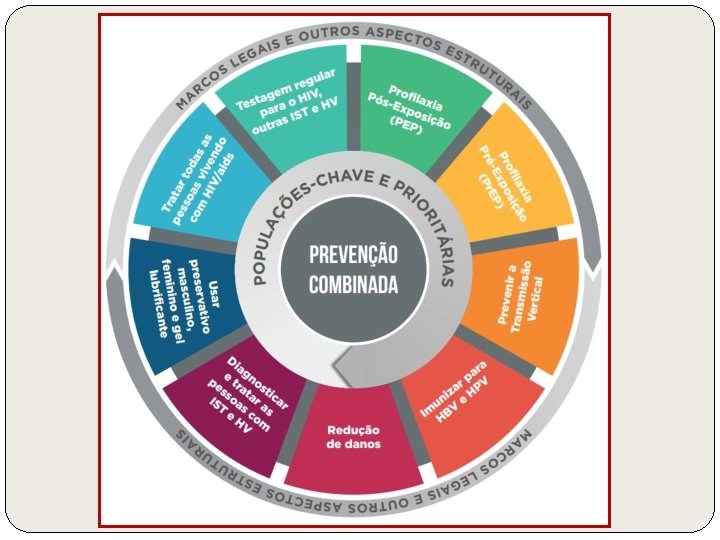
Prevenção primária

Ações programáticas para o enfrentamento do HIV Ø Prevenção primária § Sexo mais seguro § Prevenção da transmissão parenteral § redução de danos § triagem em bancos de sangue § Prevenção da transmissão materno- infantil § Novas tecnologias

Medidas de Prevenção e Controle ü Prevenção primária ü Prevenção da transmissão parenteral: Ø triagem de doadores de sangue, órgãos e esperma obrigatória no Brasil desde 1994.

Diminuição da transmissão vertical ü Prevenção da transmissão vertical: Ø Condição incluída separadamente na lista de Doenças de Notificação Compulsória (Gestante HIV positivo e criança exposta).

Diminuição da transmissão vertical Ø Gestante e criança exposta: Ø Com carga viral < 1000 cópias/ml, mas detectéval. Ø Mãe - Zidovudina intravenosa durante o trabalho de parto normal até clampeamento do cordão umbilical, e xarope de AZT por 4 semanas para o RN. Ø Com varga viral >1000 cópias/ml ou desconhecida. Ø Mãe - Zidovudina intravenosa durante o trabalho de parto cesárea* e xarope de AZT por 4 semanas para o RN + associada à Nevirapina suspensão oral. * Retirada do saco amniótico íntegro, protegendo assim criança de contato com sangue

Medidas de Prevenção e Controle Ø Prevenção primária – outras tecnologias biomédicas: § circuncisão masculina voluntária – em outros países. § microbicidas em mulheres – não implementada no Brasil § Pr. EP – profilaxia pré-exposição –implementando. § PEP – profilaxia pós-exposição – implementada.

Diminuição da cadeia de transmissão Prevenção primária Ø Ensaios de utilização de TARV para a prevenção primária da infecção pelo HIV: Ø Partner’s Pr. EP, da University of Washington – casais soro discordantes J M Baeten et al. Antiretroviral prophylaxis for HIV prevention in heterossexual men and women. The New England Journal of Medicine, 2012. Ø TDF 2 Study, dos CDC- jovens adultos www. cdc. gov/hiv/prep Ø Estudo i. Pr. Ex – homossexuais masculinos e transexuais Robert M. Grant, Preexposure Chemoprophylaxis for HIV Prevention in Men Who Have Sex with Men. N Engl J Med 2010 363; 27: 2587 -2599. Ø Casais heterossexuais Kenneth K Mugwanya - Sexual behaviour of heterosexual men and women receiving

No Brasil Estudo prospectivo, multicêntrico, com objetivo de mostrar o uso de Pr. EP no sistema de saúde. Ø População elegível -HSH HIV negativos e trangêneros sob risco (nos últimos 12 meses ter tido sexo anal sem preservativo + que 2 vezes, 2 episódios se sexo anal com parceiro HIV + ou história de DST). Ø 3 centros brasileiros – RJ e SP Ø Foram elegíveis para receber diariamente emtricitabine + tenofovir – 750 pessoas Ø Resultados: Ø 450 receberam de fato (60, 9% de retenção dos 738 elegíveis); Ø Quem não aderiu foram jovens, com baixa percepção de risco para HIV; Ø Semana 4, foi obtido amostra de sangue papel de filtro; Ø 94, 1% tinham nível protetor correspondente a 2 pílulas por semana e 78, 0% com 4 pílulas por semana;

No Brasil Ø Resultados (cont. ) Ø Aderência vista na 4º semana para HSH de alto risco e de transgêneros foi bem sucedida no contexto dos serviços de saúde do país; Ø Sexo anal receptivos nos 3 meses anteriores foi associado com altos níveis de medicamentos no sangue (OR 1, 78/ IC 1, 08 -2, 94); Ø Uso de presevativo em intercurso anal nos 3 mese anteriores foi associada com altos nível de droga no sangue (4 pípulas por semana). Ø Participantes com 12 anos ou + de escolaridade – OR 1, 9 a(IC 95% 1, 10 Conclusão: Necessidade de intervenção dirigida a corrigir 3, 29) 1, 9 em vezes maisde debaixa uso em relação a <(para 12 anos; disparidade jovens escolaridade perpcepção de risco e de necessidade e de adoção de medidas preventivas). Brenda Hoagland. High pre-exposure prophylaxis uptake and early adherence among men who have sex with men and transgender women at risk for HIV Infection: the Pr. EP Brasil demonstration Project. Journal of the International AIDS Society 2017, 20: 21472

Intervenção – Profilaxia pós exposição (PEP) Ø Medida de prevenção de urgência à infecção pelo HIV, hepatites virais e outras infecções sexualmente transmissíveis (IST), que consiste no uso de medicamentos para reduzir o risco de adquirir essas infecções. Ø HIV - ARV que deve ser iniciada preferencialmente nas primeiras duas horas após a exposição e no máximo em até horas e por 28 dias. com materiais pérfuro • 72 Acidente de trabalho cortantes • Exposição sexual: • violência sexual

Prevenção secundária

Tratamento como prevenção secundária do HIV • Quais são as ações programáticas mais importantes? Ø diagnóstico precoce Ø tratamento específico

Rastreamento e tratamento: (90/90/90)

Principais Estudos HPTN 052 – 2011 PARTNER -2014 ESTUDO START - 2015 OPPOSITES ATRACT - 2017

Estudo HPTN 52/pares discordantes Ensaio clínico para demonstrar a eficácia do uso de HAART na prevenção da transmissão do HIV entre casais sorodiscordantes. Casais sorodiscordantes, parceiro HIV+ sem HAART (CD 4+ entre 350 e 550). 1. 763 casais recrutados, em 9 países (África do Sul, Botswana, Brasil, Índia, Malaui, Quênia, Tailândia, EUA e Zimbabue). Alocados em dois grupos: início imediato do tratamento com HAART - 886 indivíduos início tardio (quando CD 4+<250 ou com doença definidora de Aids ) – 877 indivíduos Piloto em 2005 e recrutamento e acompanhamento de junho de 2007 a maio de 2010. 39 novas infecções pelo HIV, com 27 no Grupo Tardio e apenas 1 no Grupo imediato. Redução de 96% da transmissão.

Estudo Opposites Atract - Opostos se atraem e Estudo START Ø Austrália, Brasil e Tailândia Ø Incluiu 343 casais homossexuais masculinos sorodiscordantes, sendo o HIV + com carga viral indetectável. Ø Em 16. 889 atos de sexo anal sem preservativos - não houve nenhum caso de infecção entre os parceiros. Bavinton R Benjamin et al. The Opposites Attract Study of viral load, HIV, treatment and HIV transmission in serodiscordant homosexual male couples: design and methods. BMC Public Health 2014, 14: 917

Diminuição da cadeia de transmissão Forte associação a nível populacional entre aumento de cobertura de HAART, decréscimo de carga viral e diminuição de novas infecções por

Desafios para o Brasil ü Números estabilizada em patamar muito alto. ü Epidemia concentrada em populações chave. ü Aumento expressivo em HSH. ü Necessidade do fortalecimento das atividades de prevenção. ü Acesso oportuno ao diagnóstico e tratamento. ü Adesão ao tratamento.