TEMA 9 1 REACCIONES QUMICAS 2 REACCIONES QUMICAS








































- Slides: 46

TEMA 9 1

REACCIONES QUÍMICAS 2

REACCIONES QUÍMICAS • EJEMPLOS DE CAMBIOS FÍSICOS • EJEMPLOS DE CAMBIOS QUÍMICOS 3

REACCIONES QUÍMICAS • • CAMBIOS FÍSICOS Mezclas Disoluciones Cambios de estado • CAMBIOS QUÍMICOS • Oxidación • Combustión 4

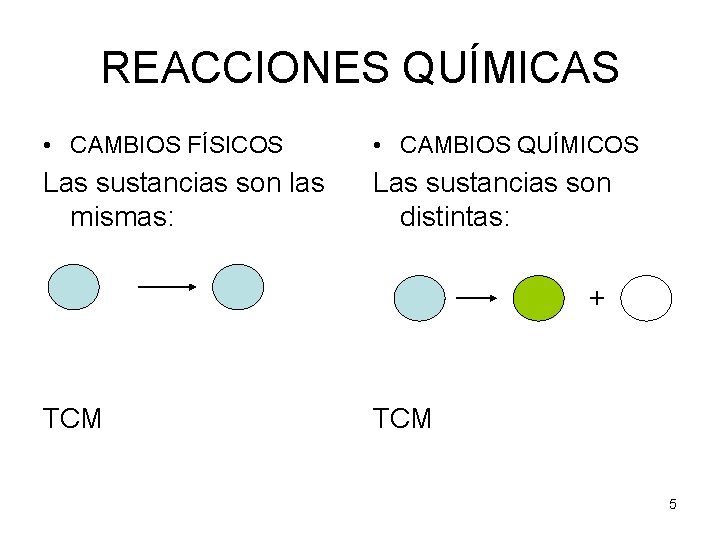
REACCIONES QUÍMICAS • CAMBIOS FÍSICOS • CAMBIOS QUÍMICOS Las sustancias son las mismas: Las sustancias son distintas: + TCM 5

REACCIONES QUÍMICAS • Proceso en el cual unas sustancias se transforman en otras. TCM • Proceso en el cual se rompen los enlaces de las sustancias reaccionantes y se forman los enlaces de los productos de la reacción. TAM 6

REACCIÓN QUÍMICA SEGÚN LA TEORÍA ATÓMICO MOLECULAR • H 2 + O 2 H 2 O • El número de átomos no es el mismo en reactivos que en productos por lo que la reacción será: 7

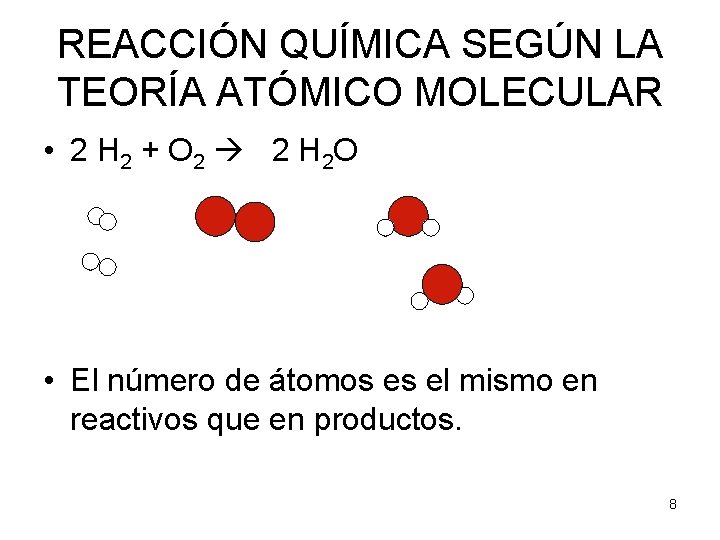
REACCIÓN QUÍMICA SEGÚN LA TEORÍA ATÓMICO MOLECULAR • 2 H 2 + O 2 2 H 2 O • El número de átomos es el mismo en reactivos que en productos. 8

REPRESENTACIÓN DE UNA RECCIÓN QUÍMICA. • ECUACIÓN QUÍMICA: es la representación de una reacción química. • Tiene: – – – Reactivos, reaccionantes, sustancias iniciales Productos, productos de la reacción Estado en el que se encuentran las sustancias Flecha Energía que se pone en juego en la reacción Coeficientes estequiométricos. 9

PRINCIPIO DE CONSERVACIÓN DE LA MASA EN LAS REACCIONES QUÍMICAS • LEY DE LAVOISIER: la masa de los reactivos es igual a la masa de los productos. • JUSTIFICACIÓN: los átomos que hay en los reactivos son los mismos que los que hay en los productos. 10

LEY DE LAVOISIER. EJERCICIOS. Carbono (s) + Oxígeno (g) Dióxido de carbono (g) 12 g 32 g Hidrógeno (g) + Cloro (g) cloruro de hidrógeno (g) 2 g 73 g Carbonato de calcio (s) dióxido de carbono (g) + óxido de calcio (s) 44 g 56 g 11

COEFICIENTES ESTEQUIOMÉTRICOS • Escribe y ajusta las reacciones siguientes: Carbono (s) + Oxígeno (g) Dióxido de carbono (g) Hidrógeno (g) + Cloro (g) cloruro de hidrógeno (g) Carbonato de calcio (s) dióxido de carbono (g) + óxido ce calcio (s) Ajusta las reacciones del ejercicio 18 de la página 229 de tu libro. 12

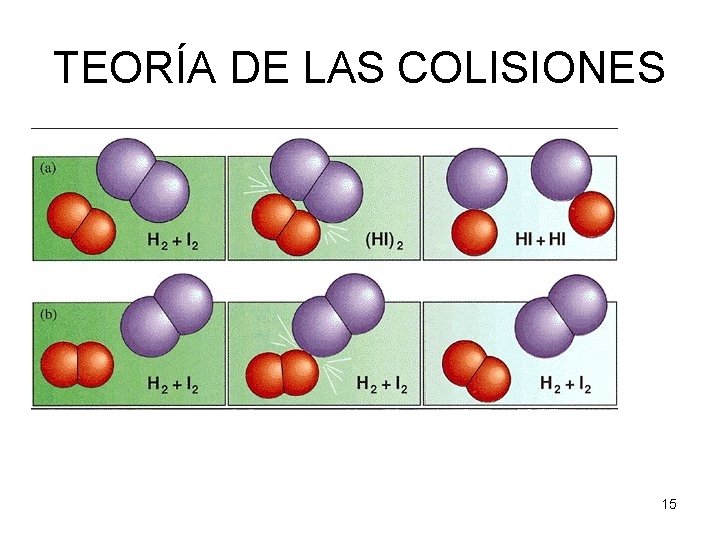
TEORÍA DE LAS COLISIONES • Explica cómo tiene lugar una reacción química. • Para que se rompan los enlaces de las sustancias iniciales se tiene que producir un choque eficaz: – Con la suficiente energía – Con la orientación adecuada • En ese choque se empiezan a romper los enlaces de los reactivos. • Se forma una sustancia intermedia llamada complejo activado. • Se terminan de romper los enlaces de los reactivos y se forman los enlaces de los productos de la reacción. 13

TEORÍA DE LAS COLISIONES 14

TEORÍA DE LAS COLISIONES 15

TEORÍA DE LAS COLISIONES 16

TIPOS DE REACCIONES: SEGÚN LA ENERGÍA QUE SE PONE EN JUEGO. • REACCIONES EXOTÉRMICAS: se desprende energía. • La energía de los productos es menor que la energía de los reactivos. • REACCIONES ENDOTÉRMICAS: se absorbe energía. • La energía de los productos en mayor que la energía de los reactivos. 17

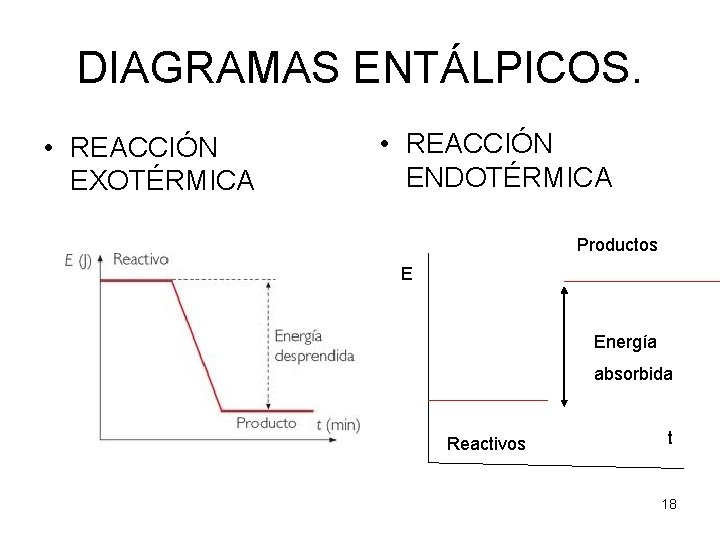
DIAGRAMAS ENTÁLPICOS. • REACCIÓN EXOTÉRMICA • REACCIÓN ENDOTÉRMICA Productos E Energía absorbida Reactivos t 18

DIAGRAMAS ENTÁLPICOS. EJEMPLOS. • REACCIÓN EXOTÉRMICA • Cloro (g) + Hidrógeno (g) cloruro de hidrógeno (g) • REACCIÓN ENDOTÉRMICA • Agua (l) hidrógeno (g) + oxígeno (g) • • ESCRIBIR LA REACCIÓN Y DIBUJAR EL DIAGRAMA ENTÁLPICO 19

VELOCIDAD DE UNA REACCIÓN • Rapidez con la que los reactivos desaparecen. • Depende: – Temperatura – Concentración de los reactivos – Grado de división de los reactivos – Otros (naturaleza de los reactivos, presencia de catalizadores) 20

Temperatura • • + temperatura + velocidad de las partículas + choques + velocidad de la reacción 21

Concentración de los reactivos 22

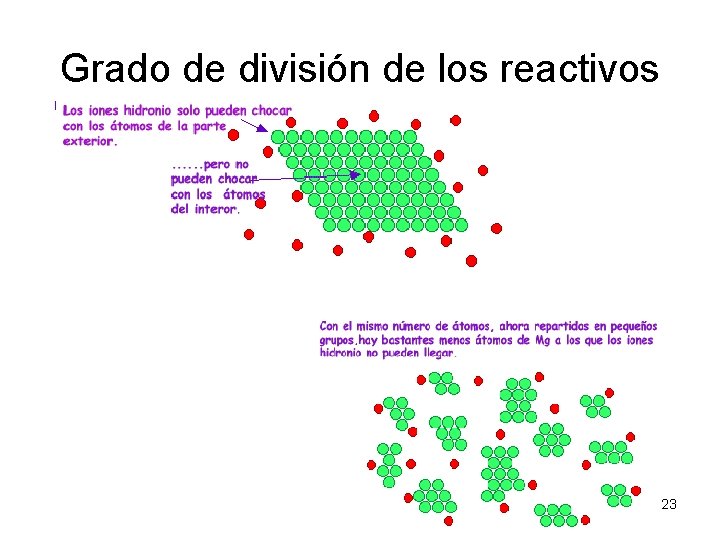
Grado de división de los reactivos 23

CANTIDAD DE SUSTANCIA 24

Cálculo de la masa de un átomo de Na • 11 protones x 1, 672 × 10− 27 kg • 11 electrones x 9, 11× 10 -31 Kg • 12 neutrones x 1, 675× 10− 27 kg • La masa de los átomos es muy pequeña 25

Patrón para determinar masas atómicas • • Patrón: átomo de 12 C Masa del átomo de 12 C = 12 u. Unidad: u o uma Definición: la doceava parte de la masa del 12 C “La masa del átomo de Na es 23 u, significa que es 23 veces mayor que la doceava parte de la masa del 12 C” 26

UNIDAD DE MASA ATÓMICA • Masa atómica: masa de un átomo en u. Está en la T. P. • Masa molecular: masa de una sustancia en u. Se calcula 27

Cantidad de sustancia • Definición: cantidad de átomos, moléculas o sustancia que hay. • Unidad: mol • En 1 mol de sustancia siempre hay el mismo número de partículas (6, 023 10 23 partículas) AVOGADRO. 28

Masa atómica y molecular • Masa atómica: la masa de 1 mol de átomos expresada en g. • M (H)= 1 g/mol; M (Na)= 23 g/mol • Se busca en la Tabla Periódica. • Masa molecular: la masa de 1 mol de moléculas (compuesto en general) expresada en g. • M(H 2 O) 1+ 1+ 16= 18 g/mol • Se calcula. 29

Cantidad de sustancia • 1 átomo de H, 1 u de H, 1 átomo de H • 1 mol de H, 1 g de H, 6, 023 10 23 átomos de H • 1 molécula de H 2, 2 u de H 2, 1 moléculas de H 2 • 1 mol de H 2, 2 g de H 2, 6, 023 10 23 moléculas de H 2 • 1 molécula de H 2 O, 18 u de H 2 O, 1 moléculas de H 2 O • 1 mol de H 2 O, 18 g de H 2 O, 6, 023 10 23 moléculas de H 2 O • EJERCICIOS 1, 2, 3, 4, 5, 22, 23 30

DISOLUCIONES 31

¿Qué es una disolución? • Es una mezcla homogénea, formada por 2 o más sustancias. • Según la TCM 32

Componentes de una disolución • Soluto: el que se encuentra en menor proporción. • Disolvente: el que se encuentra en mayor proporción. • Si uno de los componentes es agua será siempre el disolvente tenga la proporción que tenga. 33

Concentración de una disolución • Cantidad de soluto que hay en relación a la cantidad de disolvente o disolución. 34

Formas de expresar la concentración de una disolución: • % en masa: gramos de soluto en 100 gramos de disolución • % en volumen: m. L (L) de soluto en 100 m. L (L) de disolución • g/L: gramos de soluto en 1 L de disolución • M (molaridad): cantidad de sustancia de soluto (en moles) en 1 L de disolución M= n/V 35

Ejercicios de disoluciones: • Ejercicios del libro: 6, 7, 8, 27, 28, 29, 30 36

CÁLCULOS EN LAS REACCIONES QUÍMICAS 37

Ejercicios con reacciones químicas: 9, 10, 11, 12 38

TIPOS DE REACCIONES OXIDACIÓN COMBUSTIÓN ÁCIDO BASE 39

OXIDACIÓN • Fe + O 2 óxido de hierro (II) • Hierro + sulfato de cobre (II) sulfato de hierro (II) + cobre El hierro se oxida de hierro metálico a hierro con valencia 2. 40

COMBUSTIÓN • Reacción con el oxígeno. Da dióxido de carbono y agua. • Son reacciones exotérmicas • Ejemplos: • Metano (g) + O 2 (g) • Butano (g) + O 2 (g) • Gasolina (g) + O 2 (g) 41

ÁCIDO BASE • ÁCIDO: • Sabor agrio • Disuelven algunos metales desprendiendo hidrógeno • Disuelven el mármol desprendiendo CO 2 • Ej: ácido cítrico, ácido acético • BASE • Sabor amargo • Favorece la disolución de las grasas, productos de limpieza • Ej: amoniaco, hidróxido de sodio, “bicarbonato” 42

ÁCIDO BASE • EJEMPLOS DE ÁCIDOS • HCl: digestión • H 2 SO 4: materia prima industrial, responsable de la lluvia ácida • HNO 3: fabricar explosivos, responsable de la lluvia ácida • EJEMPLOS DE BASES • NH 3: productos de limpieza, fertilizantes • Na. OH: productos químicos, jabón, desatascar cañerías • Na. HCO 3: contrarresta la acidez de estómago, levadura de panadería. 43

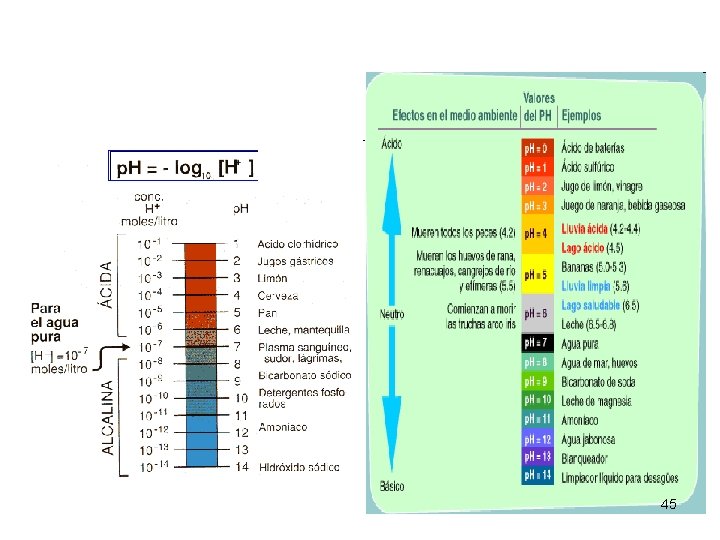
ÁCIDO BASE • La acidez se determina con el p. H • ÁCIDOS: p. H< 7 • BASE: p. H>7 44

45

REACCIÓN DE NEUTRALIZACIÓN • • ÁCIDO + BASE SAL + AGUA Reacciones exotérmicas Ejemplos: Ácido clorhídrico + hidróxido de sodio cloruro de sodio + agua • Ácido sulfúrico + hidróxido de calcio sulfato de calcio + agua 46