Reacciones Qumicas OBJETIVO Describir que son las reacciones

Reacciones Químicas OBJETIVO: Describir que son las reacciones químicas e identificar las partes de una ecuación química.

¿Qué son las reacciones químicas? En la naturaleza se producen gran variedad de cambios, como la dilatación de un metal, los cambios de estado del agua, la oxidación de algunos metales. . . Cambio físico – la composición química de una sustancia permanece constante. ◦ Fundir hielo La mantequilla, al derretirse, sigue siendo mantequilla. La botella rota sigue siendo de vidrio. Cambio químico – la composición química de una sustancia cambia. Oxidación del Hierro La herrumbre que se forma en la viga es una sustancia distinta al hierro. La ceniza que se crea en la hoguera es una sustancia distinta a la madera. Reacción química ocurre reordenamiento de átomos; se rompen enlaces y se forman nuevos enlaces.

¿Qué se observa en una reacción química? Cuando: ◦ ◦ Se produce un gas. Emisión de luz. Se produce un sólido insoluble. Se observa un cambio de color. permanentemente. ◦ Se observa transferencia de calor. Exotérmico – se libera calor. Endotérmico – se absorbe calor.
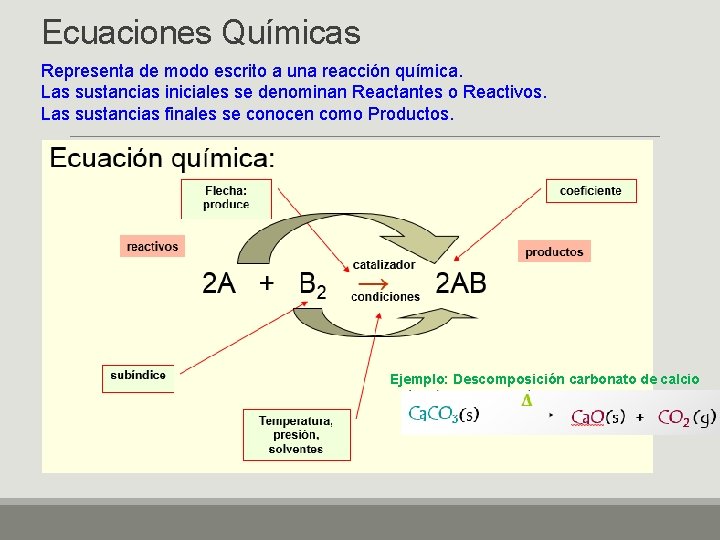
Ecuaciones Químicas Representa de modo escrito a una reacción química. Las sustancias iniciales se denominan Reactantes o Reactivos. Las sustancias finales se conocen como Productos. Ejemplo: Descomposición carbonato de calcio

Estado físico 2 HCl(ac) + Na 2 CO 3(s) H 2 O (l) + CO 2(g) + 2 Na. Cl(ac) s: sólido g: gas l: líquido ac: disuelto en agua

ESCRIBAMOS UNA REACCIÓN QUIMICA CON UNA ECUACIÓN QUÍMICA El vinagre y polvos de hornear son los nombres comunes para el ácido acético (C 2 H 4 O 2) y bicarbonato de sodio (Na. HCO 3), respectivamente. La reacción produce acetato de sodio sólido(C 2 H 3 O 2 Na), agua líquida (H 2 O) y dióxido de carbono gaseoso (CO 2).
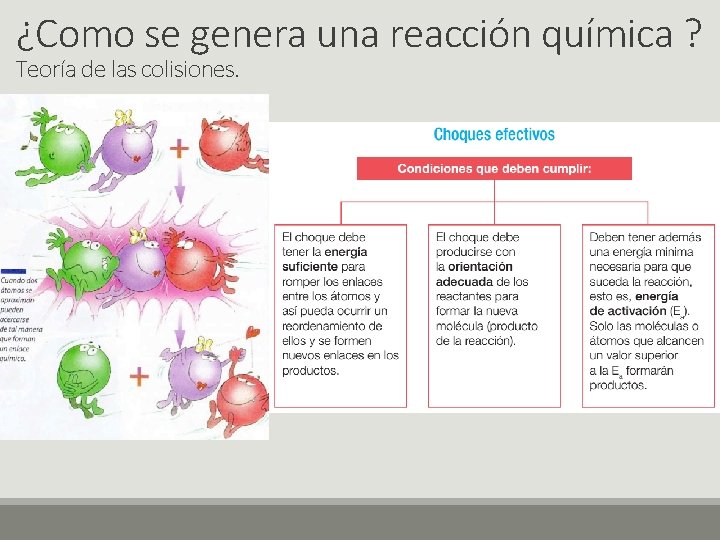
¿Como se genera una reacción química ? Teoría de las colisiones.
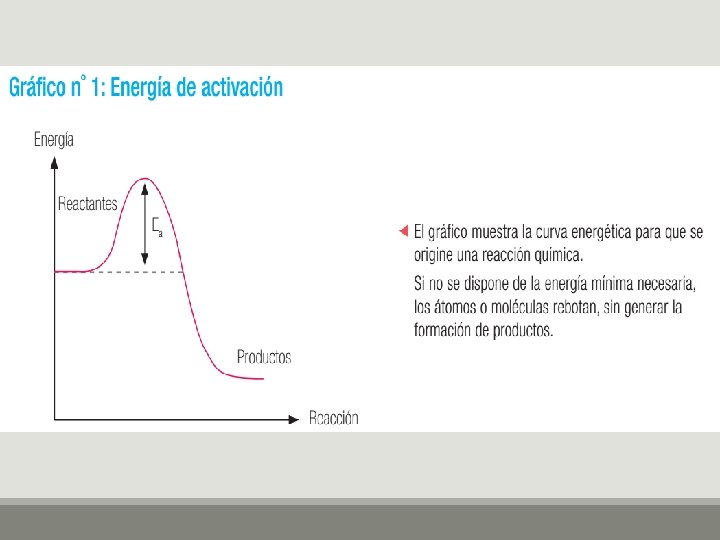

Ley de conservación de la masa Antoine Lavoisier (1734 -1794)

BALANCE DE ECUACIONES Todas las reacciones químicas deben cumplir fielmente la Ley de Lavoisier (conservación de la masa) para ello siempre debemos equilibrarlas o balancearlas. N 2 + H 2 NH 3

¿Qué significa esta ecuación? N 2 + 3 H 2 1 molécula de nitrógeno (con 2 átomos) reacciona con 3 moléculas de hidrógeno (con 2 átomos) para formar: 1 mol de nitrógeno (N 2) reacciona con 3 moles de hidrógeno (H 2) para formar: 2 NH 3 2 moléculas de amoníaco ( Cada molécula contiene 1 átomo de N y 3 átomos de H) 2 moles de amoníaco (NH 3)
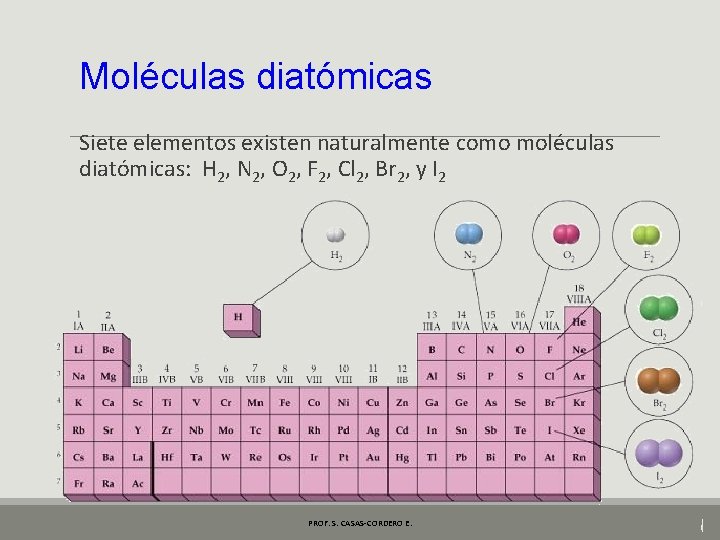
Moléculas diatómicas Siete elementos existen naturalmente como moléculas diatómicas: H 2, N 2, O 2, F 2, Cl 2, Br 2, y I 2 PROF. S. CASAS-CORDERO E.

Ejercicios Balancee los siguientes ejercicios por el método de tanteo e indique los estados si es necesario ◦ ◦ ◦ Ejercicios: H 2(g) + Cl 2(g) HCl(g) C 5 H 12 + O 2 CO 2 + H 2 O Al(s) +O 2(g) Al 2 O 3(s) N 2 O 5 + H 2 O HNO 3 CH 4(g) + 2 O 2(g) CO 2(g) + 2 H 2 O(l) Mg 3 N 2 + H 2 O Mg(OH) 2 + NH 3 Ba. Cl 2 + (NH 4)2 CO 3 Ba. CO 3 + NH 4 Cl Al(OH)3 + HCl Al. Cl 3 + H 2 O Na + H 2 O Na. OH + H 2 Mg + O 2 Mg. O 13
- Slides: 13