REACCIONES REDOX REACCIONES REDOX Tambin llamadas reacciones de

REACCIONES REDOX

REACCIONES REDOX También llamadas reacciones de reducción y oxidación. Son aquellas que ocurren mediante transferencia de electrones, por lo tanto hay sustancias que pierden electrones (se oxidan) y otras que ganan electrones (se reducen)


La gran mayoría de reacciones que son de interés, en química son reacciones de reducción y oxidación, como ejemplos tenemos: • La combustión de los hidrocarburos. • La acción de los agentes blanqueadores de uso domestico • La obtención de los metales a partir de sus minerales • El proceso de respiración • El proceso de digestión • La reacción que ocurre en la pila seca y baterías, etc. .

En toda reacción redox se cumple: El fenómeno de reducción y oxidación es simultáneo, es decir la oxidación y reducción no se presenta en forma aislada #e- (ganados) = #e- (perdidos) La igualdad justifica la ley de conservación de carga eléctrica.

Oxidación Es el fenómeno mediante el cual una especie química pierde electrones, por lo tanto el número de oxidación (N. O. ) aumenta algebraicamente porque pierde carga negativas.

El número de electrones perdidos se halla así: #e-= (mayor carga total ) – (Menor carga total)

Reducción Es el fenómeno mediante el cual una especie química gana electrones, por lo tanto el número de oxidación (N. O. ) disminuye algebraicamente porque gana carga negativas.
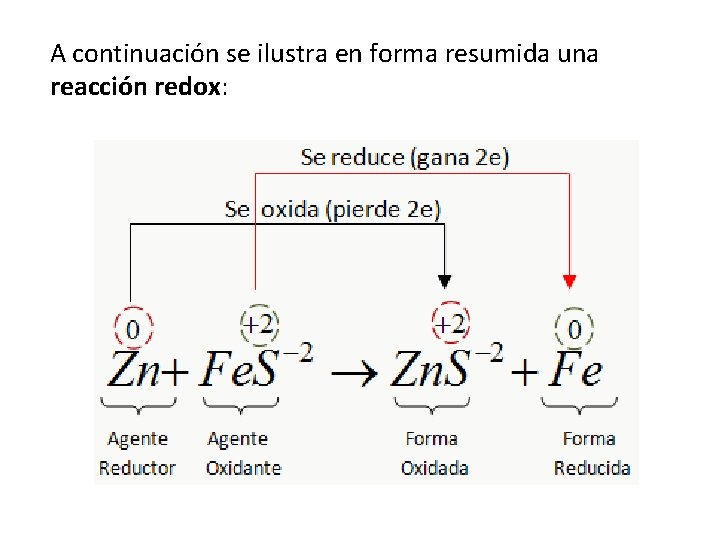
A continuación se ilustra en forma resumida una reacción redox:

Descripción del Proceso: El átomo neutro del Zn (Zn 0) pierde 2 electrones y se convierte en ion cinc (Zn+2) según la siguiente reacción: Zn 0 → Zn+2 + 2 e- ………………. semireacción de oxidación Los dos átomos que pierde el Zn es ganado por el ión ferroso (Fe+2) para convertirse en átomo neutro (Fe 0) Fe+2 + 2 e- → Fe 0 ………………. . semireacción de reducción El ión Zn+2 es forma oxidada del Zn 0 y el Fe 0 es la forma reducida del Fe+2

El sulfuro ferroso Fe. S, se llama oxidante porque contiene al ión Fe+2 , que al reducirse provoca la oxidación del Zn. Al sulfuro de Zinc, Zn. S, se le llama forma oxidada porque contiene al Zn+2 que es la forma oxidada del Zn 0
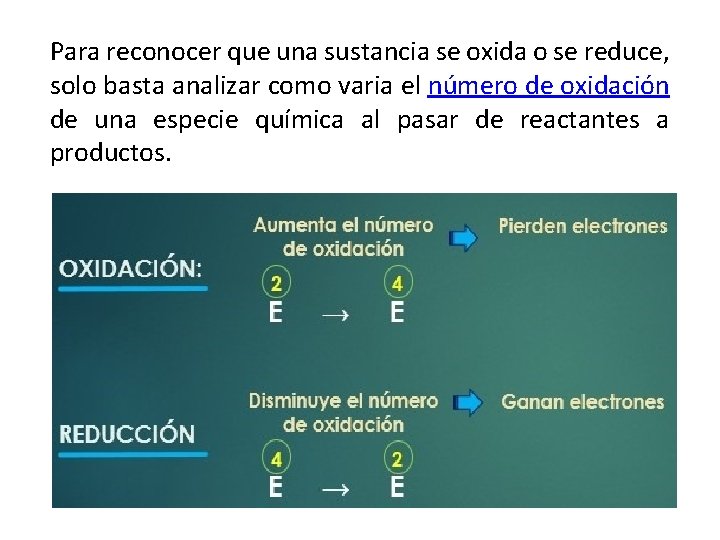
Para reconocer que una sustancia se oxida o se reduce, solo basta analizar como varia el número de oxidación de una especie química al pasar de reactantes a productos.

El agente oxidante, es la sustancia química que al reducirse provoca la oxidación de otro; por lo tanto la sustancia que se reduce es agente oxidante. El agente reductor, es la sustancia quimica que al oxidarse provoca o causa la reducción de otro; por lo tanto la sustancia que se oxida es agente reductor.

Tipos de Reacciones Redox: Las reacciones redox pueden ser clasificadas en tres grupos: 1 Reacción Redox Intermolecular: Son las más comunes, se caracterizan porque el elemento que se oxida y el elemento que se reduce se encuentran en sustancias químicas diferentes, por lo tanto el agente oxidante y el agente reductor son sustancias también diferentes. 2 Reacción Redox Intramolecular: En este caso, el elemento que se oxida y el elemento que se reduce se encuentran en el mismo compuesto, por lo tanto el agente oxidante y el agente reductor es la misma sutancia. 3 Reacción Redox de dismutación o desproporción: Llamada también de autoreducción - oxidación, es aquella donde un mismo elemento se oxida y se reduce. Por lo tanto una misma sustancia química es oxidante y reductor.

Ejercicio 1 Indique en que casos hay oxidación y en cuales hay reducción. a) Fe 0 → Fe 2+ b) S 2 → S 1 c) C 4 → C 2 d) Au-3 → Au-1 Ejercicio 2 Del ejercicio anterior, indicar cuantos electrones ganan o pierden, según cada caso.

Ejercicio 3 En la siguiente reacción química, identificar cada uno de sus términos. 4 N-3 + 5 S 6+ → 3 S 0 + 2 N 5+ Ejercicio 4 del ejercicio 3, calcular la relación de coeficientes del agente reductor y su forma oxidada. Ejercicio 5 del ejercicio 3, calcular la relación de coeficientes del agente oxidante y su forma oxidada.

SOLUCIONARIO

Solución Ejercicio 1 De acuerdo a esto diremos: a) Fe 0 → Fe 2+ : Oxidación b) S 2 → S 1 : Reducción c) C 4 → C 2 : Reducción d) Au-3 → Au-1 : Oxidación Solución Ejercicio 2 a) Fe 0 → Fe 2+ : Oxidación = pierde 2 electrones b) S 2 → S 1 : Reducción = gana 1 electrón c) C 4 → C 2 : Reducción = gana 2 electrones d) Au-3 → Au-1 : Oxidación = pierde 2 electrones
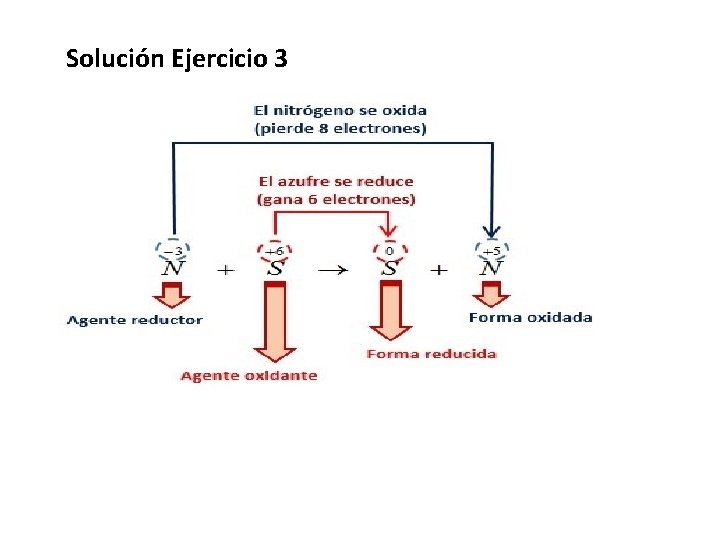
Solución Ejercicio 3

Solución Ejercicio 4 Agente reductor: 4 N-3 Forma oxidada: 2 N 5+. : Entonces la relación de coeficientes: Agente Reductor / Forma oxidada Relación = 4 / 2 Solución Ejercicio 5 Agente oxidante: 5 S-3 Forma oxidada: 2 N 5+. : Entonces la relación de coeficientes: Agente Oxidante / Forma oxidada Relación = 5 / 2



http: //www. fullquimica. com/2014/02/ejercici os-sobre-reacciones-redox. html

http: //www. fullquimica. com/2011/12/reaccio nes-redox. html
- Slides: 24












































