Reacciones en la qumica del carbono polmeros Qumica

Reacciones en la química del carbono polímeros
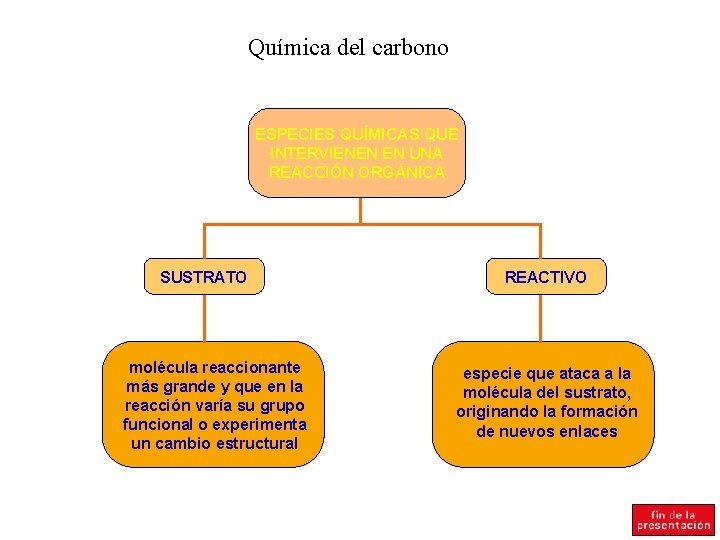
Química del carbono ESPECIES QUÍMICAS QUE INTERVIENEN EN UNA REACCIÓN ORGÁNICA SUSTRATO molécula reaccionante más grande y que en la reacción varía su grupo funcional o experimenta un cambio estructural REACTIVO especie que ataca a la molécula del sustrato, originando la formación de nuevos enlaces
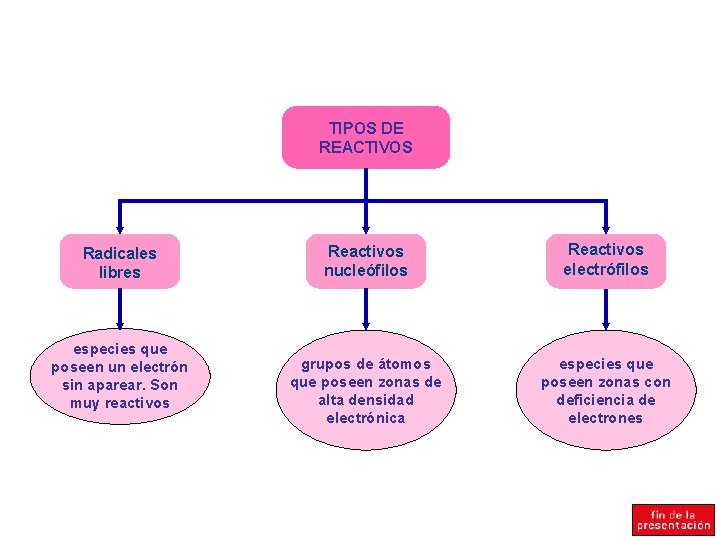
TIPOS DE REACTIVOS Radicales libres especies que poseen un electrón sin aparear. Son muy reactivos Reactivos nucleófilos Reactivos electrófilos grupos de átomos que poseen zonas de alta densidad electrónica especies que poseen zonas con deficiencia de electrones
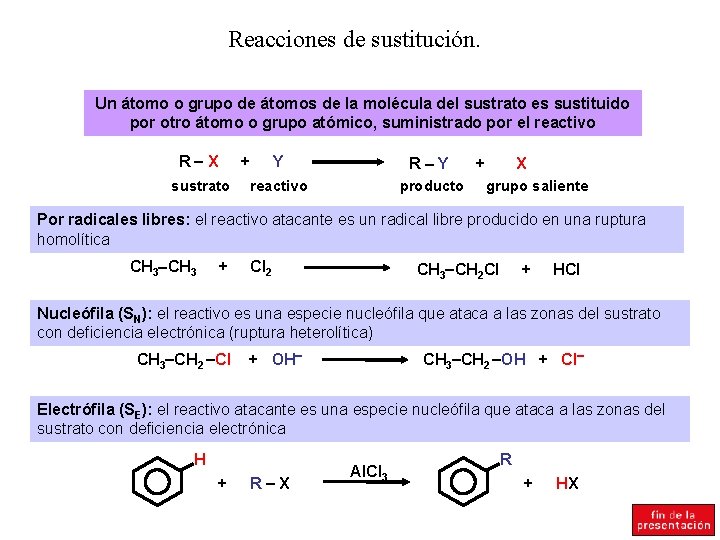
Reacciones de sustitución. Un átomo o grupo de átomos de la molécula del sustrato es sustituido por otro átomo o grupo atómico, suministrado por el reactivo R X + sustrato Y R Y reactivo producto + X grupo saliente Por radicales libres: el reactivo atacante es un radical libre producido en una ruptura homolítica CH 3 + Cl 2 CH 3 CH 2 Cl + HCl Nucleófila (SN): el reactivo es una especie nucleófila que ataca a las zonas del sustrato con deficiencia electrónica (ruptura heterolítica) CH 3 CH 2 Cl CH 3 CH 2 OH + Cl + OH Electrófila (SE): el reactivo atacante es una especie nucleófila que ataca a las zonas del sustrato con deficiencia electrónica H + R X Al. Cl 3 R + HX
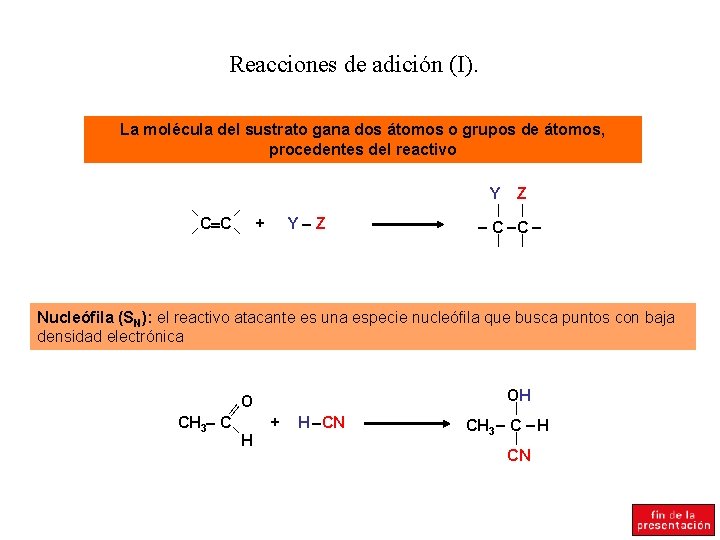
Reacciones de adición (I). La molécula del sustrato gana dos átomos o grupos de átomos, procedentes del reactivo Y C C Y Z + Z C C Nucleófila (SN): el reactivo atacante es una especie nucleófila que busca puntos con baja densidad electrónica ll O CH 3 C H OH + H CN CH 3 C H CN
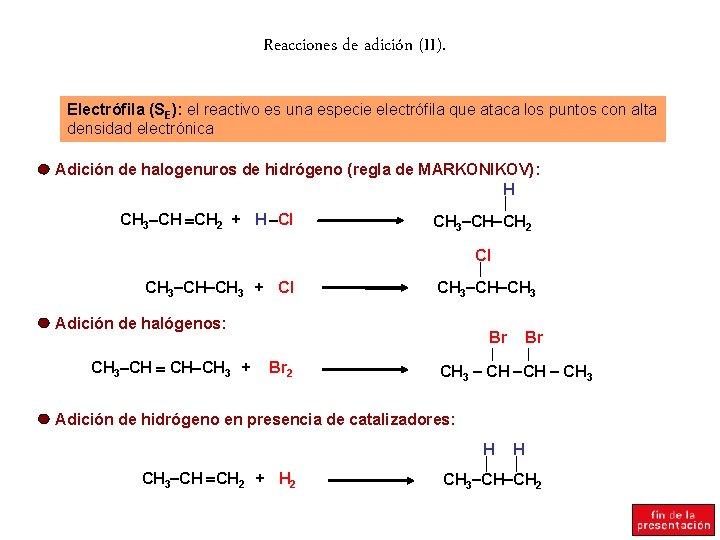
Reacciones de adición (II). Electrófila (SE): el reactivo es una especie electrófila que ataca los puntos con alta densidad electrónica Adición de halogenuros de hidrógeno (regla de MARKONIKOV): H CH 3 CH CH 2 + H Cl CH 3 CH CH 2 Cl CH 3 CH CH 3 + Cl CH 3 CH CH 3 Adición de halógenos: CH 3 CH CH 3 + Br Br 2 Br CH 3 CH CH 3 Adición de hidrógeno en presencia de catalizadores: H CH 3 CH CH 2 + H 2 H CH 3 CH CH 2
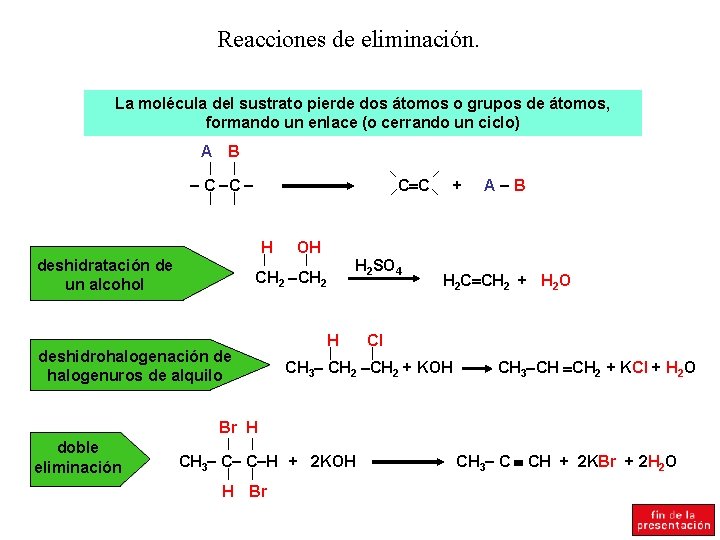
Reacciones de eliminación. La molécula del sustrato pierde dos átomos o grupos de átomos, formando un enlace (o cerrando un ciclo) A B C C H deshidratación de un alcohol + C C OH H 2 SO 4 CH 2 deshidrohalogenación de halogenuros de alquilo A B H H 2 C CH 2 + H 2 O Cl CH 3 CH 2 + KOH CH 3 CH CH 2 + KCl + H 2 O Br H doble eliminación CH 3 C C H + 2 KOH H Br CH 3 C CH + 2 KBr + 2 H 2 O
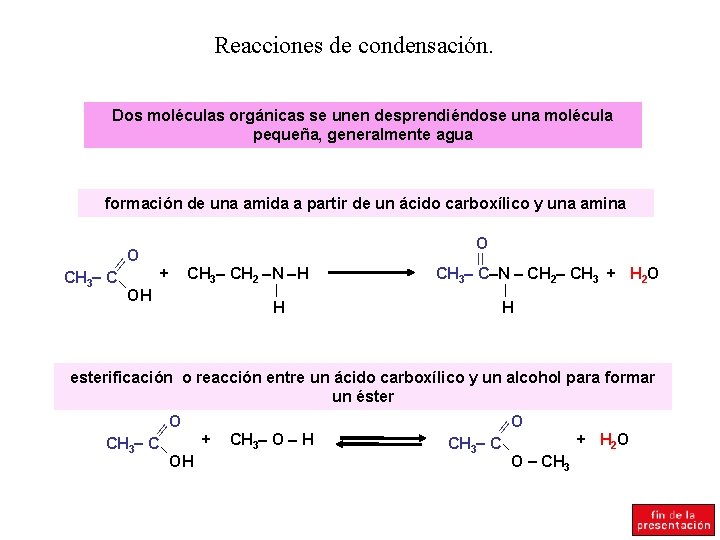
Reacciones de condensación. Dos moléculas orgánicas se unen desprendiéndose una molécula pequeña, generalmente agua formación de una amida a partir de un ácido carboxílico y una amina ll O + CH 3 C OH CH 3 CH 2 N H H O ll CH 3 C N CH 2 CH 3 + H 2 O H esterificación o reacción entre un ácido carboxílico y un alcohol para formar un éster ll O + CH 3 C OH CH 3 O H ll O + H 2 O CH 3 C O CH 3
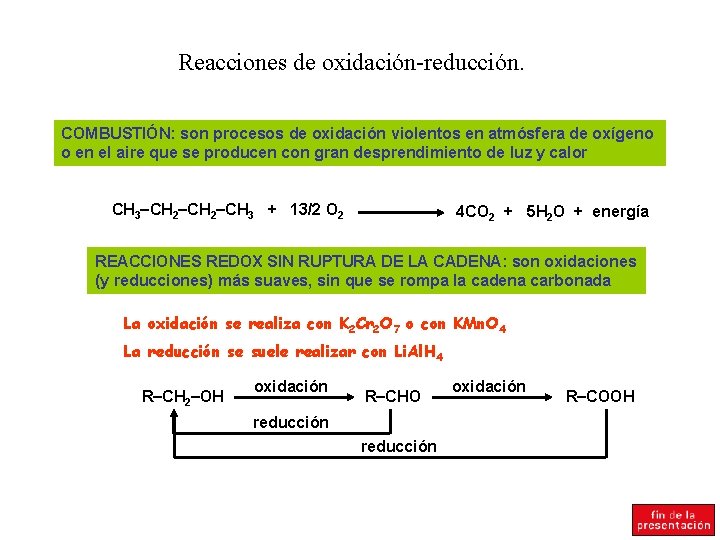
Reacciones de oxidación-reducción. COMBUSTIÓN: son procesos de oxidación violentos en atmósfera de oxígeno o en el aire que se producen con gran desprendimiento de luz y calor CH 3 CH 2 CH 3 + 13/2 O 2 4 CO 2 + 5 H 2 O + energía REACCIONES REDOX SIN RUPTURA DE LA CADENA: son oxidaciones (y reducciones) más suaves, sin que se rompa la cadena carbonada La oxidación se realiza con K 2 Cr 2 O 7 o con KMn. O 4 La reducción se suele realizar con Li. Al. H 4 R CH 2 OH oxidación R CHO reducción oxidación R COOH
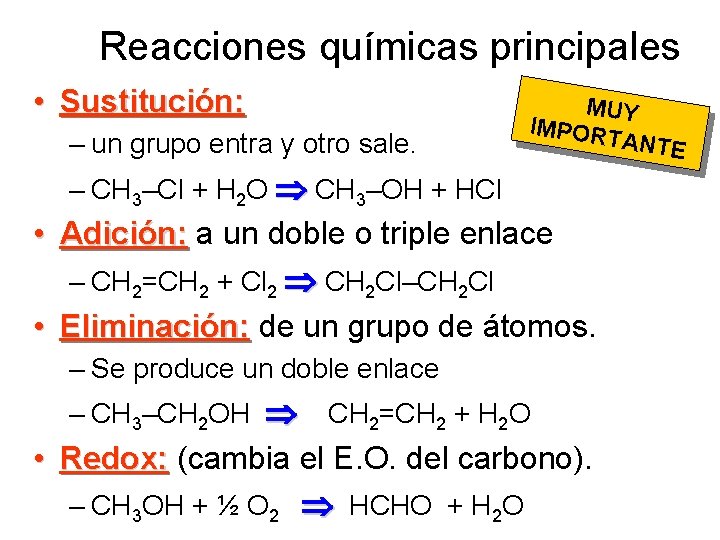
Reacciones químicas principales • Sustitución: – un grupo entra y otro sale. MUY IMPOR TANTE – CH 3–Cl + H 2 O CH 3–OH + HCl • Adición: a un doble o triple enlace – CH 2=CH 2 + Cl 2 CH 2 Cl–CH 2 Cl • Eliminación: de un grupo de átomos. – Se produce un doble enlace – CH 3–CH 2 OH CH 2=CH 2 + H 2 O • Redox: (cambia el E. O. del carbono). – CH 3 OH + ½ O 2 HCHO + H 2 O

• Habitualmente, se sigue utilizando el concepto de oxidación como aumento en la proporción de oxígeno y reducción como disminución es la proporción de oxígeno.
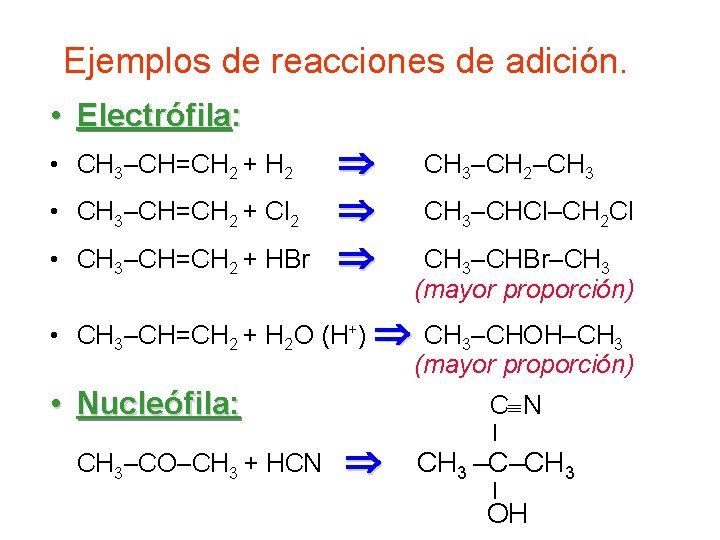
Ejemplos de reacciones de adición. • Electrófila: • CH 3–CH=CH 2 + H 2 • CH 3–CH=CH 2 + Cl 2 • CH 3–CH=CH 2 + HBr CH 3–CH 2–CH 3–CHCl–CH 2 Cl CH 3–CHBr–CH 3 (mayor proporción) • CH 3–CH=CH 2 + H 2 O (H+) CH 3–CHOH–CH 3 (mayor proporción) • Nucleófila: CH 3–CO–CH 3 + HCN C N | CH 3 –C–CH 3 | OH
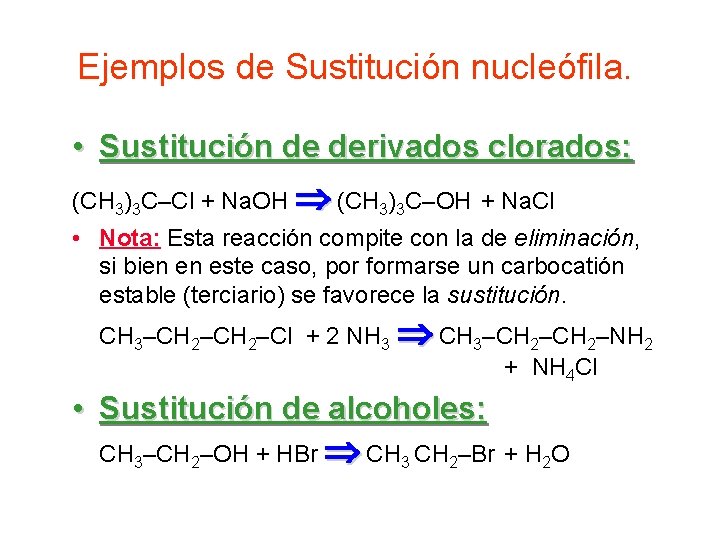
Ejemplos de Sustitución nucleófila. • Sustitución de derivados clorados: (CH 3)3 C–Cl + Na. OH (CH 3)3 C–OH + Na. Cl • Nota: Esta reacción compite con la de eliminación, si bien en este caso, por formarse un carbocatión estable (terciario) se favorece la sustitución. CH 3–CH 2–Cl + 2 NH 3 CH 3–CH 2–NH 2 + NH 4 Cl • Sustitución de alcoholes: CH 3–CH 2–OH + HBr CH 3 CH 2–Br + H 2 O
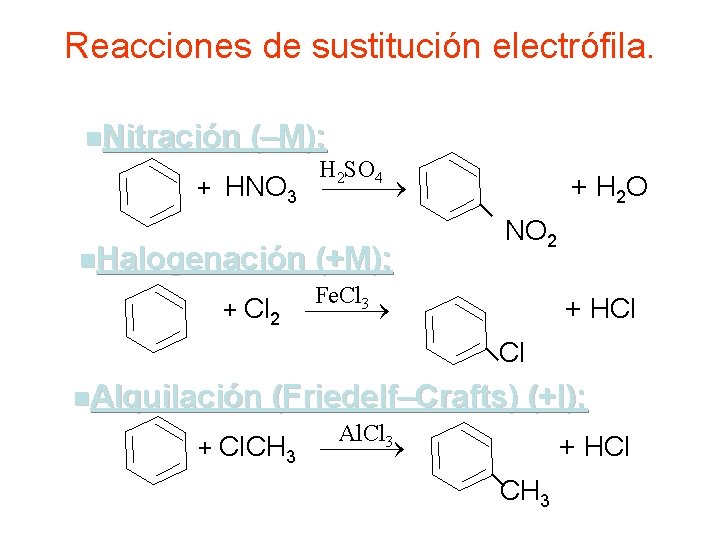
Reacciones de sustitución electrófila. n. Nitración (–M): H 2 SO 4 + HNO 3 n. Halogenación + Cl 2 (+M): + H 2 O NO 2 Fe. Cl 3 + HCl Cl n. Alquilación (Friedelf–Crafts) (+I): + Cl. CH 3 Al. Cl 3 + HCl CH 3

Ejemplos de reacciones de eliminación • Deshidrohalogenación de halogenuros de alquilo. – Se produce en medio básico. CH 3–CH 2–CHBr–CH 3 + Na. OH CH 3–CH=CH–CH 3 • Deshidratación de alcoholes. – Se produce en medio ácido. mayoritario CH 3–CH 2–CHOH–CH 3 + H 2 SO 4 CH 3–CH=CH–CH 3

Reacciones más importantes por grupos funcionales

Alcanos y halogenuros de alquilo COMBUSTIÓN: (la dan todos los compuestos) son procesos de oxidación violentos en atmósfera de oxígeno o en el aire que se producen con gran desprendimiento de luz y calor CH 3 CH 2 CH 3 + 13/2 O 2 4 CO 2 + 5 H 2 O + energía Sustitución: Por radicales libres: el reactivo atacante es un radical libre producido en una ruptura homolítica CH 3 + Cl 2 CH 3 CH 2 Cl + HCl halogenuros de alquilo: deshidrohalogenación con KOH (r. de eliminación) H Cl CH 3 CH CH 2 + KOH CH 3 CH CH 2 + KCl + H 2 O
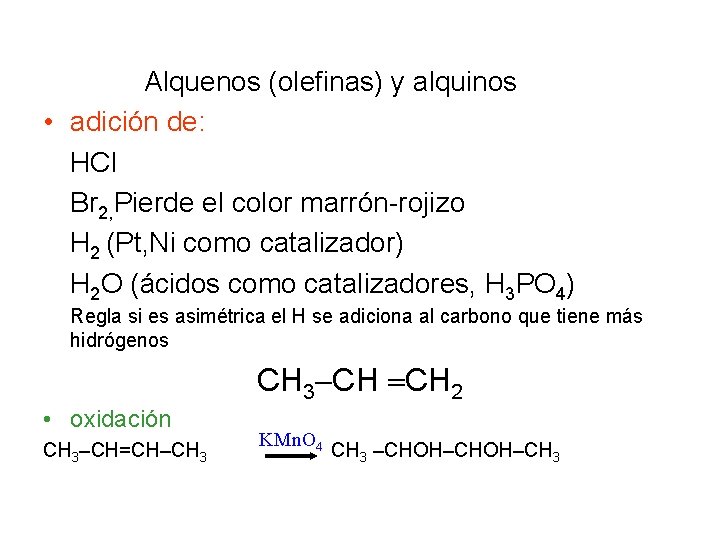
Alquenos (olefinas) y alquinos • adición de: HCl Br 2, Pierde el color marrón-rojizo H 2 (Pt, Ni como catalizador) H 2 O (ácidos como catalizadores, H 3 PO 4) Regla si es asimétrica el H se adiciona al carbono que tiene más hidrógenos CH 3 CH CH 2 • oxidación CH 3–CH=CH–CH 3 KMn. O 4 CH 3 –CHOH–CH 3
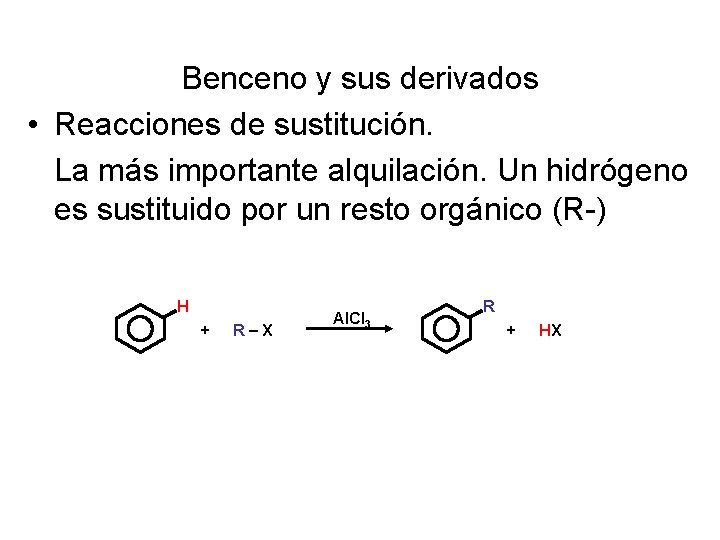
Benceno y sus derivados • Reacciones de sustitución. La más importante alquilación. Un hidrógeno es sustituido por un resto orgánico (R-) H + R X Al. Cl 3 R + HX
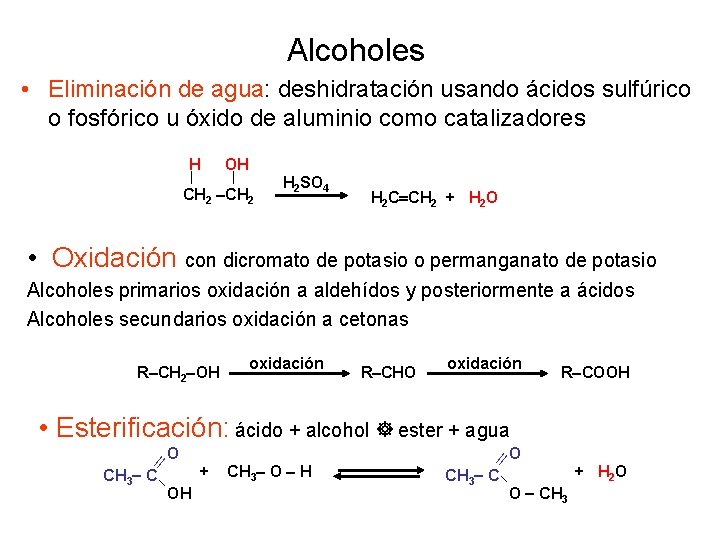
Alcoholes • Eliminación de agua: deshidratación usando ácidos sulfúrico o fosfórico u óxido de aluminio como catalizadores H OH CH 2 H 2 SO 4 H 2 C CH 2 + H 2 O • Oxidación con dicromato de potasio o permanganato de potasio Alcoholes primarios oxidación a aldehídos y posteriormente a ácidos Alcoholes secundarios oxidación a cetonas R CH 2 OH oxidación R CHO oxidación R COOH • Esterificación: ácido + alcohol ester + agua ll O + CH 3 C OH CH 3 O H ll O + H 2 O CH 3 C O CH 3
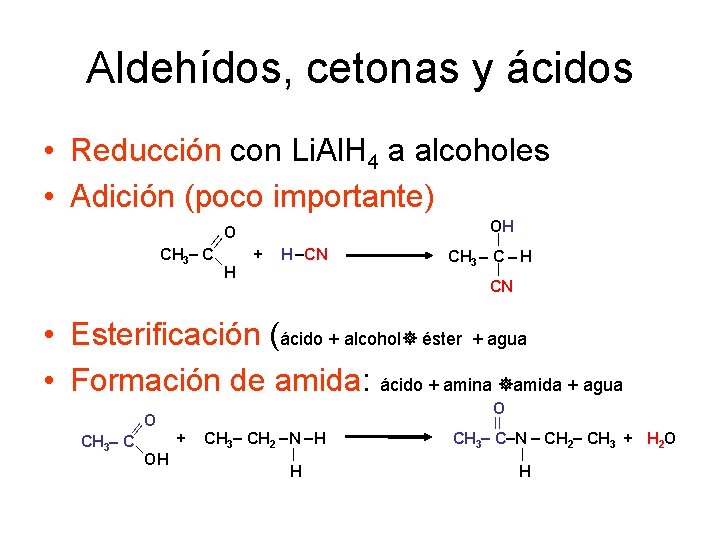
Aldehídos, cetonas y ácidos • Reducción con Li. Al. H 4 a alcoholes • Adición (poco importante) ll O CH 3 C H OH + H CN CH 3 C H CN • Esterificación (ácido + alcohol éster + agua • Formación de amida: ácido + amina amida + agua ll O + CH 3 C OH CH 3 CH 2 N H H O ll CH 3 C N CH 2 CH 3 + H 2 O H
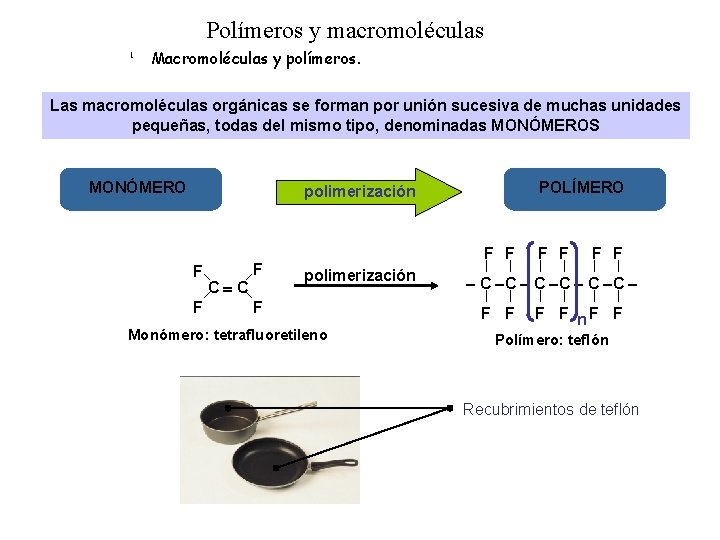
Polímeros y macromoléculas 1 Macromoléculas y polímeros. Las macromoléculas orgánicas se forman por unión sucesiva de muchas unidades pequeñas, todas del mismo tipo, denominadas MONÓMEROS MONÓMERO POLÍMERO polimerización F F C C F F F polimerización F Monómero: tetrafluoretileno F F C C F F n. F F Polímero: teflón Recubrimientos de teflón
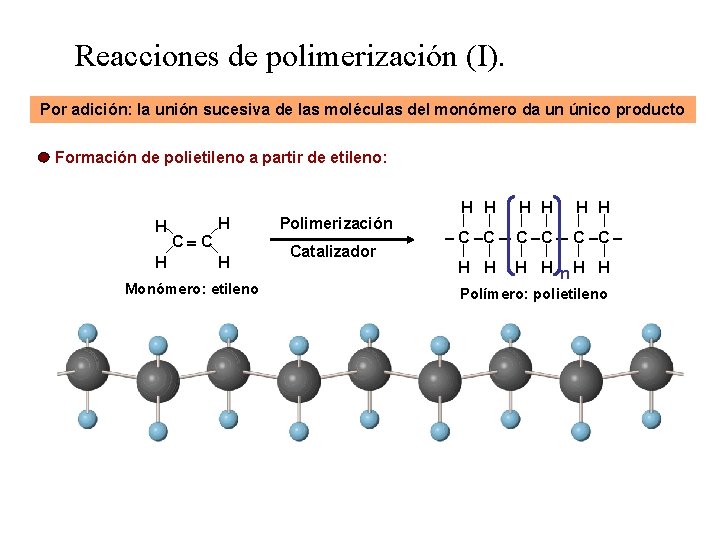
Reacciones de polimerización (I). Por adición: la unión sucesiva de las moléculas del monómero da un único producto Formación de polietileno a partir de etileno: H H C C H H Monómero: etileno Polimerización Catalizador H H H C C H H n. H H Polímero: polietileno
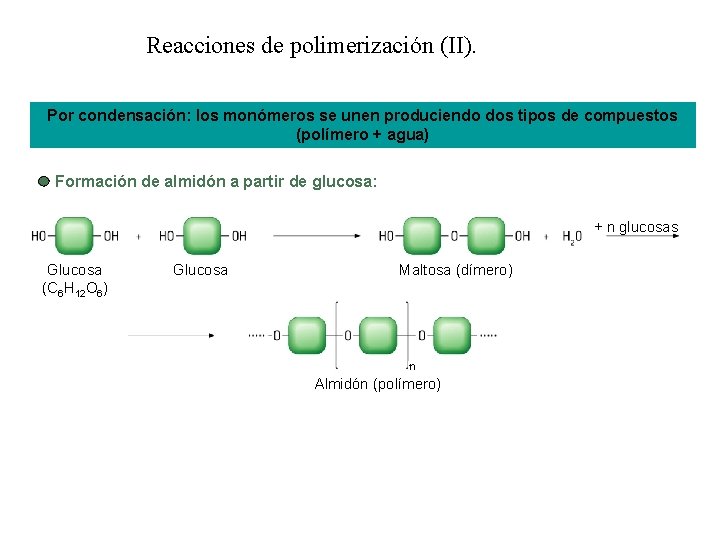
Reacciones de polimerización (II). Por condensación: los monómeros se unen produciendo dos tipos de compuestos (polímero + agua) Formación de almidón a partir de glucosa: + n glucosas Glucosa (C 6 H 12 O 6) Glucosa Maltosa (dímero) n Almidón (polímero)
![Polímeros de adición Monómero Polímero CH 2 [ CH 2 ] n Eteno CH Polímeros de adición Monómero Polímero CH 2 [ CH 2 ] n Eteno CH](http://slidetodoc.com/presentation_image_h/83c0e7fec6529753e82221187f330a57/image-25.jpg)
Polímeros de adición Monómero Polímero CH 2 [ CH 2 ] n Eteno CH 2 CH CH 3 Propeno CH 2 CHCl Cloroeteno CH 2 CHCN Polietileno [ CH 2 CH ] n CH 3 Polipropileno [ CH 2 CH ] n Cl Policloruro de vinilo (PVC) [ CH 2 CH ] n Acrilonitrilo CN Poliacrilonitrilo CH 2 CH [ CH 2 CH ] n Estireno Poliestireno CF 2 Tetrafluoreteno [ CH 2 ] n Teflón Usos típicos Contenedores, tuberías, bolsas, juguetes, cables aislantes. Fibras para alfombras, redes de pesca, cuerdas, cesped artificial. Cañerías, mangueras, discos, cuero artificial, envoltorios para alimentos, baldosas. Fibras para ropa, alfombras, tapices. Espuma de poliestireno, vasos para bebidas calientes, embalajes, aislamientos. Recubrimientos antiadherentes para utensilios de cocina.
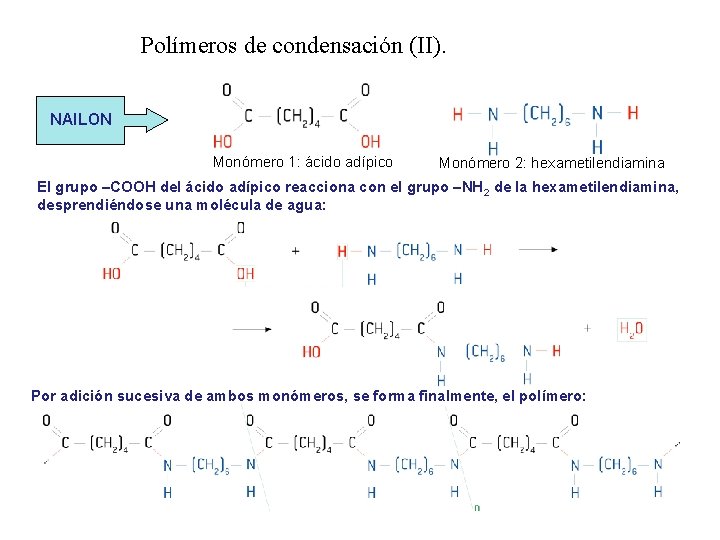
Polímeros de condensación (II). NAILON Monómero 1: ácido adípico Monómero 2: hexametilendiamina El grupo –COOH del ácido adípico reacciona con el grupo –NH 2 de la hexametilendiamina, desprendiéndose una molécula de agua: Por adición sucesiva de ambos monómeros, se forma finalmente, el polímero:
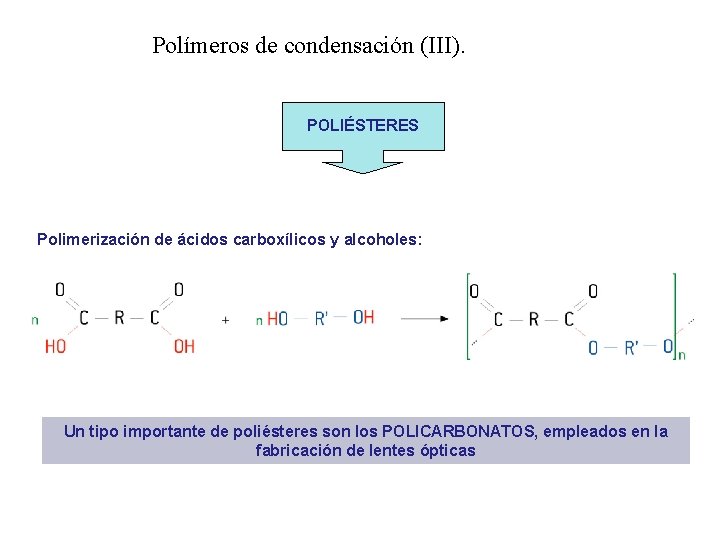
Polímeros de condensación (III). POLIÉSTERES Polimerización de ácidos carboxílicos y alcoholes: Un tipo importante de poliésteres son los POLICARBONATOS, empleados en la fabricación de lentes ópticas
- Slides: 27