Reacciones de transferencia cidoBase PROFESORA ROXANA REINOSO CARO

Reacciones de transferencia: Ácido-Base PROFESORA: ROXANA REINOSO CARO MATERIAL DE APOYO QUÍMICA 4º MEDIO

ÁCIDOS Y BASES

Teoría de Arrhenius Según esta teoría, en medio acuoso los ácidos se disocian en iones positivos (H+, protones) e iones negativos (aniones). Las bases se disocian en iones positivos (cationes) e iones negativos (OH–, hidroxilos). Las sustancias que en disolución acuosa conducen la corriente eléctrica se llaman electrolitos.
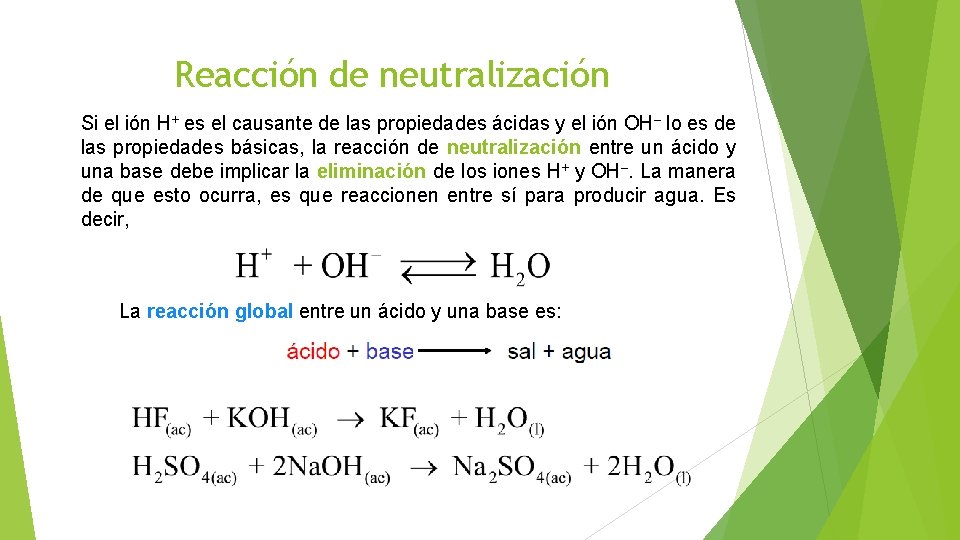
Reacción de neutralización Si el ión H+ es el causante de las propiedades ácidas y el ión OH– lo es de las propiedades básicas, la reacción de neutralización entre un ácido y una base debe implicar la eliminación de los iones H+ y OH–. La manera de que esto ocurra, es que reaccionen entre sí para producir agua. Es decir, La reacción global entre un ácido y una base es:

Teoría de Bronsted-Lowry Esta teoría engloba todos los aspectos de la teoría de Arrhenius, elimina la necesidad de una disolución acuosa y considera mayor cantidad de sustancias que pueden considerarse ácidas y básicas. Según Bronsted y Lowry: Ácidos: son las sustancias (moleculares o iónicas) que pueden ceder iones H+: Bases: son las sustancias (moleculares o iónicas) que pueden captar iones H+ : Según la teoría de Bronsted-Lowry, se producen otro ácido y otra base, que son conjugados, respectivamente, de la base y del ácido que constituyen los reactivos del proceso.
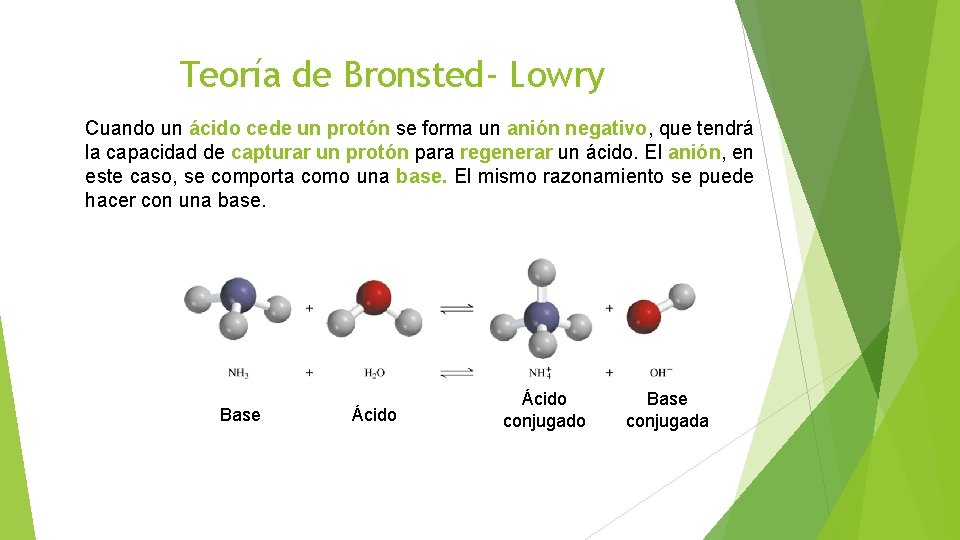
Teoría de Bronsted- Lowry Cuando un ácido cede un protón se forma un anión negativo, que tendrá la capacidad de capturar un protón para regenerar un ácido. El anión, en este caso, se comporta como una base. El mismo razonamiento se puede hacer con una base. Base Ácido conjugado Base conjugada
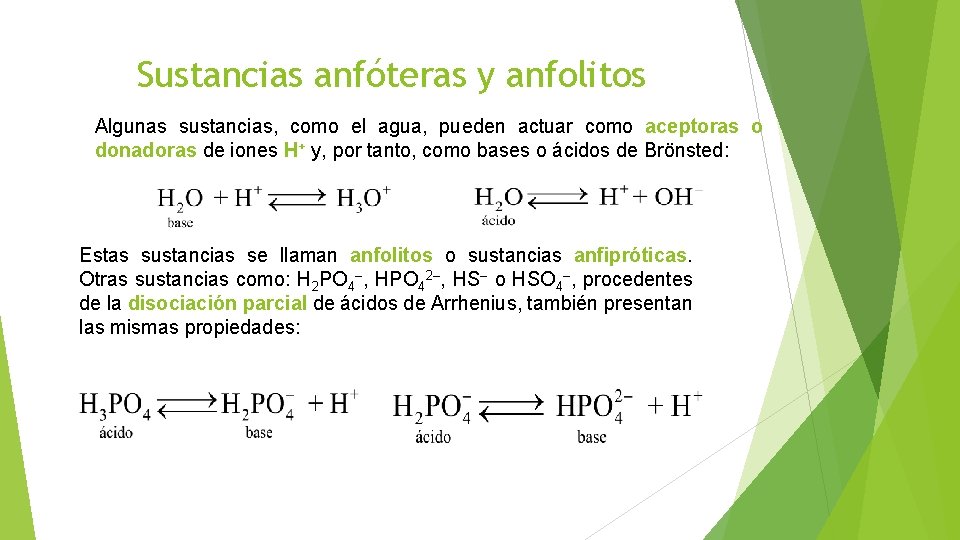
Sustancias anfóteras y anfolitos Algunas sustancias, como el agua, pueden actuar como aceptoras o donadoras de iones H+ y, por tanto, como bases o ácidos de Brönsted: Estas sustancias se llaman anfolitos o sustancias anfipróticas. Otras sustancias como: H 2 PO 4–, HPO 42–, HS– o HSO 4–, procedentes de la disociación parcial de ácidos de Arrhenius, también presentan las mismas propiedades:
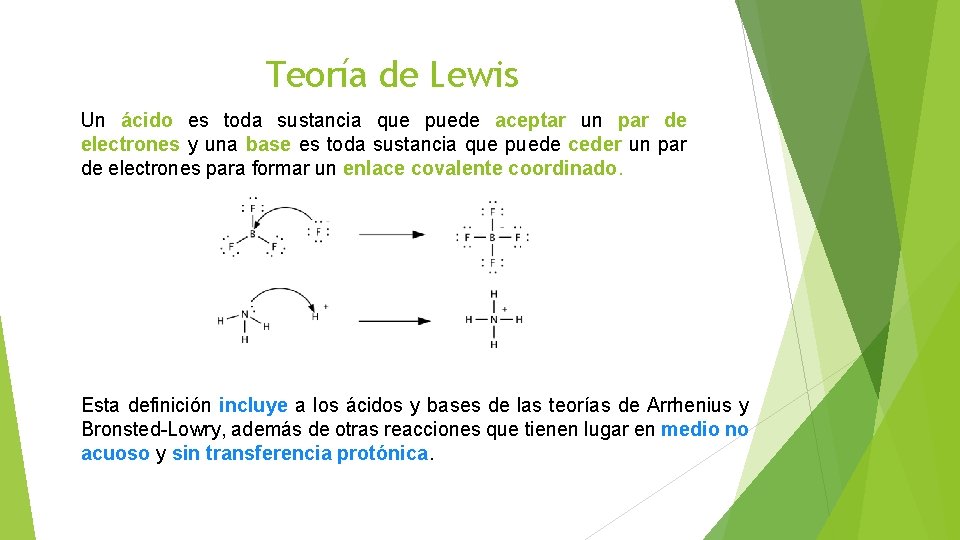
Teoría de Lewis Un ácido es toda sustancia que puede aceptar un par de electrones y una base es toda sustancia que puede ceder un par de electrones para formar un enlace covalente coordinado. Esta definición incluye a los ácidos y bases de las teorías de Arrhenius y Bronsted-Lowry, además de otras reacciones que tienen lugar en medio no acuoso y sin transferencia protónica.
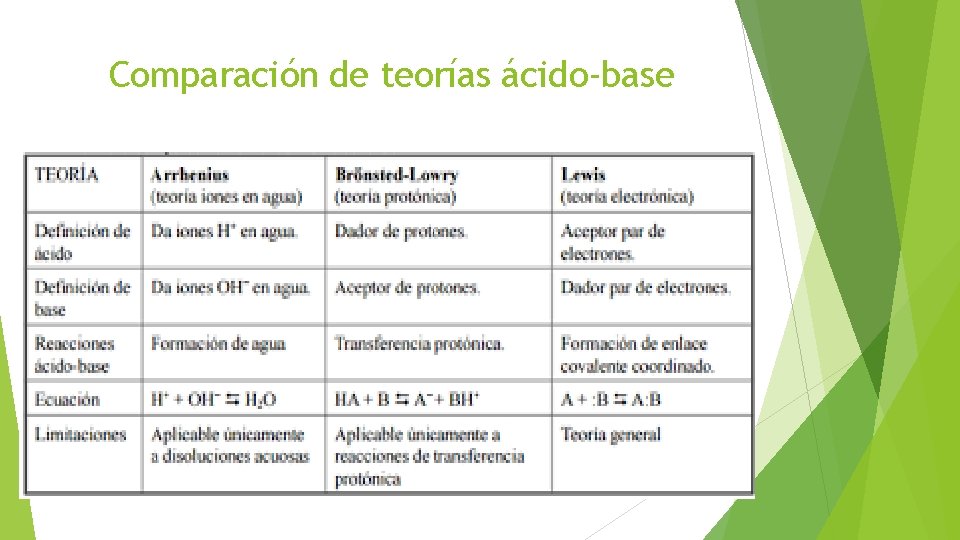
Comparación de teorías ácido-base

Fuerzas de ácidos y bases Las disoluciones de los ácidos y bases son equilibrios químicos para los que los valores de sus constantes de equilibrio Ka y Kb (constantes de disociación para un ácido y una base, respectivamente) representan una medida cuantitativa de su fuerza.

Fuerzas de ácidos y bases Para el amoniaco, base de Brönsted, se puede hacer el mismo análisis, hasta obtener la constante de basicidad, Kb. Teóricamente, se consideran ácidos y bases fuertes aquellos que están totalmente disociados en disoluciones diluidas. Ácidos y bases débiles son los que están disociados parcialmente, coexistiendo en el equilibrio las formas iónicas y moleculares.
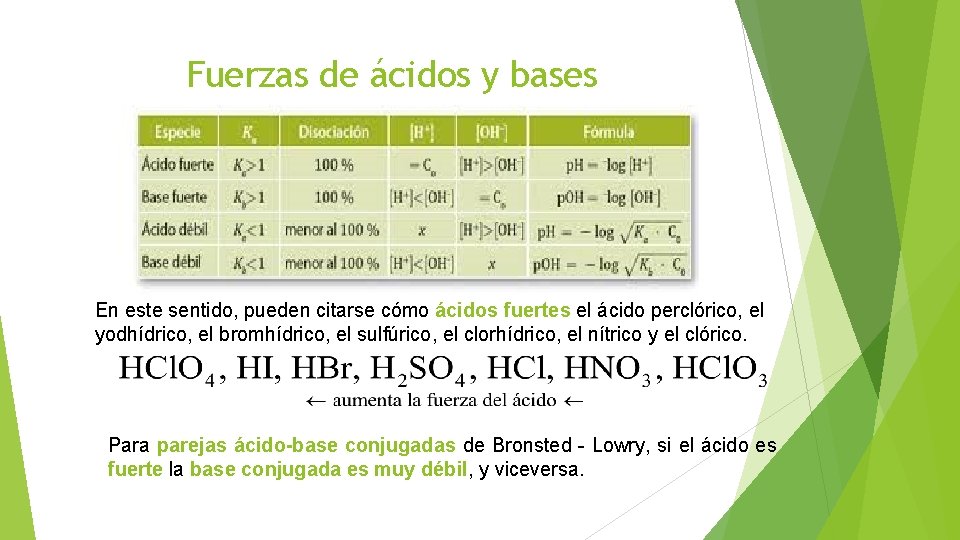
Fuerzas de ácidos y bases En este sentido, pueden citarse cómo ácidos fuertes el ácido perclórico, el yodhídrico, el bromhídrico, el sulfúrico, el clorhídrico, el nítrico y el clórico. Para parejas ácido-base conjugadas de Bronsted - Lowry, si el ácido es fuerte la base conjugada es muy débil, y viceversa.
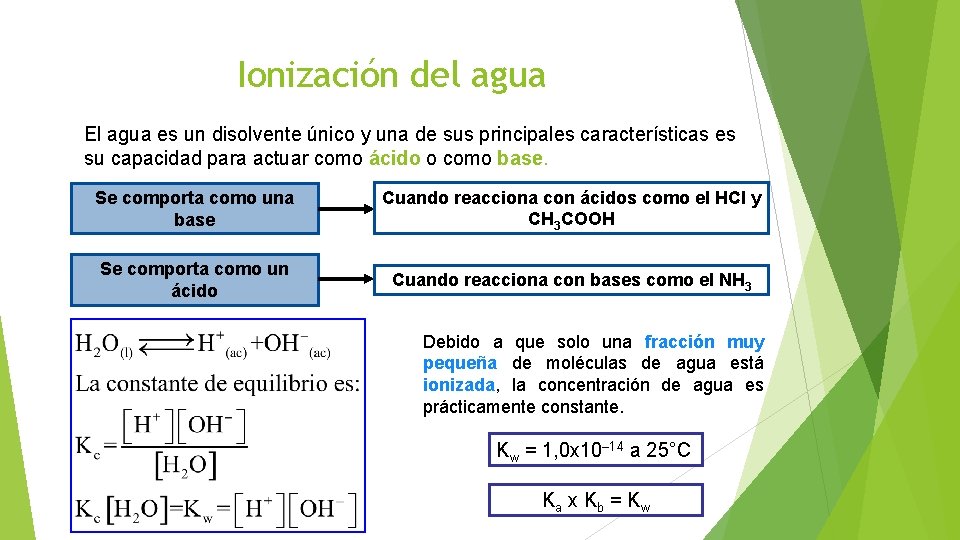
Ionización del agua El agua es un disolvente único y una de sus principales características es su capacidad para actuar como ácido o como base. Se comporta como una base Cuando reacciona con ácidos como el HCl y CH 3 COOH Se comporta como un ácido Cuando reacciona con bases como el NH 3 Debido a que solo una fracción muy pequeña de moléculas de agua está ionizada, la concentración de agua es prácticamente constante. Kw = 1, 0 x 10– 14 a 25°C Ka x K b = K w

Concepto de p. H Para indicar la concentración de iones hidrógeno en una disolución, se emplea la notación denominada p. H, cuya definición es: p. H = log = –log [H+] Una disolución neutra, [H+] = 1 x 10– 7, tendrá un p. H = 7 p. H= –log [H+] = –log 1 x 10– 7 = – 7(–log 10)= 7 Una disolución ácida, [H+] > 1 x 10– 7, tendrá un p. H < 7 por ejemplo, [H +] = 1 x 10– 5 implica que p. H= 5 Una disolución básica, [H+] <1 x 10– 7, tendrá un p. H > 7 por ejemplo [H +] = 1 x 10– 9 implica que p. H= 9 [H+] x [OH–] =1 x 10– 14 p. H + p. OH = 14 El p. H y p. OH resultan muy útiles para establecer de manera rápida la acidez y basicidad de una sustancia.

Escala de p. H

Disoluciones amortiguadoras o reguladoras Las disoluciones que están formadas por ácidos débiles y una de sus sales (que provenga de una base fuerte) o bases débiles y una de sus sales (que provenga de un ácido fuerte), se denominan disoluciones reguladoras o amortiguadoras. La disolución tiene la capacidad de resistir los cambios de p. H cuando se agregan pequeñas cantidades de ácido o base. La capacidad amortiguadora, es decir, la efectividad de la disolución amortiguadora, depende de la cantidad de ácido y de base conjugada que tenga la disolución. Cuanto mayor sea esa cantidad, mayor será la capacidad amortiguadora. El sistema amortiguador suele representarse como sal/ácido o base conjugada/ácido: CH 3 COONa/CH 3 COOH ; KH 2 PO 4/H 3 PO 4 ; C 5 H 5 N/C 5 H 5 NHCl

Indicadores de p. H Se llaman indicadores ciertas sustancias generalmente orgánicas de carácter ácido (o básico) débil, que tienen la propiedad de cambiar de color al variar el p. H entre valores bien determinados. Estos son muy utilizados para las valoraciones ácido-base. El cambio de color de los indicadores es debido a la distinta coloración que ofrecen la forma molecular y la forma iónica del mismo.
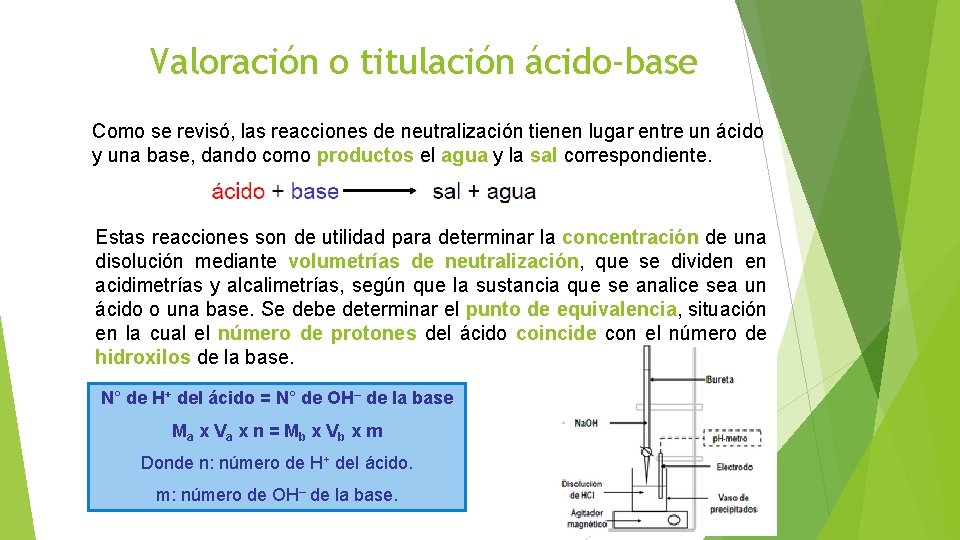
Valoración o titulación ácido-base Como se revisó, las reacciones de neutralización tienen lugar entre un ácido y una base, dando como productos el agua y la sal correspondiente. Estas reacciones son de utilidad para determinar la concentración de una disolución mediante volumetrías de neutralización, que se dividen en acidimetrías y alcalimetrías, según que la sustancia que se analice sea un ácido o una base. Se debe determinar el punto de equivalencia, situación en la cual el número de protones del ácido coincide con el número de hidroxilos de la base. N° de H+ del ácido = N° de OH– de la base Ma x V a x n = M b x V b x m Donde n: número de H+ del ácido. m: número de OH– de la base.
- Slides: 18