Qumica Reacciones qumicas Profesora Lucia Carballada 1 REACCIONES

Química Reacciones químicas Profesora : Lucia Carballada 1

REACCIONES QUÍMICAS CONCEPTO Son cambios o transformaciones en la cual una o más sustancias iniciales llamadas reactantes, mediante choque efectivos entre si, originan la ruptura de enlaces, produciéndose entonces la formación de nuevos enlaces químicos, los que darán lugar a la formación de nuevas sustancias denominados productos con propiedad distintas a los reactantes. 2

ECUACIÓN QUÍMICA Una ecuación química es la representación escrita y abreviada de una reacción química. § A la izquierda se escriben las fórmulas de los reactivos (sustancias reaccionantes) § A la derecha se escriben las fórmulas de los productos (sustancias resultantes) § Separadas por una flecha. También pueden contener información sobre el estado físico de las sustancias y sobre las condiciones de la reacción. Ejemplo: 3

Donde: sólido (s) vapor (v) 1, 2, 1, 1 y 1 líquido (l) acuoso (ac) gaseoso (g) coeficientes estequiométricos EVIDENCIAS DE OCURRENCIA DE UNA REACCIÓN QUÍMICA Ø Ø Liberación de gas (burbujas) Cambio en color, olor y sabor Formación de precipitados (son los insolubles) Variación en la temperatura del sistema (cambio térmico) 4

CLASIFICACIÓN DE LAS REACCIONES QUÍMICAS I. POR LA NATURALEZA DE LOS REACTANTES 1. Reacción de Adición (Síntesis). Cuando reaccionan dos o más reactantes para formar un solo producto Ejemplo: § Las reacciones entre dos no metales dan compuestos covalentes: N 2 + 3 H 2 2 NH 3 § Las reacciones entre un no metal y un metal dan sales: S + Fe Fe. S § Las reacciones entre un óxido y agua producen hidróxidos: Ca. O + H 2 O Ca(OH)2 § Las reacciones entre un anhídrido y agua producen ácidos: SO 2 + H 2 O H 2 SO 3 § Las reacciones entre un óxido y un anhídrido dan sales: Ca. O + SO 2 Ca. SO 3 5

En general: 2. Reacción de Descomposición. Denominada también de análisis se caracteriza porque a partir de un reactante, se obtiene 2 o más productos. Por lo general se necesita energía. Ejemplo: En general: 3. Reacción de Desplazamiento Simple. Es la reacción de una sustancia simple (elemento químico) con un compuesto, donde el elemento desplaza a otro que se encentra formando parte del compuesto. Esto se fundamenta en la mayor actividad química. Ejemplo: 6

§ Algunos metales reaccionan con ciertos ácidos reemplazando el hidrógeno y formando la sal correspondiente: Zn + H 2 SO 4 Zn. SO 4 + H 2 § Un metal puede ser desplazado de sus sales por otro metal más activo: Zn + Cu. SO 4 Zn. SO 4 + Cu En General: 4. Reacción de Doble Desplazamiento (METATESIS). Es la reacción entre dos compuestos donde existe un intercambio de elementos generando dos compuestos. En este tipo de reacción los reactantes están generalmente en medio acuoso. Ejemplo: Precipitado Neutralización 7

En General: II. POR LA VARIACIÓN DE LA ENERGÍA (ENTALPÍA) Entalpía (H). Indica el contenido calórico característico de cada sustancia química. Se mide a 25ºC y 1 atm. llamada condición Standard. El cuadro siguiente muestra algunos valores de entalpía. Sustancia NO NO 2 H 2 O Na. Cl H 2 H(kcal/mol) 20 8 -68 -98 0 Cambio de Entalpía (ΔH). Se llama calor de reacción y determina la energía liberada o absorvida a condición Standard Sea la reacción: A+B HR C+D HP 8

ΔH = HP - HR HP: Entalpía de los productos HR: Entalpía de los reactantes 1. Reacción Exotérmica (ΔH < 0). Reacción en donde hay una pérdida (libera) neta de energía en forma de calor, por lo tanto la entalpía de los productos es menor respecto a los reactantes. Ejemplo: ó 9
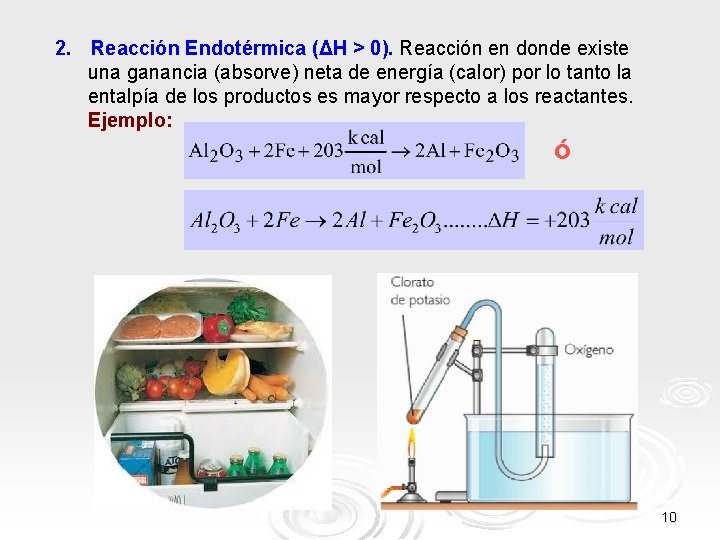
2. Reacción Endotérmica (ΔH > 0). Reacción en donde existe una ganancia (absorve) neta de energía (calor) por lo tanto la entalpía de los productos es mayor respecto a los reactantes. Ejemplo: ó 10
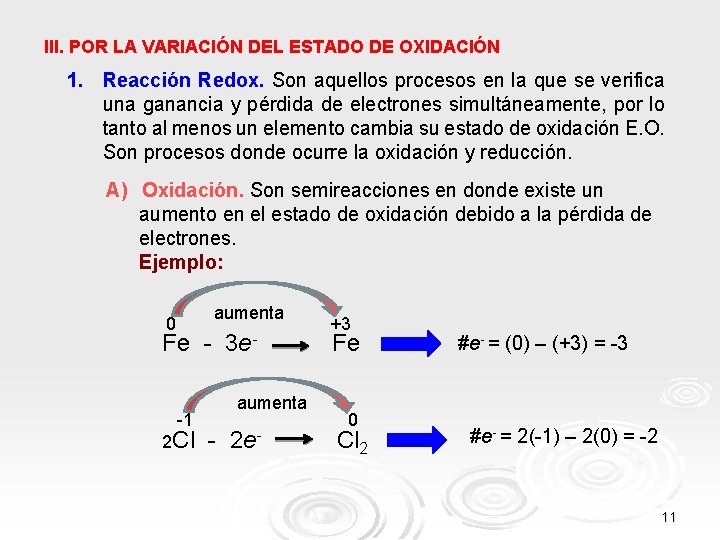
III. POR LA VARIACIÓN DEL ESTADO DE OXIDACIÓN 1. Reacción Redox. Son aquellos procesos en la que se verifica una ganancia y pérdida de electrones simultáneamente, por lo tanto al menos un elemento cambia su estado de oxidación E. O. Son procesos donde ocurre la oxidación y reducción. A) Oxidación. Son semireacciones en donde existe un aumento en el estado de oxidación debido a la pérdida de electrones. Ejemplo: aumenta 0 Fe - 3 e-1 2 Cl aumenta - 2 e- +3 Fe 0 Cl 2 #e- = (0) – (+3) = -3 #e- = 2(-1) – 2(0) = -2 11
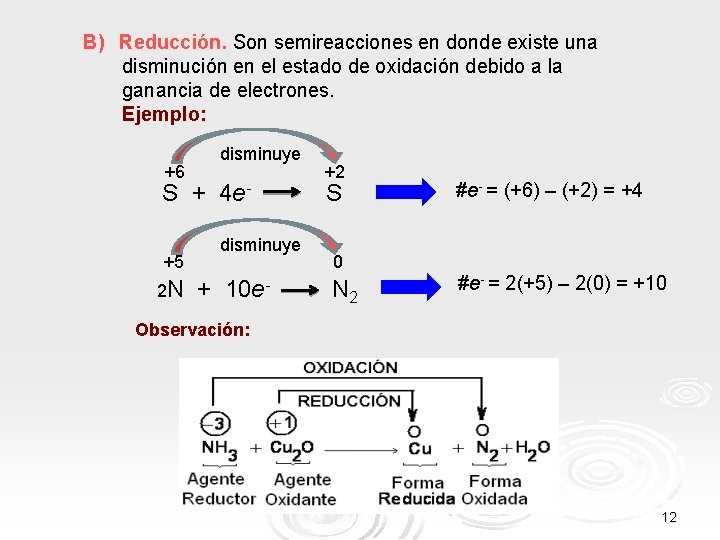
B) Reducción. Son semireacciones en donde existe una disminución en el estado de oxidación debido a la ganancia de electrones. Ejemplo: disminuye +6 S + 4 edisminuye +5 2 N + 10 e- +2 S #e- = (+6) – (+2) = +4 0 N 2 #e- = 2(+5) – 2(0) = +10 Observación: 12
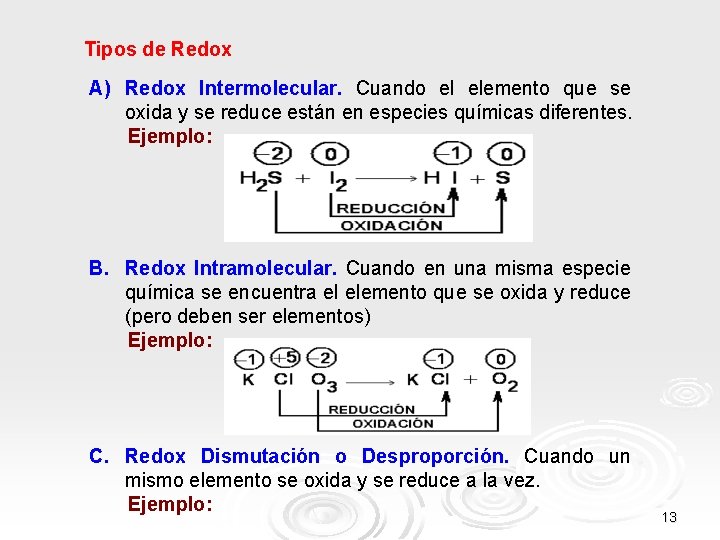
Tipos de Redox A) Redox Intermolecular. Cuando el elemento que se oxida y se reduce están en especies químicas diferentes. Ejemplo: B. Redox Intramolecular. Cuando en una misma especie química se encuentra el elemento que se oxida y reduce (pero deben ser elementos) Ejemplo: C. Redox Dismutación o Desproporción. Cuando un mismo elemento se oxida y se reduce a la vez. Ejemplo: 13
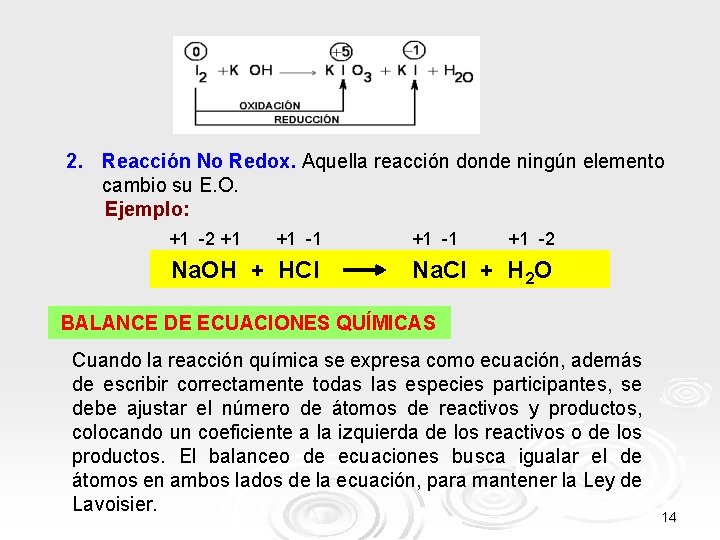
2. Reacción No Redox. Aquella reacción donde ningún elemento cambio su E. O. Ejemplo: +1 -2 +1 +1 -1 Na. OH + HCl +1 -1 +1 -2 Na. Cl + H 2 O BALANCE DE ECUACIONES QUÍMICAS Cuando la reacción química se expresa como ecuación, además de escribir correctamente todas las especies participantes, se debe ajustar el número de átomos de reactivos y productos, colocando un coeficiente a la izquierda de los reactivos o de los productos. El balanceo de ecuaciones busca igualar el de átomos en ambos lados de la ecuación, para mantener la Ley de Lavoisier. 14

MÉTODOS PARA BALANCEAR UNA DE ECUACIÓN QUÍMICA 1. MÉTODO DE SIMPLE INSPECCIÓN (TANTEO) Pasos a seguir: Ø Ø Se balancean los metales Se balancean los no metales Se balancean los átomos de hidrógeno. Se balancean los átomos de oxígeno. Ejemplo: Balancear las siguientes ecuaciones químicas ü N 2 + H 2 ü C 3 H 8 + O 2 ü H 3 PO 4 + Mg ü KCl. O 3 NH 3 CO 2 + H 2 O Mg 3(PO 4)2 + H 2 KCl + O 2 15

2. MÉTODO DEL NÚMERO DE OXIDACIÓN (REDOX) Pasos a seguir: Ø Asignar el estado de oxidación a cada uno de los átomos de los elementos. Ø Identificar los elementos que han cambiado de estado de oxidación. Ø Escribir por separado los pares redox hacia la oxidación y hacia la reducción, balanceando el número de átomos de los elementos que han cambiado su estado de oxidación y el número de electrones intercambiados. Ø Multiplicar la ecuaciones por los menores números que permitan igualar el número de electrones donados y recibidos. Ø Transferir los coeficientes encontrados a la ecuación original. Ø Terminar el balanceo de los átomos de los elementos restantes (por “tanteo”). 16

Ejemplo: (CEPRE-UNMSM) Balancee la siguiente reacción y marque la secuencia correcta: KCl. O 3 + KI + HCl KCl + H 2 O + I 2 I. El I 2 es el agente reductor. II. Se transfieren 10 moles de electrones. III. El agente oxidante es KCIO 3. Solución: 17
- Slides: 17