QUMICA ORGNICA Bachillerato Internacional NM Mila Madiedo NDICE

QUÍMICA ORGÁNICA Bachillerato Internacional NM (Mila Madiedo)

ÍNDICE ISOMERÍA HIDROCARBUROS ALCANOS ALQUENOS POLÍMEROS SINTÉTICOS ALCOHOLES HALOGENUROS DE ALQUILO GRUPOS FUNCIONALES BI RESUMEN PROPIEDADES FÍSICAS

ISOMERÍA Estructural o plana: difieren en el orden en que están enlazados los átomos en la molécula. Estereoisomería: difieren en la disposición tridimensional de sus átomos.

ISOMERÍA ESTRUCTURAL De cadena: difieren en la colocación de algún átomo o grupo de átomos Geométrica, cis-trans o Z-E, característica de compuestos con doble enlace. 1 -buteno (CH 3 CH 2 CH=CH 2) Cis-2 -buteno Metilpropeno ((CH 3)2 C=CH 2) Trans-2 -buteno De posición: difieren en la posición del grupo funcional 1 -propanol (CH 3 CH 2 OH) 2 -propanol (CH 3 CHOHCH 3) ESTEREOISOMERÍA De función: difieren en el grupo funcional Propanona (CH 3 COCH 3) Propanal (CH 3 CH 2 CHO) Óptica, que se da en moléculas con átomos de carbono asimétricos o quirales. Ácido 2 -hidroxipropanoico (láctico)

HIDROCARBUROS Serie homóloga: conjunto de compuestos con la misma fórmula general. Sus propiedades químicas son similares y las propiedades físicas varían de forma gradual. En los hidrocarburos: ALCANOS ALQUENOS ALQUINOS AROMÁTICOS

ALCANOS 1. 2. 3. 4. Hidrocarburos saturados formados por carbono, hidrógeno y enlaces simples. Según la cadena puede ser: Alifáticos: de cadena lineal: Cn. H 2 n+2 Cicloalcanos: de cadena cíclica: Cn. H 2 n Los carbonos se clasifican en: Primarios: enlazados a un átomo de C Secundarios: enlazados a dos átomos de C Terciarios: enlazados a tres átomos de C Cuaternarios: enlazados a cuatro átomos de C

PROPIEDADES DE LOS ALCANOS Propiedades físicas: El punto de fusión y ebullición aumenta regularmente al aumentar el número de carbonos que forman la cadena. www. rena. edu. ve/cuarta. Etapa/quimica/Tema 8. html Malos conductores de la electricidad, sus moléculas son muy poco polares. Insolubles en agua, solubles en disolventes no polares.

PROPIEDADES DE LOS ALCANOS 1. 2. Presentan poca reactividad debido a que los enlaces de carbono son relativamente estables (parafinas). Dan reacciones de oxidación-reducción: Combustión: alcano + oxígeno = dióxido de carbono + agua Reacción con halógenos: reacciones de sustitución

REACCIÓN DE COMBUSTIÓN Cuando se produce una combustión incompleta de los alcanos debido a la insuficiente cantidad de oxígeno, la reacción que tiene lugar es la siguiente: Alcano + oxígeno = C(s) + CO(g) + CO 2(g) + H 2 O (l) Cuando la cantidad de oxígeno es suficiente la combustión completa produce dióxido de carbono y agua: 2 C 8 H 8(l) + 25 O 2(g) = 16 CO 2(g) + 18 H 2 O (l)

REACCIÓN DE HALOGENACIÓN Es una reacción de sustitución que tiene lugar en presencia de luz ultravioleta a través de radicales libres: UV CH 4(g) + Cl 2 (g) = CH 3 Cl(g) + HCl(g) El mecanismo de la reacción tiene varias etapas: Iniciación Cl-Cl(g) = 2 Cl. (g) Propagación Cl. (g) + CH 4(g) = CH 3. (g) + HCl(g) CH 3. (g) + Cl 2(g) = CH 3 Cl(g) + Cl. (g) Terminación Cl. (g) + Cl. (g) = Cl 2(g) Cl. (g) + CH 3. (g) = CH 3 Cl(g) CH 3. (g) + CH 3. (g) = C 2 H 6(g) Si hay suficiente cloro la reacción da lugar a todos los productos de halogenación, no sólo el monosustituido.

ALQUENOS Serie homóloga de fórmula general: Cn. H 2 n Propiedades físicas (similares a las de los alcanos) Bajos puntos de ebullición, los tres primeros alquenos son gases a temperatura ambiente. Los isómeros Z presentan mayor punto de ebullición que los E. No polares o muy poco polares. Insolubles en disolventes polares como el agua.
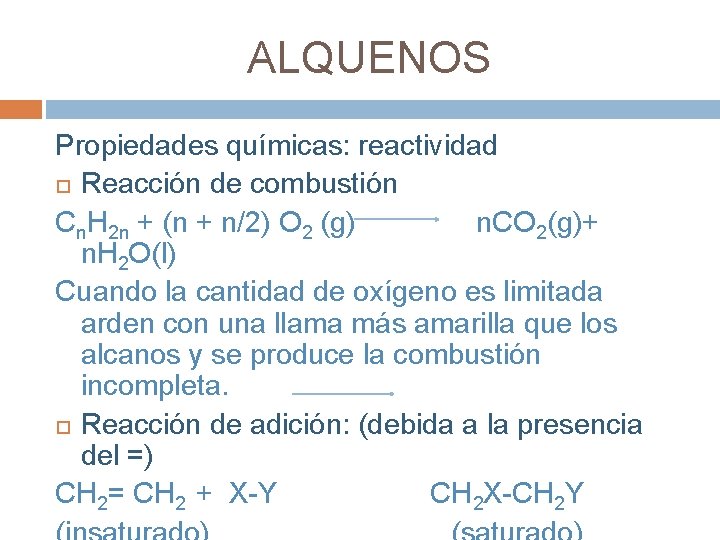
ALQUENOS Propiedades químicas: reactividad Reacción de combustión Cn. H 2 n + (n + n/2) O 2 (g) n. CO 2(g)+ n. H 2 O(l) Cuando la cantidad de oxígeno es limitada arden con una llama más amarilla que los alcanos y se produce la combustión incompleta. Reacción de adición: (debida a la presencia del =) CH 2= CH 2 + X-Y CH 2 X-CH 2 Y
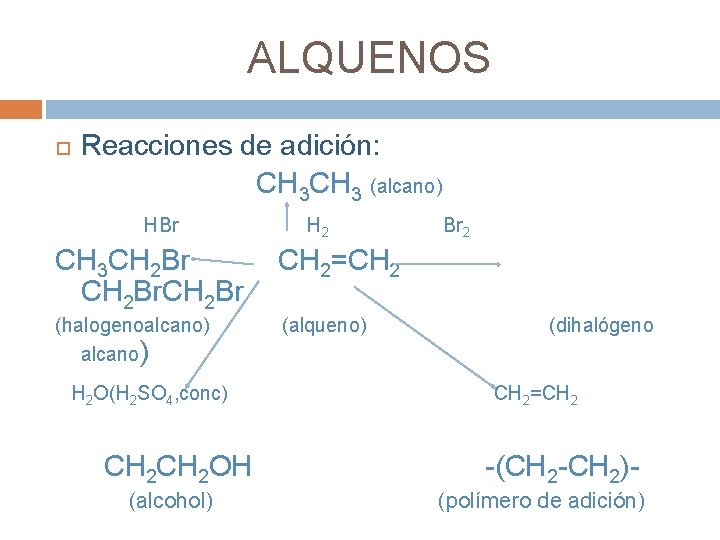
ALQUENOS Reacciones de adición: CH 3 (alcano) HBr H 2 CH 3 CH 2 Br CH 2=CH 2 (halogenoalcano) (alqueno) H 2 O(H 2 SO 4, conc) CH 2 OH (alcohol) Br 2 (dihalógeno CH 2=CH 2 -(CH 2 -CH 2)(polímero de adición)

ALCOHOLES Propiedades físicas Los de baja mas molecular son líquidos y emanan un olor característico. Al aumentar la masa molecular aumentan los puntos de fusión y ebullición y pueden llegar a ser sólidos. Son polares y, por tanto, solubles en agua. A medida que aumenta el tamaño de la molécula disminuye su polaridad.

ALCOHOLES Propiedades químicas: reactividad Reacción de combustión C 2 H 5 OH(l) + 3 O 2 (g) = 2 CO 2 (g)+ 3 H 2 O (l) ∆H 0= -1371 k. Jmol-1 Los alcoholes pueden usarse como combustibles, pueden utilizarse como sustitutos de la gasolina o el gasóleo o mezclados con ellos (no producen mucha energía)

ALCOHOLES Reacción de oxidación Oxidación del etanol H+/Cr 2 O 72 - CH 3 CH 2 OH CH 3 CHO CH 3 COOH etanol etanal ácido etanoico Oxidación de alcoholes primarios, secundarios y terciarios: Primarios: H+/Cr 2 O 72 - RCH 2 OH Secundarios: RCHO RCOOH H+/Cr 2 O 72 - RCHOHR’ RCOR’ (cetonas) Terciarios: No dan esta reacción, se produciría una ruptura de la cadena
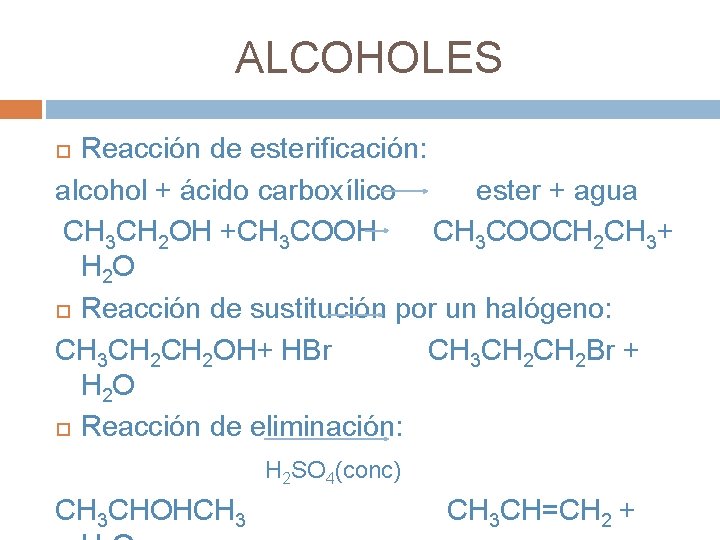
ALCOHOLES Reacción de esterificación: alcohol + ácido carboxílico ester + agua CH 3 CH 2 OH +CH 3 COOH CH 3 COOCH 2 CH 3+ H 2 O Reacción de sustitución por un halógeno: CH 3 CH 2 OH+ HBr CH 3 CH 2 Br + H 2 O Reacción de eliminación: H 2 SO 4(conc) CH 3 CHOHCH 3 CH=CH 2 +

HALOGENUROS DE ALQUILO Propiedades físicas Tienen puntos de ebullición más altos que los alcanos correspondientes debido a su mayor peso molecular. Para un mismo R el punto de ebullición aumenta con el peso atómico del halógeno. A pesar de sus polaridades son insolubles en agua.

HALOGENUROS DE ALQUILO Propiedades químicas: reactividad Sustitución nucleófila: (excepto los fluoruros de alquilo debido a la fortaleza del enlace C-F) R: X + : Z(reactivo nucleófilo) R: Z + : X-(grupo saliente) Reaccionan con un gran número de reactivos nucleófilos: tanto iones negativos como bases neutras con pares electrónicos no compartidos (NH 3; H 2 O)
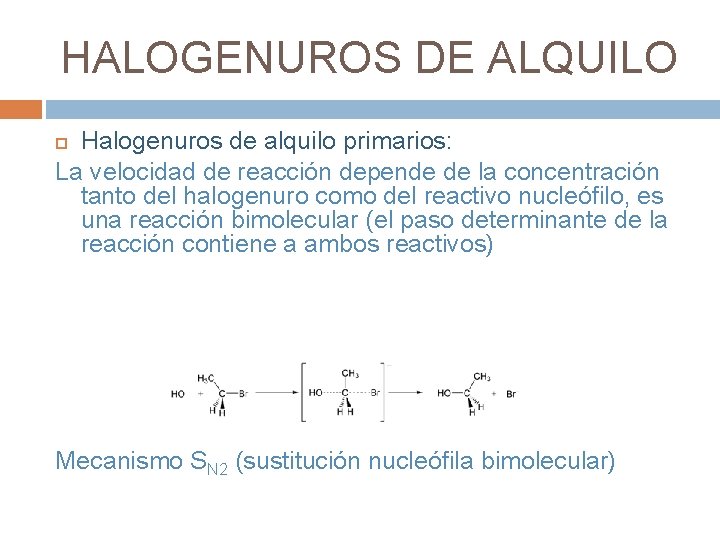
HALOGENUROS DE ALQUILO Halogenuros de alquilo primarios: La velocidad de reacción depende de la concentración tanto del halogenuro como del reactivo nucleófilo, es una reacción bimolecular (el paso determinante de la reacción contiene a ambos reactivos) Mecanismo SN 2 (sustitución nucleófila bimolecular)

HALOGENUROS DE ALQUILO Halogenuros de alquilo terciarios La velocidad de reacción depende sólo de la concentración del halogenuro y no del reactivo nucleófilo, es decir, es una reacción unimolecular. El mecanismo propuesto es el siguiente: lento (CH 3)3 -C-Br reac (CH 3)3 -C+ + Br- paso determinante de la v de la rápido (CH 3)3 -C+ + OH(CH 3)3 -C-OH Mecanismo SN 1 (sustitución nucleófila unimolecular)

HALOGENUROS DE ALQUILO SN 2 frente a SN 1 Los halogenuros de alquilo terciarios no reaccionan mediante SN 2 debido a impedimentos estéricos. En el estado de transición propio del mecanismo SN 2 se ven envueltos 5 grupos alrededor del átomo central, que en el caso del halogenuro terciario son relativamente voluminosos. R R [HO…. . C……Br][HO…. . C…. Br]H H R’ R” halogenuro primario halogenuro terciario

HALOGENUROS DE ALQUILO Los halogenuros de alquilo primarios no reaccionan mediante SN 1 debido a que la estabilidad del carbocatión formado en la etapa determinante de la velocidad de reacción decrece en el siguiente orden: primario<secundario<terciario Los grupos R ejercen un efecto inductivo positivo, esto quiere decir que la carga positiva del carbocatión puede dispersarse entre más átomos aumentando la estabilidad del carbocatión: I I G C+ G< C+ I I G suelta electrones G atrae electrones dispersa la carga intensifica la carga estabiliza el ión desestabiliza el ión “efecto inductivo”: depende de la tendencia intrínseca de un sustituyente de atraer electrones.

GRUPOS FUNCIONALES (BI NM) Alcoholes R-OH Halógenoalcanos R-X Aldehidos R-CHO Cetonas R-CO-R’ Ácidos carboxílicos R-COO-R’ Esteres R-COO-R’ Aminas R-NH 2 Compuestos aromáticos
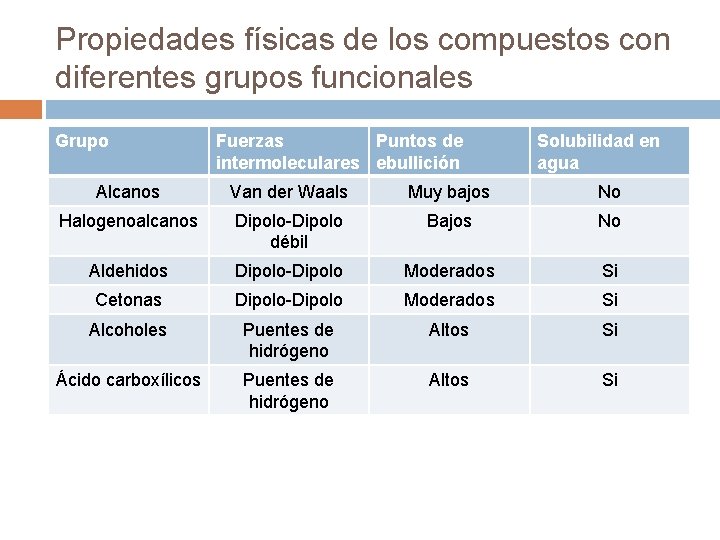
Propiedades físicas de los compuestos con diferentes grupos funcionales Grupo Fuerzas Puntos de intermoleculares ebullición Solubilidad en agua Alcanos Van der Waals Muy bajos No Halogenoalcanos Dipolo-Dipolo débil Bajos No Aldehidos Dipolo-Dipolo Moderados Si Cetonas Dipolo-Dipolo Moderados Si Alcoholes Puentes de hidrógeno Altos Si Ácido carboxílicos Puentes de hidrógeno Altos Si

POLÍMEROS Los polímeros, a pesar de su gran tamaño, suelen ser muy simples químicamente, ya que están formados por la repetición de moléculas sencillas llamadas monómeros.

Clasificación de los polímeros § § Atendiendo a su cadena carbonada: Lineales: cada monómero, excepto las unidades terminales, forma un enlace en cada extremo. Ramificados: algún monómero puede unirse por tres o más puntos a otros monómeros. Según su composición: § Homopolímeros: un solo tipo de monómero (polipropileno, polietileno, PVC). § Copolímeros: por unión de dos o más clases de monómeros (dacrón, resinas de fenolformaldehido).

Clasificación de los polímeros § § Según su respuesta al calor: Termoplásticos: se funden o ablandan por calentamiento, pero recuperan sus propiedades al enfriarse, pudiendo moldearse de nuevo (poliamidas, sedas artificiales, celofán) Termoestables: no pueden moldearse de nuevo por la acción del calor (baquelita, ebonita) Según su importancia industrial: § Polímeros etilénicos: polietileno, PVC, teflón § Cauchos sintéticos o elastómeros § Poliamidas y poliésteres: componentes de muchas fibras sintéticas § Poliuretanos § Siliconas


Polímeros etilénicos

Cauchos sintéticos

Siliconas

Propiedades físicas de los polímeros q q q § § Las propiedades de los polímeros dependen tanto de las cualidades del monómero o monómeros que lo forman como de las características de su estructura interna, debidas a las fuerzas intermoleculares. Los polímeros suelen presentar propiedades físicas bastante diferentes a las de los monómeros que los constituyen. Entre las propiedades físicas caben destacar: Su baja reactividad, dada la complejidad de las moléculas de los polímeros su estabilidad es muy alta. Poseen bajas densidades (entre 900 y 1300 kg m-3 ), no obstante mediante adición de gas en el proceso de formación se puede disminuir aún más la densidad. En general son elásticos y con buena resistencia mecánica Poseen baja conductividad, tanto térmica como eléctrica. Aunque hay excepciones.

Proceso de polimerización § Reacción de polimerización: combinación química de un cierto número de moléculas simples (monómeros) para formar una sola molécula de gran tamaño (polímero). Estas reacciones siguen básicamente dos mecanismos: Reacciones de adición: son reacciones que transcurren a través de radicales libres que se unen al doble enlace de la molécula de monómero. Son reacciones en cadena. n (CH 2=CH 2) → -(CH 2 - CH 2)-n La cadena crece de forma lineal o ramificada hasta que la reacción finaliza con el choque entre dos radicales libres que dan origen a formas moleculares: 2 R- CH 2∙ → R- CH 2 - CH 3 + R- CH= CH 2 Estas reacciones son muy rápidas, pudiéndose adicionar más de 1000 monómeros por segundo. Si todo el monómero se consume la masa del polímero equivaldría a la masa de monómero utilizado. Pueden formarse isómeros irregulares pues la adición de los monómeros es aleatoria, en estos casos se obtienen polímeros amorfos, blandos y de resistencia relativamente baja. Para conseguir polímeros estereorregulares se utilizan estereocatalizadores (catalizadores de Ziegler-Nata)

Proceso de polimerización Reacciones de condensación: se producen por reacción entre dos monómeros diferentes, cada uno con grupos funcionales en los extremos de la molécula. La unión entre monómeros supone la eliminación de una molécula pequeña. Formación de nailon 66: HOOC-(CH 2)4 -COOH + NH 2 -(CH 2)6 -NH 2 → HOOC-(CH 2)4 -CO- NH-(CH 2)6 -NH 2 + H 2 O ∙∙-CH 2 -NH-[CO-CH 2 -CH 2 -CO-NH-CH 2 -CH 2 -NH]-CO-CH 2 -∙∙ Son comunes las reacciones entre dialcoholes, diaminas, ácidos dicarboxílicos… para obtener poliamidas, poliésteres, etc, que son la base de la mayoría de fibras sintéticas (nailon, tergal, Dracón…) De manera similar se forman otros compuestos muy utilizados como poliuretanos, baquelita, etc.

Polímeros de interés industrial § - - § Polímeros etilénicos: todos ellos se obtienen por adición. Los más importantes son: Polietileno o polieteno, puede obtenerse de dos formas distintas: Por síntesis radicálica: se obtiene un polietileno de baja densidad con estructura poco cristalina, muy flexible y manejable. Se utiliza para bolsas de plástico y como material de empaquetado. En presencia de catalizadores específicos: se obtiene un polietileno de alta densidad con una estructura más lineal y mayor carácter cristalino. Se utiliza en la fabricación de objetos semirrígidos (cubos, botellas, juguetes…) Cloruro de polivinilo (PVC), es un polímero termoplástico no cristalino. Como homopolímero es frágil e inestable, pero cuando se copolimeriza con otros monómeros se obtienen polímeros de características muy variadas. El PVC, junto con el polietileno, es el plástico más importante de la industria química.

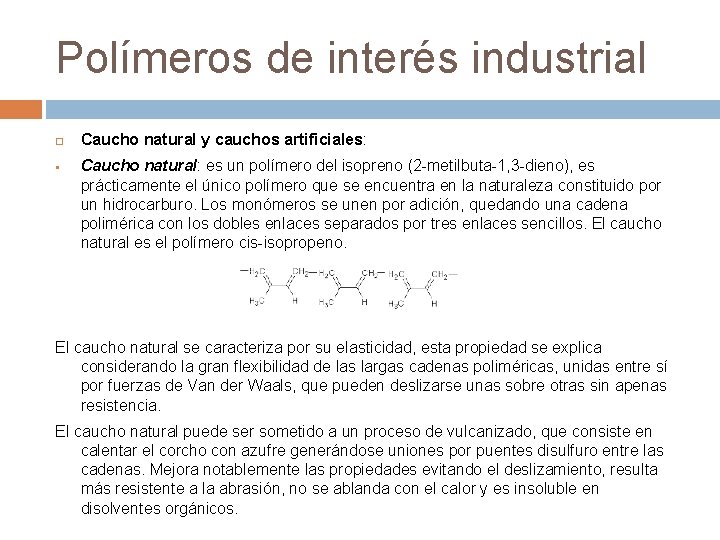
Polímeros de interés industrial § Caucho natural y cauchos artificiales: Caucho natural: es un polímero del isopreno (2 -metilbuta-1, 3 -dieno), es prácticamente el único polímero que se encuentra en la naturaleza constituido por un hidrocarburo. Los monómeros se unen por adición, quedando una cadena polimérica con los dobles enlaces separados por tres enlaces sencillos. El caucho natural es el polímero cis-isopropeno. El caucho natural se caracteriza por su elasticidad, esta propiedad se explica considerando la gran flexibilidad de las largas cadenas poliméricas, unidas entre sí por fuerzas de Van der Waals, que pueden deslizarse unas sobre otras sin apenas resistencia. El caucho natural puede ser sometido a un proceso de vulcanizado, que consiste en calentar el corcho con azufre generándose uniones por puentes disulfuro entre las cadenas. Mejora notablemente las propiedades evitando el deslizamiento, resulta más resistente a la abrasión, no se ablanda con el calor y es insoluble en disolventes orgánicos.

Polímeros de interés industrial § § Caucho sintético: se empezó a fabricar en la Primera Guerra Mundial. Existen diferentes tipos que reciben el nombre genérico de elastómeros. Los más utilizados son el buna-S, el buna-N y el caucho-butilo Neoprenos: Se desarrollaron a partir de 1931, tienen como monómero el cloropreno (2 -clorobuta-1, 3 -dieno), utilizan óxido de cinc para los entrecruzamientos.

Polímeros de interés industrial § § Las fibras textiles: Se dividen en dos grandes grupos poliamidas y poliésteres, en los dos casos el polímero se obtiene por reacciones de condensación. Las macromoléculas deben ser larga e interaccionar mediante fuerzas intermoleculares, lo que les confiere una gran resistencia mecánica, estabilidad frente al calor y los agentes químicos y gran facilidad para recibir tintes y cambiar de color. Poliésteres: poseen diferentes estructuras según los monómeros que los forman. El más utilizado es el Terylene o Dracón (ácido benceno-1, 4 dicarbocílico y etano-1, 2 -diol): Poliamidas: también conocidas como náilones, poseen gran variedad de estructuras. A menudo se combinan con fibras naturales para mejorar las propiedades de estas.

Polímeros de interés industrial § Poliuretanos: El uretano es un grupo funcional que es al mismo tiempo un éster y una amida. Se obtiene por reacción entre un isocianato y un alcohol. R-N=C=O + OH-R’ → R-NH-COO-R’ Los poliuretanos se sintetizan por reacción de condensación entre diisocianatos y dialcoholes, en esta reacción no hay pérdida de agua. O=C=N-(CH 2)3 -N=C=O + OH-CH 2 -OH …-CO-NH-(CH 2)3 -NH-CO-O-CH 2 -O-CO-NH-(CH 2)3 -NH-CO-… Su uso más habitual es para espumas de poliuretano (colchones, cojines, revestimentos. . ) § Baquelita: Uno de los primeros polímeros sintetizados. Se obtienen a partir de fenol y metanal. La reacción de polimerización dependiendo de las condiciones en que se realice da lugar a polímeros lineales o ramificados.

Polímeros de interés industrial § Siliconas: Tienen la particularidad de poseer naturaleza orgánica e inorgánica a la vez. Contienen silicio componente inorgánico y radicales alquilo o arilo como orgánico. Son inertes, inmiscibles en agua y con elevadas temperaturas de ignición. Se obtienen por condensación entre derivados hidroxilados del silicio.

Macromoléculas naturales Las macromoléculas naturales constituyen un alto porcentaje de la materia viva. Son el fundamento de las funciones vitales de los seres vivos. Los enlaces más fuertes que intervienen en estas biomoléculas son enlaces covalentes, pero su actividad biológica está más condicionada por las fuerzas intermoleculares que condicionan sus estructuras tridimensionales e intervienen en las reacciones específicas entre ellas.

Macromoléculas naturales § § § Polisacáridos o hidratos de carbono: formadas por moléculas sencillas denominadas monosacáridos, polihidroxialdehídos (aldosas) y polihidroxicetonas (cetosas), que contienen de tres a nueve átomos de C. Los monosacáridos son sólidos solubles en agua. La unión de dos monosacáridos da lugar a un disacárido, está reacción es reversible por lo que el disacárido puede hidrolizarse dando los azúcares simples. Los polisacáridos se obtienen por condensación sucesiva de monosacáridos. También pueden hidrolizarse. Los polisacáridos más importantes son: Almidón: reserva alimenticia que se almacena en raíces, frutas y semillas. Celulosa: constituyente básico de los tejidos de sostén de la célula vegetal. Glucógeno: es el encargado de almacenar los glúcidos en músculos e hígado en los animales.
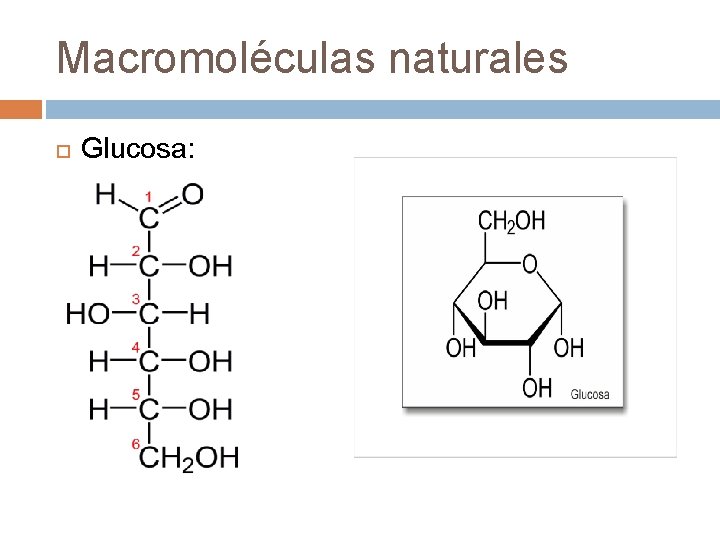
Macromoléculas naturales Glucosa:
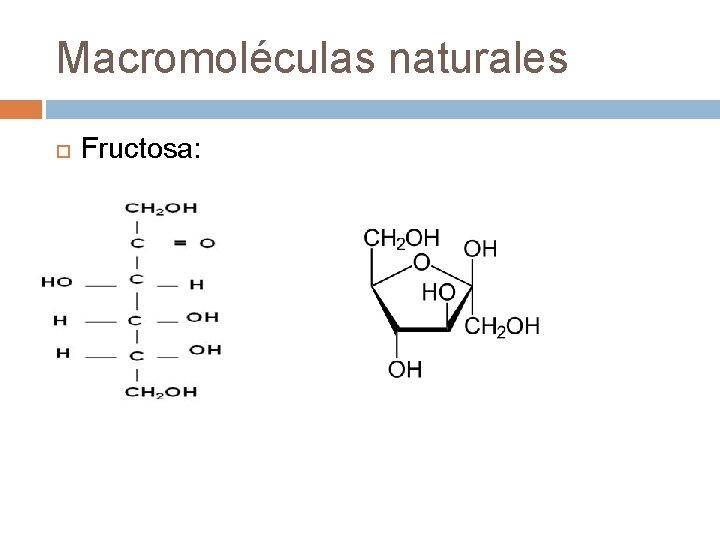
Macromoléculas naturales Fructosa:

Macromoléculas naturales § § Lípidos: son un conjunto de sustancias orgánicas que se caracterizan por ser prácticamente insolubles en agua. Junto con los hidratos de carbono son la principal fuente de energía para los seres vivos. Algunos lípidos no son polímeros sino moléculas no muy complejas con masas moleculares relativamente pequeñas. Los lípidos que presentan estructuras poliméricas deben estas a la presencia del isopreno. La unión por condensación de varias unidades de isopreno (2, 3, 4, 6…) da lugar a unas sustancias denominadas terpenos. Los carotenos son pigmentos vegetales formados por largas cadenas isoprénicas con numerosos dobles enlaces conjugados que les confieren colores característicos. Del β-caroteno se obtiene la vitamina A o retinol.
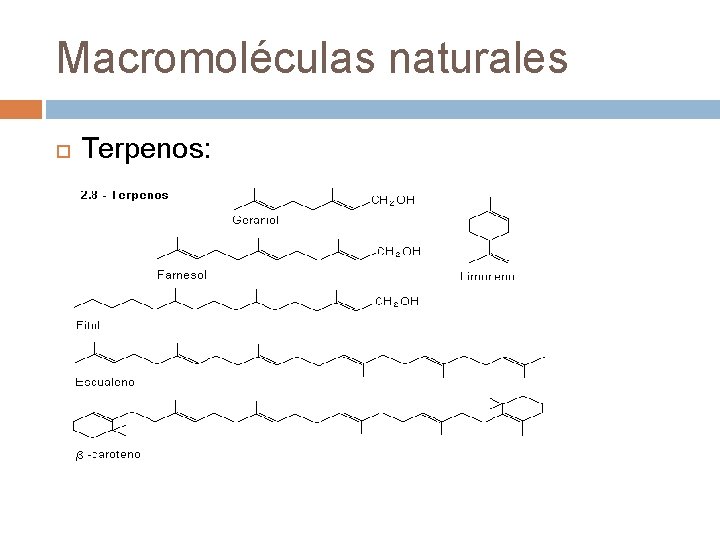
Macromoléculas naturales Terpenos:

Macromoléculas naturales § § Proteínas: moléculas fundamentales en la organización celular por la gran variedad de funciones que desempeñan. Son biopolímeros formados por unidades de aminoácidos. Aminoácidos: son sustancias que contienen como mínimo un grupo carboxilo y un grupo amino. El carácter polar de estos grupos facilita su disolución en agua y el establecimiento de fuerzas intermoleculares muy intensas. Todos ellos son sólidos a temperatura ambiente. Los aminoácidos se unen entre sí a través de un enlace peptídico entre el grupo carboxilo de un aminoácido y el grupo amino de otro perdiéndose una molécula de agua.

Macromoléculas naturales § § ü ü § El dipéptido formado puede seguir uniéndose a otros aminoácidos dando lugar a un polipéptido o a una proteína. Proteínas: se denominan así las poliamidas de los alfa-aminoácidos. Pueden tener desde cien hasta 10000 aminoácidos. Se clasifican en: Proteínas simples: formadas por una sucesión de aminoácidos. Proteínas conjugadas o heteroproteínas: contienen además de aminoácidos otros grupos de naturaleza no peptídica llamados grupos prostéticos. Desnaturalización de proteínas: consiste en la pérdida o modificación de la organización tridimensional de la proteína, puede ocasionar la pérdida de su actividad biológica. El proceso se origina por exceso de temperatura, variaciones bruscas de p. H, por la presión osmótica del medio o por la utilización de agentes desnaturalizantes.
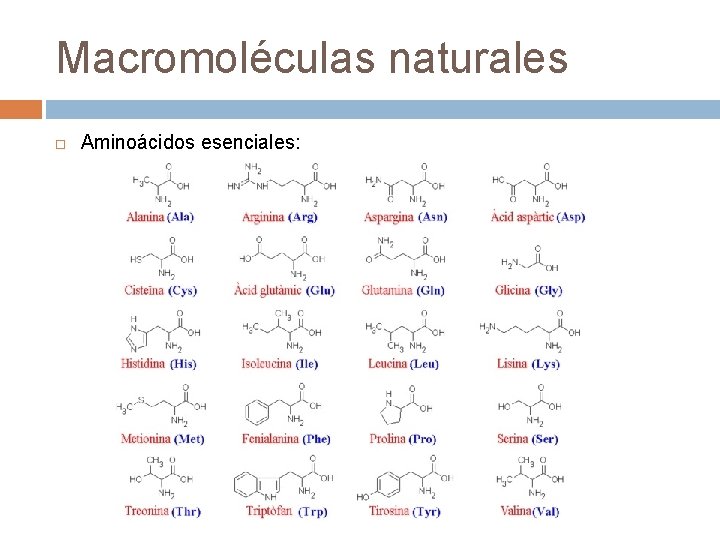
Macromoléculas naturales Aminoácidos esenciales:

Macromoléculas naturales Ácidos nucleicos: son las macromoléculas naturales encargadas de la reproducción de los seres vivos. En ellos se almacena la información genética. q Un ácido nucleico consta de: § Una molécula de ácido fósforico § Una pentosa (ribosa o desoxirribosa) § § Una base nitrogenada: estas pueden ser púricas (adenina y guanina) o pirimídicas (citosina, timina y uracilo) La unión de una base púrica o pirimídinica al C-1 de la pentosa forma un nucleósido. La adición de una molécula de ácido fosfórico en el C-3 de la pentosa da un nucleótido. La unión de nucleótidos siempre tiene lugar a través del ácido fosfórico que se enlaza al C-5 de la pentosa del nucleótido siguiente.
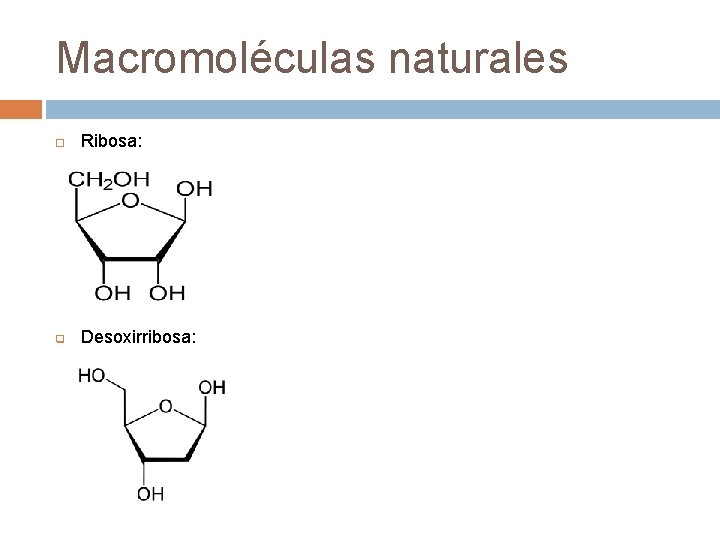
Macromoléculas naturales Ribosa: q Desoxirribosa:
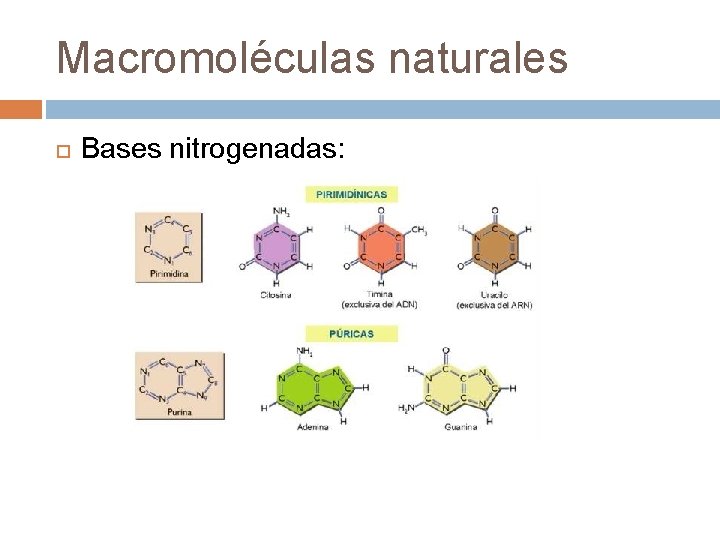
Macromoléculas naturales Bases nitrogenadas:

Macromoléculas naturales § § § Ácidos nucleicos: son las cadenas formadas por eslabones alterno pentosa-ácido fosfórico y, saliendo de la cadena, perpendicularmente, las bases púricas y pirimidínicas. Si la pentosa es la ribosa tenemos el ácido ribonucleico (RNA o ARN) Si la pentosa es la desoxirribosa tenemos el ácido desoxirribonucleico (DNA o ADN) Las moléculas de ADN están formadas por dos de estas cadenas enrolladas en forma de doble hélice. En el interior se encuentran las bases que se acoplan por pares mediante puentes de hidrógeno (A-T y C-G) La secuenciación de las bases nitrogenadas en la cadena no es casual, constituye el código genético. Estructuralmente el ARN se diferencia del ADN en que su cadena es sencilla y utiliza el uracilo en lugar de timina.
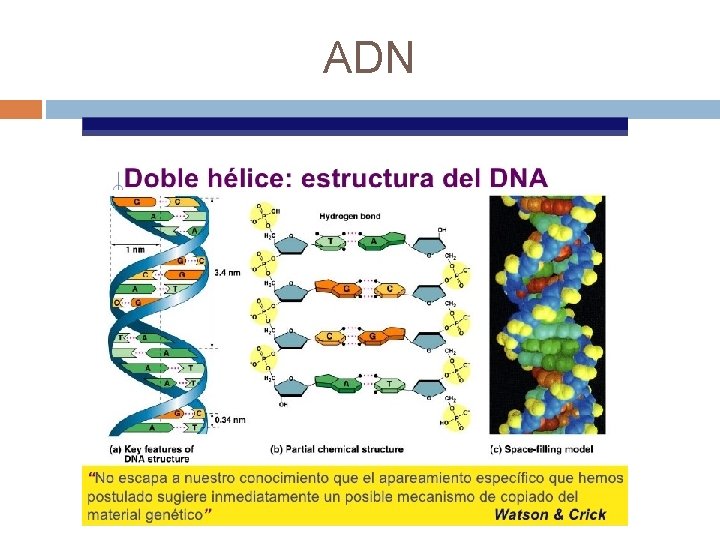
ADN
- Slides: 56