QUMICA ORGNICA Qumica 2 Bachillerato MAGC11 1 CARACTERSTICAS

QUÍMICA ORGÁNICA Química 2º Bachillerato MAGC-11 1

CARACTERÍSTICAS DEL CARBONO • Electronegatividad intermedia – Enlace covalente con metales como con no metales • Posibilidad de unirse a sí mismo formando cadenas. hibridación 2 2 s p p p • Tetravalencia: s p x y z 400 k. J/mol (enlaces muy fuertes, se desprenden 830 k. J/mol al formar 2 enlaces C–H) • Tamaño pequeño, por lo que es posible que los átomos se aproximen lo suficiente para formar enlaces “ ”, formando enlaces dobles y triples (esto no es posible en el Si). 2

La química del carbono o química orgánica, estudia todas aquellas sustancias en cuyas moléculas toma parte el carbono Los átomos de carbono, tienen mucha facilidad para unirse entre sí y formar cadenas muy variadas. Todos sus átomos forman siempre cuatro enlaces covalentes
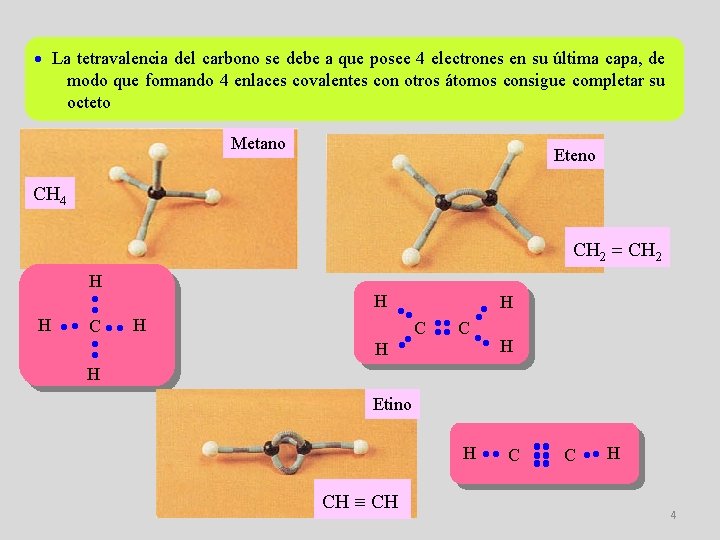
La tetravalencia del carbono se debe a que posee 4 electrones en su última capa, de modo que formando 4 enlaces covalentes con otros átomos consigue completar su octeto Metano Eteno CH 4 CH 2 = CH 2 H H H C C H H C H Etino H C CH C H 4

TIPOS DE ENLACE QUE USA EL CARBONO • • • Enlace simple: Los cuatro pares de electrones se comparten con cuatro átomos distintos. Ejemplo: CH 4, CH 3–CH 3 Enlace doble: Hay dos pares electrónicos compartidos con el mismo átomo. Ejemplo: H 2 C=CH 2, H 2 C=O Enlace triple: Hay tres pares electrónicos compartidos con el mismo átomo. Ejemplo: HC CH, CH 3–C N • El carbono puede hibridarse de tres maneras distintas: • Hibridación sp 3: – 4 orbitales sp 3 iguales que forman 4 enlaces simples de tipo “ ” (frontales). • Hibridación sp 2: – 3 orbitales sp 2 iguales que forman enlaces “ ” + 1 orbital “p” (sin hibridar) que formará un enlace “ ” (lateral) • Hibridación sp: – 2 orbitales sp iguales que forman enlaces “ ” + 2 orbitales “p” (sin hibridar) que formarán sendos enlaces “ ” 5

Hibridación sp 3 • • 4 orbitales sp 3 iguales que forman 4 enlaces simples de tipo “ ” (frontales). Los cuatro pares de electrones se comparten con cuatro átomos distintos. Geometría tetraédrica: ángulos C–H: 109’ 5 º y distancias C–H iguales. Ejemplo: CH 4, CH 3–CH 3 6

Hibridación sp 2 • 3 orbitales sp 2 iguales que forman enlaces “ ” + 1 orbital “p” (sin hibridar) que formará un enlace “ ” (lateral) • Forma un enlace doble, uno “ ” y otro “ ”, es decir, hay dos pares electrónicos compartidos con el mismo átomo. • Geometría triangular: ángulos C–H: 120 º y distancia C=C < C–C • Ejemplo: H 2 C=CH 2, H 2 C=O H H H C=C 120º H 7

Hibridación sp • • 2 orbitales sp iguales que forman enlaces “ ” + 2 orbitales “p” (sin hibridar) que formarán sendos enlaces “ ” Forma bien un enlace triple –un enlace “ ” y dos “ ”–, es decir, hay tres pares electrónicos compartidos con el mismo átomo, o bien dos enlaces dobles, si bien este caso es más raro. Geometría lineal: ángulos C–H: 180 º y distancia C C < C=C < C–C Ejemplo: HC CH, CH 3–C N Ejercicio A: Indica la hibridación que cabe esperar en cada uno de los átomos de carbono que participan en las siguientes moléculas : CH C–CH 2 –CHO; CH 3 –CH=CH–C N • sp sp 3 sp 2 sp 8
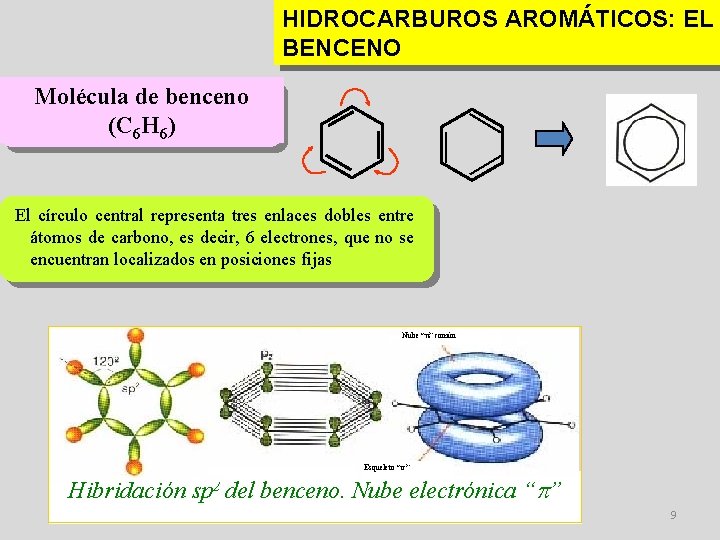
HIDROCARBUROS AROMÁTICOS: EL BENCENO Molécula de benceno (C 6 H 6) El círculo central representa tres enlaces dobles entre átomos de carbono, es decir, 6 electrones, que no se encuentran localizados en posiciones fijas Nube “ ” común Esqueleto “ ” Hibridación sp 2 del benceno. Nube electrónica “ ” 9

ISOMERÍA Dos compuestos son isómeros cuando, siendo diferentes, responden a la misma fórmula molecular Clasificación Se dividen en en dos grupos: isómeros estructurales y estereoisómeros a) Los isómeros constitucionales o estructurales se subdividen en: - Isómeros de cadena - Isómeros de posición - Isómeros de función a) Los estereoisómeros se subdividen en: - Enantiómeros - Isómeros geométricos o diastereoisómeros 10

LOS ISÓMEROS ESTRUCTURALES - Isómeros de cadena Son aquellos que difieren en la colocación de los átomos de carbono CH 3 - CH 2 - CH 3 y CH 3 - CH 3 - Ejemplo: CH 2 - Isómeros de posición Son aquellos que teniendo el mismo esqueleto carbonado, se distinguen por la posición que ocupa el grupo funcional Ejemplo: CH - OH y CH - CHOH- CH 3 2 2 2 3 - Isómeros de función Son aquellos que teniendo la misma fórmula molecular, poseen grupos funcionales diferentes Ejemplo: CH 3 - CH 2 - OH y CH 3 - O- CH 2 - CH 3 11
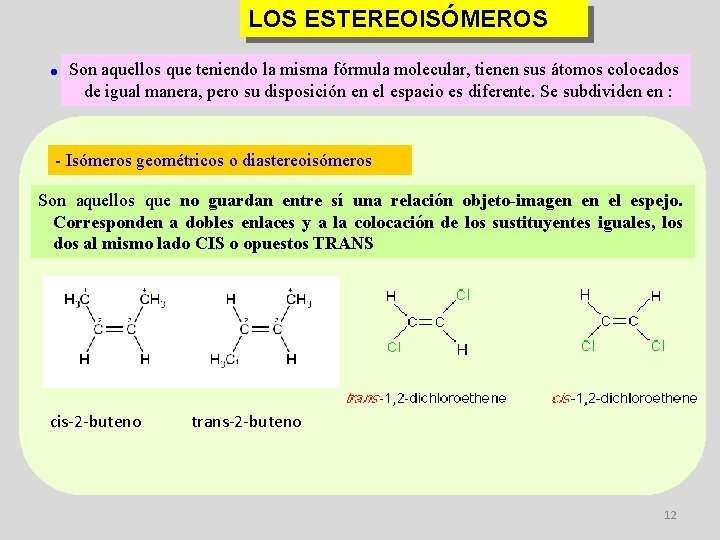
LOS ESTEREOISÓMEROS Son aquellos que teniendo la misma fórmula molecular, tienen sus átomos colocados de igual manera, pero su disposición en el espacio es diferente. Se subdividen en : - Isómeros geométricos o diastereoisómeros Son aquellos que no guardan entre sí una relación objeto-imagen en el espejo. Corresponden a dobles enlaces y a la colocación de los sustituyentes iguales, los dos al mismo lado CIS o opuestos TRANS cis-2 -buteno trans-2 -buteno 12
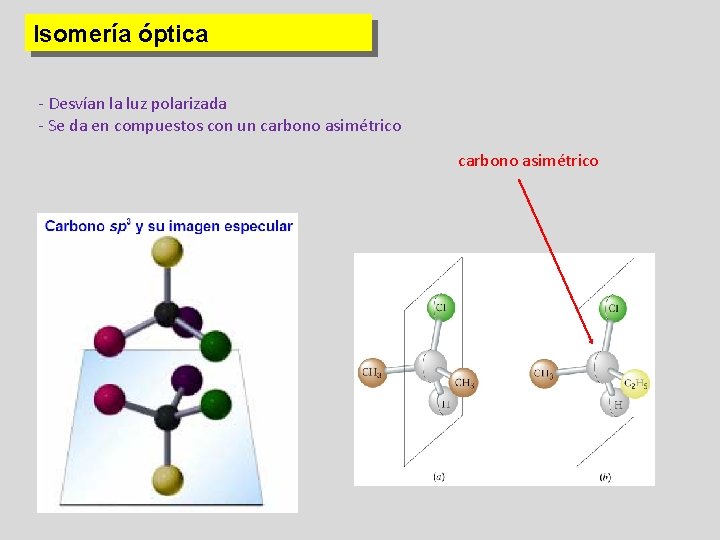
Isomería óptica - Desvían la luz polarizada - Se da en compuestos con un carbono asimétrico
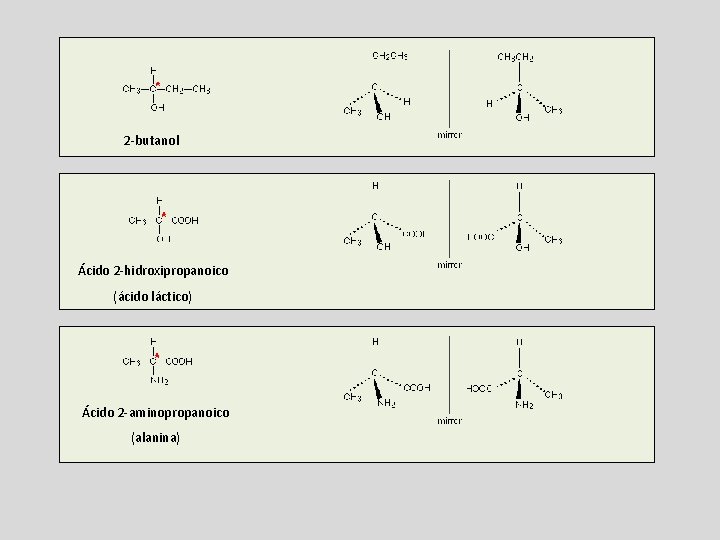
2 -butanol Ácido 2 -hidroxipropanoico (ácido láctico) Ácido 2 -aminopropanoico (alanina)
- Slides: 14