Introducci a la Qumica Orgnica Unitat 9 1






















![31 Compostos oxigenats. • OH ÀCIDS [Grup –C=O (carboxil)]: Àcid + Prefix (nº C) 31 Compostos oxigenats. • OH ÀCIDS [Grup –C=O (carboxil)]: Àcid + Prefix (nº C)](https://slidetodoc.com/presentation_image/1f3038f25ed83032eb7f411b8f5f12ed/image-30.jpg)


![34 Compostos oxigenats. • ALDEHIDS [Grup C=O (carbonil) en un carboni terminal]: Prefix (núm. 34 Compostos oxigenats. • ALDEHIDS [Grup C=O (carbonil) en un carboni terminal]: Prefix (núm.](https://slidetodoc.com/presentation_image/1f3038f25ed83032eb7f411b8f5f12ed/image-33.jpg)

![37 Compostos oxigenats. • ALCOHOLS: [Grup –OH (hidroxil)]: Nombre del C en el que 37 Compostos oxigenats. • ALCOHOLS: [Grup –OH (hidroxil)]: Nombre del C en el que](https://slidetodoc.com/presentation_image/1f3038f25ed83032eb7f411b8f5f12ed/image-36.jpg)


![40 Compostos nitrogenats • NRR’ AMIDES [Grup –C=O]: Prefi. X (nº C) + sufi. 40 Compostos nitrogenats • NRR’ AMIDES [Grup –C=O]: Prefi. X (nº C) + sufi.](https://slidetodoc.com/presentation_image/1f3038f25ed83032eb7f411b8f5f12ed/image-39.jpg)
![41 Compostos nitrogenats • NITRILS (o cianurs) [Grup –C N] Prefix (nº C) + 41 Compostos nitrogenats • NITRILS (o cianurs) [Grup –C N] Prefix (nº C) +](https://slidetodoc.com/presentation_image/1f3038f25ed83032eb7f411b8f5f12ed/image-40.jpg)







- Slides: 50

Introducció a la Química Orgànica Unitat 9 1

2 Berzelius (1807) Classifica la química en Inorgànica i Orgànica. Els va anomenar així perquè pensava que els compostos orgànics només eren produïts pels éssers vius. Tots els compost orgànics posseeixen en la seua composició àtoms de carboni. No obstant això, hi ha molts compost amb carboni en la seua composició que són típicament inorgànics, com ara el CO 2 o els carbonats.

3 COMPOSTOS INORGÀNICS Sintetitzats per els éssers vius Tenen "Força vital"

4 Friedrich Wölher (1828) • Primera Síntesi orgànica: calor NH 4 OCN (cianat d’amoni) NH 2 CONH 2 (urea)

5 August Kekulé (1861) • QUÍMICA ORGÁNICA: – La Química dels “Compostos del Carboni”.

6 Química orgànica en l'actualitat: • La Química dels “Compostos del Carboni”. • També tenen hidrogen. • S'exceptuen CO, CO 2, carbonats, bicarbonats, cianurs. . . • Poden tindre altres elements: O, N, S, P, halògens. . .

7 Actualidad: • Nombre de compostos : – Inorgànics: – Orgànics: uns 100. 000 uns 7. 000 (plàstics, insecticides, sabons, medicaments, gasolines, fibres tèxtils. . . )

8 Activitat: Donats els següents compostos, identifica quals d'ells són compostos orgànics: CH 3 -COOH; Ca. CO 3; KCN; CH 3 -CN; NH 4 Cl; CH 3 -NH-CH 2 -CH 3; Cl-CH 2 -CH 3 • CH 3 -COOH; CH 3 -CN; CH 3 -NH-CH 2 -CH 3; Cl-CH 2 -CH 3

9 Propietats del Carboni Estructura dels compostos orgànics • • Electronegativitat intermèdia el que permet formar enllaç covalent tant amb metalls com amb no metalls. Possibilitat d'unir-se a si mateix formant cadenes. Grandària xicoteta el que li possibilita formar enllaços dobles i triples. Tetravalència: s 2 p 2 → s px py pz aportant tan sols 400 k. J/mol hibridació

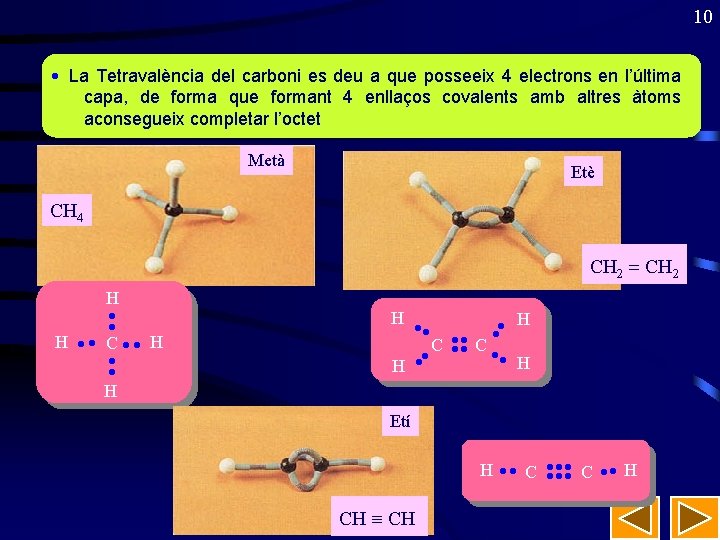
10 La Tetravalència del carboni es deu a que posseeix 4 electrons en l’última capa, de forma que formant 4 enllaços covalents amb altres àtoms aconsegueix completar l’octet Metà Etè CH 4 CH 2 = CH 2 H H H C C H H C H Etí H C C H CH

11 TIPUS D'ENLLAÇ • Enllaç simple: • Els quatre parells d'electrons es comparteixen amb quatre àtoms distints. • Exemple: CH 4, CH 3–CH 3 • Enllaç doble: • Hi ha dos parells electrònics compartits amb el mateix àtom. • Exemple: H 2 C=CH 2, H 2 C=O • Enllaç triple: • Hi ha tres parells electrònics compartits amb el mateix àtom. • Exemple: HC≡CH, CH 3 –C≡N

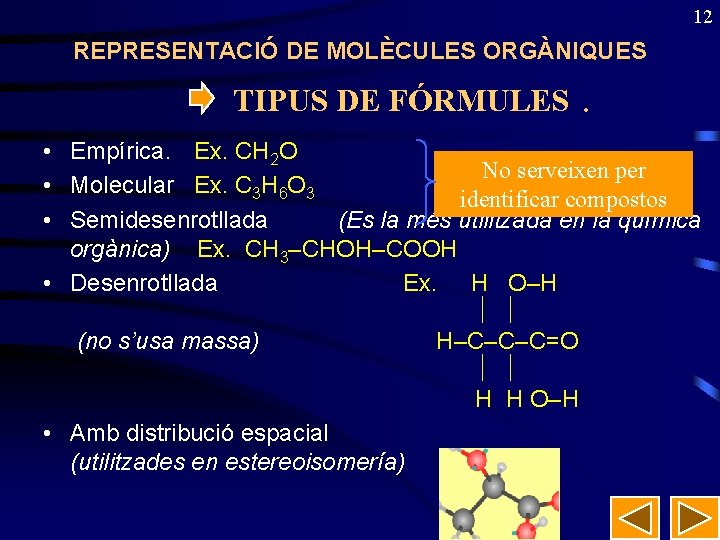
REPRESENTACIÓ DE MOLÈCULES ORGÀNIQUES 12 TIPUS DE FÓRMULES. • Empírica. Ex. CH 2 O No serveixen per • Molecular Ex. C 3 H 6 O 3 identificar compostos • Semidesenrotllada (Es la més utilitzada en la química orgànica) Ex. CH 3–CHOH–COOH • Desenrotllada Ex. H O–H (no s’usa massa) H–C–C–C=O H H O–H • Amb distribució espacial (utilitzades en estereoisomería)

Exemple: Sabem que un compost orgànic té de fórmula empírica C 2 H 5 N i la seua massa molecular aproximada és de 130 g/mol. Escriu qual serà la seua fórmula molecular. • 12 x 2 + 5 x 1 + 14 = 43 130/43 = 3 (aprox) (Buscar nombre enter) La fórmula molecular serà: C 6 H 15 N 3 13

14 Exercici A: Un compost orgànic va donar els següents percentatges en la seua composició: 71, 7 % de clor i 4, 1 % d'hidrogen. A més, 1 litre del dit compost en estat gasós mesurat a 745 mm Hg i 110 ºC té una massa de 3, 12 g. Trobar la seua fórmula empírica i la seua fórmula molecular. 71, 7 g 4, 1 g ———— = 2’ 02 mol Cl; ———— = 4, 1 mol H 35, 5 g/mol 1 g/mol 24, 2 g ———— = 2, 02 mol C 12 g/mol • Dividint tots pel menor (2, 02) obtenim la fórmula empírica: CH 2 Cl • m ·R ·T 3, 12 g · 0’ 082 atm ·L · 383 K 760 mm Hg M= ———— =—————— ·————— = 100 g/mol p · V mol ·K · 745 mm Hg · 1 L 1 atm • La fórmula molecular serà: C 2 H 4 Cl 2

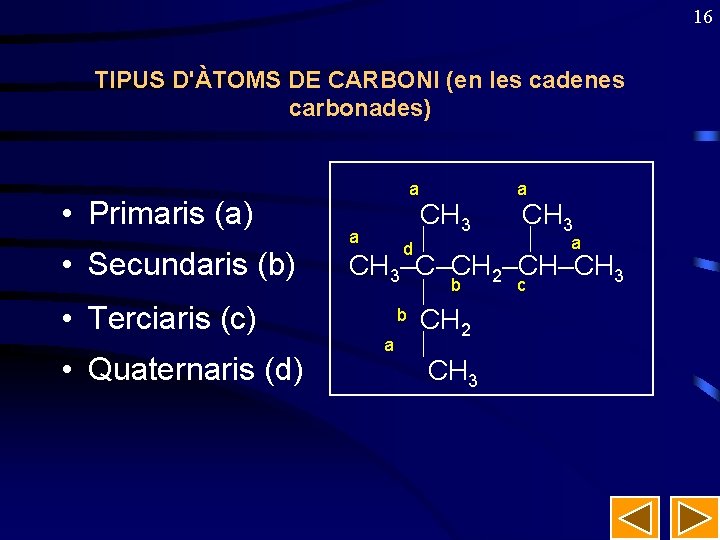
16 TIPUS D'ÀTOMS DE CARBONI (en les cadenes carbonades) • Primaris (a) • Secundaris (b) • Terciaris (c) • Quaternaris (d) a a CH 3 a a d CH 3–C–CH 2–CH–CH 3 c b b CH 2 a CH 3

Exercici B: Indica el tipus de carboni, primari (a), secundari (b), terciari (c) o quaternari (d) que hi ha en la següent cadena de carbonis: • a CH 3 b b CH 3–C – CH–CH 2 –CH–CH 3 b CH 2 CH 3 CH 3 3 a a CH 3 a d c a 17

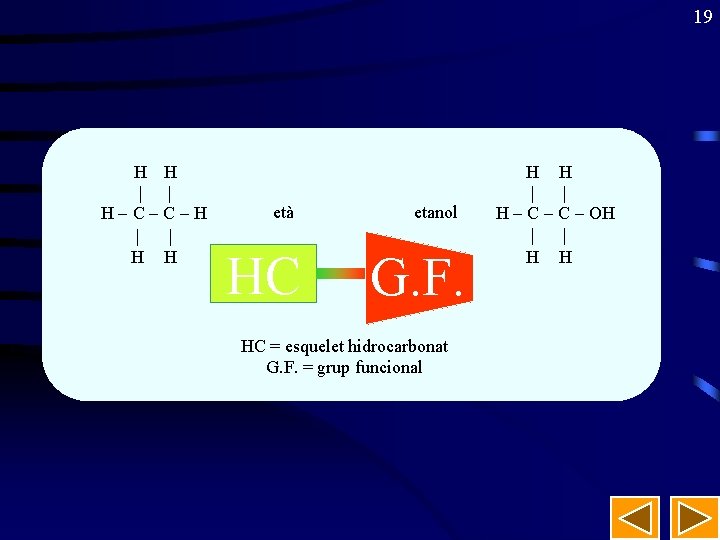
18 GRUPS FUNCIONALS. SÈRIES HOMÒLOGUES. • Grup funcional: “És un àtom o grup d'àtoms units de manera característica i que determinen, preferentment, les propietats del compost que estan presents”. • Sèrie homòloga: “És un grup de compostos en els que l'única diferència formal entre els seus membres es troba en el nombre de grups metilé, -CH 2 -, que conté”

19 H H | | H - C - H | | H H età HC etanol G. F. HC = esquelet hidrocarbonat G. F. = grup funcional H H | | H - C - OH | | H H

20 PRINCIPALS GRUPS FUNCIONALS orde de prioritat) • • Àcid carboxílic Éster Amida Nitril Aldehíd Cetona Alcohol • Fenol R–COOH R–COOR’ R–CONR’R’’ R–C N R–CH=O R–CO–R’ R–OH OH (per

21 PRINCIPALS GRUPS FUNCIONALS (per orde de prioritat) • Amina • • • (primària) (secundària) (terciària) Èter Doble enllaç Triple enllaç Nitro Halogen Radical R–NH 2 R–NHR’ R–NR’R’’ R–O–R’ R–CH=CH–R’ R– C C–R’ R–NO 2 R–X R–

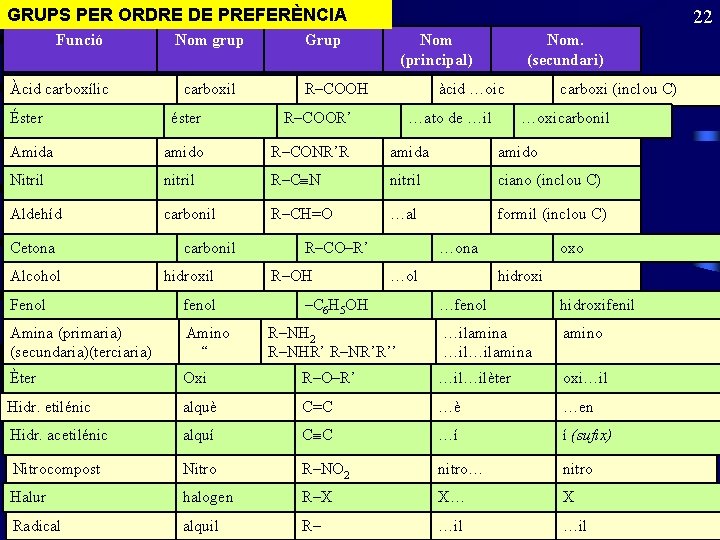
GRUPS PER ORDRE DE PREFERÈNCIA Funció Àcid carboxílic Éster Nom grup carboxil 22 Grup Nom (principal) R–COOH Nom. (secundari) àcid …oic éster R–COOR’ Amida amido R–CONR’R amida amido Nitril nitril R–C N nitril ciano (inclou C) Aldehíd carbonil R–CH=O …al formil (inclou C) Cetona Alcohol carbonil hidroxil …ato de …il carboxi (inclou C) R–CO–R’ R–OH …oxicarbonil …ona …ol –C 6 H 5 OH oxo hidroxi Fenol fenol Amina (primaria) (secundaria)(terciaria) Amino “ Èter Oxi R–O–R’ …il…ilèter oxi…il Hidr. etilénic alquè C=C …è …en Hidr. acetilénic alquí C C …í í (sufix) Nitrocompost Nitro R–NO 2 nitro… nitro Halur halogen R–X X… X Radical alquil R– …il R–NH 2 R–NHR’ R–NR’R’’ …fenol hidroxifenil …ilamina …il…ilamina amino

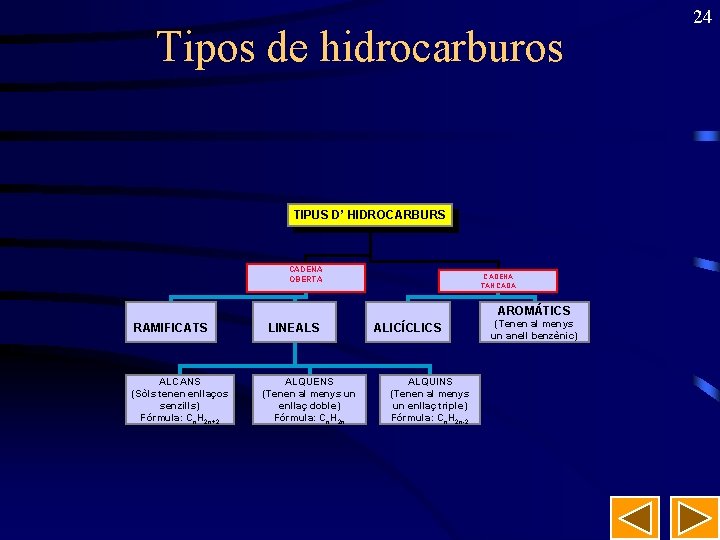
23 HIDROCARBURS • Són compostos orgànics que només contenen àtoms de carboni i d'hidrogen. • Tenen fórmules molt variades: Ca. Hb. • Els àtoms de carboni s’uneixen entre si per a formar cadenes carbonades.

Tipos de hidrocarburos TIPUS D’ HIDROCARBURS CADENA OBERTA CADENA TANCADA AROMÁTICS RAMIFICATS ALCANS (Sòls tenen enllaços senzills) Fórmula: Cn. H 2 n+2 LINEALS ALQUENS (Tenen al menys un enllaç doble) Fórmula: Cn. H 2 n ALICÍCLICS ALQUINS (Tenen al menys un enllaç triple) Fórmula: Cn. H 2 n-2 (Tenen al menys un anell benzènic) 24

25 Prefixos segons nombre d'àtoms de C. • • • Nº àtoms C Prefix 1 met 2 et 3 prop 4 but 5 pent • • • Nº àtoms C Prefix 6 hex 7 hept 8 oct 9 non 10 dec

26 Hidrocarburs de cadena oberta. • • • ALCANS: Prefix (núm. C) + sufix “à” Exemple: CH 3–CH 2–CH 3: propà ALQUENS: Prefix (núm. C) + sufix “è” indicant la posició del doble enllaç si este pot col·locar-se en uns quants llocs. Exemple: CH 3–CH =CH–CH 3: 2 butè ALQUINS: Prefix (núm. C) + sufix “í” indicant la posició del triple enllaç si este pot col·locarse en uns quants llocs. Exemple: CH 3–CH 2–C≡CH: 1 butí

27 Hidrocarburs ramificats. • La cadena principal és la més llarga que conté el grup funcional (el doble o triple enllaç). Esta regla també serà vàlida per a qualsevol compost orgànic encara que no siga hidrocarbur. • Es numera per l'extrem més pròxim al grup funcional (doble o triple enllaç) i si no haguera pel que la ramificació tinga el nombre més baix. • La ramificació s'anomena acabant en “il”. • Exemple: : CH 3–CH–CH=CH 2 | CH 2–CH 3 • 3 -metil-1 -pentè.

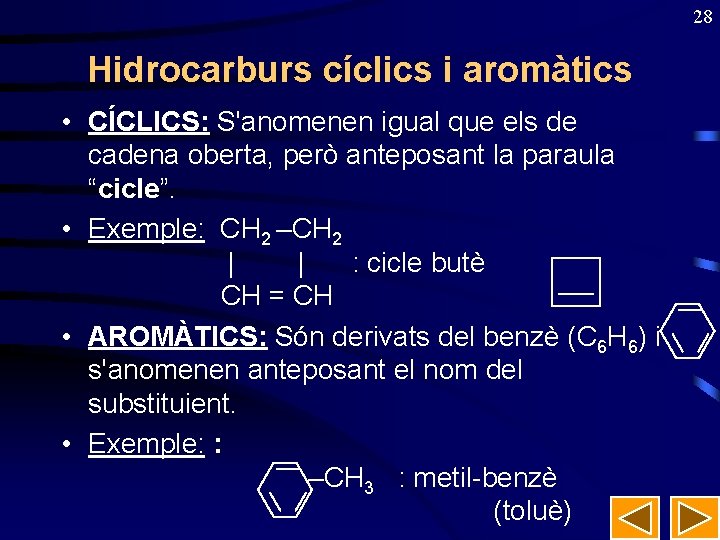
28 Hidrocarburs cíclics i aromàtics • CÍCLICS: S'anomenen igual que els de cadena oberta, però anteposant la paraula “cicle”. • Exemple: CH 2 –CH 2 | | : cicle butè CH = CH • AROMÀTICS: Són derivats del benzè (C 6 H 6) i s'anomenen anteposant el nom del substituient. • Exemple: : –CH 3 : metil-benzè (toluè)

29 Exercici C: Formular: pentà, 2 -hexè, Propí, metil-butí, 3 -etil-2 -pentè • • Pentà 2 -hexè propí metil-butí • 3 -etil-2 -pentè CH 3–CH 2–CH 3 CH 3–CH=CH–CH 2–CH 3 CH C–CH 3 | CH 3–CH =C–CH 2–CH 3 | CH 2–CH 3

30 Exercici D: Anomenar CH 3–CH 2–CH 3–C C–CH 2–C CH CH 2=CH–CH 2–CH 3–CH–CH 2–CH 3 | CH 2–CH 3 hexà CH 3–C =CH–CH–CH 3 | CH 3 2, 4 -dimetil 2 -pentè 1, 4 -hexadií 1 -butè 3 -metil-pentano
![31 Compostos oxigenats OH ÀCIDS Grup CO carboxil Àcid Prefix nº C 31 Compostos oxigenats. • OH ÀCIDS [Grup –C=O (carboxil)]: Àcid + Prefix (nº C)](https://slidetodoc.com/presentation_image/1f3038f25ed83032eb7f411b8f5f12ed/image-30.jpg)
31 Compostos oxigenats. • OH ÀCIDS [Grup –C=O (carboxil)]: Àcid + Prefix (nº C) + sufix “oic”. – Exemple: CH 3–COOH : àcid etanoic (acètic) • O–R ÉSTERS [Grup –C=O]: Prefix (nº C) + sufix “at” de nom de radical acabat en “il”. – Exemple: CH 3–COO–CH 2–CH 3: acetat de etil

32 Exercici E: Formular els següents àcids carboxílics i esters: , àcid pentanoic butanoat de metil ácid 2 -butenoic ácid metil-propanoic metil-propanoat de metil CH 3–CH 2–CH 2–COOH CH 3–CH 2–COO–CH 3–CH=CH–COOH CH 3–CH–COOH | CH 3–CH–COO–CH 3 | CH 3

33 Exercici F: Anomenar: CH 3–C C–COOH CH 3–CH 2–COO–CH 2–CH 3 HOOC–CH 2–COOH CH 3–CH–COO–CH 2–CH 3 | CH 2– CH 3 Àcid 2 -butinoic propanoat de etil àcid propanodioic 2 -metil-butanoat de etil CH 3–CH–CH 2–COO–CH 3 | CH 3 3 -metil-butanoat de metil
![34 Compostos oxigenats ALDEHIDS Grup CO carbonil en un carboni terminal Prefix núm 34 Compostos oxigenats. • ALDEHIDS [Grup C=O (carbonil) en un carboni terminal]: Prefix (núm.](https://slidetodoc.com/presentation_image/1f3038f25ed83032eb7f411b8f5f12ed/image-33.jpg)
34 Compostos oxigenats. • ALDEHIDS [Grup C=O (carbonil) en un carboni terminal]: Prefix (núm. C) + sufix “al”. • Exemple: CH 3–CH 2 –CHO: butanal • CETONA [Grup C=O (carbonil) en un carboni no terminal]: Nombre del C en el que està el grup (si és necessari) + Prefix (núm. C) + sufix “ona”. • Exemple : CH 3–CO–CH 3: propanona

35 Exercici G: Formular: pentanal propanodial 4 -penten-2 -ona metil-propanal dimetil-butanona CH 3–CH 2–CHO CHO–CH 2–CHO CH 3–CO–CH 2–CH=CH 2 CH 3–CH–CHO | CH 3 | CH 3–C–CO–CH 3 | CH 3

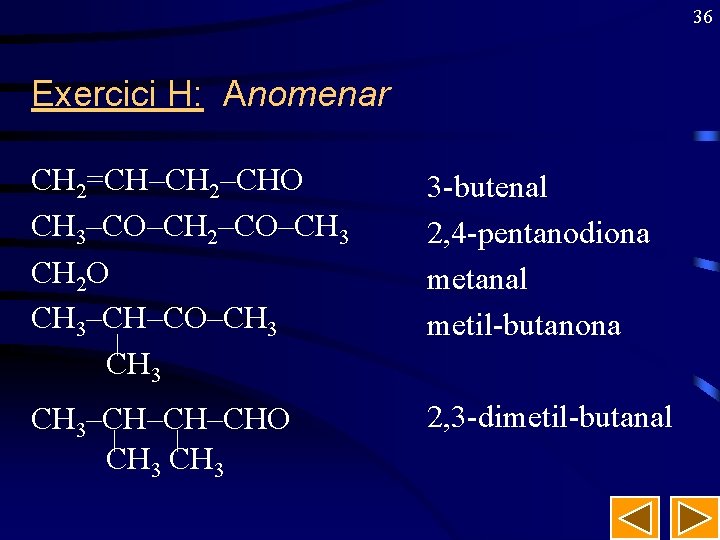
36 Exercici H: Anomenar CH 2=CH–CH 2–CHO CH 3–CO–CH 2–CO–CH 3 CH 2 O CH 3–CH–CO–CH 3 | CH 3 3 -butenal 2, 4 -pentanodiona metanal metil-butanona CH 3–CH–CH–CHO | | CH 3 2, 3 -dimetil-butanal
![37 Compostos oxigenats ALCOHOLS Grup OH hidroxil Nombre del C en el que 37 Compostos oxigenats. • ALCOHOLS: [Grup –OH (hidroxil)]: Nombre del C en el que](https://slidetodoc.com/presentation_image/1f3038f25ed83032eb7f411b8f5f12ed/image-36.jpg)
37 Compostos oxigenats. • ALCOHOLS: [Grup –OH (hidroxil)]: Nombre del C en el que està el grup (si és necessari) + Prefix (núm. C) + sufix “ol”. • ATENCIÓ!: No pot haver-hi dos grups OH en el mateix C. • Exemple: CH 3–CH 2 OH: 1 -propanol • ÈTERS [Grup –O– (oxi)]: S'anomenen els radicals (acabats en“il”) per orde alfabètic seguits de la paraula “èter”. • Exemple: CH 3–O–CH 2–CH 3: etil-metil-éter

38 Exercici I: Formular els següents alcohols i èters 1 -butanol propanotriol 2 -penten-1 -ol metil-1 -propanol CH 3–CH 2–CH 2 OH–CH 2 OH CH 3–CH 2–CH=CH–CH 2 OH CH 3–CH–CH 2 OH | CH 3 | 3, 3 -dimetil-1 -butanol CH 3–C–CH 2 OH | CH 3

39 Exercici J: Anomenar els següents alcohols i èters : CH 2=CH–CHOH–CH 3 – CHOH–CH 2 OH CH 3–O–CH 3–CH–CHOH–CH 3 | CH 3 3 -buten-2 -ol 1, 2 -propanodiol dimetil-éter 3 -metil-2 -butanol CH 3–CH 2–CH–CH 2 OH | CH 3 2 -metil-1 -butanol
![40 Compostos nitrogenats NRR AMIDES Grup CO Prefi X nº C sufi 40 Compostos nitrogenats • NRR’ AMIDES [Grup –C=O]: Prefi. X (nº C) + sufi.](https://slidetodoc.com/presentation_image/1f3038f25ed83032eb7f411b8f5f12ed/image-39.jpg)
40 Compostos nitrogenats • NRR’ AMIDES [Grup –C=O]: Prefi. X (nº C) + sufi. X “amida”. –Ejemplo: CH 3–CONH 2 : etanamida (acetamida) • AMINES [Grup –NH 2 (primària), –NH – (secundària), o –N– (terciària)]: S'anomenen els radicals (acabats en“il”) per orde alfabètic seguits de la paraula “amina”. • Exemple: CH 3–NH–CH 2–CH 3: etil metil amina
![41 Compostos nitrogenats NITRILS o cianurs Grup C N Prefix nº C 41 Compostos nitrogenats • NITRILS (o cianurs) [Grup –C N] Prefix (nº C) +](https://slidetodoc.com/presentation_image/1f3038f25ed83032eb7f411b8f5f12ed/image-40.jpg)
41 Compostos nitrogenats • NITRILS (o cianurs) [Grup –C N] Prefix (nº C) + sufix “nitril”. També pot usar-se cianur de nom de radical acabat en “il acabat en “ ” – Exemple: CH 3–CH 2 –CN: butanonitril o cianur de propil

42 Exercici K: Formular els següents derivats nitrogenats: pentanamida etil-metil-amina 2 -butenonitril N-metil-propanamida trietilamina CH 3–CH 2–CH 2–CONH 2 CH 3–CH 2–NH–CH 3–CH=CH–C N CH 3–CH 2–CONH–CH 3 metil-propanonitril CH 3–CH–C N | CH 3–CH 2–N–CH 2–CH 3 | CH 2–CH 3

43 Exercici: Anomenar : CH 3–CH=CH–CONH–CH 3–CONH–CH 2–CH 3–C N CH 3–CH 2–NH–CH 3–CH 2–CON–CH 2–CH 3 | CH 2–CH 3–CH–CH 2–NH 2 | CH 3 N-metil-2 -butenamida N-etil-etanamida etanonitril metil-propilamina N, N-dietilpropanamida 2 -metilpropilamina (isobutilamina)

44 Altres derivats DERIVATS HALOGENATS: • Prefix (nom de l'halogen) + nom del compost orgànic. • Exemple: : CH 3–CHCl –CH 2 –CH 3 2 -clorbutà. • Nitrocompostos: Prefix (nitro) + nom del compost orgànic. – Exemple: CH 3–CH 2 NO 2 1 -nitrobutà • Compostos ramificats: Prefix (nom del radical) + nom del compost orgànic. – Exemple: CH 3–CH(CH 3)–CH 2 –CH 3 metil butà • En tots els casos s'anteposarà el nombre del carboni al que va unit en el cas de que siga necessari per haver diferents compostos.

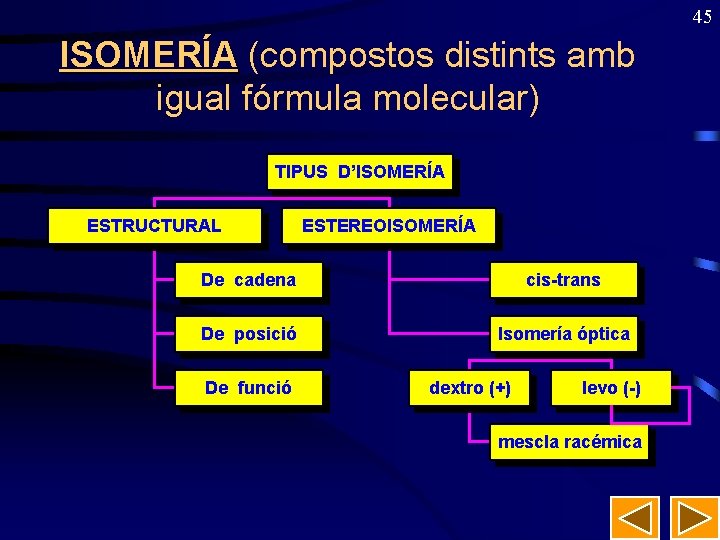
45 ISOMERÍA (compostos distints amb igual fórmula molecular) TIPUS D’ISOMERÍA ESTRUCTURAL ESTEREOISOMERÍA De cadena cis-trans De posició Isomería óptica De funció dextro (+) levo (-) mescla racémica

46 ISOMERÍA ESTRUCTURAL (distinta fórmula Semidesenrotllada). • De cadena: CH 3 – (C 4 H 10) metilpropà CH 3–CH–CH 3 i butà CH 3–CH 2–CH 3 • De posició: – 1 -propanol CH 3–CH 2 OH i 2 -propanol CH 3–CHOH–CH 3 • De funció: – propanal CH 3–CH 2–CHO – i propanona CH 3–CO–CH 3

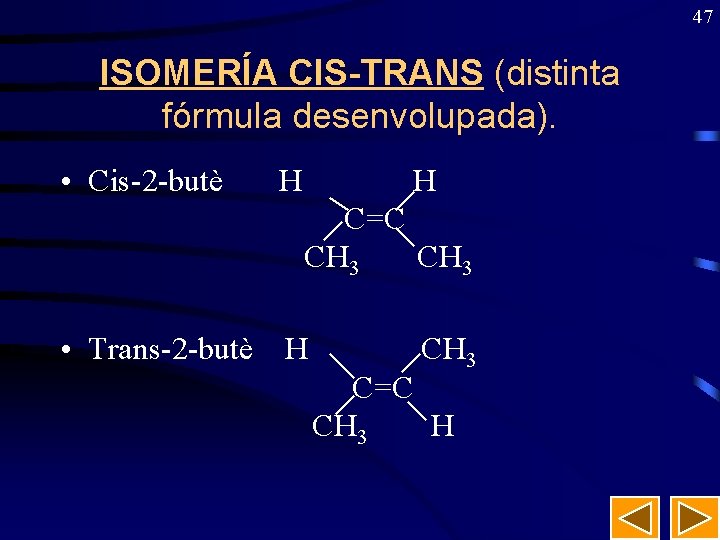
47 ISOMERÍA CIS-TRANS (distinta fórmula desenvolupada). • Cis-2 -butè H C=C CH 3 • Trans-2 -butè H CH 3 C=C CH 3 H

48 ISOMERÍA ÒPTICA • Només s'observa distinta distribució espacial (en tres dimensions) dels grups units a un àtom de carboni. • Perquè hi haja isòmers òptics és necessari que els quatre sustituïents units a un àtom de carboni siguin “distints” (carboni asimètric).

49 ISOMERÍA ÒPTICA • S'assigna un orde de prioritat als grups (per nombre atòmic). Si dos d'ells foren el mateix àtom l'orde es determina per la prioritat dels seus substituients. • Se situa el substituient 4 cap arrere i s'observa el triangle que formen els altres. Si l'orde 1 -2 -3 segueix les agulles del rellotge l'isòmer es denomina R i si seguix el contrari es denomina S.

50 Exemple isomería òptica • R àcid làctic OH (2 hidroxi-propanoic) C H CH 3 COOH • S àcid làctic COOH (2 hidroxi-propanoic) C H CH 3 OH

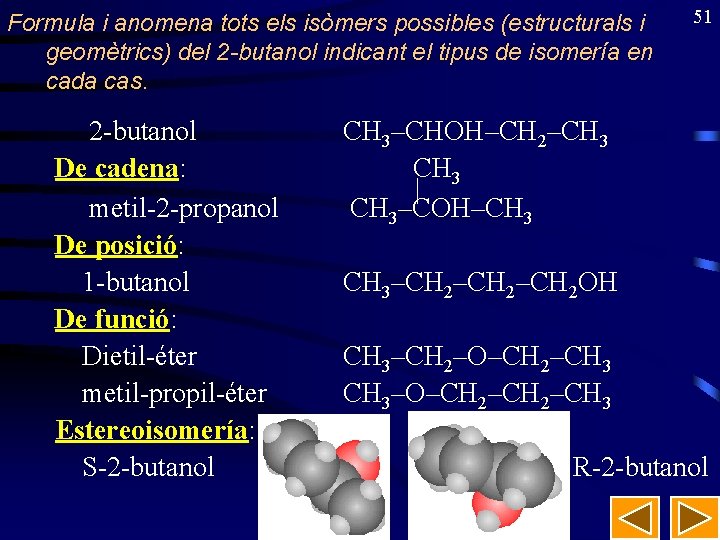
Formula i anomena tots els isòmers possibles (estructurals i geomètrics) del 2 -butanol indicant el tipus de isomería en cada cas. 2 -butanol De cadena: metil-2 -propanol De posició: 1 -butanol De funció: Dietil-éter metil-propil-éter Estereoisomería: S-2 -butanol 51 CH 3–CHOH–CH 2–CH 3 CH 3–COH–CH 3–CH 2–CH 2 OH CH 3–CH 2–O–CH 2–CH 3–O–CH 2–CH 3 R-2 -butanol