Qumica Orgnica o Qumica del Carbono H Es

Química Orgánica o Química del Carbono H Es una rama de la química en la que se estudian los compuestos del carbono y sus reacciones. C H H Acetileno C H H C Metano H

Fuentes Naturales Se encuentra puro en la naturaleza en tres variedades alotrópicas: diamante, grafito y carbono amorfo, que son sólidos con puntos de fusión sumamente altos e insolubles en todos los disolventes a temperaturas ordinarias. Grafito Diamante Carbonos amorfos Hulla Antracita

EL ÁTOMO DE CARBONO C CCC EL ÁTOMO DE CARBONO Nombre: Carbono Símbolo: C Número atómico(Z): 6 Masa atómica(A): 12 Electrones de Valencia: 4 Configuración electrónica: Basal Ubicación en la Tabla Periódica: Grupo: IVA Periódo: 2 1 s 2 2 p 2 Excitada

Propiedades de los compuestos orgánicos vs inorgánicos Propiedad Compuestos Orgánicos Compuestos Inorgánicos Elementos: Enlace químico Densidad Punto de fusión Punto de ebullición Solubilidad en agua Solubilidad en solventes orgánicos Conductividad en solución Estabilidad térmica C, H, O, N, S, P Covalente Baja Bajo Insolubles Son no electrolítos Termolábiles Todos los elementos existentes Iónico Alta Alto Solubles en su mayoría Insolubles en su mayoría Son electrolíticos Termo estables
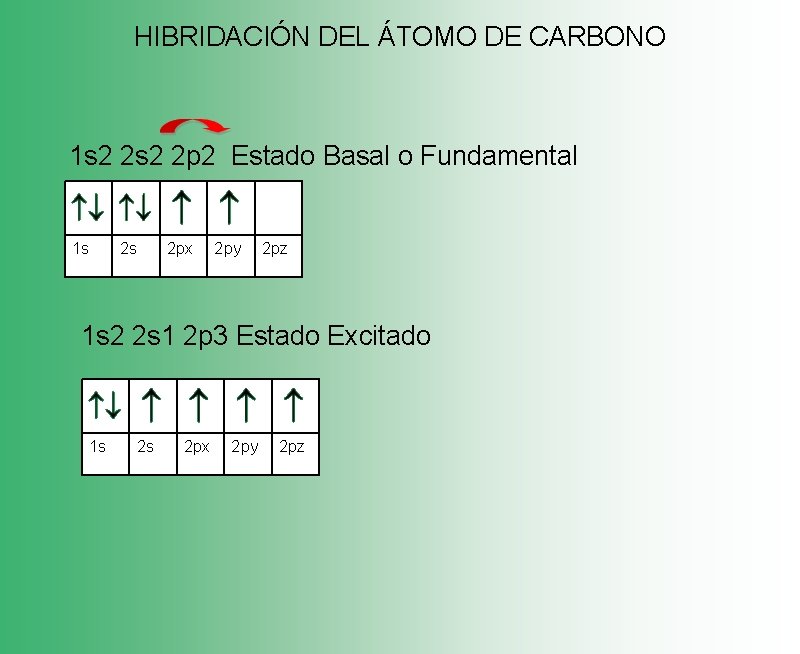
HIBRIDACIÓN DEL ÁTOMO DE CARBONO 1 s 2 2 p 2 Estado Basal o Fundamental 1 s 2 s 2 px 2 py 2 pz 1 s 2 2 s 1 2 p 3 Estado Excitado 1 s 2 s 2 px 2 py 2 pz

Orbitales Atómicos-Moleculares Orbital Atómico: Región del espacio de la corteza del átomo donde existe la mayor probabilidad de hallar un electrón. Un orbital se puede representar, así: ( ), O, [ ], Configuración electrónica del carbono por orbitales para el estado excitado: 1 s 2 2 s 1 2 px 1 2 py 1 2 pz 1
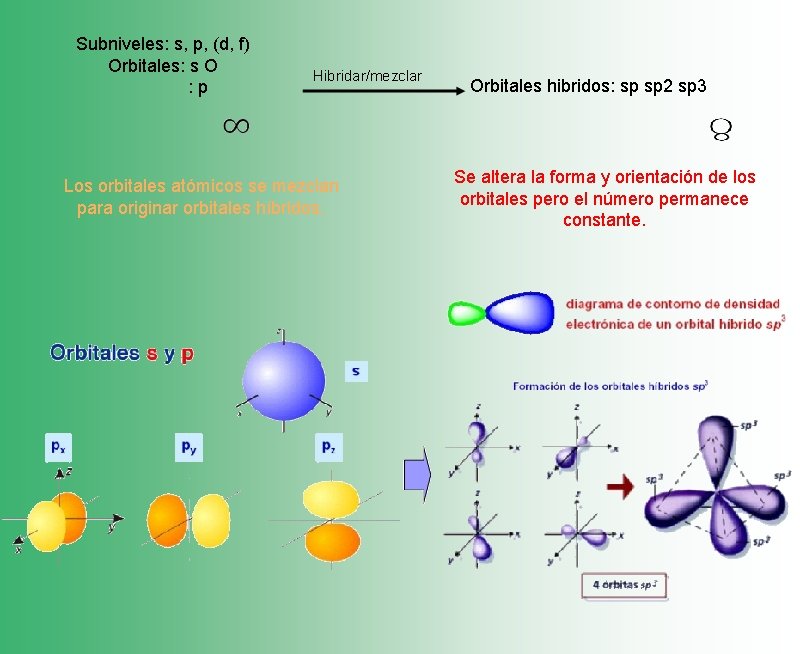
Subniveles: s, p, (d, f) Orbitales: s O : p Hibridar/mezclar Los orbitales atómicos se mezclan para originar orbitales híbridos. Orbitales hibridos: sp sp 2 sp 3 Se altera la forma y orientación de los orbitales pero el número permanece constante.

El proceso de hibridación se caracteriza por: Se produce el mismo número de orbitales híbridos que orbitales atómicos de partida. Son todos iguales: energética y formalmente. Se diferencian en la orientación espacial. Para que haya hibridación los orbitales atómicos de partida deben ser energéticamente muy similares. Los ángulos entre estos es igual.

Puede haber diferente combinación de orbitales atómicos Esa simbología indica el número de orbitales atómicos puros que se están combinando y el tipo de cada uno de ellos. sp Significa que se combinan un orbital s con uno p sp 2 Significa que se combinan un orbital s con dos p sp 3 Significa que se combinan un orbital s con tres p sp 3 d Significa que se combinan un orbital s, tres p y uno d sp 3 d 2 Significa que se combinan un orbital s, tres p y dos d
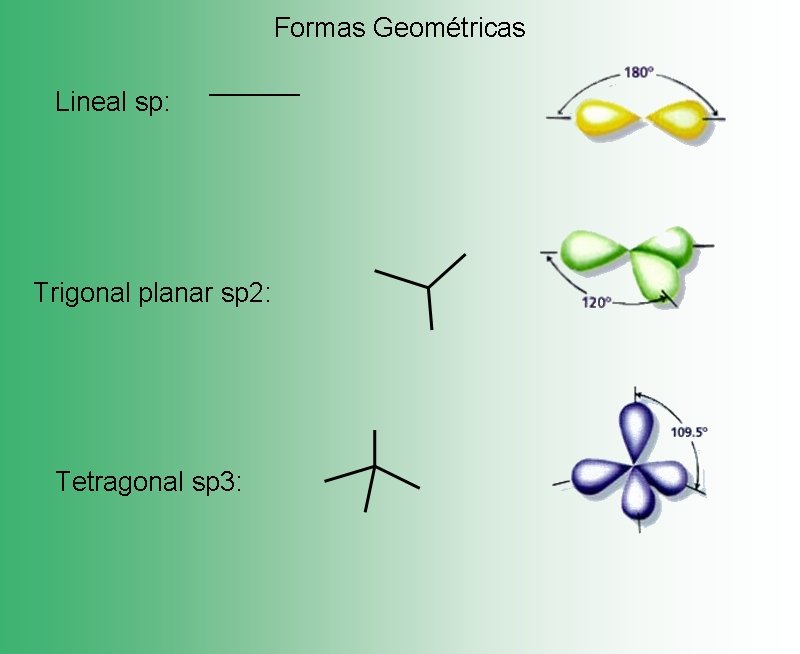
Formas Geométricas Lineal sp: ______ Trigonal planar sp 2: Tetragonal sp 3:
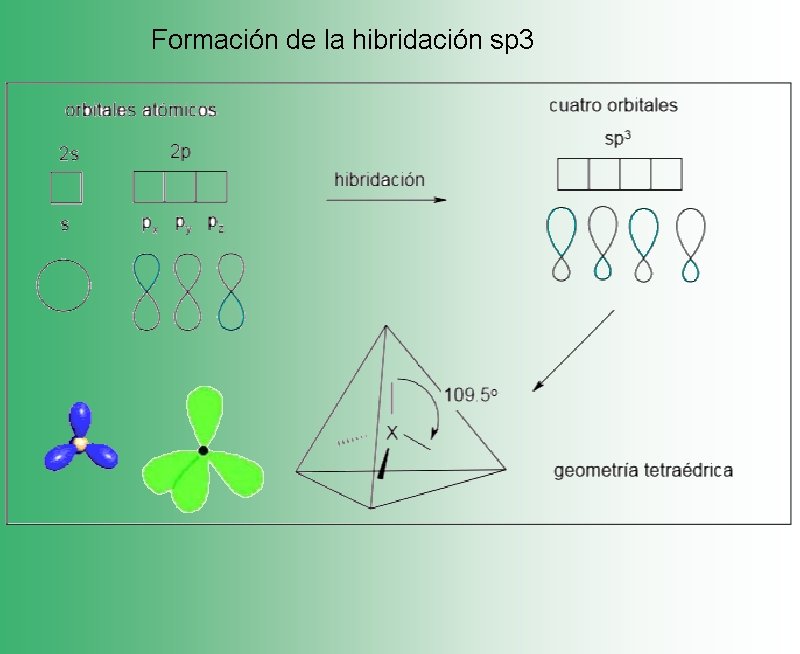
Formación de la hibridación sp 3
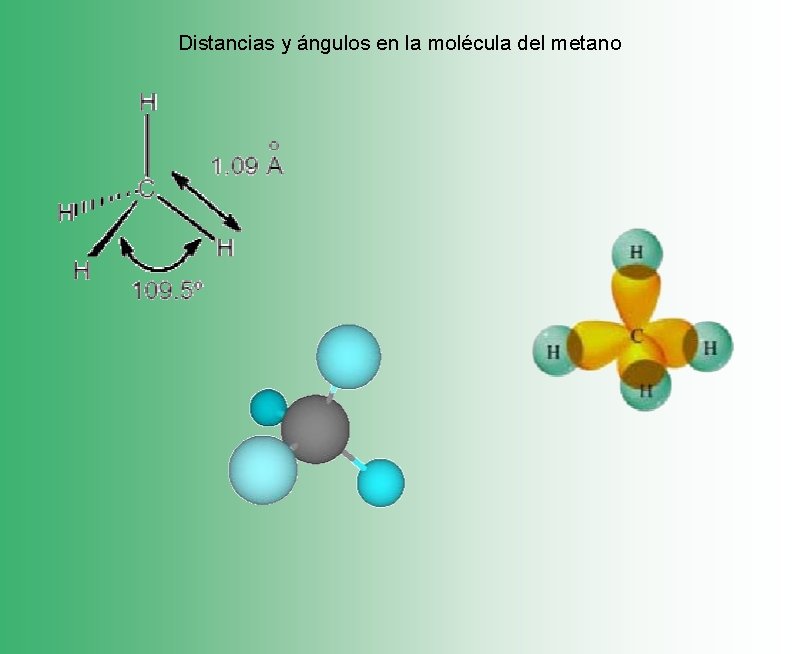
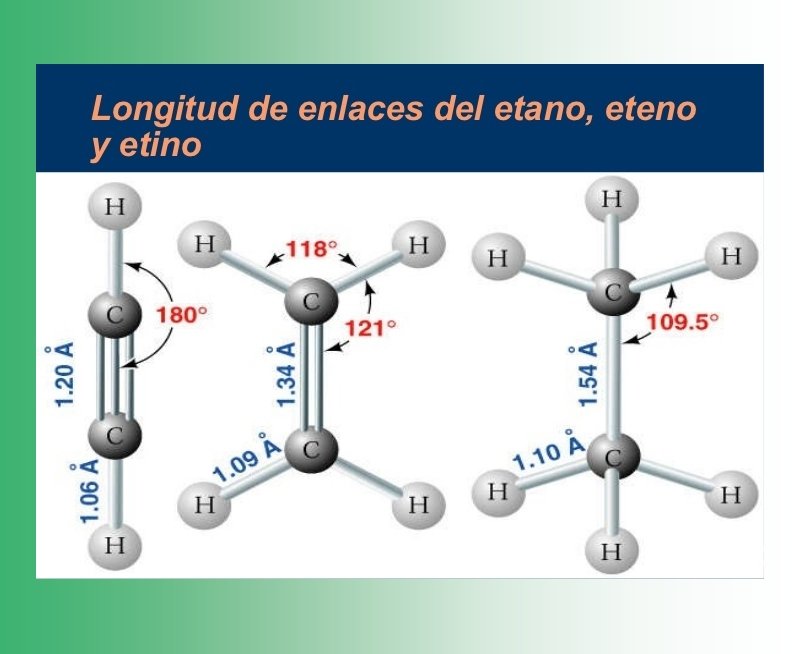
Distancias y ángulos en la molécula del metano
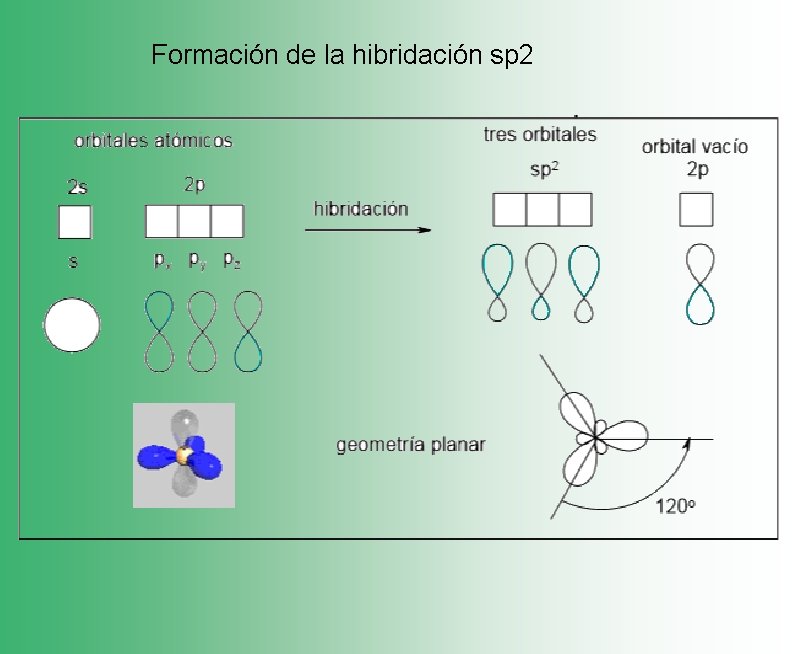
Formación de la hibridación sp 2
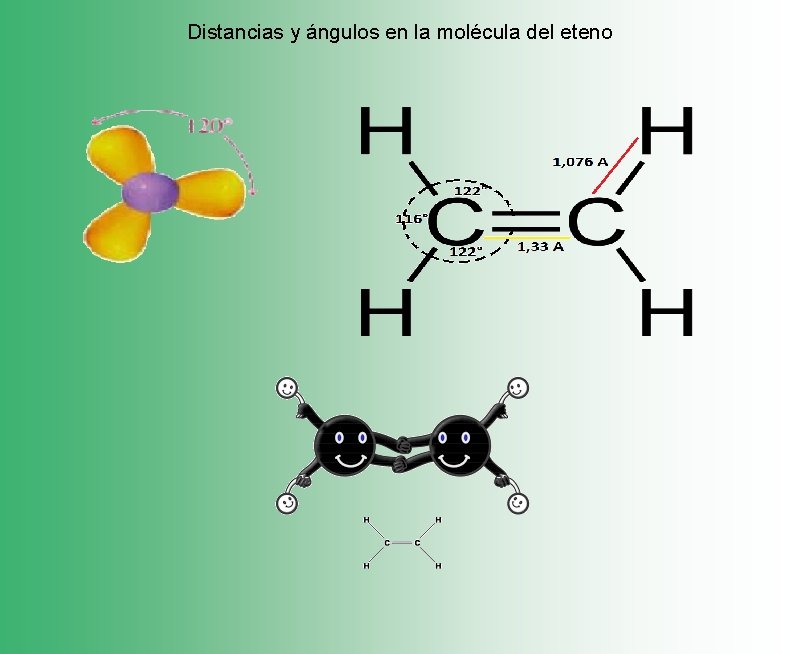
Distancias y ángulos en la molécula del eteno
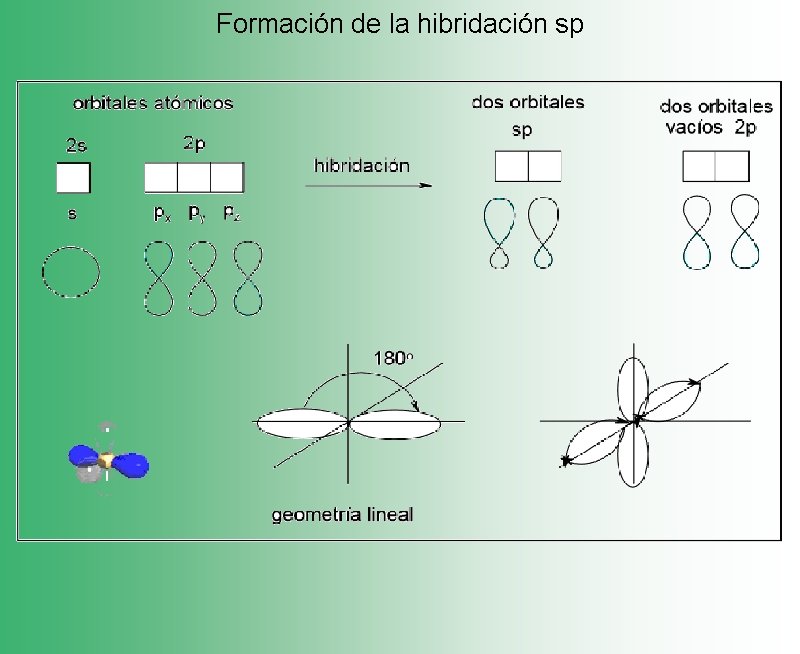
Formación de la hibridación sp
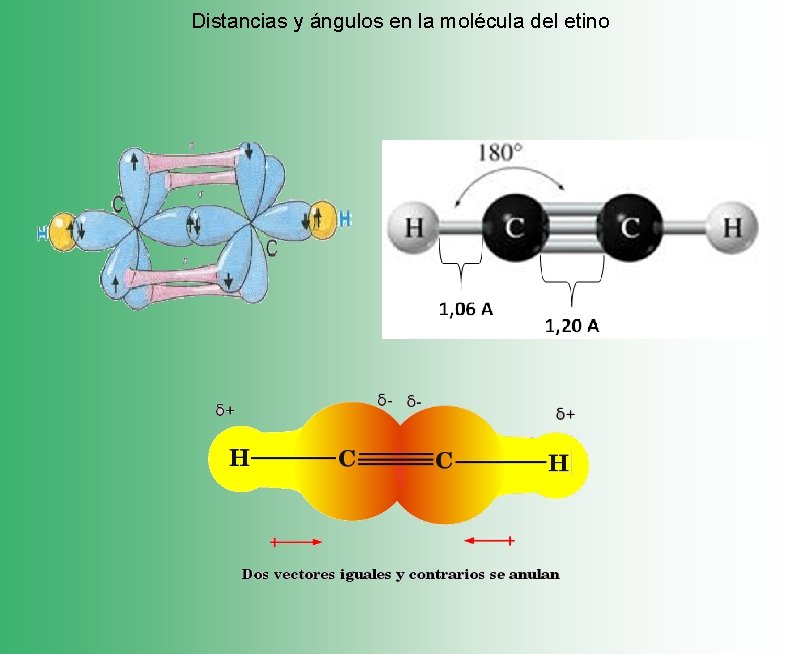
Distancias y ángulos en la molécula del etino
- Slides: 18