Defeitos na Estrutura Cristalina e Difuso a prata











































- Slides: 82

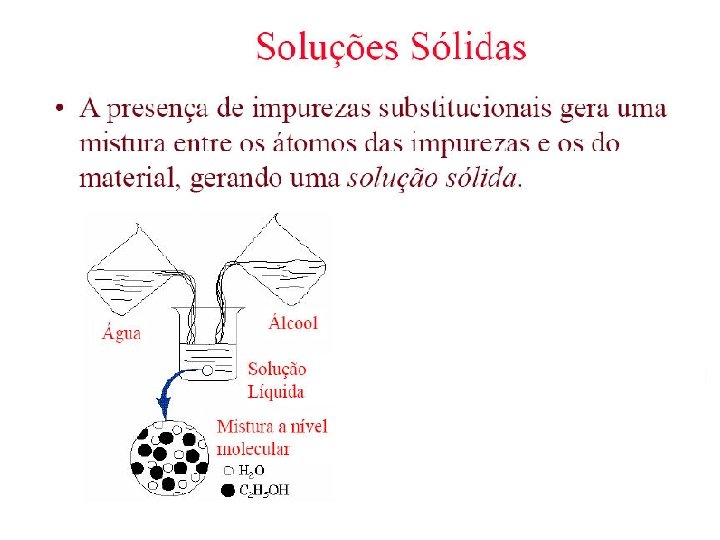
Defeitos na Estrutura Cristalina e Difusão








a prata de lei é uma liga composta por 92, 5% de prata e 7, 5% de cobre.

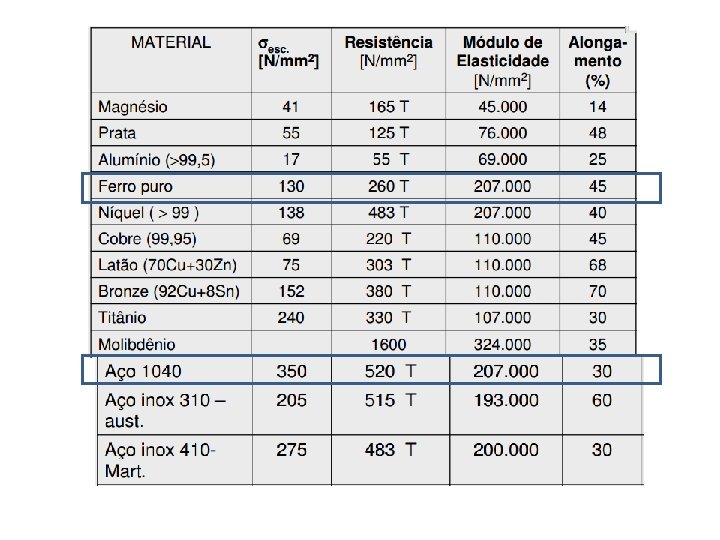
O alumínio comercialmente puro tem uma resistência à tração de aproximadamente 90 Mpa. Aumentos maiores na sua resistência podem ser obtidos com pequenas adições de outros metais como elementos de liga, tais como: silício, cobre, manganês, magnésio, cromo, zinco, ferro etc. E as “ligas tratáveis” podem ainda apresentar aumento de resistência através de tratamento térmico, tanto que hoje algumas ligas podem ter resistência à tração de aproximadamente 700 MPa




Definições e Conceitos Básicos

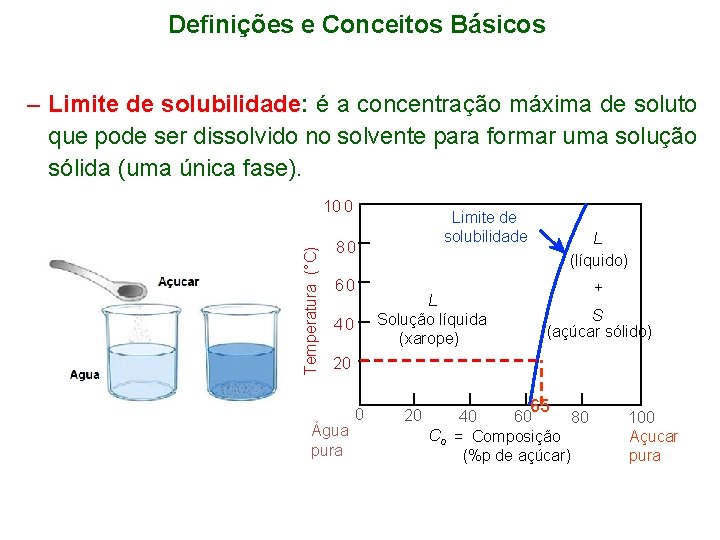
Definições e Conceitos Básicos – Limite de solubilidade: é a concentração máxima de soluto que pode ser dissolvido no solvente para formar uma solução sólida (uma única fase). Temperatura (°C) 10 0 Limite de solubilidade 80 60 L Solução líquida (xarope) 40 L (líquido) + S (açúcar sólido) 20 Água pura 0 20 65 40 60 80 Co = Composição (%p de açúcar) 100 Açucar pura

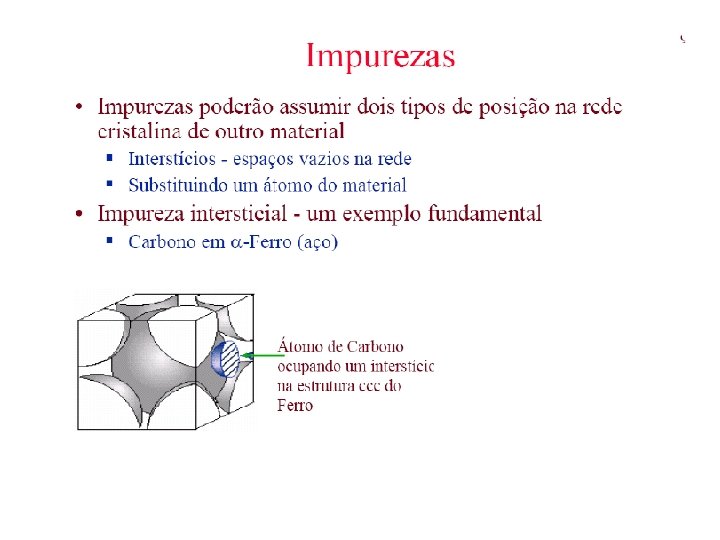
Características das Fases do Ferro FERRO = FERRITA n Estrutura= ccc n Temperatura “existência”= até 912 C n Fase Magnética até 768 C (temperatura de Curie) n Solubilidade máx do Carbono= 0, 02% a 727 C FERRO = AUSTENITA n Estrutura= cfc (tem + posições intersticiais) n Temperatura “existência”= 912 1394 C n Fase Não-Magnética n Solubilidade máx do Carbono= 2, 14% a 1148 C FERRO = FERRITA b. Estrutura= ccc b. Temperatura “existência”= acima de 1394 C b. Fase Não-Magnética bÉ a mesma que a ferrita b. Como é estável somente a altas temperaturas não apresenta interesse 16 comercial

CEMENTITA (FE 3 C) • Forma-se quando o limite de solubilidade do carbono é ultrapassado (6, 7% de C) • É dura e frágil • é um composto intermetálico metaestável, embora a velocidade de decomposição em ferro e C seja muito lenta • A adição de Si acelera a decomposição da cementita para formar grafita 17

























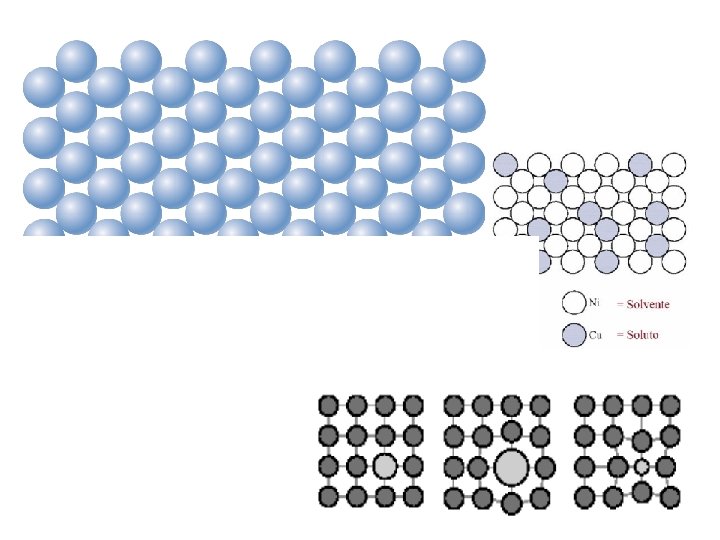
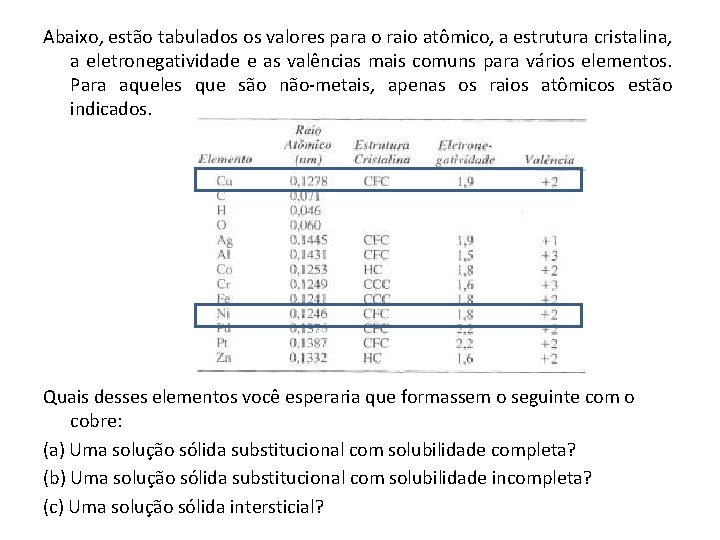
Abaixo, estão tabulados os valores para o raio atômico, a estrutura cristalina, a eletronegatividade e as valências mais comuns para vários elementos. Para aqueles que são não-metais, apenas os raios atômicos estão indicados. Quais desses elementos você esperaria que formassem o seguinte com o cobre: (a) Uma solução sólida substitucional com solubilidade completa? (b) Uma solução sólida substitucional com solubilidade incompleta? (c) Uma solução sólida intersticial?

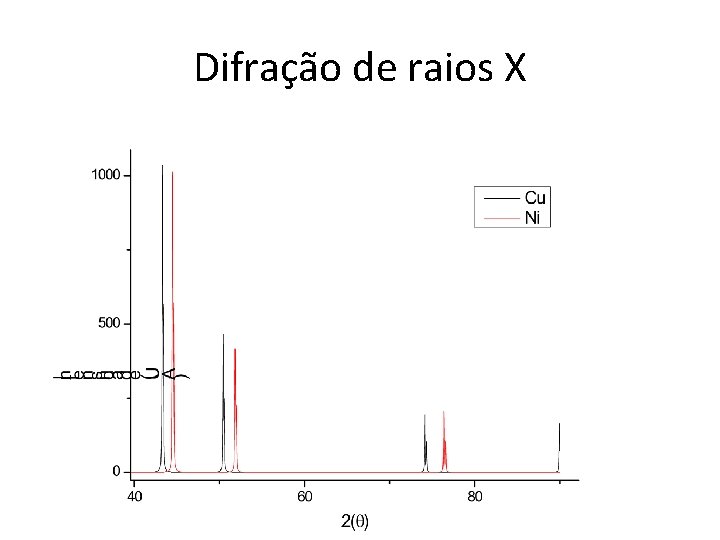
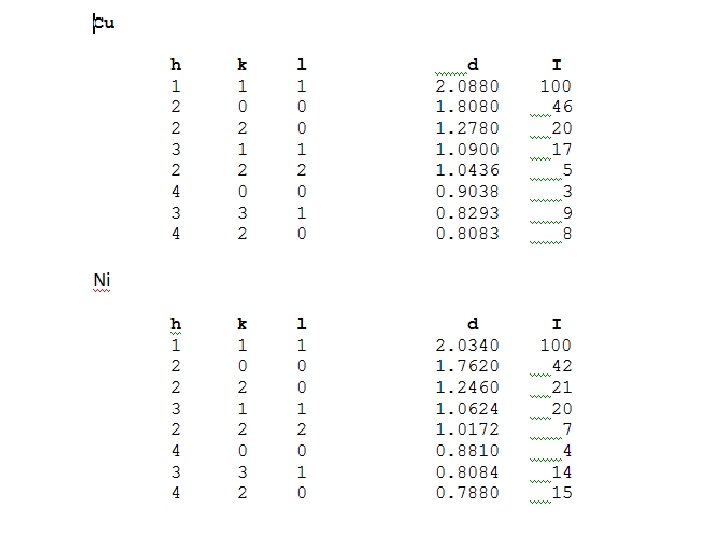
Difração de raios X


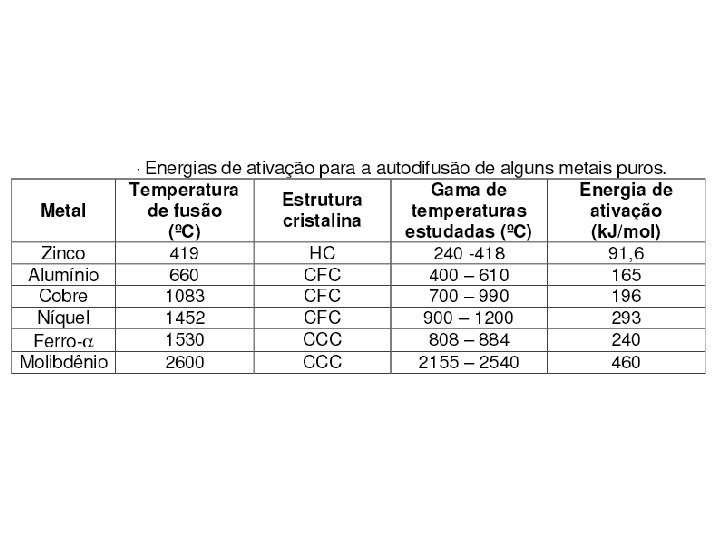
Difusão de impurezas ou interdifusão Autodifusão – ocorre nos metais puros, os átomos que mudam de posição são do mesmo tipo




* Usada para melhorar as propriedades mecânicas de alguns materiais; • Temperaturas e tempos podem ser estimados através das taxas de difusão.

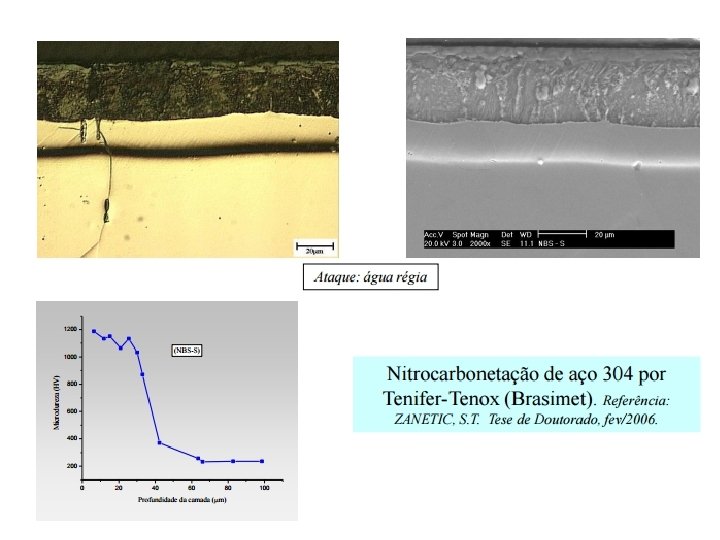
Aplicações industriais de processos de difusão


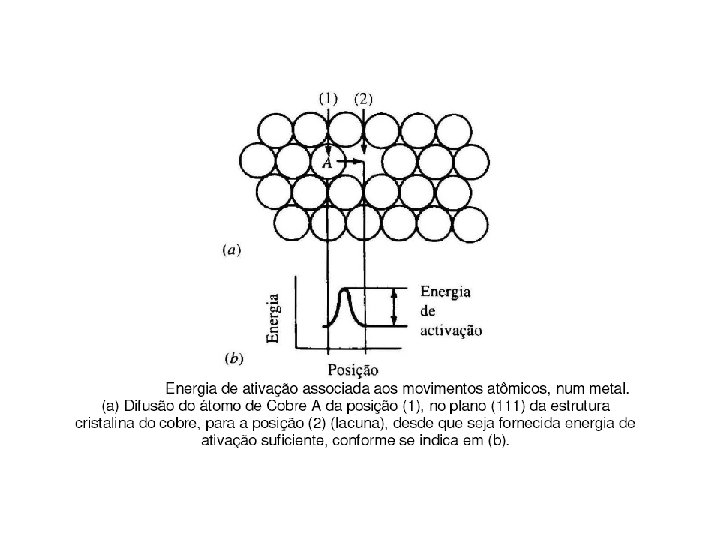
• De uma perspectiva atômica difusão é a migração em etapas de átomos de um sítio ao outro do reticulado cristalino. • Os átomos em materiais sólidos estão em movimento constante • Para o átomo se movimentar é preciso: • deve existir um sítio adjacente vazio; • o átomo deve possuir energia suficiente para quebrar as ligações atômicas e causar alguma distorção na rede cristalina durante deslocamento • Essa energia é de natureza vibracional e aumenta com aumento da temperatura; • Nos metais os átomos se movimento de 2 maneiras: por lacuna ou por difusão intersticial.

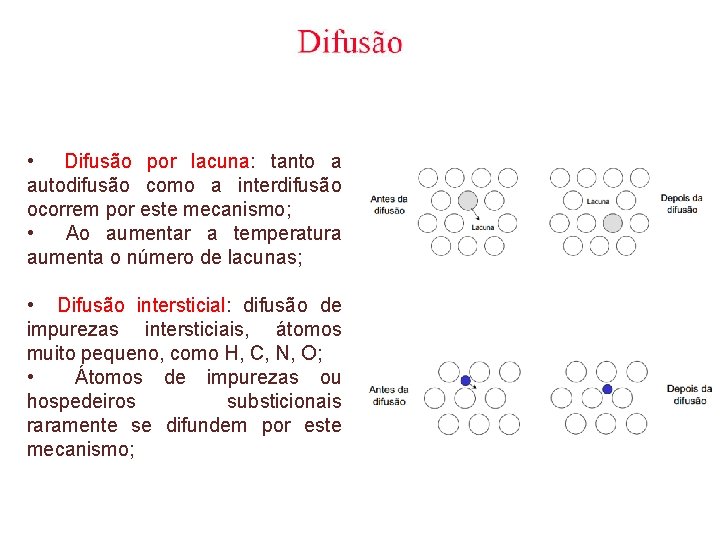
• Difusão por lacuna: tanto a autodifusão como a interdifusão ocorrem por este mecanismo; • Ao aumentar a temperatura aumenta o número de lacunas; • Difusão intersticial: difusão de impurezas intersticiais, átomos muito pequeno, como H, C, N, O; • Átomos de impurezas ou hospedeiros substicionais raramente se difundem por este mecanismo;

Na maioria das ligas metálicas, a difusão intersticial ocorre muito mais rapidamente do que a difusão por lacunas, uma vez que os átomos intersticiais são menores, e dessa forma são também mais móveis. Além disso, existem mais posições intersticiais vazias do que lacunas; portanto, a probabilidade de um movimento atômico intersticial é maior do que para a difusão por lacunas.

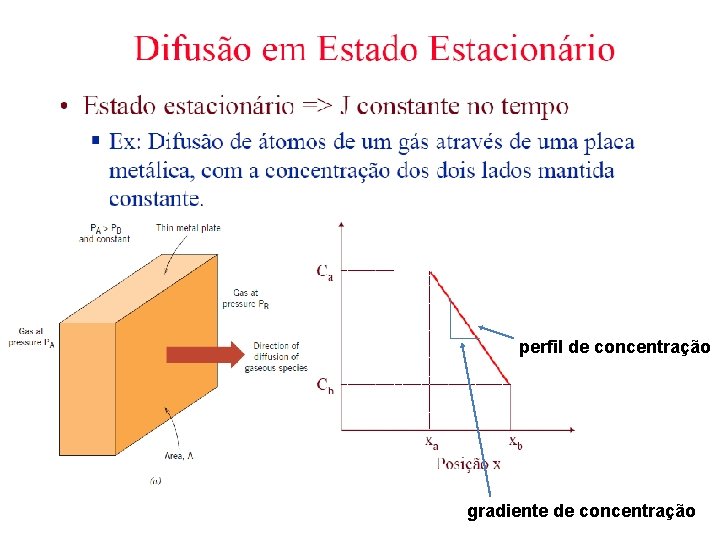
Difusão Processo espontâneo de transporte de massa num sistema, por efeito de gradientes de concentração.

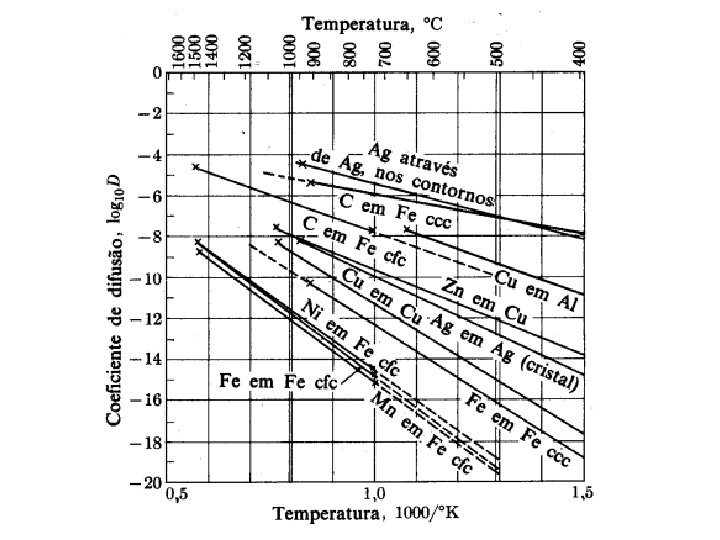
Quão rápido ocorre a difusão?



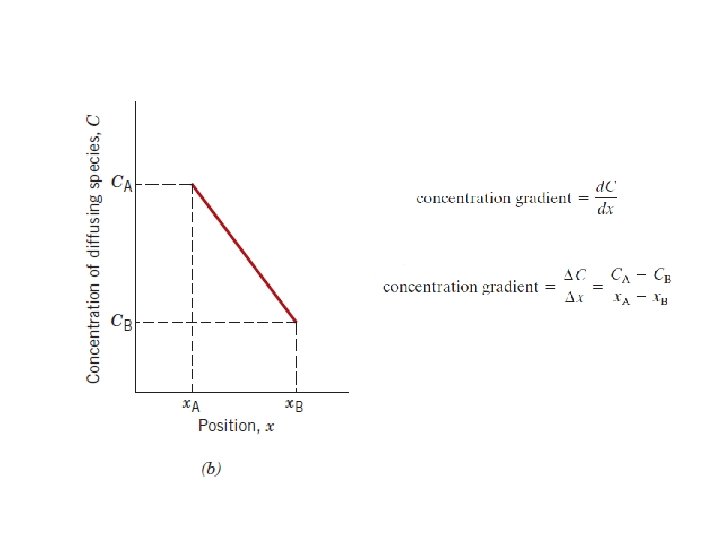
perfil de concentração gradiente de concentração







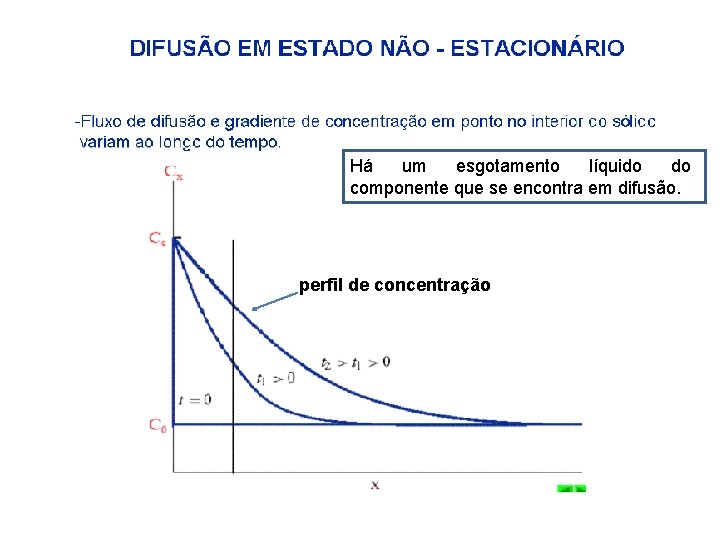
Há um esgotamento líquido do componente que se encontra em difusão. perfil de concentração












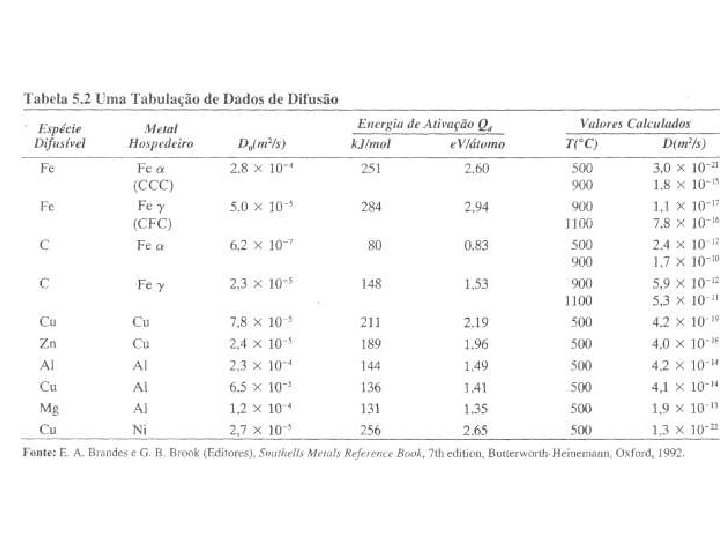
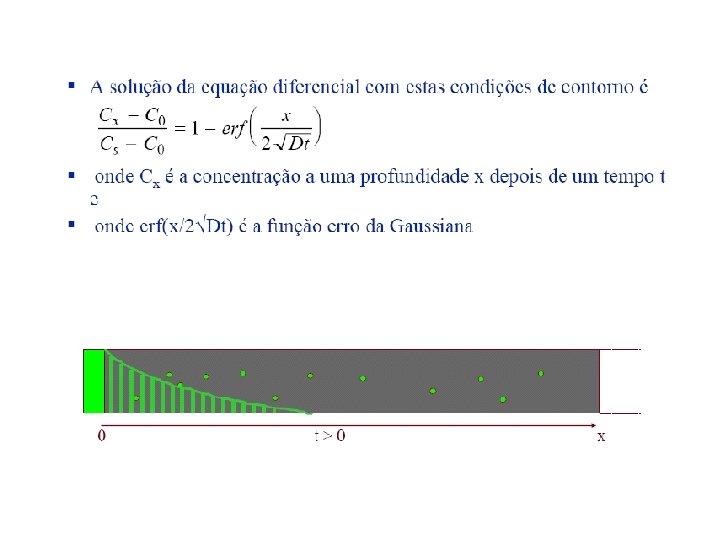
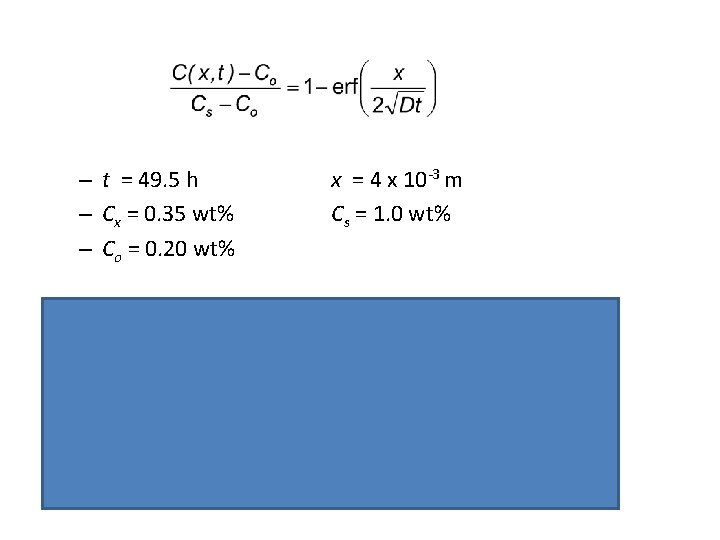
Outro exemplo de carbonetação: • Sample Problem: An FCC iron-carbon alloy initially containing 0. 20 wt% C is carburized at an elevated temperature and in an atmosphere that gives a surface carbon concentration constant at 1. 0 wt%. If after 49. 5 h the concentration of carbon is 0. 35 wt% at a position 4. 0 mm below the surface, determine the temperature at which the treatment was carried out. Use:

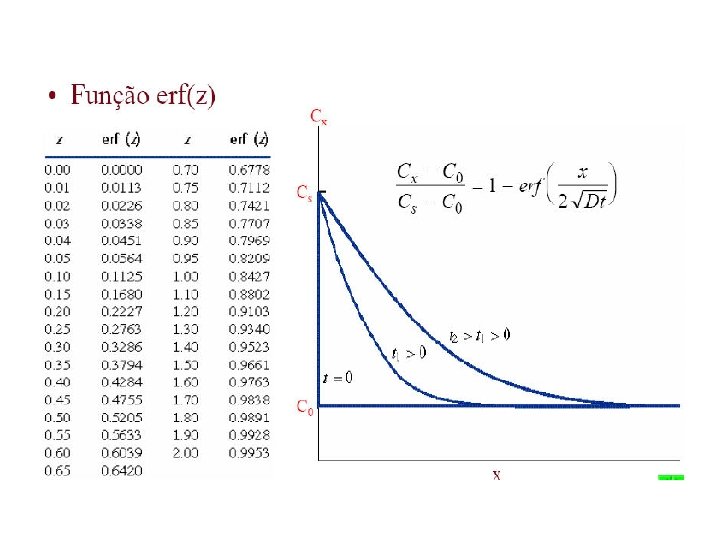
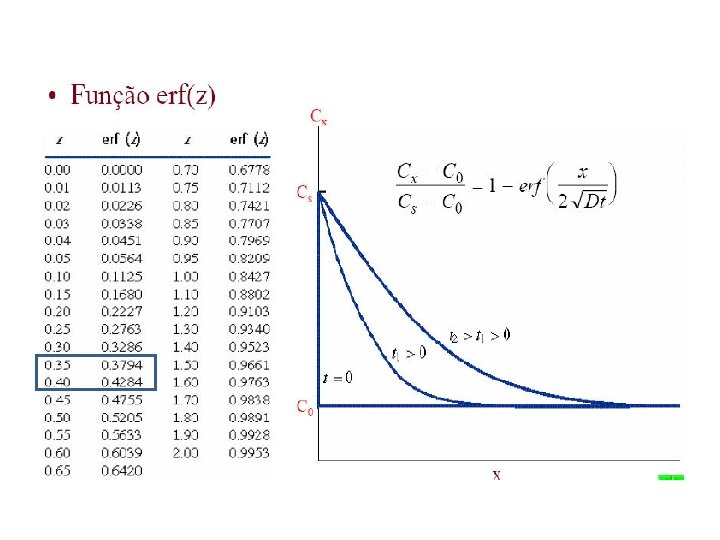
– t = 49. 5 h – Cx = 0. 35 wt% – Co = 0. 20 wt% x = 4 x 10 -3 m Cs = 1. 0 wt% erf(z) = 0. 8125

z erf(z) 0. 90 z 0. 95 0. 7970 0. 8125 0. 8209 Now solve for D z = 0. 93


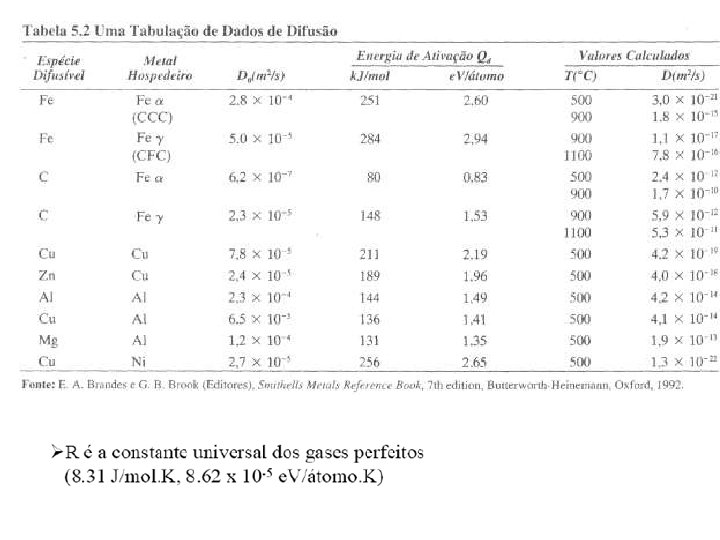
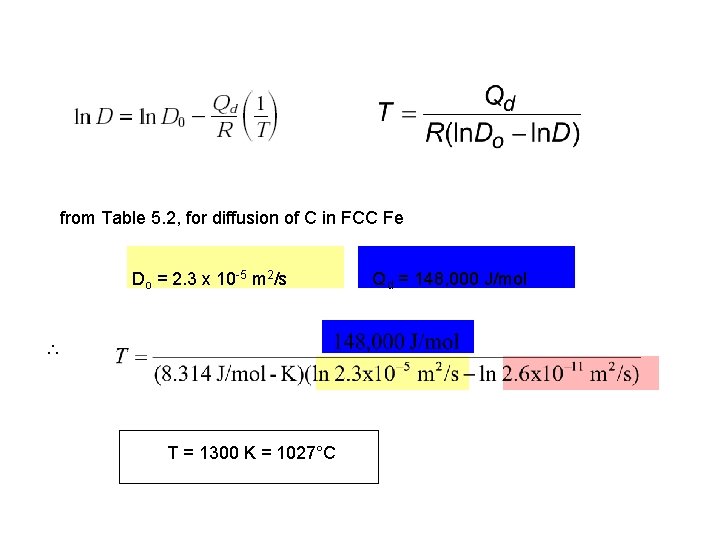
from Table 5. 2, for diffusion of C in FCC Fe Do = 2. 3 x 10 -5 m 2/s T = 1300 K = 1027°C Qd = 148, 000 J/mol