Sistemik Lupus Eritematozus SLE Tedavisinde Yeni Gelimeler Salih



















- Slides: 52

Sistemik Lupus Eritematozus (SLE) Tedavisinde Yeni Gelişmeler Salih Kavukçu Dokuz Eylül Üniversitesi Tıp Fakültesi

• Tedavi bireyseldir. • Hastanın tutulum tipi dikkate alınır. • Hastanın tedaviyi tolere etmesi esastır. • Hastaların çoğunluğu adölesan olduğundan tedavi uyumu güçtür.

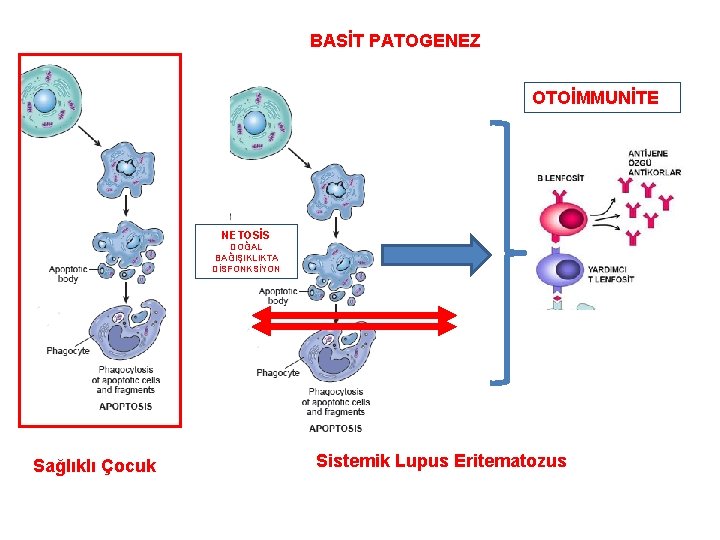
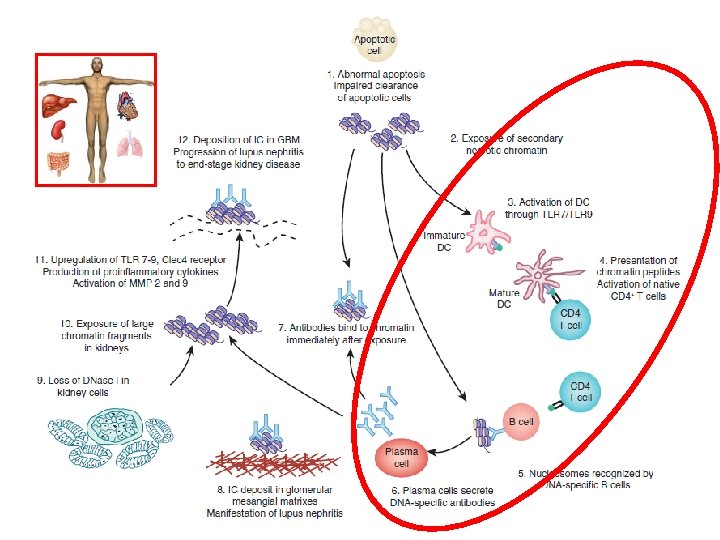
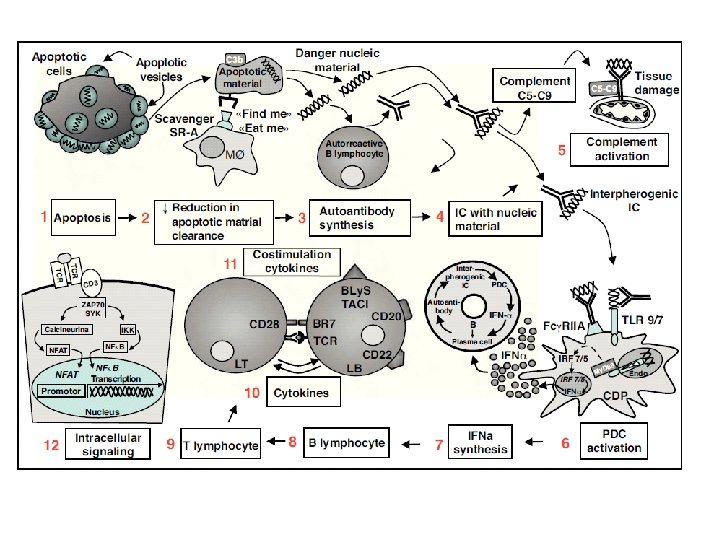
BASİT PATOGENEZ OTOİMMUNİTE NETOSİS DOĞAL BAĞIŞIKLIKTA DİSFONKSİYON Sağlıklı Çocuk Sistemik Lupus Eritematozus

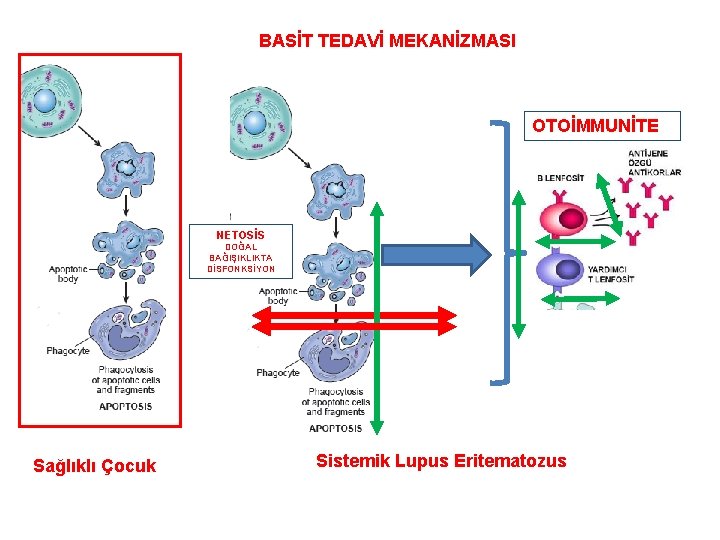
BASİT TEDAVİ MEKANİZMASI OTOİMMUNİTE NETOSİS DOĞAL BAĞIŞIKLIKTA DİSFONKSİYON Sağlıklı Çocuk Sistemik Lupus Eritematozus


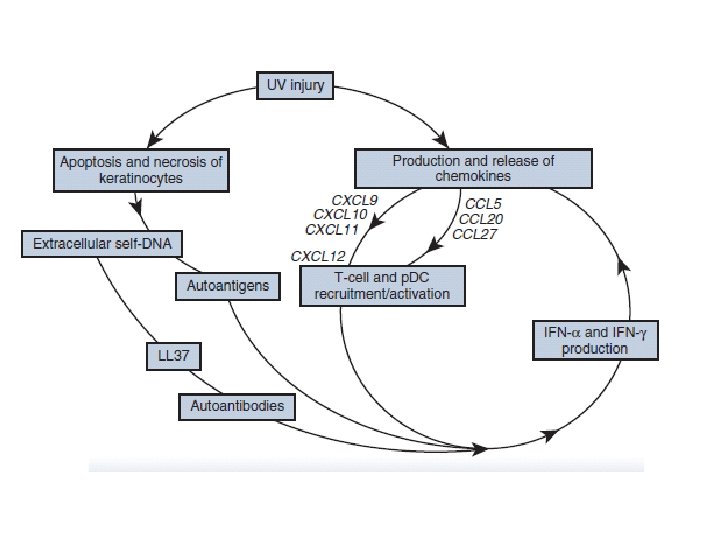
• Tüm hastalara güneş koruyucu önerilmelidir. • Uzun süre doğrudan güneş ışınlarına maruz kalınması önlenmelidir. • Diğer ultraviyole ışın kaynaklarından sakınılmalıdır. • Bu öneriler, hastanın her kontrolunda kendisine anımsatılmalıdır.




SLE tedavisinde amaç • Hastalığın aktivitesi kontrol altına alınacak • Beraberinde olan morbidite azaltılacak • İlaç toksisitesi önlenecek • Hedef organ hasarı azaltılacak • Yaşam kalitesi düzeltilecek • Mortalite riski azaltılacak


İMMUNOSÜPRESYON OTOİMMUN DİSFONKSİYONUN DÜZELTİLMESİ ORGAN HASARININ ÖNLENMESİ Tedavi edilmezse, mortalite 5 yılda %95

SLE TEDAVİSİNİ BELİRLEYEN FAKTÖRLER SLE de tutulan organın tutulum düzeyi SLE de Irk Böbrek Kalp Perikardit Myokardit Endokardit Asya Böbrek Class III (A) Class III (A/C) Class III (C) Class IV-S (A) Class IV-G (A) Class IV-S (A/C) Class IV-G (A/C) Class IV-S (C) Class IV-G (C) Class VI Afrika kökenli Amerikalı Kalp Akciğer Kas-iskelet Sinir sistemi Göz Endokrin Deri Sinir sistemi Santral sinir sistemi Periferik sinir Beyaz Hispanik

İNDÜKSİYON TEDAVİSİ immunosupresyon Neden tek bir immunsupresyon protokolu seçerek sürekli onu kullanmıyoruz? Neden başlangıçta yoğun immunsupresyona gereksinim duyuyoruz? Uygulanan yoğun immunsupresyon protokolunun sonradan kullanılan idame protokole yararı nedir? immunosupresyon Önce otoimmuniteyi durdurmak için immun sistemi indüksiyon tedavisi ile baskılıyoruz. Ardından idame tedavi ile nüksün ortaya çıkmasını önlüyoruz, Hedefteki organın zedelenmesini azaltıyoruz. İDAME TEDAVİ

Hidroksiklorokin • Tolere edebilen her SLE olgusuna hidroksiklorokin (5 -7 mg/kg/gün, maksimum 400 mg/day) önerilir. • Döküntü, hafif derecede artrit gibi SLE bulgularını tedavi eder, SLE aktivasyonunu önler, lipid profilini düzeltir, böbrek tutulumu ve mortalite üzerinde olumlu etkileri olabilir. Antitrombotik ve glukoz düzeyini düşürücü etkisi vardır. • Lupus nefriti olgularında rutin olarak önerilmektedir. • Retinal pigmentasyon ve görmenin bozulmasına neden olabilir. hidroksiklorokin alan hastaların 6 -12 ayda oftalmolojik muayenelerinin yapılması gerekir. • ETKİ MEKANİZMASI: Endozomal Ph artırarak nükleik asidin TLR e bağlanmasını inhibe eder.

Kortikosteroidler • SLE nin önemli organ tutulumlarında tedavinin esası kortikosteroidlerdir. • Hastalıktaki akut olarak izlenen kötü gidişi hızla düzeltmek için kullanılır. Yan etkileri özellikle adölesanlarda ilacın kullanımını kısıtlamaktadır. • Kortikosteroidlerin dozu ve kullanım süresi elden geldiğince sınırlandırılmalıdır. Total steroid doz ve süresini azaltmak amacı ile, diğer immunosüpresif ajanlar ile tedaviyi sürdürmek gerekmektedir. • Büyüme geriliği, stria, akne, hiperglisemi, hipertansiyon, katarakt, avasküler nekroz ve osteoporoz tedavi sırasında görülen başlıca yan etkilerdir. • SLE li çocuk ve adölesanlarda kortikosteroidlerin optimal dozu bilinmemektedir. Ağır olgularda IV metil prednisolon (30 mg/kg/gün, 3 gün ve takiben haftada bir gün ) veya yüksek dozda oral prednison (1 -2 mg/kg/gün) verilebilir. Hastalık bulguları geriledikçe doz tedricen azaltılarak aylar içinde kesilebilir. • IV metil prednisolon, plasmasitoid dendritik hücre sayısını düşürerek, ekspresyonunu azaltır, oral prednisolonun bu etkisi yoktur. interferon alfa gen

Kortikosteroidin SLE de etki mekanizması • Proinflamatuvar sitokinleri azaltır T hücre, monosit ve makrofajları azaltır. Yangı alanlarında lökosit aktivitelerini inhibe eder. Yangı alanlarında endotelial hücre geçirgenliği, adezyon molekülü yapımı ve fibroblast fonksiyonunu inhibe eder. • Genomik yolakta: Sitozolik reseptörlere bağlanır, nükleus içine girer. “Glucocorticoid corticosteroid” yanıtlayan elemanlar bölgesine bağlanır, antienflamatuar proteinlerin ekspresyonunu aktive eder. (TRANSAKTİVASYON) Nükleer koaktivatörlerin transkripsiyon faktörlerini bağlar, proinflamatuar sitokinlerin ekspresyonunu önler (TRANSREPRESYON) • Geliştirilmekte olan “selektif kortikosteroid reseptörü agonistleri” steroidin etkisini transrepresyon genomik etki ile yan etki yaratmadan sağlayacaklardır. • Steroidlerin yüksek dozlarda, hızlı antienflamatuvar etkisi non-genomik mekanizma ile olur. Kortikosteroidler mitokondri ve plazma membranını etkileyerek, araşidonik asid salınımını inhibe ederek proinflamatuar sitokin salınımını azaltarak, membrana bağlı reseptörler aracılığı ile immun hücrelerin fonksiyonlarını azaltırlar.

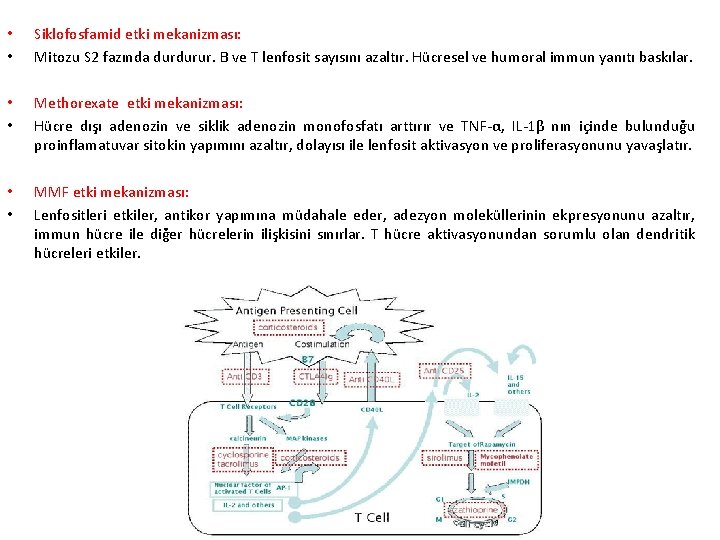
• • Siklofosfamid etki mekanizması: Mitozu S 2 fazında durdurur. B ve T lenfosit sayısını azaltır. Hücresel ve humoral immun yanıtı baskılar. • • Methorexate etki mekanizması: Hücre dışı adenozin ve siklik adenozin monofosfatı arttırır ve TNF-α, IL-1β nın içinde bulunduğu proinflamatuvar sitokin yapımını azaltır, dolayısı ile lenfosit aktivasyon ve proliferasyonunu yavaşlatır. • • MMF etki mekanizması: Lenfositleri etkiler, antikor yapımına müdahale eder, adezyon moleküllerinin ekpresyonunu azaltır, immun hücre ile diğer hücrelerin ilişkisini sınırlar. T hücre aktivasyonundan sorumlu olan dendritik hücreleri etkiler.

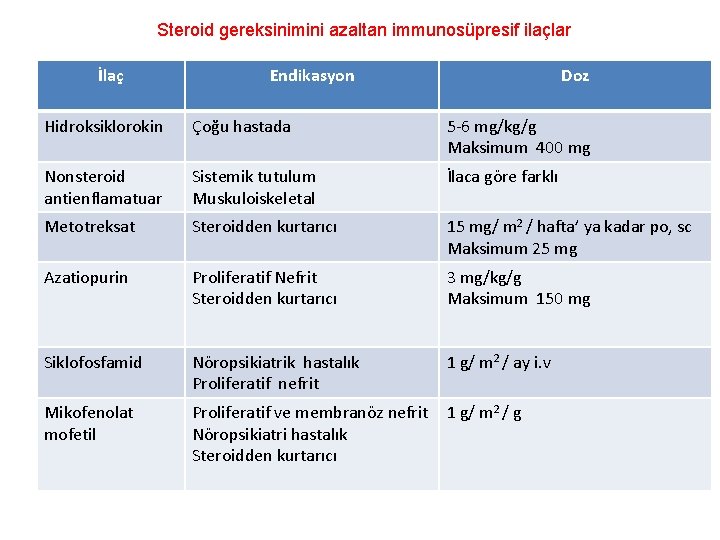
Steroid gereksinimini azaltan immunosüpresif ilaçlar İlaç Endikasyon Doz Hidroksiklorokin Çoğu hastada 5 -6 mg/kg/g Maksimum 400 mg Nonsteroid antienflamatuar Sistemik tutulum Muskuloiskeletal İlaca göre farklı Metotreksat Steroidden kurtarıcı 15 mg/ m 2 / hafta’ ya kadar po, sc Maksimum 25 mg Azatiopurin Proliferatif Nefrit Steroidden kurtarıcı 3 mg/kg/g Maksimum 150 mg Siklofosfamid Nöropsikiatrik hastalık Proliferatif nefrit 1 g/ m 2 / ay i. v Mikofenolat mofetil Proliferatif ve membranöz nefrit Nöropsikiatri hastalık Steroidden kurtarıcı 1 g/ m 2 / g

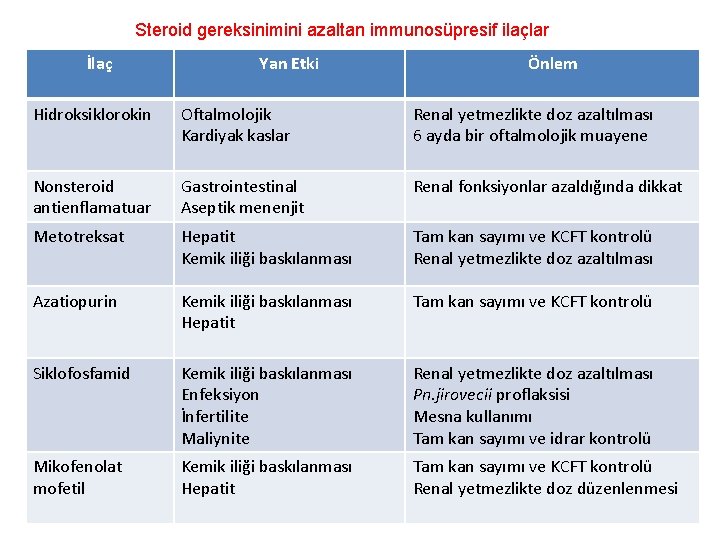
Steroid gereksinimini azaltan immunosüpresif ilaçlar İlaç Yan Etki Önlem Hidroksiklorokin Oftalmolojik Kardiyak kaslar Renal yetmezlikte doz azaltılması 6 ayda bir oftalmolojik muayene Nonsteroid antienflamatuar Gastrointestinal Aseptik menenjit Renal fonksiyonlar azaldığında dikkat Metotreksat Hepatit Kemik iliği baskılanması Tam kan sayımı ve KCFT kontrolü Renal yetmezlikte doz azaltılması Azatiopurin Kemik iliği baskılanması Hepatit Tam kan sayımı ve KCFT kontrolü Siklofosfamid Kemik iliği baskılanması Enfeksiyon İnfertilite Maliynite Renal yetmezlikte doz azaltılması Pn. jirovecii proflaksisi Mesna kullanımı Tam kan sayımı ve idrar kontrolü Mikofenolat mofetil Kemik iliği baskılanması Hepatit Tam kan sayımı ve KCFT kontrolü Renal yetmezlikte doz düzenlenmesi

Biyolojik tedavi nedir? • İmmun sistemin biyolojik yanıtını etkilemeye, düzenlemeye ve değiştirmeye yönelik tedavidir • Biyoteknolojik olarak üretilenler: . . mab. • Monoklonal antikor. . omab • Murine origine. . ximab • Chimeric antikor. . zumab • Humanized antikor. . cept • Rekombinan derived fusion. . inib • inhibitör. . imob • immunomodülatör. . umab • Completely human antikor

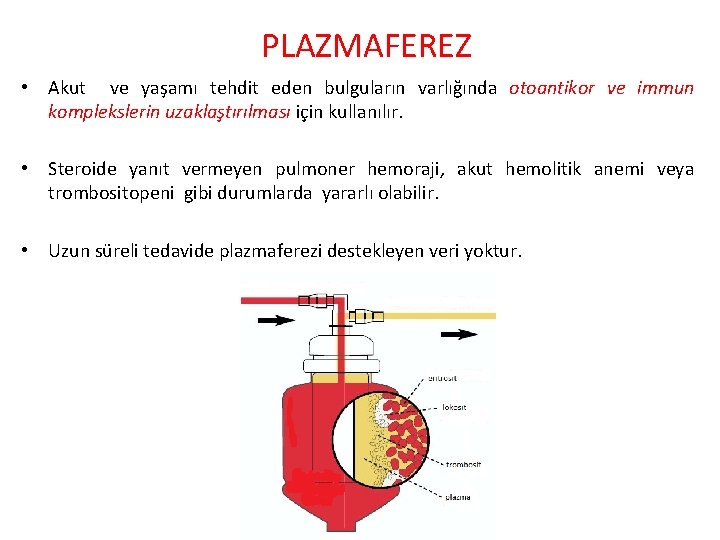
PLAZMAFEREZ • Akut ve yaşamı tehdit eden bulguların varlığında otoantikor ve immun komplekslerin uzaklaştırılması için kullanılır. • Steroide yanıt vermeyen pulmoner hemoraji, akut hemolitik anemi veya trombositopeni gibi durumlarda yararlı olabilir. • Uzun süreli tedavide plazmaferezi destekleyen veri yoktur.

İNTRAVENÖZ İMMUNGLOBULİN (İVİG) • SLE tedavisinde İVİG kullanımını destekleyen veri yoktur. • Sitopenilerin tedavisinde geçici yanıt alınabilir. • Hastalığın seyrini değiştirmemektedir.



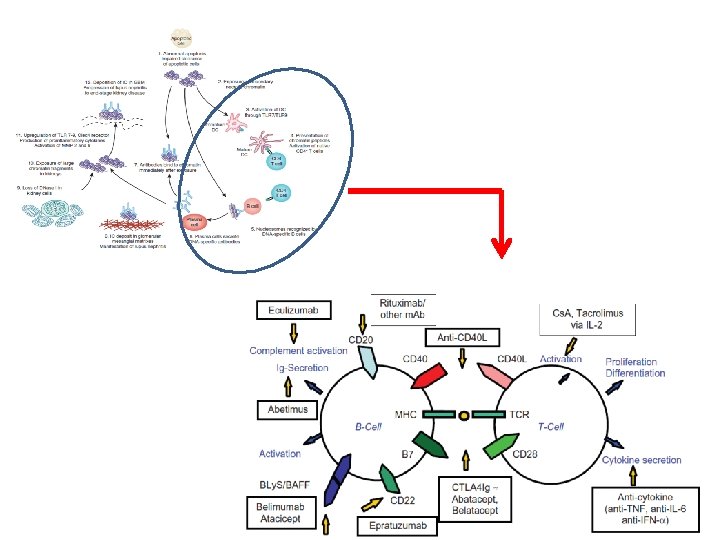
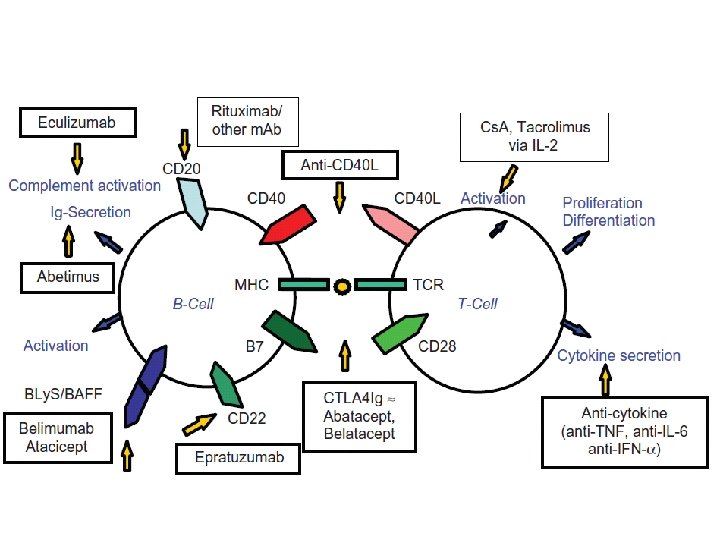
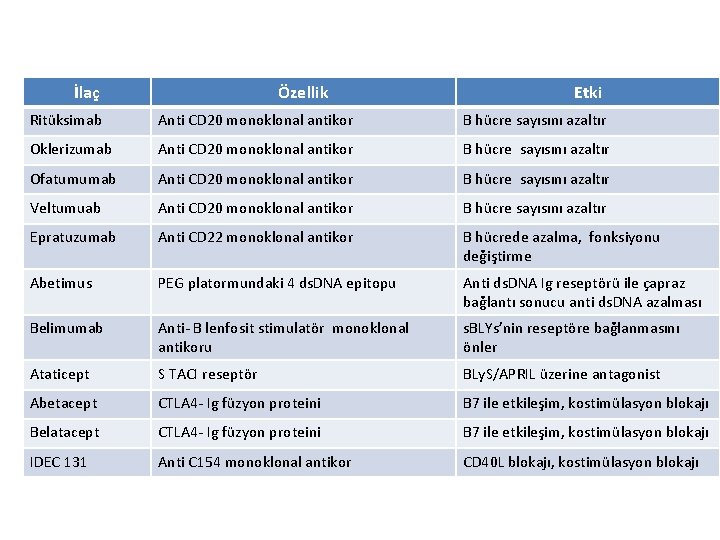
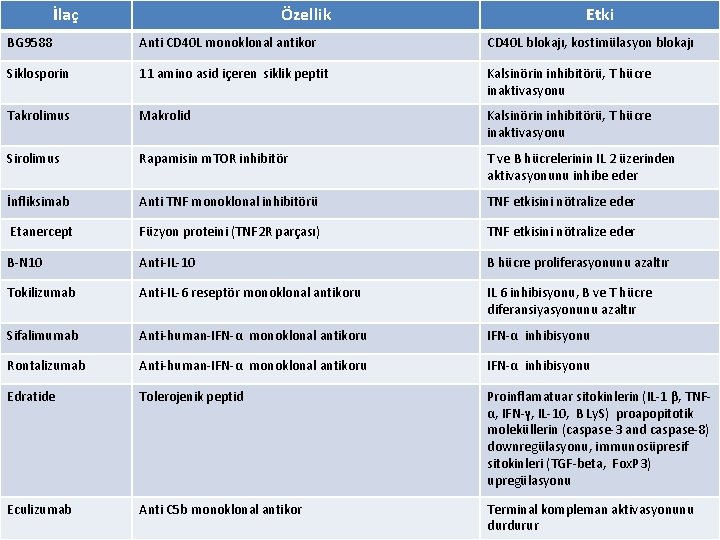
İlaç Özellik Etki Ritüksimab Anti CD 20 monoklonal antikor B hücre sayısını azaltır Oklerizumab Anti CD 20 monoklonal antikor B hücre sayısını azaltır Ofatumumab Anti CD 20 monoklonal antikor B hücre sayısını azaltır Veltumuab Anti CD 20 monoklonal antikor B hücre sayısını azaltır Epratuzumab Anti CD 22 monoklonal antikor B hücrede azalma, fonksiyonu değiştirme Abetimus PEG platormundaki 4 ds. DNA epitopu Anti ds. DNA Ig reseptörü ile çapraz bağlantı sonucu anti ds. DNA azalması Belimumab Anti- B lenfosit stimulatör monoklonal antikoru s. BLYs’nin reseptöre bağlanmasını önler Ataticept S TACI reseptör BLy. S/APRIL üzerine antagonist Abetacept CTLA 4 - Ig füzyon proteini B 7 ile etkileşim, kostimülasyon blokajı Belatacept CTLA 4 - Ig füzyon proteini B 7 ile etkileşim, kostimülasyon blokajı IDEC 131 Anti C 154 monoklonal antikor CD 40 L blokajı, kostimülasyon blokajı

İlaç Özellik Etki BG 9588 Anti CD 40 L monoklonal antikor CD 40 L blokajı, kostimülasyon blokajı Siklosporin 11 amino asid içeren siklik peptit Kalsinörin inhibitörü, T hücre inaktivasyonu Takrolimus Makrolid Kalsinörin inhibitörü, T hücre inaktivasyonu Sirolimus Rapamisin m. TOR inhibitör T ve B hücrelerinin IL 2 üzerinden aktivasyonunu inhibe eder İnfliksimab Anti TNF monoklonal inhibitörü TNF etkisini nötralize eder Etanercept Füzyon proteini (TNF 2 R parçası) TNF etkisini nötralize eder B-N 10 Anti-IL-10 B hücre proliferasyonunu azaltır Tokilizumab Anti-IL-6 reseptör monoklonal antikoru IL 6 inhibisyonu, B ve T hücre diferansiyasyonunu azaltır Sifalimumab Anti-human-IFN-α monoklonal antikoru IFN-α inhibisyonu Rontalizumab Anti-human-IFN-α monoklonal antikoru IFN-α inhibisyonu Edratide Tolerojenik peptid Proinflamatuar sitokinlerin (IL-1 β, TNFα, IFN-γ, IL-10, B Ly. S) proapopitotik moleküllerin (caspase-3 and caspase-8) downregülasyonu, immunosüpresif sitokinleri (TGF-beta, Fox. P 3) upregülasyonu Eculizumab Anti C 5 b monoklonal antikor Terminal kompleman aktivasyonunu durdurur

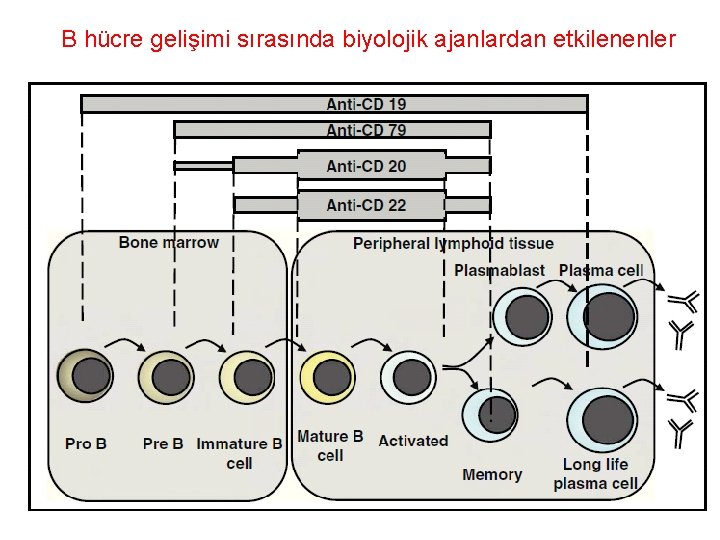
B hücre gelişimi sırasında biyolojik ajanlardan etkilenenler

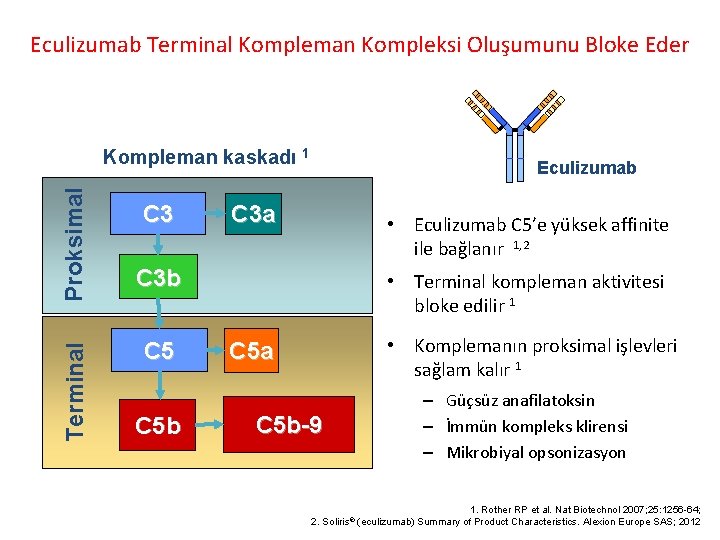
Eculizumab Terminal Kompleman Kompleksi Oluşumunu Bloke Eder Terminal Proksimal Kompleman kaskadı 1 C 3 Eculizumab C 3 a • Eculizumab C 5’e yüksek affinite ile bağlanır 1, 2 C 3 b C 5 b • Terminal kompleman aktivitesi bloke edilir 1 • Komplemanın proksimal işlevleri sağlam kalır 1 C 5 a C 5 b-9 – Güçsüz anafilatoksin – İmmün kompleks klirensi – Mikrobiyal opsonizasyon 1. Rother RP et al. Nat Biotechnol 2007; 25: 1256 -64; 2. Soliris® (eculizumab) Summary of Product Characteristics. Alexion Europe SAS; 2012

Kompleman yetersizliğine sekonder SLE de tedavi • C 1 q yetersizliğine sekonder SLE olgularında düzenli taze donmuş plazma infüzyonu ile yeterli yanıt alınmıştır. • Topaloglu R, et al. C 1 q deficiency: identification of a novel missense mutation and treatment with fresh frozen plasma. Clin Rheumatol. 2012 • Hematopoetik kök hücre transplantasyonu ile başarılı sonuç alınan C 1 q yetmezliğine bağlı SLE rapor edilmiştir. • Arkwright PD, et al. Successful cure of C 1 q deficiency in human subjects treated with hematopoietic stem cell transplantation. J Allergy Clin Immunol. 2014

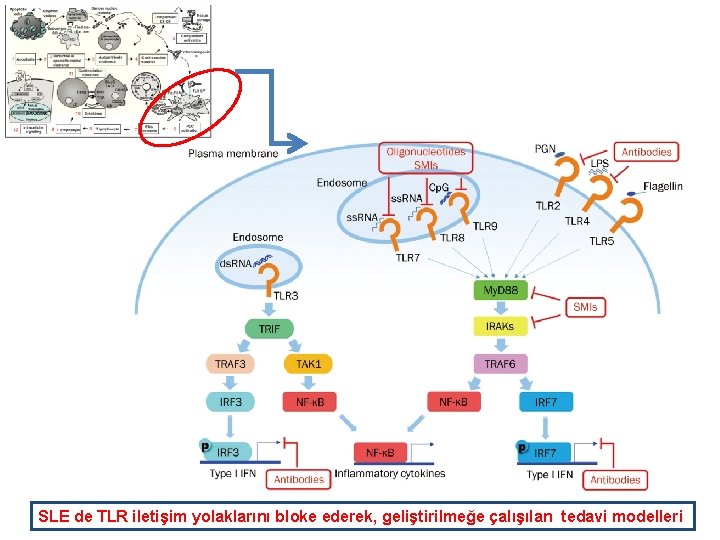
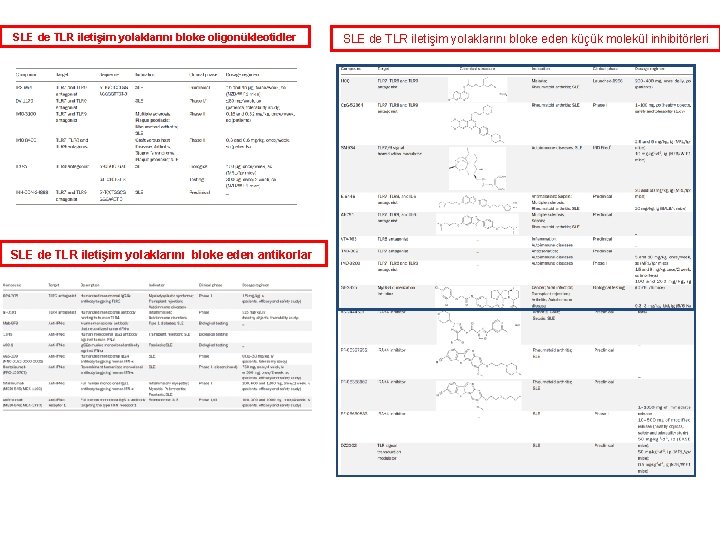
SLE de TLR iletişim yolaklarını bloke ederek, geliştirilmeğe çalışılan tedavi modelleri

SLE de TLR iletişim yolaklarını bloke oligonükleotidler SLE de TLR iletişim yolaklarını bloke eden antikorlar SLE de TLR iletişim yolaklarını bloke eden küçük molekül inhibitörleri

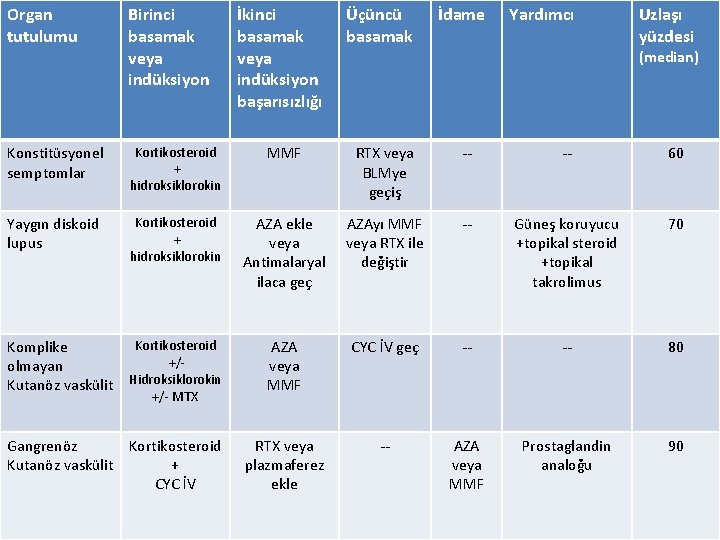
Organ tutulumu Birinci basamak veya indüksiyon Konstitüsyonel semptomlar Kortikosteroid + hidroksiklorokin MMF RTX veya BLMye geçiş -- -- 60 Yaygın diskoid lupus Kortikosteroid + hidroksiklorokin AZA ekle veya Antimalaryal ilaca geç AZAyı MMF veya RTX ile değiştir -- Güneş koruyucu +topikal steroid +topikal takrolimus 70 Kortikosteroid Komplike +/olmayan Kutanöz vaskülit Hidroksiklorokin AZA veya MMF CYC İV geç -- -- 80 Gangrenöz Kortikosteroid Kutanöz vaskülit + CYC İV RTX veya plazmaferez ekle -- AZA veya MMF Prostaglandin analoğu 90 +/- MTX İkinci basamak veya indüksiyon başarısızlığı Üçüncü basamak İdame Yardımcı Uzlaşı yüzdesi (median)

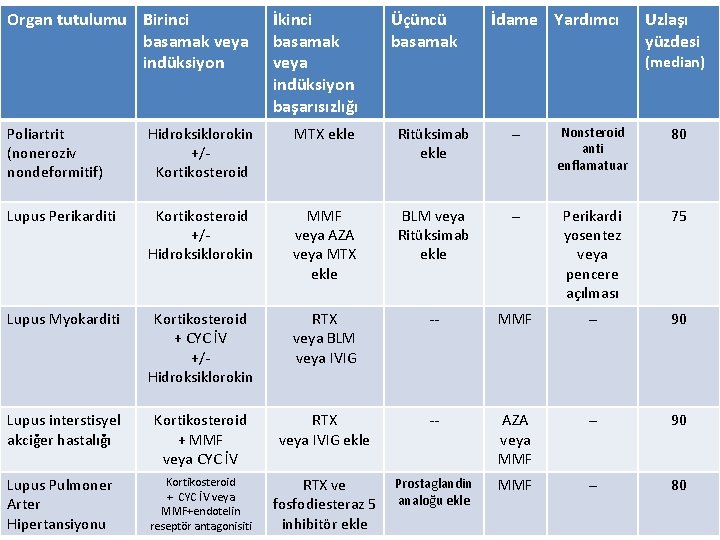
Organ tutulumu Birinci basamak veya indüksiyon İkinci basamak veya indüksiyon başarısızlığı Üçüncü basamak İdame Yardımcı Uzlaşı yüzdesi (median) Poliartrit (noneroziv nondeformitif) Hidroksiklorokin +/Kortikosteroid MTX ekle Ritüksimab ekle -- Nonsteroid anti enflamatuar 80 Lupus Perikarditi Kortikosteroid +/Hidroksiklorokin MMF veya AZA veya MTX ekle BLM veya Ritüksimab ekle -- Perikardi yosentez veya pencere açılması 75 Lupus Myokarditi Kortikosteroid + CYC İV +/Hidroksiklorokin RTX veya BLM veya IVIG -- MMF -- 90 Lupus interstisyel akciğer hastalığı Kortikosteroid + MMF veya CYC İV RTX veya IVIG ekle -- AZA veya MMF -- 90 Kortikosteroid + CYC İV veya MMF+endotelin reseptör antagonisiti RTX ve fosfodiesteraz 5 inhibitör ekle Prostaglandin analoğu ekle MMF -- 80 Lupus Pulmoner Arter Hipertansiyonu

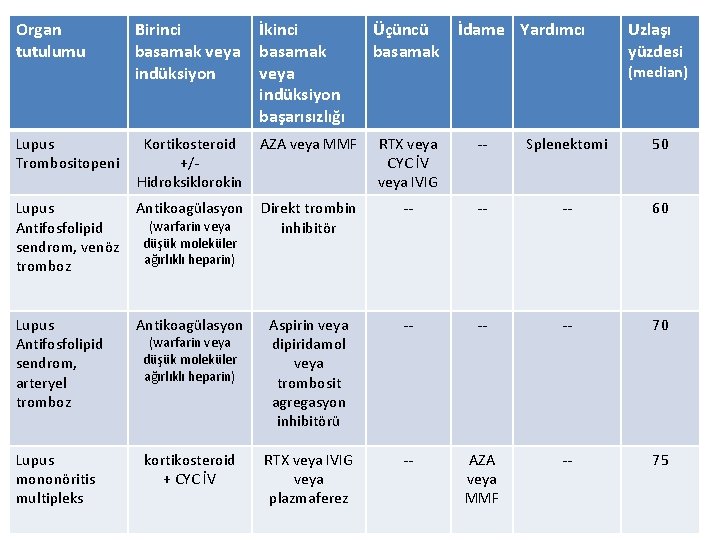
Organ tutulumu Birinci basamak veya indüksiyon İkinci basamak veya indüksiyon başarısızlığı Lupus Trombositopeni Kortikosteroid +/Hidroksiklorokin AZA veya MMF RTX veya CYC İV veya IVIG -- Splenektomi 50 Lupus Antifosfolipid sendrom, venöz tromboz Antikoagülasyon Direkt trombin inhibitör -- -- -- 60 Lupus Antifosfolipid sendrom, arteryel tromboz Antikoagülasyon Aspirin veya dipiridamol veya trombosit agregasyon inhibitörü -- -- -- 70 Lupus mononöritis multipleks kortikosteroid + CYC İV RTX veya IVIG veya plazmaferez -- AZA veya MMF -- 75 (warfarin veya düşük moleküler ağırlıklı heparin) Üçüncü basamak İdame Yardımcı Uzlaşı yüzdesi (median)

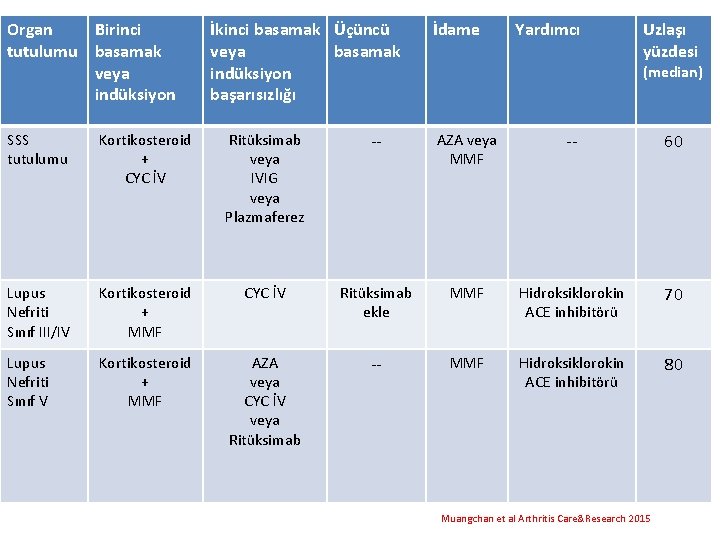
Organ Birinci tutulumu basamak veya indüksiyon İkinci basamak Üçüncü veya basamak indüksiyon başarısızlığı İdame Yardımcı Uzlaşı yüzdesi (median) SSS tutulumu Kortikosteroid + CYC İV Ritüksimab veya IVIG veya Plazmaferez -- AZA veya MMF -- 60 Lupus Nefriti Sınıf III/IV Kortikosteroid + MMF CYC İV Ritüksimab ekle MMF Hidroksiklorokin ACE inhibitörü 70 Lupus Nefriti Sınıf V Kortikosteroid + MMF AZA veya CYC İV veya Ritüksimab -- MMF Hidroksiklorokin ACE inhibitörü 80 Muangchan et al Arthritis Care&Research 2015

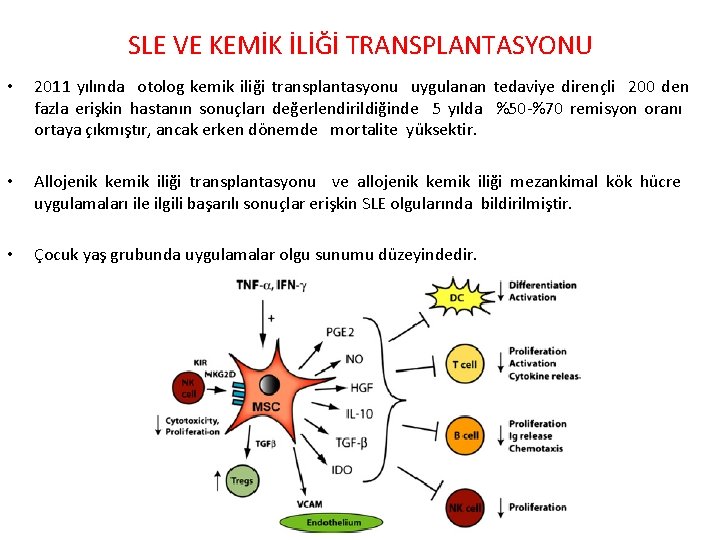
SLE VE KEMİK İLİĞİ TRANSPLANTASYONU • 2011 yılında otolog kemik iliği transplantasyonu uygulanan tedaviye dirençli 200 den fazla erişkin hastanın sonuçları değerlendirildiğinde 5 yılda %50 -%70 remisyon oranı ortaya çıkmıştır, ancak erken dönemde mortalite yüksektir. • Allojenik kemik iliği transplantasyonu ve allojenik kemik iliği mezankimal kök hücre uygulamaları ile ilgili başarılı sonuçlar erişkin SLE olgularında bildirilmiştir. • Çocuk yaş grubunda uygulamalar olgu sunumu düzeyindedir.

Ağır renal tutulumda SLE prognozu • STEROİD-SİKLOFOSFAMİD-AZATİOPURİN ÖNCESİ • Ağır lupus nefritli olgularda 2 yıllık yaşam oranı %50 (1954) • STEROİD-SİKLOFOSFAMİD-AZATİOPURİN SONRASI • Ağır lupus nefritli olgularda 10 yıllık yaşam oranı %90 (1994) • Ağır lupus nefritli olgularda 15 yıllık yaşam oranı %90 (2002)

İndüksiyon tedavi süresi nedir? • EULAR/ERA–EDTA lupus nefritinde kısmi veya tam yanıt için beklenecek sürenin indüksiyon tedavisinden sonra 6 -12 ay olmasını, 24 ayda tam remisyona ulaşmanın hedeflenmesini önermektedir. • İlk 3 -4 ay içinde tedaviye yanıt izlenmezse, immunosupresif ajanlar değişitrilebilir veya biyolojik tedavi eklenebilir. • Rebiyopsi düşünülebilir. Bertsias, G. K. et al. Joint European League Against Rheumatism and European Renal Association– European Dialysis and Transplant Association (EULAR/ ERA–EDTA) recommendations for the management of adult and paediatric lupus nephritis. Ann. Rheum. Dis. (2012).

İdame tedavi süresi nedir? • Optimal idame tedavi süresi bilinmemektedir. • EULAR/ERA-EDTA indüksiyon tedavisme yanıt verenler için en az 3 yıllık idame tedavi süresi önermektedir. Böbrek fonksiyonları için riskin yüksek olduğu hastalarda : Afrikalı Amerikalılar, Hispanikler, Gençler Erkekler İndüksiyon tedavisi sonrası tam remisyona girmeyen (proteinüri veya aktif lupus serolojisi sürenler ) Böbrek biyopsisinde kresentleri olanlar (kronisite indeksi nden bağımsız)) Sık nüks edenler idame immunosüpresyon tedavisini uzatmak gerekmektedir. • Bertsias, G. K. et al. Joint European League Against Rheumatism and European Renal Association– European Dialysis and Transplant Association (EULAR/ ERA–EDTA) recommendations for the management of adult and paediatric lupus nephritis. Ann. Rheum. Dis. (2012).

LUPUS NEFRİTİ TEDAVİSİ • Class III ve IV nefropatiler (proliferatif) tedavi edilmezse son dönem böbrek hastalığı ve mortalite oranı yüksektir. • 1970 -1980 ler: “National Institute of Health (NIH)” önerisi: IV siklofosfamid, daha sonraları IV siklofosfamid + kortikosteroid • The Euro-Lupus Nephritis Trial (ELNT): Düşük doz IV siklofosfamidin, yüksek doz ve uzun süreli siklofosfamid tedavisine (NIH önerisine) üstün olduğunu bildirdi. • Son 10 yılda indüksiyon ve idame tedavilerinde MMF in daha düşük yan etki oranları ile CYC e eş değerde veya daha üstün olduğu erişkinlerde kanıtlanmıştır. • “ The MAINTAIN Nephritis Trial “ MMF ve AZA nın uzun süreli idame tedavisinde nüks, hastalık aktivitesi, böbrek fonksiyonları açısından etkinliğinin benzer olduğunu, ancak MMF de anemi ve lökopeninin daha az oranda ortaya çıktığını göstermiştir.

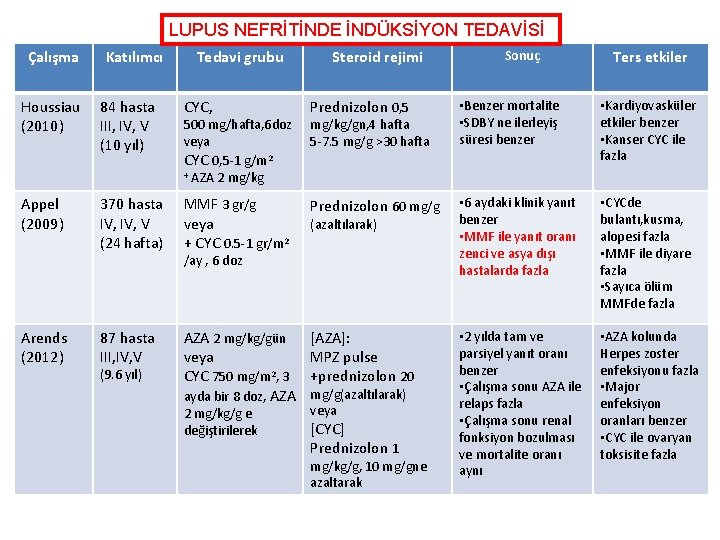
LUPUS NEFRİTİNDE İNDÜKSİYON TEDAVİSİ Çalışma Katılımcı Tedavi grubu Steroid rejimi Sonuç Ters etkiler Houssiau (2010) 84 hasta III, IV, V (10 yıl) CYC, Prednizolon 0, 5 • Benzer mortalite • SDBY ne ilerleyiş süresi benzer • Kardiyovasküler etkiler benzer • Kanser CYC ile fazla Appel (2009) 370 hasta IV, V (24 hafta) MMF 3 gr/g veya + CYC 0. 5 -1 gr/m 2 Prednizolon 60 mg/g • 6 aydaki klinik yanıt benzer • MMF ile yanıt oranı zenci ve asya dışı hastalarda fazla • CYCde bulantı, kusma, alopesi fazla • MMF ile diyare fazla • Sayıca ölüm MMFde fazla 87 hasta III, IV, V AZA 2 mg/kg/gün veya CYC 750 mg/m 2, 3 ayda bir 8 doz, AZA [AZA]: MPZ pulse +prednizolon 20 • 2 yılda tam ve parsiyel yanıt oranı benzer • Çalışma sonu AZA ile relaps fazla • Çalışma sonu renal fonksiyon bozulması ve mortalite oranı aynı • AZA kolunda Herpes zoster enfeksiyonu fazla • Major enfeksiyon oranları benzer • CYC ile ovaryan toksisite fazla Arends (2012) (9. 6 yıl) 500 mg/hafta, 6 doz veya CYC 0, 5 -1 g/m 2 + AZA 2 mg/kg/gn, 4 hafta 5 -7. 5 mg/g >30 hafta (azaltılarak) /ay , 6 doz 2 mg/kg/g e değiştirilerek mg/g(azaltılarak) veya [CYC] Prednizolon 1 mg/kg/g, 10 mg/gne azaltarak

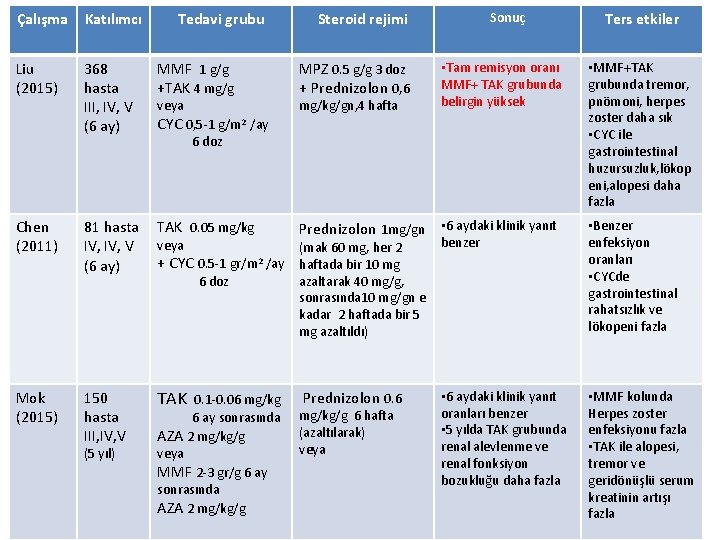
Çalışma Katılımcı Liu (2015) 368 hasta III, IV, V (6 ay) MMF 1 g/g +TAK 4 mg/g 81 hasta IV, V (6 ay) TAK 0. 05 mg/kg 150 hasta III, IV, V TAK Chen (2011) Mok (2015) (5 yıl) Tedavi grubu veya CYC 0, 5 -1 g/m 2 /ay Steroid rejimi MPZ 0. 5 g/g 3 doz + Prednizolon 0, 6 mg/kg/gn, 4 hafta Sonuç • Tam remisyon oranı MMF+ TAK grubunda belirgin yüksek 6 doz veya + CYC 0. 5 -1 gr/m 2 /ay 6 doz 0. 1 -0. 06 mg/kg 6 ay sonrasında AZA 2 mg/kg/g veya MMF 2 -3 gr/g 6 ay sonrasında AZA 2 mg/kg/g Prednizolon 1 mg/gn • 6 aydaki klinik yanıt (mak 60 mg, her 2 haftada bir 10 mg azaltarak 40 mg/g, sonrasında 10 mg/gn e kadar 2 haftada bir 5 mg azaltıldı) benzer Prednizolon 0. 6 • 6 aydaki klinik yanıt oranları benzer • 5 yılda TAK grubunda renal alevlenme ve renal fonksiyon bozukluğu daha fazla mg/kg/g 6 hafta (azaltılarak) veya Ters etkiler • MMF+TAK grubunda tremor, pnömoni, herpes zoster daha sık • CYC ile gastrointestinal huzursuzluk, lökop eni, alopesi daha fazla • Benzer enfeksiyon oranları • CYCde gastrointestinal rahatsızlık ve lökopeni fazla • MMF kolunda Herpes zoster enfeksiyonu fazla • TAK ile alopesi, tremor ve geridönüşlü serum kreatinin artışı fazla

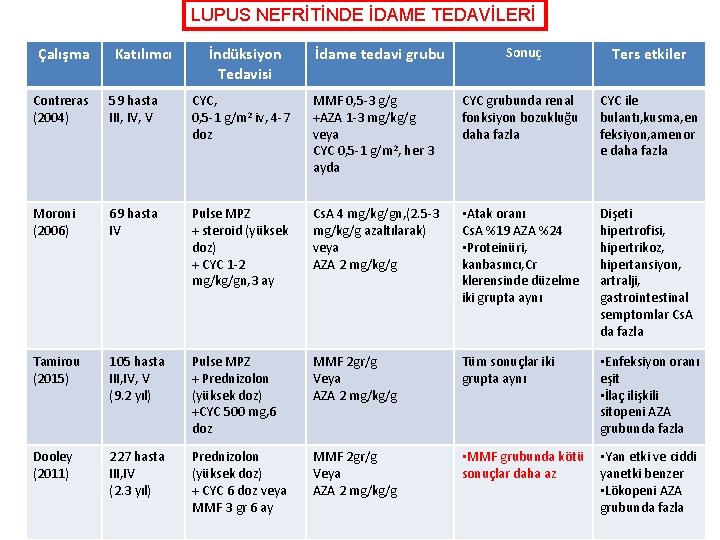
LUPUS NEFRİTİNDE İDAME TEDAVİLERİ Çalışma Katılımcı İndüksiyon Tedavisi İdame tedavi grubu Sonuç Ters etkiler Contreras (2004) 59 hasta III, IV, V CYC, 0, 5 -1 g/m 2 iv, 4 -7 doz MMF 0, 5 -3 g/g +AZA 1 -3 mg/kg/g veya CYC 0, 5 -1 g/m 2, her 3 ayda CYC grubunda renal fonksiyon bozukluğu daha fazla CYC ile bulantı, kusma, en feksiyon, amenor e daha fazla Moroni (2006) 69 hasta IV Pulse MPZ + steroid (yüksek doz) + CYC 1 -2 mg/kg/gn, 3 ay Cs. A 4 mg/kg/gn, (2. 5 -3 mg/kg/g azaltılarak) veya AZA 2 mg/kg/g • Atak oranı Cs. A %19 AZA %24 • Proteinüri, kanbasıncı, Cr klerensinde düzelme iki grupta aynı Dişeti hipertrofisi, hipertrikoz, hipertansiyon, artralji, gastrointestinal semptomlar Cs. A da fazla Tamirou (2015) 105 hasta III, IV, V (9. 2 yıl) Pulse MPZ + Prednizolon (yüksek doz) +CYC 500 mg, 6 doz MMF 2 gr/g Veya AZA 2 mg/kg/g Tüm sonuçlar iki grupta aynı • Enfeksiyon oranı eşit • İlaç ilişkili sitopeni AZA grubunda fazla Dooley (2011) 227 hasta III, IV (2. 3 yıl) Prednizolon (yüksek doz) + CYC 6 doz veya MMF 3 gr 6 ay MMF 2 gr/g Veya AZA 2 mg/kg/g • MMF grubunda kötü sonuçlar daha az • Yan etki ve ciddi yanetki benzer • Lökopeni AZA grubunda fazla

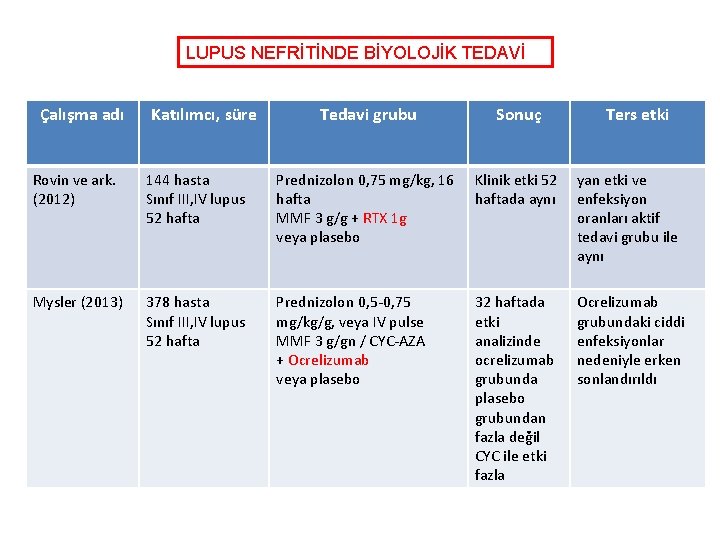
LUPUS NEFRİTİNDE BİYOLOJİK TEDAVİ Çalışma adı Katılımcı, süre Tedavi grubu Sonuç Ters etki Rovin ve ark. (2012) 144 hasta Sınıf III, IV lupus 52 hafta Prednizolon 0, 75 mg/kg, 16 hafta MMF 3 g/g + RTX 1 g veya plasebo Klinik etki 52 haftada aynı yan etki ve enfeksiyon oranları aktif tedavi grubu ile aynı Mysler (2013) 378 hasta Sınıf III, IV lupus 52 hafta Prednizolon 0, 5 -0, 75 mg/kg/g, veya IV pulse MMF 3 g/gn / CYC-AZA + Ocrelizumab veya plasebo 32 haftada etki analizinde ocrelizumab grubunda plasebo grubundan fazla değil CYC ile etki fazla Ocrelizumab grubundaki ciddi enfeksiyonlar nedeniyle erken sonlandırıldı

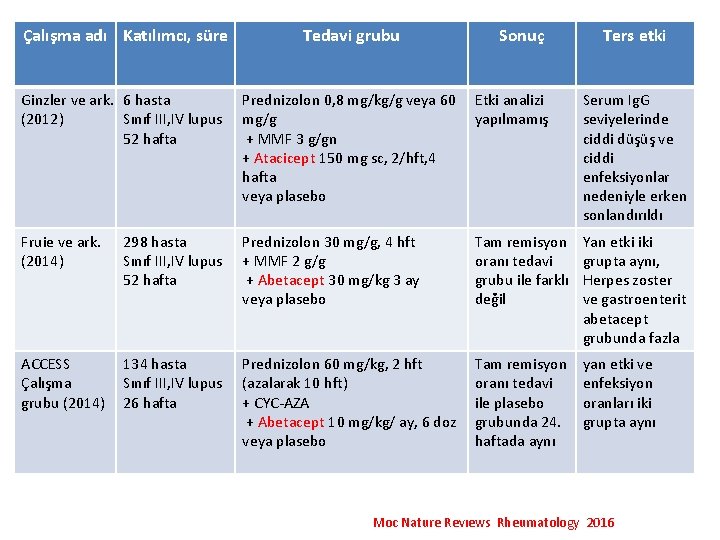
Çalışma adı Katılımcı, süre Tedavi grubu Sonuç Ters etki Ginzler ve ark. 6 hasta (2012) Sınıf III, IV lupus 52 hafta Prednizolon 0, 8 mg/kg/g veya 60 mg/g + MMF 3 g/gn + Atacicept 150 mg sc, 2/hft, 4 hafta veya plasebo Etki analizi yapılmamış Serum Ig. G seviyelerinde ciddi düşüş ve ciddi enfeksiyonlar nedeniyle erken sonlandırıldı Fruie ve ark. (2014) 298 hasta Sınıf III, IV lupus 52 hafta Prednizolon 30 mg/g, 4 hft + MMF 2 g/g + Abetacept 30 mg/kg 3 ay veya plasebo Tam remisyon oranı tedavi grubu ile farklı değil Yan etki iki grupta aynı, Herpes zoster ve gastroenterit abetacept grubunda fazla ACCESS Çalışma grubu (2014) 134 hasta Sınıf III, IV lupus 26 hafta Prednizolon 60 mg/kg, 2 hft (azalarak 10 hft) + CYC-AZA + Abetacept 10 mg/kg/ ay, 6 doz veya plasebo Tam remisyon oranı tedavi ile plasebo grubunda 24. haftada aynı yan etki ve enfeksiyon oranları iki grupta aynı Moc Nature Revıews Rheumatology 2016

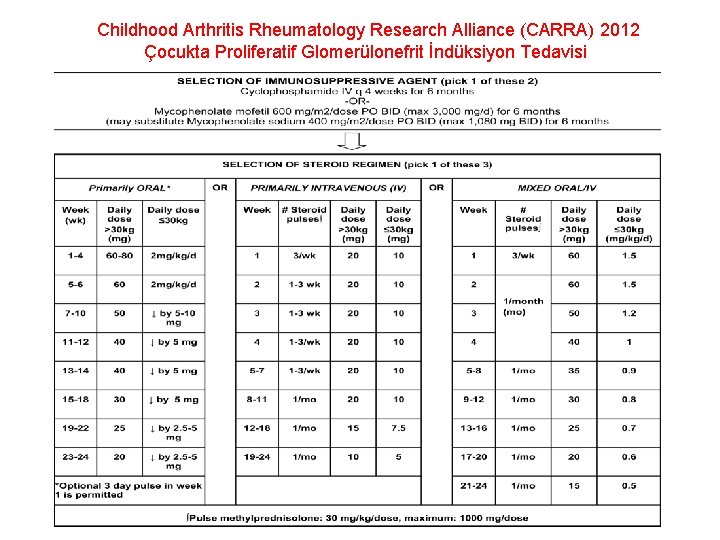
Childhood Arthritis Rheumatology Research Alliance (CARRA) 2012 Çocukta Proliferatif Glomerülonefrit İndüksiyon Tedavisi

• “The Childhood Arthritis Rheumatology Research Alliance“ ın pediatrik SLE popülasyonuna spesifik, yeni tanı almış proliferatif lupus nefriti için önerisi: • İlk 6 ay: İndüksiyon tedavi planı : Siklofosfamid veya mikofenolat mofetil standart kortikosteroid tedavisi ile birlikte kullanılacaktır. İlk 6 ay içinde parsiyel yanıt alınamaz ise, kullanılan ilaç (siklofosfamid veya mikofenolat mofetil ‘den biri ) kesilip, diğeri başlanarak tedavi sürdürülecektir. • Sonraki 12 ay: İdame tedavi: İndüksiyon tedavisi tamamlandıktan sonra mikofenolat mofetil, her 3 ayda bir kez İV siklofosfamid veya azatiopurin 12 ay süre ile önerilmektedir.

B hücrelerini hedef alan ilaçlar • • RİTUXİMAB CD 20 hedefleyen antikorlar • EXPLORER Çalışmasında 237 hasta orta ve ağır derecede böbrek dışı tutulumu olan SLE nedeni ile rituximab (1000 mg , 1, 15, 168, ve 182. günlerde) ve plasebo kullanıyorlar. Hastaların kullandıkları tedavi azathioprine, MMF or methotrexate ve prednisolone (0. 5– 1. 0 mg/kg tedricen azaltılıyor). Plasebo ile Rituximab gruplarında klinik yanıt (BILAG skoruna göre değerlendiriliyor) sırası ile % 15. 9 ve % 12. 4 olup, anlamlı fark yok. Rituximab grubunda B hücre sayısı ve anti-Ds DNA antikorları geriliyor, ve C 3 ve C 4 normal düzeye ulaşıyor. • • LUNAR Çalışmasında 144 hastada class III-IV histopatoloji bulguları olan SLE nedeni ile tedavi edilirken (MMF ve prednisolon), rituximab (1000 mg , 1, 15, 168, ve 182. günlerde) ve plasebo kullanıyorlar. Plasebo ile Rituximab gruplarında klinik yanıt sırası ile % 30. 6 ve % 25. 4 olup, anlamlı fark yok. Rituximab grubunda anti-Ds DNA antikorları gerilimesi ve normal düzeye ulaşan kompleman oranları plasebo grubuna göre anlamlı olarak yüksek bulunuyor. ÇOCUKLARDA GEREKİRSE KULLANILABİLİR

Lupus nefriti son dönem böbrek hastalığı olursa: • Diyalizden önce transplantasyon yapılırsa, hasta ve graft yaşam süresi artar, böbrek dışı lupus aktivitesi düzelir. • Lupus nefriti nedeni ile diyaliz uygulanan çocuklarda diğer nedenlerden son dönem böbrek hastalığı olup da diyaliz uygulanan çocuklara göre ölüm riski iki kattan daha fazladır. • Transplantasyon öncesinde SLE li çocukların 6 -12 ay remisyonda kalması önerilmektedir. • Transplantasyon sonrasında SLE nüks oranı %2 -%30 olarak bildirilmektedir. Nüks hafif şiddettedir. Çocuğun ömrünü kısaltmaz, ancak graft kaybı için risk oluşturur. • Son dönem böbrek hastalığı sırasında Afrika kökenli Amerikalı çocuklarda ölüm riski beyaz ırk çocuklarına göre iki kat yüksektir. • Lupus nefriti olan çocuklarda son dönem böbrek hastalığı öncesinde ve sonrasında ölüm nedeni infeksiyon ve kardiyovasküler komplikasyonlardır.

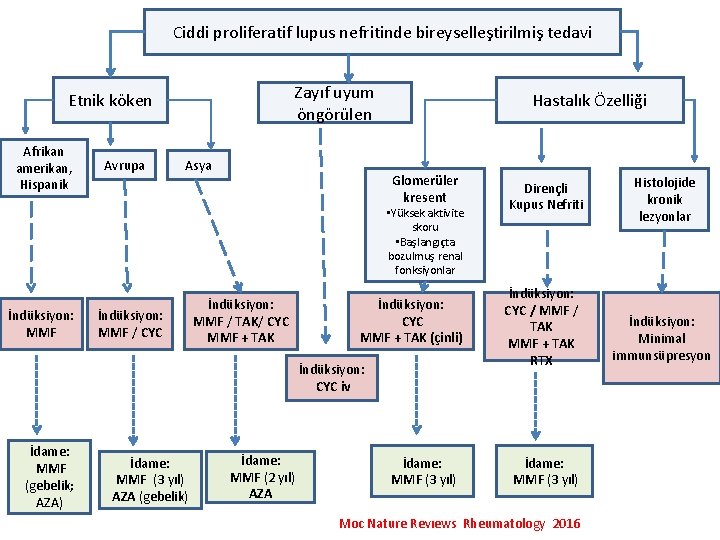
Ciddi proliferatif lupus nefritinde bireyselleştirilmiş tedavi Zayıf uyum öngörülen Etnik köken Afrikan amerikan, Hispanik Avrupa Asya Hastalık Özelliği Glomerüler kresent • Yüksek aktivite skoru • Başlangıçta bozulmuş renal fonksiyonlar İndüksiyon: MMF / CYC İndüksiyon: MMF / TAK/ CYC MMF + TAK İndüksiyon: CYC MMF + TAK (çinli) İndüksiyon: CYC iv İdame: MMF (gebelik; AZA) İdame: MMF (3 yıl) AZA (gebelik) İdame: MMF (2 yıl) AZA İdame: MMF (3 yıl) Dirençli Kupus Nefriti İndüksiyon: CYC / MMF / TAK MMF + TAK RTX İdame: MMF (3 yıl) Moc Nature Revıews Rheumatology 2016 Histolojide kronik lezyonlar İndüksiyon: Minimal immunsüpresyon

• SLE yaşam boyu süren bir hastalık olduğundan , çocuk ve adölesan hastalara optimal bakım hizmeti sırasında hastalıkla ilgili önlemler de sağlanmalıdır. • SLE de ateroskleroz riski arttığından kolesterol düzeyleri, sigara kullanımı, vücut kitle indeksi, kan basıncı ve diğer kardiyovasküler risk faktörlerine dikkat çekilmelidir. • Atherosclerosis Prevention in Pediatric Lupus Erythematosus (APPLE) çalışması SLE li çocuklarda statin uygulamasını desteklememiştir. Ancak, özellikle CRP yüksekliği olan pubertadaki SLE hastaları gibi belirli klinik durumlarda aterosklerozisden primer korunma sağlamak için statin gerekebilir. • Tüm hastalar yeterli D vitamini ve kalsiyum alarak gelecekteki osteoporozisden korunmalıdır. • İnfeksiyonlar SLE de önemli komplikasyonlardan olup, olgulara rutin aşılama programı önerilmelidir. Yıllık influenza aşılaması ve 23 türü kapsayan pnömokok aşısı bu çocuklara yapılmalıdır. • Ateşli olgulara dikkat edilmeli, ağır enfeksiyon açısından ayrıntılı bir şekilde değerlendirilmelidir. • Gebelik SLE nin seyrini kötüleştirebilir. Obstetrik komplikasyonlar SLE de sık olarak karşımıza çıkar. SLE tedavisinde kullanılan ilaçların çoğu teratojen özelliğe sahiptir. Adölesan kızlara bu durum anlatılmalı ve uygun kontrasepsiyon yöntemleri sunulmalıdır. • Antifosfolipid antikor sendromu olan SLE li hastalarda trombotik gelişmeleri önlemek için yaşam boyu antikoagülasyon uygulaması yapılır.