leri Evre Nonskuamoz KHDAK Sistemik Tedavisinde Gncel Yaklam


































- Slides: 72

İleri Evre Nonskuamoz KHDAK Sistemik Tedavisinde Güncel Yaklaşım Dr. Özden Altundağ Başkent Üniversitesi Medikal Onkoloji 14 Mayıs 2013

NSCLC-Evreye Göre Dağılım Scagliotti GV, JCO 2008

Akciğer Kanseri Subtipleri • WHO klasifikasyonu: 4 majör histolojik tip Diğer* %24. 0 Large-cell Ca %5 Small-cell %13 Adeno. Ca %38. 3 *Adenoskuamöz Ca, Pleomorfik, Sarkomatoid Ca, Karsinoid, Salivary gland tipi adenoca, Klasifiye edilemeyen Ca Skuamoz cell %19. 7 SEER Database, 2004

NSCLC Heterojenitesi Evre IV NSCLC hastaları 39 y, kadın never-smoker, adenoca EGFR Mt Yıl 2013: • Çoğu onkolog NSCLC nin tek hastalık olmadığı konusunda hemfikir • Çoğu onkolog bu hastaların farklı tedaviler alması konusunda hemfikir

NSCLC Heterogenitesi Evre IV NSCLC hastaları 65 y, erkek smoker, skuamöz KRAS Mt 39 y, kadın never-smoker, adenoca Yıl 2013: • Çoğu onkolog NSCLC nin tek hastalık olmadığı konusunda hemfikir • Çoğu onkolog bu hastaların farklı tedaviler alması konusunda hemfikir EGFR Mt

NSCLC Heterogenitesi Evre IV NSCLC hastaları 65 y, erkek smoker, skuamöz KRAS Mt 39 y, kadın never-smoker, adenoca 54 y, erkek never-smoker, adenoca ALK füzyon Yıl 2013: • Çoğu onkolog NSCLC nin tek hastalık olmadığı konusunda hemfikir • Çoğu onkolog bu hastaların farklı tedaviler alması konusunda hemfikir EGFR Mt

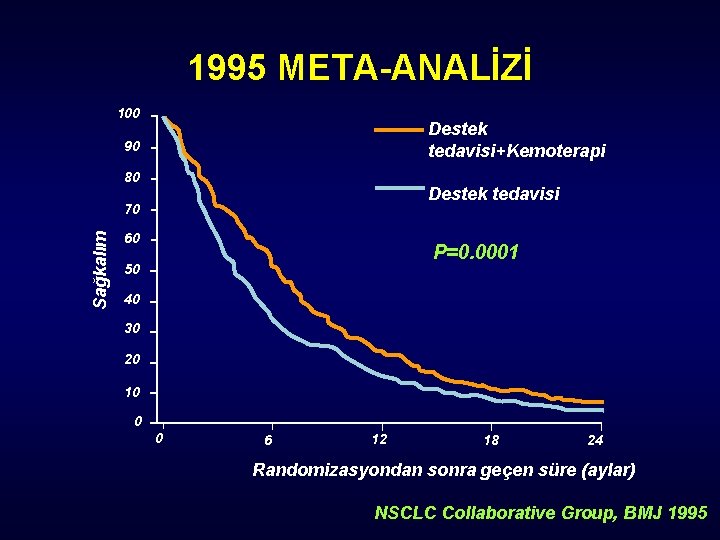
1995 META-ANALİZİ 100 Destek tedavisi+Kemoterapi 90 80 Destek tedavisi Sağkalım 70 60 P=0. 0001 50 40 30 20 10 0 0 6 12 18 24 Randomizasyondan sonra geçen süre (aylar) NSCLC Collaborative Group, BMJ 1995

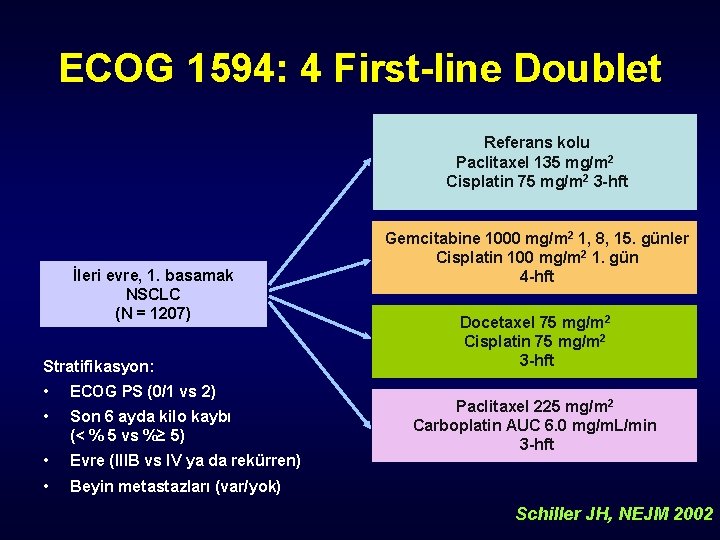
ECOG 1594: 4 First-line Doublet Referans kolu Paclitaxel 135 mg/m 2 Cisplatin 75 mg/m 2 3 -hft İleri evre, 1. basamak NSCLC (N = 1207) Stratifikasyon: • ECOG PS (0/1 vs 2) • Son 6 ayda kilo kaybı (< % 5 vs %≥ 5) • Evre (IIIB vs IV ya da rekürren) • Beyin metastazları (var/yok) Gemcitabine 1000 mg/m 2 1, 8, 15. günler Cisplatin 100 mg/m 2 1. gün 4 -hft Docetaxel 75 mg/m 2 Cisplatin 75 mg/m 2 3 -hft Paclitaxel 225 mg/m 2 Carboplatin AUC 6. 0 mg/m. L/min 3 -hft Schiller JH, NEJM 2002

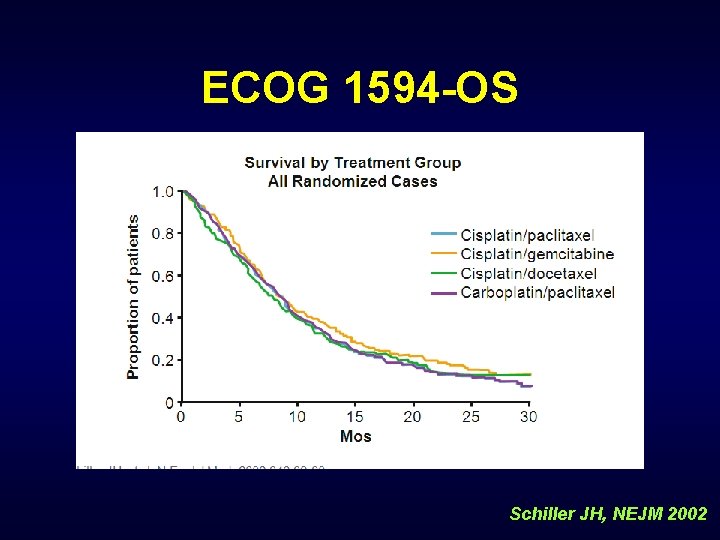
ECOG 1594 -OS Schiller JH, NEJM 2002

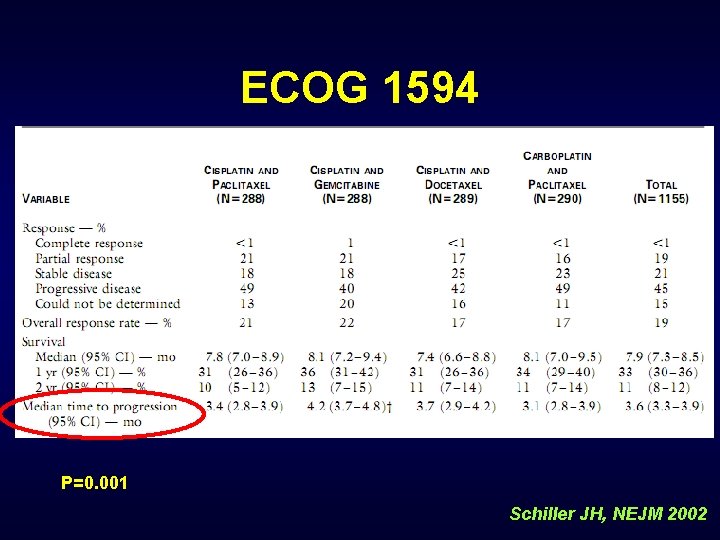
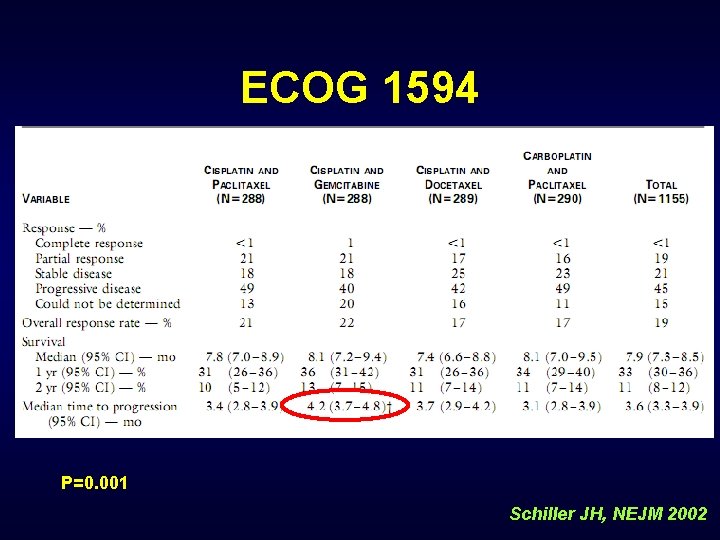
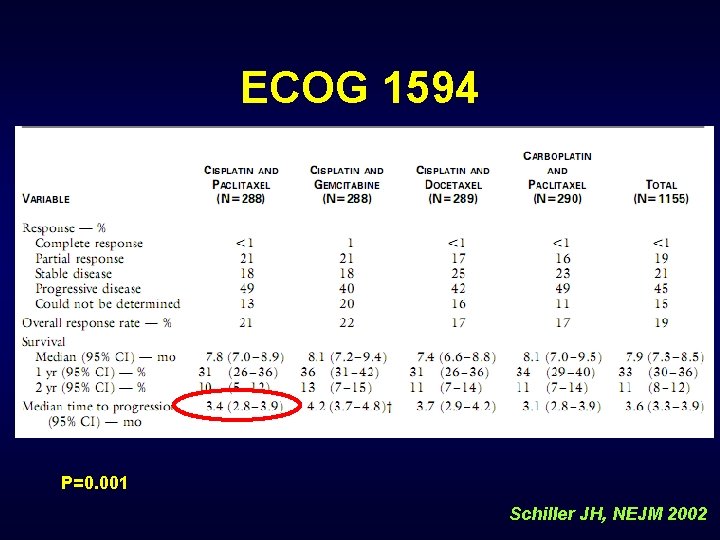
ECOG 1594 P=0. 001 Schiller JH, NEJM 2002

ECOG 1594 P=0. 001 Schiller JH, NEJM 2002

ECOG 1594 P=0. 001 Schiller JH, NEJM 2002

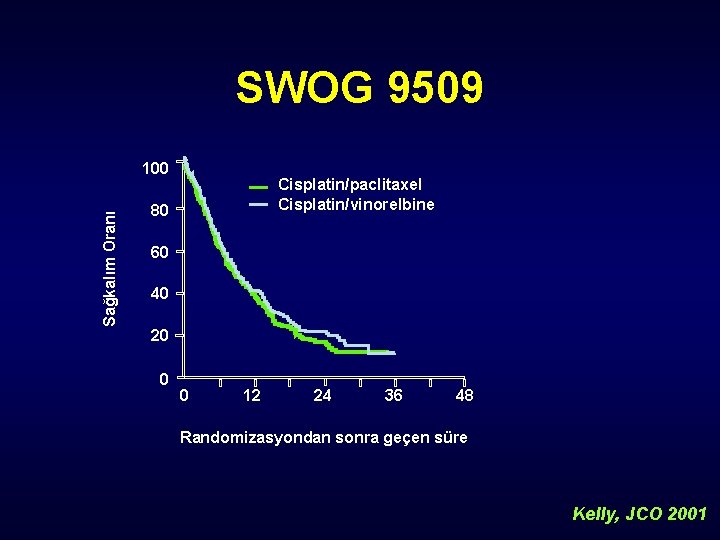
SWOG 9509 Sağkalım Oranı 100 Cisplatin/paclitaxel Cisplatin/vinorelbine 80 60 40 20 0 0 12 24 36 48 Randomizasyondan sonra geçen süre Kelly, JCO 2001

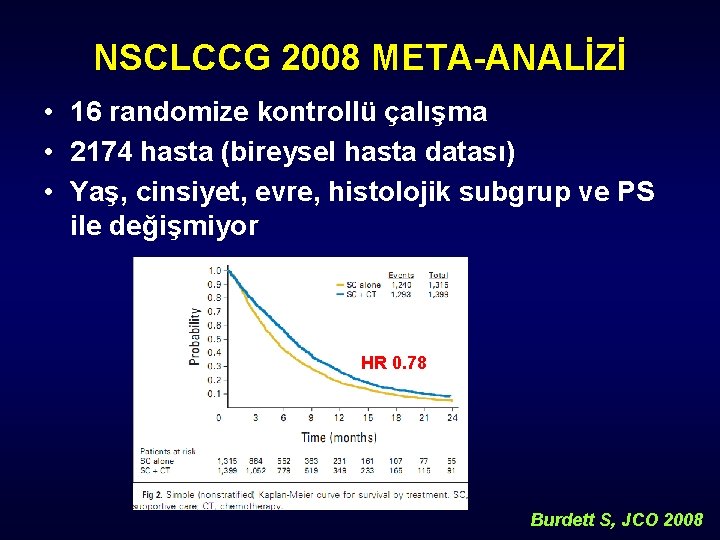
NSCLCCG 2008 META-ANALİZİ • 16 randomize kontrollü çalışma • 2174 hasta (bireysel hasta datası) • Yaş, cinsiyet, evre, histolojik subgrup ve PS ile değişmiyor HR 0. 78 Burdett S, JCO 2008

İleri Evre NSCLC 2013 Histoloji İdame Prediktif biyomarkerlar Gandara DR Clin Lung Cancer. 2009

Carboplatin Cisplatinden Daha Az mı Etkili? CISCA Meta-analiz • 2968 hasta (9 çalışma) Cis ya da Carbo randomize edilmiş. • RR: Cis > carbo (% 30 cis; % 24 carbo) • Overall survivalde anlamlı faklılık yok – Subgrup analiz: Survival: Cis > Carbo (3. jenerasyon ajanlarla kombine edildiğinde ve non-skuamöz histolojide) • Cisplatin-bazlı kemoterapi: Köşetaşı Ardizzoni et al, JNCI 2007

Hipotez: NSCLC Tedavisi Histoloji Bazlı Olmalıdır Pemetrexed ile skuamoz vs nonskuamoz histolojilerde farklı etkinlik – JMDB: 1. basamak tedavide Pemetrexed/cisplatin vs Gemcitabine/cisplatin[1] – JMEI: 2. basamak tedavide Pemetrexed vs docetaxel[2] – JMEN: İİdame tedavide Pemetrexed vs plasebo[3] 1. Scagliotti GV. J Clin Oncol. 2008 2. Otani S. Gan To Kagaku Ryoho. 2012 3. Greenhalgh J. Health Technol Assess. 2010; 14(suppl 2)

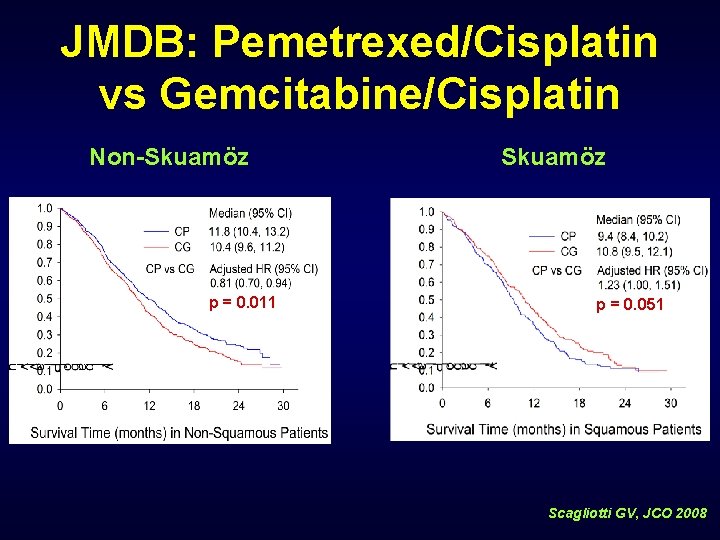
JMDB: Pemetrexed/Cisplatin vs Gemcitabine/Cisplatin PC Pemetrexed 500 mg/m 2 Cisplatin 75 mg/m 2 (n = 862) Evre IIIB / IV ECOG 0, 1 Kemonaive GC Gemcitabine 1250 mg/m 2 1, 8. Cisplatin 75 mg/m 2 (n = 863) Scagliotti GV, JCO 2008

JMDB: Pemetrexed/Cisplatin vs Gemcitabine/Cisplatin Non-Skuamöz p = 0. 011 Skuamöz p = 0. 051 Scagliotti GV, JCO 2008

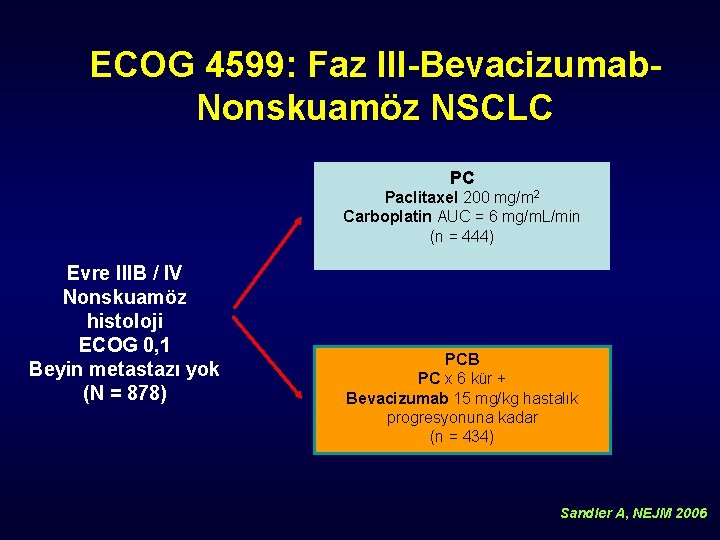
ECOG 4599: Faz III-Bevacizumab. Nonskuamöz NSCLC PC Paclitaxel 200 mg/m 2 Carboplatin AUC = 6 mg/m. L/min (n = 444) Evre IIIB / IV Nonskuamöz histoloji ECOG 0, 1 Beyin metastazı yok (N = 878) PCB PC x 6 kür + Bevacizumab 15 mg/kg hastalık progresyonuna kadar (n = 434) Sandler A, NEJM 2006

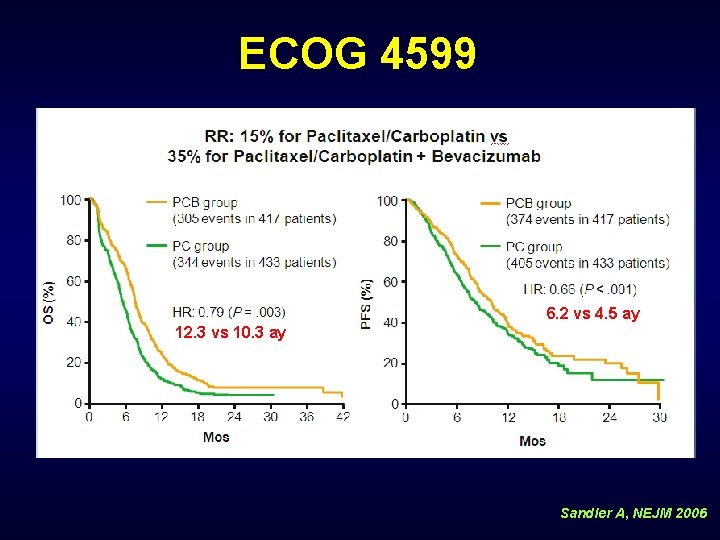
ECOG 4599 6. 2 vs 4. 5 ay 12. 3 vs 10. 3 ay Sandler A, NEJM 2006

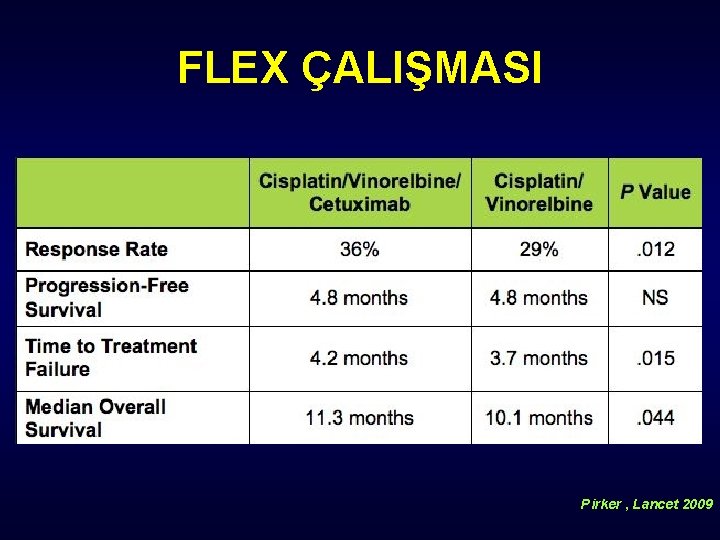
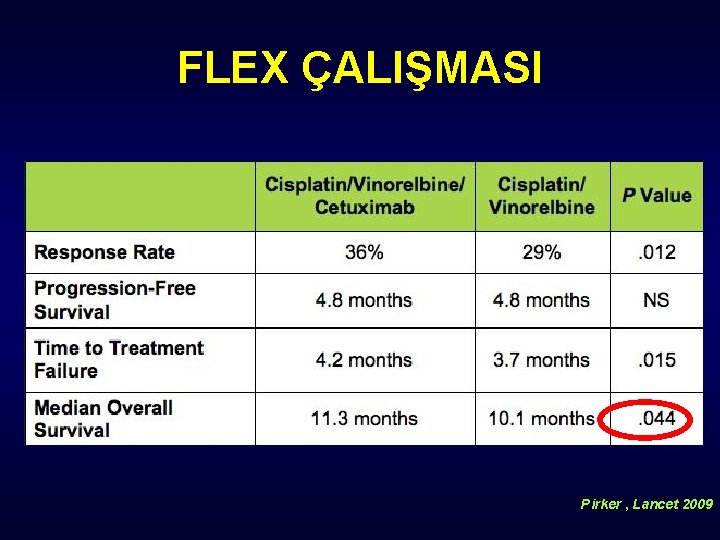
FLEX ÇALIŞMASI Pirker R, Lancet. 2009; Pirker R, WCLC 2011. Abs. O-01. 06.

FLEX ÇALIŞMASI Pirker , Lancet 2009

FLEX ÇALIŞMASI Pirker , Lancet 2009

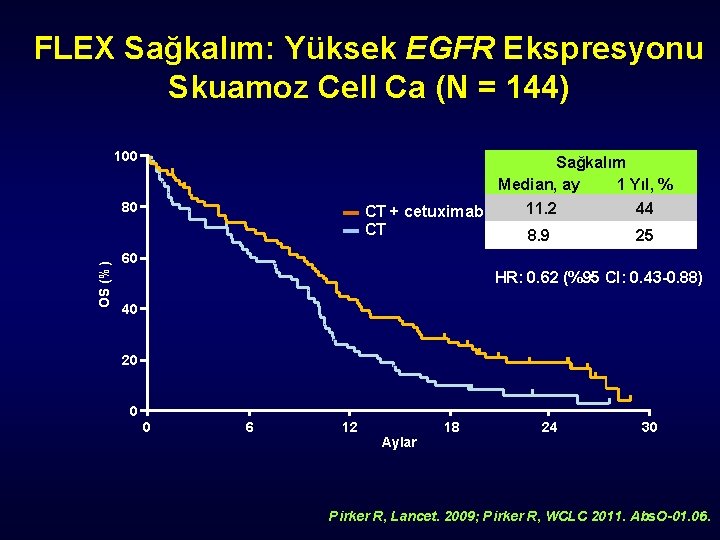
FLEX Sağkalım: Yüksek EGFR Ekspresyonu Skuamoz Cell Ca (N = 144) 100 Sağkalım Median, ay 1 Yıl, % OS (%) 80 ▬ CT + cetuximab ▬ CT 11. 2 44 8. 9 25 60 HR: 0. 62 (%95 CI: 0. 43 -0. 88) 40 20 0 0 6 12 18 Aylar 24 30 Pirker R, Lancet. 2009; Pirker R, WCLC 2011. Abs. O-01. 06.

İleri Evre NSCLC 2013 Histoloji İdame Prediktif biyomarkerlar Gandara DR Clin Lung Cancer. 2009

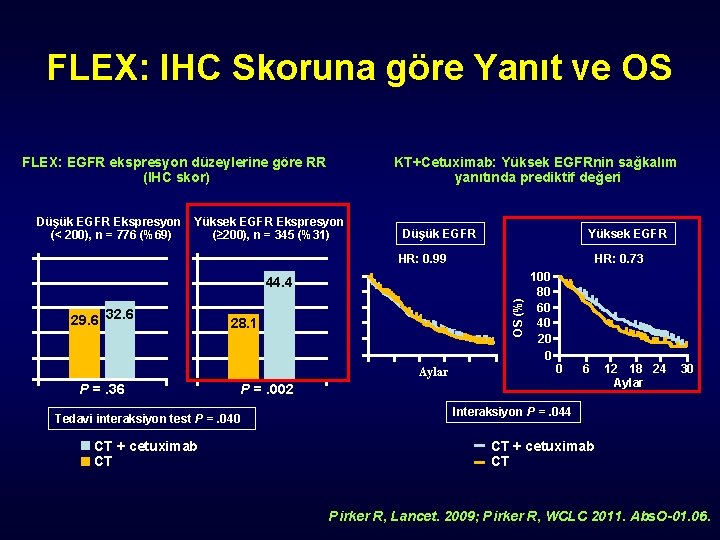
FLEX: IHC Skoruna göre Yanıt ve OS FLEX: EGFR ekspresyon düzeylerine göre RR (IHC skor) Düşük EGFR Ekspresyon (< 200), n = 776 (%69) KT+Cetuximab: Yüksek EGFRnin sağkalım yanıtında prediktif değeri Yüksek EGFR Ekspresyon (≥ 200), n = 345 (%31) Düşük EGFR Yüksek EGFR HR: 0. 99 HR: 0. 73 29. 6 32. 6 OS (%) 44. 4 28. 1 Aylar P =. 36 Tedavi interaksiyon test P =. 040 CT + cetuximab CT 100 80 60 40 20 0 0 6 P =. 002 12 18 24 Aylar 30 Interaksiyon P =. 044 CT + cetuximab CT Pirker R, Lancet. 2009; Pirker R, WCLC 2011. Abs. O-01. 06.

Metastatik NSCLC-TKI (Gefitinib) IDEAL 1, 2: Mayıs 2003 Gefitinib hızlandırılmış onay Cohen MH, The Oncologist, 2003

ISEL-Sağkalım (#1129) Aralık 2004 te Gefitinib onayı geri çekildi Planlanmamış subgrup analizlerinde: • Never smoker ve • Asya orijinlilerde daha uzun sağkalım Thatcher N, Lancet 2005

Gefitinib+Kemoterapi ile kombine kullanımda etkinlik ya da sağkalımda iyileşme yok. • INTACT 1: Gemcitabine/Cisplatin+Gefitinib • INTACT 2: Paclitaxel/Carboplatin+Gefitinib Giaccone G JCO 2004; Herbst R JCO 2004

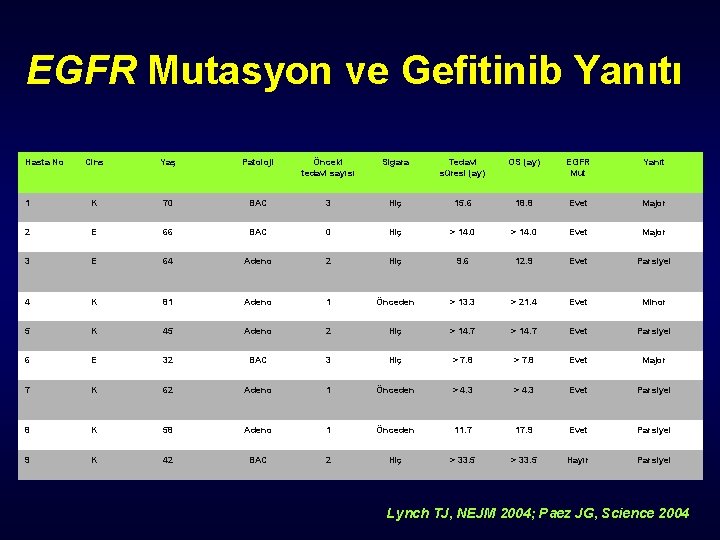
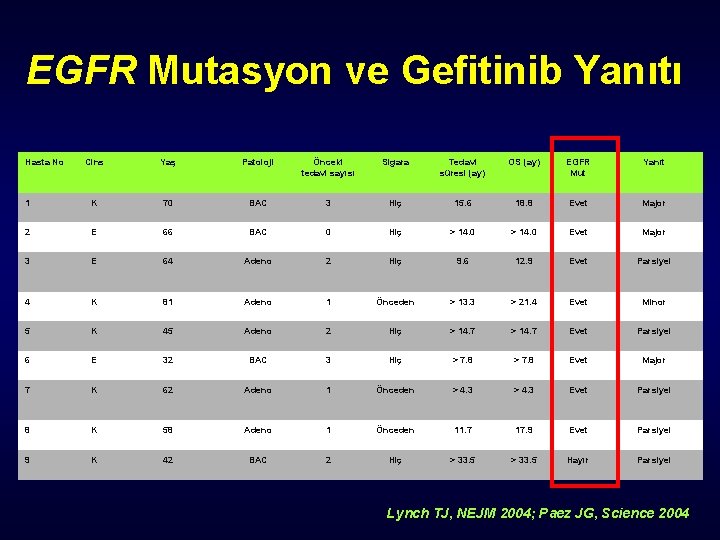
EGFR Mutasyon ve Gefitinib Yanıtı Hasta No Cins Yaş Patoloji Önceki tedavi sayısı Sigara Tedavi süresi (ay) OS (ay) EGFR Mut Yanıt 1 K 70 BAC 3 Hiç 15. 6 18. 8 Evet Major 2 E 66 BAC 0 Hiç > 14. 0 Evet Major 3 E 64 Adeno 2 Hiç 9. 6 12. 9 Evet Parsiyel 4 K 81 Adeno 1 Önceden > 13. 3 > 21. 4 Evet Minor 5 K 45 Adeno 2 Hiç > 14. 7 Evet Parsiyel 6 E 32 BAC 3 Hiç > 7. 8 Evet Major 7 K 62 Adeno 1 Önceden > 4. 3 Evet Parsiyel 8 K 58 Adeno 1 Önceden 11. 7 17. 9 Evet Parsiyel 9 K 42 BAC 2 Hiç > 33. 5 Hayır Parsiyel Lynch TJ, NEJM 2004; Paez JG, Science 2004

EGFR Mutasyon ve Gefitinib Yanıtı Hasta No Cins Yaş Patoloji Önceki tedavi sayısı Sigara Tedavi süresi (ay) OS (ay) EGFR Mut Yanıt 1 K 70 BAC 3 Hiç 15. 6 18. 8 Evet Major 2 E 66 BAC 0 Hiç > 14. 0 Evet Major 3 E 64 Adeno 2 Hiç 9. 6 12. 9 Evet Parsiyel 4 K 81 Adeno 1 Önceden > 13. 3 > 21. 4 Evet Minor 5 K 45 Adeno 2 Hiç > 14. 7 Evet Parsiyel 6 E 32 BAC 3 Hiç > 7. 8 Evet Major 7 K 62 Adeno 1 Önceden > 4. 3 Evet Parsiyel 8 K 58 Adeno 1 Önceden 11. 7 17. 9 Evet Parsiyel 9 K 42 BAC 2 Hiç > 33. 5 Hayır Parsiyel Lynch TJ, NEJM 2004; Paez JG, Science 2004

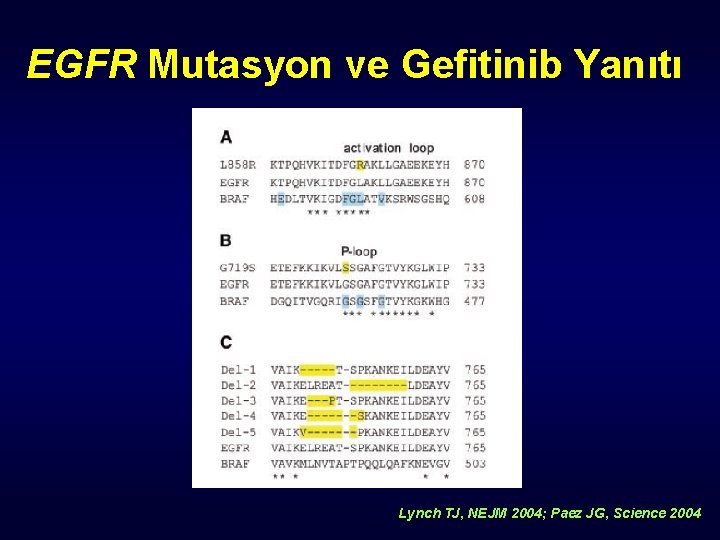
EGFR Mutasyon ve Gefitinib Yanıtı Lynch TJ, NEJM 2004; Paez JG, Science 2004

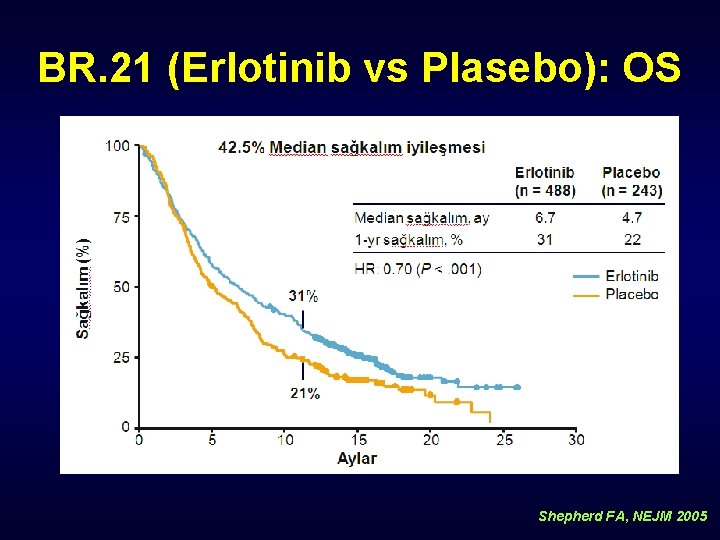
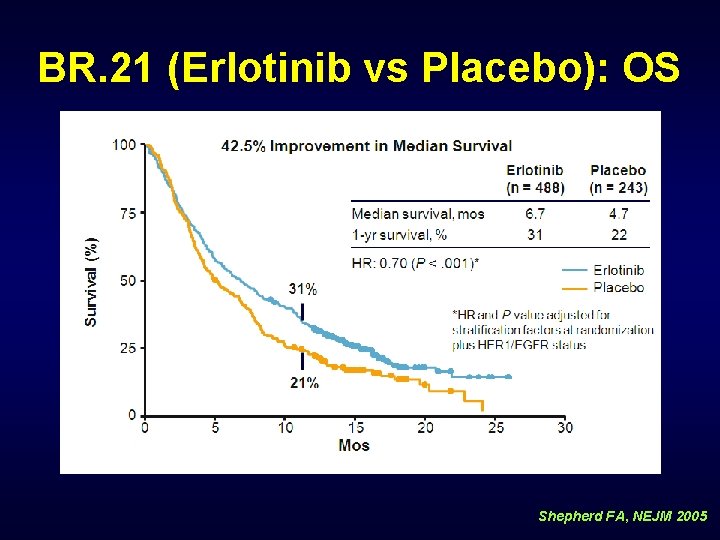
BR. 21 (Erlotinib vs Plasebo): OS Shepherd FA, NEJM 2005

BR. 21 (Erlotinib vs Plasebo): OS Shepherd FA, NEJM 2005

BR. 21: Erlotinib Genel Sağkalımı Uzatıyor-2. /3. basamak Sonuç Erlotinib Plasebo HR P Değeri 1 yıl survival, % 31 21 -- -- Median OS, aylar 6. 7 4. 7 0. 70 . 001 Tek değişkenli analizde uzun sağkalımı etkileyen faktörler: – Erlotinib tedavisi (P =. 002) – Asya kökenli (P =. 01) – Adenokarsinom (P =. 004) – Sigara içmemiş (P =. 048) Shepherd FA, NEJM 2005

IPASS ÇALIŞMASI 1: 1 Primer endpoint: RFS Sekonder endpointler: ORR, OS, QOL Diğer: EGFR mutasyonları, gen amplifikasyonu, ekspresyon Mok TS, NEJM 2009

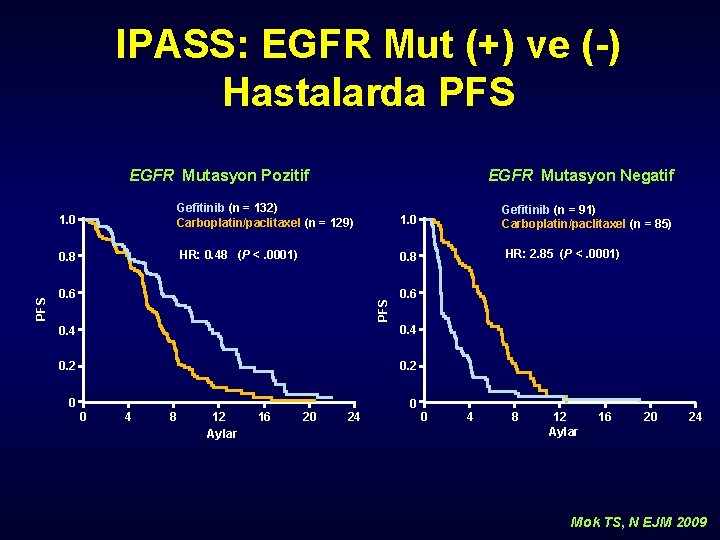
IPASS: EGFR Mut (+) ve (-) Hastalarda PFS EGFR Mutasyon Negatif 1. 0 Gefitinib (n = 132) Carboplatin/paclitaxel (n = 129) 1. 0 0. 8 HR: 0. 48 (P <. 0001) 0. 8 0. 6 PFS EGFR Mutasyon Pozitif 0. 4 0. 2 0 0 4 8 12 Aylar 16 20 24 HR: 2. 85 (P <. 0001) 0. 6 0. 4 0 Gefitinib (n = 91) Carboplatin/paclitaxel (n = 85) 0 4 8 12 Aylar 16 20 24 Mok TS, N EJM 2009

EURTAC: Erlotinib vs KT EGFR Mutasyon (+) Mutasyon tipine göre stratifikasyon*, ECOG PS (0 vs 1 vs 2) Daha önceden KT almamış, stage IIIB/IV, mutated EGFR* (N = 174) *Exon Erlotinib 150 mg/gün PD Platinum Doublet† q 3 w x 4 kür PD 19 delesyon ya da exon 21 L 858 R mutasyon. †Cisplatin /docetaxel; cisplatin/gemcitabine; carboplatin/docetaxel; carboplatin/gemcitabine Rosell R, Lancet Oncology 2012

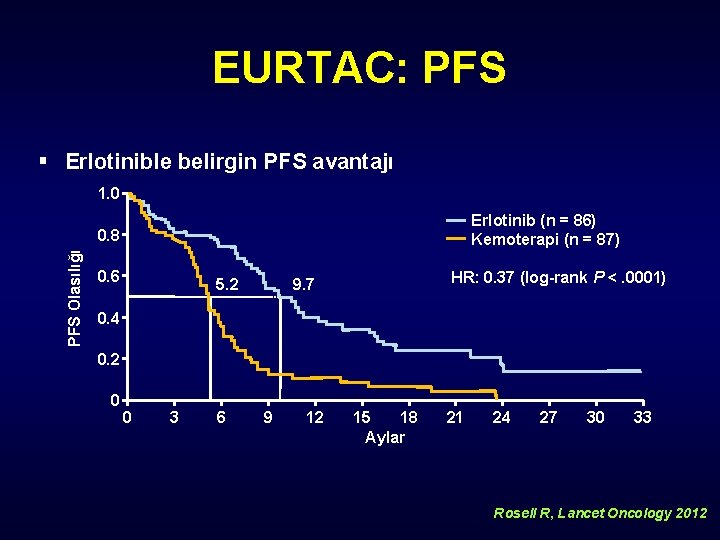
EURTAC: PFS § Erlotinible belirgin PFS avantajı 1. 0 Erlotinib (n = 86) Kemoterapi (n = 87) PFS Olasılığı 0. 8 0. 6 5. 2 HR: 0. 37 (log-rank P <. 0001) 9. 7 0. 4 0. 2 0 0 3 6 9 12 15 18 Aylar 21 24 27 30 33 Rosell R, Lancet Oncology 2012

LUX-Lung 3: First-line Afatinib vs Cisplatin/Pemetrexed EGFR+ NSCLC • Afatinib: ERB ailesi reseptörlerini irreversibl bloke eder – Faz II LUX-Lung 2: EGFR mutant AC Ca da aktif (del(19) and L 858 R mutasyonları) Stratifikasyon: EGFR mutasyon (del[19], L 858 R, diğer) ve Asyalı Önceden tedavi almamış EGFR mutasyon (+) stage IIIB (wet)/IV Akciğer Adeno. Ca (N = 345) Afatinib 40* mg/day Progresyona kadar Cisplatin 75 mg/m 2 + Pemetrexed 500 mg/m 2 IV 21 günde bir 6 kür (n = 115) Yang JC, ASCO 2012

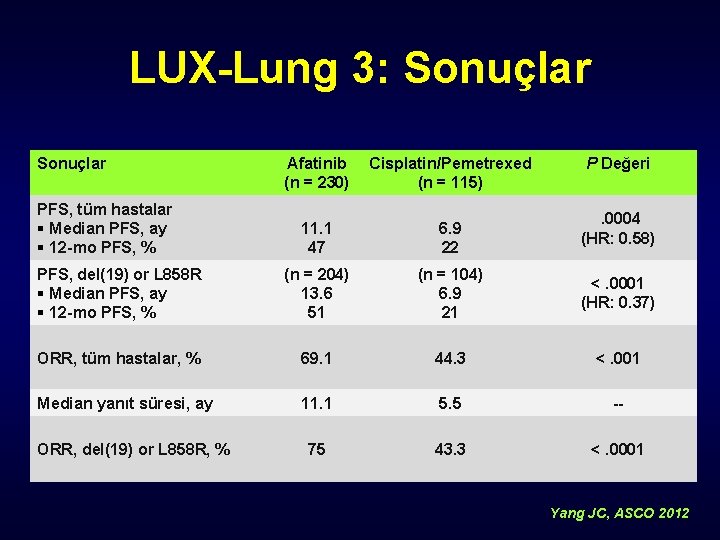
LUX-Lung 3: Sonuçlar Afatinib (n = 230) Cisplatin/Pemetrexed (n = 115) 11. 1 47 6. 9 22 PFS, del(19) or L 858 R § Median PFS, ay § 12 -mo PFS, % (n = 204) 13. 6 51 (n = 104) 6. 9 21 <. 0001 (HR: 0. 37) ORR, tüm hastalar, % 69. 1 44. 3 <. 001 Median yanıt süresi, ay 11. 1 5. 5 -- 75 43. 3 <. 0001 PFS, tüm hastalar § Median PFS, ay § 12 -mo PFS, % ORR, del(19) or L 858 R, % P Değeri. 0004 (HR: 0. 58) Yang JC, ASCO 2012

2. Basamak Tedavi

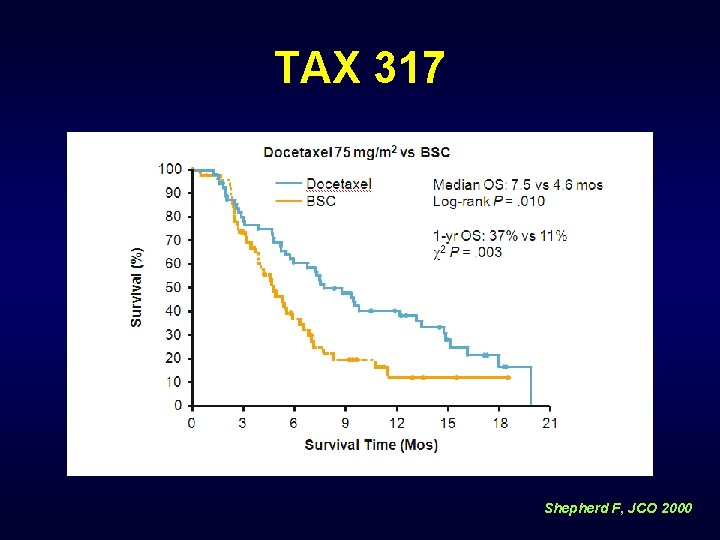
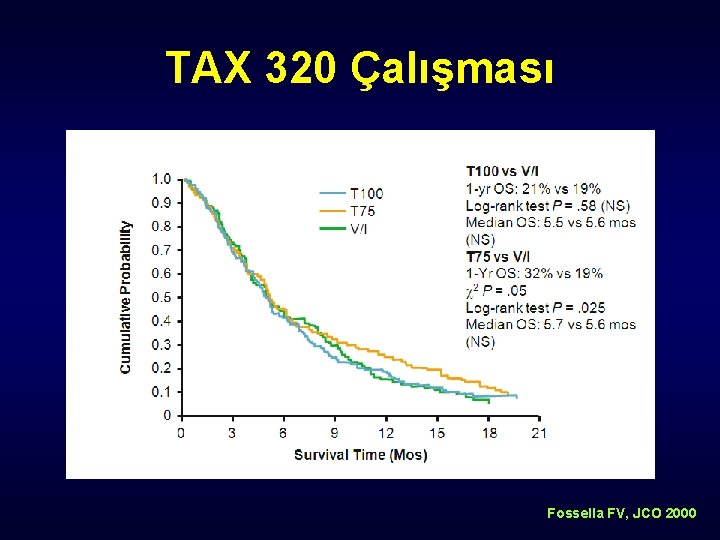
Docetaxel : TAX 317 ve TAX 320 • TAX 317 (N = 103) – Stage IIIB/IV NSCLC – Daha önceden platin bazlı tedavi almış – Docetaxel vs BSC • TAX 320 (N = 103) – Lokal ileri evre/Metastatik NSCLC – Daha önceden platin bazlı tedavi almış – Docetaxel vs vinorelbine ya da ifosfamide Shepherd F, JCO 2000 Fossella FV, JCO 2000

TAX 317 Shepherd F, JCO 2000

TAX 320 Çalışması Fossella FV, JCO 2000

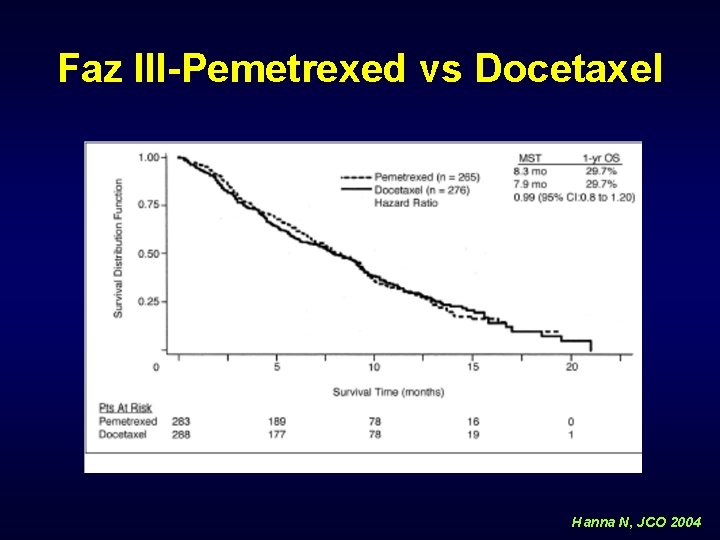
Faz III-Pemetrexed vs Docetaxel Hanna N, JCO 2004

BR. 21 (Erlotinib vs Placebo): OS Shepherd FA, NEJM 2005

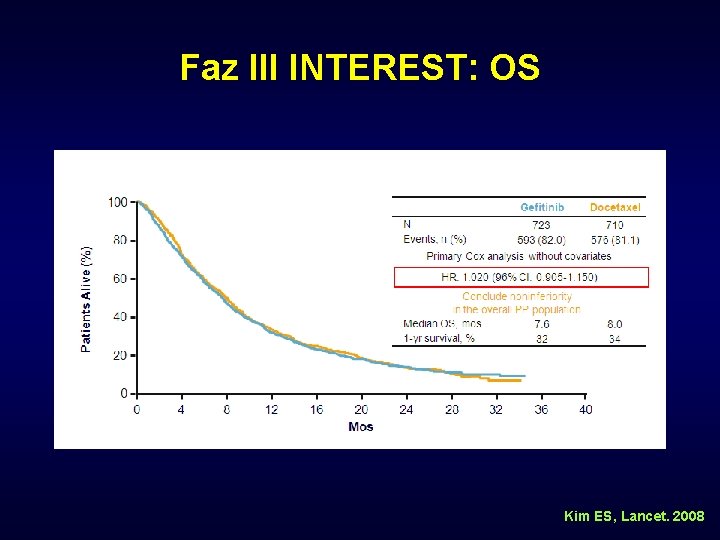
Faz III INTEREST: Gefitinib vs Docetaxel Daha önceden 1 -2 basamak tedavi almış (≥ 1 platin), PS 0 -2 (N = 1466) Gefitinib 250 mg/gün PO (n = 733) Docetaxel 75 mg/m 2 q 3 w (n = 733) Kim ES, Lancet. 2008

Faz III INTEREST: OS Kim ES, Lancet. 2008

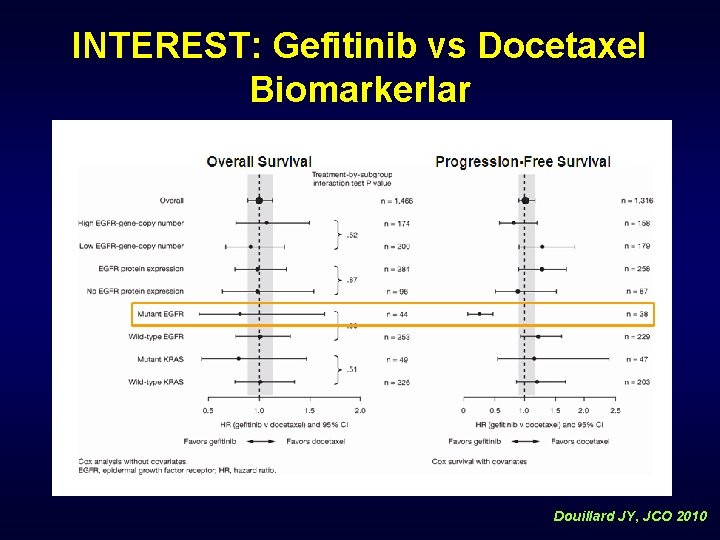
INTEREST: Gefitinib vs Docetaxel Biomarkerlar Douillard JY, JCO 2010

ALK-Pozitif NSCLC • ALK (Anaplastic Lymphoma Kinase) • Kromozomal rearrangement sonrasında onkojenik füzyon kinaz=EML 4 -ALK • Hastaların klinik özellikleri: – Genç yaş – Hiç ya da çok az sigara içmiş – Adeno. Ca Kwak EL, NEJM, 2010

Crizotinib-ALK (+) NSCLC • Crizotinib (PF-02341066) – Dual selektif inhibitor (ALK ve c-MET) • ATP-kompetitif inhibitor • Oral küçük molekül – NSCLC hücre serilerinde hücre büyüme inhibisyonu ve apoptozisin indüksiyonu – Doz-eskalasyon çalışmasında güvenilir Kwak EL, NEJM, 2010

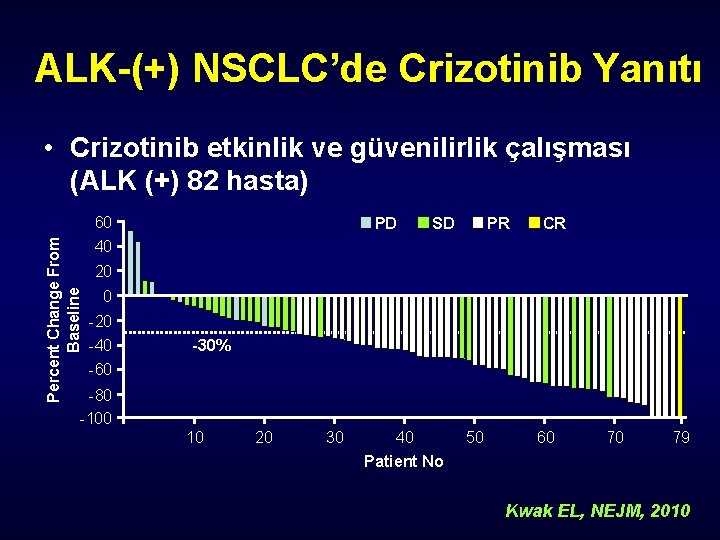
ALK-(+) NSCLC’de Crizotinib Yanıtı Percent Change From Baseline • Crizotinib etkinlik ve güvenilirlik çalışması (ALK (+) 82 hasta) 60 40 PD SD PR CR 20 0 -20 -40 -30% -60 -80 -100 10 20 30 40 50 60 70 79 Patient No Kwak EL, NEJM, 2010

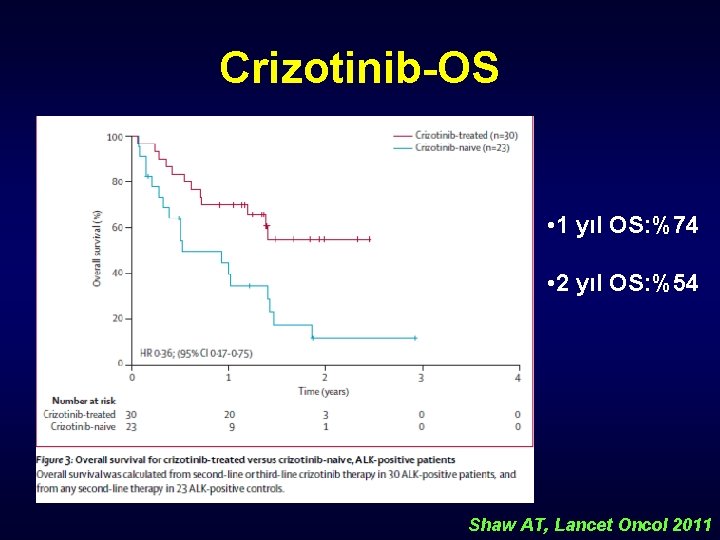
Crizotinib-OS • 1 yıl OS: %74 • 2 yıl OS: %54 Shaw AT, Lancet Oncol 2011

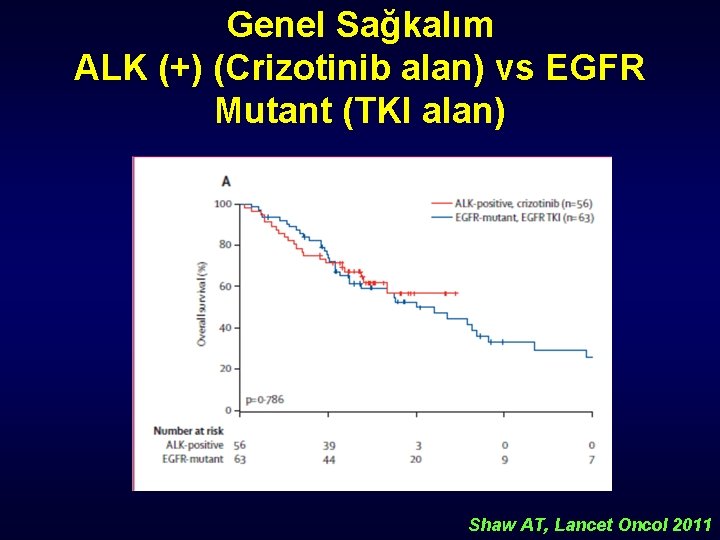
Genel Sağkalım ALK (+) (Crizotinib alan) vs EGFR Mutant (TKI alan) Shaw AT, Lancet Oncol 2011

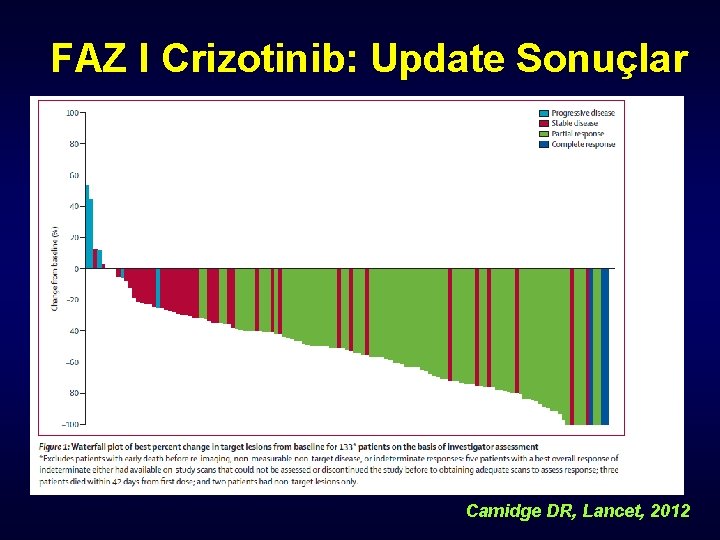
FAZ I Crizotinib: Update Sonuçlar Camidge DR, Lancet, 2012

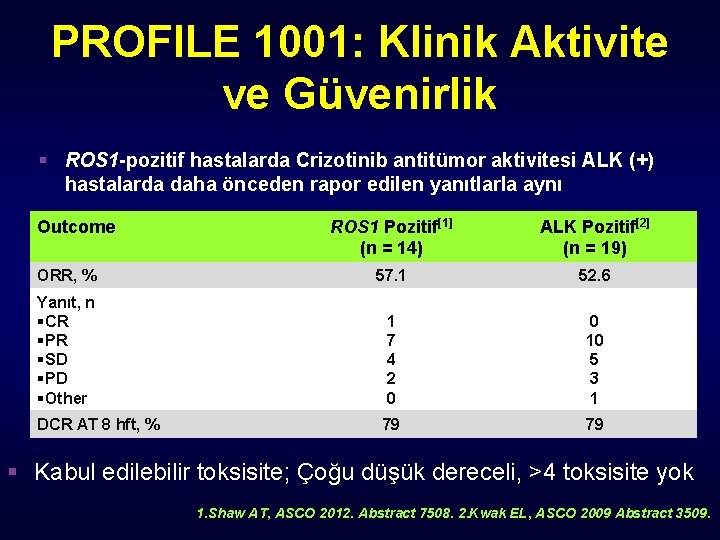
PROFILE 1001: Crizotinib ROS 1 Rearrangement • ROS 1 kromozomal rearrangement: Onkojenik füzyon sonrası aberran tirozin kinaz aktivitesi • Faz I dose-eskalasyon çalışması – ROS 1 -positif NSCLC’ de Crizotinib 250 mg BID etkinlik ve güvenilirlik (n = 15) • ORR • 8. haftada hastalık kontrol oranı – ALK-negatif adenoca Shaw AT, e. ASCO 2012. Abstract 7508.

PROFILE 1001: Klinik Aktivite ve Güvenirlik § ROS 1 -pozitif hastalarda Crizotinib antitümor aktivitesi ALK (+) hastalarda daha önceden rapor edilen yanıtlarla aynı Outcome ROS 1 Pozitif[1] (n = 14) ALK Pozitif[2] (n = 19) ORR, % 57. 1 52. 6 Yanıt, n §CR §PR §SD §PD §Other 1 7 4 2 0 0 10 5 3 1 DCR AT 8 hft, % 79 79 § Kabul edilebilir toksisite; Çoğu düşük dereceli, >4 toksisite yok 1. Shaw AT, ASCO 2012. Abstract 7508. 2. Kwak EL, ASCO 2009 Abstract 3509.

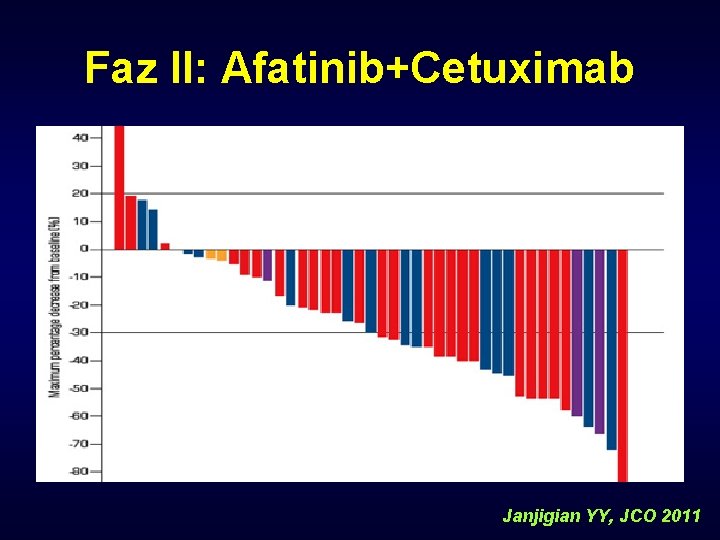
Faz II: Afatinib+Cetuximab Janjigian YY, JCO 2011

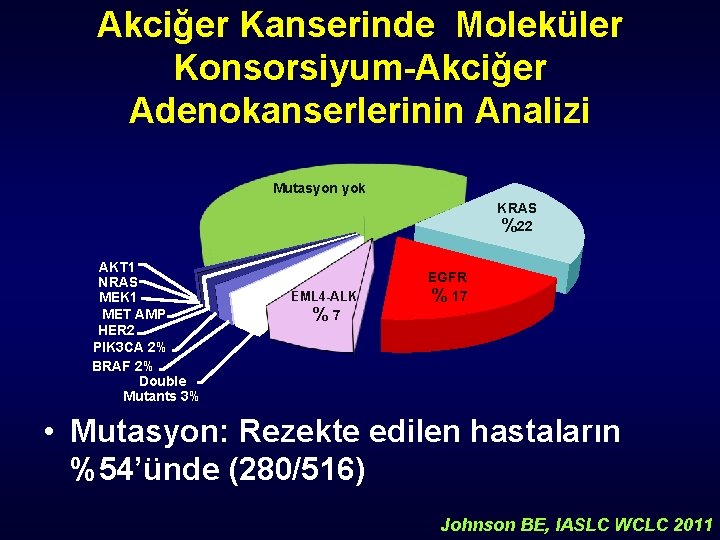
Akciğer Kanserinde Moleküler Konsorsiyum-Akciğer Adenokanserlerinin Analizi Mutasyon yok KRAS %22 AKT 1 NRAS MEK 1 MET AMP HER 2 PIK 3 CA 2% BRAF 2% Double Mutants 3% EML 4 -ALK %7 EGFR % 17 • Mutasyon: Rezekte edilen hastaların %54’ünde (280/516) Johnson BE, IASLC WCLC 2011

Met. MAb + Erlotinib vs Erlotinib • Met. MAb (Onartuzumab): Met reseptör targeting Ab • Met diagnostik pozitif (n = 66); Met diagnostik negatif (n = 62)-IHC • Met. MAb + erlotinib: Met (+) populasyonda sağkalım avantajı Spigel DR, ASCO 2011

Met. MAb + Erlotinib vs Erlotinib PFS OS Placebo + Met. MAb + Erlotinib 1. 5 2. 9 Median, ay 0. 53 HR 0. 04 Log-rank P 1. 0 0. 8 Met. MAb + Erlotinib 12. 6 0. 37 0. 002 0. 8 PFS HR: 0. 53 0. 6 OS HR: 0. 37 0. 6 OS PFS Placebo + Erlotinib 3. 8 Median, ay HR Log-rank P 0. 4 0. 2 0 0 0 3 6 9 12 TTP (Aylar) 15 18 0 3 6 9 12 15 18 21 OS (Aylar) Progresyon riskinde 2 kat azalma ve ölüm riskinde 3 kat azalma Spigel DR, ASCO 2011

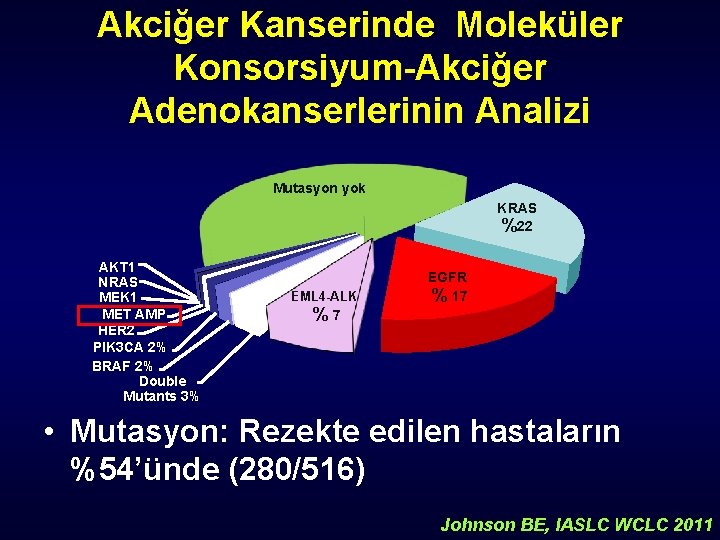
Akciğer Kanserinde Moleküler Konsorsiyum-Akciğer Adenokanserlerinin Analizi Mutasyon yok KRAS %22 AKT 1 NRAS MEK 1 MET AMP HER 2 PIK 3 CA 2% BRAF 2% Double Mutants 3% EML 4 -ALK %7 EGFR % 17 • Mutasyon: Rezekte edilen hastaların %54’ünde (280/516) Johnson BE, IASLC WCLC 2011

Potansiyel “Druggable” Moleküler Hedefler? Other (Undefined) K-ras EGFR B-raf HER 2 PIK 3 CA ALK MET Other Gene Event Type Frequency, % FGFR 1 Amplification 20 -25 FGFR 2 Mutation 5 PIK 3 CA Mutation 9 Mutation-deletion 18 Amplification 8 CDKN 2 A Deletion/mutation 45 PDGFRA Amplificationmutation 9 EGFR Amplification 10 MCL 1 Amplification 10 BRAF Mutation 3 DDR 2 Mutation 4 ERBB 2 Amplification 2 PTEN CCND 1 Hammerman P, IASLC WCLC 2011

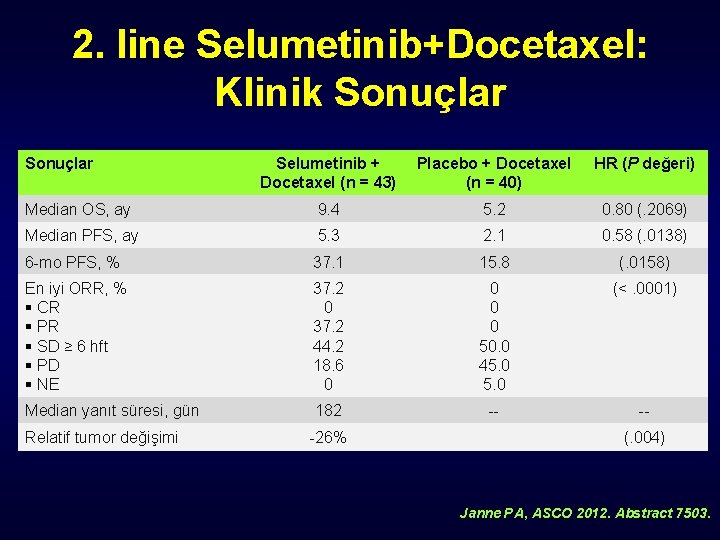
KRAS-mutated NSCLCde 2. line Selumetinib+Docetaxel • Faz II randomize, plasebo-kontrollü – Selumetinib: Potent MEK 1 ve MEK 2 nin potent, selektif inhibitörü, downstream KRAS üzerinde etki KRAS-mutant, lokal ileri veya metastatik stage IIIB/IV NSCLC (1. basamak tedavi sonrası progressif) (N = 87) Selumetinib 75 mg BID + Docetaxel 75 mg/m 2 21 günde bir (n = 44) Placebo BID + Docetaxel 75 mg/m 2 21 günde bir Janne PA, ASCO 2012. Abstract 7503.

2. line Selumetinib+Docetaxel: Klinik Sonuçlar Selumetinib + Docetaxel (n = 43) Placebo + Docetaxel (n = 40) HR (P değeri) Median OS, ay 9. 4 5. 2 0. 80 (. 2069) Median PFS, ay 5. 3 2. 1 0. 58 (. 0138) 6 -mo PFS, % 37. 1 15. 8 (. 0158) En iyi ORR, % § CR § PR § SD ≥ 6 hft § PD § NE 37. 2 0 37. 2 44. 2 18. 6 0 0 50. 0 45. 0 (<. 0001) Median yanıt süresi, gün 182 -- -- Relatif tumor değişimi -26% (. 004) Janne PA, ASCO 2012. Abstract 7503.

‘Take Home’ Mesajlar • Birinci Basamak Tedavi: – PC, nonskuamözde GC’den üstün – Kemoterapi ile hedefe yönelik ajanlarin kombinasyonu • Bevacizumab (nonskuamöz, hemoptizisi olmayan) • Cetuximabla sağkalımda orta dereceli iyileşme (skuamözde de etkili) – Frontline EGFR TKI, EGFR mutasyonu (+) hastalarda seçenek olabilir (özellikle exon 19 del) • IPASS de ve EURTAC PFS de olumlu etki (OS Ø) • EML 4 -ALK: Crizotinib (Prospektif çalışma yok)

‘Take Home’ Mesajlar • İkinci Basamak: – – Docetaxel Pemetrexed Erlotinib Crizotinib • Üçüncü basamak: – Erlotinib

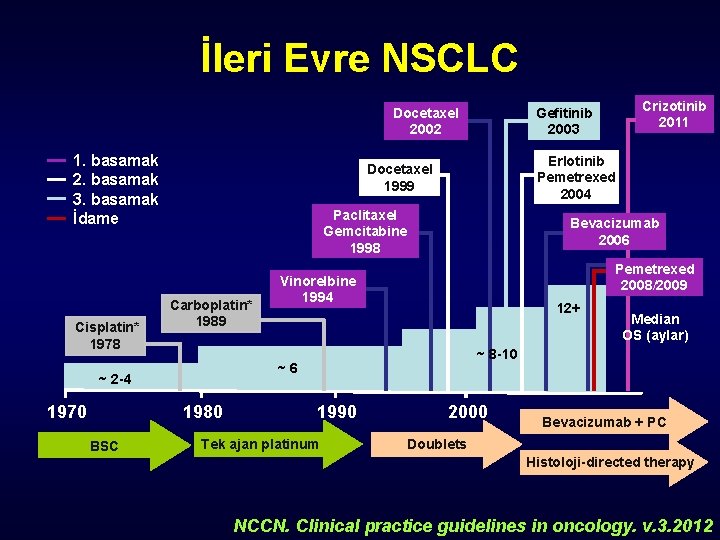
İleri Evre NSCLC Docetaxel 2002 1. basamak 2. basamak 3. basamak İdame Cisplatin* 1978 Paclitaxel Gemcitabine 1998 1980 BSC Bevacizumab 2006 Pemetrexed 2008/2009 Vinorelbine 1994 12+ Median OS (aylar) ~ 8 -10 ~6 ~ 2 -4 1970 Erlotinib Pemetrexed 2004 Docetaxel 1999 Carboplatin* 1989 Crizotinib 2011 Gefitinib 2003 1990 Tek ajan platinum 2000 Bevacizumab + PC Doublets Histoloji-directed therapy NCCN. Clinical practice guidelines in oncology. v. 3. 2012

Bireyselleştirilmiş vs Ampirik Tedavi Doğru hasta-Doğru ilaç

TEŞEKKÜRLER