Interpretazione dei risultati Come vengono espressi i risultati






































































- Slides: 101

Interpretazione dei risultati • • Come vengono espressi i risultati biochimici Variabilità nei risultati Accuratezza , precisione, sensibilità Valori di riferimento

Il dato di laboratorio È un segno che contribuisce • a distinguere tra stato di salute e stato morboso, o tra diverse condizioni patologiche • a controllare l’evoluzione dello stato morboso, o l’efficacia della terapia È, quindi, un atto semeiologico, non un giudizio clinico

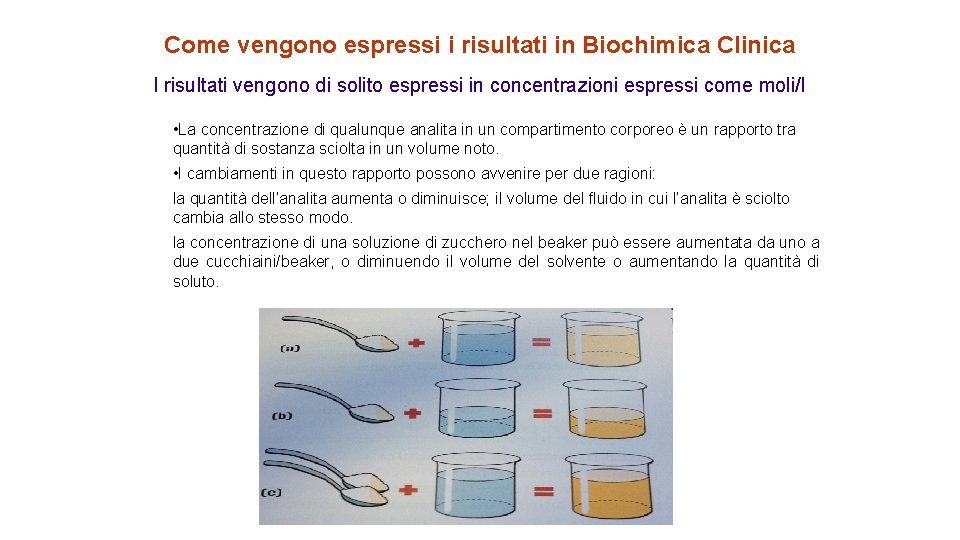
Come vengono espressi i risultati in Biochimica Clinica I risultati vengono di solito espressi in concentrazioni espressi come moli/l • La concentrazione di qualunque analita in un compartimento corporeo è un rapporto tra quantità di sostanza sciolta in un volume noto. • I cambiamenti in questo rapporto possono avvenire per due ragioni: la quantità dell’analita aumenta o diminuisce; il volume del fluido in cui l’analita è sciolto cambia allo stesso modo. la concentrazione di una soluzione di zucchero nel beaker può essere aumentata da uno a due cucchiaini/beaker, o diminuendo il volume del solvente o aumentando la quantità di soluto.

Come vengono espressi i risultati in Biochimica Clinica (II) Le grandi molecole, come le proteine vengono riportate in unità di massa (grammi o milligrammi per litro). Gli enzimi sono espressi come attività enzimatica, in “unità”. I dosaggi enzimatici sono eseguiti in modo che l’attività enzimatica sia direttamente proporzionale alla quantità di enzima presente I risultati dell’emogasanalisi (PCO 2 e PO 2) sono espressi in Kilopascal, le unità in cui le pressioni parziali sono misurate. L'emogasanalisi viene adoperata per la diagnosi di insufficienza respiratoria, per valutarne la gravità e nella valutazione dei diversi meccanismi fisiopatologici.

VALORI DI RIFERIMENTO Sono i valori “normali” o meglio usuali , caratteristici di una popolazione di soggetti sani. I valori di riferimento devono essere considerati in rapporto ai fattori che provocano variazioni analitiche e biologiche. Intervallo di riferimento come si costruisce: individui sani e non soggetti a nessuna terapia donano un campione per il test da eseguire La distribuzione dei valori ottenuti viene riportata in grafico. La quantità di valori deve essere sufficientemente grande da essere statisticamente attendibile.

Intervallo di riferimento: come si costruisce Poichè i dati non sono sempre distribuiti in modo gaussiano, l’intervallo di riferimento dovrebbe comprendere il 95% dei soggetti sani per ciascun parametro. Quindi per definizione, il 5% di qualunque popolazione avrà risultati al di fuori dell’intervallo di riferimento. Non ci sono, limiti rigidi per demarcare una popolazione malata da una sana.

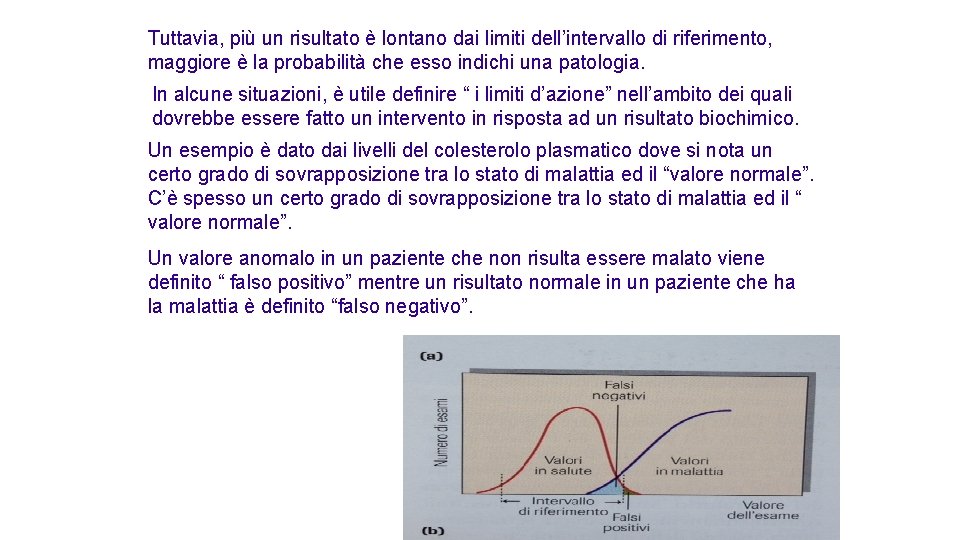
Tuttavia, più un risultato è lontano dai limiti dell’intervallo di riferimento, maggiore è la probabilità che esso indichi una patologia. In alcune situazioni, è utile definire “ i limiti d’azione” nell’ambito dei quali dovrebbe essere fatto un intervento in risposta ad un risultato biochimico. Un esempio è dato dai livelli del colesterolo plasmatico dove si nota un certo grado di sovrapposizione tra lo stato di malattia ed il “valore normale”. C’è spesso un certo grado di sovrapposizione tra lo stato di malattia ed il “ valore normale”. Un valore anomalo in un paziente che non risulta essere malato viene definito “ falso positivo” mentre un risultato normale in un paziente che ha la malattia è definito “falso negativo”.

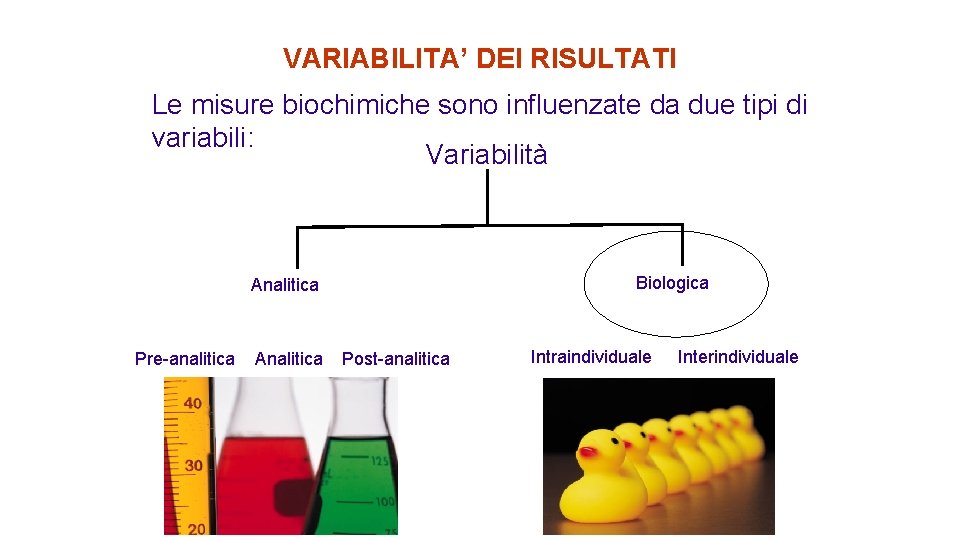
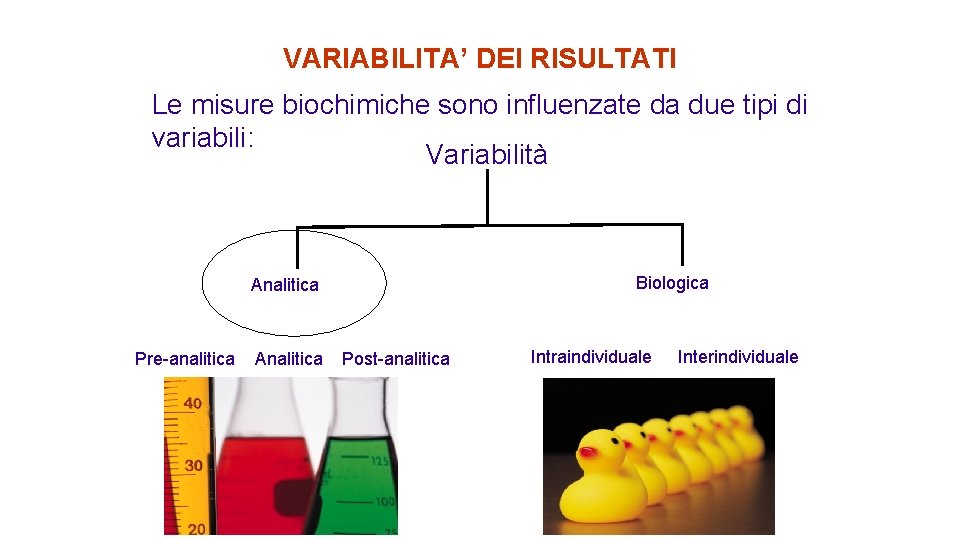
VARIABILITA’ DEI RISULTATI Le misure biochimiche sono influenzate da due tipi di variabili: Variabilità Biologica Analitica Pre-analitica Analitica Post-analitica Intraindividuale Interindividuale

Variabilità biologica • La variabilità biologica è il risultato di diverse componenti: individuali, etniche, ambientali, fisiologiche e patologiche. • La variabilità individuale dei parametri biochimici si suddivide in variabilità Intra-individuale intesa come variazione nel tempo dei parametri nello stesso soggetto e inter-individuale, ovvero variazione dei parametri tra soggetti diversi. • La variabilità individuale in assenza di fattori patologici, dipende da alcuni fattori come l’interazione tra genotipo ed ambiente che determina la produzione di un determinato fenotipo biochimico individuale, punto di equilibrio tra assetto genetico e le influenze ambientali.

Variabilità biologica • Una seconda forma di variabilità è relativa ai marcatori d’organo e tessuti. • Ad esempio l’attività AST, Aspartato aminotrasferasi nel siero presenta una correlazione con la massa muscolare, per cui gli individui con massa muscolare più sviluppata, per costituzione o per allenamento, presentano in media livelli di AST più elevati rispetto ai limiti di riferimento. • Tale comportamento ha una particolare importanza per molti marker tissutali in condizioni di alterata fisiopatologia.

Fonti secondarie di variabilità intra-individuale • Sesso • Età • Ritmi fisiologici (ritmi circadiani, variazioni stagionali) • Massa Corporea • Dieta • Postura • Alcool • Farmaci

VARIABILITA’ DEI RISULTATI Le misure biochimiche sono influenzate da due tipi di variabili: Variabilità Biologica Analitica Pre-analitica Analitica Post-analitica Intraindividuale Interindividuale

IL CICLO ANALITICO va ria bi lit à r va lit à bi ria à ia FASE POSTANALITICA FASE PREANALITICA va lit i b FASE ANALITICA va ria b ilit à

FASE PREANALITICA: identificazione del paziente valutazione della richiesta delle analisi prelievo e raccolta del materiale biologico trasporto del campione al laboratorio accettazione del campione preparazione del campione prima dell’esecuzione dell’analisi FASE ANALITICA: esecuzione delle analisi misura e calcolo dei risultati FASE POSTANALITICA: validazione dei risultati analisi della loro coerenza refertazione invio del referto al medico richiedente

VARIABILITA’ ANALITICA FASE ANALITICA: • esecuzione delle analisi • misura e calcolo dei risultati

Il dato di laboratorio È un segno che contribuisce • a distinguere tra stato di salute e stato morboso, o tra diverse condizioni patologiche, • a controllare l’evoluzione dello stato morboso, o l’efficacia della terapia Deve essere attendibile

ATTENDIBILITA’ ANALITICA L’attendibilità analitica di una misura è rappresentata dal grado di concordanza tra il valore “vero” oggetto della misura e la stima che se ne ottiene. Nelle operazioni di stima, il procedimento impiegato (metodo) è il fattore principale delle possibili discordanze tra il valore vero e la sua stima. Per “metodo”, in Biochimica clinica, s’intendono tutte le operazioni che, partendo dal campione in esame, conducono alla disponibilità del valore numerico della grandezza oggetto della misura.

L’attendibilità Caratterizza un risultato (o un metodo) analitico FATTORI CHE DETERMINANO L’ATTENDIBILITÀ: PRECISIONE ACCURATEZZA SENSIBILITA’ SPECIFICITA’

PRECISIONE di un metodo • La precisione è il grado di concordanza tra i valori di una grandezza ottenuti da misure replicate ottenute con lo stesso metodo sul medesimo campione stabile ed identico per composizione in condizioni definite. • Per “condizioni definite” si intendono le diverse modalità con cui può essere calcolata la precisione. Quando queste condizioni definite riguardano un breve intervallo di tempo si parla di ripetibilità.

PRECISIONE di un metodo • Si parla di precisione intermedia quando le misure ripetute si estendono per un ampio intervallo, riguardano diverse calibrazioni, diversi operatori, diversi lotti di reattivi. In questo caso si parla di riproducibilità. • L’imprecisione è una misura del grado di discordanza tra più misure replicate sullo stesso campione e si esprime numericamente con il valore della deviazione standard, DS, calcolata sui risultati sperimentali ottenuti.

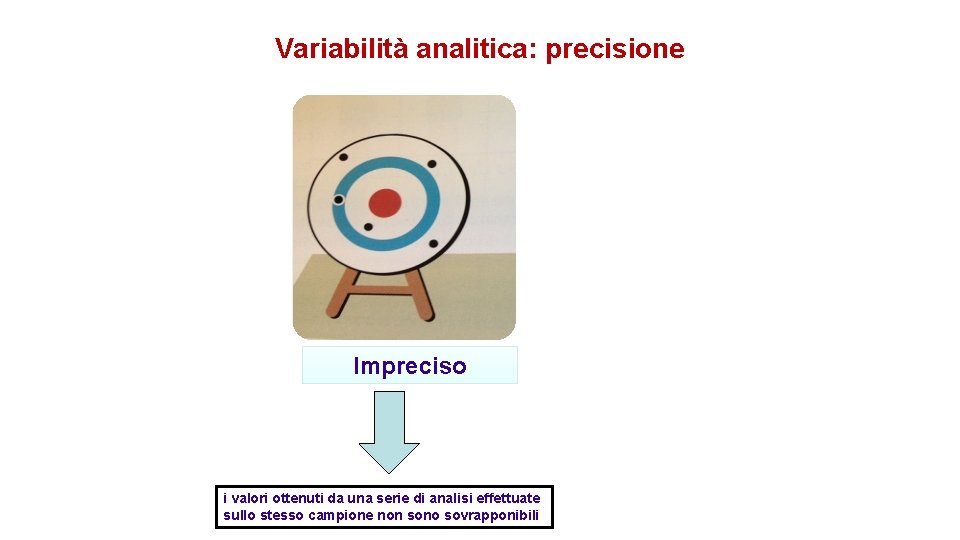
Variabilità analitica: precisione Impreciso i valori ottenuti da una serie di analisi effettuate sullo stesso campione non sono sovrapponibili

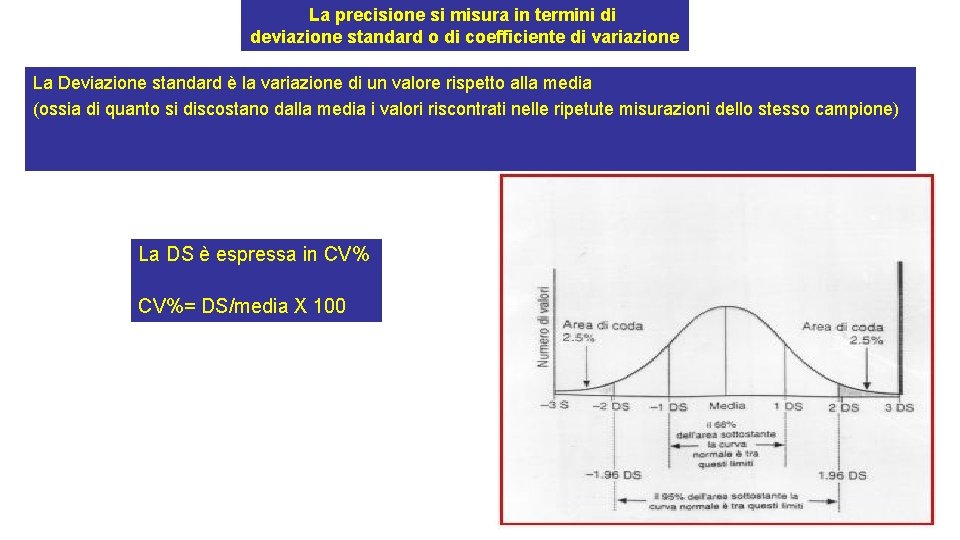
La precisione si misura in termini di deviazione standard o di coefficiente di variazione La Deviazione standard è la variazione di un valore rispetto alla media (ossia di quanto si discostano dalla media i valori riscontrati nelle ripetute misurazioni dello stesso campione) La DS è espressa in CV%= DS/media X 100

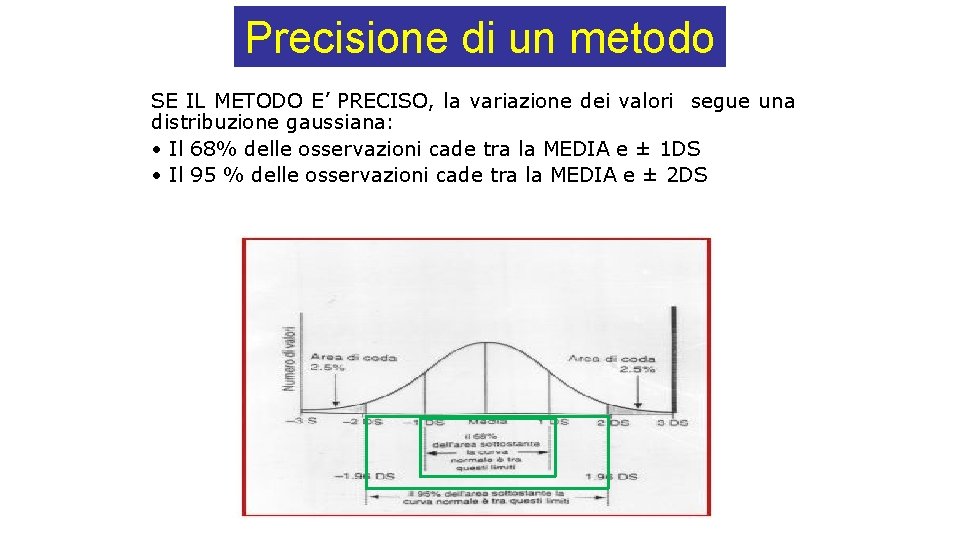
Precisione di un metodo SE IL METODO E’ PRECISO, la variazione dei valori segue una distribuzione gaussiana: • Il 68% delle osservazioni cade tra la MEDIA e ± 1 DS • Il 95 % delle osservazioni cade tra la MEDIA e ± 2 DS

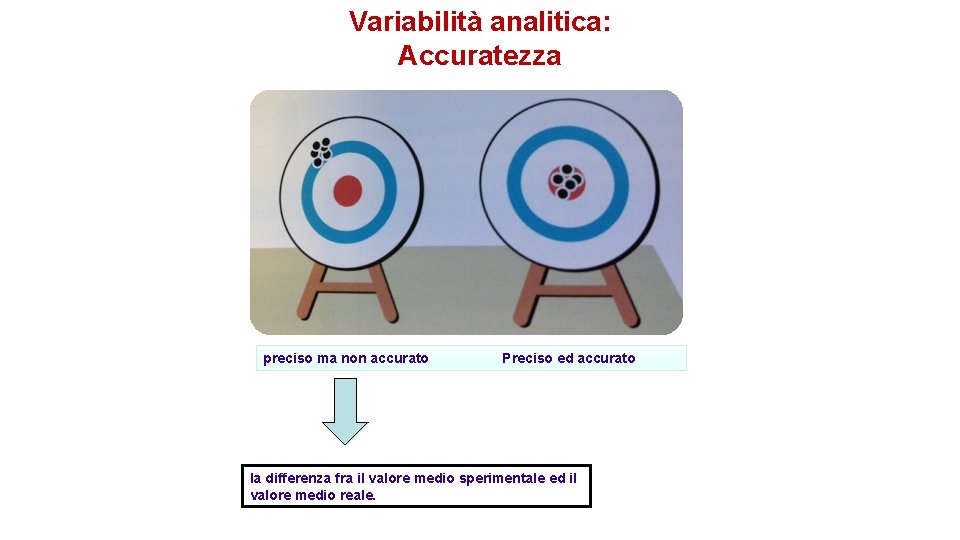
ACCURATEZZA E’ il grado di concordanza fra il valore medio determinato in una serie di distinte repliche di una stessa analisi sul medesimo campione ed il “valore vero” della grandezza. L’inaccuratezza è la differenza fra il valore medio sperimentale ed il “valore vero”. Può essere espressa sia nelle unità della grandezza misurata, sia come scostamento percentuale dal valore vero.

Variabilità analitica: Accuratezza preciso ma non accurato Preciso ed accurato la differenza fra il valore medio sperimentale ed il valore medio reale.

SPECIFICITA’analitica E’ la capacità del metodo di identificare solo e interamente l’analita in esame. Un metodo non è specifico quando grandezze differenti generano un segnale non distinguibile da quello generato dalla grandezza oggetto della misura.

Interferenza • Fenomeno correlato all’aspecificità • Situazione in cui componenti differenti, pur non generando di per sé un segnale, amplificano o deprimono il segnale generato nel metodo dal componente oggetto della misura. Aspecificità e interferenza costituiscono gli EFFETTI-MATRICE Per matrice di un campione si intende tutto quanto nel campione circonda il componente o la grandezza oggetto della misura. Ad esempio: nel siero il glucosio si trova in una matrice di acqua, proteine, vari componenti organici ed inorganici, ecc.

SENSIBILITA’ analitica E’ la capacità del metodo di identificare anche piccole quantità di un analita il limite di rivelabilità o di rivelazione indica la più piccola quantità che il metodo riesce a dosare, cioè a distinguere dal bianco con un certo limite fiduciario (in genere 95%). Esso è tanto più basso quanto maggiore è la sensibilità del metodo e quanto minore è la sua imprecisione.

Il metodo deve essere molto sensibile quando: • Si misurano analiti presenti in piccolissime concentrazioni (nanomoli, picomoli), e ciò riguarda soprattutto analisi di ormoni o farmaci; • Piccole variazioni delle concentrazioni di analita sono significative da un punto di vista clinico, ad esempio determinazioni degli elettroliti, oppure determinazioni collegate all’equilibrio acido-base.

L’imprecisione: cause • L’imprecisione è dovuta all’errore casuale (inevitabile, involontario, di piccola entità). • Per effetto dell’errore casuale, i valori analitici replicati risultano occasionalmente superiori o inferiori al valore vero.

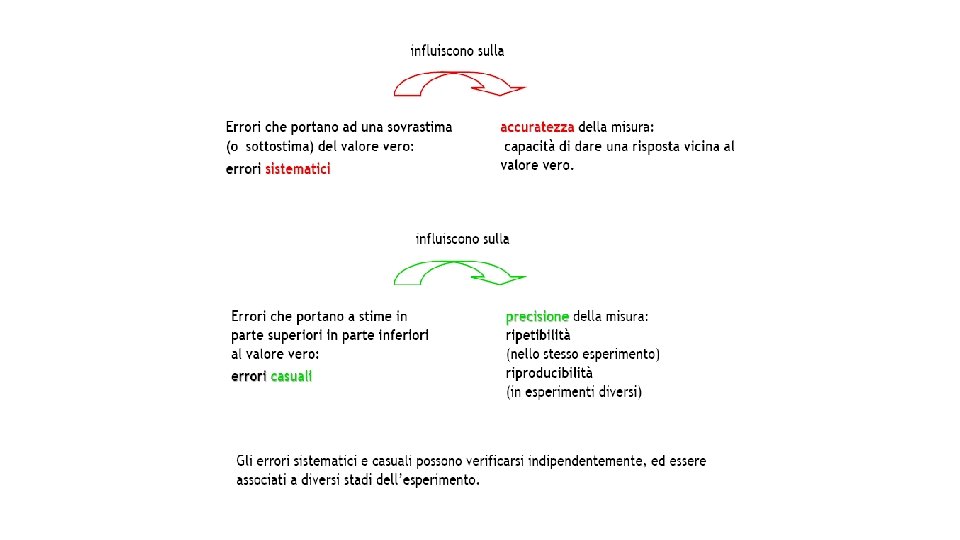
ERRORI DI MISURA Si definisce errore di un’analisi la differenza tra il valore vero della sostanza dosata ed il valore determinato con il procedimento analitico Classificazione degli errori di misura • ERRORE GROSSOLANO • ERRORE CASUALE • ERRORE SISTEMATICO

ERRORE GROSSOLANO Ø Sono accidentali e dovuti generalmente all’operatore (es. scambio di reagenti, uso di pipette sbagliate, errori di calcolo, ecc. ). Ø Sono veri e propri sbagli, eliminabili. Ø Possono essere prevenuti ed eliminati solo attraverso provvedimenti organizzativi facenti parte della buona pratica di laboratorio.

ERRORE CASUALE Ø Conseguenza dell’imprecisione analitica Ø Sono inevitabili, in genere di piccola entità, e compiuti dall’operatore senza che se ne possa rendere conto (es. piccole variazioni della tensione di alimentazione degli strumenti elettrici, di misure di volumi, di tempi analitici, di miscelamento dei reagenti, ecc. ). Ø Può essere ridotto ma mai completamente eliminato

• L’accuratezza è il grado di concordanza fra il valore medio determinato in una serie di distinte repliche di una stessa analisi sul medesimo campione ed il “valore vero” della grandezza. • L’inaccuratezza è la differenza fra il valore medio sperimentale ed il “valore vero”.

ERRORE SISTEMATICO Ø Conseguenza dell’inaccuratezza analitica. Ø In seguito all’errore sistematico i valori determinati sono tutti maggiori o minori del valore vero. Ø Sono caratterizzati dall’avere una causa conosciuta o individuabile (es. poca sensibilità o aspecificità di un metodo, errata taratura di strumenti, reattivi non puri o alterati, uso di vetreria lavata in maniera non idonea, ecc. )


• L’errore casuale e quello sistematico che caratterizzano la misura definiscono l’ambito in cui con una probabilità del 95% potrebbe cadere il valore vero.

Il CONTROLLO DEI METODI ANALITICI

CONTROLLI DI QUALITA’ Allo scopo di tenere sotto controllo l’efficienza dei metodi di misura, ed in particolare la precisione e l’accuratezza, si utilizzano i sistemi di controllo di qualità. Controllo di Qualità Interno: insieme di procedure messe in atto da ciascun laboratorio per la sorveglianza della qualità analitica dei risultati. Controllodi Qualità Esterno: un sistema per la verifica collaborativa della qualità analitica, organizzato da un ente esterno.

Controllo di qualità Nei sistemi “esterni” o “extralaboratorio”, il laboratorio riceve, periodicamente, campioni di controllo a concentrazione ignota e li analizza insieme ai campioni da paziente. Nei sistemi di controllo “interni” o “intralaboratorio” si utilizzano invece campioni di controllo a concentrazione nota, che vengono analizzati insieme ai campioni da paziente. In genere, il controllo interno è effettuato per ogni serie analitica, ed è buona norma usare campioni che hanno concentrazioni diverse, in tutto il range di valori che si possono ottenere da un paziente.

Controllo di Qualità Interno • E’ un programma di controllo della qualità analitica che può essere eseguito da ciascun laboratorio indipendentemente. • Il CQI deve fornire informazioni immediate per consentire una azione di correzione immediata: – Metodo con campione e carta di controllo – schema più frequentemente seguito per il controllo di qualità interno • È necessario un campione di controllo nel quale la concentrazione degli analiti sotto controllo si mantenga stabile per un periodo minimo di 5 -7 mesi; • metodologia: i risultati analitici ottenuti per il materiale di controllo vengono analizzati statisticamente per valutare l’accuratezza e la precisione

Metodo con Campione e Carta di Controllo • punto critico di questo tipo di schema è il materiale di controllo che deve avere i seguenti requisiti: – caratteristiche chimico fisiche sovrapponibili a quelle dei campioni in esame – gli analiti in esso contenuti devono essere stabili per un periodo sufficientemente lungo.

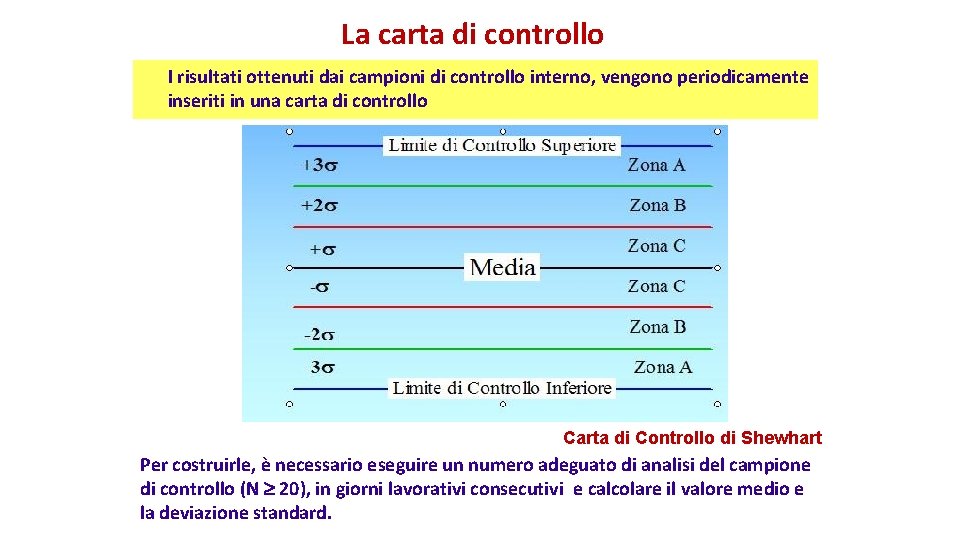
La carta di controllo I risultati ottenuti dai campioni di controllo interno, vengono periodicamente inseriti in una carta di controllo Carta di Controllo di Shewhart Per costruirle, è necessario eseguire un numero adeguato di analisi del campione di controllo (N 20), in giorni lavorativi consecutivi e calcolare il valore medio e la deviazione standard.

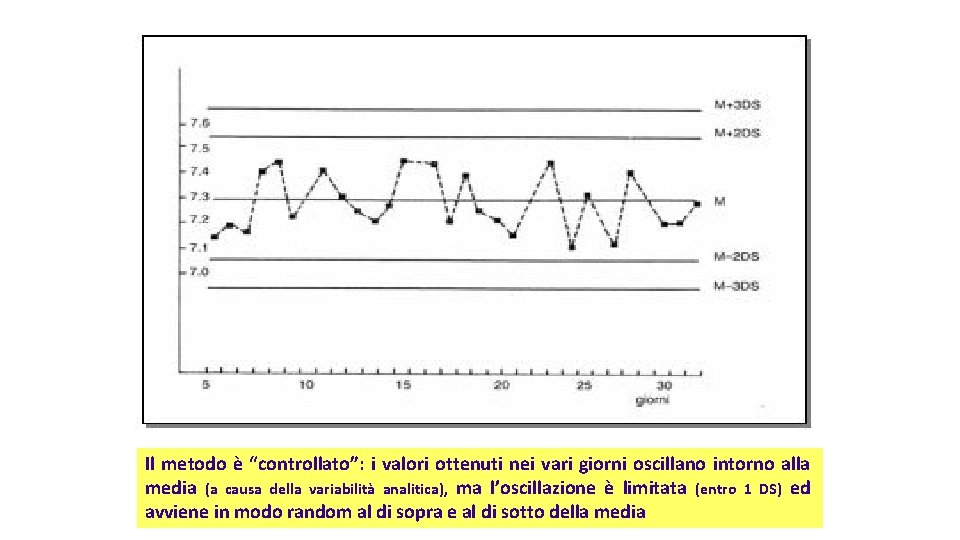
Il metodo è “controllato”: i valori ottenuti nei vari giorni oscillano intorno alla media (a causa della variabilità analitica), ma l’oscillazione è limitata (entro 1 DS) ed avviene in modo random al di sopra e al di sotto della media

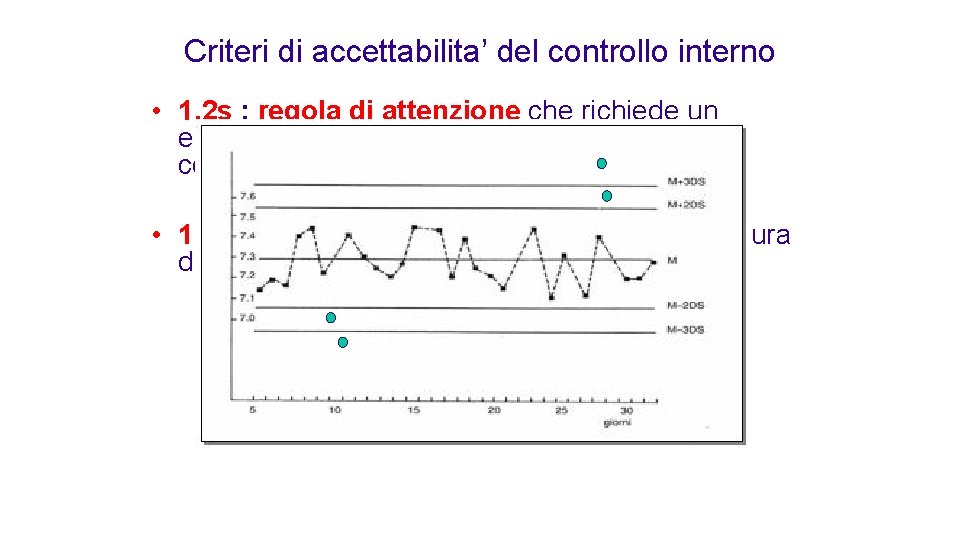
Criteri di accettabilita’ del controllo interno • 1, 2 s : regola di attenzione che richiede un esame ulteriore dei dati quando una misura di controllo cade fuori dell’intervallo 2 s. • 1, 3 s : la serie viene rifiutata quando una misura di controllo cade fuori dell’intervallo 3 s.

Essere dentro i limiti della carta di controllo è solo una condizione necessaria ma non sufficiente per poter dire che un processo è sotto controllo, infatti….

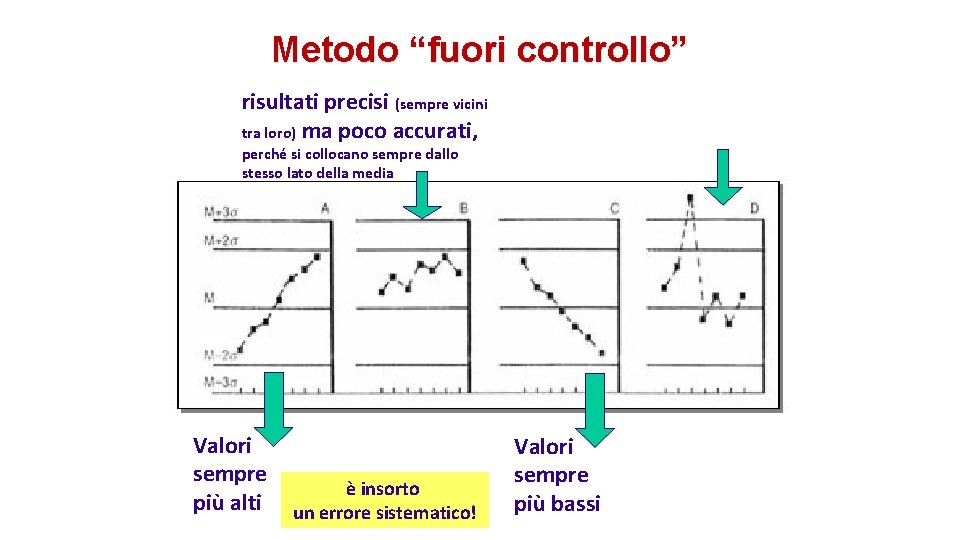
Metodo “fuori controllo” risultati precisi (sempre vicini tra loro) ma poco accurati, in una delle determinazioni il risultato è fuori 1 DS: solo in quella seduta analitica si è verificata una anomalia (non sistematica) perché si collocano sempre dallo stesso lato della media Valori sempre più alti è insorto un errore sistematico! Valori sempre più bassi

Valutazione Esterna della Qualità (VEQ) I programmi di VEQ si realizzano mediante la partecipazione collaborativa di più laboratori e sono organizzati da un laboratorio e da un ente (Agenzia esterna) che ne promuove la messa in opera e ne coordina lo svolgimento.

Scopi del programma di Valutazione Esterna della Qualità (VEQ) – registrare lo “stato dell’arte” per una determinata analisi – mettere a disposizione dei partecipanti dati comparativi – fungere da supplemento ai programmi di controllo di qualità interno – stimolare i laboratori a promuovere il miglioramento della qualità analitica – valutazione comparativa dei differenti metodi, strumenti e sistemi analitici – valutazione della variabilità analitica inter-laboratori

Come funziona un programma VEQ • il centro organizzatore predispone i materiali e ne cura la distribuzione ai partecipanti • i partecipanti eseguono le analisi previste, nel tempo prefissato, ed inviano i risultati al centro • il centro provvede all’elaborazione statistica dei valori analitici e distribuisce ai partecipanti i risultati di tale elaborazione

Validità diagnostica dei test di laboratorio • Un buon test di laboratorio dovrebbe essere in grado di distinguere i soggetti affetti da una malattia rispetto ai sani. • Questi parametri vengono indicati come “sensibilità diagnostica” e “specificità diagnostica” che non vanno confusi con i parametri di sensibilità e specificità analitiche

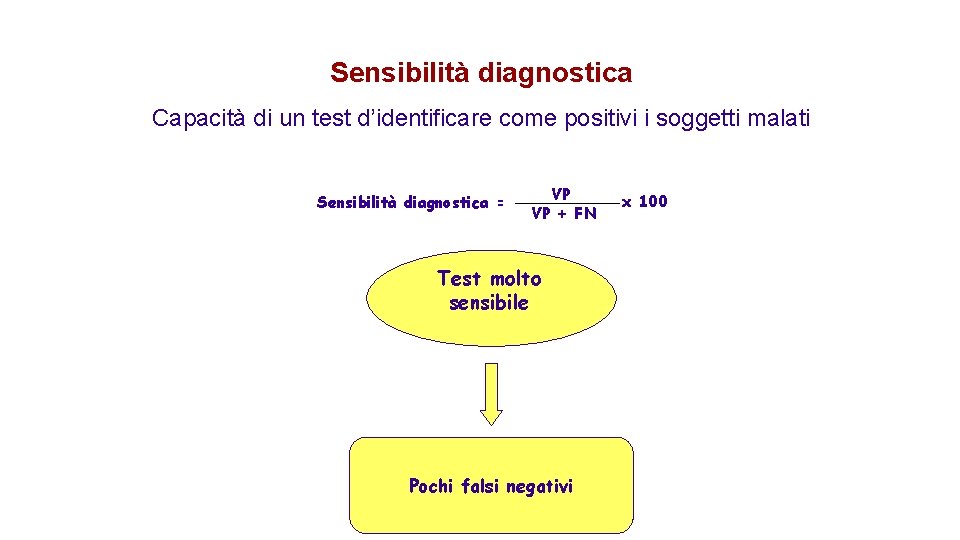
Sensibilità diagnostica Capacità di un test d’identificare come positivi i soggetti malati Sensibilità diagnostica = VP VP + FN Test molto sensibile Pochi falsi negativi x 100

Specificità diagnostica Capacità di un test d’identificare come negativi i soggetti sani Specificità diagnostica = VN VN + FP Test molto specifico Pochi falsi positivi x 100

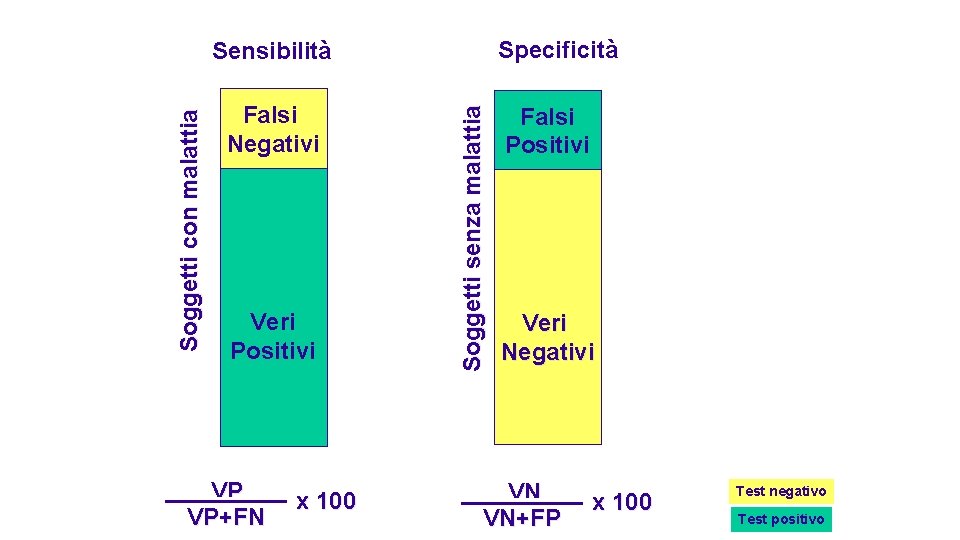
Specificità Falsi Negativi Veri Positivi VP VP+FN x 100 Soggetti senza malattia Soggetti con malattia Sensibilità Falsi Positivi Veri Negativi VN VN+FP x 100 Test negativo Test positivo

Ø Se su 100 soggetti affetti il test è positivo, ovvero al di fuori dei limiti di riferimento, la sua sensibilità diagnostica è del 100%; se è positivo in 75 mentre negli altri 25 non è diverso dalla popolazione di riferimento, la sua sensibilità diagnostica è pari al 75%. Ø Se su 100 soggetti non affetti il test fornisce 100 risultati negativi, il test ha una specificità del 100%; se, sugli stessi 100 soggetti è negativo in 75 mentre è positivo in 25, la sua specificità è pari al 75 %.

Ø Specificità e sensibilità diagnostica sono quindi valori convenzionali. Ø Essi dipendono, oltre che dallo spettro della malattia da diagnosticare (per cui la specificità e sensibilità dello stesso test possono essere ben diverse in contesti diagnostici differenti) ed in particolare dalla scelta del valore soglia (punto di cut off, livello decisionale), non necessariamente identificabile con i valori di riferimento, oltre il quale considerare un determinato test come positivo o negativo.

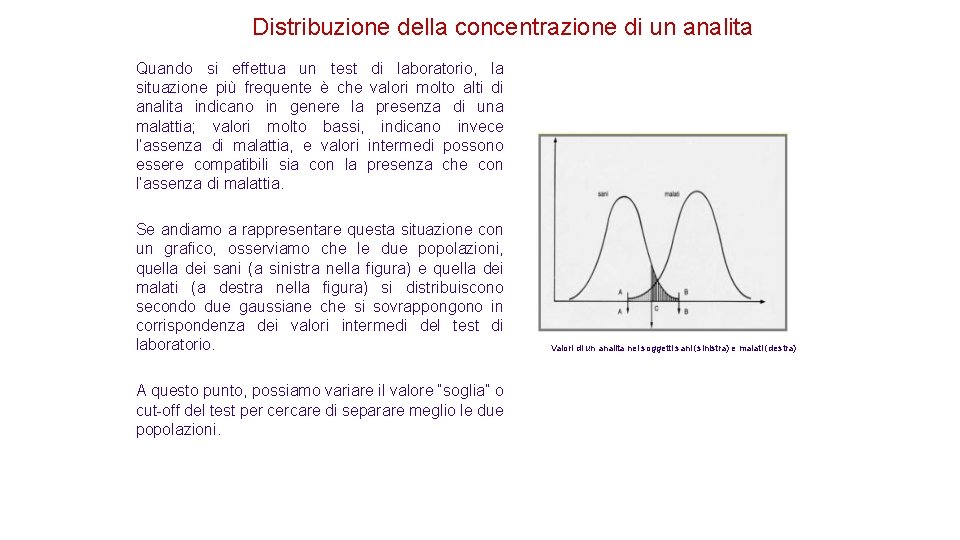
Distribuzione della concentrazione di un analita Quando si effettua un test di laboratorio, la situazione più frequente è che valori molto alti di analita indicano in genere la presenza di una malattia; valori molto bassi, indicano invece l’assenza di malattia, e valori intermedi possono essere compatibili sia con la presenza che con l’assenza di malattia. Se andiamo a rappresentare questa situazione con un grafico, osserviamo che le due popolazioni, quella dei sani (a sinistra nella figura) e quella dei malati (a destra nella figura) si distribuiscono secondo due gaussiane che si sovrappongono in corrispondenza dei valori intermedi del test di laboratorio. A questo punto, possiamo variare il valore “soglia” o cut-off del test per cercare di separare meglio le due popolazioni. Valori di un analita nei soggetti sani (sinistra) e malati (destra)

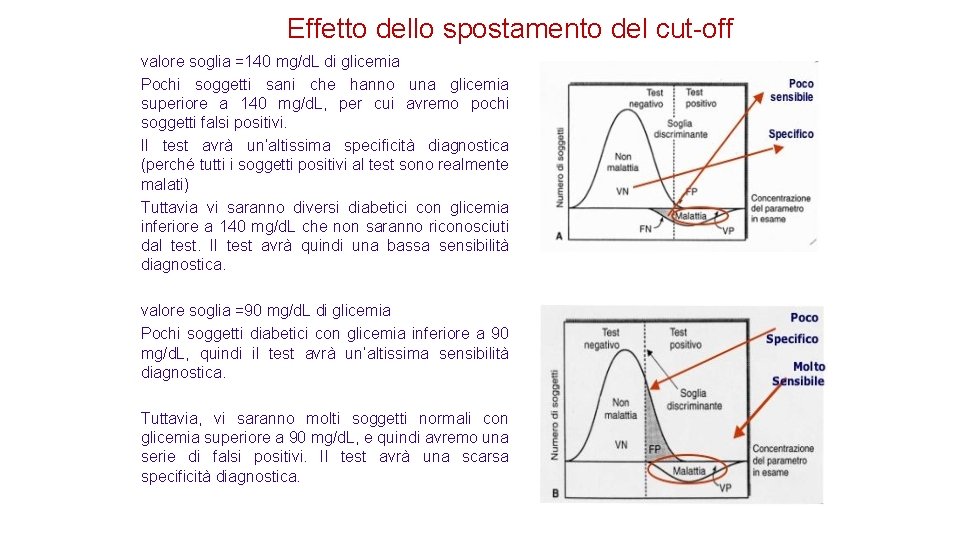
Effetto dello spostamento del cut-off valore soglia =140 mg/d. L di glicemia Pochi soggetti sani che hanno una glicemia superiore a 140 mg/d. L, per cui avremo pochi soggetti falsi positivi. Il test avrà un’altissima specificità diagnostica (perché tutti i soggetti positivi al test sono realmente malati) Tuttavia vi saranno diversi diabetici con glicemia inferiore a 140 mg/d. L che non saranno riconosciuti dal test. Il test avrà quindi una bassa sensibilità diagnostica. valore soglia =90 mg/d. L di glicemia Pochi soggetti diabetici con glicemia inferiore a 90 mg/d. L, quindi il test avrà un’altissima sensibilità diagnostica. Tuttavia, vi saranno molti soggetti normali con glicemia superiore a 90 mg/d. L, e quindi avremo una serie di falsi positivi. Il test avrà una scarsa specificità diagnostica.

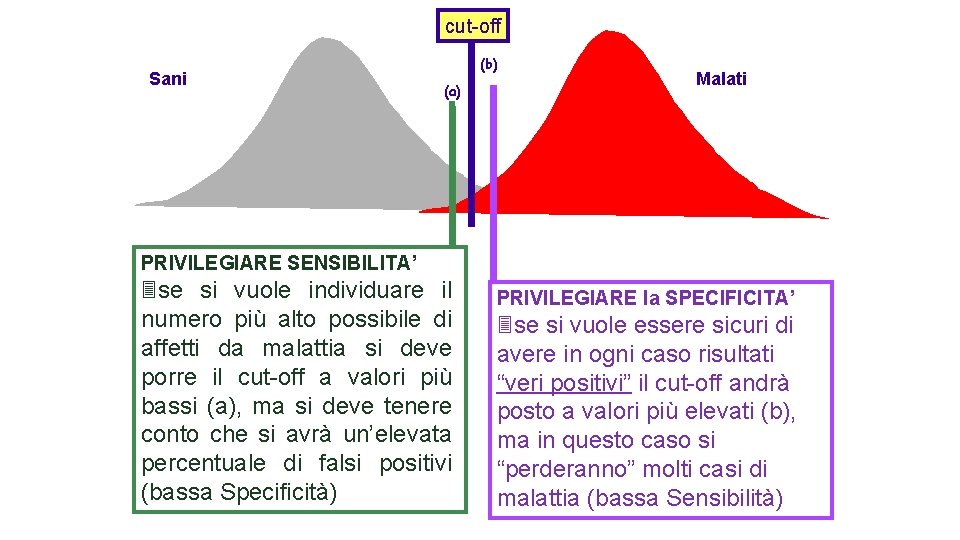
cut-off Sani (b) (a) Malati PRIVILEGIARE SENSIBILITA’ 3 se si vuole individuare il numero più alto possibile di affetti da malattia si deve porre il cut-off a valori più bassi (a), ma si deve tenere conto che si avrà un’elevata percentuale di falsi positivi (bassa Specificità) PRIVILEGIARE la SPECIFICITA’ 3 se si vuole essere sicuri di avere in ogni caso risultati “veri positivi” il cut-off andrà posto a valori più elevati (b), ma in questo caso si “perderanno” molti casi di malattia (bassa Sensibilità)

Validità diagnostica dei test di screening Negli screening, è necessario identificare tutti i soggetti affetti, anche se questo può significare un aumento di falsi positivi. Quindi, usiamo un valore soglia basso, che permetta un forte aumento della sensibilità diagnostica. • Ad esempio, nello screening effettuato sui donatori di sangue, per escludere i campioni infetti, è necessario adottare test provvisti della massima sensibilità diagnostica: infatti, se da un lato è tollerabile lo scarto di una quota considerevole di campioni non infetti (falsi positivi), dall'altro è indispensabile tutelare chi riceve la donazione e quindi non si può correre il rischio di trasfondere sangue infetto risultato falsamente negativo ai test. • Nello screening neonatale per la fenilchetonuria occorre diagnosticare la malattia alla nascita perché occorre tempestivamente porre il paziente in restrizione dietetica, per evitare danni irreparabili al sistema nervoso. Utilizzeremo quindi un test con un valore soglia basso, allo scopo di avere la massima sensibilità diagnostica ed esser certi di individuare tutti i pazienti affetti; successivamente potremo usare un secondo test più specifico per escludere quelli sani che risultavano positivi al test di screening (falsi positivi).

Validità diagnostica della mioglobina e della Troponina Per la diagnosi di infarto del miocardio, sono disponibili due marcatori biochimici, la mioglobina e la troponina. Il dosaggio della miogobina presenta una sensibilità diagnostica del 98% e una specificità diagnostica del 55%. Il dosaggio della Troponina presenta una sensibilità diagnostica pari all’ 85% e una specificità diagnostica del 100%. Inoltre la mioglobina aumenta nel siero più precocemente rispetto alla troponina. In un pronto soccorso è assolutamente necessario riconoscere quanti più soggetti possibile affetti da infarto. Quindi, la strategia più idonea è quella di utilizzare la mioglobina (che ha un’elevata sensibilità diagnostica) e successivamente la troponina (molto specifica).

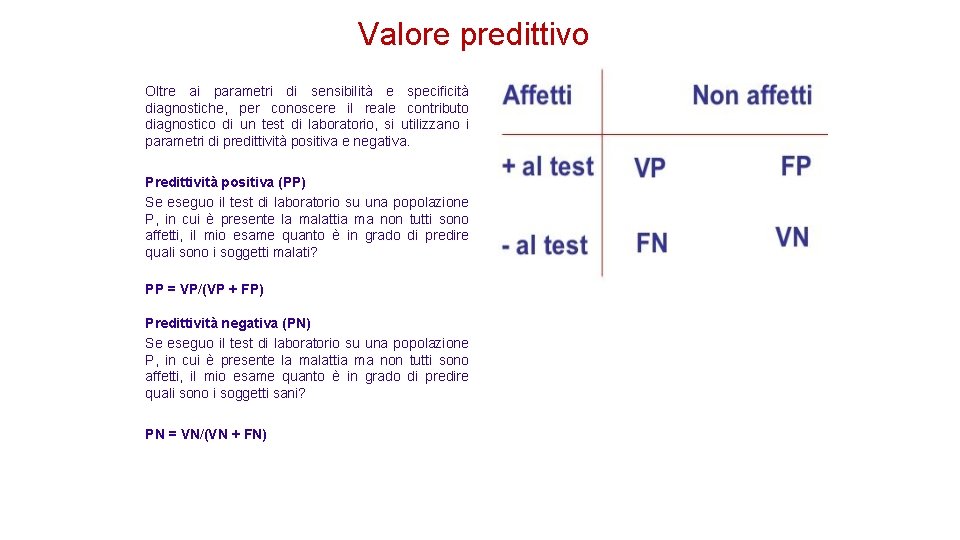
Valore predittivo Se applichiamo un test ad una popolazione mista composta da soggetti sani e malati, la capacità del test di evidenziare i soggetti malati che presentano un risultato positivo al test, oppure di soggetti sani che presentano un valore negativo al test viene definita valore predittivo

Valore predittivo Positivo La probabilità che un risultato positivo del test identifichi un soggetto malato Negativo La probabilità che un risultato negativo del test identifichi un soggetto sano Può essere considerato o per la valutazione delle caratteristiche di un test diagnostico in cui è noto il n. di sani e malati e dopo l’applicazione del test si confrontano i numeri di veri e falsi positivi e negativi; Oppure per applicazione clinica su popolazioni generali e quindi il numero dei veri positivi e falsi positivi è in funzione della prevalenza della malattia oltre che della sensibilità e specificità. Quindi il valore predittivo di un test positivo è influenzato dalla prevalenza della malattia. In questo caso sarà necessario adoperare un test di conferma.

Valore predittivo di un risultato positivo (in presenza di malattia): indica la probabilità che un soggetto con un test positivo abbia realmente la malattia VP x 100 VP + FP Valore predittivo di un risultato negativo (in assenza di malattia): indica la probabilità che un soggetto sano con un test negativo realmente non abbia la malattia VN x 100 VN + FN

Il dato di laboratorio deve essere…. • Preciso • Sensibile La precisione è subordinata alla ripetitività dei risultati sullo stesso campione in tempi diversi e da parte di operatori diversi La sensibilità esprime la probabilità che un soggetto malato presenti un test positivo • Specifico La specificità esprime la probabilità che un soggetto sano presenti un test negativo

Validità diagnostica dei test di laboratorio - Sensibilità diagnostica = VP/(VP + FN) - Specificità diagnostica = VN/(FP +VN) Dove VP (veri positivi) è la percentuale di soggetti affetti, positivi al test; FP (falsi positivi) è la percentuale di soggetti sani positivi al test; FN (falsi negativi) è la percentuale di soggetti affetti negativi al test; VN (veri negativi) la percentuale di soggetti sani, negativi al test.

Esempio 100 soggetti diabetici e 100 soggetti sani - eseguiamo la glicemia, e verifichiamo che in 90 diabetici la glicemia è superiore al massimo valore di riferimento (100 mg/d. L), ma vi sono 15 soggetti sani che hanno la glicemia alterata. Quindi: - VP: 90/100 (soggetti diabetici con test alterato) - FP: 15/100 (soggetti sani con test alterato) - FN: 10/100 (soggetti diabetici con test normale) - VN: 85/100 (soggetti sani con test normale) Quindi, la sensibilità diagnostica sarà: VP/VP+FN*100 90 / (90 + 10) = 90% La specificità diagnostica sarà: VN/VN+FP*100 85 / (15 + 85) = 85%

Valore predittivo Oltre ai parametri di sensibilità e specificità diagnostiche, per conoscere il reale contributo diagnostico di un test di laboratorio, si utilizzano i parametri di predittività positiva e negativa. Predittività positiva (PP) Se eseguo il test di laboratorio su una popolazione P, in cui è presente la malattia ma non tutti sono affetti, il mio esame quanto è in grado di predire quali sono i soggetti malati? PP = VP/(VP + FP) Predittività negativa (PN) Se eseguo il test di laboratorio su una popolazione P, in cui è presente la malattia ma non tutti sono affetti, il mio esame quanto è in grado di predire quali sono i soggetti sani? PN = VN/(VN + FN)

Esempio Predittività positiva (PP) PP = VP/(VP + FP) PP = 90 / (90 + 15) = 85. 7% Predittività negativa (PN) PN = VN/(VN + FN) PN = 85 / (85 + 10) = 89. 5% Utilizzando ancora i numeri del precedente esempio sulla glicemia e i soggetti diabetici, calcoliamo i valori di predittività: Quindi, se effettuiamo la glicemia ed ottengo un risultato positivo, avrò l’ 85. 7% di probabilità che il paziente sia affetto da diabete. Se viceversa troviamo un valore normale, avrò l’ 89. 5% di probabilità che il soggetto sia sano. Ancora una volta dobbiamo ricordare che il test di laboratorio, da solo, non è in grado di escludere o confermare con certezza una diagnosi.

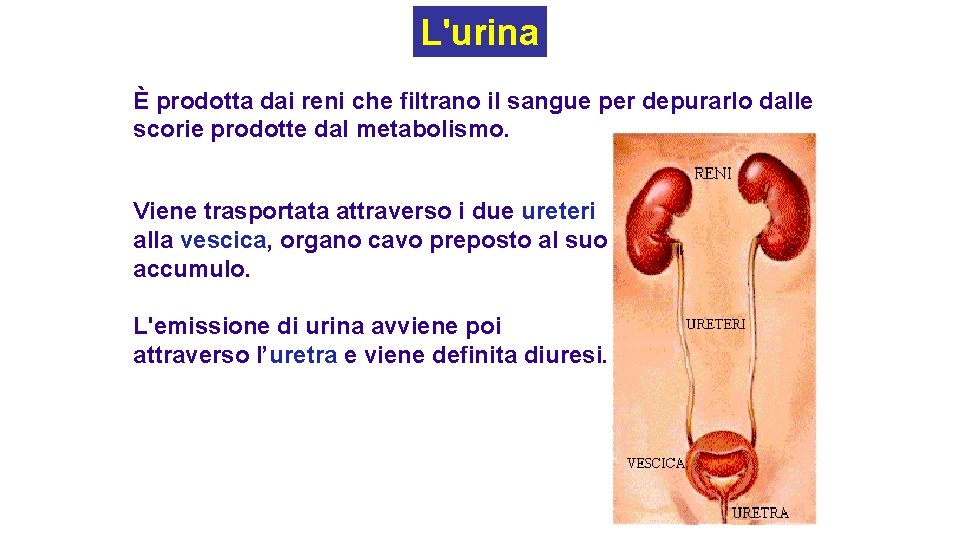
L'urina È prodotta dai reni che filtrano il sangue per depurarlo dalle scorie prodotte dal metabolismo. Viene trasportata attraverso i due ureteri alla vescica, organo cavo preposto al suo accumulo. L'emissione di urina avviene poi attraverso l’uretra e viene definita diuresi.

Un litro di urina è composto da: • acqua (960 g) • urea (20 -25 g) • azoto (10 -15 g) • cloruro di sodio (10 -16 g) • acido solforico • acido fosforico • acido cloridrico • potassio • sodio • acido urico • calcio • magnesio • acido ippurico • creatinina • urobilina • ferro • ammoniaca

Raccolta delle urine ll campione di urina può essere raccolto secondo distinte modalità, in relazione al tipo di indagine da eseguire, all’età ed allo stato del paziente. Possono essere distinte 3 differenti modalità di raccolta dell’urina: 1. Raccolta del primo mattino (per l’esame completo delle urine: l’urina è più concentrata, quindi sono più evidenti eventuali alterazioni) 2. Seconda minzione o mitto intermedio (per le analisi di chimica clinica e le indagini colturali) 3. Raccolta temporizzata (negli studi di clearance; se devono essere dosate sostanze escrete con ritmi variabili durante il giorno; se è necessario aumentare l’accuratezza di misura per sostanze presenti in concentrazione ridotta)

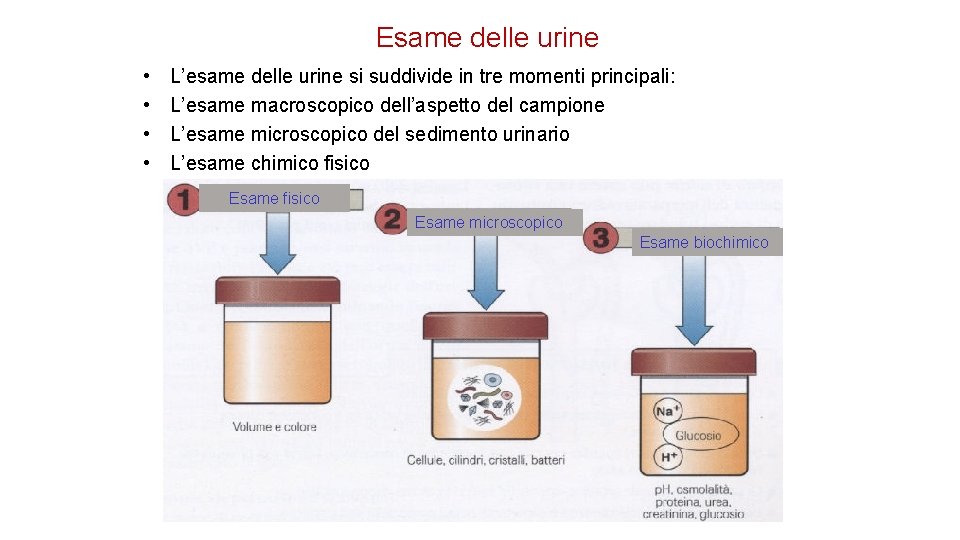
Esame delle urine • • L’esame delle urine si suddivide in tre momenti principali: L’esame macroscopico dell’aspetto del campione L’esame microscopico del sedimento urinario L’esame chimico fisico Esame microscopico Esame biochimico



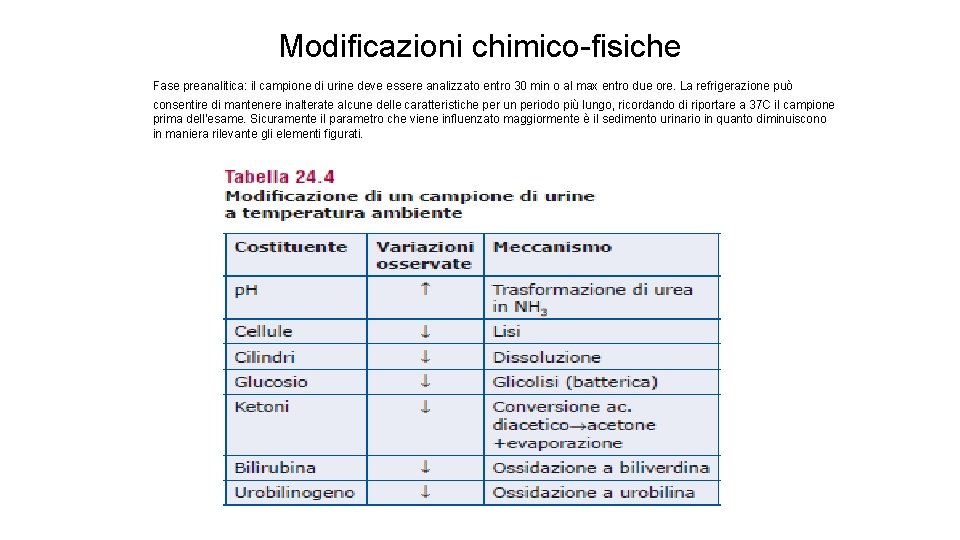
Modificazioni chimico-fisiche Fase preanalitica: il campione di urine deve essere analizzato entro 30 min o al max entro due ore. La refrigerazione può consentire di mantenere inalterate alcune delle caratteristiche per un periodo più lungo, ricordando di riportare a 37 C il campione prima dell’esame. Sicuramente il parametro che viene influenzato maggiormente è il sedimento urinario in quanto diminuiscono in maniera rilevante gli elementi figurati.

Esame fisico Volume: in quantità necessaria ad eseguire tutte le analisi necessarie. Varia in funzione dell’età

Colore Aspetto: limpido e Colore: giallo paglierino

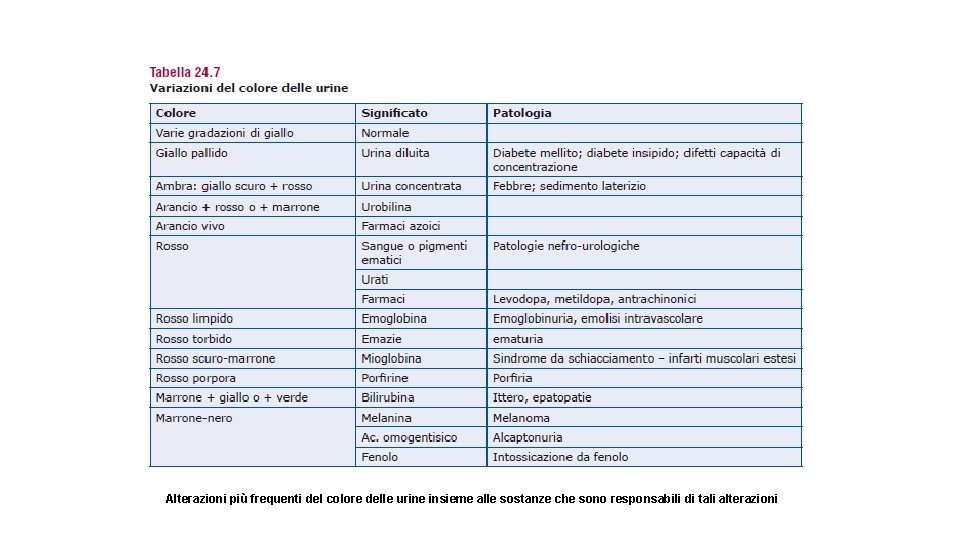
Alterazioni più frequenti del colore delle urine insieme alle sostanze che sono responsabili di tali alterazioni

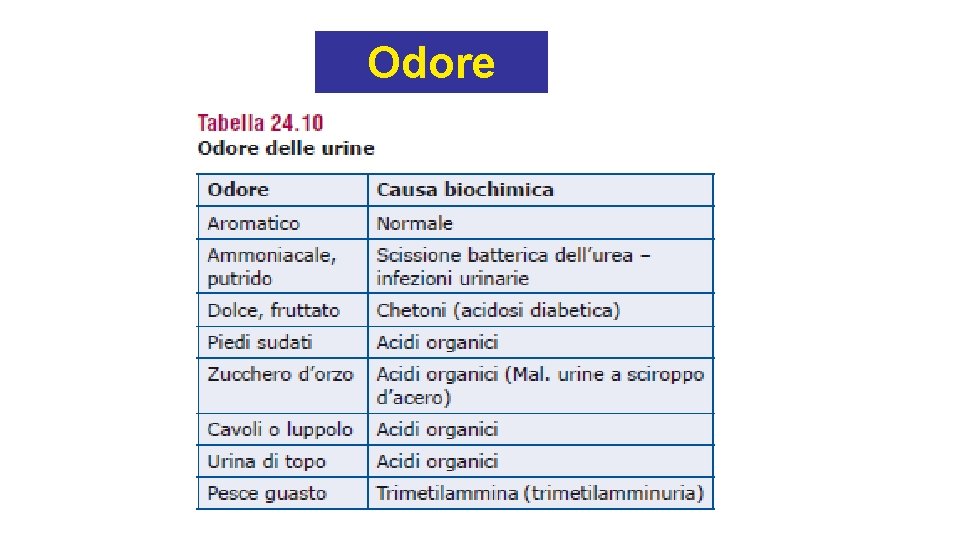
Odore

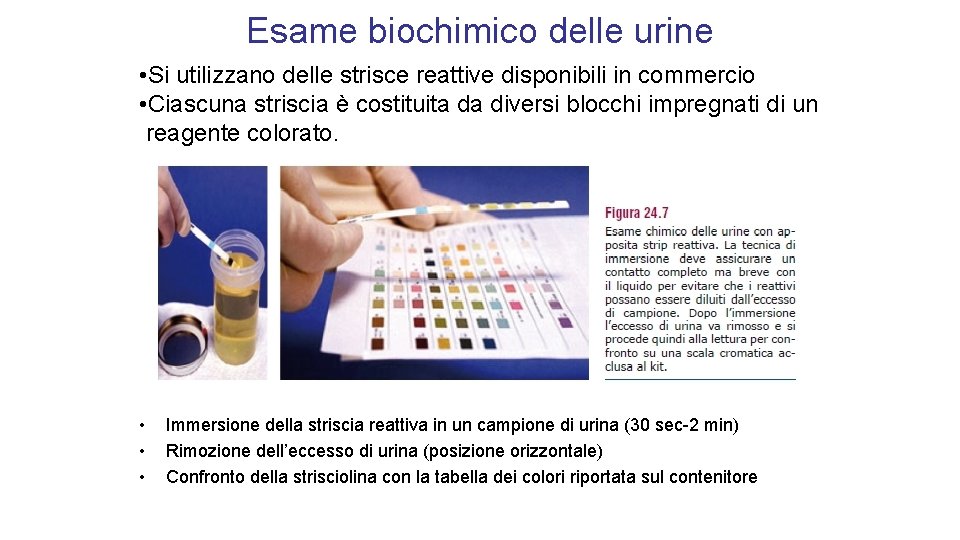
Esame biochimico delle urine • Si utilizzano delle strisce reattive disponibili in commercio • Ciascuna striscia è costituita da diversi blocchi impregnati di un reagente colorato. • • • Immersione della striscia reattiva in un campione di urina (30 sec-2 min) Rimozione dell’eccesso di urina (posizione orizzontale) Confronto della strisciolina con la tabella dei colori riportata sul contenitore

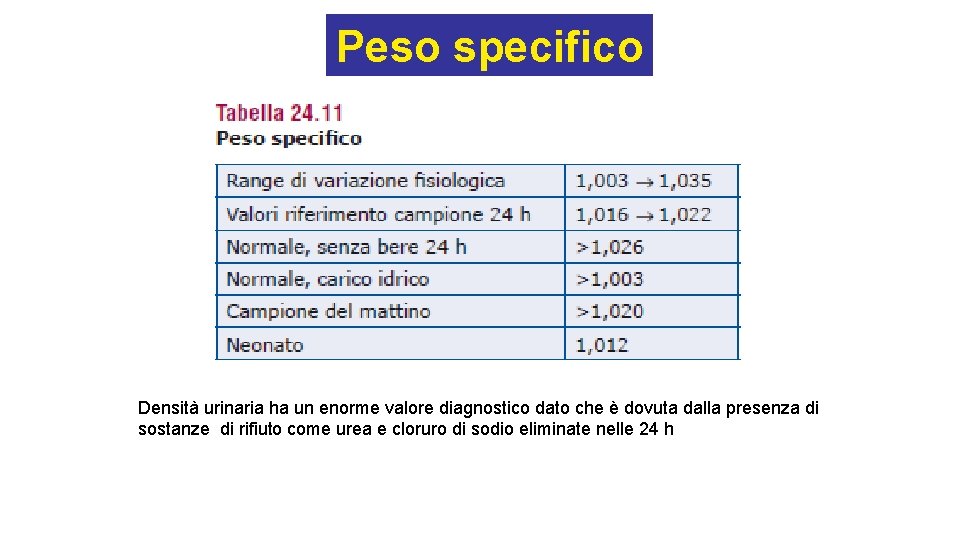
Peso specifico Densità urinaria ha un enorme valore diagnostico dato che è dovuta dalla presenza di sostanze di rifiuto come urea e cloruro di sodio eliminate nelle 24 h

Peso specifico • La capacità di produrre urine ad alto p. s indica una buona funzionalità renale, in quanto l’urina è più concentrata del plasma • Una diminuzione del p. s si ha in condizioni fisiologiche dopo assunzione abbondante di liquidi oppure in caso di insufficienza renale o per malattie extrarenali (diabete insipido, edemi, versamenti) • Un aumento del p. s urinario può dipendere in condizioni fisiologiche dopo pasti asciutti, nei mesi estivi, oppure in caso di nefropatie.

Esame chimico - Glucosio - Bilirubina - Urobilina - Corpi chetonici - Proteine - p. H - Emoglobina - Nitriti

GLUCOSIO Deve essere assente nelle urine Glicosuria: presenza di glucosio nelle urine Indica che la quantità di glucosio filtrato supera la capacità dei tubuli renali di riassorbirlo completamente. iperglicemia Può essere determinata da: • Diabete (programmare altri esami, es. glicemia a digiuno) • Gravidanza (causata da Glicosuria renale: abbassamento della soglia renale per il glucosio, anche se la glicemia è normale) • Altre cause: catecolamine (feocromocitoma), cortisolo (sindrome di Cushing, uso di steroidi), danno tubulare.

BILIRUBINA Normalmente non deve essere presente nell’urina Di colore giallo-rosso, è prodotta dalla scissione dell’emoglobina, pigmento rosso presente nei globuli rossi del sangue. E’il principale pigmento presente nella bile. Esiste nel sangue nella forma coniugata e non-coniugata In presenza di bilirubina le urine assumono colore marsala scuro. Cause: - Ostruzione meccanica delle vie biliari: calcoli, tumori delle vie biliari o del pancreas, cirrosi epatica - Danno all’epatocita: epatite da virus, alcool, farmaci, avvelenamento da arsenico, fosforo e piombo

UROBILINOGENO Valori normali: 0, 2 mg (milligrammi) nelle urine raccolte nell’arco delle 24 ore Prodotto di trasformazione, per mezzo dei batteri intestinali, della bilirubina coniugata Entra a far parte del circolo enteroepatico. Nell’urina è presente solo in tracce, quindi ha un significato diagnostico meno rilevante della bilirubina. Si possono rilevare livelli alti di urobilinogeno nelle urine quando il turnover della bilirubina è aumentato (emolisi) Valori inferiori possono essere determinati da ostruzione delle vie biliari.

CORPI CHETONICI Non devono essere presenti nell’urina Sono dei composti chimici, formati dalla degradazione di altri composti chimici (acidi grassi) e ciò succede quando l’organismo non ha più una quantità sufficiente di zuccheri. La loro presenza indica che l’organismo utilizza acidi grassi per produrre energia, piuttosto che immagazzinarli Chetoacidosi diabetica Chetoacidosi alcolica Iponutrizione (sottonutrizione)

PROTEINE Dovrebbero essere assenti, ma a volte sono presenti in quantità minime e non patologiche e comunque in quantità inferiore a 150 mg nelle urine delle 24 ore. Proteinuria: escrezione abnorme di proteine dai reni Presenza significativa può essere determinata da patologie che danneggiano il glomerulo L’entità del danno glomerulare può essere valutata in base a: - Quantità della proteinuria - Peso molecolare delle proteine eliminate

p. H valori normali: variano da 4. 5 a 7. 5 I tubuli renali normalmente operano l’escrezione di ioni idrogeno, con meccanismi che assicurano la regolazione della concentrazione di ioni idrogeno nel sangue p. H maggiore di 7. 5 può essere determinato da dieta ricca di frutta, oppure da alcalosi metabolica o respiratoria. p. H inferiore a 4. 5 è indice di acidosi che può essere determinata da dieta ricca di proteine, da digiuno prolungato, da acidosi metabolica o respiratoria.

EMOGLOBINA (Hb) Non deve essere presente nell’urina La presenza nell’urina può essere determinata da anemia (dovuta a una produzione ridotta o difettosa di globuli rossi o a un ritmo troppo elevato della loro distruzione) e da emolisi E’ importante distinguere: - Emoglobinuria presenza di emoglobina nell’urina - Ematuria presenza di sangue nell’urina

Nitriti • Sono indice di infezione delle vie urinarie • La positività indica batteriuria >100. 000/ml e batteri che metabolizzano l’azoto ed hanno nitriti come prodotto terminale (E. Coli, Proteus, Klebsiella, Pseudomonas, Stafilococco, Enterococco, ecc. )

Esame microscopico sedimento urinario

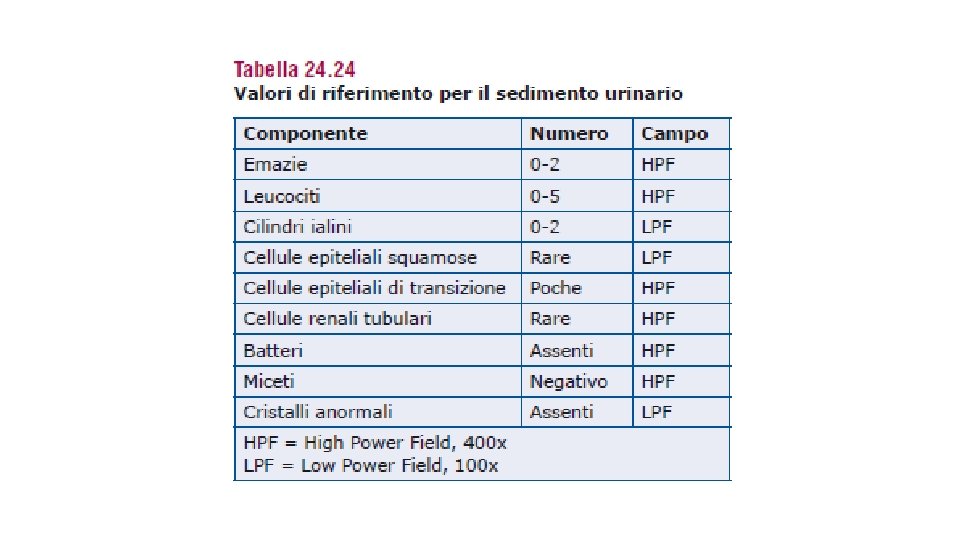
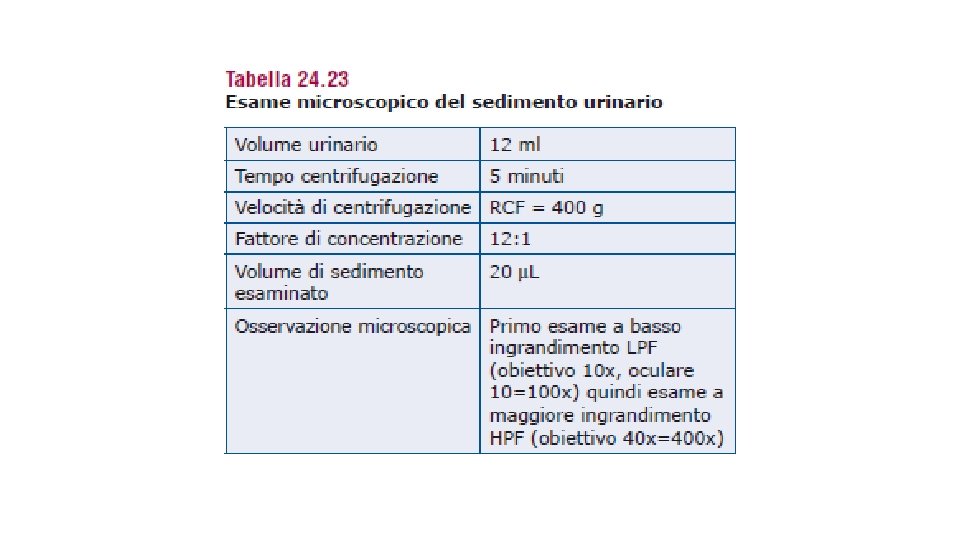
SEDIMENTO URINARIO • É costituito dagli elementi presenti nell’urina in forma di sospensione che si raccolgono nella provetta dopo centrifugazione • spesso fornisce informazioni essenziali non ottenibili con il solo esame chimico fisico • I principali elementi che si possono riscontrare dall’analisi al microscopio sono i globuli rossi, i globuli bianchi e i cilindri • Si possono, inoltre, osservare cristalli, cellule epiteliali (prodotte dallo sfaldamento delle vie urinarie) e anche batteri e parassiti • In condizioni normali, nell’urina non si dovrebbero riscontrare questi elementi e quindi il sedimento dovrebbe essere quasi nullo





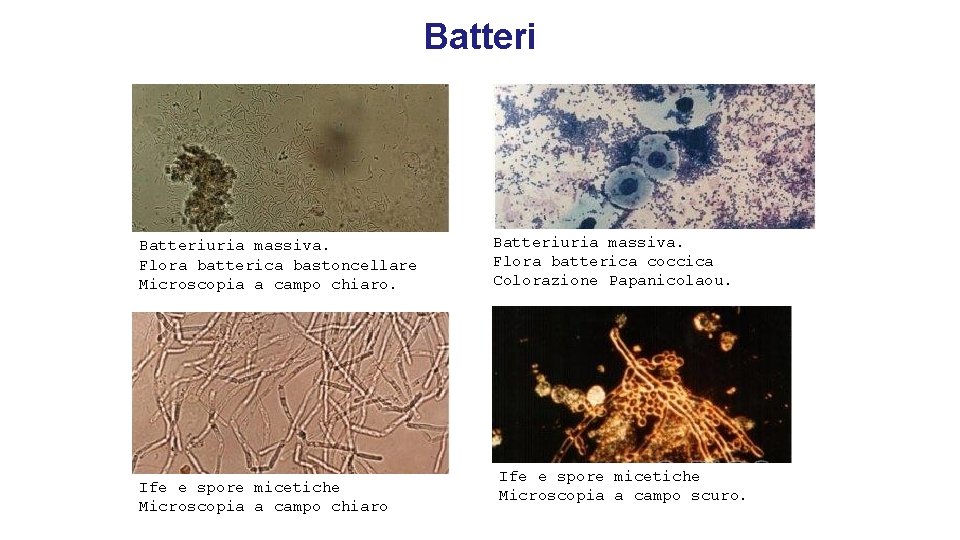
Batteriuria massiva. Flora batterica bastoncellare Microscopia a campo chiaro. Ife e spore micetiche Microscopia a campo chiaro Batteriuria massiva. Flora batterica coccica Colorazione Papanicolaou. Ife e spore micetiche Microscopia a campo scuro.

URINOCOLTURA Esame delle urine per accertare lo sviluppo di batteri che possono essere responsabili di infezioni delle vie urinarie. Qualora vengano riscontrate infezioni, può essere eseguito l’antibiogramma, che permette di stabilire quale sia l’antibiotico più adatto per sconfiggere il batterio. Antibiogramma Questo è un esame per testare in vitro la sensibilità di un agente batterico, individuato in un materiale biologico prelevato, ad esempio urine, escreato, muco, ecc. , verso un determinato antibiotico. Convenzionalmente si testa la resistenza o la sensibilità del microrganismo espresse in: • R (resistenza) • MS (media sensibilità) • S (sensibile)

1) Si piastrano 1 o 2 gocce di sospensione batterica sul terreno di coltura in modo che la piastra sia omogeneamente ricoperta dal campione. 2) Si dispensano su dischetti di carta assorbente sterili aliquote di 20 ml degli antibiotici che si desidera confrontare. le piastre vanno messe a + 4°C per 2 ore Trascorso questo tempo incubare la piastra a 37°C per 18 -24 ore. 3) Si divide la piastra in spicchi, uno per ciascun antibiotico, e si deposita al centro di ogni spicchio il dischetto corrispondente. 4) Valutare il diametro di inibizione dello sviluppo per ogni antibiotico.