IDROLISI DEI SALI Molti sali solubili contengono un

IDROLISI DEI SALI Molti sali solubili contengono un anione o un catione che possono reagire con acqua rendendo le loro soluzioni ACIDE o BASICHE. Il p. H della soluzione di un sale Caso I: Sali di acido forte e base forte (es. Na. Cl) 1) Na. Cl → Na+ + Cl- (dissociazione completa) 2) Na+ + 2 H 2 O ↛ H 3 O+ + Na. OH (nessuna idrolisi) 3) Cl- + H 2 O ↛ HCl + OH- (nessuna idrolisi) Non hanno idrolisi i sali di: (Br-, I-, Cl. O 4 -, NO 3 -, Cl-) Na+ e Cl- sono specie coniugate debolissime di elettroliti forti e, quindi, non hanno proprietà acide o basiche. Il p. H della soluzione sarà pari a quello dell’acqua pura (p. H = 7). Caso II: Sali di acido forte e base debole (es. NH 4 Cl) 1) NH 4 Cl → NH 4+ + Cl- (dissociazione completa) 2) Cl- + H 2 O ↛ HCl + OH- (nessuna idrolisi) 3) NH 4 + H 2 O ⇄ H 3 + O+ + NH 3 (idrolisi parziale) HA + H 2 O ⇄ H 3 O+ + A- [H 3 O+] = √Ka. CHA = √KWCS/ Kb Si tratta come le soluzioni di acidi deboli: [H 3 O+] = (p. H acido) √Ka. CHA
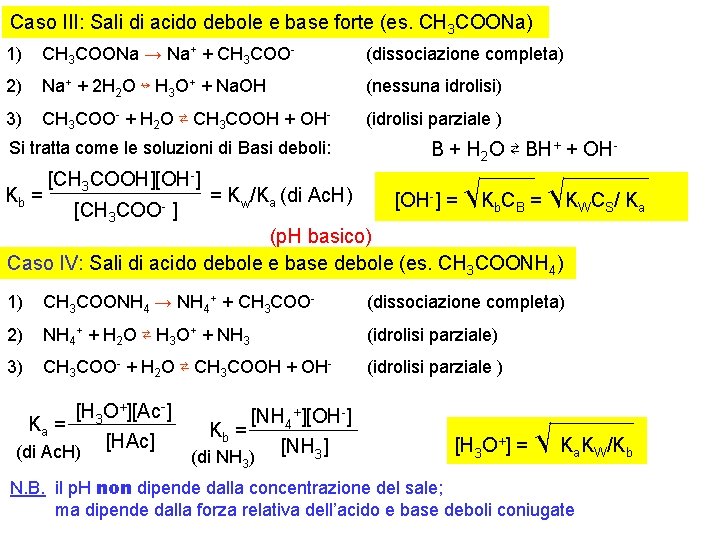
Caso III: Sali di acido debole e base forte (es. CH 3 COONa) 1) CH 3 COONa → Na+ + CH 3 COO- (dissociazione completa) 2) Na+ + 2 H 2 O ↛ H 3 O+ + Na. OH (nessuna idrolisi) 3) CH 3 COO- + H 2 O ⇄ CH 3 COOH + OH- (idrolisi parziale ) Si tratta come le soluzioni di Basi deboli: Kb = [CH 3 COOH][OH-] [CH 3 COO- ] = Kw/Ka (di Ac. H) B + H 2 O ⇄ BH+ + OH[OH-] = √Kb. CB = √KWCS/ Ka (p. H basico) Caso IV: Sali di acido debole e base debole (es. CH 3 COONH 4) 1) CH 3 COONH 4 → NH 4+ + CH 3 COO- (dissociazione completa) 2) NH 4+ + H 2 O ⇄ H 3 O+ + NH 3 (idrolisi parziale) 3) CH 3 COO- + H 2 O ⇄ CH 3 COOH + OH- (idrolisi parziale ) [H 3 O+][Ac-] Ka = [HAc] (di Ac. H) [NH 4+][OH-] Kb = [NH 3] (di NH 3) [H 3 O+] = √ Ka. KW/Kb N. B. il p. H non dipende dalla concentrazione del sale; ma dipende dalla forza relativa dell’acido e base deboli coniugate

Soluzioni tampone • Una soluzione acquosa si definisce tampone quando il suo p. H varia in misura relativamente piccola all’aggiunta di acidi o di basi. • Le soluzioni tampone contengono o un acido debole e un sale dell’acido debole, o una base debole e un sale della base debole, in quantità approssimativamente uguali. Caso I: Miscela di un acido debole HA e di un suo sale con una base forte Na. A Concentrazione nominale dell’acido : CHA; concentrazione nominale del sale : CS; [H 3 O+][A-] Ka = [HA] [H 3 O+ ] Ka[HA] = [A-] [H 3 O+ ] Ka. CHA = CS p. H = p. Ka + log(CS/CHA) Caso II: Miscela di una base debole B e di un suo sale con un acido forte BHCl Concentrazione nominale della base : CB; concentrazione nominale del sale : CS; [BH+][OH-] Kb = [B] Kb[B] [OH ] = [BH+] p. H = 14 - p. Kb + log(CB/CS) [OH-] K b CB = CS

Potere tampone Se aggiungiamo 10 -2 equivalenti di HCl ad un litro di acqua pura (p. H = 7), il p. H si abbassa di ben 5 unità (p. H = 2). Facciamo la stessa aggiunta ad una soluzione tampone, costituita da un acido HA ([HA] = 0. 1 M; Ka =1. 8 • 10 -5; p. Ka = 4. 75) e dal suo sale sodico Na. A ([A-] = 0. 1 M), il cui p. H = p. Ka = 4. 75. H 3 O+ + A ⇄ H 2 O + HA [HA] = 0. 1+0. 01 = 0. 11 M; [A-] = 0. 1 -0. 01 = 0. 09 M p. H = p. Ka + log(CS/CHA) = 4. 75 + log(0. 09/0. 11) = 4. 66 Il p. H si è abbassato di sole 4. 75 – 4. 66 = : 0. 09 unità
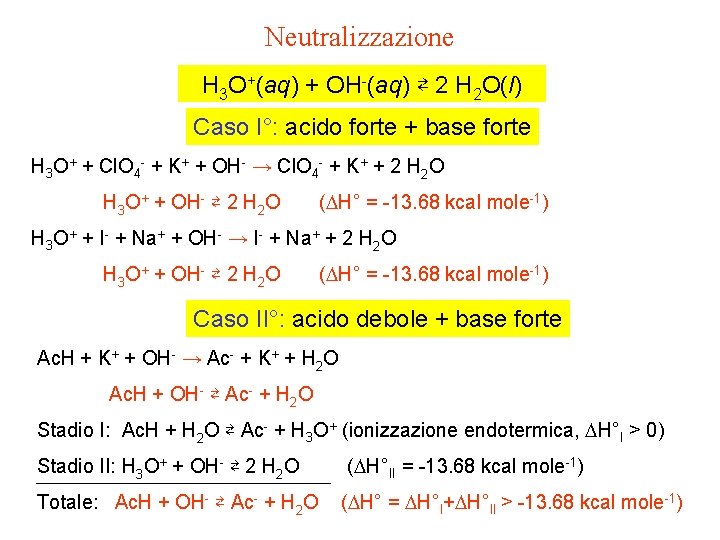
Neutralizzazione H 3 O+(aq) + OH-(aq) ⇄ 2 H 2 O(l) Caso I°: acido forte + base forte H 3 O+ + Cl. O 4 - + K+ + OH- → Cl. O 4 - + K+ + 2 H 2 O H 3 O+ + OH- ⇄ 2 H 2 O (DH° = -13. 68 kcal mole-1) H 3 O+ + I- + Na+ + OH- → I- + Na+ + 2 H 2 O H 3 O+ + OH- ⇄ 2 H 2 O (DH° = -13. 68 kcal mole-1) Caso II°: acido debole + base forte Ac. H + K+ + OH- → Ac- + K+ + H 2 O Ac. H + OH- ⇄ Ac- + H 2 O Stadio I: Ac. H + H 2 O ⇄ Ac- + H 3 O+ (ionizzazione endotermica, DH°I > 0) Stadio II: H 3 O+ + OH- ⇄ 2 H 2 O Totale: Ac. H + OH- ⇄ Ac- + H 2 O (DH°II = -13. 68 kcal mole-1) (DH° = DH°I+DH°II > -13. 68 kcal mole-1)
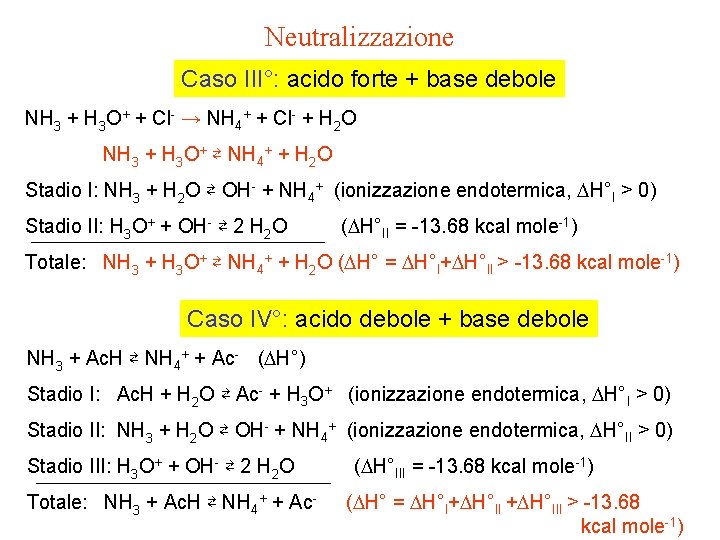
Neutralizzazione Caso III°: acido forte + base debole NH 3 + H 3 O+ + Cl- → NH 4+ + Cl- + H 2 O NH 3 + H 3 O+ ⇄ NH 4+ + H 2 O Stadio I: NH 3 + H 2 O ⇄ OH- + NH 4+ (ionizzazione endotermica, DH°I > 0) Stadio II: H 3 O+ + OH- ⇄ 2 H 2 O (DH°II = -13. 68 kcal mole-1) Totale: NH 3 + H 3 O+ ⇄ NH 4+ + H 2 O (DH° = DH°I+DH°II > -13. 68 kcal mole-1) Caso IV°: acido debole + base debole NH 3 + Ac. H ⇄ NH 4+ + Ac- (DH°) Stadio I: Ac. H + H 2 O ⇄ Ac- + H 3 O+ (ionizzazione endotermica, DH°I > 0) Stadio II: NH 3 + H 2 O ⇄ OH- + NH 4+ (ionizzazione endotermica, DH°II > 0) Stadio III: H 3 O+ + OH- ⇄ 2 H 2 O Totale: NH 3 + Ac. H ⇄ NH 4+ + Ac- (DH°III = -13. 68 kcal mole-1) (DH° = DH°I+DH°III > -13. 68 kcal mole-1)

Titolazioni acido-base Equivalenti di reattivo a titolo noto: V 0 N 0 Equivalenti di reattivo a titolo incognito: V 1 N 1 buretta All’equivalenza: V 0 N 0 = V 1 N 1 La reazione deve essere: 1) completa; 2) veloce; 3) punto di equivalenza rivelabile. V 0 N 0 H 3 O++ OH- ⇄ 2 H 2 O Basi forti per titolare acidi forti e deboli Acidi forti per titolare basi forti e deboli V 1 N 1 -V 0 N 0 + Zona 1: Eccesso di V 1 N 1 [H 3 O ] = V 1+V 0 All’equivalenza: [H 3 O+] = [OH-] = 10 -7 M Zona 2: Eccesso di V 0 N 0 [OH-] V 0 N 0 -V 1 N 1 = V 1+V 0 V 1 N 1 rubinetto indicatore colorimetrico
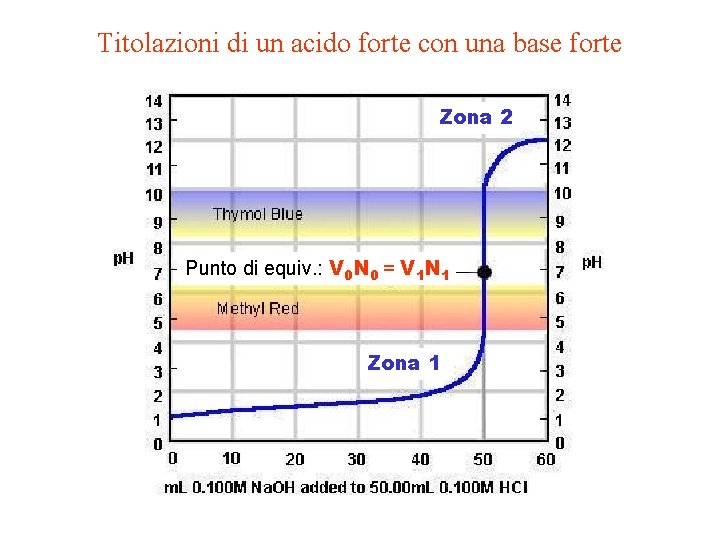
Titolazioni di un acido forte con una base forte Zona 2 Punto di equiv. : V 0 N 0 = V 1 N 1 Zona 1
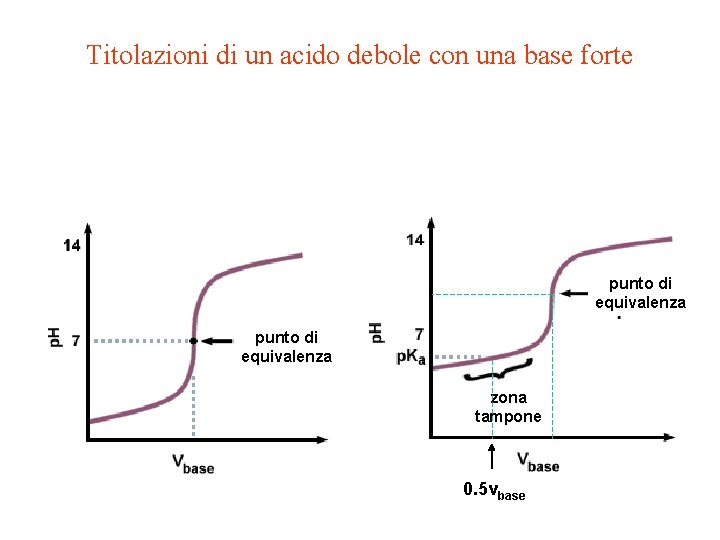
Titolazioni di un acido debole con una base forte punto di equivalenza zona tampone 0. 5 vbase
![Titolazioni di un acido debole con una base forte [OH-] = [H 3 O+ Titolazioni di un acido debole con una base forte [OH-] = [H 3 O+](http://slidetodoc.com/presentation_image_h/d99d346975f9ff2dd66d1f992862e03f/image-10.jpg)
Titolazioni di un acido debole con una base forte [OH-] = [H 3 O+ ] Ka[HA] = [A-] punto di equivalenza [H 3 O+] = √Ka. CHA acido debole acido forte √KWCS/ Ka [OH-] ≃ CB
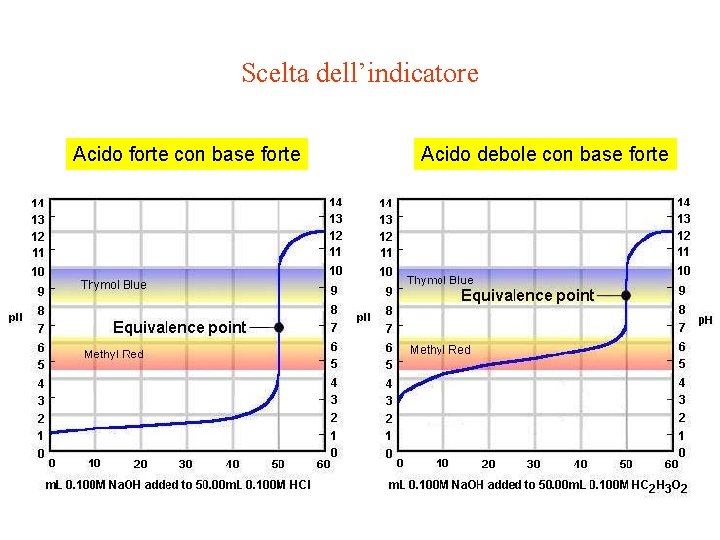
Scelta dell’indicatore Acido forte con base forte Acido debole con base forte
![Titolazioni di una base debole con un acido forte [OH-] = K b CB Titolazioni di una base debole con un acido forte [OH-] = K b CB](http://slidetodoc.com/presentation_image_h/d99d346975f9ff2dd66d1f992862e03f/image-12.jpg)
Titolazioni di una base debole con un acido forte [OH-] = K b CB = CS base forte √ K b CB base debole punto di equivalenza [H 3 O+] = √KWCS/ Kb [H 3 O+] ≃ CHA
- Slides: 12