Scheikunde Chemie overal Week 1 1 1 Chemie
































































- Slides: 79

Scheikunde Chemie overal Week 1

1. 1 Chemie om je heen • Scheikunde is overal – Scheiden of zuiveren van stoffen – Veranderen van grondstoffen in bruikbare stoffen – Drinkwater uit zeewater – Poetsen – Enz.

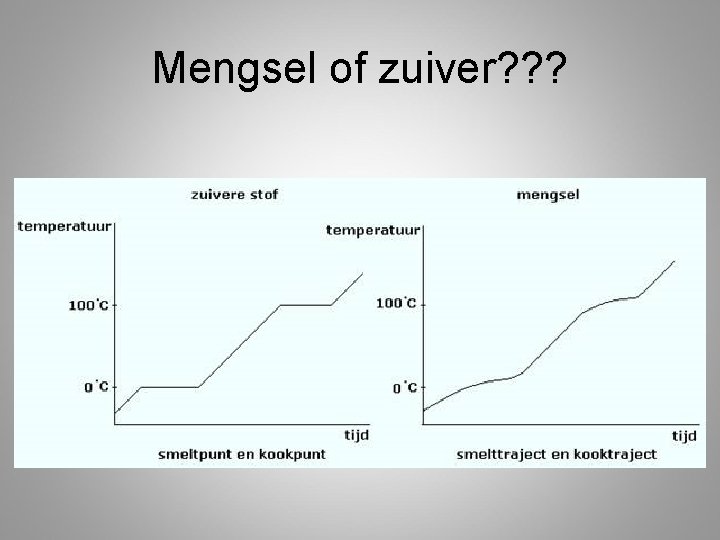
1. 2 Zuivere stoffen en mengsels • Zuivere stof: – Maar 1 soort deeltjes (moleculen) – Niet kleiner te krijgen – Vb: gedestilleerd water, suiker • Mengsel (onzuiver): – Meerdere soorten deeltjes (moleculen) – Kun je door scheiden uit elkaar halen – Vb: suikerwater

Stofeigenschappen – Kleur – Geur – Smaak – Smeltpunt en kookpunt – Dichtheid of soortelijke massa – oplosbaarheid – Brandbaarheid

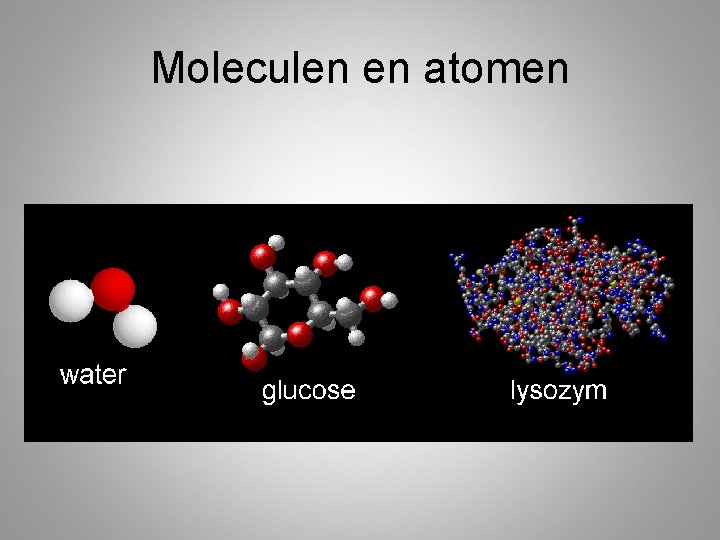
Moleculen en atomen

Element of een verbinding • Een zuivere stof kan een element of een verbinding zijn • Element bestaat uit 1 soort atomen • Verbinding bestaat uit meerdere soorten atomen

Elementen • Fientje Cliedert Bruine Inkt Op Haar Neus – Fluor (F), – Chloor (Cl), – Broom (Br), – Jood (I), – Zuurstof (O), – Waterstof (H), – Stikstof (N) • Twee atomige elementen

Mengsel of zuiver? ? ?

Hydrofiel/hydrofoob • Hydro = water • Fiel = houden van • Foob = vrezen • Hydrofiel = houdt van water – Lost dus makkelijk op in water (zout) • Hydrofoob = Houdt niet van water – Lost dus niet makkelijk op in water (Olie)

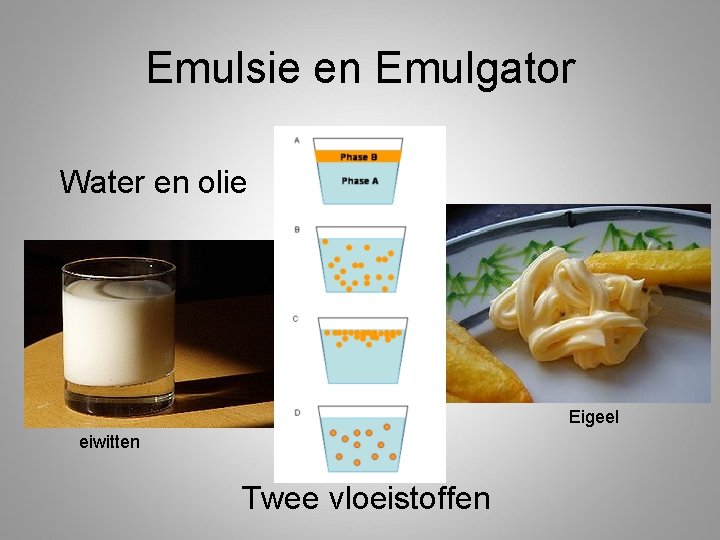
Soorten mengsels • Oplossing: helder, doorzichtig – Kleurloos of gekleurd (nooit wit) • Suspensie: troebel, ondoorzichtig – wit of gekleurd (nooit kleurloos) – Vaste stof in vloeistof die niet goed oplossen • Emulsie: troebel, ondoorzichtig – Wit of gekleurd (nooit kleurloos) – Vloeistof in vloeistof die niet goed oplossen

Emulsie en Emulgator Water en olie Eigeel eiwitten Twee vloeistoffen

Hoe werkt een emulgator • Kop en staart principe • Kop is hydrofiel en staart is hydrofoob

Scheikunde Week 2

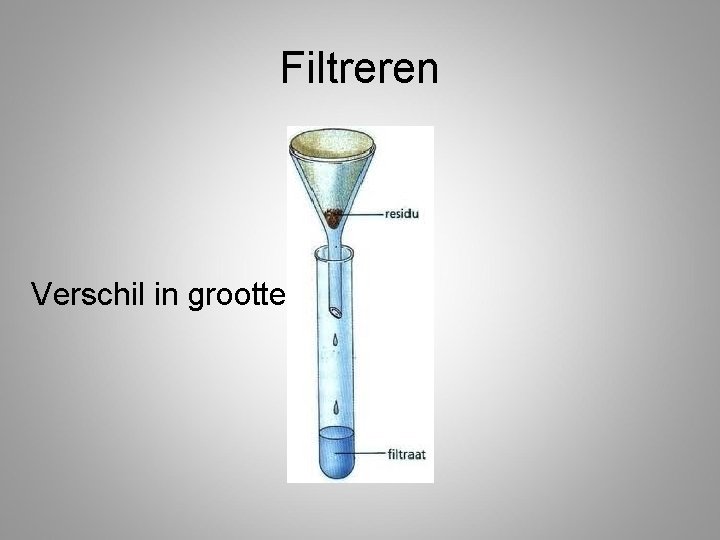
1. 3 Scheidingsmethoden • • • Methode Zeven Filtreren Indampen Destilleren Extraheren Bezinken verschil in eigenschap deeltjesgrootte kookpunt oplosbaarheid dichtheid

Zeven Deeltjesgrootte

Filtreren Verschil in grootte

Bezinken of Centrifugeren • Verschil in massa of dichtheid • Bezinken

Indampen Verschil in kookpunt

Destilleren Verschil in kookpunt

Extraheren • Twee vaste stoffen uit elkaar halen • Een vaste stof eerst oplossen en daarna filtreren en indampen • Voorbeeld zand en zout • Verschil in oplosbaarheid

Adsorberen • Bepaalde stoffen aan een stof onttrekken • Vaak kleurstoffen • Bijv – actieve kool en limonade siroop – Gasmaskers – Norrit (allemaal actieve kool)

Chromatograferen • Verschil in aanhechtingsvermogen en oplosbaarheid van het oplosmiddel • Bij zuivere stof 1 vlek bij mengsel meerdere vlekken

Scheikunde week 3

Bouwstenen van stoffen

2. 2 De bouw van een atoom • Modellen • Dalton: een atoom is een massief bolletje. Elk atoomsoort heeft zijn eigen afmetingen

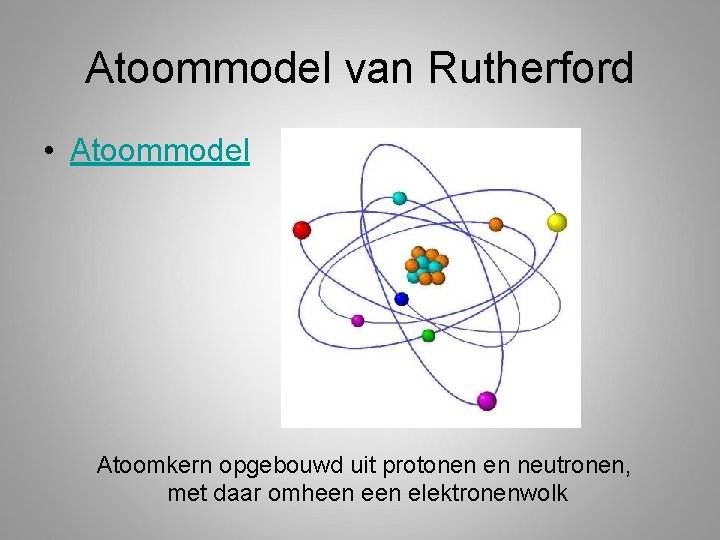
Atoommodel van Rutherford • Atoommodel Atoomkern opgebouwd uit protonen en neutronen, met daar omheen elektronenwolk

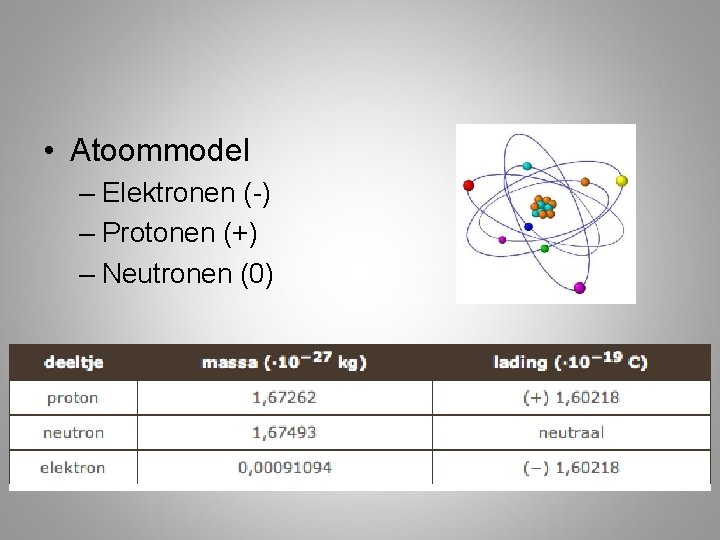
• Atoommodel – Elektronen (-) – Protonen (+) – Neutronen (0)

Atoomnummer en massagetal • Atoomnummer geeft aan hoeveel protonen en elektronen in een atoom zitten • Massagetal geeft de som van protonen en neutronen aan

Voorbeeld K atoomnummer: 19 K massagetal: 39 Aantal protonen en elektronen= 19 Aantal neutronen= 39 -19= 20

Elektronen-verdeling • De elektronen zijn over schillen verdeeld: Schil naam 1 e schil K schil Maximaal aantal elektronen 2 2 e schil L schil 8 3 e schil M schil 18 4 e schil N schil 32 • De elektronen worden van binnenuit naar buiten toe opgevuld • Uit het periodiek systeem is de elektronen-verdeling (elektronenconfiguratie) per atoom af te leiden

Het atoomnummer geeft het aantal protonen in de kern aan Dit komt overeen met de kernlading (+) en het aantal elektronen in de elektronenwolk (-)

Elektronenconfigatie: elektronenverdeling over de 4 schillen (banen) Valentie-elektronen: De elektronen in de buitenste schil

Isotopen • Isotopen zijn elementen met hetzelfde atoomnummer maar met een verschillend massagetal • Aantal neutronen bij een atoom verschillen • Bijv waterstof: – “Gewoon” waterstof 1 proton geen neutronen – “Zwaar” waterstof 1 proton 1 neutron – Tritium 1 proton 2 neutronen

Chloor Lichtere soort komt 3 x zovaak voor Het gemiddelde massagetal wordt dan: Massagetal: (3*35+1*37)/4 = 35, 5 Dit is de atoommassa!!!

Scheikunde Week 4

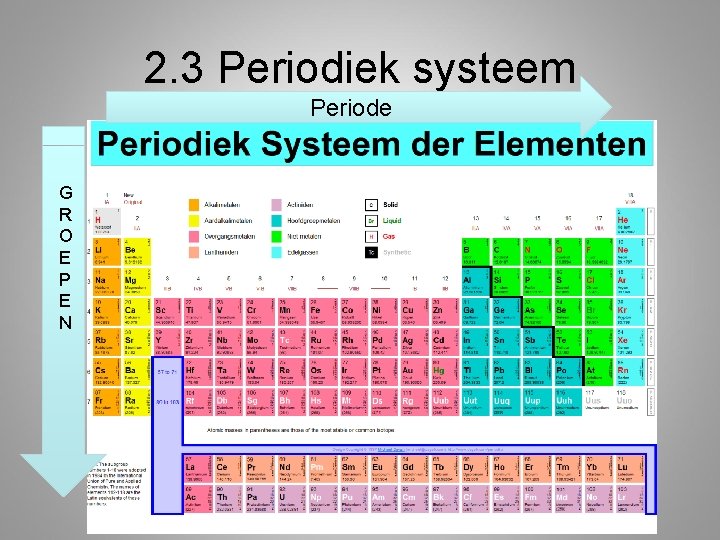
2. 3 Periodiek systeem Periode G R O E P E N

Groepen • Groep 1 Alkalimetalen (Film) – Reageren heftig met water • Groep 2 Aardalkalimetalen – Reageren heftig met lucht (felle vlam) • Groep 17 Halogenen – F, Cl, Br, I reageren goed metalen • Groep 18 Edelgassen – Verbinden zich niet en tasten niets aan

Atomen • Kleinste deeltjes van een molecuul • Symbolen – Eerste letter van de Latijnse naam – Bijvoorbeeld: • Koolstof = Carboneum dus C • Koper = Cuprum dus Cu • Denk aan hoofdletter kleine letter!!!

Elementen • Fientje Cliedert Bruine Inkt Op Haar Neus – Fluor (F), – Chloor (Cl), – Broom (Br), – Jood (I), – Zuurstof (O), – Waterstof (H), – Stikstof (N) • Twee atomige elementen

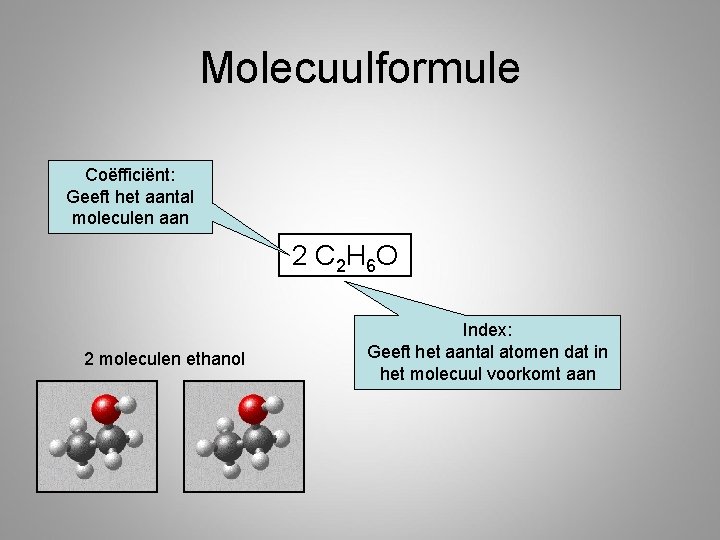
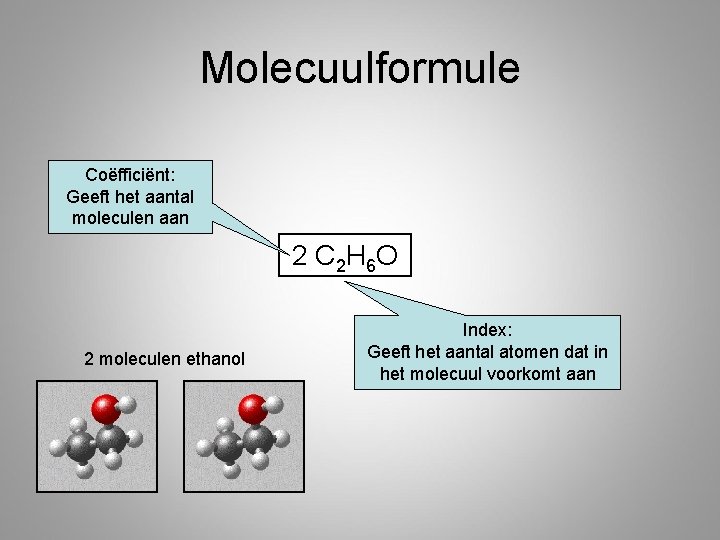
Molecuulformule Coëfficiënt: Geeft het aantal moleculen aan 2 C 2 H 6 O 2 moleculen ethanol Index: Geeft het aantal atomen dat in het molecuul voorkomt aan

Atoombinding • Covalentie: het aantal elektronen dat een atoom beschikbaar heeft voor de atoombinding

Atoombinding Er zijn ook atomen die meer dan een covalentie hebben. Bijvoorbeeld: Zwavel (S) covalentie 2, 4 en 6

Molecuulformule • Koolstof en zwavel atomen Covalentie aantallen vereenvoudigen : C : 4 : 2 : 1 S 2 4 2 Formule : CS 2 Koolstofdisulfide

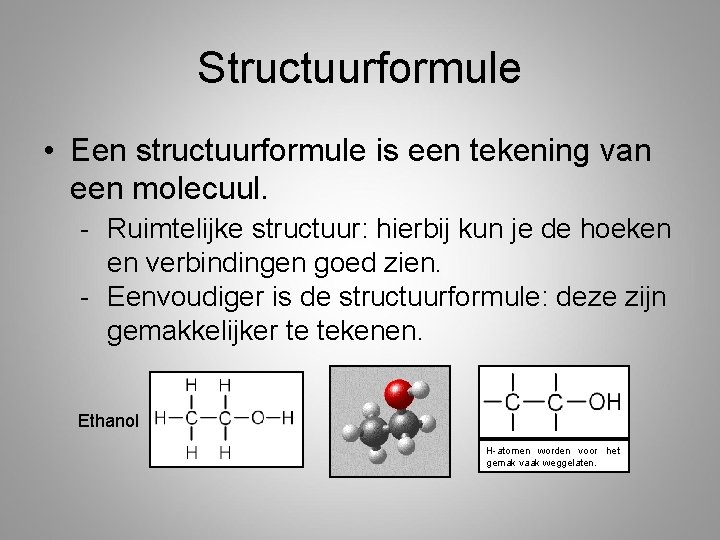
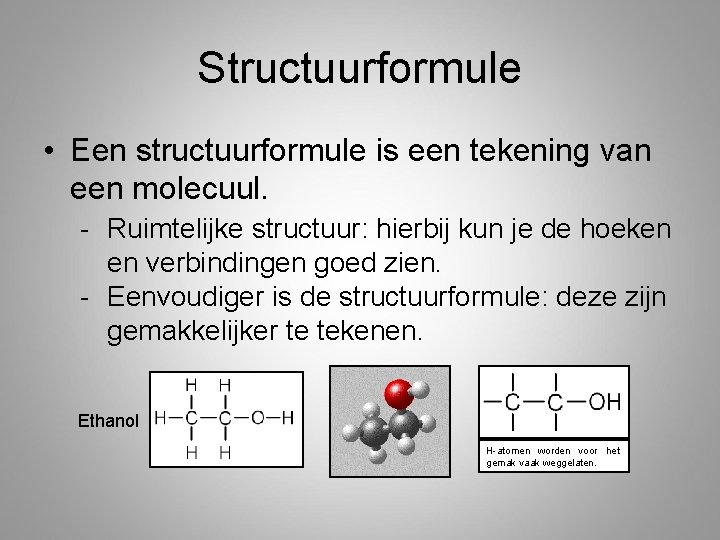
Structuurformule • Een structuurformule is een tekening van een molecuul. - Ruimtelijke structuur: hierbij kun je de hoeken en verbindingen goed zien. - Eenvoudiger is de structuurformule: deze zijn gemakkelijker te tekenen. Ethanol H-atomen worden voor het gemak vaak weggelaten.

Scheikunde Week 5

2. 4 Ionen • • • Atomen met een lading Sterkere aantrekkingskracht Hogere smeltpunten Kern blijft altijd gelijk Elektronen kunnen veranderen Ionen willen lijken op edelgassen

Ionen • Atomen kunnen elektronen opnemen of afstaan (buitenste schil) • Atomen willen zijn als edelgas • Atomen uit groep 1 staan makkelijk 1 elektron af (elektron positief) • Atomen uit groep 17 nemen makkelijk 1 elektron op (elektron negatief)

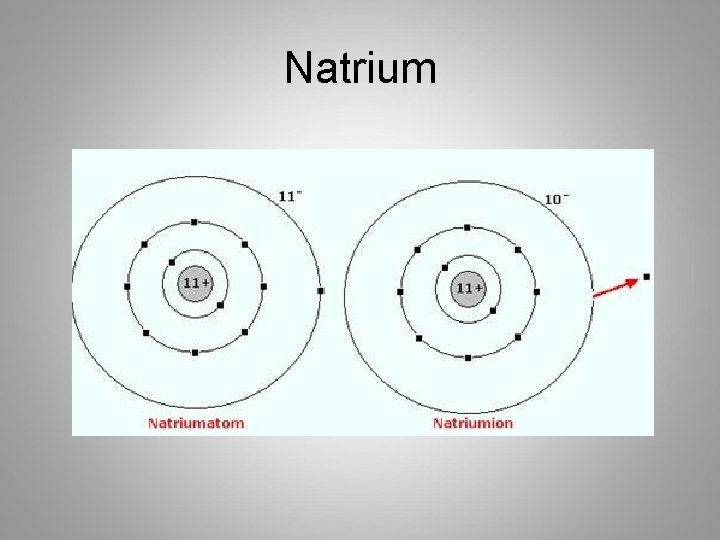
Bijvoorbeeld Na • • Atoomnummer 11 Kernlading is dus +11 11 protonen en 11 elektronen Na kan 1 elektron afstaan – Buitenste schil 1 e • 11 P 10 E (+11 -10= +1) • Natrium ion (Na+-ion)

Natrium

Bijvoorbeeld Cl • • • Atoomnummer 17 Kernlading is dus +17 17 protonen en 17 elektronen Cl kan 1 elektron opnemen 17 P 18 E (+17 -18= -1) Chloride (Cl- ion)

Periodiek systeem en ionen • Atomen uit groep 1 – 1 afstaan dus lading van 1+ • Atomen uit groep 2 – 2 afstaan dus lading van 2+ • Atomen uit groep 16 – 2 opnemen dus lading van 2 - • Atomen uit groep 17 – 1 opnemen dus lading van 1 -

Waardigheid van atomen • Ook wel elektovalentie • Atomen uit groep 1 – Waardigheid van 1 • Atomen uit groep 2 – Waardigheid van 2 • Atomen uit groep 15 – Waardigheid van 3 • Atomen uit groep 17 – Waardigheid van 1

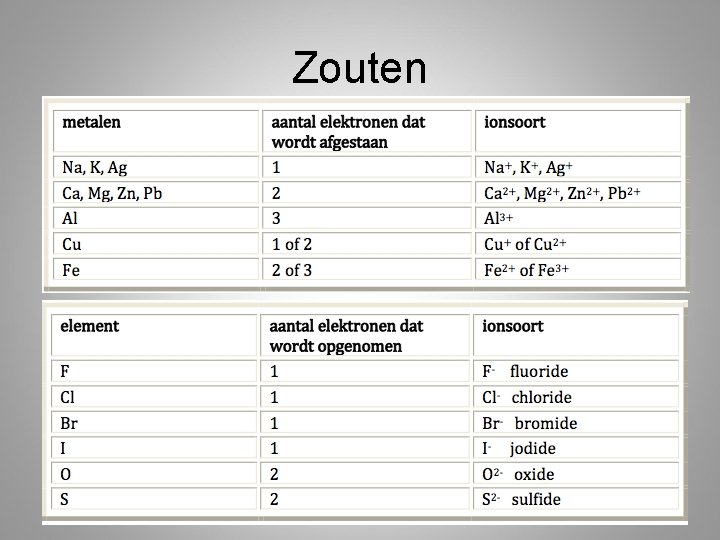
2. 5 naamgeving van ionen • Positieve ionen behouden dezelfde naam – Mg 2+ = Magnesium ion – Na+ = Natrium ion – K+ = Kalium ion

Metalen • Er zijn metalen die meerdere valenties kunnen hebben • Fe 2+ of Fe 3+ • Deze geven we aan met romeinse cijfers • Ijzer(II) ion of ijzer(III)ion • Cu+ en Cu 2+ • Koper(I)ion en Koper(II)ion

Valenties van metalen Metaal valentie Na, K, Ag (1) + Mg, Ba, Ca, Zn, Ni 2+ Al, Cr, Au 3+ Fe 2+ en 3+ Cu, Hg 1+ en 2+ Pb, Sn 2+ en 4+ Uitzondering: Waterstof (enige niet metaal) positieve valentie: H+

Valenties niet metalen Niet-metaal Valentie F, Cl, Br, I (1) - O, S 2 - N, P 3 -

Negatieve ionen • Achtervoegsel –ide – F– Cl– Br – I– O 2– S 2– N 3 - Fluoride Chloride Bromide Jodide Oxide Sulfide Nitride

Scheikunde Week 6

3. 3 structuurformules en namen van moleculaire stoffen • Molecuul bestaat altijd uit 2 of meer atomen • Altijd niet-metalen • Covalentie • structuurformules

Molecuulformule Coëfficiënt: Geeft het aantal moleculen aan 2 C 2 H 6 O 2 moleculen ethanol Index: Geeft het aantal atomen dat in het molecuul voorkomt aan

Atoombinding • Covalentie: het aantal elektronen dat een atoom beschikbaar heeft voor de atoombinding

Atoombinding Er zijn ook atomen die meer dan een covalentie hebben. Bijvoorbeeld: Zwavel (S) covalentie 2, 4 en 6

Structuurformule • Een structuurformule is een tekening van een molecuul. - Ruimtelijke structuur: hierbij kun je de hoeken en verbindingen goed zien. - Eenvoudiger is de structuurformule: deze zijn gemakkelijker te tekenen. Ethanol H-atomen worden voor het gemak vaak weggelaten.

Structuurformule • Dubbele bindingen • Drievoudige bindingen

Molecuulformule • Koolstof en zwavel atomen Covalentie aantallen vereenvoudigen : C : 4 : 2 : 1 S 2 4 2 Formule : CS 2 Koolstofdisulfide

Index en naamgeving Index Voorvoegsel 1 Mono 2 Di 3 Tri 4 Tetra 5 Penta 6 Hexa

Naamgeving • H 2 O – Diwaterstofmono-oxide • P 2 O 5 – Difosforpenta-oxide • Monostikstofdioxide – NO 2

huiswerk • Opdracht: 21 t/m 33 • Niet maken: 22, 26, 29.

Scheikunde Week 7

3. 2 elektrisch geleidingsvermogen • Een stof kan stroom geleiden wanneer – De stof moet bestaan uit geladen deeltjes – De geladen deeltjes moeten vrij kunnen bewegen

Onderscheid in stoffen 1. Moleculaire stoffen 2. Zouten (opgebouwd uit ionen) 3. Metalen

Welke stoffen geleiden niet? • • Gedestilleerd water Alcohol Hout perspex Moleculaire stoffen (bestaan uit niet-metalen): Dit komt doordat deze stoffen geen vrije elektronen bevatten!!

Zouten • Stoffen opgebouwd uit positieve en negatieve ionen

Zouten bestaan uit: een metaal en een niet-metaal • Natrium en Chloor – Natrium staat steeds 1 elektron af – Chloor neemt steeds 1 elektron op • Er ontstaat Natriumchloride (keukenzout)

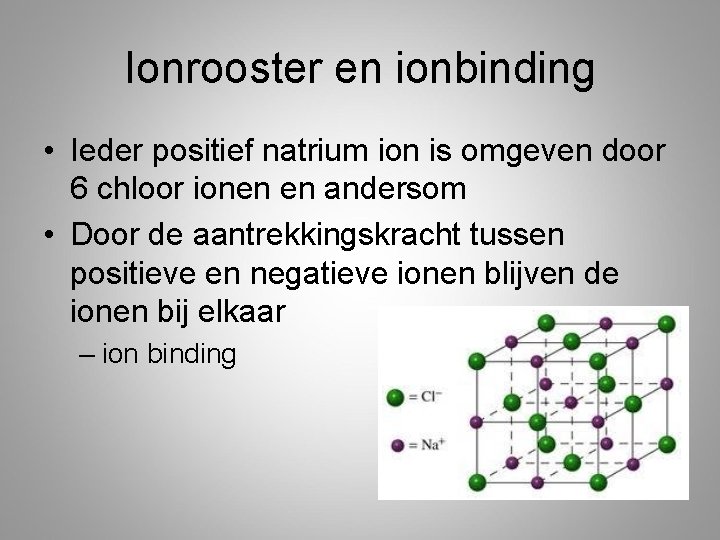
Ionrooster en ionbinding • Ieder positief natrium ion is omgeven door 6 chloor ionen en andersom • Door de aantrekkingskracht tussen positieve en negatieve ionen blijven de ionen bij elkaar – ion binding

Metalen • Eigenschappen van metalen – Glanzend uiterlijk – Hoog smeltpunt – Geleiden goed warmte – Geleiden elektrische stroom – Goed vervormbaar door walsen en smeden – In gesmolten toestand goed te mengen

Even terug • IJzer atoomnummer 26 • Aantal protonen is dus: 26 (positief) • Aantal elektronen is dus: 26 (negatief) • IJzer staat graag 2 elektronen af • Dan krijgt ijzer een lading van: +2 • Dat is het ijzer ion

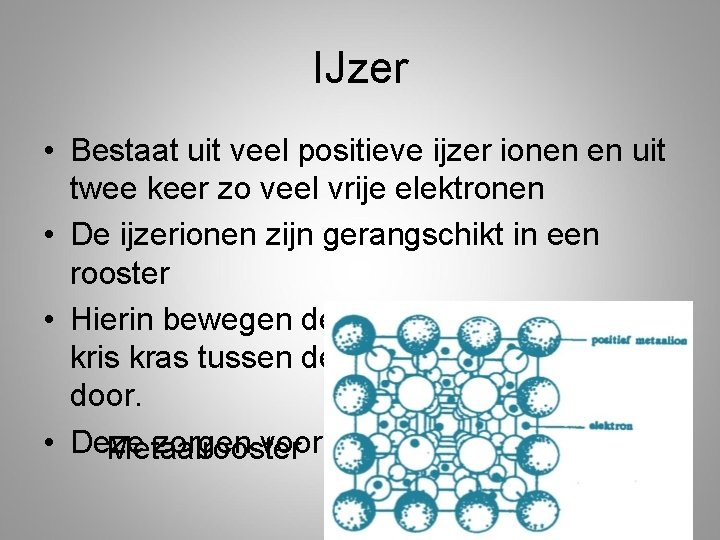
IJzer • Bestaat uit veel positieve ijzer ionen en uit twee keer zo veel vrije elektronen • De ijzerionen zijn gerangschikt in een rooster • Hierin bewegen de vrije elektronen zich kris kras tussen de positieve ijzerionen door. • Deze zorgen voor de binding Metaalrooster

Metaalrooster • Bestaat dus uit positieve metaalionen en uit vrije elektronen die voor de binding (metaalbinding) in het rooster zorgen • Wanneer het metaal aangesloten wordt op stroom gaan alle elektronen dezelfde kant op – De beweging van vrije elektronen wordt gericht