Hoofdstuk I structuur en binding HOOFDSTUK I STRUCTUUR

Hoofdstuk I: structuur en binding HOOFDSTUK I: STRUCTUUR EN BINDING Mc Murry: pagina 1 -28 pagina 34 -43

Hoofdstuk I: structuur en binding I. 1 Inleiding • Waarom : Elk levend wezen bestaat uit organische verbindingen: o Haar, huid, spieren: proteïnen o Genetisch materiaal: DNA o Geneesmiddelen: (aspirine) o Kleding: synthetische vezels (nylon) o Voeding: vitaminen, kleurstoffen • Wat: Chemie van koolstof en zijn verbindingen C: tweede periode, vierde groep zes elektronen, vier valentie-elektronen http: //www. webelements. com; http: //www. periodictableonline. org
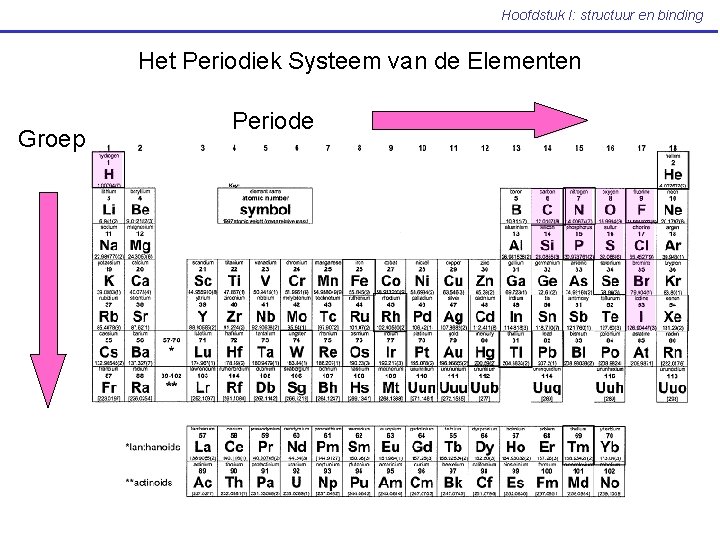
Hoofdstuk I: structuur en binding Het Periodiek Systeem van de Elementen Groep Periode
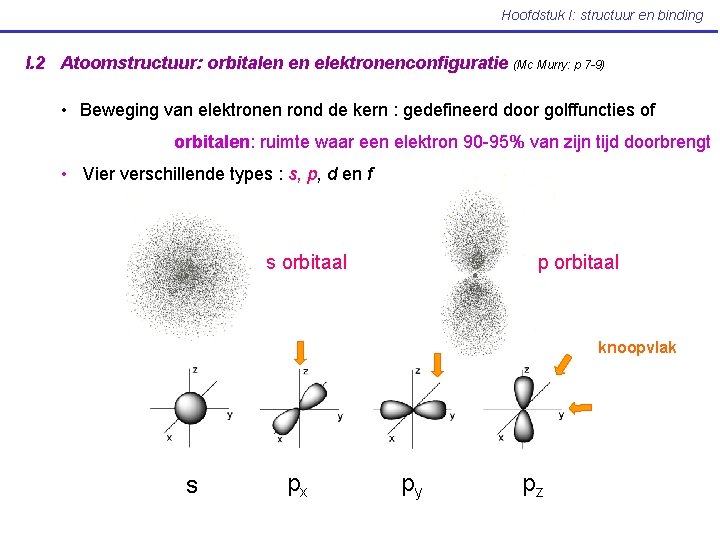
Hoofdstuk I: structuur en binding I. 2 Atoomstructuur: orbitalen en elektronenconfiguratie (Mc Murry: p 7 -9) • Beweging van elektronen rond de kern : gedefineerd door golffuncties of orbitalen: ruimte waar een elektron 90 -95% van zijn tijd doorbrengt • Vier verschillende types : s, p, d en f s orbitaal p orbitaal knoopvlak s px py pz
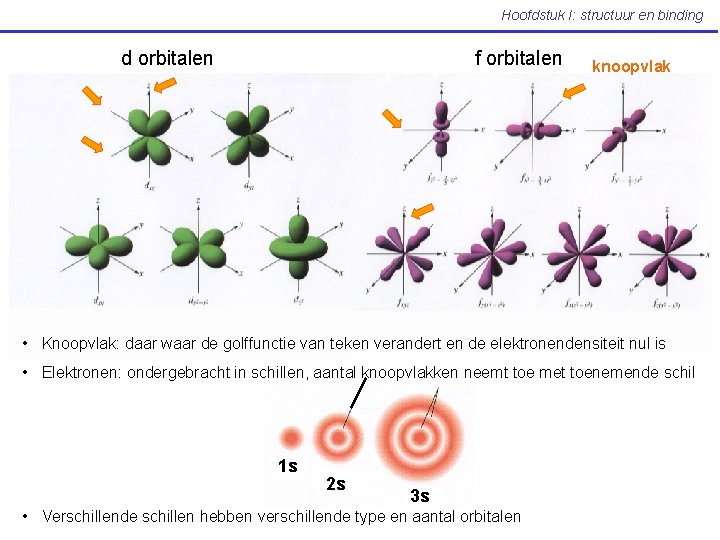
Hoofdstuk I: structuur en binding d orbitalen f orbitalen knoopvlak • Knoopvlak: daar waar de golffunctie van teken verandert en de elektronendensiteit nul is • Elektronen: ondergebracht in schillen, aantal knoopvlakken neemt toe met toenemende schil 1 s 2 s 3 s • Verschillende schillen hebben verschillende type en aantal orbitalen

Hoofdstuk I: structuur en binding De energie en de aard van de orbitalen in het atoom beschikbaar voor de elektronen: 5 f 4 f Beschrijving van een elektronenconfiguratie: = beschrijving van de orbitalen die door de elektronen ingenomen worden 3 regels

Hoofdstuk I: structuur en binding (1) Aufbau-regel : eerst bezetting van de orbitalen met de laagste energie-inhoud, !!! 3 p < 4 s < 3 d (2) Exclusieprincipe van Pauli: per orbitaal: maximaal twee elektronen, met tegenovergestelde spin (3) Regel van Hund: in geval van verschillende orbitalen met dezelfde energie (bv. de drie p-orbitalen) eerst in elk van die orbitalen één elektron tot alle orbitalen halfvol, de elektronen in de halfgevulde orbitalen hebben gelijke spinoriëntatie
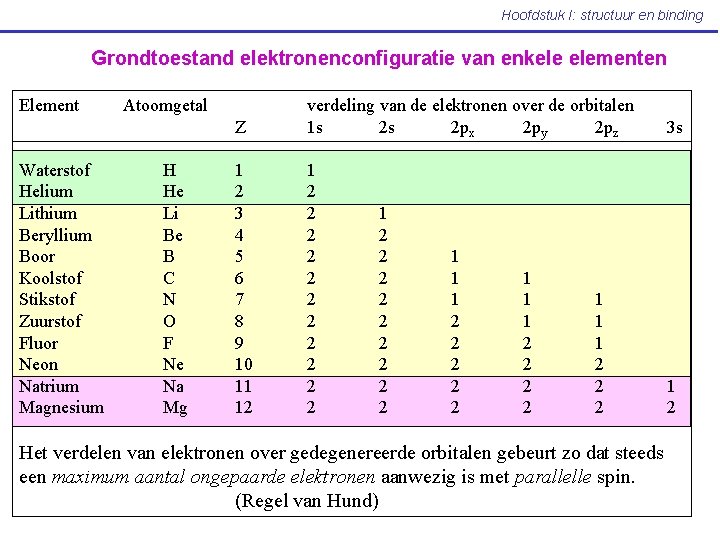
Hoofdstuk I: structuur en binding Grondtoestand elektronenconfiguratie van enkele elementen Element Waterstof Helium Lithium Beryllium Boor Koolstof Stikstof Zuurstof Fluor Neon Natrium Magnesium Atoomgetal H He Li Be B C N O F Ne Na Mg Z verdeling van de elektronen over de orbitalen 1 s 2 s 2 px 2 py 2 pz 3 s 1 2 3 4 5 6 7 8 9 10 11 12 1 2 2 2 2 2 1 1 1 2 2 2 2 1 1 1 2 2 2 Het verdelen van elektronen over gedegenereerde orbitalen gebeurt zo dat steeds een maximum aantal ongepaarde elektronen aanwezig is met parallelle spin. (Regel van Hund)

Hoofdstuk I: structuur en binding Valentie-elektronen van de eerste 18 elementen

Hoofdstuk I: structuur en binding ionaire binding covalente binding
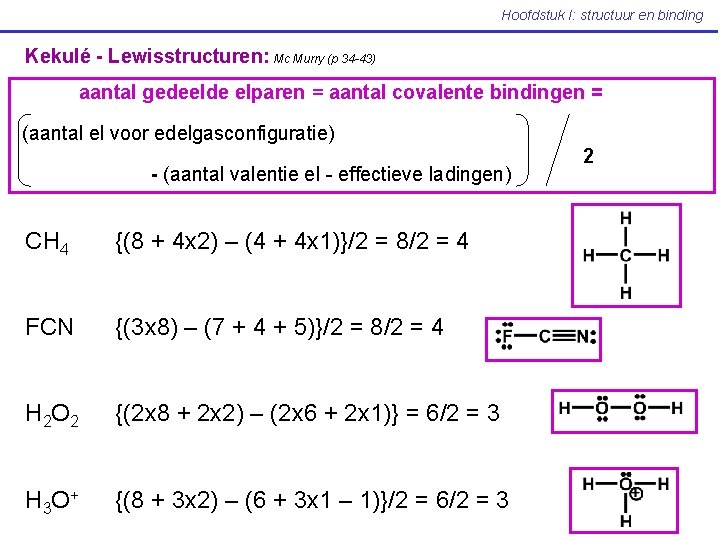
Hoofdstuk I: structuur en binding Kekulé - Lewisstructuren: Mc Murry (p 34 -43) aantal gedeelde elparen = aantal covalente bindingen = (aantal el voor edelgasconfiguratie) - (aantal valentie el - effectieve ladingen) CH 4 {(8 + 4 x 2) – (4 + 4 x 1)}/2 = 8/2 = 4 FCN {(3 x 8) – (7 + 4 + 5)}/2 = 8/2 = 4 H 2 O 2 {(2 x 8 + 2 x 2) – (2 x 6 + 2 x 1)} = 6/2 = 3 H 3 O + {(8 + 3 x 2) – (6 + 3 x 1 – 1)}/2 = 6/2 = 3 2
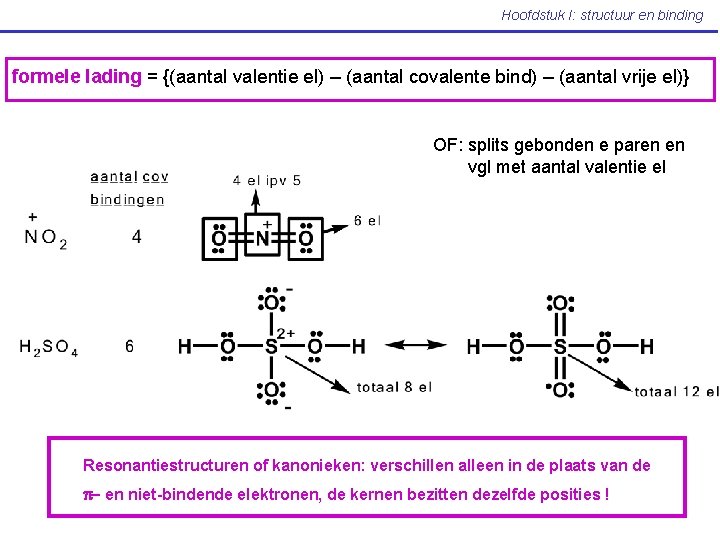
Hoofdstuk I: structuur en binding formele lading = {(aantal valentie el) – (aantal covalente bind) – (aantal vrije el)} OF: splits gebonden e paren en vgl met aantal valentie el Resonantiestructuren of kanonieken: verschillen alleen in de plaats van de p- en niet-bindende elektronen, de kernen bezitten dezelfde posities !

Hoofdstuk I: structuur en binding Kekulé - Lewisstructuren: voorbeelden Geladen moleculen
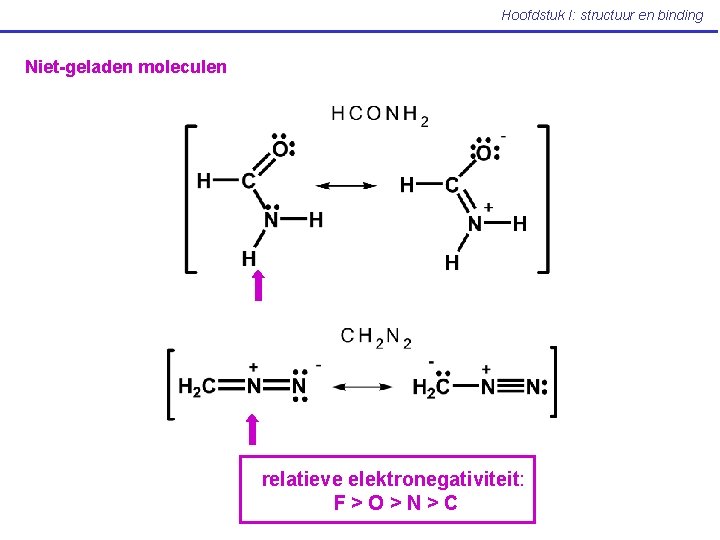
Hoofdstuk I: structuur en binding Niet-geladen moleculen relatieve elektronegativiteit: F>O>N>C
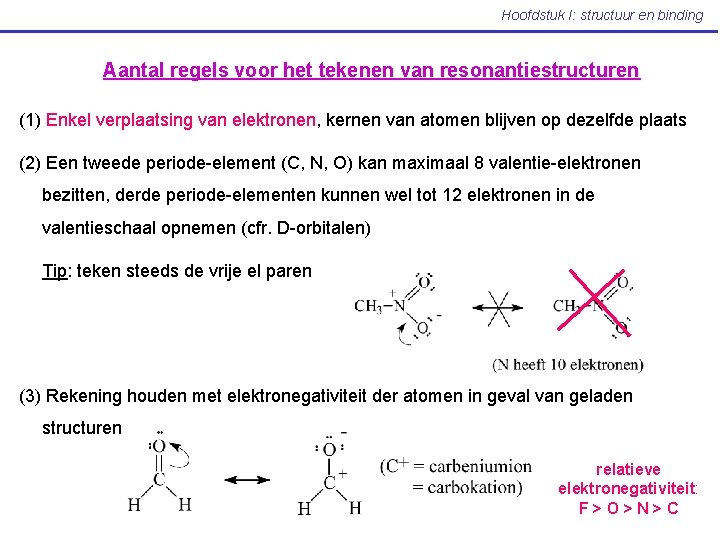
Hoofdstuk I: structuur en binding Aantal regels voor het tekenen van resonantiestructuren (1) Enkel verplaatsing van elektronen, kernen van atomen blijven op dezelfde plaats (2) Een tweede periode-element (C, N, O) kan maximaal 8 valentie-elektronen bezitten, derde periode-elementen kunnen wel tot 12 elektronen in de valentieschaal opnemen (cfr. D-orbitalen) Tip: teken steeds de vrije el paren (3) Rekening houden met elektronegativiteit der atomen in geval van geladen structuren relatieve elektronegativiteit: F>O>N>C
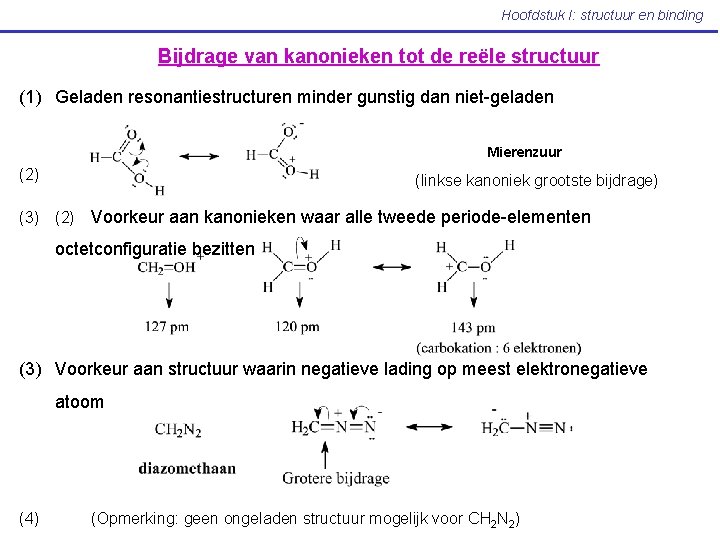
Hoofdstuk I: structuur en binding Bijdrage van kanonieken tot de reële structuur (1) Geladen resonantiestructuren minder gunstig dan niet-geladen Mierenzuur (2) (linkse kanoniek grootste bijdrage) (3) (2) Voorkeur aan kanonieken waar alle tweede periode-elementen octetconfiguratie bezitten (3) Voorkeur aan structuur waarin negatieve lading op meest elektronegatieve atoom (4) (Opmerking: geen ongeladen structuur mogelijk voor CH 2 N 2)
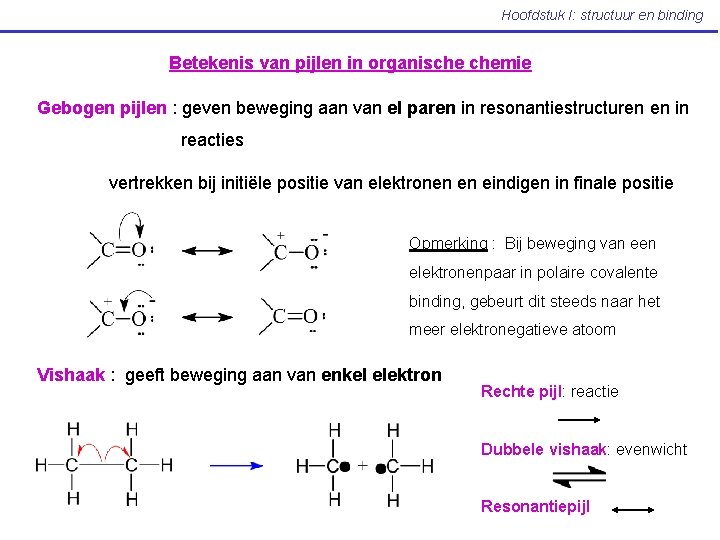
Hoofdstuk I: structuur en binding Betekenis van pijlen in organische chemie Gebogen pijlen : geven beweging aan van el paren in resonantiestructuren en in reacties vertrekken bij initiële positie van elektronen en eindigen in finale positie Opmerking : Bij beweging van een elektronenpaar in polaire covalente binding, gebeurt dit steeds naar het meer elektronegatieve atoom Vishaak : geeft beweging aan van enkel elektron Rechte pijl: reactie Dubbele vishaak: evenwicht Resonantiepijl
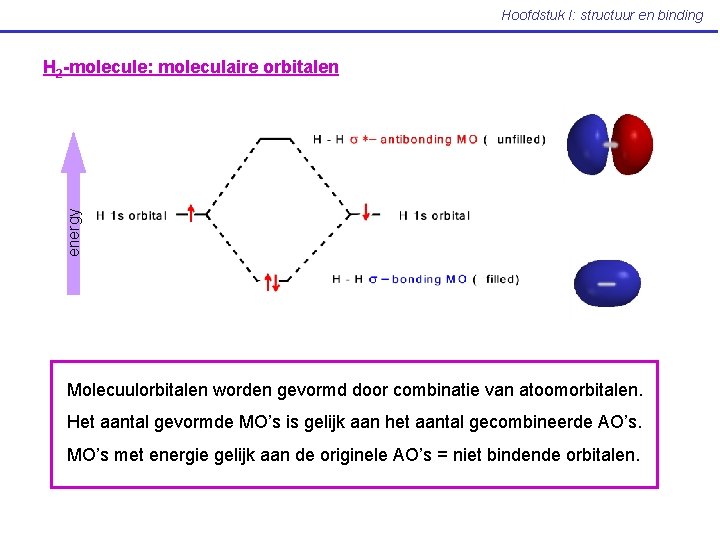
Hoofdstuk I: structuur en binding energy H 2 -molecule: moleculaire orbitalen Molecuulorbitalen worden gevormd door combinatie van atoomorbitalen. Het aantal gevormde MO’s is gelijk aan het aantal gecombineerde AO’s. MO’s met energie gelijk aan de originele AO’s = niet bindende orbitalen.
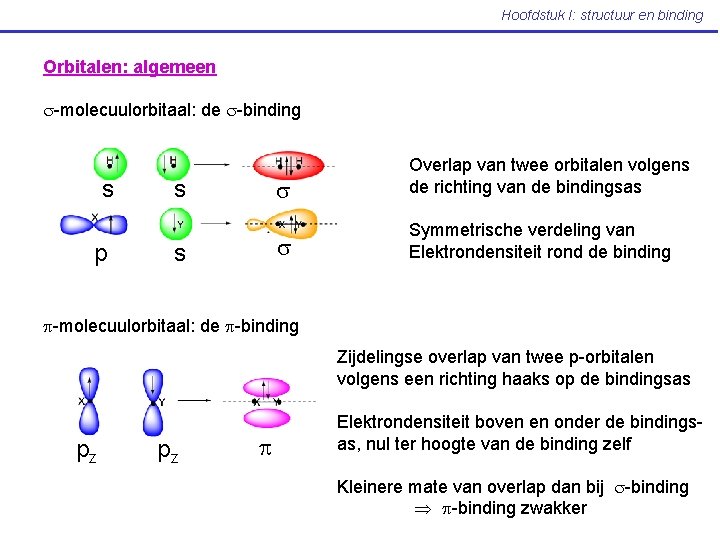
Hoofdstuk I: structuur en binding Orbitalen: algemeen s-molecuulorbitaal: de s-binding s p s s s Overlap van twee orbitalen volgens de richting van de bindingsas s Symmetrische verdeling van Elektrondensiteit rond de binding p-molecuulorbitaal: de p-binding Zijdelingse overlap van twee p-orbitalen volgens een richting haaks op de bindingsas pz pz p Elektrondensiteit boven en onder de bindingsas, nul ter hoogte van de binding zelf Kleinere mate van overlap dan bij s-binding p-binding zwakker
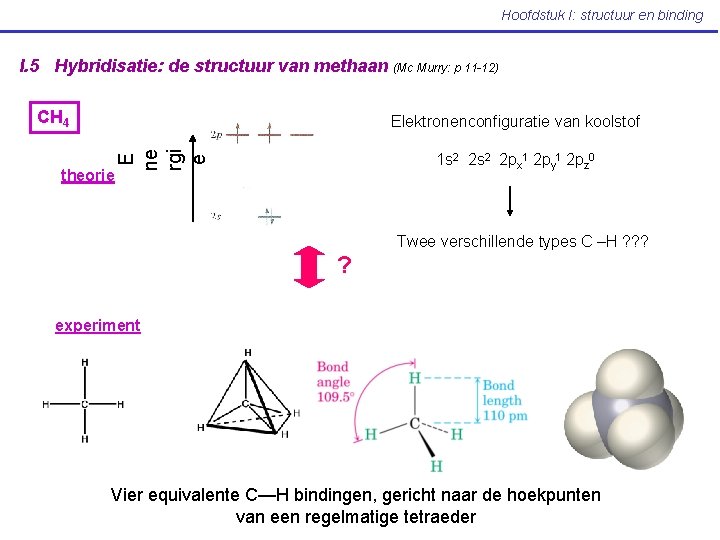
Hoofdstuk I: structuur en binding I. 5 Hybridisatie: de structuur van methaan (Mc Murry: p 11 -12) CH 4 theorie E ne rgi e Elektronenconfiguratie van koolstof 1 s 2 2 px 1 2 py 1 2 pz 0 Twee verschillende types C –H ? ? ? ? experiment Vier equivalente C—H bindingen, gericht naar de hoekpunten van een regelmatige tetraeder

Hoofdstuk I: structuur en binding De oplossing van Linus Pauling: E ne rgi e 1 s en 3 p-orbitalen combineren of hybridizeren tot 4 gelijkwaardige sp 3 hybrideorbitalen Orbitalen zijn zo georiënteerd dat ze gericht zijn naar de hoekpunten van een tetraëder: valentiehoek = 109, 5°
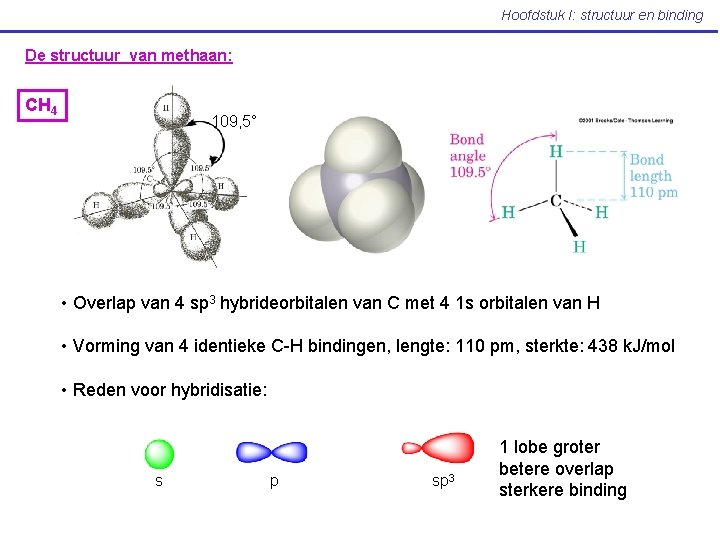
Hoofdstuk I: structuur en binding De structuur van methaan: CH 4 109, 5° • Overlap van 4 sp 3 hybrideorbitalen van C met 4 1 s orbitalen van H • Vorming van 4 identieke C-H bindingen, lengte: 110 pm, sterkte: 438 k. J/mol • Reden voor hybridisatie: s p sp 3 1 lobe groter betere overlap sterkere binding
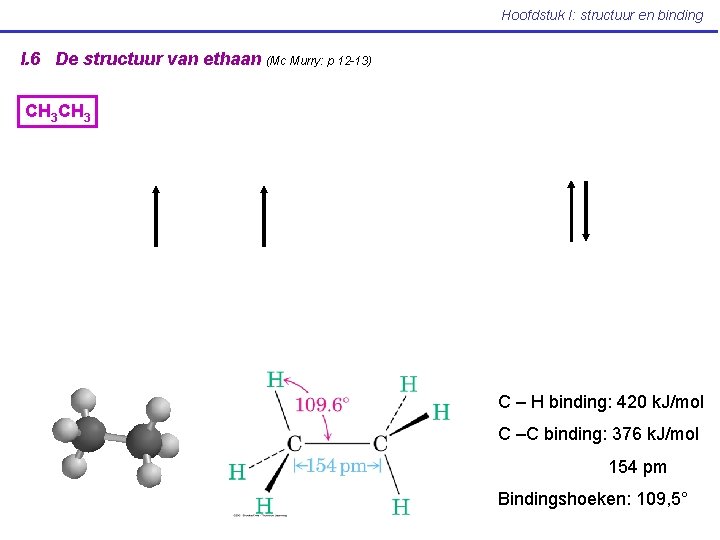
Hoofdstuk I: structuur en binding I. 6 De structuur van ethaan (Mc Murry: p 12 -13) CH 3 C – H binding: 420 k. J/mol C –C binding: 376 k. J/mol 154 pm Bindingshoeken: 109, 5°
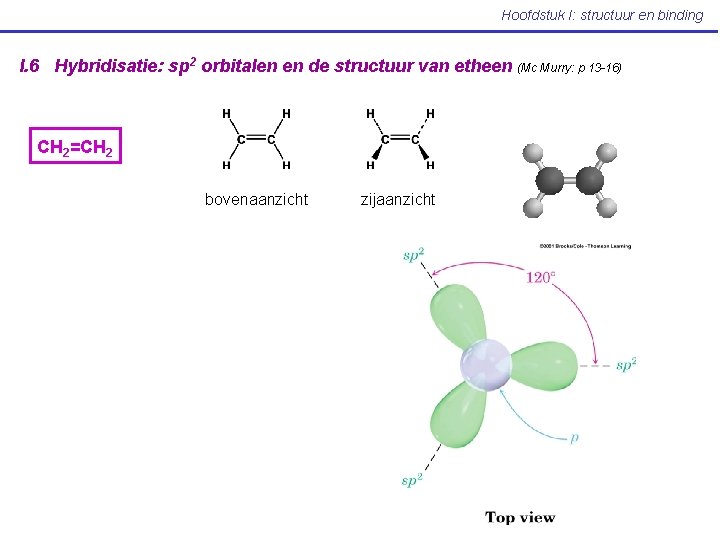
Hoofdstuk I: structuur en binding I. 6 Hybridisatie: sp 2 orbitalen en de structuur van etheen (Mc Murry: p 13 -16) CH 2=CH 2 bovenaanzicht zijaanzicht
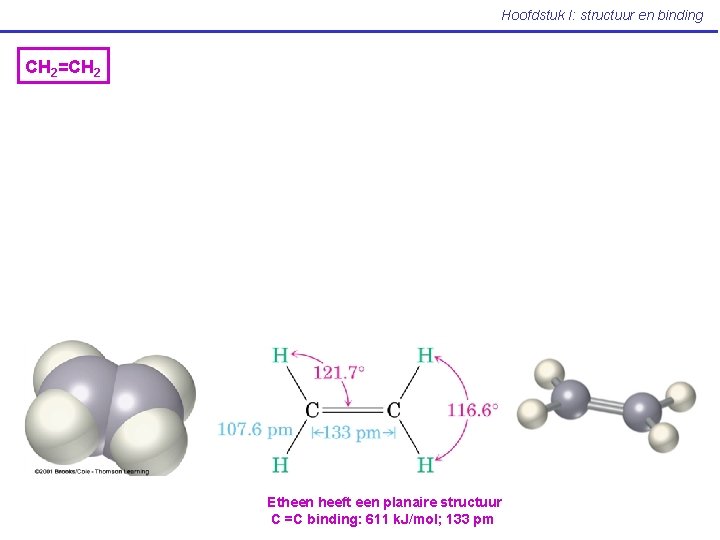
Hoofdstuk I: structuur en binding CH 2=CH 2 Etheen heeft een planaire structuur C =C binding: 611 k. J/mol; 133 pm
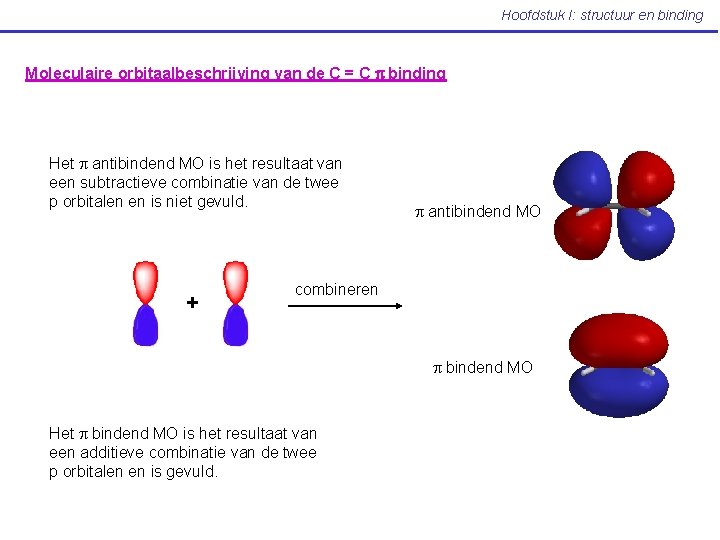
Hoofdstuk I: structuur en binding Moleculaire orbitaalbeschrijving van de C = C p binding Het p antibindend MO is het resultaat van een subtractieve combinatie van de twee p orbitalen en is niet gevuld. + p antibindend MO combineren p bindend MO Het p bindend MO is het resultaat van een additieve combinatie van de twee p orbitalen en is gevuld.
Hoofdstuk I: structuur en binding I. 6 Hybridisatie: sp orbitalen en de structuur van ethyn HC CH (Mc Murry: p 16 -17)
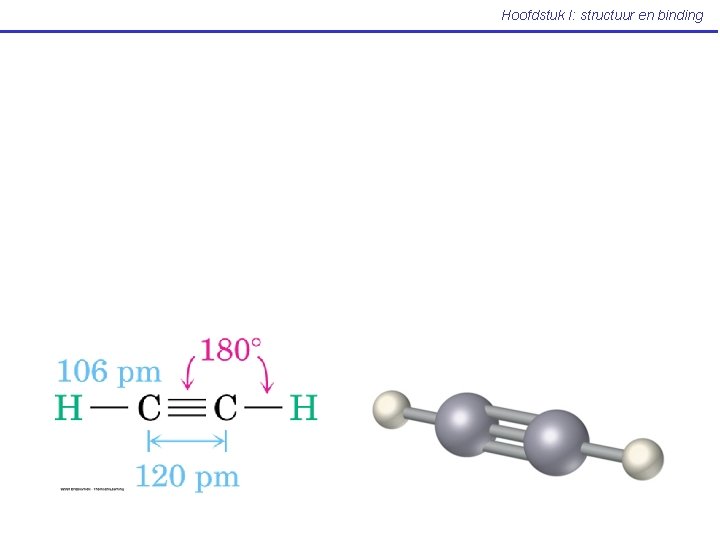
Hoofdstuk I: structuur en binding
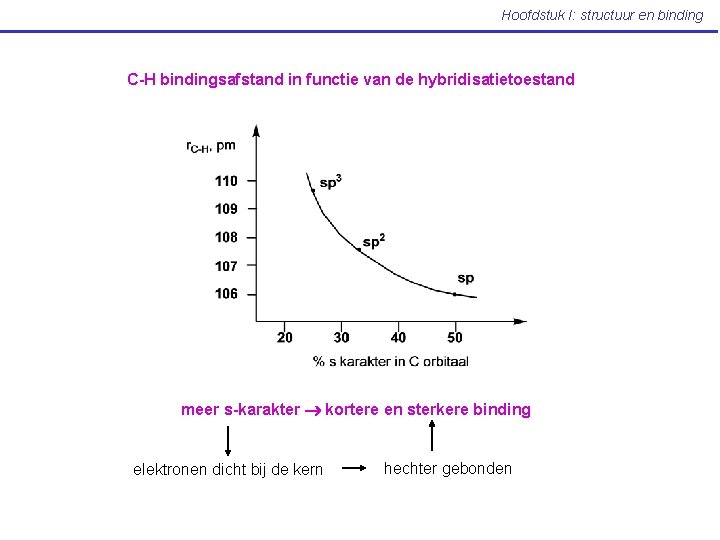
Hoofdstuk I: structuur en binding C-H bindingsafstand in functie van de hybridisatietoestand meer s-karakter kortere en sterkere binding elektronen dicht bij de kern hechter gebonden
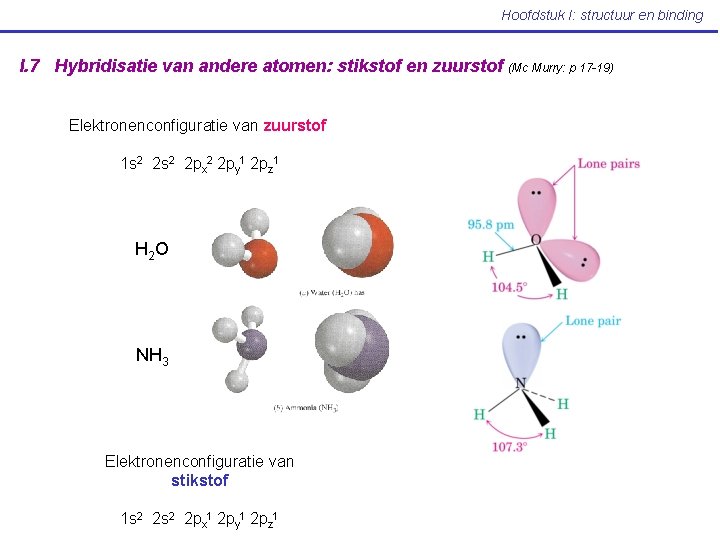
Hoofdstuk I: structuur en binding I. 7 Hybridisatie van andere atomen: stikstof en zuurstof Elektronenconfiguratie van zuurstof 1 s 2 2 px 2 2 py 1 2 pz 1 H 2 O (a) NH 3 (b) Elektronenconfiguratie van stikstof 1 s 2 2 px 1 2 py 1 2 pz 1 (Mc Murry: p 17 -19)
- Slides: 30