Scheikunde SCHEIKUNDE 01 februari 2018 vwo 4 Waarom

Scheikunde

SCHEIKUNDE 01 februari 2018 vwo 4 • Waarom rekenen in de scheikunde? • Waarom iets over zouten, mineralen? • Deze les, volgende les, deze week, volgende week: planning en werkwijze 01 feb 2018 2

• Waarom iets over zouten, mineralen? historisch / geologisch / economisch: • http: //www. geologievannederland. nl/ondergrond/afzettingen-en-delfstoffen/steenzout • http: //www. geologievannederland. nl/mineralen/beschrijvingen/haliet • https: //www. mindat. org/lsearch. php? from=nsearch&loc=netherland • http: //www. mijnbouwgroningen. nl/waar/ Wat is de economische rol anno 2018 van zout voor Noord-Nederland? Wanneer en waarom werd zout als betaalmiddel gebruikt? Welke vormen van zout, mineralen komen in Drenthe in de grond voor? https: //www. gezondheidsnet. nl/bloeddruk/de-functie-van-zout medisch / gezondheid: • • • http: //www. voedingscentrum. nl/encyclopedie/mineralen. aspx Wat is de functie van mineralen in het lichaam en wat als dat niet in balans is? https: //www. cyberpoli. nl/epilepsie/medisch/werkinghersenen http: //www. nederland-davos. nl/site/Ziektebeelden_en_Onderzoeken/Ziektebeelden/Cystische_fibrose. html Hoe worden zouten, mineralen in het lichaam getransporteerd (cel in, cel uit, https: //www. menselijklichaam. nl/lichaams-elektriciteit/actiepotentiaal/ orgaan in, orgaan uit)? sieraden / kunst: • http: //www. edelstenenenmineralen. nl/malachiet. html • Hoe worden en hoe kunnen zouten in de kunst gebruikt worden, wat is hun https: //www. ad. nl/cultuur/japanner-maakt-magische-kunstwerken-van-zout~af 946 e 19/ functie? https: //creators. vice. com/nl/article/78 qm 8 b/de-kunstenaar-die-zelfrijdende-autos-opsluit-in-cirkels-van-zout • https: //nl. wikibooks. org/wiki/Schilderen/Palet_van_enkele_beroemde_schilders • • Welke zouten worden gebruikt als edelstenen, wat is hun waarde en hoe worden http: //simonkoopman. nl/pigmenten/ ze bewerkt en gebruikt? nieuwe technologie: Wat zijn nieuwe technologische materialen die variaties zijn op bestaande zouten? • https: //en. wikipedia. org/wiki/Ionic_liquid • https: //www. alurvs. nl/aluminium/artikelen/2787/ • https: //www. c 2 w. nl/nieuws/geen-damp-wel-spanning/item 13398 • Waardoor zijn de ionische vloeistoffen echt verschillend van alle andere 'natuurlijke' http: //www. scheikundeinbedrijf. nl/Mediatheek/Kanjerkaart/index. rails? id=5 zouten (mineralen)? Wat zijn toepassingen van die ionische vloeistoffen? 01 feb 2018 3

• Waarom iets over zouten, mineralen? historisch / geologisch / economisch: • http: //www. geologievannederland. nl/ondergrond/afzettingen-en-delfstoffen/steenzout • http: //www. geologievannederland. nl/mineralen/beschrijvingen/haliet • https: //www. mindat. org/lsearch. php? from=nsearch&loc=netherland • http: //www. mijnbouwgroningen. nl/waar/ medisch / gezondheid: • https: //www. gezondheidsnet. nl/bloeddruk/de-functie-van-zout • http: //www. voedingscentrum. nl/encyclopedie/mineralen. aspx • https: //www. cyberpoli. nl/epilepsie/medisch/werkinghersenen • http: //www. nederland-davos. nl/site/Ziektebeelden_en_Onderzoeken/Ziektebeelden/Cystische_fibrose. html • https: //www. menselijklichaam. nl/lichaams-elektriciteit/actiepotentiaal/ sieraden / kunst: • http: //www. edelstenenenmineralen. nl/malachiet. html • https: //www. ad. nl/cultuur/japanner-maakt-magische-kunstwerken-van-zout~af 946 e 19/ • https: //creators. vice. com/nl/article/78 qm 8 b/de-kunstenaar-die-zelfrijdende-autos-opsluit-in-cirkels-van-zout • https: //nl. wikibooks. org/wiki/Schilderen/Palet_van_enkele_beroemde_schilders • http: //simonkoopman. nl/pigmenten/ nieuwe technologie: • https: //en. wikipedia. org/wiki/Ionic_liquid • https: //www. alurvs. nl/aluminium/artikelen/2787/ • https: //www. c 2 w. nl/nieuws/geen-damp-wel-spanning/item 13398 • http: //www. scheikundeinbedrijf. nl/Mediatheek/Kanjerkaart/index. rails? id=5 01 feb 2018 4

Kennen en kunnen Voorkennis en pag. 95, 96, 97 • Zouten zijn (net als alle andere zuivere vaste stoffen, zuiver vloeistoffen en gassen) altijd elektrisch neutraal (ongeladen). • Zouten bestaan altijd uit een combinatie van positieve ionen en negatieve ionen, bij elkaar gehouden in een ionrooster door sterke ionbinding Binas T 67 D. De sterke binding zorgt ervoor dat 'natuurlijke' zouten altijd vaste stoffen zijn bij kamertemperatuur (zeer sterke binding in vergelijking met de zwakke vander. Waalsbinding tussen kleine moleculen). • vb zouten • • Na. Cl KF Ca. O Mg. Cl 2 Al 2 O 3 • Ladingen van metaalionen en van niet-metaalionen van elementen staan in Binas Tabel 40 A laatste kolom. • NB. Metalen zijn ook opgebouwd uit positieve ionen (metaalionen) en uit negatieve deeltjes, de vrije electronen. Metaalbinding is ook een sterke binding. Alle 5 metalen, behalve kwik zijn vaste stoffen bij kamertemperatuur.

Kennen en kunnen Voorkennis en pag. 95, 96, 97 • De (verhoudings)formule van een zout stel je op door altijd een zo klein mogelijke getalcombinatie van de ionen in dat zout te maken waardoor het geheel neutraal is. vb Pb 4+3 N 3 -4 • In de verhoudingsformule van een zout hoeft de ionlading niet opgeschreven te worden (mag wel). vb Pb 3 N 4 • Naast de metaalionen en de niet-metaalionen komen ook samengestelde ionen voor in zouten. vb Binas tabel 66 B • De atomen in samengestelde ionen zitten sterk aan elkaar gebonden (meestal door atoombinding), hierdoor is het als het ware een ‘apart’ –geladen- deeltje geworden. • vb NH 4+ SO 32 - PO 43 - 01 feb 2018 6

Kennen en kunnen • Voorkennis en pag. 95, 96, 97 Een zout kan oplossen in water als de nieuwe ion-dipool binding die tussen de losse ionen en watermoleculen (dipoolmoleculen) gemaakt wordt energetisch ‘voordeliger’ is dan het on-oplosbaar zijn van dit zout Binas Tabel 45 A Oplosvergelijkingen (GEEN reactievergelijking) vb 1 • Na 2 SO 3 ----- vb 2 (NH 4)2 SO 4 vb 3 Fe. Cl 3 ----- 2 Na+ + SO 32 - ----- Fe 3+ 2 NH 4+ + SO 42 - + 3 Cl- Positieve ionen worden bij oplossen omringd door de O-atomen van de watermoleculen, negatieve ionen worden dan omringd door de H-atomen van de watermoleculen 7

Kennen en kunnen • pagina 98, Oplossingen met opgeloste ionen kunnen onderling gemengd worden waardoor nieuw gevormde onoplosbare zouten kunnen ontstaan, deze kunnen dan neerslaan Binas Tabel 45 A vb 1 Na 2 SO 3 vb 3 Fe. Cl 3 ----- 2 Na+ + SO 32 Fe 3+ + 3 Cl- Oplossing 1 en oplossing 3 mengen, dan zijn in water aanwezig: de ionen Na+ , SO 32 - , Fe 3+ , Cl. Na. Cl is een zout dat goed oplosbaar is in water, deze ionen zullen dus in oplossing blijven, maar … de combinatie van Fe 3+ positieve ionen en SO 32 - negatieve ionen vormt een zout met sterke ionbinding tussen deze deeltjes, er ontstaat een vaste stof die slecht oplosbaar is in water Neerslagreactie 2 Fe 3+ + 3 SO 32 - ----- Fe 2(SO 3)3 • NB. Sommige zouten lossen niet op, maar reageren met water! 8

Kennen en kunnen • Voorkennis en § 3. 1, § 3. 2 Categorieën verschillende soorten stoffen Metalen Vaste stoffen bij kamertemperatuur, uitzondering Hg( l) Geleiden electrische stroom (ook in vaste toestand) Zouten Vaste stoffen bij kamertemperatiuur. Geleiden in vaste toestand geen electrische stroom, alleen wanneer gesmolten of opgelost. Moleculaire stoffen hydrofiel hydrofoob Gasvormig (bijv. H 2, Cl 2, I 2, F 2, Br 2, O 2, N 2, C 2 H 6, C 2 H 4 , H 2 O 2), vloeistof (bijv. C 2 H 5 OH, H 2 O, C 6 H 14) of vast (bijv. C 6 H 12 O 6, C 17 H 35 COOH) Edel gassen 9

Kennen en kunnen Voorkennis en § 3. 1, § 3. 2 Sterkte van de bindingen tussen deeltjes in verschillende soorten stoffen Metalen Zouten Moleculaire stoffen hydrofiel hydrofoob Edel gassen Tussen de moleculen: Metaalrooster Zoutkristalrooster positieve metaalionen gebonden door negatieve vrije electronen positieve ionen (vaak metaalionen) gebonden aan negatieve ionen Metaalbinding: Sterke Coulombkrachten tussen positieve en negatieve deeltjes. Ionbinding: Sterke Coulombkrachten tussen positieve en negatieve deeltjes. altijd vander. Waalsbinding: de vander. Waalsbinding is het sterkst tussen grote (dus zwaardere), lange, onvertakte moleculen. Soms ook dipool-dipool binding (dit is een relatief sterkere binding dan de vander. Waalsbinding). Bij –OH groepen, -NH groepen en HF -moleculen ook nog sterkere waterstofbruggen binding mogelijk. (Tussen atomen in de moleculen: sterke atoombinding of sterke polaire atoombinding. Deze binding wordt alleen verbroken in chemische reacties. ) ‘Geen’ binding tussen de los ‘zwevende’ atomen 10

Kennen en kunnen Voorkennis en § 3. 1, § 3. 2 Een zout kan oplossen in water als de nieuwe ion-dipool binding tussen ionen en watermoleculen energetisch ‘voordeliger’ is dan het on-oplosbaar zijn van dit zout Binas Tabel 45 A Clg Na+ Oplosvergelijking (GEEN reactievergelijking) • vb. Na. Cl (s) ----- Na+ (aq) + Cl- (aq) Als het water uit een oplossing verdampt, kun je voor dit proces een indampvergelijking noteren: vb. Na+ (aq) + Cl- (aq) ----- Na. Cl (s) • Reactievergelijkingen Sommige metalen reageren heel snel en explosief met water, er worden nieuwe stoffen, nieuwe ionen gevormd: https: //www. youtube. com/watch? v=uixx. Jt. JPVXk https: //www. youtube. com/watch? v=cqe. VEFFzz 7 E vb. 2 Na (s) + 2 H 2 O (l) ----- 2 Na+ (aq) + 2 OH- (aq) + H 2 (g) 11

Kennen en kunnen Voorkennis en § 3. 1, § 3. 2 • Reactievergelijkingen Sommige zouten reageren met water, er worden nieuwe stoffen, nieuwe ionen gevormd: vb. Na 2 O (s) + H 2 O (l) voor de pijl: Na+Na+O 2 - & ----- 2 Na+ (aq) + 2 OH- (aq) H 2 O na de pijl: Na+ , OH- , OHhydroxide ionen • Neerslagvergelijkingen een neerslag kan ontstaan wanneer meerdere zout-oplossingen met verschillende soorten positieve en negatieve ionen bij elkaar worden gevoegd. Er kan een suspensie, een vaste stof ontstaan die niet goed oplosbaar is. vb 1. Oplossing van natriumjodide met een oplossing van lood(II)nitraat samenvoegen natriumjodide oplossing bevat: lood(II)nitraat oplossing bevat: Na+ (aq) , I- (aq) Pb 2+ (aq) , NO 3 - (aq) 12
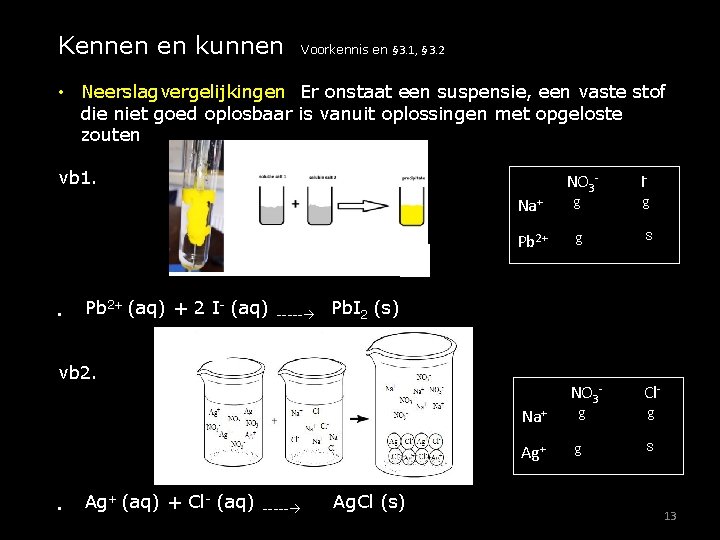
Kennen en kunnen Voorkennis en § 3. 1, § 3. 2 • Neerslagvergelijkingen Er onstaat een suspensie, een vaste stof die niet goed oplosbaar is vanuit oplossingen met opgeloste zouten vb 1. Na+ Pb 2+ • Pb 2+ (aq) + 2 I- (aq) ----- Na+ Ag+ (aq) + Cl- (aq) ----- I- g g g s Pb. I 2 (s) vb 2. • NO 3 - Ag. Cl (s) NO 3 g g Clg s 13
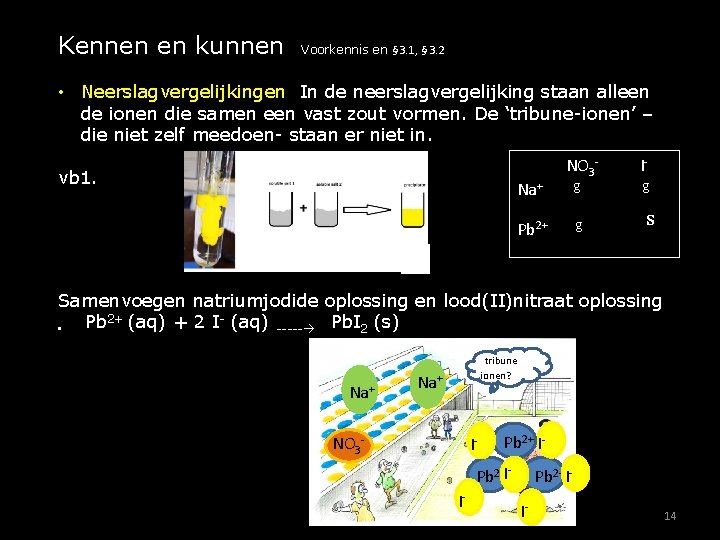
Kennen en kunnen Voorkennis en § 3. 1, § 3. 2 • Neerslagvergelijkingen In de neerslagvergelijking staan alleen de ionen die samen een vast zout vormen. De ‘tribune-ionen’ – die niet zelf meedoen- staan er niet in. vb 1. Na+ NO 3 - Pb 2+ I- g g g s Samenvoegen natriumjodide oplossing en lood(II)nitraat oplossing Pb 2+ (aq) + 2 I- (aq) ----- Pb. I 2 (s) • Na+ tribune ionen? Na+ NO 3 - I- Pb 2+II- 14

SCHEIKUNDE van ZOUTEN • Significantie van gemeten waarden: aantal cijfers waarin meetwaarde nauwkeurig (precies en juist) afgelezen en bepaald kan worden Voorbeelden 0, 0456 x 10 -3 L : 3 cijfers significant 30, 2 m. L : 3 cijfers significant 2, 32 x 103 g : 3 cijfers significant 0, 024 g : 2 cijfers significant ρ ( g L-1) = 2, 32 x 103 / 0, 0456 x 10 -3 ρ ( g L-1) = 0, 024 / 30, 2 x 10 -3 = 5, 08 772 x 107 = 0, 79 47 g L-1 = 5, 09 x 107 g L-1 afgelezen na aanvullen: 21, 3 m. L daarin opgelost: 0, 456 g koper(II)chloride, dus 0, 456 g : 134, 45 g mol -1 = 3, 3916 x 10 -3 mol 2+ Cu. Cl 2 (s) Cu (aq) + 2 Cl (aq) 3, 3916 mmol 2 x 3, 3916 mmol [Cl- ] = (2 x 3, 3916) mmol : 21, 3 m. L = 0, 318 46 mol L-1 15

SCHEIKUNDE van ZOUTEN Molariteit (mol per L, mol L-1) = hoeveelheid ‘’los’’ (mol) volume oplossing (Liter) Los 10 gram suiker, C 12 H 22 O 11 (s) op in 1, 0 liter water. Geef de oplosvergelijking. Wat is de molariteit van deze suikeroplossing? Los 10 gram keukenzout, Na. Cl (s) op in 1, 0 liter water. Geef de oplosvergelijking. Wat is de chloride-molariteit in deze oplossing? Los 2, 34 gram ijzer(III)sulfaat op in 250 m. L water. Geef de oplosvergelijking. Wat is de sulfaat-molariteit in deze oplossing? 6 maart 2018 16

SCHEIKUNDE van ZOUTEN • Molariteit : alleen in geval van OPGELOSTE stoffen Los 2, 34 gram ijzer(III)sulfaat op in 250 m. L water. Geef de oplosvergelijking. Fe 2(SO 4)3 (s) Molverhouding: 1 mol 2 Fe 3+ (aq) + 3 SO 42 - (aq) : 2 mol : 3 mol Wat is de sulfaat-molariteit in deze oplossing? 2, 34 gram Fe 2(SO 4)3 komt overeen met 2, 34 g : 399, 88 g mol-1 = 0, 005852 mol Dus 3 x 0, 005852 mol SO 42 - (aq) in 250 m. L en dus in 1, 00 L is molariteit [SO 42 - ] = 4 x 3 x 0, 005852 mol L-1 = 0, 0702 mol L-1 https: //maken. wikiwijs. nl/34870/Sk_09_Zouten#!page-249385 https: //maken. wikiwijs. nl/35204/Sk_01_Eenheden_en_meten#!page-263405 https: //maken. wikiwijs. nl/45399/Sk_10_Rekenen_in_de_chemie#!page-613503 17

SCHEIKUNDE van ZOUTEN H 3 • § 3. 1 opgaven 3, 4, 5, 6, 7, +8 • § 3. 2 opgaven 9 bce, 11, 12, 14, 15 • § 3. 3 opgaven 17 bcdefg, 18, 19 • § 3. 4 opgaven 20, 22, 23, 24, 25, 26, 27, 28, 29, 30 • § 3. 5 opgaven 31, 32, 34, 33, 35 • Practicum zouten (PO proeven 1, 2, 3) https: //maken. wikiwijs. nl/34870/Sk_09_Zouten#!page-249385 https: //maken. wikiwijs. nl/35204/Sk_01_Eenheden_en_meten#!page-263405 https: //maken. wikiwijs. nl/45399/Sk_10_Rekenen_in_de_chemie#!page-613503 21 mrt 2018 18

SCHEIKUNDE : ENERGIE & BEWEGING H 4 • § 4. 1 opgaven 6, 9, +10 (eventueel 7 ) • § 4. 2 opgaven 11, 13, 14, 15 • § 4. 4 opgaven 21, 23, 24, 25, 28, 29, 31, 32, 37 • § 4. 3 opgaven 19 a, b, c, 20, § 4. 4 opgave 36 • Extra oefenopgaven • Practicum zouten (PO proeven 1, 2, 3, 4, 5) 27 mrt 2018 19
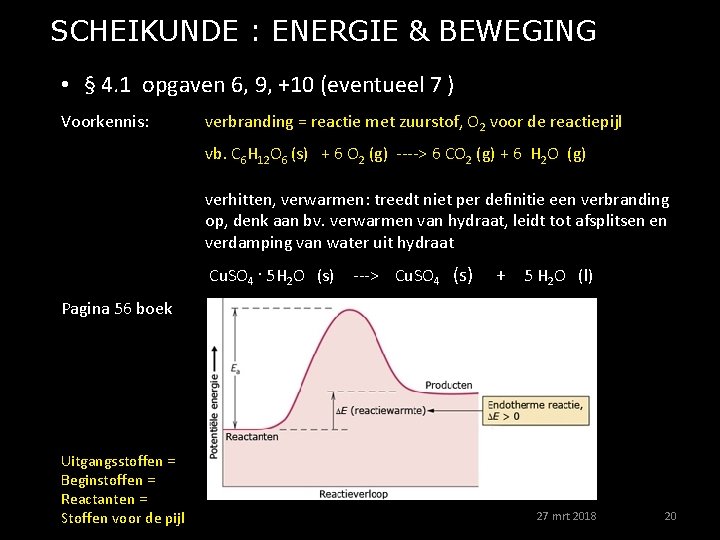
SCHEIKUNDE : ENERGIE & BEWEGING • § 4. 1 opgaven 6, 9, +10 (eventueel 7 ) Voorkennis: verbranding = reactie met zuurstof, O 2 voor de reactiepijl vb. C 6 H 12 O 6 (s) + 6 O 2 (g) ----> 6 CO 2 (g) + 6 H 2 O (g) verhitten, verwarmen: treedt niet per definitie een verbranding op, denk aan bv. verwarmen van hydraat, leidt tot afsplitsen en verdamping van water uit hydraat Cu. SO 4. 5 H 2 O (s) ---> Cu. SO 4 (s) + 5 H 2 O (l) Pagina 56 boek Uitgangsstoffen = Beginstoffen = Reactanten = Stoffen voor de pijl 27 mrt 2018 20
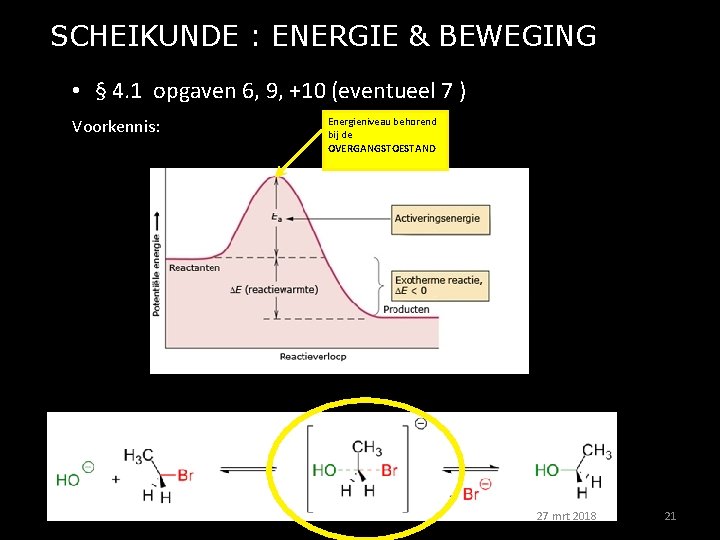
SCHEIKUNDE : ENERGIE & BEWEGING • § 4. 1 opgaven 6, 9, +10 (eventueel 7 ) Voorkennis: Energieniveau behorend bij de OVERGANGSTOESTAND 27 mrt 2018 21

• § 4. 1 opgaven 6, 9, +10 (eventueel 7 ) Reactiewarmte berekenen Bij alle reacties geldt; de totale energie blijft behouden. Maar het is wel zo dat er energie kan worden afgegeven aan de omgeving: exotherme reactie of energie wordt opgenomen uit de omgeving: endotherme reactie. Uit vormingswarmten van de verschillende stoffen kan de reactie-energie van een reactie berekend worden. De geleverde of opgenomen energie van een reactie kan worden beschouwd als de optelsom van warmte Q en arbeid W, bij constante druk geldt Q + W ≈ Q + 0, 0000 … , bij constante druk wordt bij reacties een te verwaarlozen hoeveelheid energie omgezet in bruikbare ‘arbeid’. Hierdoor kunnen reactiewarmtes, vormingswarmtes en energieveranderingen dan in elkaar omgerekend worden. Bij constante druk wordt de reactiewarmte Qp en de enthalpieverandering ΔH genoemd (Binas T 38 A). In de scheikunde-tabellen 56, 57, 59 vind je (bij bepaalde constante druk en temperatuur) de verschillende waarden aan warmten en energieën. ΔE = ΔH bij constante druk (Binas tabellen 56, 57, 59) 27 mrt 2018 22
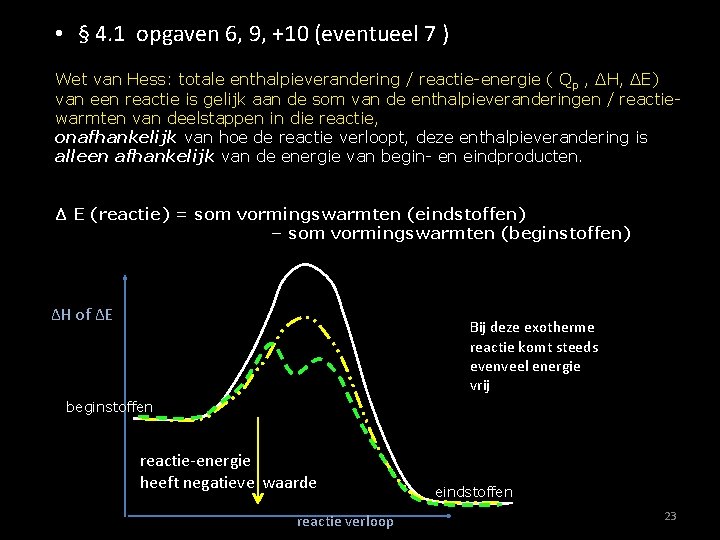
• § 4. 1 opgaven 6, 9, +10 (eventueel 7 ) Wet van Hess: totale enthalpieverandering / reactie-energie ( Qp , ΔH, ΔE) van een reactie is gelijk aan de som van de enthalpieveranderingen / reactiewarmten van deelstappen in die reactie, onafhankelijk van hoe de reactie verloopt, deze enthalpieverandering is alleen afhankelijk van de energie van begin- en eindproducten. Δ E (reactie) = som vormingswarmten (eindstoffen) – som vormingswarmten (beginstoffen) ΔH of ΔE Bij deze exotherme reactie komt steeds evenveel energie vrij beginstoffen reactie-energie heeft negatieve waarde reactie verloop eindstoffen 23
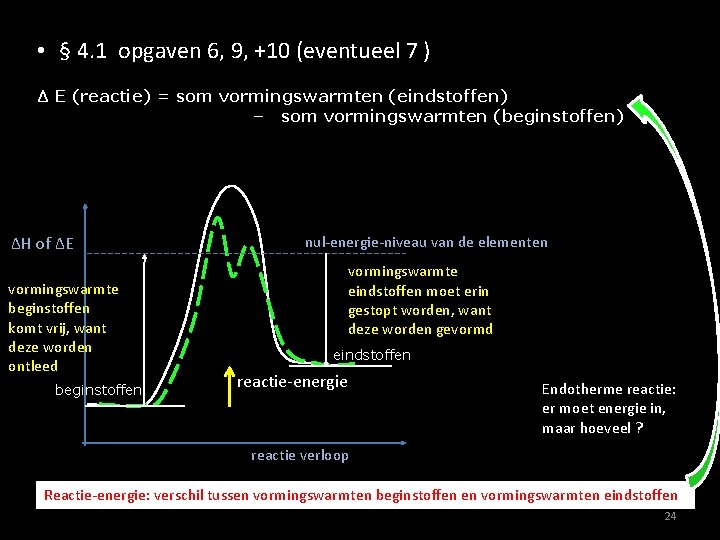
• § 4. 1 opgaven 6, 9, +10 (eventueel 7 ) Δ E (reactie) = som vormingswarmten (eindstoffen) – som vormingswarmten (beginstoffen) ΔH of ΔE vormingswarmte beginstoffen komt vrij, want deze worden ontleed beginstoffen nul-energie-niveau van de elementen vormingswarmte eindstoffen moet erin gestopt worden, want deze worden gevormd eindstoffen reactie-energie Endotherme reactie: er moet energie in, maar hoeveel ? reactie verloop Reactie-energie: verschil tussen vormingswarmten beginstoffen en vormingswarmten eindstoffen 24
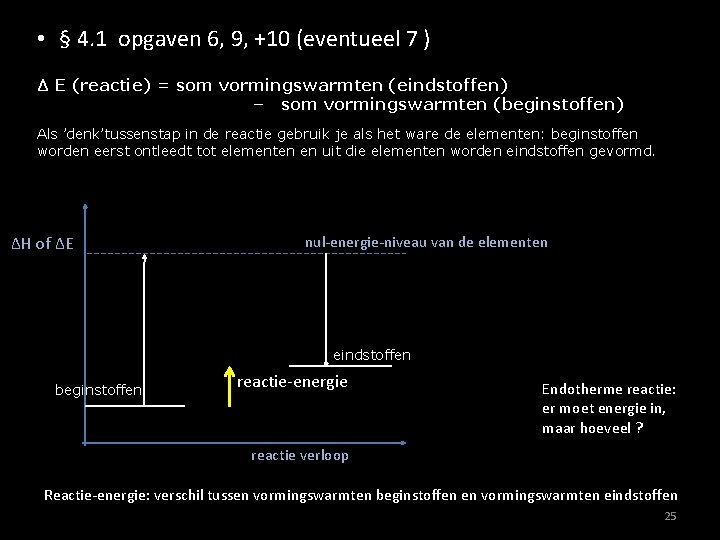
• § 4. 1 opgaven 6, 9, +10 (eventueel 7 ) Δ E (reactie) = som vormingswarmten (eindstoffen) – som vormingswarmten (beginstoffen) Als ’denk’tussenstap in de reactie gebruik je als het ware de elementen: beginstoffen worden eerst ontleedt tot elementen en uit die elementen worden eindstoffen gevormd. ΔH of ΔE nul-energie-niveau van de elementen eindstoffen beginstoffen reactie-energie Endotherme reactie: er moet energie in, maar hoeveel ? reactie verloop Reactie-energie: verschil tussen vormingswarmten beginstoffen en vormingswarmten eindstoffen 25
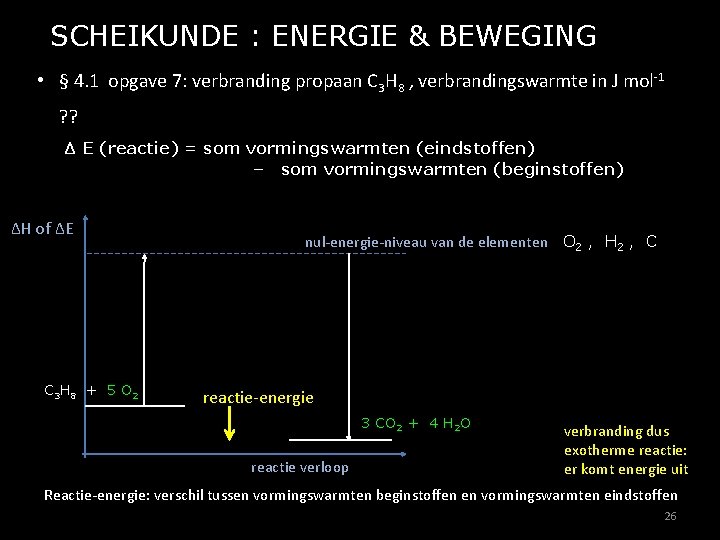
SCHEIKUNDE : ENERGIE & BEWEGING • § 4. 1 opgave 7: verbranding propaan C 3 H 8 , verbrandingswarmte in J mol-1 ? ? Δ E (reactie) = som vormingswarmten (eindstoffen) – som vormingswarmten (beginstoffen) ΔH of ΔE C 3 H 8 + 5 O 2 nul-energie-niveau van de elementen O 2 , H 2 , C reactie-energie 3 CO 2 + 4 H 2 O reactie verloop verbranding dus exotherme reactie: er komt energie uit Reactie-energie: verschil tussen vormingswarmten beginstoffen en vormingswarmten eindstoffen 26
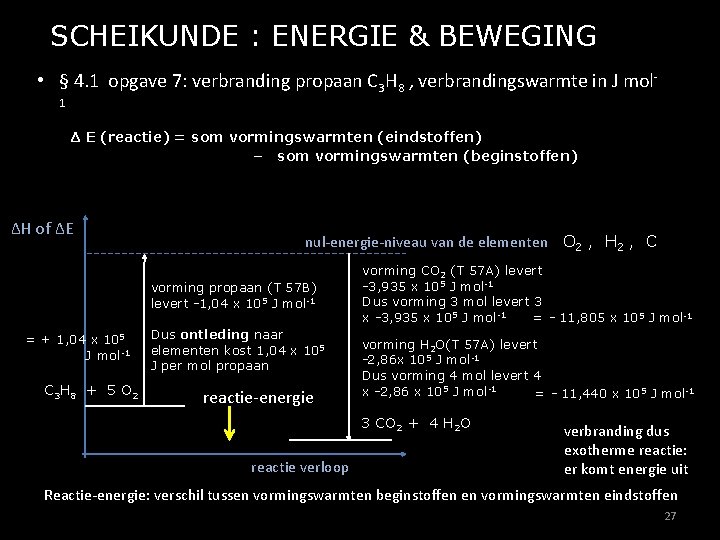
SCHEIKUNDE : ENERGIE & BEWEGING • § 4. 1 opgave 7: verbranding propaan C 3 H 8 , verbrandingswarmte in J mol 1 Δ E (reactie) = som vormingswarmten (eindstoffen) – som vormingswarmten (beginstoffen) ΔH of ΔE nul-energie-niveau van de elementen O 2 , H 2 , C vorming propaan (T 57 B) levert -1, 04 x 105 J mol-1 = + 1, 04 x 105 J mol-1 C 3 H 8 + 5 O 2 Dus ontleding naar elementen kost 1, 04 x 105 J per mol propaan reactie-energie vorming CO 2 (T 57 A) levert -3, 935 x 105 J mol-1 Dus vorming 3 mol levert 3 x -3, 935 x 105 J mol-1 = - 11, 805 x 105 J mol-1 vorming H 2 O(T 57 A) levert -2, 86 x 105 J mol-1 Dus vorming 4 mol levert 4 x -2, 86 x 105 J mol-1 = - 11, 440 x 105 J mol-1 3 CO 2 + 4 H 2 O reactie verloop verbranding dus exotherme reactie: er komt energie uit Reactie-energie: verschil tussen vormingswarmten beginstoffen en vormingswarmten eindstoffen 27
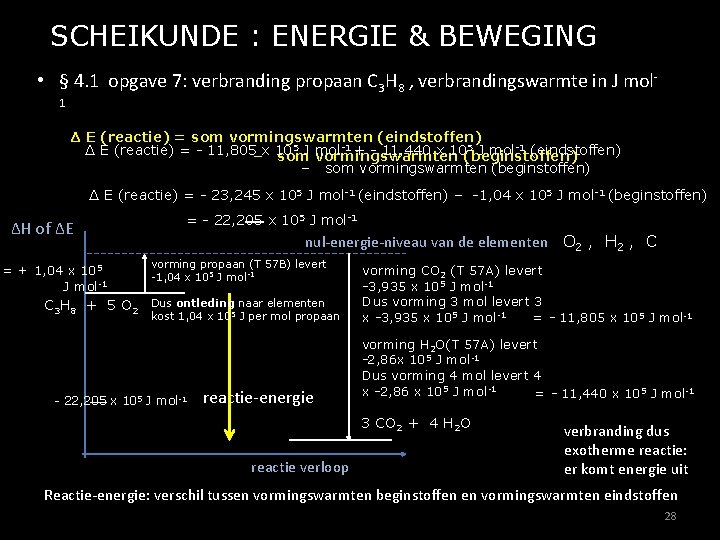
SCHEIKUNDE : ENERGIE & BEWEGING • § 4. 1 opgave 7: verbranding propaan C 3 H 8 , verbrandingswarmte in J mol 1 Δ E (reactie) = som vormingswarmten (eindstoffen) 5 -1 + - 11, 440 x 105 J mol-1 (eindstoffen) Δ E (reactie) = - 11, 805–x 10 som. J mol vormingswarmten (beginstoffen) – som vormingswarmten (beginstoffen) Δ E (reactie) = - 11, 805 x 1055 J mol-1 -1+ - 11, 440 x 105 J mol-1 (eindstoffen) Δ E (reactie) = - 23, 245 x 10 J mol (eindstoffen) – -1, 04 x 105 J mol-1 (beginstoffen) 5 -1 – -1, 04 x 10 J mol (beginstoffen) = 5 = - 22, 205 x 10 J mol-1 ΔH of ΔE = + 1, 04 x 105 J mol-1 C 3 H 8 + 5 O 2 nul-energie-niveau van de elementen O 2 , H 2 , C vorming propaan (T 57 B) levert -1, 04 x 105 J mol-1 Dus ontleding naar elementen kost 1, 04 x 105 J per mol propaan - 22, 205 x 105 J mol-1 reactie-energie vorming CO 2 (T 57 A) levert -3, 935 x 105 J mol-1 Dus vorming 3 mol levert 3 x -3, 935 x 105 J mol-1 = - 11, 805 x 105 J mol-1 vorming H 2 O(T 57 A) levert -2, 86 x 105 J mol-1 Dus vorming 4 mol levert 4 x -2, 86 x 105 J mol-1 = - 11, 440 x 105 J mol-1 3 CO 2 + 4 H 2 O reactie verloop verbranding dus exotherme reactie: er komt energie uit Reactie-energie: verschil tussen vormingswarmten beginstoffen en vormingswarmten eindstoffen 28
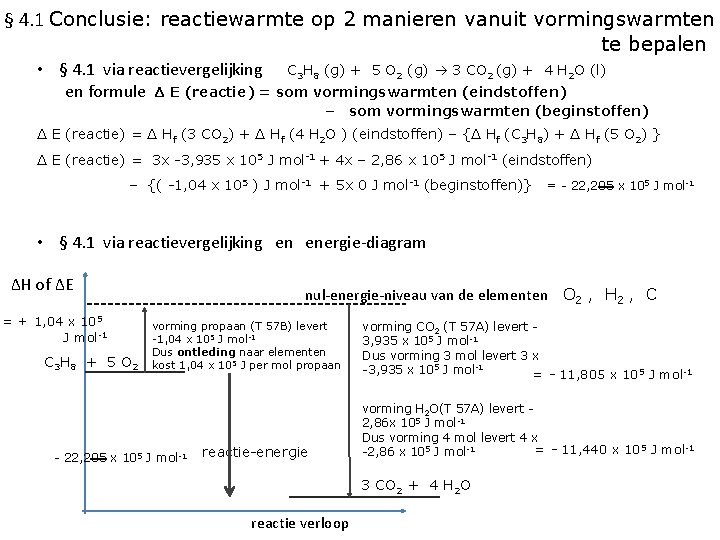
§ 4. 1 Conclusie: reactiewarmte op 2 manieren vanuit vormingswarmten te bepalen • § 4. 1 via reactievergelijking C 3 H 8 (g) + 5 O 2 (g) 3 CO 2 (g) + 4 H 2 O (l) en formule Δ E (reactie) = som vormingswarmten (eindstoffen) – som vormingswarmten (beginstoffen) Δ E (reactie) = Δ Hf (3 CO 2) + Δ Hf (4 H 2 O ) (eindstoffen) – {Δ Hf (C 3 H 8) + Δ Hf (5 O 2) } Δ E (reactie) = 3 x -3, 935 x 105 J mol-1 + 4 x – 2, 86 x 105 J mol-1 (eindstoffen) – {( -1, 04 x 105 ) J mol-1 + 5 x 0 J mol-1 (beginstoffen)} = - 22, 205 x 105 J mol-1 • § 4. 1 via reactievergelijking en energie-diagram ΔH of ΔE = + 1, 04 x 105 J mol-1 C 3 H 8 + 5 O 2 nul-energie-niveau van de elementen O 2 , H 2 , C vorming propaan (T 57 B) levert -1, 04 x 105 J mol-1 Dus ontleding naar elementen kost 1, 04 x 105 J per mol propaan - 22, 205 x 105 J mol-1 reactie-energie vorming CO 2 (T 57 A) levert 3, 935 x 105 J mol-1 Dus vorming 3 mol levert 3 x -3, 935 x 105 J mol-1 = - 11, 805 x 105 J mol-1 vorming H 2 O(T 57 A) levert 2, 86 x 105 J mol-1 Dus vorming 4 mol levert 4 x = - 11, 440 x 105 J mol-1 -2, 86 x 105 J mol-1 3 CO 2 + 4 H 2 O reactie verloop

• § 4. 2 opgaven 11, 13, 14, 15 § 4. 1 opgaven 6, 9, +10 Belangrijke term: soortelijke warmte cp – van een stof of mengsel De hoeveelheid Joule die nodig is om 1 kilogram van die stof/dat mengsel 1 graad Kelvin (of 1 graad Celsius of Fahrenheit) in temperatuur te doen stijgen, gemeten bij constante druk. Symbool cp. Eenheid soortelijke warmte? J kg-1 K-1 Formule voor warmteberekening: Qp = cp m T Binas tabel 35 C 4 § 4. 2 reactiewarmte vanuit reactievergelijking en soortelijke warmte bepalen (via formule Qp = cp m T met juiste eenheden) § 4. 2 opgave 13: reactie magnesium met zoutzuur, reactiewarmte of enthalpie-verandering in J mol-1 voor Mg ? ? Gegevens in opgave: 0, 500 g magnesium + 100 m. L 1, 00 mol L-1 H+ -ionen reactievergelijking: Mg (s) + 2 H+ (aq) Mg 2+ (aq) + 2 H 2 (g) temperatuur neemt toe van 22, 4 ◦C naar 45, 0 ◦C soortelijke warmte van het mengsel is 4, 20 x 103 J mol-1 dichtheid mengsel is 1, 05 g m. L-1 Welke stof in overmaat? Wat is de massa van het mengsel? Hoeveel warmte Qp komt er vrij als 0, 500 g Mg reageert? Wat is de reactiewarmte of enthalpie-verandering in J mol-1 voor Mg? 30
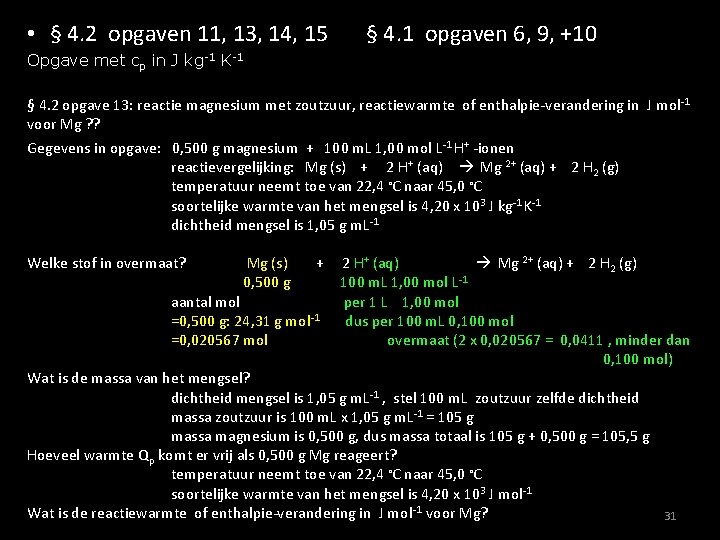
• § 4. 2 opgaven 11, 13, 14, 15 § 4. 1 opgaven 6, 9, +10 Opgave met cp in J kg-1 K-1 § 4. 2 opgave 13: reactie magnesium met zoutzuur, reactiewarmte of enthalpie-verandering in J mol-1 voor Mg ? ? Gegevens in opgave: 0, 500 g magnesium + 100 m. L 1, 00 mol L-1 H+ -ionen reactievergelijking: Mg (s) + 2 H+ (aq) Mg 2+ (aq) + 2 H 2 (g) temperatuur neemt toe van 22, 4 ◦C naar 45, 0 ◦C soortelijke warmte van het mengsel is 4, 20 x 103 J kg-1 K-1 dichtheid mengsel is 1, 05 g m. L-1 Welke stof in overmaat? Mg (s) 0, 500 g + aantal mol =0, 500 g: 24, 31 g mol-1 =0, 020567 mol 2 H+ (aq) Mg 2+ (aq) + 2 H 2 (g) 100 m. L 1, 00 mol L-1 per 1 L 1, 00 mol dus per 100 m. L 0, 100 mol overmaat (2 x 0, 020567 = 0, 0411 , minder dan 0, 100 mol) Wat is de massa van het mengsel? dichtheid mengsel is 1, 05 g m. L-1 , stel 100 m. L zoutzuur zelfde dichtheid massa zoutzuur is 100 m. L x 1, 05 g m. L-1 = 105 g massa magnesium is 0, 500 g, dus massa totaal is 105 g + 0, 500 g = 105, 5 g Hoeveel warmte Qp komt er vrij als 0, 500 g Mg reageert? temperatuur neemt toe van 22, 4 ◦C naar 45, 0 ◦C soortelijke warmte van het mengsel is 4, 20 x 103 J mol-1 Wat is de reactiewarmte of enthalpie-verandering in J mol-1 voor Mg? 31

• § 4. 2 reactiewarmte vanuit reactievergelijking en soortelijke warmte bepalen (via formule Qp = cp m ΔT met juiste eenheden) § 4. 2 opgave 13 met cp in J kg-1 K-1 : reactie magnesium met zoutzuur, reactiewarmte of enthalpieverandering in J mol-1 voor Mg ? ? Gegevens in opgave: 0, 500 g magnesium + 100 m. L 1, 00 mol L-1 H+ -ionen reactievergelijking: Mg (s) + 2 H+ (aq) Mg 2+ (aq) + 2 H 2 (g) temperatuur neemt toe van 22, 4 ◦C naar 45, 0 ◦C soortelijke warmte van het mengsel is 4, 20 x 103 J kg-1 K-1 dichtheid mengsel is 1, 05 g m. L-1 Welke stof in overmaat? Mg (s) + 2 H+ (aq) Mg 2+ (aq) + 2 H 2 (g) =0, 500 g: 24, 31 g mol-1 1, 00 mol L-1 dus per 100 m. L 0, 100 mol =0, 020567 mol overmaat (2 x 0, 020567 = 0, 0411 ) Wat is de massa van het mengsel? massa magnesium is 0, 500 g, dus massa totaal is 105 g + 0, 500 g = 105, 5 g ( Qp = cp m T ) Hoeveel warmte Qp komt er vrij als 0, 500 g Mg reageert? temperatuur neemt toe van 22, 4 ◦C naar 45, 0 ◦C (dus exotherm!) soortelijke warmte van het mengsel is 4, 20 x 103 J kg-1 K-1 105, 5 g mengsel, temperatuur stijgt (45, 0 -22, 4) = 22, 6 ◦C dus ook 22, 6 K Warmte/energie Q die in het 105, 5 gram mengsel zat en nu vrijkomt is 4, 20 x 103 J x 0, 1055 kg x 22, 6 K = 10014, 06 J = 1, 00 x 105 J Wat is de reactiewarmte of enthalpie-verandering in J mol-1 voor Mg? = 10014, 06 J per 0, 020567 mol Dus voor 1 mol = 10014, 06 : 0, 020567 J/mol = 486899 J mol -1 = 4, 87 x 105 J mol-1 deze warmte komt vrij (exotherm), daarom is de reactiewarmte -4, 87 x 105 J mol-1

• § 4. 4 Botsende deeltjes model Bij elke chemische reactie treedt een energie-effect op (voorkennis en § 4. 1 en § 4. 2) : exotherm (reactiewarmte heeft –waarde) of endotherm (reactiewarmte heeft +waarde) Het botsende deeltjes model: deeltjes van reagerende stoffen moeten met elkaar ‘botsen’ om überhaupt te kunnen reageren: 5 factoren die bepalen of een reactie snel of traag verloopt, dus die de snelheid van een reactie bepalen zijn: • reactiviteit van het soort deeltje dat reageert: grotere reactiviteit grotere reactiesnelheid, meer effectieve botsingen • concentratie van de deeltjes die reageren: grotere concentratie (mol L-1) grotere snelheid, vaker botsingen • verdelingsgraad van de reagerende stoffen: fijner verdeeld grotere snelheid, vaker botsingen • temperatuur waarbij de deeltjes reageren: hogere temperatuur grotere reactiesnelheid, botsingen met meer energie • aanwezigheid van een katalysator : hulpstof die ervoor zorgt dat de reagerende deeltjes sneller met elkaar reageren. Katalysator houdt reagerende deeltjes bij elkaar: effectievere botsing. Na afloop van de reactie is de katalysator precies hetzelfde als voor de reactie. Een katalysator verandert niet door de reactie, wordt niet verbruikt en staat niet in de reactievergelijking.
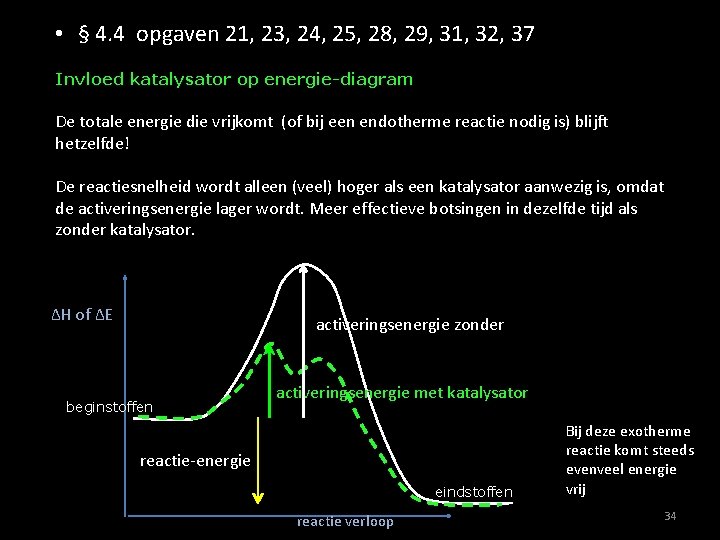
• § 4. 4 opgaven 21, 23, 24, 25, 28, 29, 31, 32, 37 Invloed katalysator op energie-diagram De totale energie die vrijkomt (of bij een endotherme reactie nodig is) blijft hetzelfde! De reactiesnelheid wordt alleen (veel) hoger als een katalysator aanwezig is, omdat de activeringsenergie lager wordt. Meer effectieve botsingen in dezelfde tijd als zonder katalysator. ΔH of ΔE activeringsenergie zonder beginstoffen activeringsenergie met katalysator reactie-energie eindstoffen reactie verloop Bij deze exotherme reactie komt steeds evenveel energie vrij 34

+ 120 - 1 x 0, 05 - 3 x 0, 05

SCHEIKUNDE : ENERGIE & BEWEGING • § 4. 1 opgaven 6, 9, +10 (eventueel 7 ) • § 4. 2 opgaven 11, 13, 14, 15 • § 4. 4 opgaven 21, 23, 24, 25, 28, 29, 31, 32, 37 • § 4. 3 opgaven 19 a, b, c, 20, § 4. 4 opgave 36 • Extra oefenopgaven • Practicum zouten (PO proeven 1, 2, 3, 4, 5) Rendement definitie – Binas T 37 H 3 april 2018 36
- Slides: 36