Chemie fr Mediziner und Medizinische Biologen Hochschuldozent Klaus

Chemie für Mediziner und Medizinische Biologen Hochschuldozent Klaus Schaper WS 2007/2008

Inhalt: Organische Chemie 10 11 12 13 14 15 16 17 18 19 20 21 PSE Einführung und Überblick Kohlenwasserstoffe Einfache funktionelle Gruppen Aldehyde und Ketone Chinone Carbonsäuren und Carbonsäurederivate Derivate anorganischer Säuren Stereochemie Aminosäuren und Peptide Kohlenhydrate Heterocyclen Spektroskopie Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 2

Definition PSE 18. Jahrhundert Verbindungen mineralischer Natur (Salze, Erze) sind anorganisch, Verbindungen die in lebenden Wesen vorkommen/entstehen sind organisch. Es galt als ausgeschlossen, dass es im Labor möglich ist anorganische Substanzen in organische Substanzen zu überführen. Friedrich Wöhler 1828: Anorganisch Organisch Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 3
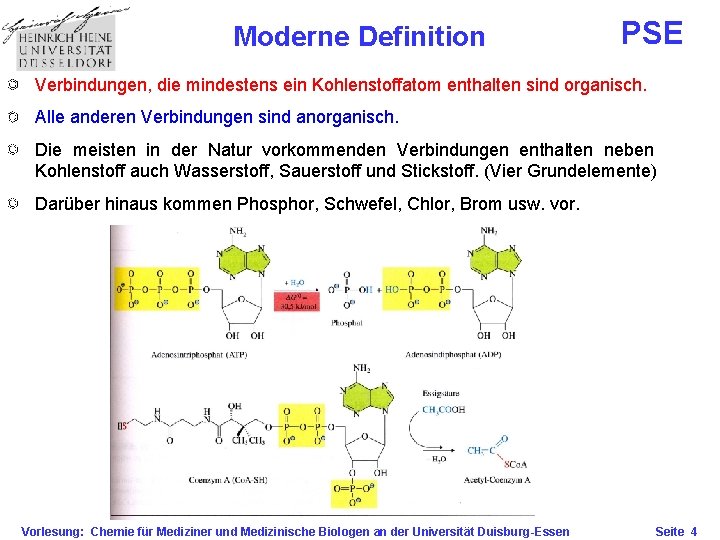
Moderne Definition PSE Verbindungen, die mindestens ein Kohlenstoffatom enthalten sind organisch. Alle anderen Verbindungen sind anorganisch. Die meisten in der Natur vorkommenden Verbindungen enthalten neben Kohlenstoff auch Wasserstoff, Sauerstoff und Stickstoff. (Vier Grundelemente) Darüber hinaus kommen Phosphor, Schwefel, Chlor, Brom usw. vor. Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 4
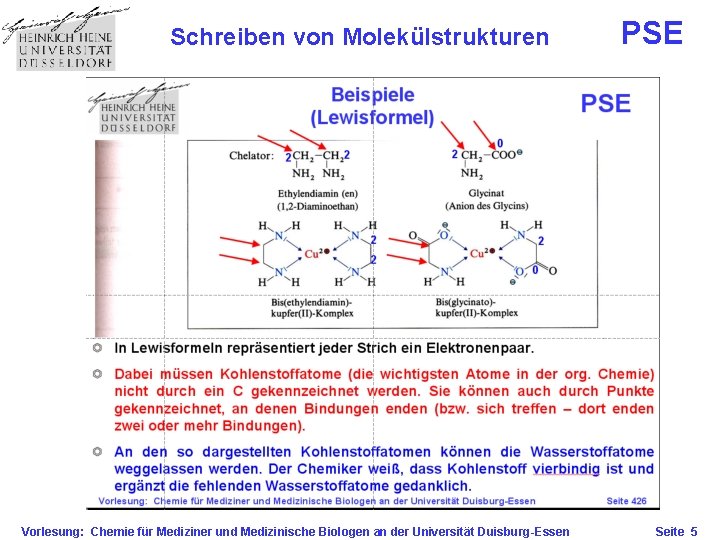
Schreiben von Molekülstrukturen Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen PSE Seite 5

Die kovalente Bindung PSE Kohlenstoff ist wie kein anderes Element in der Lage mit sich selbst und mit anderen Atomen kovalente Bindungen einzugehen. Dabei bildet Kohlenstoff vier Einfachbindungen (4 s-Bindungen), zwei Einfach und eine Doppelbindung (3 s-Bindungen und 1 p-Bindung), zwei Doppelbindungen (2 s-Bindungen und 2 p-Bindungen), oder eine Einfachbindung und eine Dreifachbindung (2 s-Bindungen und 2 p. Bindungen), Ein Kohlenstoffatom mit 4 s-Bindungen ist sp 3 -hybridisiert, mit 3 s-Bindungen und einer p-Bindung ist sp 2 -hybridisiert, und mit 2 s-Bindungen und zwei p-Bindungen ist sp-hybridisiert. Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 6

Die kovalente Bindung PSE Ein Kohlenstoffatom mit 4 s-Bindungen ist sp 3 -hybridisiert, mit 3 s-Bindungen und einer p-Bindung ist sp 2 -hybridisiert, und mit 2 s-Bindungen und zwei p-Bindungen ist sp-hybridisiert. Ein sp 3 -hybridisiert Kohlenstoffatom ist tetraedrisch, sp 2 -hybridisiert Kohlenstoffatom ist trigonal planar, und sp-hybridisiert Kohlenstoffatom ist linear. Um s-Bindungen ist eine freie Rotation möglich. An einem sp 2 -hybridisiertem Kohlenstoffatom steht das verbleibende p-Orbital senkrecht zur „trigonal-planaren“ Ebene. Es führt zur Ausbildung der p-Bindung und verhindert die freie Rotation. Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 7

Die kovalente Bindung PSE Ein Kohlenstoffatom kann Einfachbindungen bilden mit sich selbst, Wasserstoff, oder einem anderen Atom. Diese Atome nennt man Heteroatome. (Dies sind u. a. Stickstoff, Phosphor, Sauerstoff, Schwefel, Selen, Fluor, Chlor, Brom, Iod) Ein Kohlenstoffatom kann Doppelbindungen bilden mit sich selbst, oder einem Heteroatom (Stickstoff, Phosphor, Sauerstoff, Schwefel, Selen) Ein Kohlenstoffatom kann Dreifachbindungen bilden mit sich selbst, oder mit Stickstoff. Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 8

Inhalt: Organische Chemie 10 11 12 13 14 15 16 17 18 19 20 21 PSE Einführung und Überblick Kohlenwasserstoffe Einfache funktionelle Gruppen Aldehyde und Ketone Chinone Carbonsäuren und Carbonsäurederivate Derivate anorganischer Säuren Stereochemie Aminosäuren und Peptide Kohlenhydrate Heterocyclen Spektroskopie Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 9

Inhalt: Organische Chemie PSE 11 Kohlenwasserstoffe 11. 1 Alkane 11. 2 Cycloalkane 11. 3 Reaktionen der Alkane 11. 4 Alkene 11. 5 Alkine 11. 6 Aromaten 11. 7 Thermodynamik und Kinetik Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 10

Alkane PSE Alkane Gesättigte Kohlenwasserstoffe Aliphatische Kohlenwasserstoffe Aliphaten Es gibt nur C-C und C-H s-Bindungen Es gilt die allgemeine Summenformel: Cn. H 2 n+2 Man bezeichnet Alkane mit verschiedenen n als homologe Reihe Aromaten-Aliphaten: ARAL Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 11
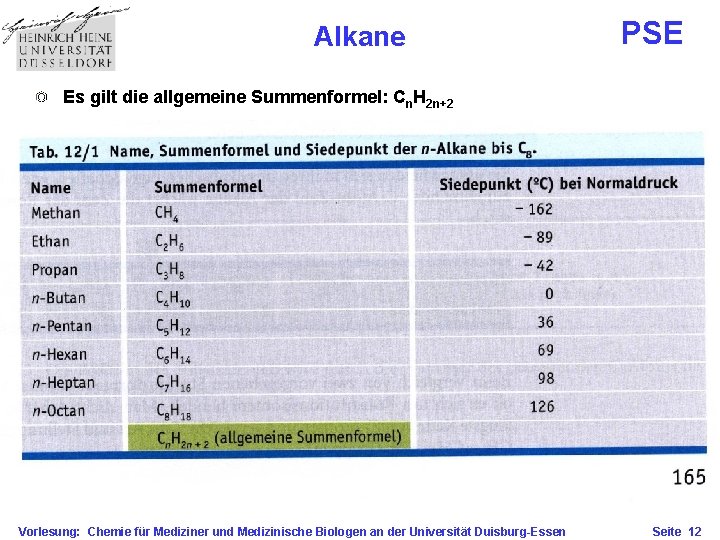
Alkane PSE Es gilt die allgemeine Summenformel: Cn. H 2 n+2 Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 12
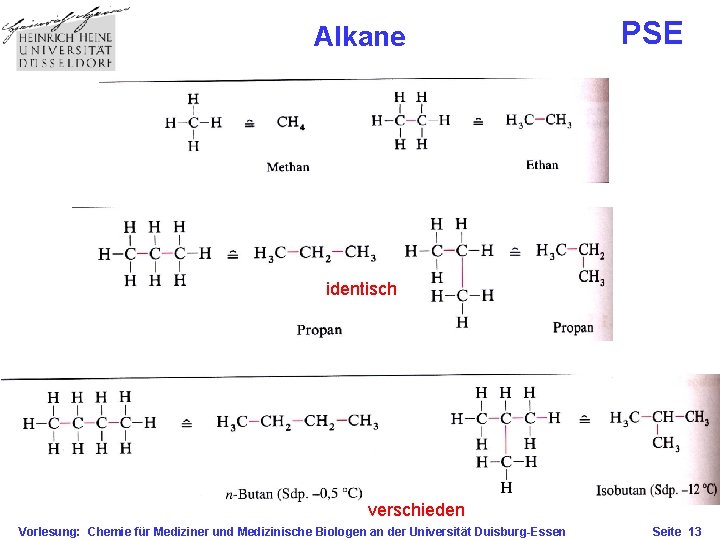
Alkane PSE identisch verschieden Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 13
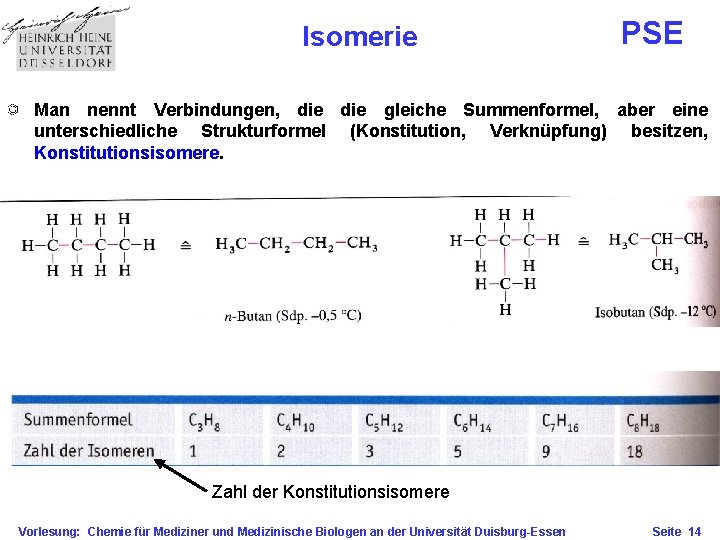
Isomerie PSE Man nennt Verbindungen, die gleiche Summenformel, aber eine unterschiedliche Strukturformel (Konstitution, Verknüpfung) besitzen, Konstitutionsisomere. Zahl der Konstitutionsisomere Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 14
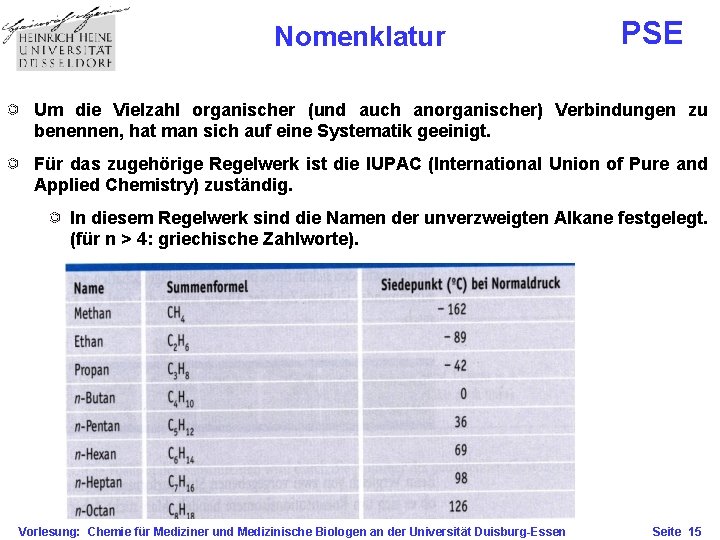
Nomenklatur PSE Um die Vielzahl organischer (und auch anorganischer) Verbindungen zu benennen, hat man sich auf eine Systematik geeinigt. Für das zugehörige Regelwerk ist die IUPAC (International Union of Pure and Applied Chemistry) zuständig. In diesem Regelwerk sind die Namen der unverzweigten Alkane festgelegt. (für n > 4: griechische Zahlworte). Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 15

Nomenklatur PSE Pentagon Methan Ethan Propan Hexagramm Butan Pentan Hexan Heptameter: sieben füßiger Vers Heptan Octupus vulgaris Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 16
PSE Nomenklatur Nonius Octan Nonan Uno Decan Undecan Dekade Dodecan Dodekaphonie Tridecan (Arnold Schönberg) Tetradecan Pentadecan Triangel … Icosan (n=20) Tetraeder Icosaeder Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 17

Nomenklatur PSE Um die Vielzahl organischer (und auch anorganischer) Verbindungen zu benennen, hat man sich auf eine Systematik geeinigt. Für das zugehörige Regelwerk ist die IUPAC (International Union of Pure and Applied Chemistry) zuständig. In diesem Regelwerk sind die Namen der unverzweigten Alkane festgelegt. (für n > 4: griechische Zahlworte). Bei verzweigten Kohlenwasserstoffen (siehe Isobutan = 2 -Methylpropan) sucht man die längste unverzweigte Kette im Molekül. Dieser Name bildet den Stamm des vollständigen Namens. Nun sucht man Kohlenstoffreste, die ein Wasserstoffatom ersetzen und so zur Verzweigung führen. Solche Reste bezeichnet man als Alkylreste (von Alkan). Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 18
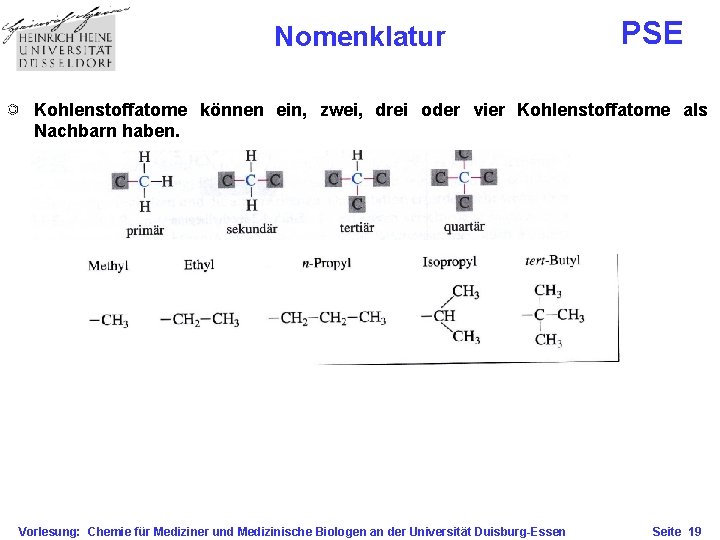
Nomenklatur PSE Kohlenstoffatome können ein, zwei, drei oder vier Kohlenstoffatome als Nachbarn haben. Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 19
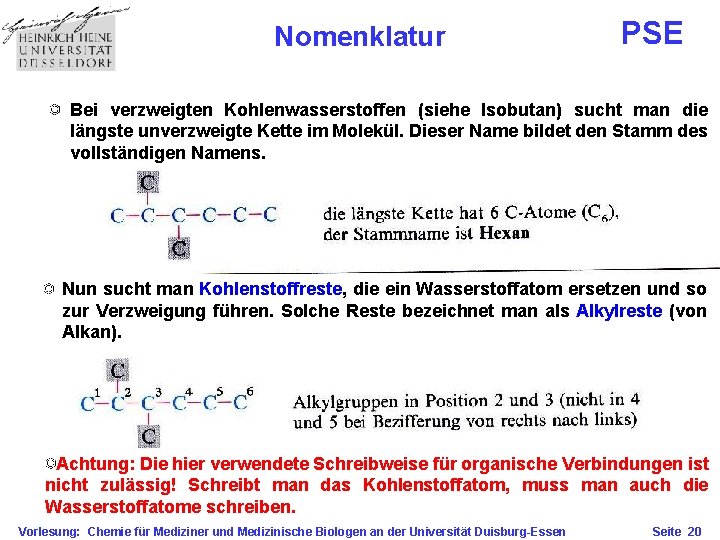
Nomenklatur PSE Bei verzweigten Kohlenwasserstoffen (siehe Isobutan) sucht man die längste unverzweigte Kette im Molekül. Dieser Name bildet den Stamm des vollständigen Namens. Nun sucht man Kohlenstoffreste, die ein Wasserstoffatom ersetzen und so zur Verzweigung führen. Solche Reste bezeichnet man als Alkylreste (von Alkan). Achtung: Die hier verwendete Schreibweise für organische Verbindungen ist nicht zulässig! Schreibt man das Kohlenstoffatom, muss man auch die Wasserstoffatome schreiben. Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 20
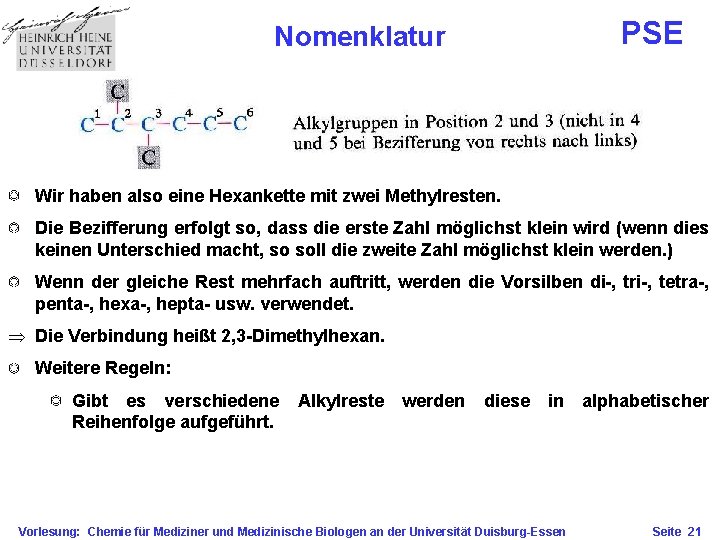
PSE Nomenklatur Wir haben also eine Hexankette mit zwei Methylresten. Die Bezifferung erfolgt so, dass die erste Zahl möglichst klein wird (wenn dies keinen Unterschied macht, so soll die zweite Zahl möglichst klein werden. ) Wenn der gleiche Rest mehrfach auftritt, werden die Vorsilben di-, tri-, tetra-, penta-, hexa-, hepta- usw. verwendet. Þ Die Verbindung heißt 2, 3 -Dimethylhexan. Weitere Regeln: Gibt es verschiedene Reihenfolge aufgeführt. Alkylreste werden diese in Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen alphabetischer Seite 21
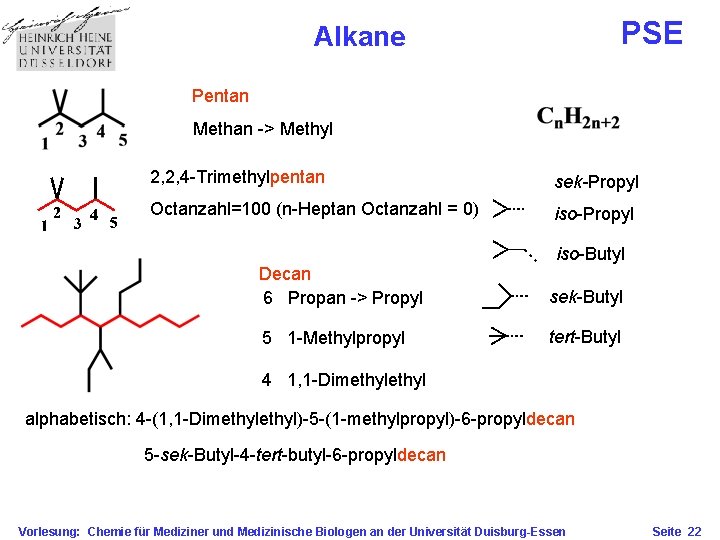
PSE Alkane Pentan Methan -> Methyl 2, 2, 4 -Trimethylpentan sek-Propyl Octanzahl=100 (n-Heptan Octanzahl = 0) iso-Propyl iso-Butyl Decan 6 Propan -> Propyl sek-Butyl 5 1 -Methylpropyl tert-Butyl 4 1, 1 -Dimethyl alphabetisch: 4 -(1, 1 -Dimethyl)-5 -(1 -methylpropyl)-6 -propyldecan 5 -sek-Butyl-4 -tert-butyl-6 -propyldecan Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 22
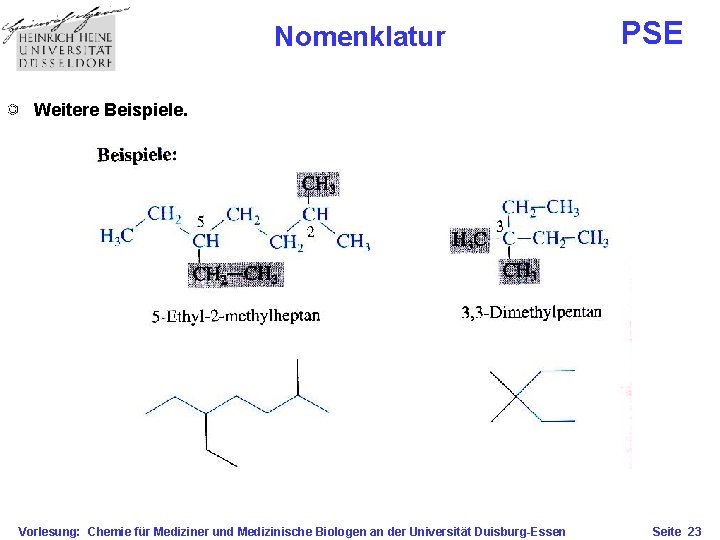
Nomenklatur PSE Weitere Beispiele. Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 23
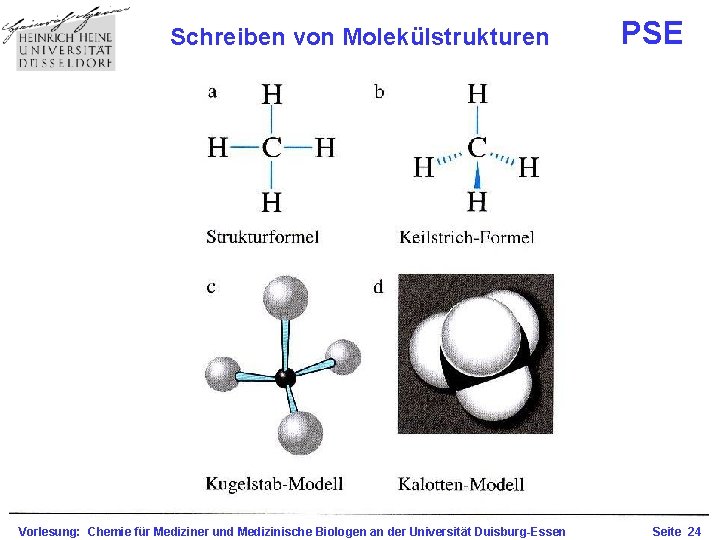
Schreiben von Molekülstrukturen Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen PSE Seite 24

Konformationsisomere/Konformere PSE Ethan besteht aus zwei Methylgruppen, die durch eine Einfachbindung miteinander verbunden sind. Um s-Bindungen ist eine freie Rotation möglich. Durch Verdrehung der beiden Methylgruppen gegeneinander entstehen unterschiedliche räumliche Anordnungen, also Isomere. Im Gegensatz zu den oben diskutierten Konstitutionsisomeren (Verküpfungsisomeren) haben hier beide Strukturen die gleiche Verknüpfung. Sie gehen durch Rotation um eine Einfachbindung auseinander hervor und werden daher als Rotationsisomere oder Konformere bezeichnet. Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 25
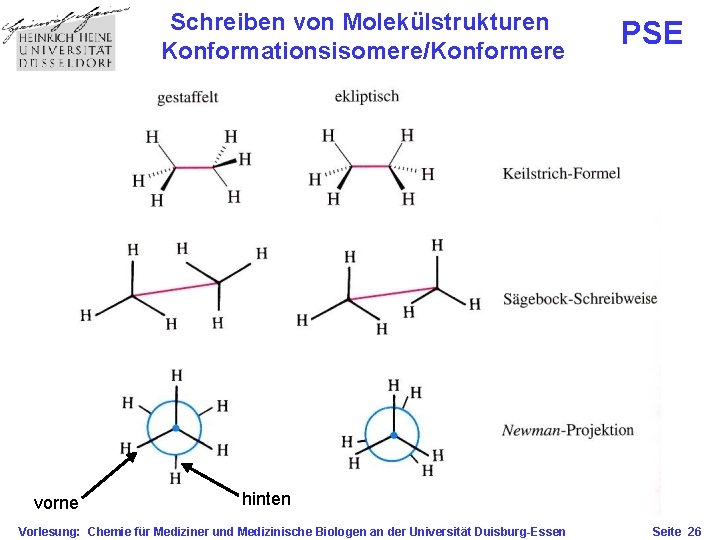
Schreiben von Molekülstrukturen Konformationsisomere/Konformere vorne PSE hinten Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 26
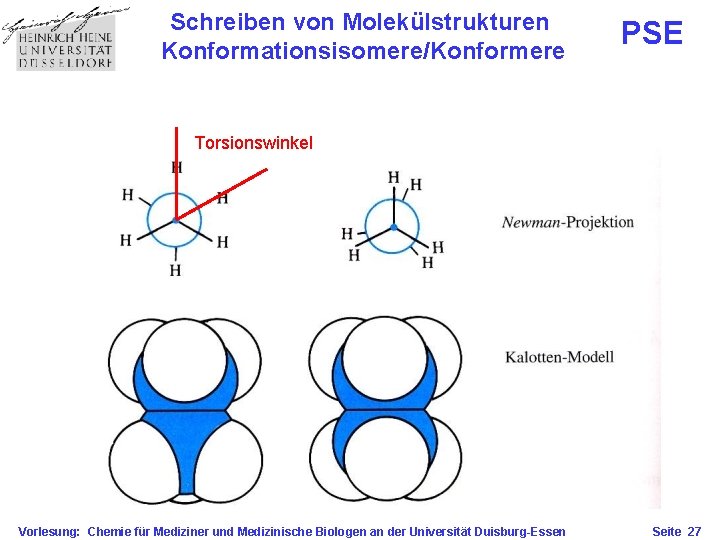
Schreiben von Molekülstrukturen Konformationsisomere/Konformere PSE Torsionswinkel Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 27
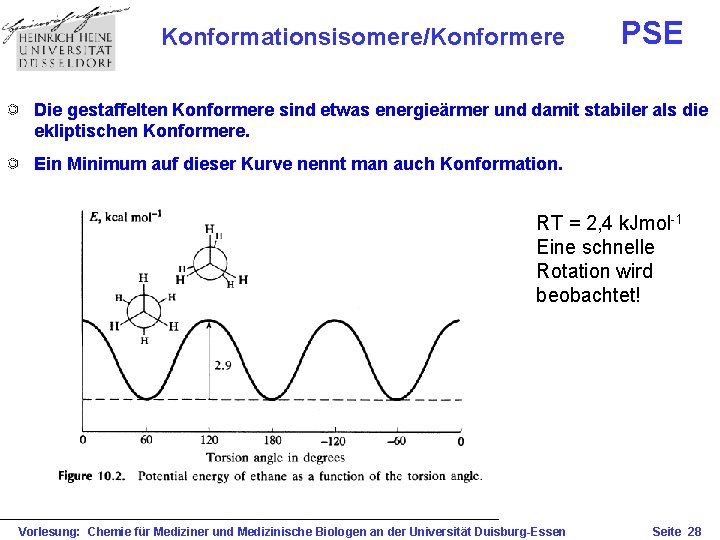
Konformationsisomere/Konformere PSE Die gestaffelten Konformere sind etwas energieärmer und damit stabiler als die ekliptischen Konformere. Ein Minimum auf dieser Kurve nennt man auch Konformation. RT = 2, 4 k. Jmol-1 Eine schnelle Rotation wird beobachtet! Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 28

Schreiben von Molekülstrukturen Konformationsisomere/Konformere Konformationen PSE keine Konformation Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 29
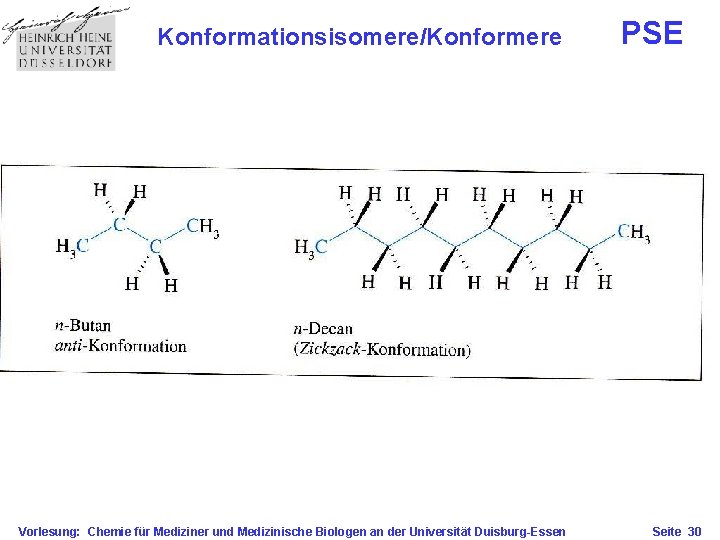
Konformationsisomere/Konformere Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen PSE Seite 30

Konformationsisomere/Konformere Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen PSE Seite 31

Physikalische Eigenschaften PSE Die C-H-Bindung ist sehr unpolar. Daher sind Kohlenwasserstoffe allgemein oder hier die Alkane hydrophob, lipophil. Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 32

Physikalische Eigenschaften PSE Die Moleküle werden untereinander nur durch Van-der-Waals-Kräfte zusammen gehalten. Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 33

Physikalische Eigenschaften PSE Die Moleküle werden untereinander nur durch Van-der-Waals-Kräfte zusammen gehalten. Diese Kräfte sind schwach. Die Kräfte nehmen zu, wenn die Moleküle größer werden. Daher steigen die Siedepunkte, wenn die Moleküle größer werden. Dabei ist die Oberfläche des Moleküls von Bedeutung. Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 34

Alkane PSE Hauptquellen für Alkane sind Erdgas (Methan, Ethan, Propan, Butan) und Erdöl wird durch stufenweise (fraktionierte) Destillation in seine Bestandteile zerlegt. Petrolether (C 5 -C 7) Benzin (C 7 -C 12) Dieselöl (C 15 -C 18) Paraffin (C 20 -C 30) Kohlenwasserstoffe schwimmen auf Wasser (Tankerunfall) Kohlenwasserstoffe werden schlecht biologisch abgebaut. Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 35

Methan, Paraffine PSE Hauptquellen für Methan ist Erdgas. Es entsteht auch in Sümpfen (Verwesung) und Reisfeldern und wird von Kühen ausgeschieden. Methan ist ein Treibhausgas. Es wirkt stärker als Kohlendioxid. Es bleibt in der Atmosphäre länger erhalten. Es wird zu Kohlendioxid abgebaut. Methan kommt als Methanhydrat in den Ozeanen vor (siehe der Schwarm). Paraffine werden als Salbengrundlage benutzt. Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 36

Fragen 12. 1/Zeeck Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen PSE Seite 37

Inhalt: Organische Chemie PSE 11 Kohlenwasserstoffe 11. 1 Alkane 11. 2 Cycloalkane 11. 3 Reaktionen der Alkane 11. 4 Alkene 11. 5 Alkine 11. 6 Aromaten 11. 7 Thermodynamik und Kinetik Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 38
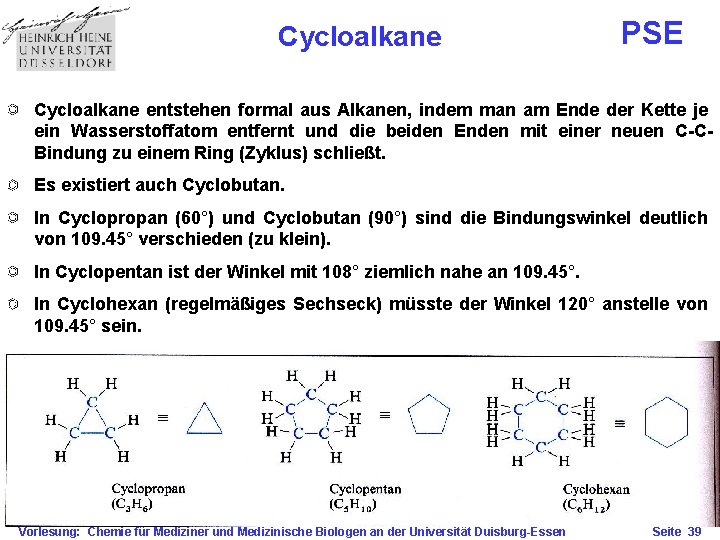
Cycloalkane PSE Cycloalkane entstehen formal aus Alkanen, indem man am Ende der Kette je ein Wasserstoffatom entfernt und die beiden Enden mit einer neuen C-CBindung zu einem Ring (Zyklus) schließt. Es existiert auch Cyclobutan. In Cyclopropan (60°) und Cyclobutan (90°) sind die Bindungswinkel deutlich von 109. 45° verschieden (zu klein). In Cyclopentan ist der Winkel mit 108° ziemlich nahe an 109. 45°. In Cyclohexan (regelmäßiges Sechseck) müsste der Winkel 120° anstelle von 109. 45° sein. Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 39

PSE Cyclohexan In Cyclohexan (regelmäßiges Sechseck) müsste der Winkel 120° anstelle von 109. 45° sein. In beiden Konformeren sind alle Bindungswinkel 109. 45°. In der Sesselform stehen alle Gruppen gestaffelt (gauche). In der Wannenform gibt es ekliptische Wechselwirkungen. Eine Konformationen Keine Konformation Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 40

Cyclohexane Axial/Equatorial PSE Nicht alle zwölf Wasserstoffatome im Cyclohexan sind gleich. Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 41
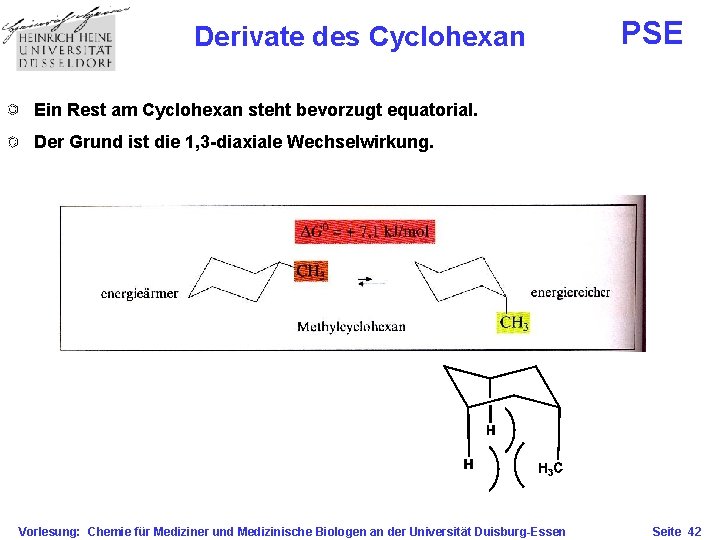
Derivate des Cyclohexan PSE Ein Rest am Cyclohexan steht bevorzugt equatorial. Der Grund ist die 1, 3 -diaxiale Wechselwirkung. Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 42
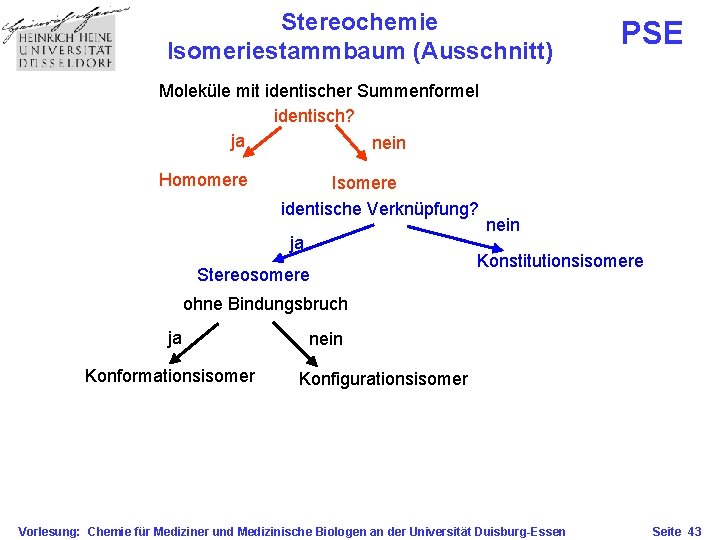
Stereochemie Isomeriestammbaum (Ausschnitt) PSE Moleküle mit identischer Summenformel identisch? ja nein Homomere Isomere identische Verknüpfung? ja Stereosomere nein Konstitutionsisomere ohne Bindungsbruch ja Konformationsisomer nein Konfigurationsisomer Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 43
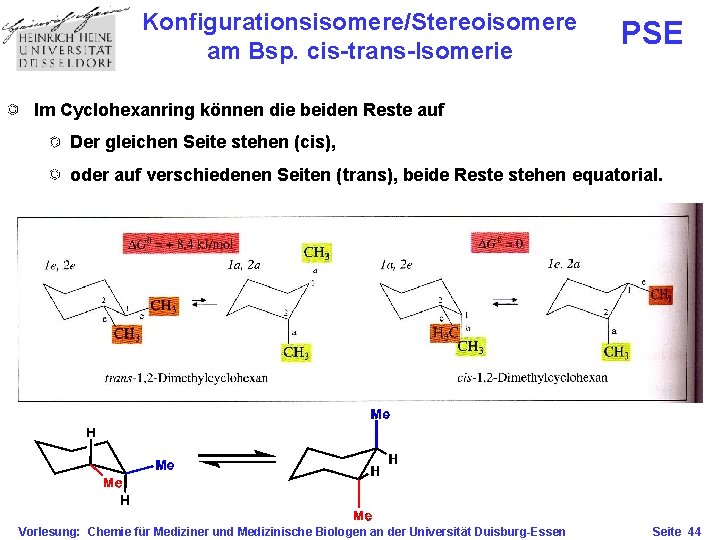
Konfigurationsisomere/Stereoisomere am Bsp. cis-trans-Isomerie PSE Im Cyclohexanring können die beiden Reste auf Der gleichen Seite stehen (cis), oder auf verschiedenen Seiten (trans), beide Reste stehen equatorial. Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 44

Derivate des Cyclohexan PSE Im Dekalin können die beiden Reste cis oder trans verknüpft sein. . Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 45

Fragen 12. 2/Zeeck Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen PSE Seite 46

Inhalt: Organische Chemie PSE 11 Kohlenwasserstoffe 11. 1 Alkane 11. 2 Cycloalkane 11. 3 Reaktionen der Alkane 11. 4 Alkene 11. 5 Alkine 11. 6 Aromaten 11. 7 Thermodynamik und Kinetik Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 47

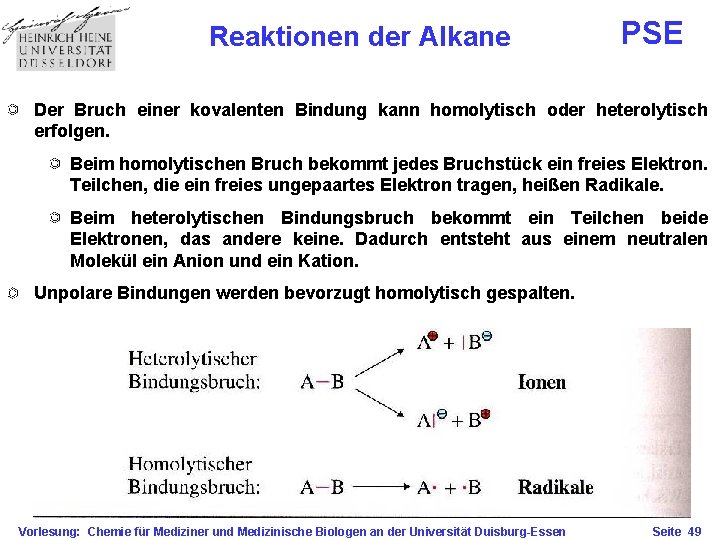
Reaktionen der Alkane PSE Der Bruch einer kovalenten Bindung kann homolytisch oder heterolytisch erfolgen. Beim homolytischen Bruch bekommt jedes Bruchstück ein freies Elektron. Teilchen, die ein freies ungepaartes Elektron tragen, heißen Radikale. Beim heterolytischen Bindungsbruch bekommt ein Teilchen beide Elektronen, das andere keine. Dadurch entsteht aus einem neutralen Molekül ein Anion und ein Kation. Unpolare Bindungen werden bevorzugt homolytisch gespalten. Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 48
Reaktionen der Alkane PSE Der Bruch einer kovalenten Bindung kann homolytisch oder heterolytisch erfolgen. Beim homolytischen Bruch bekommt jedes Bruchstück ein freies Elektron. Teilchen, die ein freies ungepaartes Elektron tragen, heißen Radikale. Beim heterolytischen Bindungsbruch bekommt ein Teilchen beide Elektronen, das andere keine. Dadurch entsteht aus einem neutralen Molekül ein Anion und ein Kation. Unpolare Bindungen werden bevorzugt homolytisch gespalten. Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 49
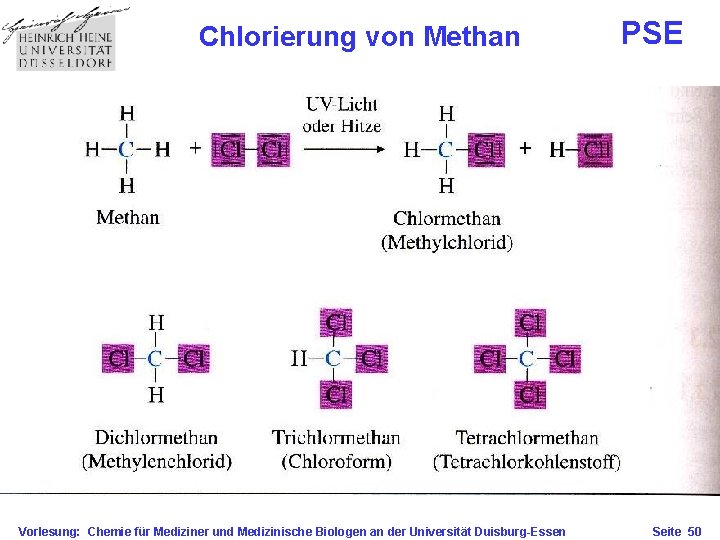
Chlorierung von Methan Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen PSE Seite 50
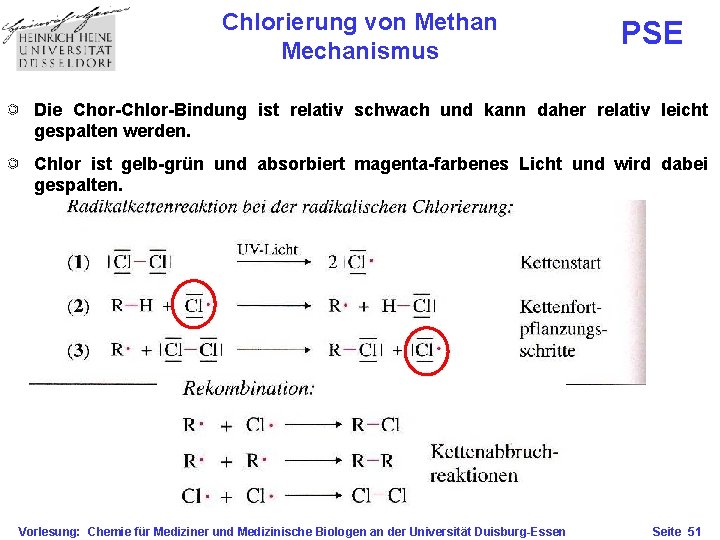
Chlorierung von Methan Mechanismus PSE Die Chor-Chlor-Bindung ist relativ schwach und kann daher relativ leicht gespalten werden. Chlor ist gelb-grün und absorbiert magenta-farbenes Licht und wird dabei gespalten. Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 51
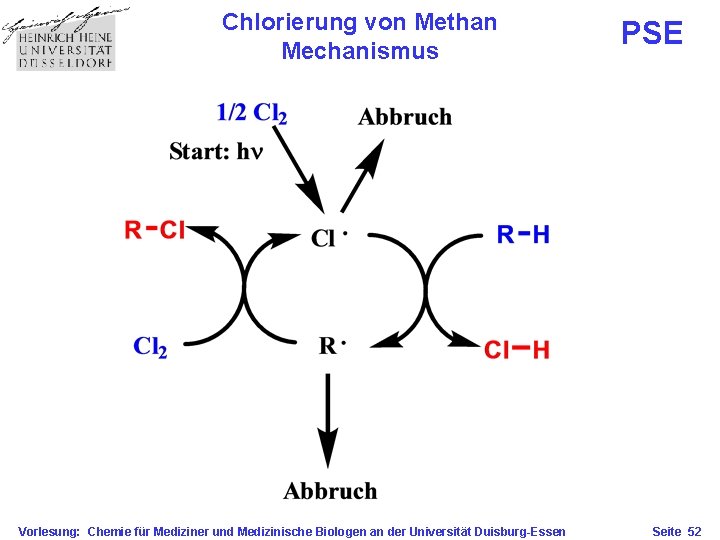
Chlorierung von Methan Mechanismus Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen PSE Seite 52
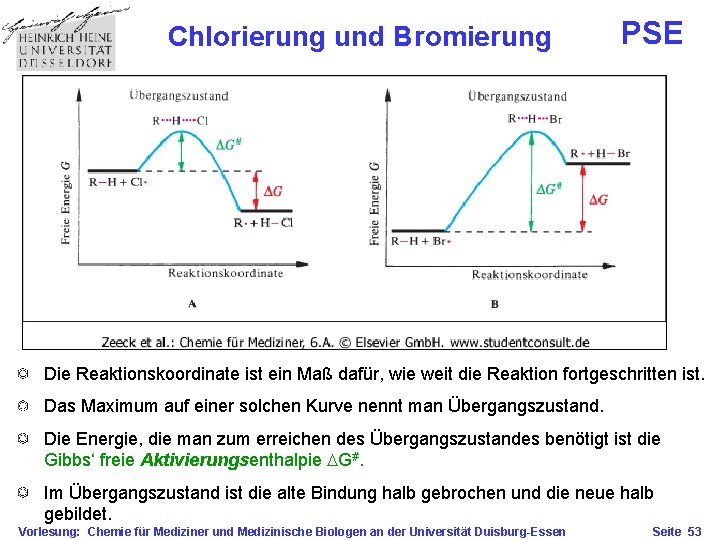
Chlorierung und Bromierung PSE Die Reaktionskoordinate ist ein Maß dafür, wie weit die Reaktion fortgeschritten ist. Das Maximum auf einer solchen Kurve nennt man Übergangszustand. Die Energie, die man zum erreichen des Übergangszustandes benötigt ist die Gibbs‘ freie Aktivierungsenthalpie DG#. Im Übergangszustand ist die alte Bindung halb gebrochen und die neue halb gebildet. Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 53
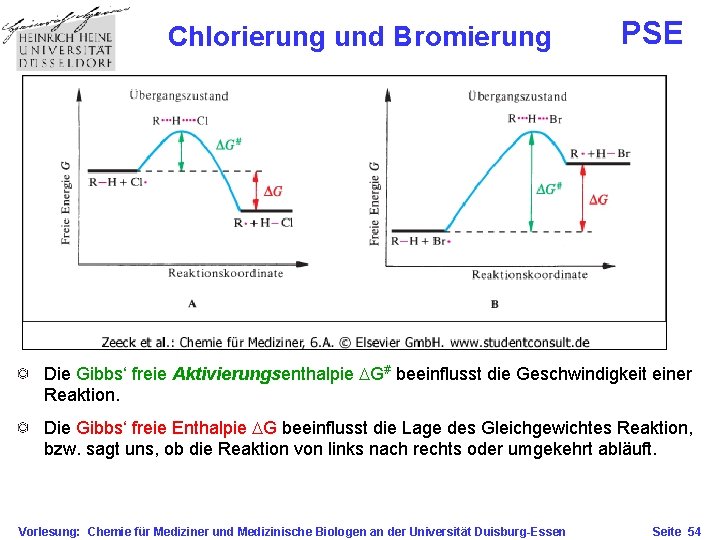
Chlorierung und Bromierung PSE Die Gibbs‘ freie Aktivierungsenthalpie DG# beeinflusst die Geschwindigkeit einer Reaktion. Die Gibbs‘ freie Enthalpie DG beeinflusst die Lage des Gleichgewichtes Reaktion, bzw. sagt uns, ob die Reaktion von links nach rechts oder umgekehrt abläuft. Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 54
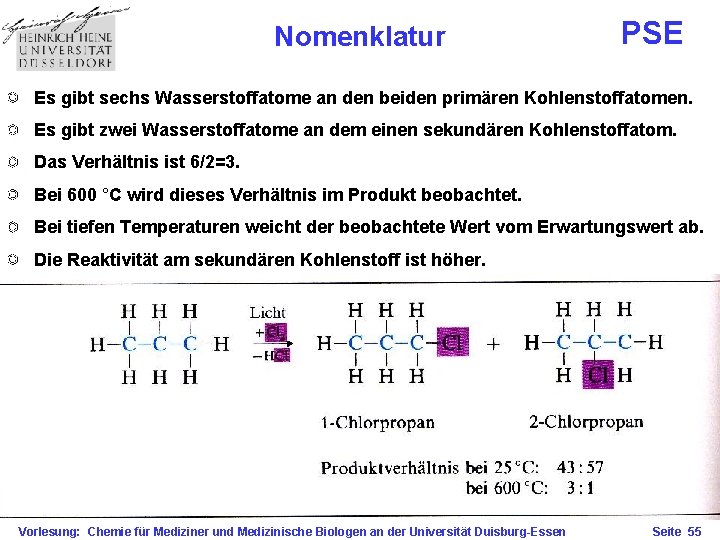
Nomenklatur PSE Es gibt sechs Wasserstoffatome an den beiden primären Kohlenstoffatomen. Es gibt zwei Wasserstoffatome an dem einen sekundären Kohlenstoffatom. Das Verhältnis ist 6/2=3. Bei 600 °C wird dieses Verhältnis im Produkt beobachtet. Bei tiefen Temperaturen weicht der beobachtete Wert vom Erwartungswert ab. Die Reaktivität am sekundären Kohlenstoff ist höher. Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 55
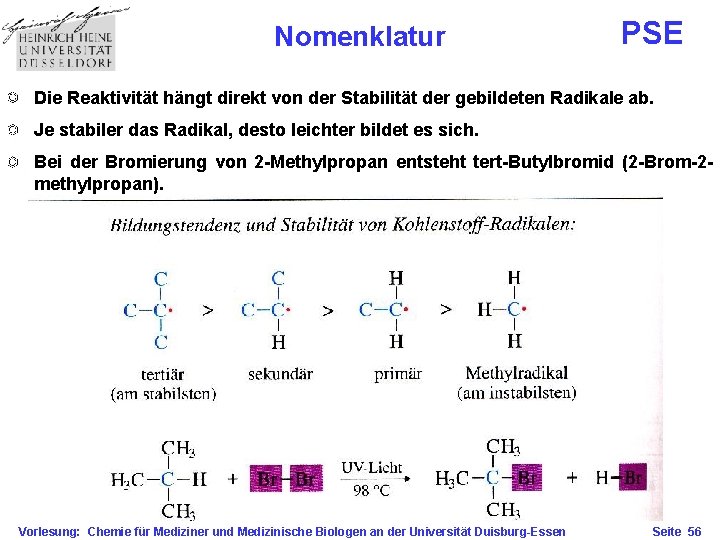
Nomenklatur PSE Die Reaktivität hängt direkt von der Stabilität der gebildeten Radikale ab. Je stabiler das Radikal, desto leichter bildet es sich. Bei der Bromierung von 2 -Methylpropan entsteht tert-Butylbromid (2 -Brom-2 methylpropan). Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 56

Nomenklatur PSE Die Radikalkettenreaktion läuft analog wie Chlorierung. Im Falle des Iod-Radikals ist eine H-Abstraktion (H-Abspaltung) aus dem Alkan energetisch sehr ungünstig. Es kommt nicht zur Bildung des Radikals. Die Radikalkettenreaktion findet nicht statt. Iod ist ein Radikalfänger. Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 57

Halogenalkane PSE Chlorethan dient als Vereisungsmittel. 2 -Brom-2 -chlor-1, 1, 1 -trifluorethan (Halothan) wirkt narkotisch. Fluorierte Kohlenwasserstoffe lösen Sauerstoff => Blutersatz! Chlorierte Kohlenwasserstoffe werden schlecht biologisch abgebaut. Beispiele sind die Lösemittel Methylenchlorid, Trichlormethan (Chloroform), Tetrachlorkohlenstoff (Tetra), Tetrachlorethen (ein Alken - chem. Reinigung), Trichlorfluormethan (FCKW – Fluorchlorkohlenwasserstoff - Ozonloch), Lindan (Insektizid), DDT (hochwirksames Insektizid, wichtig in der Malariabekämpfung - in Deutschland verboten, da es sich in der Umwelt, im Fettgewebe und der Muttermilch anreichert. ) Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 58
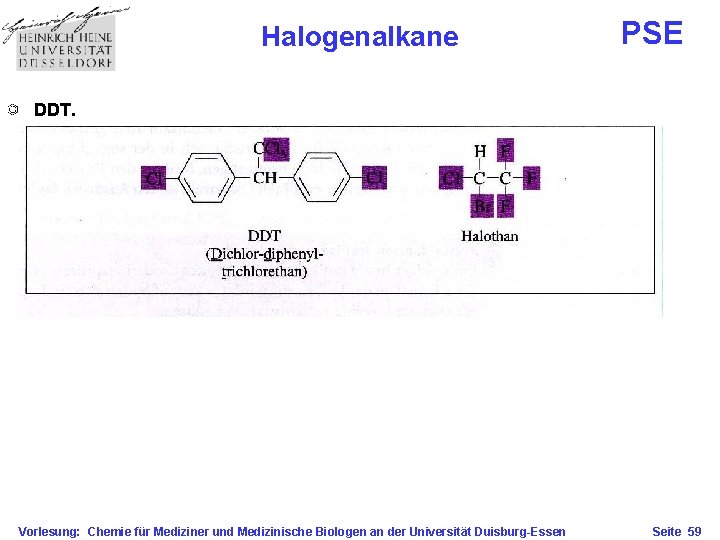
Halogenalkane PSE DDT. Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 59

Halogenalkane (FCKW) PSE Ozonloch FCKW setzen unter UV-Bestrahlung in den oberen atmosphärischen Schichten Cl-Radikale frei. Diese Radikale sind in der Lage den Zerfall von zwei Molekülen Ozon zu drei Molekülen Sauerstoff zu katalysieren. Dies ist die Ursache für das Ozonloch. Das Ozon ist ein Filter für UV-Strahlen. Das Ozonloch ist somit für zu hohe UV-Strahlung an der Erdoberfläche verantwortlich und kann so Hautkrebs hervorrufen. Ozon an der Erdoberfläche schadet den Lungen (Ozon). Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 60

Oxidation/Verbrennung PSE Die Oxidation von Alkanen spielt eine Rolle beim Heizen (Verbrennung von Erdgas und Heizöl), sowie bei der Verbrennung im Motor oder im Kraftwerk. Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 61

Treibhauseffekt PSE Die Verbrennung von Kohlenwasserstoffen führt zur Bildung von Kohlendioxid. Dieses Gas ist maßgeblich am Entstehen des Treibhauseffektes verantwortlich. Vorlesung: Chemie für Mediziner und Medizinische Biologen an der Universität Duisburg-Essen Seite 62
- Slides: 62