Ester Experimentalvortrag von Alexander Achenbach WS 0708 am
Ester Experimentalvortrag von Alexander Achenbach WS 07/08 am 16. 01. 2008 1

Gliederung 1. Einleitung 2. Carbonsäureester 2. 1 2. 2 2. 3 2. 4 2. 5 2. 6 2. 7 3. 4. Vorkommen Struktur und Nomenklatur Physikalische Eigenschaften Darstellung Verseifung CH-acide Ester Verwendung Ester anorganischer Säuren Schulrelevanz 2

1. Einleitung § Stoffgruppe organischer Verbindungen § Entstehung durch Reaktion von Sauerstoffsäuren mit Alkoholen § Es gibt Ester organischer und anorganischer Säuren § Ester sind Derivate dieser Säuren 3

1. Einleitung § Organische Ester sind Carbonsäure-Derivate § Ersatz der Hydroxylgruppe (-OH) durch eine Alkoxygruppe (-OR) § Ester anorganischer Säuren leiten sich analog her 4

2. Carbonsäureester 2. 1 Vorkommen in der Natur: Fette und Öle: Ester höherer aliphatischer, gesättigter oder ungesättigter Monocarbonsäuren Glycerin ist dreiwertige Alkoholkomponente Glycerin = 1, 2, 3 -Propantriol 5
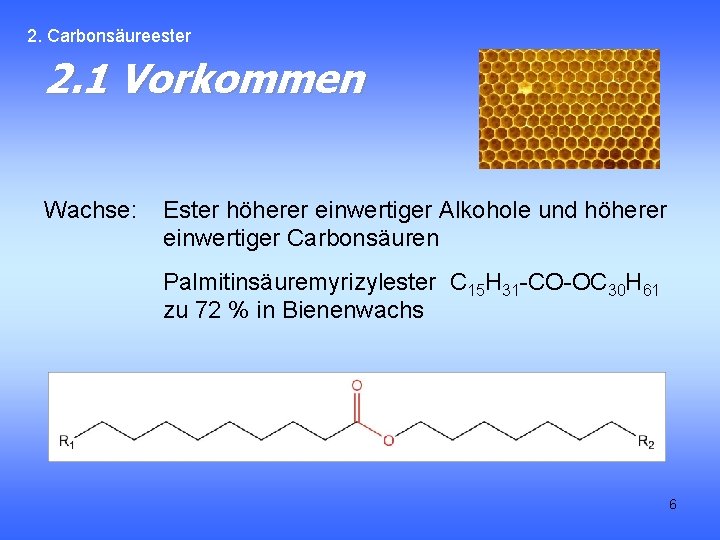
2. Carbonsäureester 2. 1 Vorkommen Wachse: Ester höherer einwertiger Alkohole und höherer einwertiger Carbonsäuren Palmitinsäuremyrizylester C 15 H 31 -CO-OC 30 H 61 zu 72 % in Bienenwachs 6

2. Carbonsäureester 2. 1 Vorkommen Riechstoffe: Ester in vielen ätherischen Ölen enthalten Verantwortlich für zahlreiche Düfte von Früchten und Blüten Meist Ester niederer Alkohole und Carbonsäuren flüchtig Pyrola uniflora (Einblütiges Wintergrün) enthält Salicylsäuremethylester 7

8
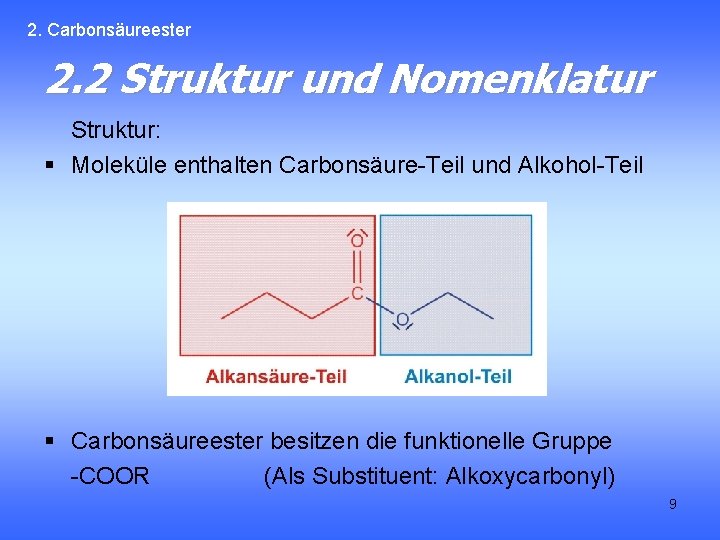
2. Carbonsäureester 2. 2 Struktur und Nomenklatur Struktur: § Moleküle enthalten Carbonsäure-Teil und Alkohol-Teil § Carbonsäureester besitzen die funktionelle Gruppe -COOR (Als Substituent: Alkoxycarbonyl) 9

2. Carbonsäureester 2. 2 Struktur und Nomenklatur Namen der Carbonsäureester hängen von den beteiligten Kohlenstoffgerüsten der eingesetzten Säuren und Alkohole ab: Mehrere Möglichkeiten: § Systematisch (IUPAC) § Alternativ (gebräuchlich) § Trivialnamen 10
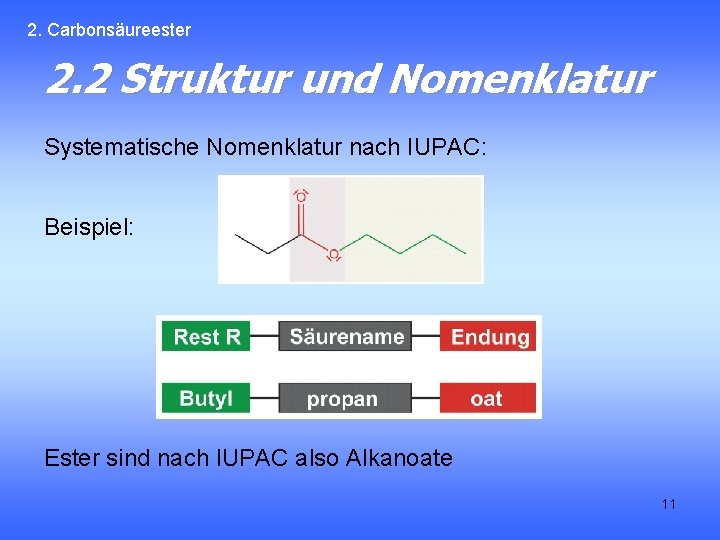
2. Carbonsäureester 2. 2 Struktur und Nomenklatur Systematische Nomenklatur nach IUPAC: Beispiel: Ester sind nach IUPAC also Alkanoate 11
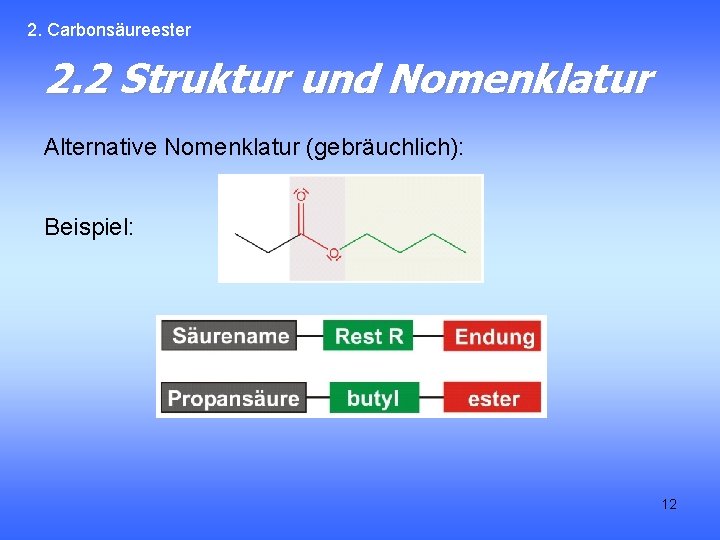
2. Carbonsäureester 2. 2 Struktur und Nomenklatur Alternative Nomenklatur (gebräuchlich): Beispiel: 12
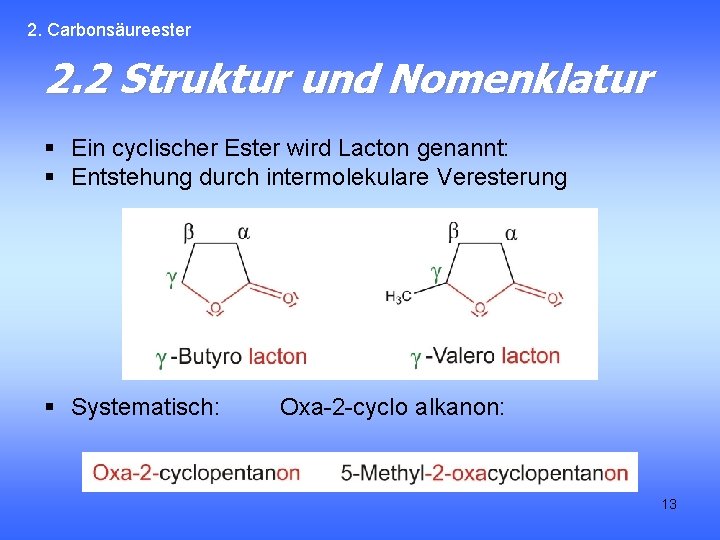
2. Carbonsäureester 2. 2 Struktur und Nomenklatur § Ein cyclischer Ester wird Lacton genannt: § Entstehung durch intermolekulare Veresterung § Systematisch: Oxa-2 -cyclo alkanon: 13

2. Carbonsäureester 2. 3 Physikalische Eigenschaften Niedermolekulare Ester: Höher molekulare Ester: § Flüssig und farblos § Brennbar § Niedrig siedend § Fest / wachsartig Siedepunkte: 14
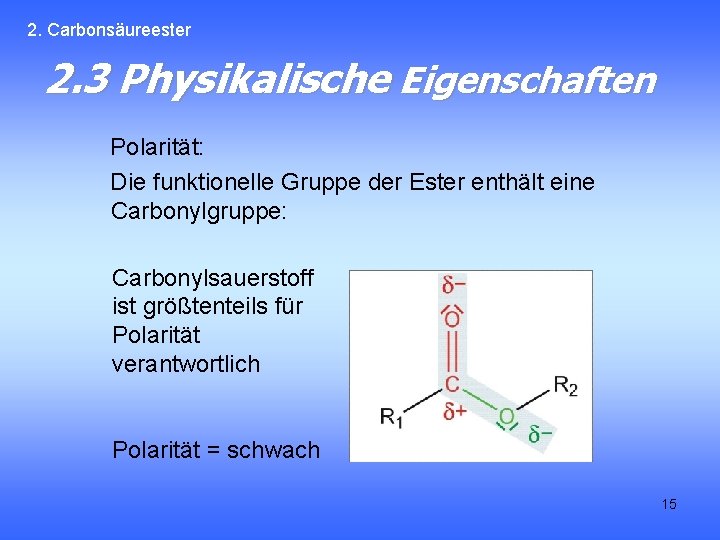
2. Carbonsäureester 2. 3 Physikalische Eigenschaften Polarität: Die funktionelle Gruppe der Ester enthält eine Carbonylgruppe: Carbonylsauerstoff ist größtenteils für Polarität verantwortlich Polarität = schwach 15

16

2. Carbonsäureester D 2 Löslichkeit von Styropor (Polystyrol) löst sich gut in Essigsäureetylester: Prinzip: Gleiche Polarität „Similia similibus solvuntur“ (Gleiches löst sich in Gleichem) 17

18
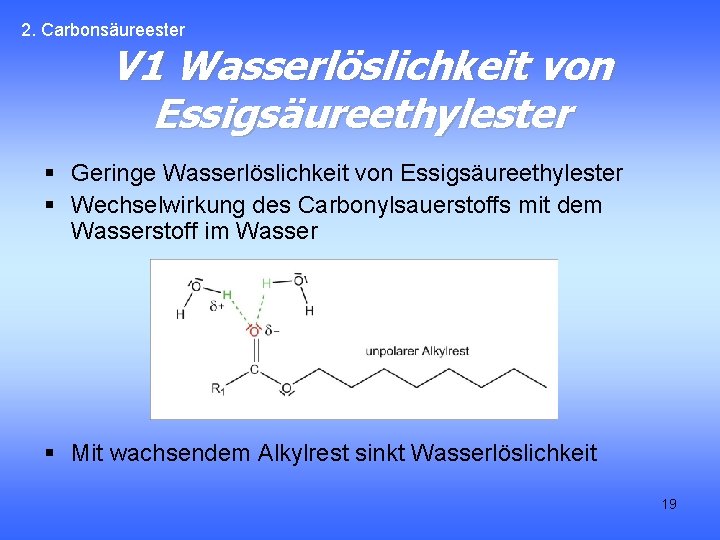
2. Carbonsäureester V 1 Wasserlöslichkeit von Essigsäureethylester § Geringe Wasserlöslichkeit von Essigsäureethylester § Wechselwirkung des Carbonylsauerstoffs mit dem Wasserstoff im Wasser § Mit wachsendem Alkylrest sinkt Wasserlöslichkeit 19
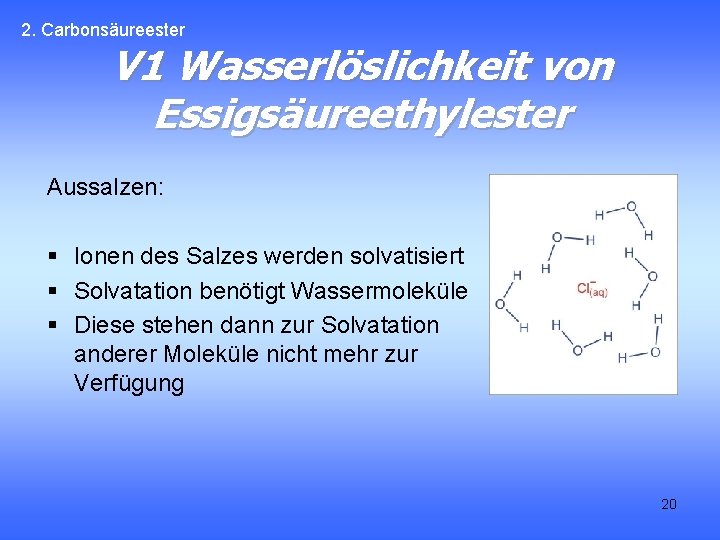
2. Carbonsäureester V 1 Wasserlöslichkeit von Essigsäureethylester Aussalzen: § Ionen des Salzes werden solvatisiert § Solvatation benötigt Wassermoleküle § Diese stehen dann zur Solvatation anderer Moleküle nicht mehr zur Verfügung 20
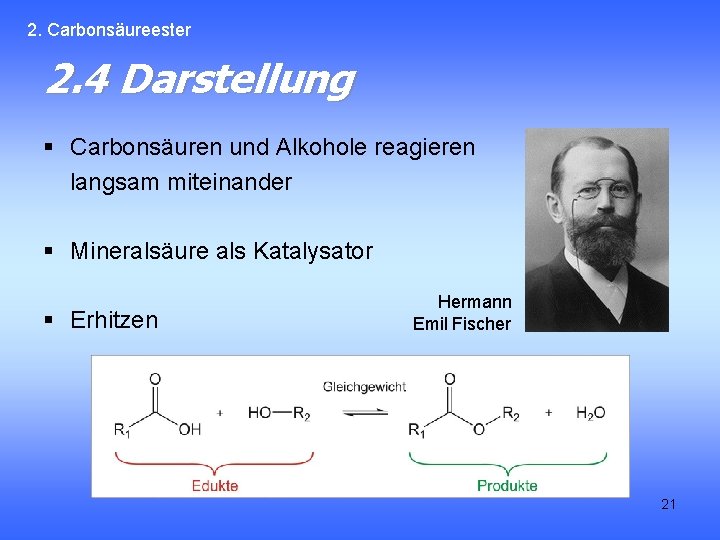
2. Carbonsäureester 2. 4 Darstellung § Carbonsäuren und Alkohole reagieren langsam miteinander § Mineralsäure als Katalysator § Erhitzen Hermann Emil Fischer 21
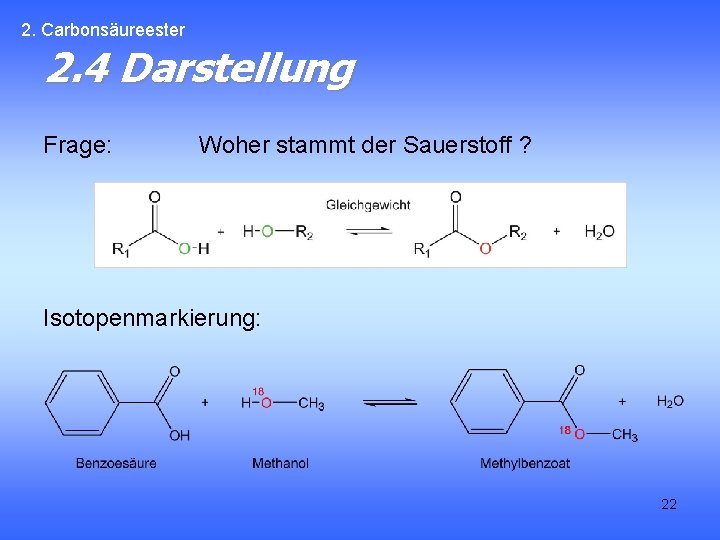
2. Carbonsäureester 2. 4 Darstellung Frage: Woher stammt der Sauerstoff ? Isotopenmarkierung: 22

23

2. Carbonsäureester V 2 Darstellung von Essigsäureethylester 24

2. Carbonsäureester 2. 5 Verseifung § Unter „Verseifung“ versteht man zunächst die basische Hydrolyse eines Esters § Der Begriff „Verseifung“ kommt aus der Nutzung dieses Reaktionstyps zur Herstellung von Seife aus Fett Andere Variante: Erhitzen von Estern mit Überschuss von Wasser in Gegenwart von Mineralsäuren 25

26
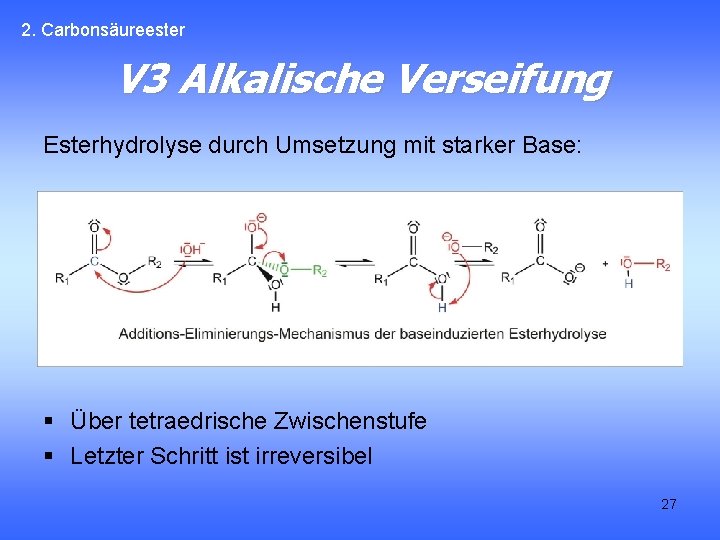
2. Carbonsäureester V 3 Alkalische Verseifung Esterhydrolyse durch Umsetzung mit starker Base: § Über tetraedrische Zwischenstufe § Letzter Schritt ist irreversibel 27

28
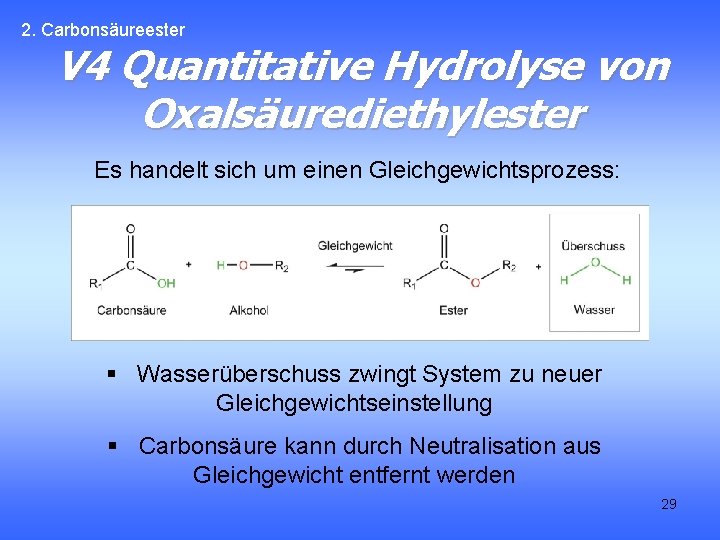
2. Carbonsäureester V 4 Quantitative Hydrolyse von Oxalsäurediethylester Es handelt sich um einen Gleichgewichtsprozess: § Wasserüberschuss zwingt System zu neuer Gleichgewichtseinstellung § Carbonsäure kann durch Neutralisation aus Gleichgewicht entfernt werden 29
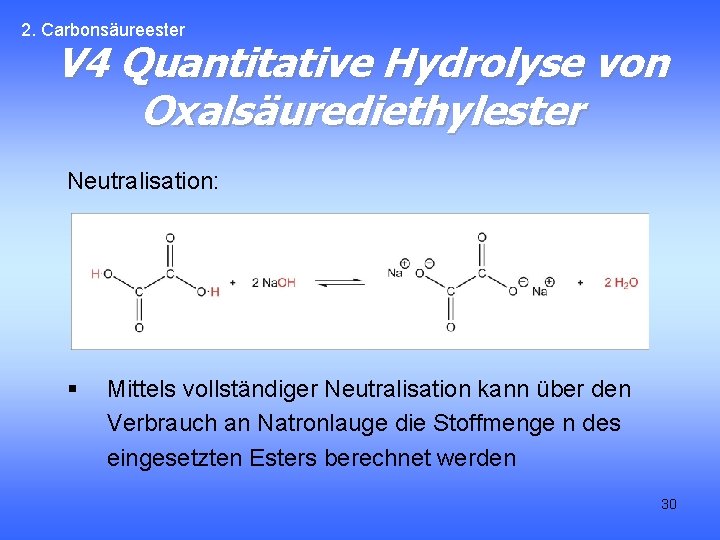
2. Carbonsäureester V 4 Quantitative Hydrolyse von Oxalsäurediethylester Neutralisation: § Mittels vollständiger Neutralisation kann über den Verbrauch an Natronlauge die Stoffmenge n des eingesetzten Esters berechnet werden 30

2. Carbonsäureester 2. 6 CH-acide Ester § Ester verfügen über eine schwache Acidität des a –Wasserstoffatoms § Besonders CH-acide Ester verdanken ihre Eigenschaft der Mesomeriestabilisierung des gebildeten Anions durch elektronenziehende CO-Gruppen in b-Stellung. 31

32

2. Carbonsäureester V 5 Keto-Enol-Tautomerie Definition: Tautomerie „Das Vorhandensein zweier im Gleichgewicht stehender Molekülformen, die sich nur durch die Stellung eines Protons (mit der entsprechenden Verschiebung der Bindungen) unterscheiden, wird als Tautomerie bezeichnet. “ 33
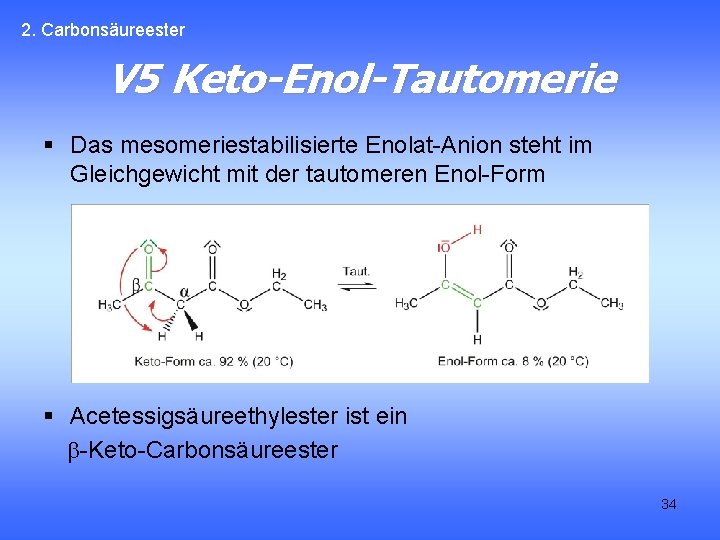
2. Carbonsäureester V 5 Keto-Enol-Tautomerie § Das mesomeriestabilisierte Enolat-Anion steht im Gleichgewicht mit der tautomeren Enol-Form § Acetessigsäureethylester ist ein b-Keto-Carbonsäureester 34
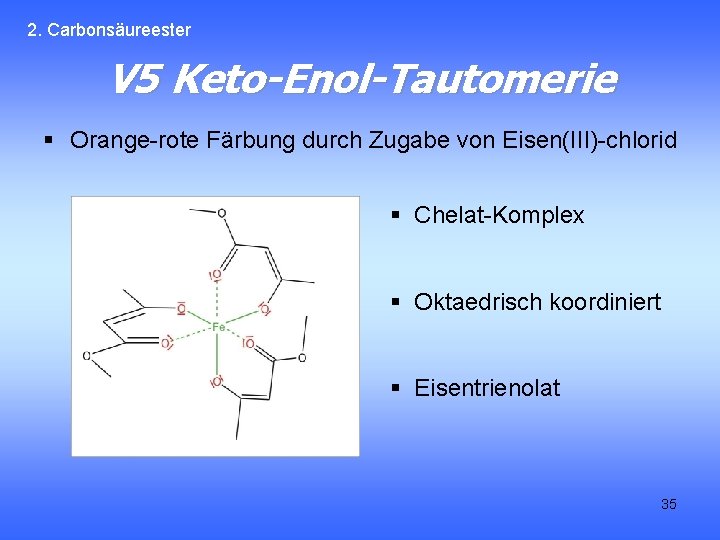
2. Carbonsäureester V 5 Keto-Enol-Tautomerie § Orange-rote Färbung durch Zugabe von Eisen(III)-chlorid § Chelat-Komplex § Oktaedrisch koordiniert § Eisentrienolat 35
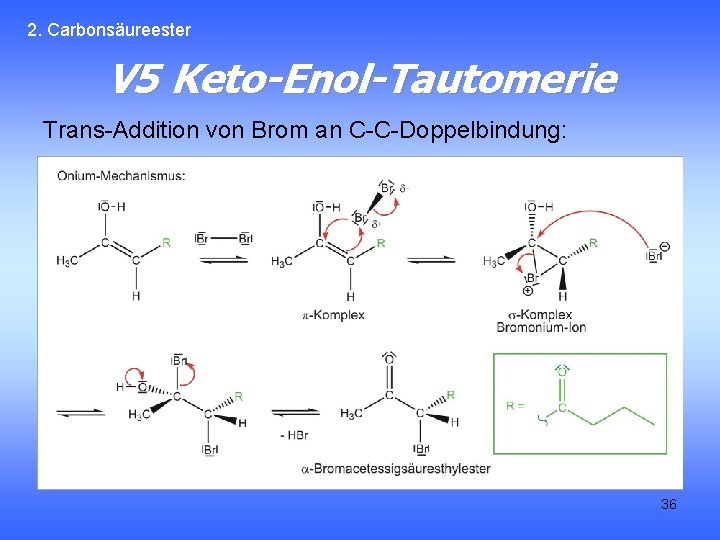
2. Carbonsäureester V 5 Keto-Enol-Tautomerie Trans-Addition von Brom an C-C-Doppelbindung: 36

2. Carbonsäureester 2. 7 Verwendung Aromastoffe: - Nahrungsmittel - Parfüme Lösungsmittel: - Lacke - Klebstoffe Emulgatoren/ - Haushaltsreiniger Konservierungstoffe: - Fischkonserven (PHB-Ester) PHB-Ester = para-Hydroxybenzoesäureester 37

2. Carbonsäureester 2. 7 Verwendung Medizin: § Acetylsalicylsäure § 1899 wurde Aspirin zum Patent angemeldet § Hemmt Prostaglandinsynthese im Körper 38

2. Carbonsäureester 2. 7 Verwendung Kunststoffe: - PET Polyethylenterephtalat (Verpackungen) - Phtalsäureester - Fettsäureester - Citronensäureester (Weichmacher für PVC) 39

40
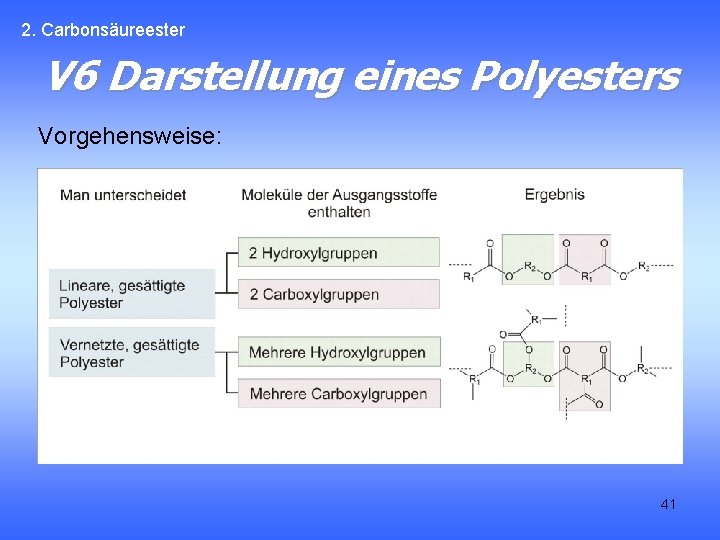
2. Carbonsäureester V 6 Darstellung eines Polyesters Vorgehensweise: 41
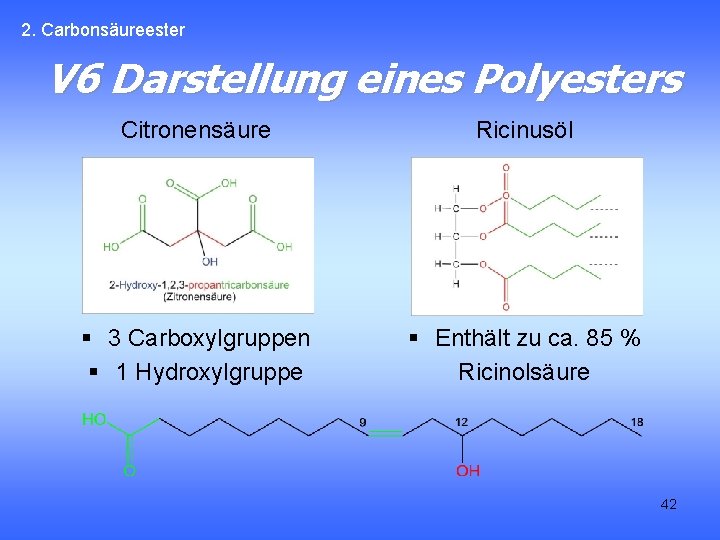
2. Carbonsäureester V 6 Darstellung eines Polyesters Citronensäure Ricinusöl § 3 Carboxylgruppen § 1 Hydroxylgruppe § Enthält zu ca. 85 % Ricinolsäure 42
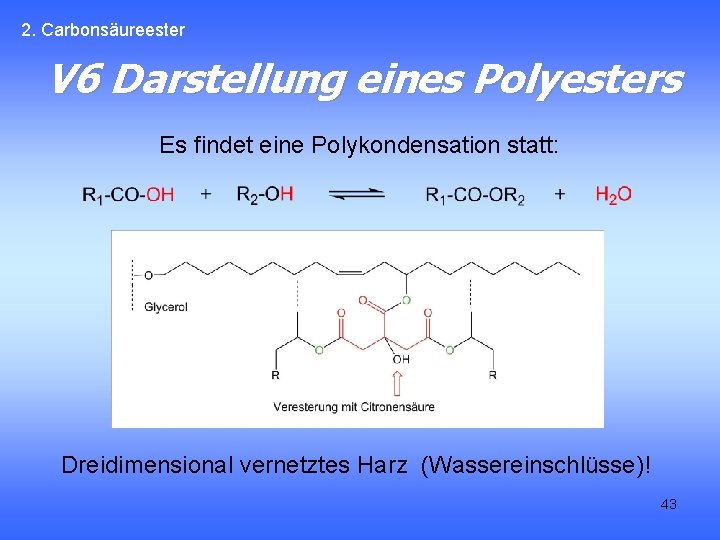
2. Carbonsäureester V 6 Darstellung eines Polyesters Es findet eine Polykondensation statt: Dreidimensional vernetztes Harz (Wassereinschlüsse)! 43

3. Ester anorganischer Säuren Entstehung durch formale oder tatsächliche Kondensationsreaktion zwischen Säure und Alkohol Im Folgenden: Bekannte Beispiele für: § § Phosphorsäureester Schwefelsäureester Salpetersäureester Borsäureester 44
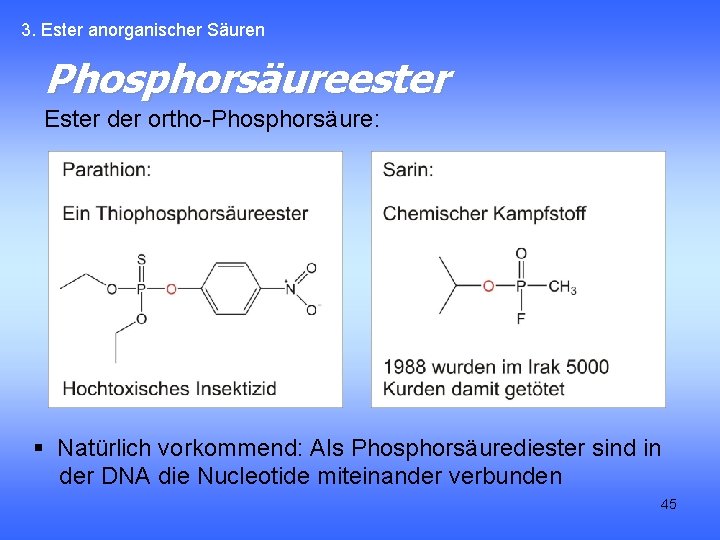
3. Ester anorganischer Säuren Phosphorsäureester Ester der ortho-Phosphorsäure: § Natürlich vorkommend: Als Phosphorsäurediester sind in der DNA die Nucleotide miteinander verbunden 45

3. Ester anorganischer Säuren Schwefelsäureester Ester der Schwefelsäure: § Natürlich vorkommend: Carrageen (E 407) aus Rotalgen (Geliermittel: z. B. in Babynahrung) 46

3. Ester anorganischer Säuren Salpetersäureester Ester der Salpetersäure: Salpetersäureester von Polyalkoholen sind Explosivstoffe Nitroglycerin: (Propan-1, 2, 3 -trioltrinitrat) Darstellung durch Veresterung der drei OH-Gruppen des Glycerols mit Nitriersäure 47

48
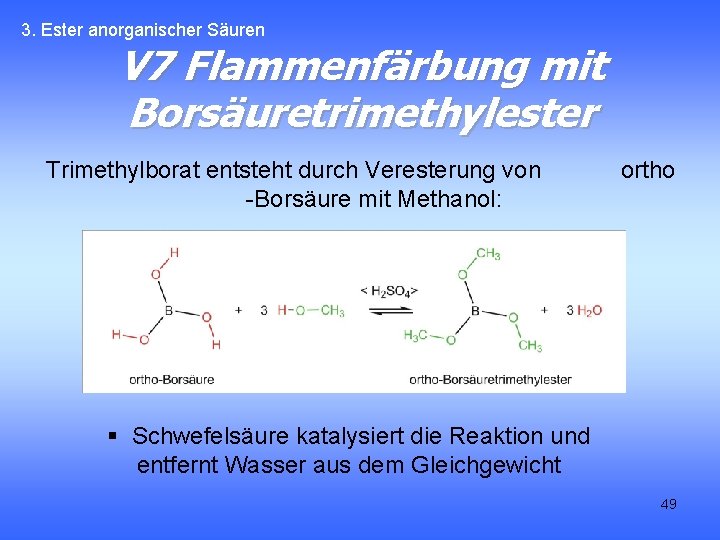
3. Ester anorganischer Säuren V 7 Flammenfärbung mit Borsäuretrimethylester Trimethylborat entsteht durch Veresterung von -Borsäure mit Methanol: ortho § Schwefelsäure katalysiert die Reaktion und entfernt Wasser aus dem Gleichgewicht 49
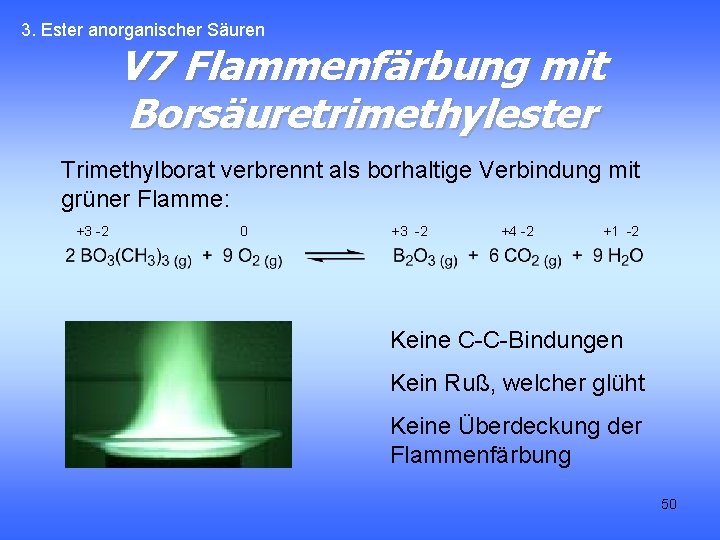
3. Ester anorganischer Säuren V 7 Flammenfärbung mit Borsäuretrimethylester Trimethylborat verbrennt als borhaltige Verbindung mit grüner Flamme: +3 -2 0 +3 -2 +4 -2 +1 -2 Keine C-C-Bindungen Kein Ruß, welcher glüht Keine Überdeckung der Flammenfärbung 50

5. Schulrelevanz 4. Schulrelevanz Gymnasialer Bildungsgang (G 8) Hessen: 11 G. 1: Alkansäuren und ihre Derivate 11 G. 2: Naturstoffe: Fette (Eigenschaften und Reaktionen) Synthese von Makromolekülen (Polykondensation) 12 G. 1: Umkehrbare Reaktionen Chemisches Gleichgewicht (MWG) Prinzip vom Zwang: Beeinflussung der Lage des Gleichgewichts 51

Ende Vielen Dank für Ihre Aufmerksamkeit 52
- Slides: 52