Hoofdstuk II organische structuren HOOFDSTUK II Organische structuren








- Slides: 35

Hoofdstuk II: organische structuren HOOFDSTUK II: Organische structuren Mc Murry: pagina 68 -102

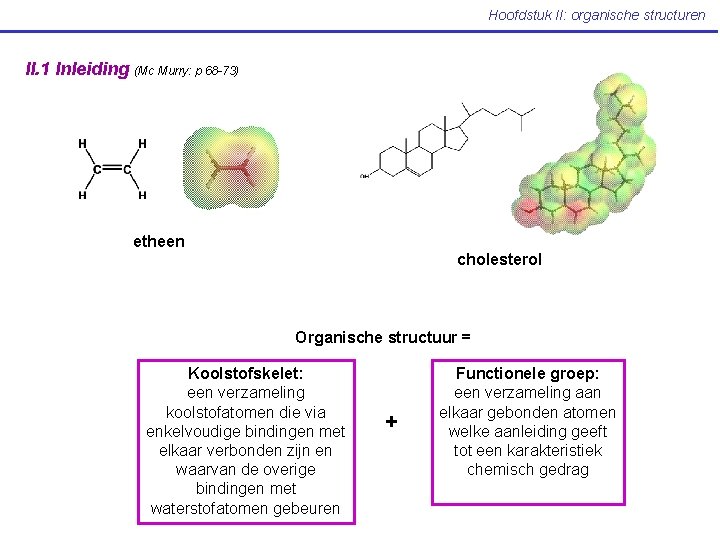
Hoofdstuk II: organische structuren II. 1 Inleiding (Mc Murry: p 68 -73) etheen cholesterol Organische structuur = Koolstofskelet: een verzameling koolstofatomen die via enkelvoudige bindingen met elkaar verbonden zijn en waarvan de overige bindingen met waterstofatomen gebeuren + Functionele groep: een verzameling aan elkaar gebonden atomen welke aanleiding geeft tot een karakteristiek chemisch gedrag

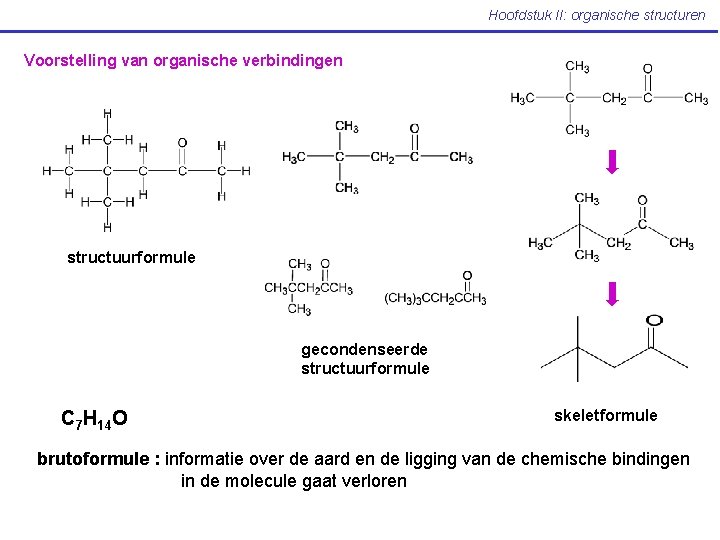
Hoofdstuk II: organische structuren Voorstelling van organische verbindingen structuurformule gecondenseerde structuurformule C 7 H 14 O skeletformule brutoformule : informatie over de aard en de ligging van de chemische bindingen in de molecule gaat verloren

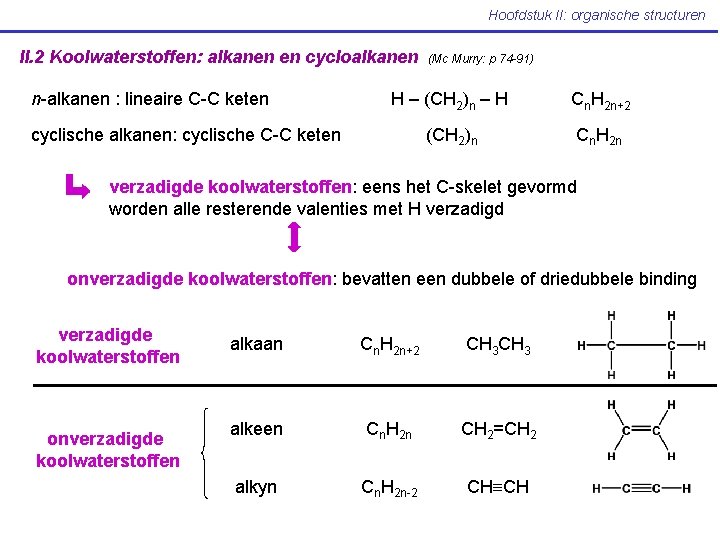
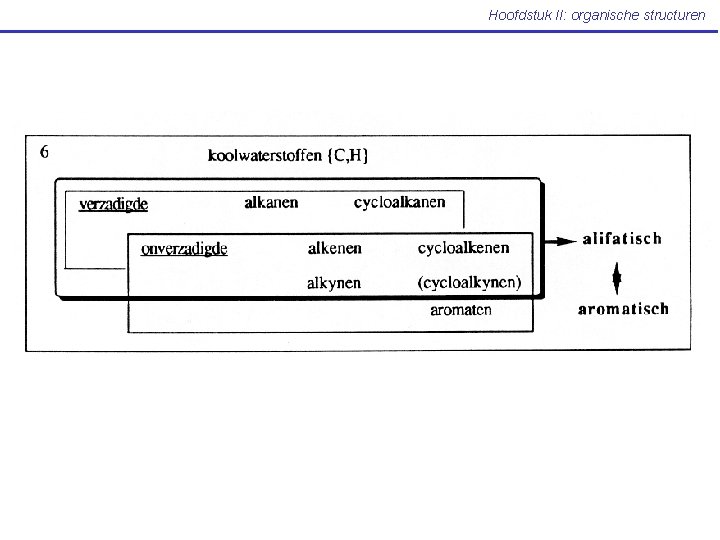
Hoofdstuk II: organische structuren II. 2 Koolwaterstoffen: alkanen en cycloalkanen n-alkanen : lineaire C-C keten (Mc Murry: p 74 -91) H – (CH 2)n – H Cn. H 2 n+2 (CH 2)n Cn. H 2 n cyclische alkanen: cyclische C-C keten verzadigde koolwaterstoffen: eens het C-skelet gevormd worden alle resterende valenties met H verzadigd onverzadigde koolwaterstoffen: bevatten een dubbele of driedubbele binding verzadigde koolwaterstoffen onverzadigde koolwaterstoffen alkaan Cn. H 2 n+2 CH 3 alkeen Cn. H 2 n CH 2=CH 2 alkyn Cn. H 2 n-2 CH CH

Hoofdstuk II: organische structuren Tabel: Namen van lineaire alkanen

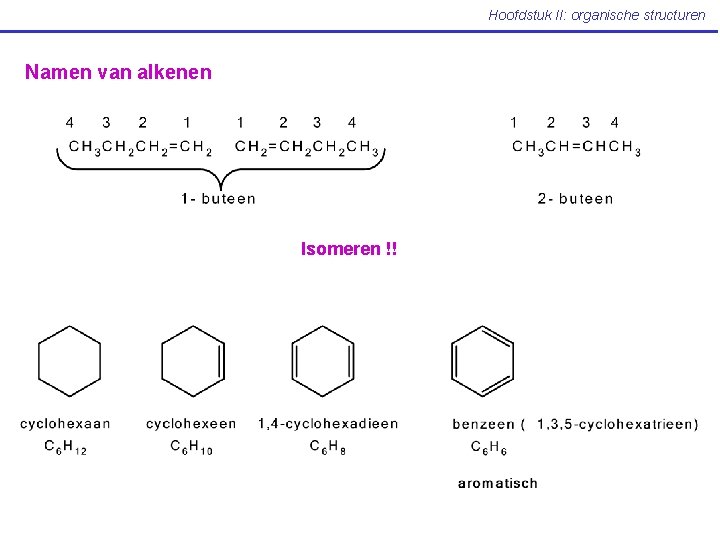
Hoofdstuk II: organische structuren Namen van alkenen Isomeren !!

Hoofdstuk II: organische structuren

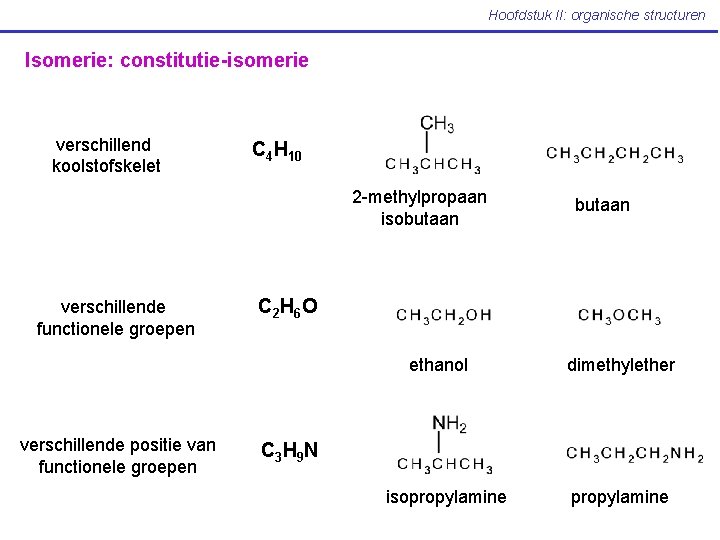
Hoofdstuk II: organische structuren Isomerie: constitutie-isomerie verschillend koolstofskelet C 4 H 10 2 -methylpropaan isobutaan verschillende functionele groepen C 2 H 6 O ethanol verschillende positie van functionele groepen butaan dimethylether C 3 H 9 N isopropylamine

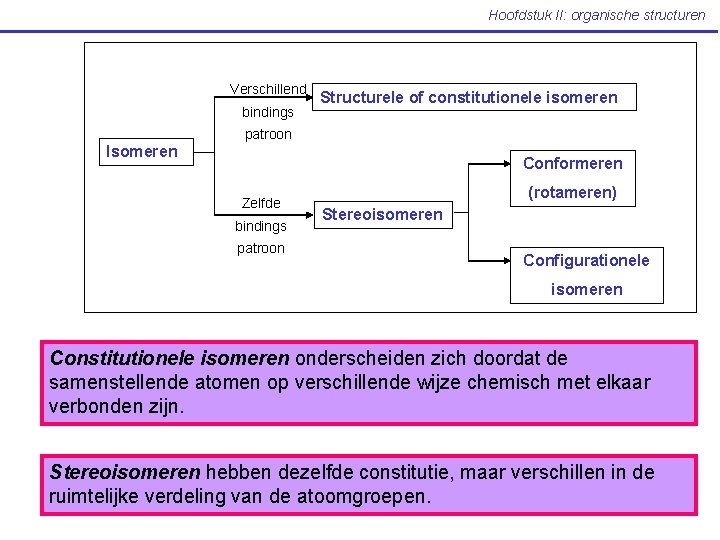
Hoofdstuk II: organische structuren Verschillend bindings Structurele of constitutionele isomeren patroon Isomeren Conformeren Zelfde bindings patroon (rotameren) Stereoisomeren Configurationele isomeren Constitutionele isomeren onderscheiden zich doordat de samenstellende atomen op verschillende wijze chemisch met elkaar verbonden zijn. Stereoisomeren hebben dezelfde constitutie, maar verschillen in de ruimtelijke verdeling van de atoomgroepen.

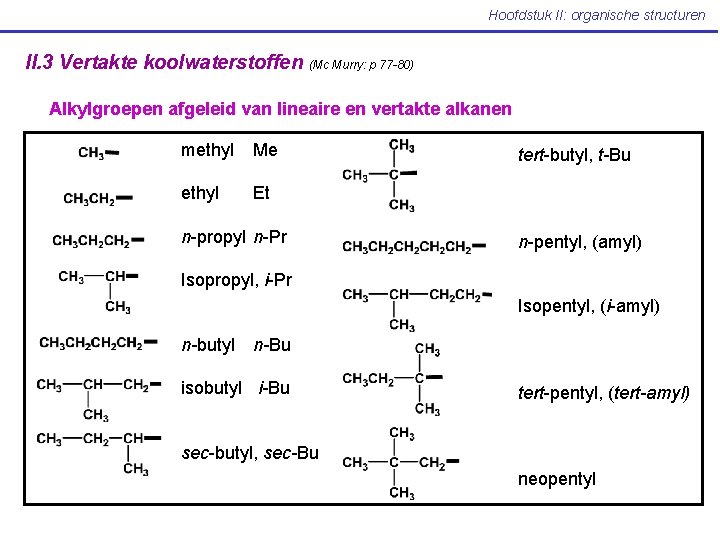
Hoofdstuk II: organische structuren II. 3 Vertakte koolwaterstoffen (Mc Murry: p 77 -80) Alkylgroepen afgeleid van lineaire en vertakte alkanen methyl Me ethyl Et n-propyl n-Pr tert-butyl, t-Bu n-pentyl, (amyl) Isopropyl, i-Pr Isopentyl, (i-amyl) n-butyl n-Bu isobutyl i-Bu tert-pentyl, (tert-amyl) sec-butyl, sec-Bu neopentyl

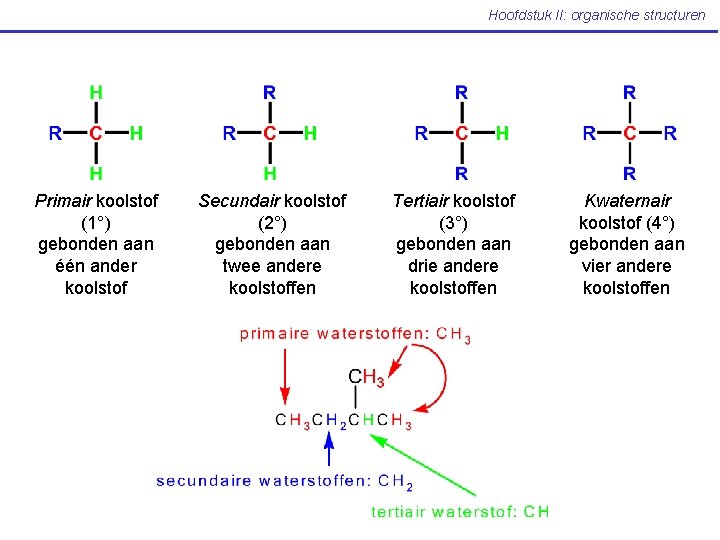
Hoofdstuk II: organische structuren Primair koolstof (1°) gebonden aan één ander koolstof Secundair koolstof (2°) gebonden aan twee andere koolstoffen Tertiair koolstof (3°) gebonden aan drie andere koolstoffen Kwaternair koolstof (4°) gebonden aan vier andere koolstoffen

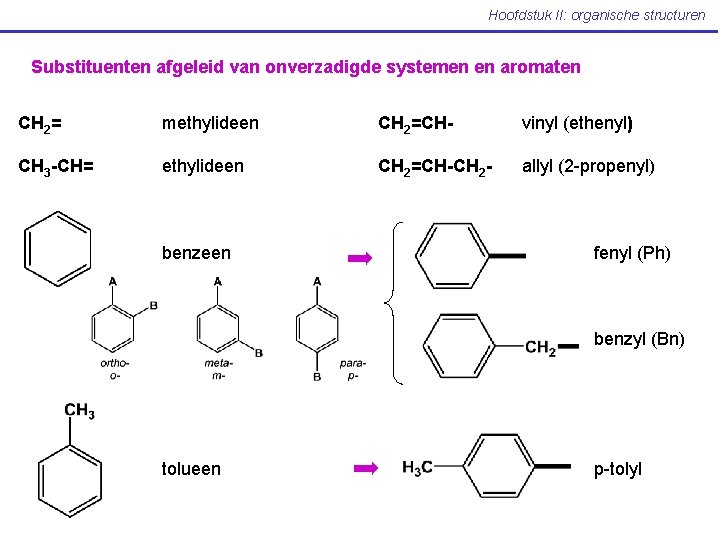
Hoofdstuk II: organische structuren Substituenten afgeleid van onverzadigde systemen en aromaten CH 2= methylideen CH 2=CH- vinyl (ethenyl) CH 3 -CH= ethylideen CH 2=CH-CH 2 - allyl (2 -propenyl) benzeen fenyl (Ph) benzyl (Bn) tolueen p-tolyl

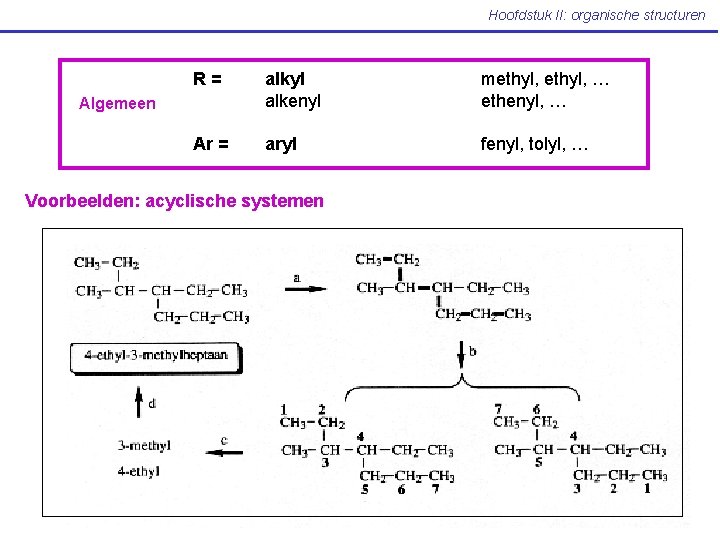
Hoofdstuk II: organische structuren R= alkyl alkenyl methyl, … ethenyl, … Ar = aryl fenyl, tolyl, … Algemeen Voorbeelden: acyclische systemen

Hoofdstuk II: organische structuren Voorbeelden: acyclische systemen 2, 3 -dimethyl-6 -(2 -methylpropyl)decaan 6 -ethyl-3, 3 -dimethyloctaan 3 -methylhexaan Niet : 2 -ethylpentaan of 4 -methylhexaan

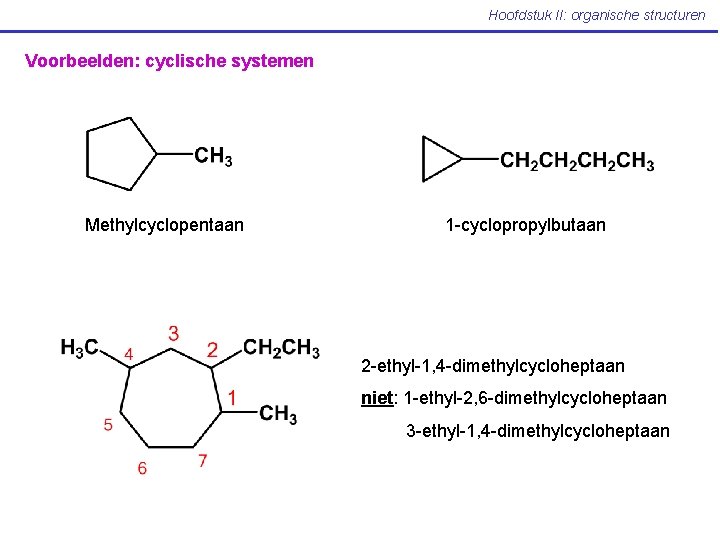
Hoofdstuk II: organische structuren Voorbeelden: cyclische systemen Methylcyclopentaan 1 -cyclopropylbutaan 2 -ethyl-1, 4 -dimethylcycloheptaan niet: 1 -ethyl-2, 6 -dimethylcycloheptaan 3 -ethyl-1, 4 -dimethylcycloheptaan

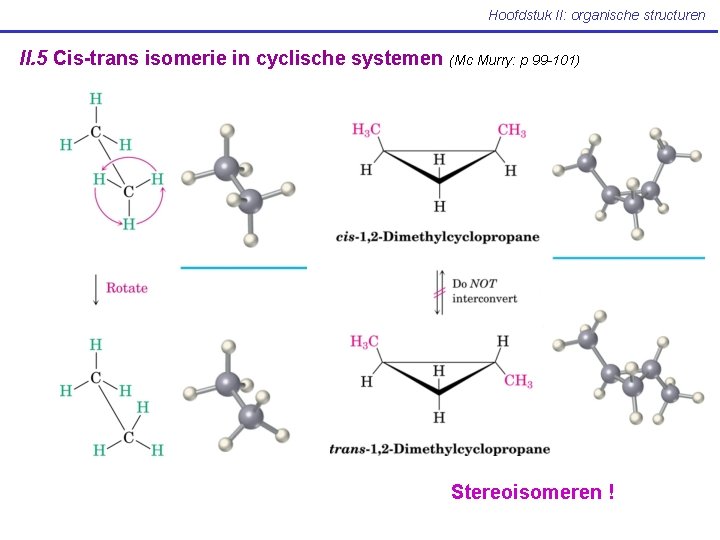
Hoofdstuk II: organische structuren II. 5 Cis-trans isomerie in cyclische systemen (Mc Murry: p 99 -101) Stereoisomeren !

Hoofdstuk II: organische structuren II. 6 Eigenschappen van koolwaterstoffen (Mc Murry: p 86 -88) • Alkanen of paraffinen (parum affinis = weinig affiniteit) lager kokende als oplosmiddelen voor niet-polaire verbindingen: n-pentaan, isoöctaan • belangrijkste bron = aardolie en aardgas (methaan) “biogas” of moerasgas • petroleum: complex mengsel van koolwaterstoffen gescheiden via gefractioneerde destillatie 30 -200°C: • benzine, C 5 – C 11 (motorbrandstof) 175 -300°C: kerosine, C 11 – C 14 (vliegtuigbrandstof) 275 -400°C: stookolie, C 14 – C 25 (verwarming) destillatie onder verminderde druk: smeerolie en was (kaarsen) residu : (wegbedekking) asfalt octaangetal: maat voor antiklop eigenschappen van benzine (klopvastheid) isoöctaan, (2, 2, 4 -trimethylpentaan) Octaangetal = 100 n-heptaan Octaangetal : 0

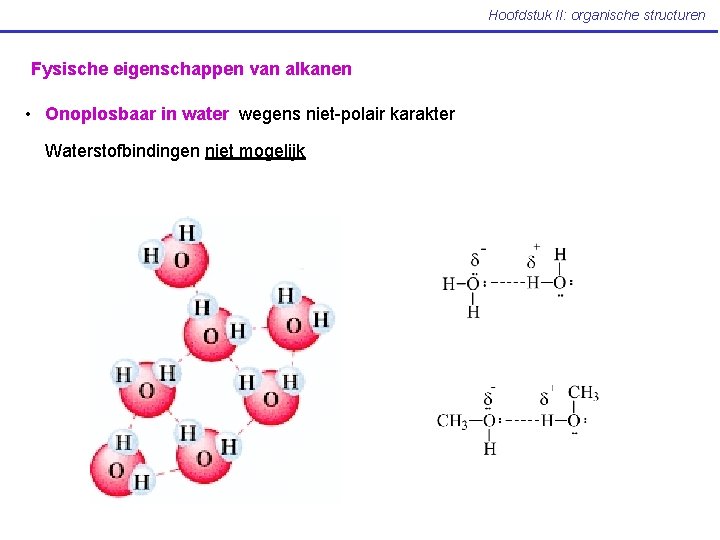
Hoofdstuk II: organische structuren Fysische eigenschappen van alkanen • Onoplosbaar in water wegens niet-polair karakter Waterstofbindingen niet mogelijk

Hoofdstuk II: organische structuren • Alkanen hebben lager kookpunt voor een bepaald moleculair gewicht vergeleken met meeste andere organische verbindingen Reden : Tussen niet-polaire moleculen bestaan enkel van der Waalskrachten (zwakke krachten) aantrekking tussen plaatsen van hoge en lage elektronendensiteit die ontstaan door tijdelijke polarisatie

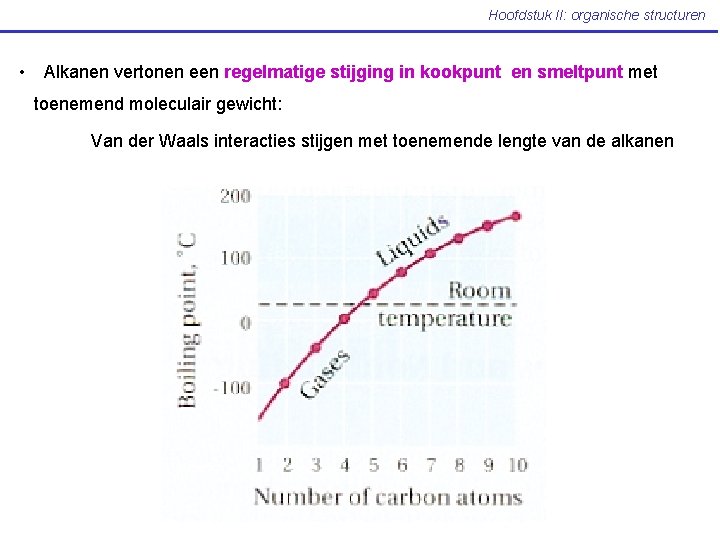
Hoofdstuk II: organische structuren • Alkanen vertonen een regelmatige stijging in kookpunt en smeltpunt met toenemend moleculair gewicht: Van der Waals interacties stijgen met toenemende lengte van de alkanen

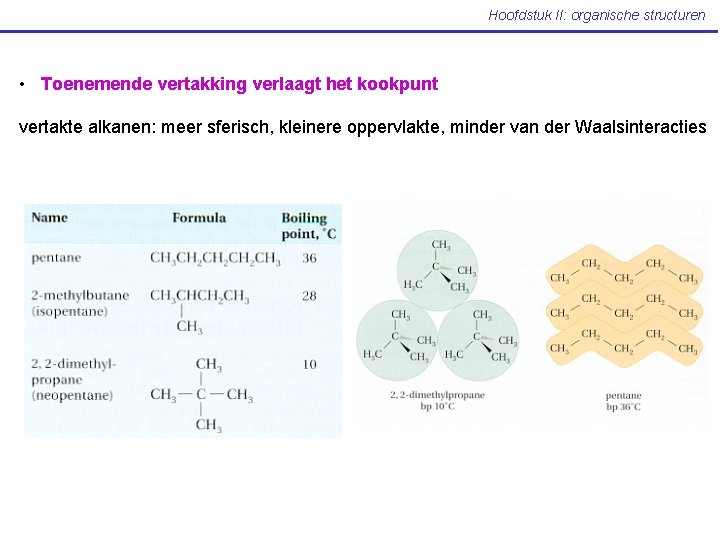
Hoofdstuk II: organische structuren • Toenemende vertakking verlaagt het kookpunt vertakte alkanen: meer sferisch, kleinere oppervlakte, minder van der Waalsinteracties

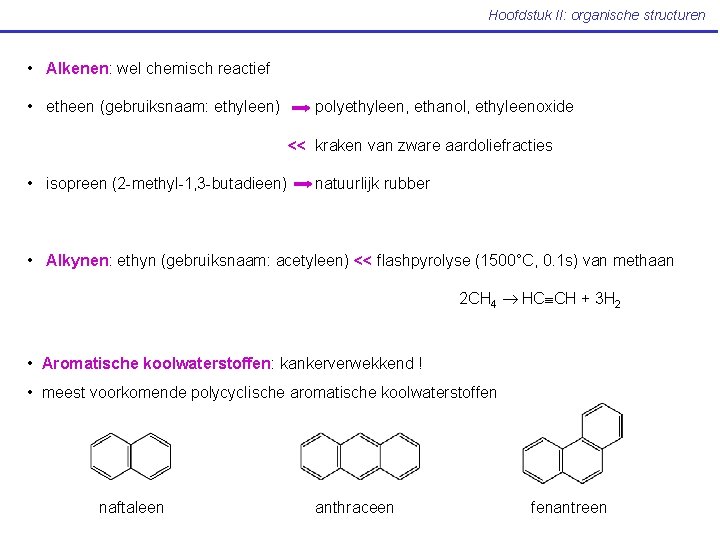
Hoofdstuk II: organische structuren • Alkenen: wel chemisch reactief • etheen (gebruiksnaam: ethyleen) polyethyleen, ethanol, ethyleenoxide << kraken van zware aardoliefracties • isopreen (2 -methyl-1, 3 -butadieen) natuurlijk rubber • Alkynen: ethyn (gebruiksnaam: acetyleen) << flashpyrolyse (1500°C, 0. 1 s) van methaan 2 CH 4 HC CH + 3 H 2 • Aromatische koolwaterstoffen: kankerverwekkend ! • meest voorkomende polycyclische aromatische koolwaterstoffen naftaleen anthraceen fenantreen

Hoofdstuk II: organische structuren II. 7 Functionele groepen

Hoofdstuk II: organische structuren

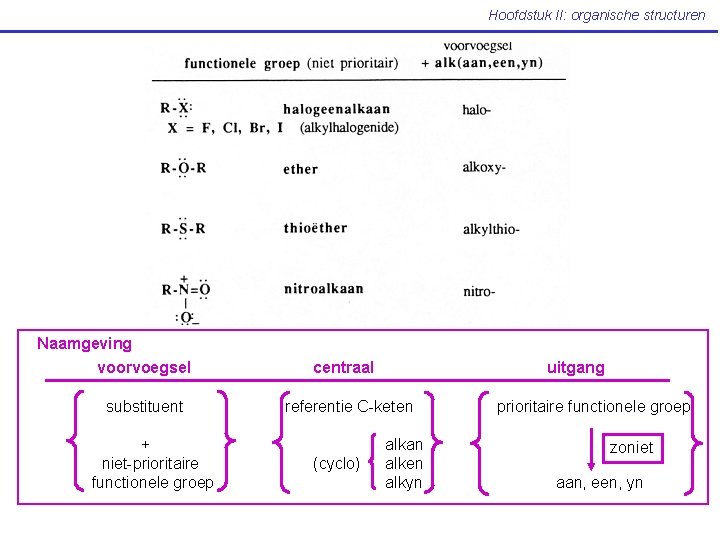
Hoofdstuk II: organische structuren Naamgeving voorvoegsel substituent + niet-prioritaire functionele groep centraal uitgang referentie C-keten (cyclo) alkan alken alkyn prioritaire functionele groep zoniet aan, een, yn

Hoofdstuk II: organische structuren II. 8 Eigenschappen van organische verbindingen • Halogeenalkanen • polychloormethanen: CCl 4, CHCl 3: toxisch, kankerverwekkend CH 2 Cl 2 (cfr. labo: oplosmiddel) • pesticiden: insecticiden, herbiciden, fungiciden DDT (1, 1, 1 -trichloor-2, 2 -bis(p-chloorfenyl)ethaan) • plaatselijke verdoving: chloorethaan (door verdamping) • anestheticum: halothaan CF 3 CHCl. Br • koelvloeistoffen en drijfgas: CFCl 3, CF 2 Cl 2, CF 3 Cl, …(freonen) ozonlaag !!! blindheid • Alcoholen • methanol (houtalcohol): CO + 2 H 2 CH 3 OH • ethanol: fermentatie van suikers (gist) • 1, 2 -ethaandiol (gebruiksnaam: ethyleenglycol) • 1, 2, 3 -propaantriol (gebruiksnaam: glycerol) • aromatische alcoholen = fenolen

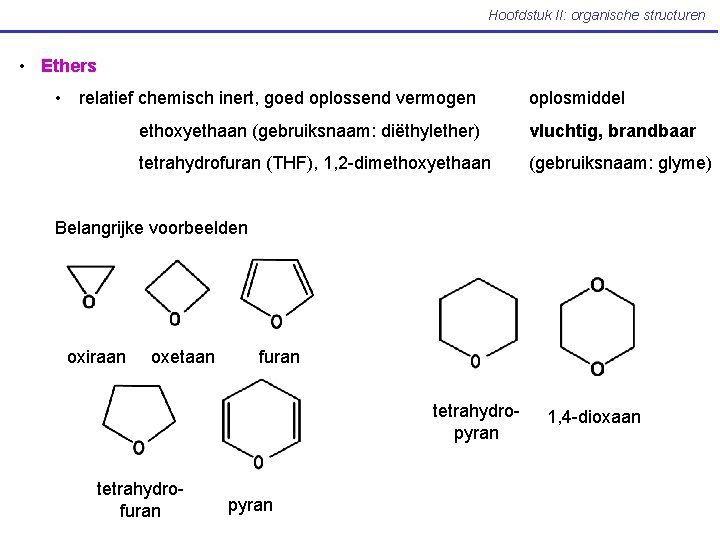
Hoofdstuk II: organische structuren • Ethers • relatief chemisch inert, goed oplossend vermogen oplosmiddel ethoxyethaan (gebruiksnaam: diëthylether) vluchtig, brandbaar tetrahydrofuran (THF), 1, 2 -dimethoxyethaan (gebruiksnaam: glyme) Belangrijke voorbeelden oxiraan oxetaan furan tetrahydropyran tetrahydrofuran pyran 1, 4 -dioxaan

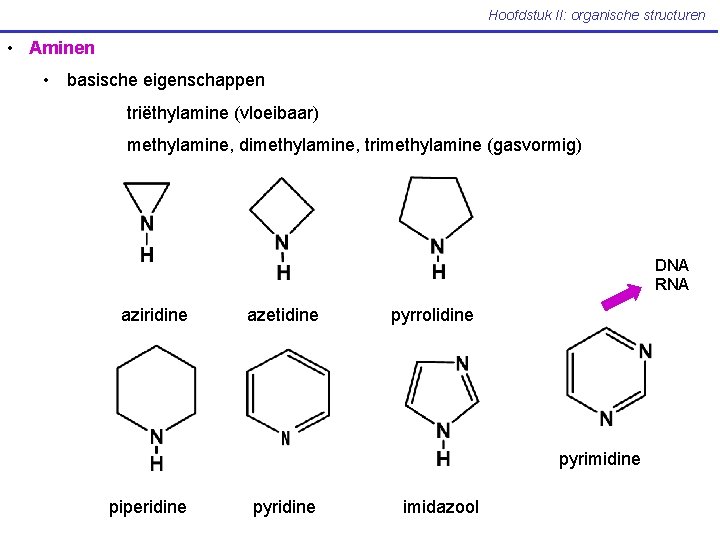
Hoofdstuk II: organische structuren • Aminen • basische eigenschappen triëthylamine (vloeibaar) methylamine, dimethylamine, trimethylamine (gasvormig) DNA RNA aziridine azetidine pyrrolidine pyrimidine piperidine pyridine imidazool

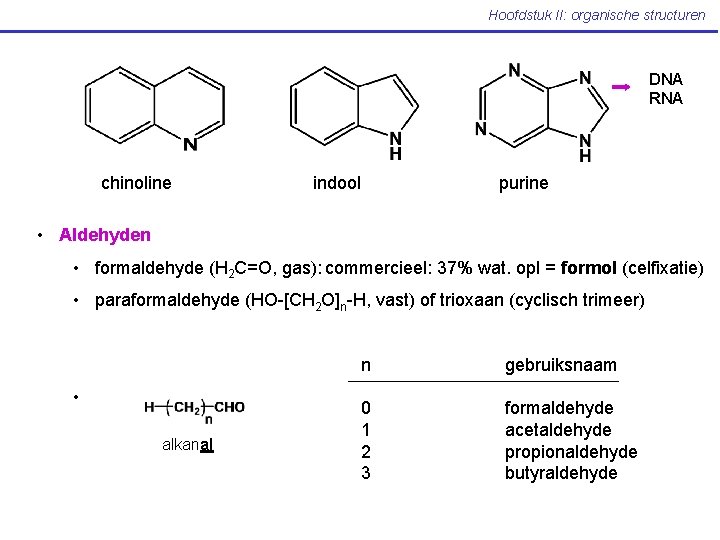
Hoofdstuk II: organische structuren DNA RNA chinoline indool purine • Aldehyden • formaldehyde (H 2 C=O, gas): commercieel: 37% wat. opl = formol (celfixatie) • paraformaldehyde (HO-[CH 2 O]n-H, vast) of trioxaan (cyclisch trimeer) • alkanal n gebruiksnaam 0 1 2 3 formaldehyde acetaldehyde propionaldehyde butyraldehyde

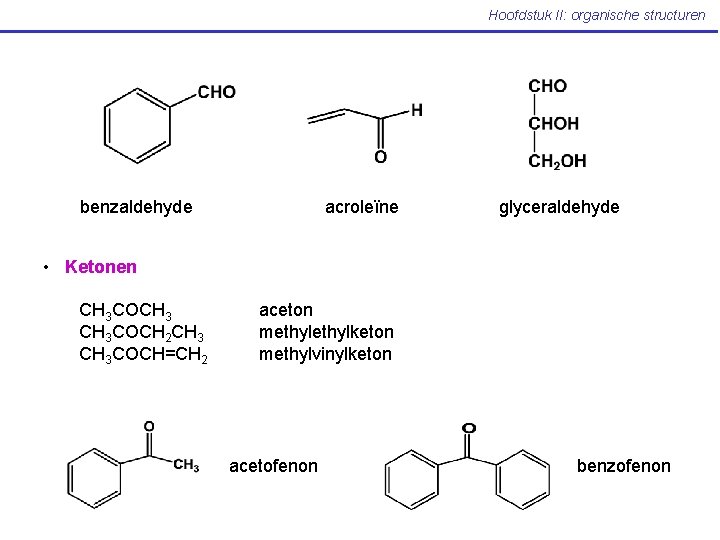
Hoofdstuk II: organische structuren benzaldehyde acroleïne glyceraldehyde • Ketonen CH 3 COCH 3 COCH 2 CH 3 COCH=CH 2 aceton methylketon methylvinylketon acetofenon benzofenon

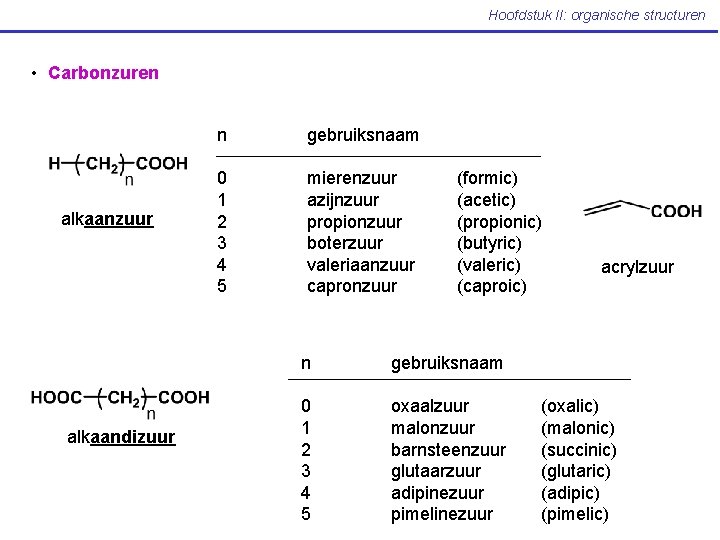
Hoofdstuk II: organische structuren • Carbonzuren alkaanzuur alkaandizuur n gebruiksnaam 0 1 2 3 4 5 mierenzuur azijnzuur propionzuur boterzuur valeriaanzuur capronzuur (formic) (acetic) (propionic) (butyric) (valeric) (caproic) n gebruiksnaam 0 1 2 3 4 5 oxaalzuur malonzuur barnsteenzuur glutaarzuur adipinezuur pimelinezuur acrylzuur (oxalic) (malonic) (succinic) (glutaric) (adipic) (pimelic)

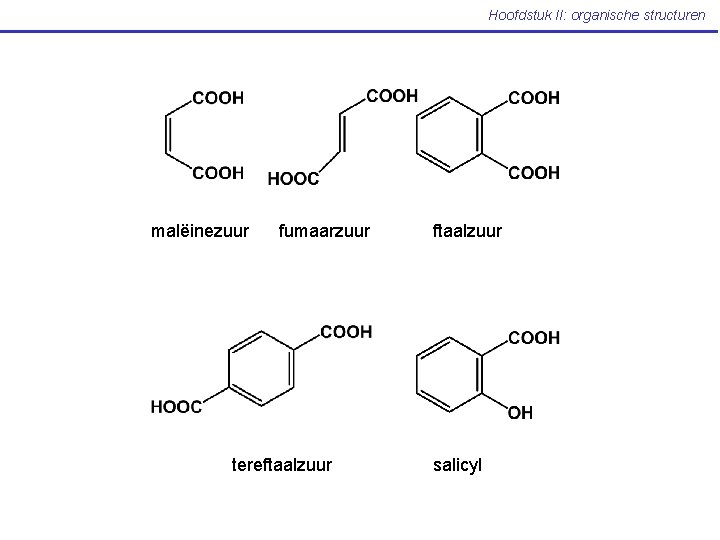
Hoofdstuk II: organische structuren malëinezuur fumaarzuur tereftaalzuur salicyl

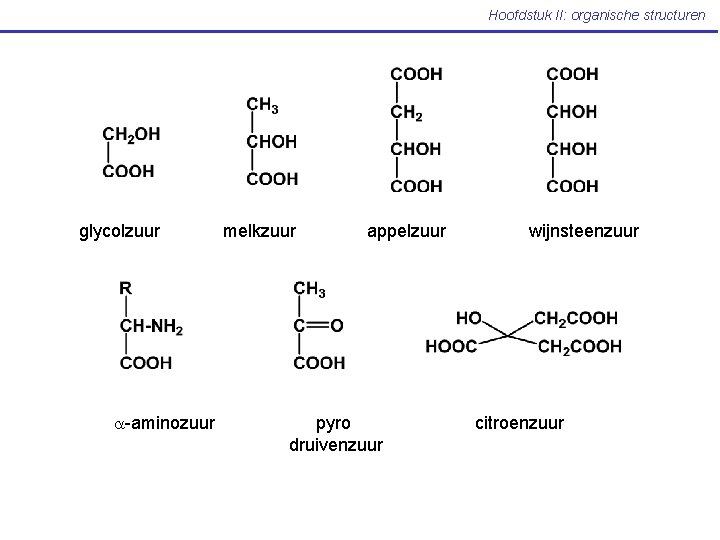
Hoofdstuk II: organische structuren glycolzuur a-aminozuur melkzuur appelzuur pyro druivenzuur wijnsteenzuur citroenzuur

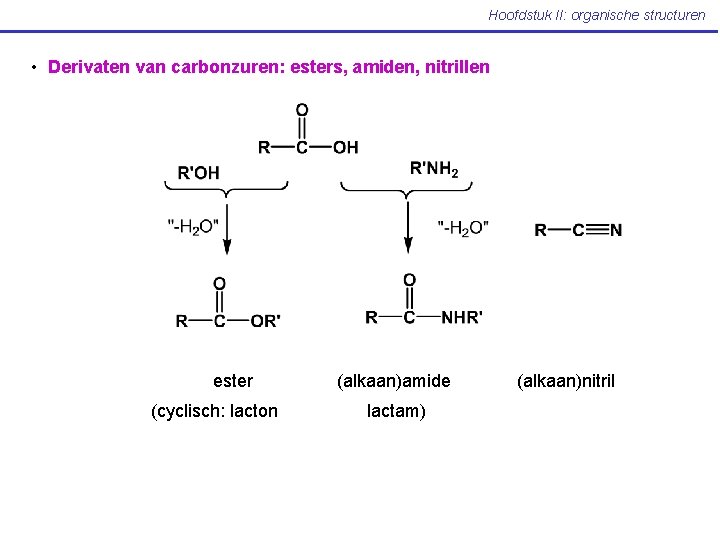
Hoofdstuk II: organische structuren • Derivaten van carbonzuren: esters, amiden, nitrillen ester (cyclisch: lacton (alkaan)amide lactam) (alkaan)nitril

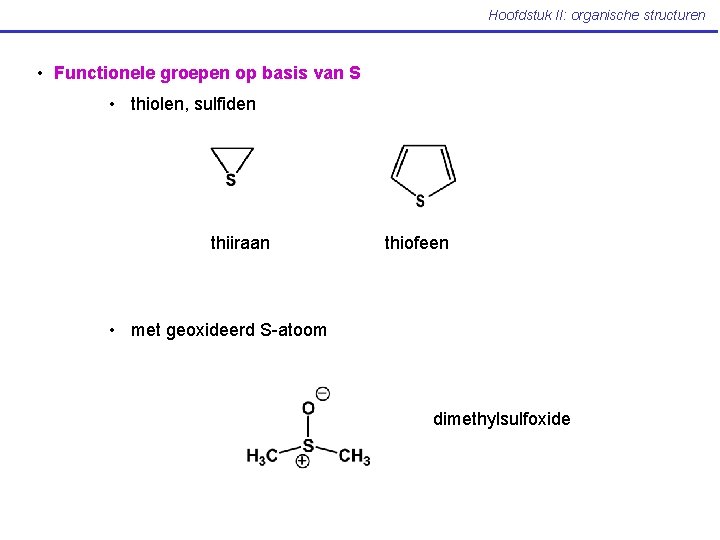
Hoofdstuk II: organische structuren • Functionele groepen op basis van S • thiolen, sulfiden thiiraan thiofeen • met geoxideerd S-atoom dimethylsulfoxide