Westflische WilhelmsUniversitt Fehlvorstellungen in der Chemie Diagnose und







































- Slides: 44

Westfälische Wilhelms-Universität Fehlvorstellungen in der Chemie Diagnose und Korrektur Sommersemester 2006 Prof. Dr. H. -D. Barke und T. Dörfler Referat zum Thema: Säure und Basen Carsten Knoop & Christoph Wacker

Gliederung 1. Einleitung 2. Säure/Base Begriff 3. Reine Säuren und Säure Lösungen 4. ph-Wert 5. Neutralisation 6. Starke und schwache Säuren 7. Zusammenfassung

Einleitung - Säure-Base Reaktion eines der Hauptthemen im Chemieunterricht - Fehlvorstellungen der Schüler aufzeigen - Vorschläge zur Korrektur machen bzw. darstellen

2. Säure/Base Begriff Was versteht man unter einer Säure bzw. unter einer Base? Brönstedsäure: Protonendonator Brönstedbase: Protonenakzeptor Lewissäure: Elektronenakzeptor Lewisbase: Elektronendonator

Vorstellungen der Schüler zum Säure/Base Begriff

Fehlvorstellungen der Schüler - Argumentation mit p. H-Wert - Säuren sind ätzend, gefährlich, gelb, rot oder sauer - Säuren wird eine aggressive Wirkung zugeschrieben - Säuren zerfressen „Dinge“ - beim Arrhenius Konzept (Säuren enthalten H+-Ionen) - beim Brönsted-Konzept (Säuren geben Protonen ab) - Basen werden oftmals vernachlässigt

Fazit: Schüler können mit der Säure-Base Theorie oftmals nicht viel anfangen.

Unterrichtsvorschläge zum Säure-Base Begriff - Reaktion von Säuren und Laugen als Substanz und ihre aggressive Wirkung Reaktion von Zucker mit konz. H 2 SO 4 Zucker + konz. Schwefelsäure schwarzer Kohlenstoff + Wasserdampf

- Alltagsbezug durch Untersuchung von Haushaltsreinigern Kalkentferner Abflussfrei

Säure-Base-Konzepte Man unterscheidet zwei wesentliche Konzepte: 1. Arrhenius: Substanz-bezogen (~1884) 2. Brönsted: Teilchen-bezogen (~1923) Was ist davon sinnvoll für den Unterricht?

Was ist davon sinnvoll für den Unterricht? Arrhenius-Konzept Brönsted-Konzept -betrachtet nur Ionen in -Säure-Base-Reaktion: wässrigen Lösungen (OH-/H+-Ionen) Übergabe von Protonen der Säure an die Base erlaubt keine Anwendung allgemeineres Konzept zur Deutung verschiedenster im allgemeinen Sinne Phänomene Feststellung: Das Konzept nach Arrhenius kann angesprochen werden, Brönsted-Konzept sollte allerdings im Vordergrund stehen!

Einstieg in das Konzept nach Brönsted-Säuren: Die Protonenspender 1. Teilversuch: Reaktion von Kochsalz und Schwefelsäure unter Bildung von gasförmigem Chlorwasserstoff H 2 SO 4 -Molekül+Cl--Ion HCl-Molekül + HSO 4 --Ion Säure 1 Base 1 Säure 2 Base 2 2. Teilversuch: Einleiten des entstandenen Chlorwasserstoff-Gases in Wasser HCl-Molekül +H 2 O-Molekül Cl-(aq)-Ion + H 3 O+(aq)-Ion Säure 1 Base 1 Base 2 Säure 2

Einstieg in das Konzept nach Brönsted-Basen: Die Protonenempfänger Versuch: Calciumoxid und Wasser reagieren stark exotherm Ca 2+-Ion + O 2 --Ion + 2 H 2 O-Molekül Ca 2+-Ion + (OH-)2 -Ion + H 2 O-Molekül Wesentliche Reaktion: O 2 --Ion + H 2 O-Molekül OH--Ion + OH--Ion Es kann festgestellt werden, dass Wasser sowohl als Säure als auch als Base reagieren kann. Solche Substanzen werden als Ampholyt-Teilchen bezeichnet!

3. Reine Säuren und Säure. Lösungen Gemeinsamkeiten und Unterschiede zwischen reiner Säure und Säurelösung am Beispiel einer Schwefelsäure

Fehlvorstellungen der Schüler - Verdünnungseffekt - Dichten unterscheiden sich - Reine Säure ätzender, reaktionsfreudiger

Beispiele für falsche Modellvorstellungen

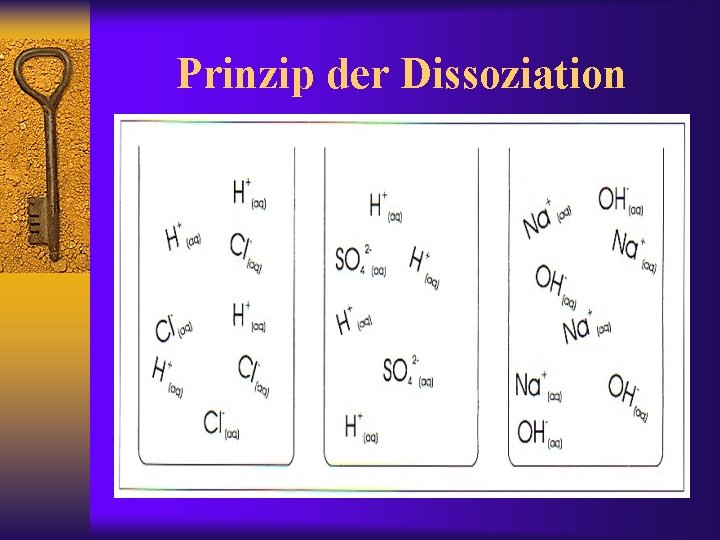
Fazit - Prinzip der Dissoziation wurde nicht verstanden - Wichtige Inhalte der Säure-Base Reaktion bleiben unverstanden

Unterrichtsvorschläge zu reinen Säuren und Säure. Lösungen Aggressivität von Säuren und ihren verdünnten Lösungen: Alltagsbezug: Magensäure, Phosphorsäure (in Cola), Zitronen- und Essigsäure (als Würzmittel), etc. Vergleich zum Verhalten reiner, konzentrierter Säuren Folgerung: Durch Verdunsten des Wassers können auch verdünnte Lösungen eine aggressive Wirkung erzielen!

Prinzip der Dissoziation

4. p. H-Wert Was ist der p. H-Wert bzw. wie definiert er sich? - negative dekadische Logarithmus der H+-Konzentration

Vorstellungen der Schüler zum Begriff des p. H-Werts

Fehlvorstellungen der Schüler - phänomenologische Antworten - viele verändern die Definition - richtige Antwort nur vereinzelt von Schülern - Argumentation mit Säuregrad/Säuregehalt

Fazit - reines Merkwissen und überwiegend Unverständnis von Schülern bezüglich des p. H-Werte - enorme Schwierigkeiten mit dem p. H-Wert umzugehen

Unterrichtsvorschläge zum p. H-Wert Einführung: Versuche zum Bestimmen des p. H-Wertes von Lösungen aus dem Alltag mit Hilfe von Universalindikator-Papier

Vertiefung: Der p. H-Wert Begriff des Mol muss den Schülern bekannt sein -Kurzübersicht geben: Beispiel: -Wasser: 18 g Wasser enthalten 1 mol H 2 O-Moleküle (nicht „ 1 mol Wasser“) -Salzsäure (1 mol/L): 1 mol H 30+(aq)-Ionen und 1 mol Cl-(aq)-Ionen Verdünnung: a)1: 10 0, 1 mol H 30+(aq)-Ionen b)1: 100 0, 01 mol H 30+(aq)-Ionen *Verweis: H+-(aq)-Ion als Kurzschreibweise für H 30+(aq)Ionen *Untersuchung des p. H-Wertes der Salzsäuren und Feststellung, dass ph-Wert = x , wenn c(H+) = 10 -x

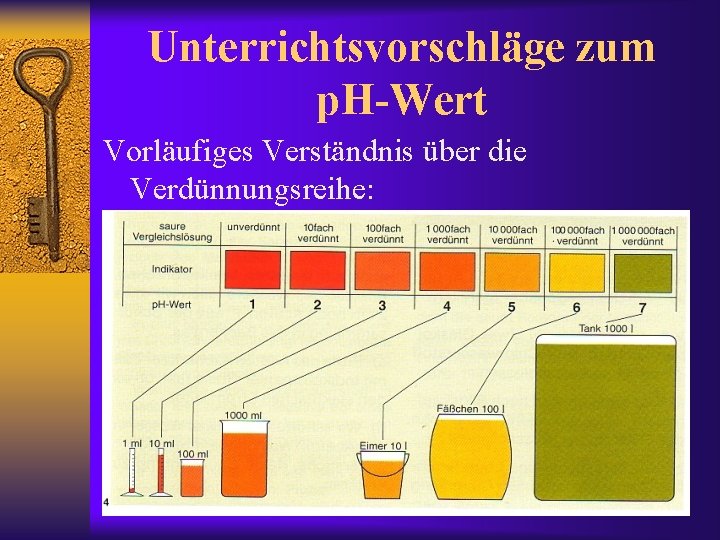
Unterrichtsvorschläge zum p. H-Wert Vorläufiges Verständnis über die Verdünnungsreihe:

Vertiefung: Der p. H-Wert Begriff des Mol muss den Schülern bekannt sein -Kurzübersicht geben: Beispiel: -Wasser: 18 g Wasser enthalten 1 mol H 2 O-Moleküle (nicht „ 1 mol Wasser“) -Salzsäure (1 mol/L): 1 mol H 30+(aq)-Ionen und 1 mol Cl-(aq)-Ionen Verdünnung: a)1: 10 0, 1 mol H 30+(aq)-Ionen b)1: 100 0, 01 mol H 30+(aq)-Ionen *Verweis: H+-(aq)-Ion als Kurzschreibweise für H 30+(aq)Ionen *Untersuchung des p. H-Wertes der Salzsäuren und Feststellung, dass ph-Wert = x , wenn c(H+) = 10 -x

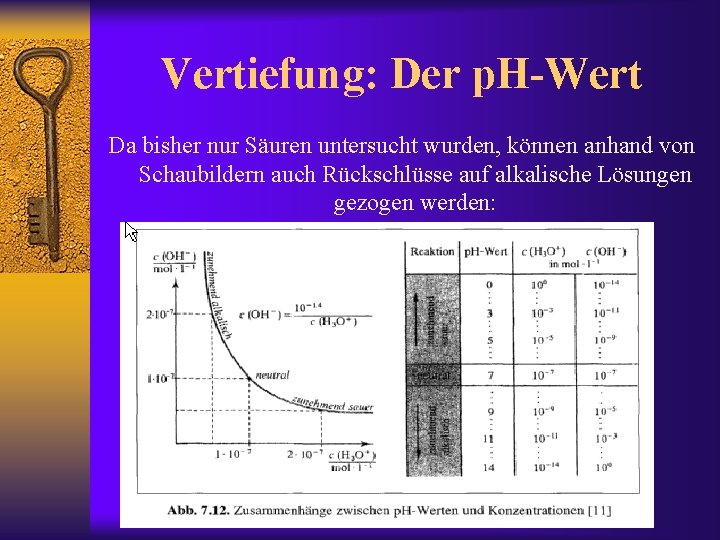
Vertiefung: Der p. H-Wert Da bisher nur Säuren untersucht wurden, können anhand von Schaubildern auch Rückschlüsse auf alkalische Lösungen gezogen werden:

5. Neutralisation - Schülerbefragung zur Neutralisation

Vorstellungen von Schülern von einer Neutralisation

Fehlvorstellungen der Schüler - Reaktionsgleichung HCl + Na. OH Na. Cl + H 2 O

Fehlvorstellungen der Schüler - Ionensymbole H+-Ionen und OH--Ionen reagieren zu H 20 - Name der Reaktion

Fazit - Salzbildung wird in den Vordergrund gestellt - Ionen werden zu „Salz-Molekülen“

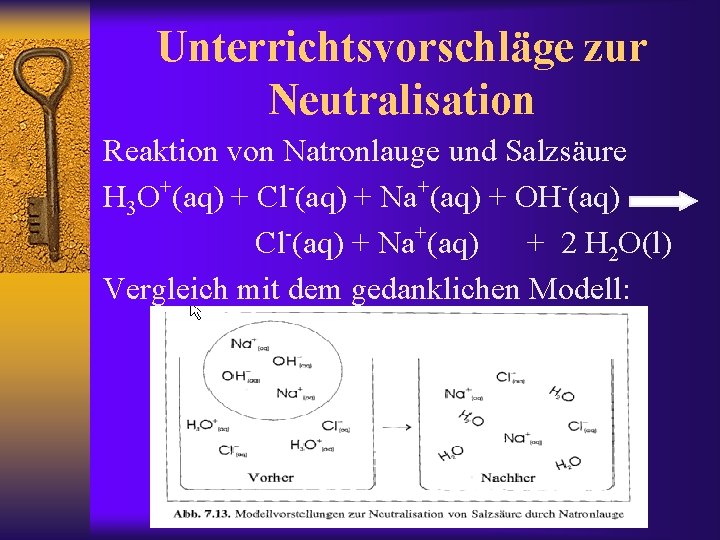
Unterrichtsvorschläge zur Neutralisation Reaktion von Natronlauge und Salzsäure H 3 O+(aq) + Cl-(aq) + Na+(aq) + OH-(aq) + Cl (aq) + Na (aq) + 2 H 2 O(l) Vergleich mit dem gedanklichen Modell:

Unterrichtsvorschläge zur Neutralisation Folgende Versuchsmethoden erlauben eine Überprüfung der Neutralisation: -p. H-Wert Bestimmung -Leitfähigkeitstitration -Überprüfung der Neutralisationswärme als Beweis, dass bei der Reaktion von starken Säuren und Basen nur die Hydronium-Ionen mit den Hydroxid -Ionen zu Wasser reagieren ( RH 0 m= -56 k. J/mol)

6. Starke und schwache Säuren Worin unterscheidet sich eine starke Säure von einer schwachen Säure?

Fehlvorstellungen der Schüler - Argumentation mit dem ph-Wert - Schwierigkeiten beim Überführen von Modellvorstellungen in konkrete Zeichnungen

Modellvorstellungen

Fazit Dissoziations- oder Protolysegard sind nicht verstanden worden

Unterrichtsvorschläge zu starken und schwachen Säuren Stärke der Säure entspricht nicht der Konzentration, sondern: - starke Säuren sind Teilchen, die leicht Protonen abgeben können. - schwache Säuren sind Teilchen, die nur schwer Protonen abgeben können. es gilt: Säurestärke wächst mit der Tendenz Protonen abzugeben [Umkehrschluss: Basenstärke wächst mit der Tendenz Protonen aufzunehmen]

Unterrichtsvorschläge zu starken und schwachen Säuren Einführung des Protoloyse-Begriffs und Vorstellung der Modelle

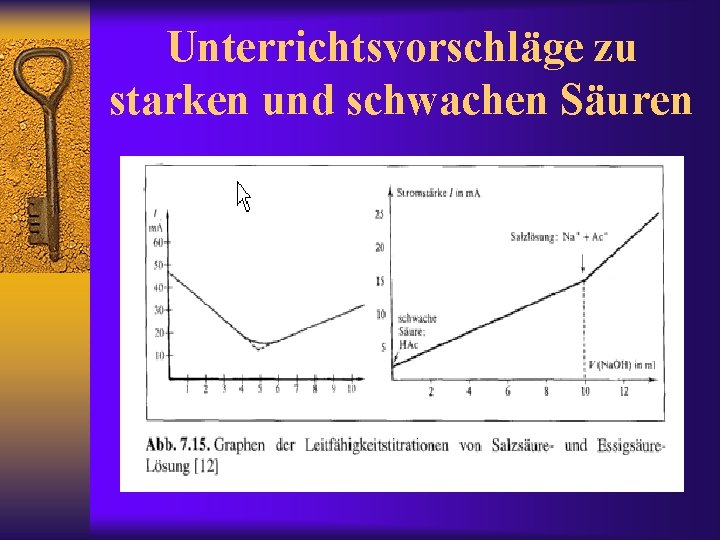
Unterrichtsvorschläge zu starken und schwachen Säuren

Zusammenfassung Schüler können mit einem Hauptthema der Chemie, der Säure-Base Theorien wenig anfangen Zusammenhänge müssen besser herausgearbeitet werden Verknüpfungen zwischen den Begriffen nicht nur auf Definitionen beschränken

Danke für eure Aufmerksamkeit!