Meningiti batteriche acute Definizione e classificazione Infiammazione delle

Meningiti batteriche acute

Definizione e classificazione • • • Infiammazione delle membrane (meningi) che avvolgono il cervello e il midollo spinale, caratterizzata da alta mortalità e morbosità e da una elevata frequenza di gravi complicanze Molteplici classificazioni: anatomica, clinica, eziologica La meningite batterica interessa pia madre e aracnoide, i fluidi dello spazio subaracnoideo e dei ventricoli cerebrali Meningismo: triade sintomatologica caratterizzata da cefalea, rigidità nucale, e fotofobia Meningiti infettive: causate da batteri, virus, miceti e parassiti. Le più frequenti sono quelle virali, in genere non gravi (sottodiagnosticate) con risoluzione nell’arco di 7 -10 giorni.

Meningiti batteriche • • • Secondo posto come frequenza, ma più rischiose (paziente e sanità pubblica) Patogeni più comuni (75% meningiti batteriche nel mondo, >90% di quelle pediatriche): – Neisseria meningitidis – Haemophilus influenzae di tipo b (Hib) – Streptococcus pneumoniae (diplococco) Altri agenti: – streptococchi di gruppo B (Streptococcus agalactiae) – enterobatteriacee (Escherichia coli) – Listeria monocytogenes. Nei pazienti con storia di trauma cranico o di intervento neurochirurgico: Streptococcus pneumoniae, Staphylococcus aureus, enterobatteriacee e Pseudomonas aeruginosa. Nei pazienti con derivazione ventricolo-peritoneale o ventricolo-atriale: Staphylococcus epidermidis, Staphylococcus aureus, enterobatteriacee, Propionibacterium acnes e, raramente, difteroidi.

Fisiopatologia della meningite batterica (1) I meccanismi fisiopatologici dipendono dalla peculiare risposta del sistema immunitario a livello del sistema nervoso centrale. L’agente causale raggiunge le meningi : • per via ematogena: o da colonizzazione asintomatica di rinofaringe, anche di cute, polmone, cuore, tratto gastrointestinale o genitourinario o da sede di infezione remota • per contiguità: o da orecchio, seni paranasali (sinusite, otite media) o da cavità orale (infezione dentale) o osteomielite di segmenti ossei contigui (mastoidite) • per impianto diretto: o in seguito a fratture del cranio o perdita di continuità per interventi chirurgici o per presenza di dispositivi di derivazione o cateteri permanenti.
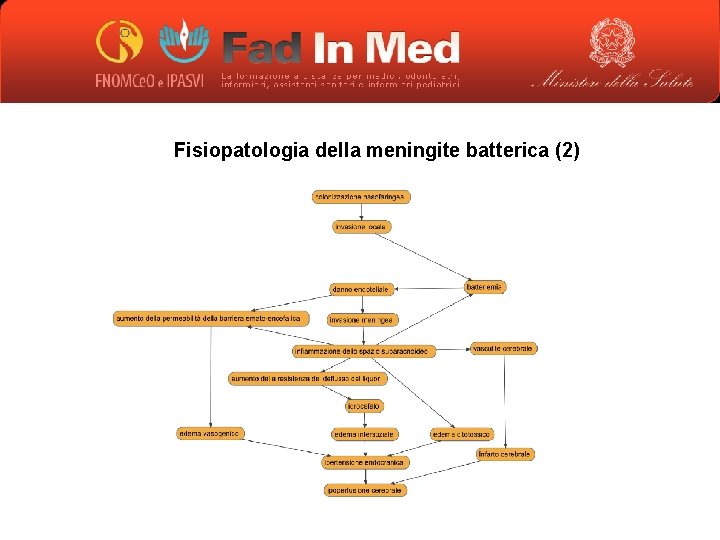
Fisiopatologia della meningite batterica (2)

Vie di trasmissione e fattori favorenti La trasmissione interumana segue diverse vie: • esposizione prolungata es. convivenza (Neisseria meningitidis) • contatto ravvicinato con germi veicolati da droplet delle secrezioni respiratorie, facilitata da tosse o starnuti (Neisseria meningitidis, Haemophilus di tipo b, Streptococcus pneumoniae) • trasmissione perinatale (streptococco di gruppo B ed Escherichia coli) • Inoltre derrate alimentari contaminate (Listeria monocytogenes ed Escherichia coli) Fattori di rischio preesistenti per l’insorgenza di una meningite batterica: • età (pediatrica <5 anni o età avanzata >65 anni) • vita in comunità (caserme, college, eccetera) e convivenza protratta (classi scolastiche) • malattie croniche (diabete, insufficienza renale cronica, insufficienza surrenalica, fibrosi cistica) • immunosoppressione, infezione da HIV, splenectomia, drepanocitosi (meningite da microrganismi capsulati es. Streptococcus pneumoniae) • malattie oncologiche • alcolismo ed epatopatia (specie la cirrosi) • storia di abuso di sostanze per via endovenosa • esposizione professionale (laboratori di microbiologia, operatori sanitari) • viaggiatori in zone ad alta frequenza di malattia • lesioni con perdita di continuità della dura madre (traumatiche, chirurgiche o congenite) o dispositivi di derivazione ventricolo-peritoneale o ventricolo-atriale. • suscettibilità genetica a una risposta infiammatoria sostenuta

Batteri patogeni L’accertamento dell’eziologia è di estrema importanza, non solo ai fini terapeutici (antibioticoterapia mirata) ma anche per l’eventuale profilassi dei contatti. Tra le varie cause l’infezione meningococcica si caratterizza per: • problema persistente, mondiale, di salute pubblica • malattia endemica, epidemica • inizio della malattia difficilmente riconoscibile, con inizio e progressione rapida • variabilità delle manifestazioni cliniche e difficoltà nella diagnosi differenziale con le comuni malattie virali • elevata morbilità e letalità • efficacia della terapia e possibilità di prevenzione con il vaccino

Neisseria meningitidis (meningococco) • Batteri aerobio Gram negativi, circondato da una capsula polisaccaridica (13 gruppi sierologici). • I sierogruppi A, B, C, W 135 e Y implicati >90% malattie sistemiche dell’uomo (in Italia più frequenti B e C) • Alberga nelle alte vie respiratorie di portatori sani e asintomatici. In <1% supera mucosa respiratoria e va in circolo; nel 50% dei casi di batteriemia si verifica la meningite • L’uomo è l’unico serbatoio naturale dell’infezione; notevole labilità fuori dall’organismo • Periodo di incubazione: 1 -7 giorni • Malattia invasiva da meningococco: può colpire tutte le età con meningite, sepsi (10 -20% decorso fulminante) • Secondo l’OMS, circa 171. 000 decessi nel mondo nel 2000, con letalità del 10 -15% per meningite, del 40% per sepsi, e sequele permanenti nel 20% dei casi • Andamento stagionale tipico con maggior frequenza nel periodo di fine inverno-inizio primavera • Nel 20% dei sopravvissuti sono presenti sequele a lungo termine, come ritardo mentale, ipoacusia/sordità, perdita (anatomica e funzionale) degli arti.

Fattori di rischio per malattia invasiva da meningococco

Lo stato di portatore del meningococco • Può permanere a lungo nel tempo senza manifestazioni cliniche. • Prevalenza: stime variabili (2 -30%) secondo fascia di età (<2% nei bambini sotto i 5 anni, 20 -25% negli adolescenti e nei giovani adulti), area geografica, condizioni socio-economiche, densità demografica. Elevati (60 -70%) in situazioni di grande affollamento. Variazioni notevoli dopo interventi di chemioprofilassi • Italia: media del 10 -12%, differenze secondo zone e gruppi di popolazione • Dubbio il rapporto tra numero di portatori e malattia (“soglia” del 20%) dato il riscontro di episodi di meningite in comunità a bassa prevalenza di portatori • L’evoluzione verso la malattia invasiva e la meningite sembra legata , più che alla virulenza del sierotipo, alla situazione immunitaria della popolazione sana e alla ricettività individuale, in particolare l’efficienza dell’immunità umorale • Trascurabile il ruolo dei portatori convalescenti e cronici • Il numero dei portatori in una determinata area geografica è un’utile informazione epidemiologica

Streptococcus pneumoniae (pneumococco) • Batterio Gram positivo, anaerobio facoltativo • Capsula ben evidenziabile, importante per la classificazione in >90 sierotipi e patogenicità (solo i tipi capsulati sono patogeni per la presenza degli antigeni polisaccaridici capsulari con attività anti fagocitaria) • I 10 sierotipi più diffusi sono responsabili del 60% circa delle malattie invasive • Pneumococco: causa più frequente delle polmoniti dell’adulto (letalità 5 -7% più elevato negli anziani) • Nel mondo 1, 6 milioni di decessi ogni anno, circa 1 milione di bambini sotto i 5 anni di età • Il 5 -90% della popolazione generale (il 20 -60% di quella pediatrica) portatore asintomatico • Nell’ambiente esterno rapida autolisi; elevata resistenza nelle secrezioni (nella saliva fino a 3 mesi), ma assai scarsa al calore (15 minuti a 55 °C) e ai comuni disinfettanti • Altamente sensibile al trattamento antibiotico (in aumento i ceppi resistenti) • Stagionalità autunnale-invernale • Dipende dalla virulenza del sierotipo e da fattori favorenti (infezioni virali, condizioni con iperproduzione e accumulo di muco, alcolismo e tabagismo, disturbi circolatori, malattie croniche, splenectomia, traumi cranici chiusi, presenza di impianto cocleare

Haemophilus influenzae • Batterio Gram positivo aerobio (anaerobio facoltativo), circondato da una capsula polisaccaridica (6 sierogruppi, indicati con le lettere minuscola da a a f); diversi sierotipi non capsulati meno virulenti • Colonizza il rinofaringe, punto di partenza per batteriemia e infezione settica o meningea. In era prevaccinale isolato nello 0, 5 -3% dei bambini, raramente nell’adulto • Fattori favorenti: infezioni respiratorie, virali o da micoplasma • Malattia più frequente nella stagione invernale • Prima dell’introduzione del vaccino contro il tipo b, era responsabile del 95% dei casi di malattia batterica invasiva prima dei 5 anni di età (60% dei casi di malattia nel primo anno di vita, picco 6 -11 mesi). All’età di 5 -6 anni molti bambini avevano acquisito l’immunità specifica per un’infezione asintomatica • Malattia invasiva: meningite (50 -65%), epiglottite con ostruzione respiratoria grave /fatale, otite, bronchite e polmonite, artrite ed osteomielite, pericardite o cellulite. L’otite media e la bronchite acuta sono causate prevalentemente da sierogruppi non capsulati. • Mortalità 3 -6%, nonostante terapia antibiotica • Conseguenze a lungo termine di tipo neurologico e l’ipoacusia/sordità: 15 -30% dei sopravvissuti

Epidemiologia • Diffusione: tutto il mondo, specie paesi a clima caldo e secco e zone densamente popolate • Casi sporadici con episodi epidemici • Incidenza più elevata: Africa subsahariana (80% dei casi nel mondo) • Nel 2010 circa 1, 2 milioni di casi nel mondo, con 180. 000 decessi soprattutto in età pediatrica • Letalità: 10 -40% secondo età (maggiore nei primi anni di vita), contesto socio-sanitario (più elevata nei Paesi non sviluppati e nelle situazioni di svantaggio), agente (maggiore con pneumococco). • Meningite da Neisseria: 500. 000 casi ogni anno nel mondo, circa il 10% mortali • Sequele a lungo termine: circa 20% dei casi, prevalentemente in seguito alle infezioni causate da Streptococcus pneumoniae. • Fascia a maggiore: bambini nel primo anno di vita (picco di incidenza tra 3 e 8 mesi) e dopo i 60 anni di età • Descritta una distribuzione di frequenza in funzione dell’età per le forme di meningite causate dai vari agenti (vedi tabella).

Principali agenti eziologici di meningite batterica e sepsi in rapporto all’età

Epidemiologia in era post vaccinale • La disponibilità di vaccini ha profondamente modificato l’epidemiologia e creato situazioni di rimpiazzo vaccinale (replacement), con un incremento del numero di casi di infezioni invasive dovute a sierotipi non contenuti nel vaccino • Esempio più clamoroso : dopo l’introduzione del vaccino anti Haemophilus influenzae tipo b, i dati dell’Istituto Superiore di Sanità riportano una riduzione da >80 casi per 100. 000 abitanti a 0, 2 casi per 100. 000 abitanti nel 2015 (USA riduzione del 99%, con un’incidenza inferiore a 1 caso per 100. 000 bambini sotto i 5 anni). Attualmente la maggioranza dei casi d’infezione invasiva da emofilo è dovuta a sierotipi diversi dal b, in particolare i sierotipi non capsulati (anche definiti non tipizzabili) • Pneumococco: dopo la campagna di vaccinazione con il vaccino coniugato 7 -valente e poi con il 13 valente ha ottenuto una diminuzione di oltre il 97% dei casi di malattia invasiva dovuti ai sierotipi vaccinali • Vaccino anti meningococco C in Europa: riduzione 2 casi per 100. 000 abitanti (1999) <1 caso per 100. 000 abitanti (2010) • Nell’insieme, nei Paesi sviluppati queste modificazioni epidemiologiche hanno determinato una netta prevalenza della quota di meningiti attribuibili a meningococco e a pneumococco, con una quota veramente marginale di quelle da emofilo. • Poiché la riduzione ha coinvolto soprattutto la popolazione pediatrica questa malattia è diventata relativamente più frequente nella popolazione adulta
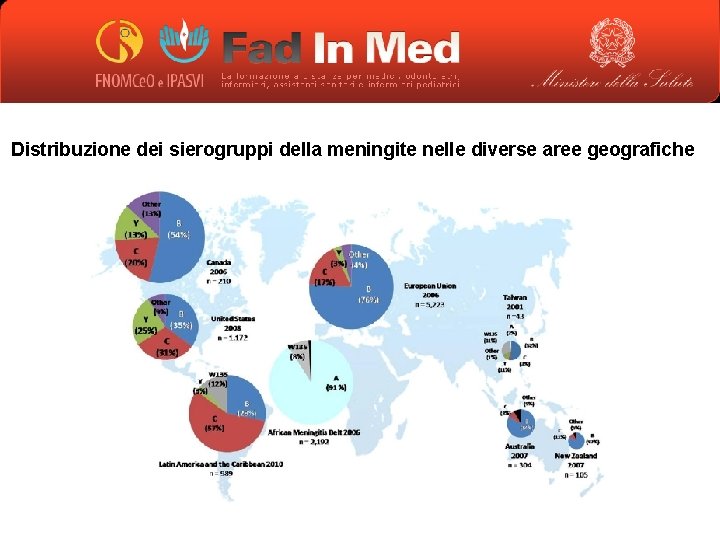
Distribuzione dei sierogruppi della meningite nelle diverse aree geografiche

La fascia della meningite • “Fascia della meningite”: zona più colpita dalla meningite da meningococco (Africa subsahariana dal Senegal all’Etiopia) che comprende 26 Paesi con 300 milioni di persone • Epidemie nella stagione secca (dicembre-giugno) della durata di anni • Scarsa igiene e sovraffollamento • Ciclicità di 7 -10 anni (alternanza di fasi con elevata immunità di gregge e fasi di suscettibilità • Incidenza annua 100 -800 casi per 100. 00 abitanti (nel mondo 3 casi per 100. 000 abitanti) • Prima del 2010 sierogruppo A, in aumento i sierotipi W, X e C, e lo pneumococco (nel 2015 prima epidemia da sierotipo C nell’Africa subsahariana) • Nel passato recente e al momento in atto campagne vaccinali e chemioprofilassiantibiotica

Dati europei, Neisseria meningitidis • Dati ECDC 2012: malattia da meningococco rara con 0, 7 casi per 100. 000 abitanti e ampia variabilità • L’Italia ha un’incidenza bassa pari a 0, 2 casi per 100. 000 abitanti • In 26 dei 28 Paesi sono attivi sistemi di sorveglianza • I dati riflettono anche il successo dei programmi vaccinali universali contro il meningococco C introdotti in alcuni Paesi (nessun programma contro il meningococco B) • Colpiti soprattutto i bambini (<1 anno 12, 3 casi per 100. 000, <5 anni 5, 1 casi per 100. 000) • Frequenza più elevata di portatori sani tra gli adolescenti (categoria su cui devono concentrarsi gli interventi sanitari • La maggior parte dei casi di malattia è causata da sierotipi B (dominante) e C, ma sta emergendo anche il sierotipo Y • Letalità 10%

Dati europei, Streptococcus pneumoniae • Dati dell’ECDC 2012: incidenza di 4, 3 casi per 100. 000 abitanti, variabile da 0, 2 a 15, 8 casi per 100. 000 abitanti (massima nei Paesi nordici) e stabile nel tempo • Italia: incidenza inferiore alla media europea 1, 3 casi per 100. 000 abitanti • Da agosto 2012: progetto pilota ECDC di sorveglianza Sp. ID-net (Streptococcus pneumoniae Invasive Disease network) • Programmi vaccinali disomogenei, ma malattia e stato di portatore in riduzione sia della malattia dopo vaccino 7 -valente, però con emergenza di sierotipi non contenuti nei vaccini • Adottati anche i nuovi vaccini 10 -valente e 23 -valente • Copertura vaccinale: 18% • Colpiti soprattutto i bambini (<5 anni 5, 1 casi per 100. 000) e gli anziani sopra i 65 anni di età (12, 2 casi per 100. 000) • Segnalata resistenza all’eritromicina nel 15, 6% dei casi e alla penicillina nel 6, 9% dei casi

Dati europei, Haemophilus influenzae • Dati ECDC 2012: incidenza bassa e relativamente stabile (0, 5 per 100. 000), tassi inferiori a 1 caso per 100. 000 in 19 su 24 Paesi • Italia compresa (0, 1 casi per 100. 000 abitanti) • Per effetto dei programmi vaccinali, calo progressivo dei casi dovuti al tipo b per effetto dei programmi vaccinali e aumento relativo degli altri sierotipi compresi quelli non capsulati • I tutti i Paesi europei la vaccinazione contro H. influenzae di tipo b è compresa nel calendario vaccinale. • I più colpiti sono i bambini sotto l’anno (4, 2 casi per 100. 000, con quadro clinico prevalente di meningite e/o sepsi), insieme agli anziani sopra i 65 anni (1, 5 casi per 100. 000, polmonite acquisita in comunità dovuta per la maggioranza dei casi a tipi non capsulati)

Dati italiani 2016 (aggiornamento 2 gennaio 2017) • 191 casi di meningite da meningococco (lieve aumento rispetto al triennio 2012 -14, diminuzione rispetto al 2015) dovuto prevalentemente alla situazione della Toscana (vedi dopo) • 940 casi di meningite da pneumococco (1. 256 nel 2015) • 80 casi da emofilo (131 nel 2015) Letalità: • 10% nei casi dovuti a pneumococco (98 deceduti su 940 pazienti nel 2016) • 12% nei casi da meningococco (21 su 178 pazienti); 23% se si considerano solo i casi da meningococco C (13 su 51 pazienti) Al momento non esiste alcuna situazione epidemica, la circolazione dei germi che causano la malattia è nella norma attesa, in linea con i numeri degli ultimi anni (vedi dopo).
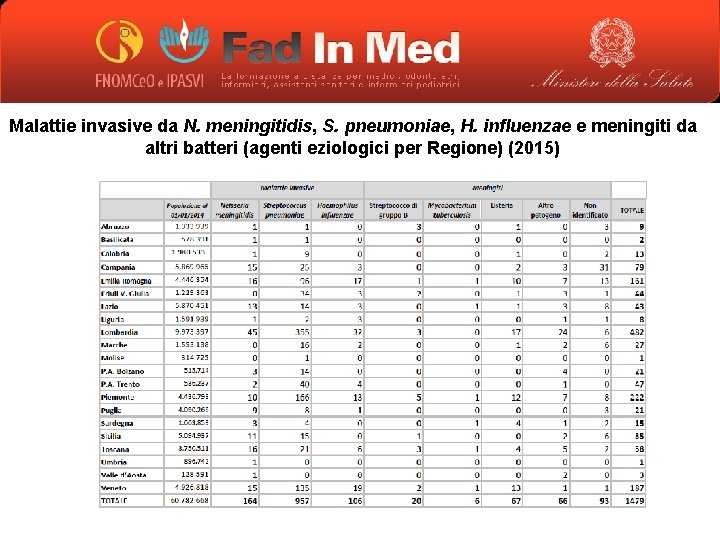
Malattie invasive da N. meningitidis, S. pneumoniae, H. influenzae e meningiti da altri batteri (agenti eziologici per Regione) (2015)
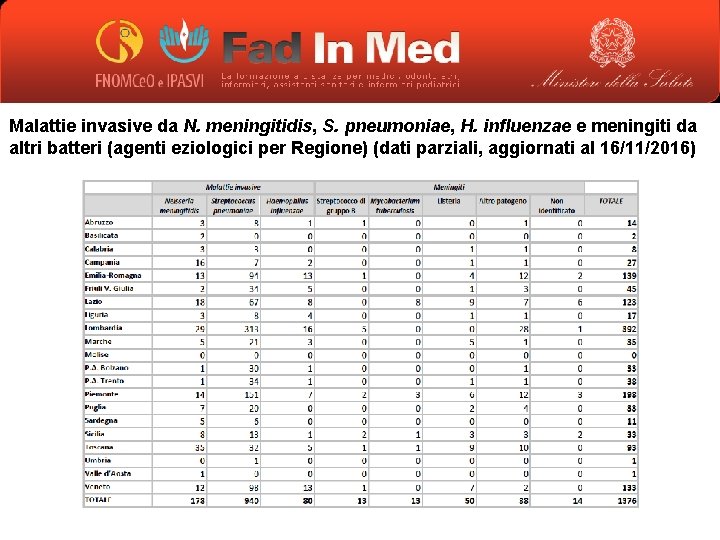
Malattie invasive da N. meningitidis, S. pneumoniae, H. influenzae e meningiti da altri batteri (agenti eziologici per Regione) (dati parziali, aggiornati al 16/11/2016)
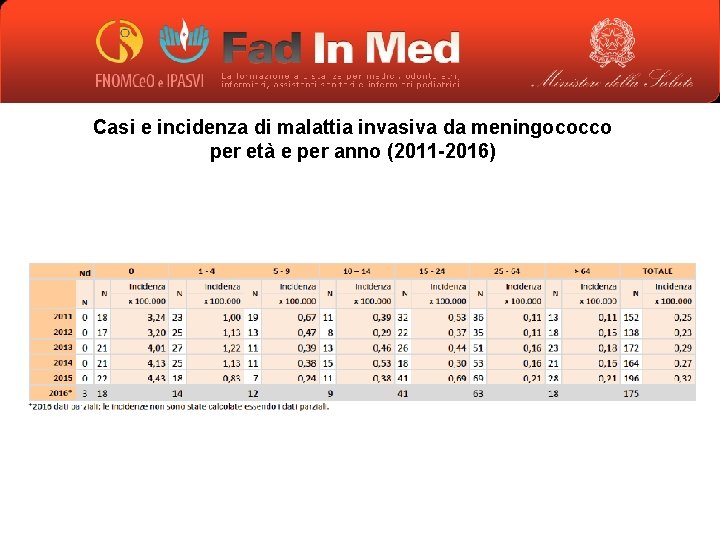
Casi e incidenza di malattia invasiva da meningococco per età e per anno (2011 -2016)
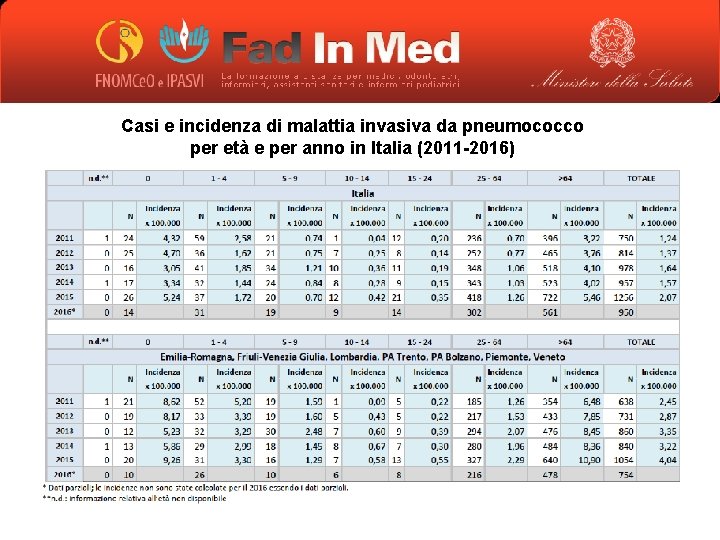
Casi e incidenza di malattia invasiva da pneumococco per età e per anno in Italia (2011 -2016)
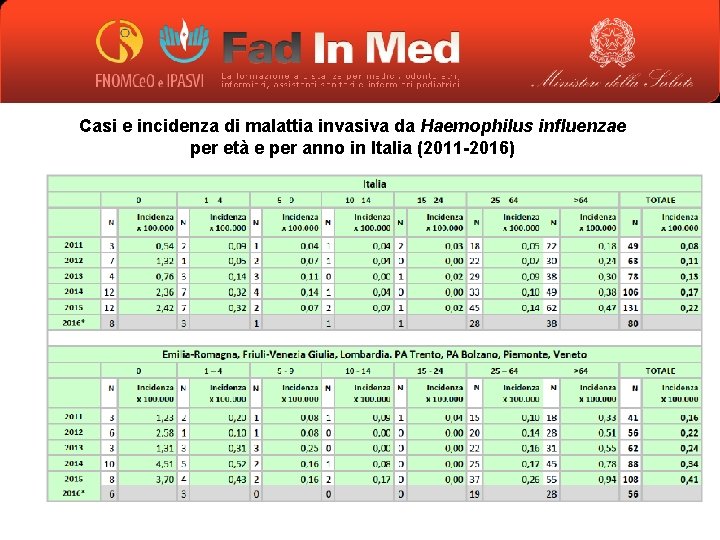
Casi e incidenza di malattia invasiva da Haemophilus influenzae per età e per anno in Italia (2011 -2016)
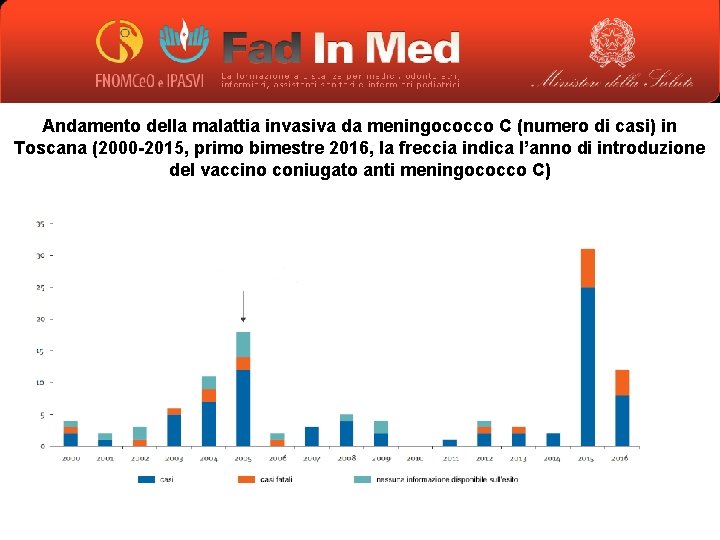
Andamento della malattia invasiva da meningococco C (numero di casi) in Toscana (2000 -2015, primo bimestre 2016, la freccia indica l’anno di introduzione del vaccino coniugato anti meningococco C)

Il caso Toscana • Pur tenendo conto dell’incremento dei casi, l’incidenza di meningite da meningococco in Regione Toscana resta nell’ambito di quella registrata a livello europeo nei Paesi con buon livello sanitario e la meningite si può ancora definire una malattia rara • Età media dei soggetti colpiti: 28 anni (9 -82 anni); fasce di età più colpite 20 -29 anni e 919 anni. Ben 18 >30 anni e ben 11 >50 anni • Quadro clinico: sepsi (18 casi), sepsi e meningite (14 casi), meningite soltanto (11 casi) • Su 42 pazienti (dati disponibili stato vaccinale): 5 vaccino anti meningococco C (1 il giorno stesso dell’insorgenza, 4 una sola dose 8 -10 prima) • Ben 35/40 casi sierotipo C 11, descritto in Italia ed Europa e dotato di marcata virulenza • La politica di offerta vaccinale molto ampia a favore della popolazione decisa dalle autorità sanitarie della Regione Toscana non ha per il momento limitato il numero di casi, simile negli anni 2015 e 2016, ma ha aumentato la consapevolezza nella popolazione.
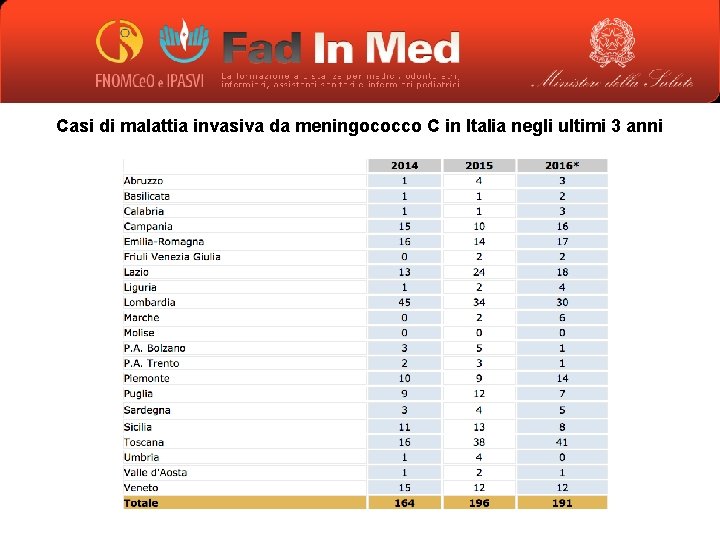
Casi di malattia invasiva da meningococco C in Italia negli ultimi 3 anni

Dove informarsi • • • Epi. Centro, la testata on line del Centro nazionale per la prevenzione delle malattie e la promozione della salute dell’ISS http: //www. epicentro. iss. it/ Ministero della Salute - AIFA. Meningite. Cosa c’è da sapere, gennaio 2017 http: //www. agenziafarmaco. gov. it/sites/default/files/Meningite_10. 01. 2017. pdf Ministero della Salute. FAQ sulla meningite, gennaio 2017. http: //www. salute. gov. it/portale/p 5_1_1. jsp? lingua=italiano&id=104 Istituto Superiore della Sanità (ISS). Meningite, come e quando difendersi con la vaccinazione, dicembre 2016 http: //www. iss. it/pres/? lang=1&id=1719&tipo=6 Da febbraio 2017 l’ECDC ha messo a punto Threat Reports, una app per computer, tablet o cellulare con informazioni aggiornate sulle malattie infettive

Quadro clinico (1) • Diagnosi clinica iniziale difficile perché i sintomi e i segni classici insorgono, soprattutto per quanto riguarda la malattia meningococcica, quando si è già verificata la batteriemia e/o l’infezione meningea, quindi tardivamente e, a volte, in modo rapidissimo • E’emergenza medica, ritardi nella diagnosi e nella terapia condizionano la letalità • Sempre da considerare per la diagnosi differenziale in presenza di cefalea, rigidità del collo, febbre e condizione mentale alterata; in età pediatrica in tutte le condizioni acute febbrili • Il solo esame clinico non è sufficiente a definire l’eziologia della meningite

Quadro clinico (2) • Età pediatrica: solo il 31% dei bambini che accedono pronto soccorso per segni meningei riceve una diagnosi effettiva di meningite batterica; il resto infezioni delle vie aeree superiori, meningiti virali e polmoniti • Petecchie che non impallidiscono alla digitopressione e di emorragie sottocutanee: presente in circa la metà dei casi di meningite da meningococco, ma anche con altri patogeni (emofilo e stafilococchi). Se rapida estensione e shock possibile sepsi meningococcica (talora fulminante con morte in 24 ore), anche in assenza di chiari segni di interessamento meningeo. • Artrite: tende ad associarsi, ma non in modo esclusivo, con le forme da meningococco.

Quadro clinico (3) In alcune categorie di pazienti fare diagnosi di meningite batterica è ancora più difficile data la sintomatologia atipica: • i pazienti precedentemente trattati con terapia antibiotica orale possono avere come unico sintomo le convulsioni • le persone anziane, in particolare quelle affette da comorbilità (diabete, malattie renali ed epatiche), possono presentare letargia e assenza di sintomi meningei • i pazienti con neutropenia possono avere sintomi lievi di irritazione meningea • i pazienti immunocompromessi che hanno ricevuto trapianti d’organo e tessuti e i pazienti con infezione da HIV e AIDS possono non mostrare un’infiammazione meningea e avere una febbricola.
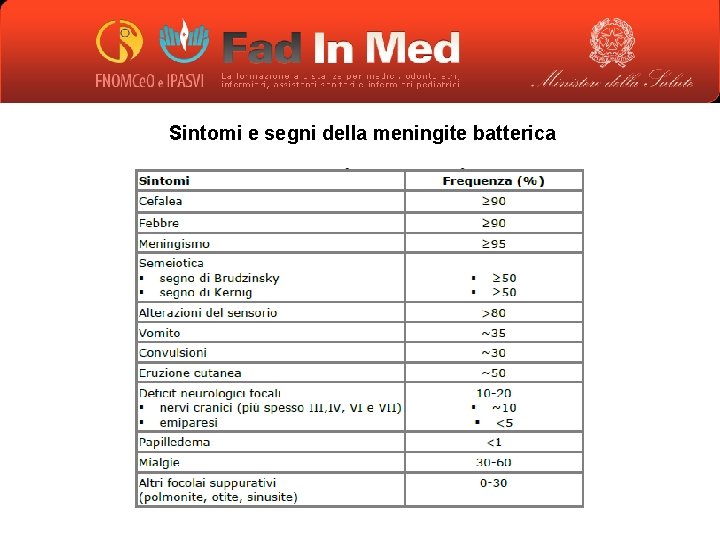
Sintomi e segni della meningite batterica

Sintomi e segni della meningite batterica in funzione dell’età

Sintomi da ipertensione endocranica Molti dei sintomi della meningite acuta sono una conseguenza dell’ipertensione endocranica: • cefalea: continua o remittente, generalizzata o parziale, esacerbata da manovre che causano aumento della pressione endocranica (tosse, starnuto, sforzo, compressione delle giugulari) • vomito da stimolazione del centro del vomito, sito nel pavimento del IV ventricolo, con insorgenza improvvisa, senza nausea, a getto, indipendente dall’introduzione di cibo • bradicardia, per stimolazione dei nuclei di origine del nervo vago, segno non sempre presente • paralisi del VI nervo cranico (abducente), che dato il lungo tragitto intracranico è particolarmente sensibile all’aumento della pressione • fontanella tesa e pulsante o diastasi delle suture (quando ancora aperte) • convulsioni, generalizzate o in forma di crisi parziali, riconducibili sia all’ipertensione endocranica, sia al rialzo termico, sia alla vasculite

Segni meningei • rigidità nucale: posizione a cane di fucile (decubito laterale con capo esteso e arti inferiori flessi), opistotono (tronco iperesteso) • segno di Kernig: impossibilità di flettere gli arti inferiori sul tronco senza che a questo movimento si associ una contemporanea flessione delle gambe; si può ricercare con il paziente seduto o supino sul letto • segno di Brudzinski o segno della nuca: la flessione passiva della nuca in avanti provoca la flessione degli arti inferiori. E’ descritto un secondo segno di Brudzinski o riflesso controlaterale: se, a malato supino, si flette fortemente la gamba e la coscia di un lato, si assiste a un movimento di flessione (riflesso identico) o di estensione (riflesso reciproco) nell’arto opposto • I segni meningei possono essere di entità variabile, e addirittura limitati a una modesta resistenza alla flessione del collo o francamente assenti, soprattutto in età pediatrica e in particolare sotto i 18 mesi di età. • Capacità predittiva limitata (sensibilità 31% rigidità nucale, 9% per il segno di Brudzinski 11% per il segno di Kernig. • Pertanto, anche in assenza di segni meningei, non si deve differire o rinunciare all’esecuzione della puntura lombare

Esame obiettivo • • • frequenza cardiaca frequenza respiratoria saturazione d’ossigeno temperatura corporea valutazione neurologica (scala del coma di Glasgow e/o la scala APVU) situazione di perfusione (per mezzo del tempo di riempimento capillare CRT): molto usato pediatria. Dopo compressione del letto capillare ungueale si osserva il ritorno del flusso facendo riferimento alla colorazione della cute (normale se <2 secondi). Tempi superiori indicano una riduzione della perfusione periferica. Tutte le linee guida raccomandano che la situazione clinica sia tenuta sotto stretto controllo attraverso verifiche ravvicinate nel tempo

Diagnosi di laboratorio • • emocromo con formula proteina C reattiva fattori della coagulazione (CID) glicemia (rapporto con glicorrachia, raccolta sincrona dei 2 campioni; non affidabile nel diabete) • prove di funzionalità epatica e renale • elettroliti (disidratazione o individuare la presenza di una sindrome da inappropriata secrezione di ADH) • lattato (stato settico soglia 18 mg/dl) • emocultura (vedi dopo) • quadro tipico: leucocitosi neutrofila e notevole incremento degli indici di flogosi (non valori soglia di leucociti e PCR, né diagnosi di esclusione se sono normali)

Rachicentesi • Esame del liquido cefalorachidiano: gold standard perché consente una diagnosi eziologica • Va eseguita in ogni caso sospetto in mancanza di controindicazioni specifiche (vedi tabella); in caso di controindicazioni si può riconsiderare a distanza di 812 ore (quadro clinico e diagnostica per immagini) • Linee guida del NICE per l’età pediatrica: la rachicentesi deve essere ripetuta in caso di ri-emergenza o persistenza della febbre, deterioramento delle condizioni cliniche, persistenza della positività dei marcatori d’infiammazione oppure comparsa di nuovi segni clinici • Qualsiasi decisione relativa al ricorso alla rachicentesi non deve essere motivo di ritardo per l’inizio della terapia antibiotica

Controindicazioni all’effettuazione della puntura lombare
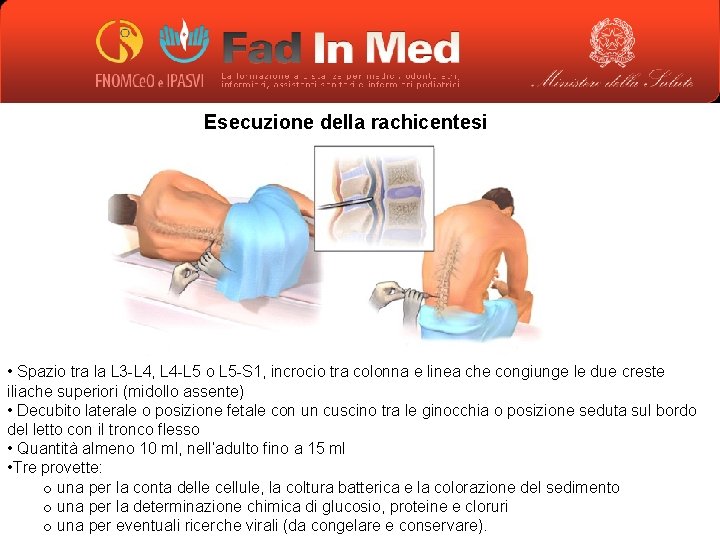
Esecuzione della rachicentesi • Spazio tra la L 3 -L 4, L 4 -L 5 o L 5 -S 1, incrocio tra colonna e linea che congiunge le due creste iliache superiori (midollo assente) • Decubito laterale o posizione fetale con un cuscino tra le ginocchia o posizione seduta sul bordo del letto con il tronco flesso • Quantità almeno 10 ml, nell’adulto fino a 15 ml • Tre provette: o una per la conta delle cellule, la coltura batterica e la colorazione del sedimento o una per la determinazione chimica di glucosio, proteine e cloruri o una per eventuali ricerche virali (da congelare e conservare).

Eventi avversi dopo rachicentesi • Cefalea: più frequente nei pazienti ipotesi e favorita dall’ortostatismo; dovuta allo stiramento meccanico della dura madre. • In genere autolimitante, se persistente si ricorre al blood patch • Per ridurre la probabilità della cefalea: ago di piccolo calibro (però prolungamento del prelievo, maggiore parestesia post intervento e più probabile insuccesso, orientamento sagittale dell’ago, riposizionamento del mandrino prima di estrarre l’ago, consolidata esperienza dell’operatore • Erniazione delle tonsille cerebellari: alterazione dello stato di coscienza e dei riflessi pupillari, postura decerebrata o decorticata, convulsioni

Caratteristiche del liquor nella meningite

Esame colturale • Esame colturale: di riferimento per la diagnosi eziologica (isolamento e tipizzazione, antibiogramma) • Prelievo al più presto, idealmente entro 1 ora dai sintomi e prima dell’antibiotico: informativo nel 50 -75% dei casi • Può essere sufficiente anche una sola somministrazione di antibiotico per abbassare la carica batterica e dare un risultato negativo della coltura (riduzione 10% della probabilità di isolamento del patogeno) oltre che interferire sui livelli di glicorrachia e protidorrachia • Il tempo di sterilizzazione del liquor dopo la prima dose di farmaco è di 2 ore per N. meningitidis e 4 ore per S. pneumoniae • Sensibilità: la positività è influenzata dal volume di liquido biologico prelevato e analizzato (rilevante in pediatria) • La mancata crescita in coltura e l’impossibilità di una sierotipizzazione ha anche un risvolto epidemiologico perche porta a sottostima o a problemi di classificazione delle infezioni

Diagnostica molecolare • Diagnostica molecolare con la metodica della reazione polimerasica a catena (PCR) su sangue e su liquor permette di rilevare anche piccole quantità di acido nucleico del patogeno responsabile, permettendo l’identificazione del batterio e del sierotipo. • Tra i metodi molecolari, la PCR standard (end point) e la real-time (RT-PCR), quest’ultima ha una maggiore sensibilità ed è in grado di fornire indicazioni sulla carica batterica • Per vantaggi e svantaggi, vedi tabella • Sensibilità 96 -98%, specificità 95 -99% • Dubbio di falsa positività nei portatori. • Dati Ospedale Universitario Meyer di Firenze: rispetto all’RT-PCR la coltura tradizionale sottostima la diagnosi di infezioni meningococciche di oltre 3 volte; c’è inoltre rischio di misclassificazione (confermato da altri studi internazionali) • RT-PCR utile nei quadri atipici

Vantaggi e limiti della RT-PCR

Imaging • TC e RMN: contributo modesto (immagini possono essere normali e l’enhancement a livello meningeo è aspecifico e tende a permanere) • Possibile contributo per diagnosi di ipertensione endocranica (rischio erniazione delle tonsille cerebellari dopo una rachicentesi e indicazione a rachicentesi) ma non deve ritardare i tempi della rachicentesi e della terapia antibiotica • Segni di ipertensione endocranica: idrocefalo ostruttivo, edema cerebrale diffuso, erniazione tonsille cerebellari, riduzione dimensioni ventricoli, attenuazione o scomparsa solchi (controindicazione alla rachicentesi) ma possono mancare • Pertanto, le indicazioni più recenti non prevedono che vada effettuata di routine una TC dell’encefalo prima della puntura lombare. Il NICE la raccomanda nei casi pediatrici con alterazioni gravi dello stato di coscienza o con segni neurologici focali; l’Infectious Diseases Society of America nei pazienti con immunodepressione, malattia neurologica, storia di convulsioni, papilledema, alterazione coscienza, defici neurologici focali • . TC e RM sono invece utili nella valutazione e nel follow up delle complicanze

Complicanze delle meningiti acute

Complicanze • Frequenza stimata complicanze a breve termine 50%, a lungo termine 30% • Effetto del danno neurologico diretto o di vasculite (trombosi vasale e lesioni ischemiche, CID), ipossia e ipertensione endocranica • Le complicanze sono più frequenti con streptococco (30% dei casi), meno con meningocco (7%), a meno di sepsi (57%) • Fattori di rischio per complicanze: età avanzata, gravità clinica (alterazione del livello di coscienza e punteggi bassi della scala del coma di Glasgow, insorgenza di convulsioni, paralisi dei nervi cranici, leucopenia) • La meningite è la causa più frequente di ipoacusia/sordità neurosensoriale in età pediatrica. con ricadute sull’acquisizione del linguaggio. Superata la fase acuta, valutazione audiometrica ed eventuale impianto cocleare • Per le cicatrici e le amputazioni, accanto ai trattamenti ricostruttivi, protesici e riabilitativi bisogna intervenire con supporti psicologici.

Terapia antibiotica empirica • Va iniziata il più precocemente possibile (al momento del sospetto) perché la tempestività incide su sopravvivenza e sequele. Evitare ritardi per qualsiasi ragione • Somministrazione da mezz’ora a un’ora dal ricovero (tempo compatibile con rachicentesi) • Scelta del farmaco: bisogna tenere conto di fattori demografici ed epidemiologici: età del paziente, probabilità di infezioni da patogeni specifici nelle diverse fasce di età, situazione locale di antibiotico-resistenza/sensibilità a penicilline e cefalosporine di III generazione (Italia è compresa, insieme a Canada, Cina, Croazia, Grecia, Messico, Pakistan, Polonia, Spagna, Stati Uniti e Turchia, nei Paesi in cui è diffusa la penicillinoresistenza) ; utile consultare sito ECDC, • Considerare che passaggio della BEE dipende da solubilità, dimensioni della molecola, legame proteico e dal grado di infiammazione delle meningi. Le cefalosporine di III generazione, contemplate dalla maggior parte delle linee guida come farmaci di scelta per la terapia empirica, hanno attività battericida per pneumococco e meningococco e penetrano attraverso le meningi infiammate. • Ceftriaxone non è indicato nel neonato (rischio ittero)
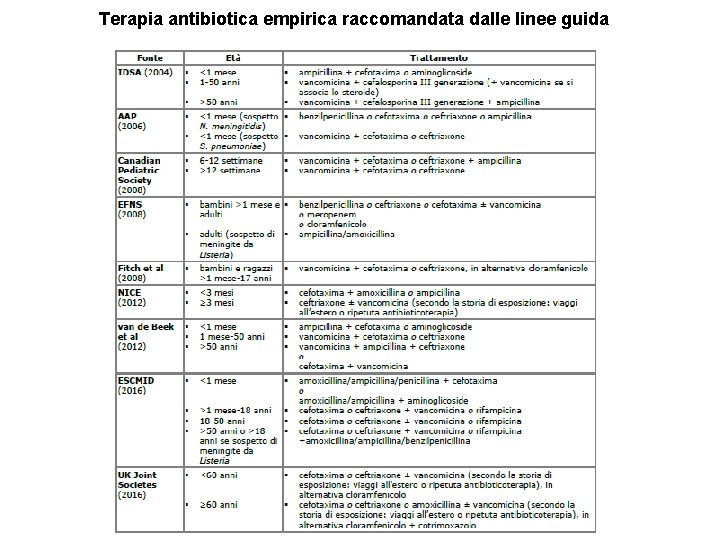
Terapia antibiotica empirica raccomandata dalle linee guida

• • Terapia antibiotica mirata Va avviata dopo diagnosi eziologica Tenere conto dell’epidemiologia locale e della prevalenza di ceppi resistenti (es. scelta di associare la vancomicina nella meningite pneumococcica) Linee guida non univoche: tendenza a proseguire la terapia empirica (quando sia a base di cefotaxima o ceftriaxone) o passare ad antibiotici a spettro più limitato (penicilline) quando sia stata accertata la sensibilità Durata del trattamento: 7 giorni per N. meningitidis, 7 -10 giorni per H. influenzae, 1014 giorni per S. pneumoniae, 2 -3 settimane per S. agalactiae e L. monocytogenes. Prolungare nei casi complicati o con risposta non soddisfacente, sulla base di un parere specialistico. La via di somministrazione standard è quella endovenosa (a bolo o in infusione). La somministrazione intratecale è prevista in casi selezionati. L’allergia a penicilline e/o alle cefalosporine (riferita come storia clinica, ma da verificare): carbapenemi dato l’ampio spettro di attività. Nei casi con sospetto clinico di origine batterica ma con esame culturale negativo: prosecuzione della terapia empirica per almeno 2 settimane

Terapia antibiotica mirata raccomandata dalle linee guida (1)
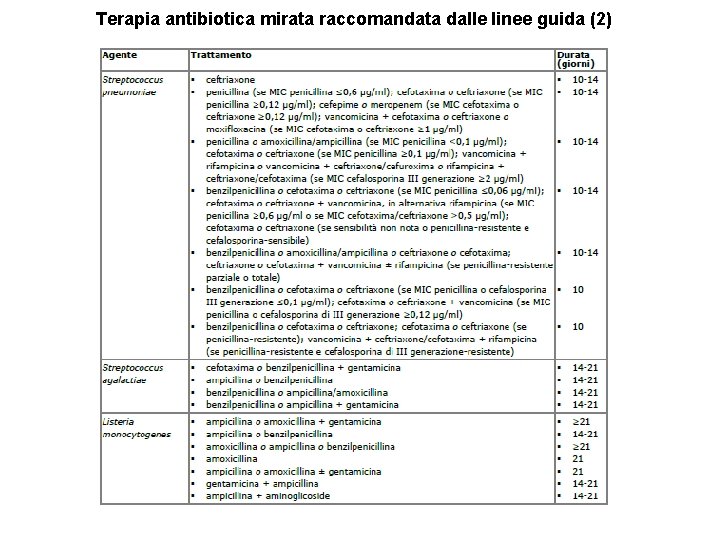
Terapia antibiotica mirata raccomandata dalle linee guida (2)

Corticosteroidi • Per via sistemica, quasi sempre desametasone • Razionale: attenuazione alcuni effetti sfavorevoli evocati dalla risposta dell’organismo all’infezione • Maggiormente indicati se nel liquor conta leucocitaria >1. 000 cellule/μl, livelli di proteine >1 g/l, batteri alla colorazione di Gram • Dubbio che si riduca il passaggio di alcuni antibiotici come la vancomicina a livello del sistema nervoso centrale • Controindicazione sotto i 3 mesi di vita (assenza prove di efficacia e sicurezza) • Iniziare nelle prime ore dopo il ricovero, con modesto anticipo o in contemporanea all’inizio degli antibiotici, non oltre le 12 ore successive. • 0, 15 mg/kg in età pediatrica fino a un massimo di 10 mg al giorno (suddivise in 4 somministrazioni) per una durata della terapia di 4 giorni • Efficacia controversa (probabile riduzione seuqele) • Non esistono dati sufficienti su altri diuretici osmotici come mannitolo e soluzioni saline ipertoniche.

Terapia di supporto • Controllo della febbre: paracetamolo • Somministrazione di liquidi: idratazione di supporto per via parenterale ma per anni tendenza a limitare l’apporto di liquidi per il rischio di favorire l’edema cerebrale e l’ipertensione endocranica (fattori favorenti aggiuntivi, come il rischio della sindrome da inappropriata secrezione di ADH). Oggi c’è indicazione a idratazione di mantenimento, a meno che non compaiano segni e sintomi di ipertensione endocranica o SIADH. • Prove recenti: idratazione di mantenimento riduce rischio di spasticità e convulsioni • Per mantenere l’equilibrio idroelettrolitico e per evitare l’ipoglicemia, vanno somministrate soluzioni isotoniche come glucosio 5% in cloruro di sodio 9% o destrosio 5% in cloruro di sodio 9%. Nei neonati è indicato glucosio 10% in cloruro di sodio 9%.

Trattamento delle emergenze Trasferimento in Unità di terapia intensiva in caso di: • rash in rapida evoluzione • coma con punteggio della scala di Glasgow ≤ 12 (indicata l’intubazione) • instabilità emodinamica • insufficienza d’organo • convulsioni non controllate. La sepsi e lo shock settico secondo le linee guida locali. Obiettivi: • mantenimento volemia (cristalloidi, in alternativa albumina o idrocortisone) • controllo ipertensione endocranica • mantenimento pressione arteriosa (valori medi ≥ 65 mm. Hg, accettabili valori ≥ 50 mm. Hg nei pazienti giovani, desiderabili valori ≥ 70 mm. Hg nei pazienti anziani) (noradrenalina in infusione venosa centrale) • controllo delle convulsioni, iniziando il trattamento anche in caso di sospetto (raccomandato il monitoraggio EEG) nei pazienti con stato di male • controllo dell’ipercapnia • trattamento dei disturbi della coagulazione

Vaccinazioni • Per ciascuna delle tre principali forme di meningite batterica è disponibile un vaccino • L’utilizzo della profilassi vaccinale è giustificato dalla gravità (potenziale letalità e morbosità) e dal fatto che i trattamenti disponibili possono fallire (ritardo o mancata risposta) • Va ricordato il valore sociale delle vaccinazioni e il vantaggio per la collettività nel contrasto a malattie prevenibili relativamente frequenti, gravi o fatali. Il raggiungimento di un’elevata copertura nella popolazione bersaglio (immunità di comunità, community immunity o immunità di gregge, herd immunity) rappresenta da sempre il valore aggiunto della vaccinazione a livello sociale. La protezione si estende anche ai non vaccinati (bambini molto piccoli o soggetti affetti da particolari patologie per cui non possono vaccinarsi, bambini non vaccinati per scelta dei genitori o perché provenienti da paesi dove non esistono le vaccinazioni per tutti, anziani, gli ammalati o le persone fragili, donne in gravidanza)
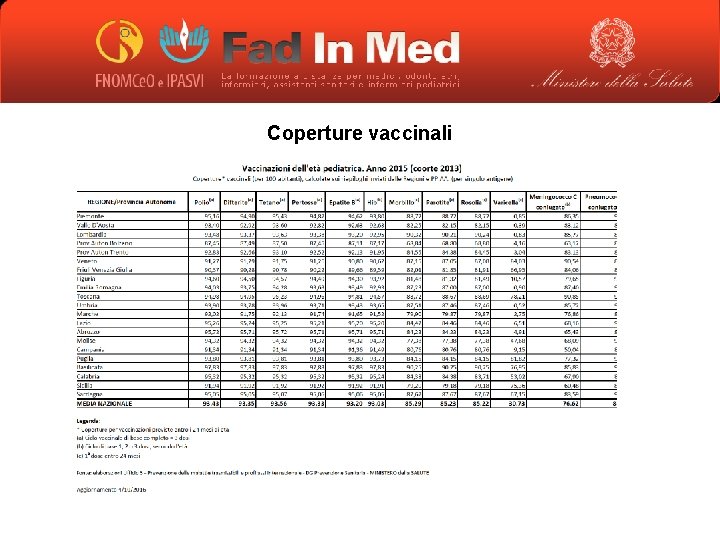
Coperture vaccinali

Offerta vaccinale • L’attuale Piano Nazionale della Prevenzione Vaccinale (PNPV) 2017 -2019, incluso nei LEA prevede l’offerta attiva dei vaccini contro le meningiti batteriche • Va superata la distinzione tra vaccinazioni “obbligatorie” e vaccinazioni “raccomandate” • Il precedenza il SSN includeva nel calendario vaccinale come vaccinazioni “raccomandate” con offerta attiva e gratuita: o nell’infanzia: vaccino anti pneumococcico, vaccino anti meningococcico C, vaccino contro le forme invasive di Haemophilus influenzae b per tutti i nuovi nati, o nell’età adulta (particolari categorie di persone): vaccino anti pneumococcico (persone oltre i 65 anni e/o con comorbilità croniche e debilitanti), vaccino anti meningococcico (viaggiatori in zone endemiche o a rischio). • La vaccinazione anti meningococcica era “obbligatoria” per le reclute all’atto dell’arruolamento

Obiettivi • raggiungimento e mantenimento di coperture vaccinali ≥ 95% per le vaccinazioni anti difterite-tetano-pertosse acellulare (DTPa), poliomielite, epatite B, infezioni invasive da Haemophilus influenzae tipo b (Hib) nei nuovi nati • raggiungimento e mantenimento nei nuovi nati di coperture vaccinali ≥ 95% per la vaccinazione anti pneumococcica • raggiungimento e mantenimento entro i 2 anni di età di coperture vaccinali ≥ 95% per la vaccinazione antimeningococcica C • raggiungimento e mantenimento nei nuovi nati di coperture vaccinali ≥ 95% per la vaccinazione antimeningococcica B, con una gradualità programmata per il triennio 2017 -2019 (passaggio da ≥ 60% a ≥ 95%) • raggiungimento e mantenimento negli adolescenti (11 -18 anni) di coperture vaccinali ≥ 95% per la vaccinazione anti meningococcica tetravalente ACYW 135, con una gradualità programmata per il triennio 2017 -2019 (passaggio da ≥ 60% a ≥ 95%) • raggiungimento nei sessantacinquenni di coperture per la vaccinazione anti pneumococcica del 75%, con una gradualità programmata per il triennio 2017 -2019 (passaggio da 40% a 75%)
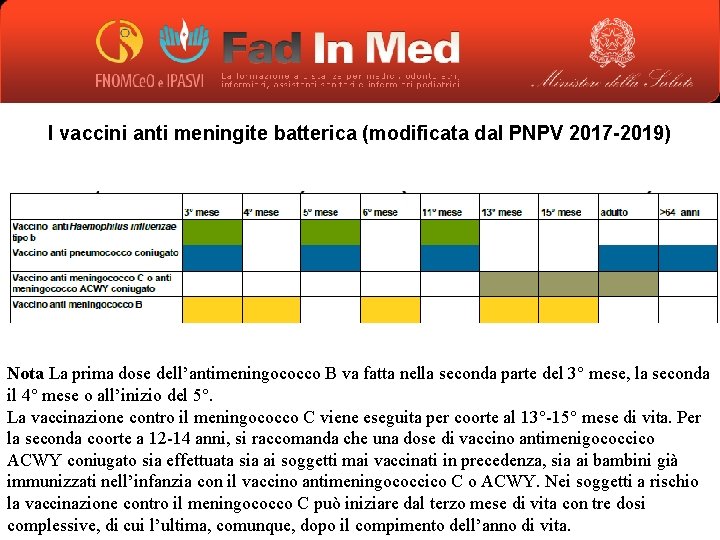
I vaccini anti meningite batterica (modificata dal PNPV 2017 -2019) Nota La prima dose dell’antimeningococco B va fatta nella seconda parte del 3° mese, la seconda il 4° mese o all’inizio del 5°. La vaccinazione contro il meningococco C viene eseguita per coorte al 13°-15° mese di vita. Per la seconda coorte a 12 -14 anni, si raccomanda che una dose di vaccino antimenigococcico ACWY coniugato sia effettuata sia ai soggetti mai vaccinati in precedenza, sia ai bambini già immunizzati nell’infanzia con il vaccino antimeningococcico C o ACWY. Nei soggetti a rischio la vaccinazione contro il meningococco C può iniziare dal terzo mese di vita con tre dosi complessive, di cui l’ultima, comunque, dopo il compimento dell’anno di vita.

Vaccinazione per fasce di età (1) • Nel primo anno di vita del bambino, il vaccino contro Haemophilus influenzae di tipo B è compreso nel ciclo di base con esavalente che va iniziato al 3° mese (61° giorno di vita). Simultaneamente alla vaccinazione con esavalente, ma in sede anatomica diversa (quadricipite femorale della coscia controlaterale) si raccomanda la somministrazione del vaccino anti pneumococco coniugato. La somministrazione delle 3 dosi iniziali del vaccino anti meningococco B (raccomandata per tutti i nuovi nati) deve essere iniziata il più presto possibile e completata nel 1° anno di vita, essendo l’incidenza delle malattie invasive causate da tale agente eziologico massima nei primi 2 anni di vita. Dal momento che la somministrazione simultanea del vaccino anti meningococcico B con altri prodotti determina aumento della frequenza di febbre di grado moderato/elevato, è opportuno evitare la cosomministrazione con altri vaccini previsti in calendario. Nel caso la vaccinazione sia iniziata dopo il 6° mese, è possibile utilizzare un ciclo a sole 3 dosi, con le prime due raccomandate, rispettivamente, al 7° e al 9° mese di vita.

Vaccinazione per fasce di età (2) • Il secondo anno è l’epoca della dose di richiamo del vaccino esavalente (11° 13° mese di vita) e, simultaneamente, della dose di richiamo della vaccinazione anti pneumococco coniugata, così come della quarta dose del vaccino anti meningococco B (o terza dose, nel caso di schedula a 3 dosi). Fra il 13° e il 15° mese è anche raccomandata la vaccinazione anti meningococco C o contro i quattro tipi di meningococco ACYW 135, allo scopo di offrire ai bambini una protezione più ampia per quei ceppi di meningococco che, pur ancora sporadici nel nostro Paese, mostrano una tendenza all’espansione. Vista la necessità di fornire in breve tempo protezione con diversi vaccini, è importante considerare gli schemi di possibili cosomministrazioni. Dal momento che la somministrazione simultanea del vaccino anti meningococcico B con altri prodotti determina aumento della frequenza di febbre di grado moderato/elevato, è opportuno evitare la cosomministrazione con altri vaccini previsti in calendario.

Vaccinazione per fasce di età (3) • Nell’adolescenza va effettuata una dose di vaccino anti meningococco quadrivalente ACYW 135 sia a chi non abbia mai effettuato nell’infanzia la vaccinazione C o quadrivalente sia a chi abbia già ricevuto una dose, in quanto la persistenza della protezione è legata a un elevato titolo anticorpale battericida, che tende a diminuire nel tempo. Per la vaccinazione contro il meningococco B, vista la sua recente introduzione, la priorità è rappresentata dal suo utilizzo nell’età in cui è massimo l’impatto della malattia (prima infanzia). In prospettiva si dovranno approntare politiche di offerta attiva di tale vaccinazione anche nella popolazione adolescente. • Nell’età adulta (19 -64 anni) è raccomandata la vaccinazione anti pneumococcica: andrà valutata la possibilità di somministrare una prima dose con vaccino coniugato (13 -valente), seguita ad almeno 2 mesi di distanza da una dose di vaccino polisaccaridico (23 -valente). Nel caso permangano situazioni epidemiologiche di rischio anche per l’età adulta, deve essere somministrata una dose di vaccino quadrivalente meningococcico ACYW 135.

Vaccinazione per fasce di età (4) • Nell’età anziana (≥ 65 anni) è necessario offrire attivamente il vaccino anti pneumococco coniugato 13 -valente, seguito da una dose di vaccino polisaccaridico 23 -valente. Va posta attenzione a non invertire l’ordine di somministrazione dei due vaccini, perché ciò comporterebbe una più bassa risposta immune. La coorte cui la vaccinazione deve essere offerta attivamente è rappresentata dai soggetti di 65 anni di età. Le Regioni che, per situazioni epidemiologiche e di contesto volessero offrire la vaccinazione a due coorti d’età, dovrebbero prediligere i 65 enni e i 70 enni. La vaccinazione anti pneumococcica può essere offerta simultaneamente alla vaccinazione antinfluenzale o indipendentemente in qualsiasi stagione dell’anno, ma va somministrata in dose singola una sola volta nella vita.

Caratteristiche dei vaccini • Tutti vaccini inattivati contenenti componenti antigeniche dell’agente • Somministrazione per via intramuscolare e sono tutti. • Vaccini anti meningococco – vaccini coniugati (disponibili contro il sierotipo C o contro i sierotipi A, C, W 135 e Y) vengono preparati legando alcune proteine ai polisaccaridi di superficie – vaccini polisaccaridici (disponibili contro i sierotipi A, C, W 135) suscitano una risposta immunitaria meno vivace. • Vaccini anti pneumococco: vaccini coniugati aventi per antigene i polisaccaridi della superficie batterica (vaccino 13 -valente è coniugato e protegge nei confronti di 13 sierotipi di pneumococco responsabili della maggior parte delle infezioni gravi nei bambini; il vaccino 23 -valente è polisaccaridico) • Vaccino contro l’Haemophilus influenzae tipo b è coniugato a un proteina antigenica ed è disponibile in forma singola o combinato nel vaccino esavalente. • Rapporto rischi-benefici e profilo di sicurezza favorevoli • L’EMA pubblica sul sito le schede tecniche (assessment report) di tutti i vaccini

I non responder • Tutti i vaccini, compresi quelli contro le meningiti batteriche non sono efficaci al 100% e non evocano nel soggetto vaccinato una immunità permanente • Esiste un 5 -10% di soggetti non responder che, per situazioni permanenti o transitorie, non sviluppano un’adeguata risposta immunitaria e che non rispondono del tutto al vaccino ovvero rispondono con una produzione anticorpale inferiore all’atteso. • Per i vaccini anti meningococco C la quota dei non responder è del 5% circa e la memoria immunitaria ha una durata limitata a 5 -6 anni. • Nei responder parziali la vaccinazione contribuisce comunque a limitare l’aggressività • Le schedule vaccinali (cicli o richiami) tengono conto di questa possibilità • Quanto descritto conferma ulteriormente l’importanza del raggiungimento nella popolazione di coperture vaccinali Ciò è particolarmente importante nel caso del meningococco, data la caratteristica di annidarsi nel rinofaringe di portatori sani

Profilassi dei contatti per la mennigite da Neisseria meningitidis

Isolamento e profilassi dei contatti (1) • Isolamento del caso indice (sospetto o accertato) per le 24 ore successive all’inizio della terapia antibiotica empirica o mirata • Personale sanitario: precauzioni per la trasmissione tramite droplet e secrezioni respiratorie, indossando mascherine chirurgiche. • Il rischio di meningite meningococcica aumenti di 400 -1. 000 volte tra le persone a stretto contatto con un caso e sia massimo per i conviventi • La profilassi è indicata per i contatti stretti dei casi sospetti o accertati di meningite meningococcica e da emofilo, non nei casi di meningite da pneumococco • Si definiscono contatti stretti: o i conviventi, compresi coloro che condividono l’ambiente di studio o di lavoro e coloro che hanno dormito o mangiato negli stessi ambienti del paziente o coloro che nei 7 -10 giorni precedenti sono stati esposti a secrezioni della cavità orale o a secrezioni respiratorie • La maggioranza dei casi si verifica nella settimana dopo l’esposizione, la massima probabilità di casi secondari persiste per la settimana successiva. Se all’identificazione del contatto sono già trascorsi 7 -10 giorni, non c’è più alcun rischio • La probabilità che i contatti sviluppino la malattia persiste per circa 6 mesi

Isolamento e profilassi dei contatti (2) • In presenza di focolai di malattia meningococcica, la profilassi va estesa secondo strategie locali di sanità pubblica, prendendo in considerazione sia l’impiego di antibiotici sia la vaccinazione (obiettivo eradicazione) • La gestione dei focolai comprende raccolta informazioni epidemiologiche e di sorveglianza • Non sono giustificate misure straordinarie come la chiusura di strutture scolastiche o gli screening per individuare i portatori sani di meningococco • Le indicazioni sulla vaccinazione dei contatti sono più controverse: sono stati pubblicati dati negativi e le seguenti raccomandazioni sono sostenute da prove di efficacia deboli

Notifica e sorveglianza • In Italia la sorveglianza delle malattie infettive si affida al Sistema Informativo delle Malattie Infettive (SIMI) che si basa sulle notifiche di medicina generale e ospedalieri e prevede segnalazioni immediate • Spetta al medico che formula la diagnosi effettuare la segnalazione alla ASL di competenza. Da qui viene avviata l’adozione di eventuali misure di profilassi a tutela della salute pubblica da parte delle ASL, azioni di supervisione e di coordinamento da parte della Regione, degli organismi centrali (Ministero della Salute, Istituto Nazionale di Statistica, Istituto Superiore di Sanità) ed eventualmente internazionali (Unione Europea, Organizzazione Mondiale della Sanità). • I dati raccolti sono disponibili nelle banca dati SIMI. • I dati ufficiali italiani sono consultabili sul sito del Ministero della Salute (Bollettino Epidemiologico) e vengono aggiornati annualmente.

Classificazione SIMI delle malattie infettive soggette a notifica

Sistema di Sorveglianza speciale per le malattie batteriche invasive (MIB) (1) • Il MIB (attivato nel 1994) è coordinato dall’Istituto Superiore di Sanità e dal Ministero della Salute ed è esteso a tutto il territorio nazionale. Nel marzo 2007 è stato stilato un protocollo che prevede la segnalazione di tutti i casi di malattie invasive batteriche causate da meningococco, pneumococco, emofilo e di tutte le meningiti batteriche e la caratterizzazione del microrganismo, • Obiettivi: monitoraggio dell’andamento temporale e geografico dei casi, descrizione della frequenza per agente patogeno, regione e fascia di età e della distribuzione dei sierogruppi/sierotipi circolanti, stima dei casi prevenibili con il vaccino e valutazione dei casi di fallimento vaccinale • Sono inclusi nella sorveglianza tutti i casi diagnosticati in Italia, in persone presenti sul territorio nazionale indipendentemente dalla loro nazionalità, residenza o domicilio.

Sistema di Sorveglianza speciale per le malattie batteriche invasive (MIB) (2) • La segnalazione dei casi va effettuata seguendo l’organizzazione regionale: i sanitari che pongono diagnosi (medici, microbiologi) o le direzioni sanitarie devono inviare la segnalazione entro 12 ore tramite una specifica scheda al Servizio di igiene pubblica della ASL di competenza che provvederà, oltre all’indagine epidemiologica e all’adozione delle eventuali misure per bloccare la possibile trasmissione, all’inserimento del caso nella piattaforma MIB. • Il protocollo contiene la scheda cartacea e le informazioni necessarie alla compilazione della segnalazione on line, le procedure per l’invio e le indicazioni tecniche per la conservazione dei ceppi di meningococco, pneumococco ed emofilo, nonché dei campioni biologici. • Un’eventuale valutazione di conferma dell’agente eziologico e la tipizzazione fenotipica e genotipica viene eseguita presso l’ISS. • I dati vengono analizzati a cadenza trimestrale. L’analisi consolidata su base annuale (compresa la tipizzazione molecolare e la antibiotico-sensibilità) viene eseguita nel mese di maggio dell’anno successivo e presentata in un rapporto.
- Slides: 76