INFECTIONS NEONATALES plan Infections maternofoetales bactriennes Infections virales
INFECTIONS NEONATALES plan Infections materno-foetales bactériennes Infections virales congénitales et périnatales Toxoplasmose congénitale Entérocolite ulcéro-nécrosante

IMF Bactériennes n Incidence sepsis: 1 à 4/1000 n (X 5 chez le préma) n Incidence IMF probables: 3 à 8/1000 n Gravité potentielle: 10% décès n 10 - 30 % séquelles (méningites)
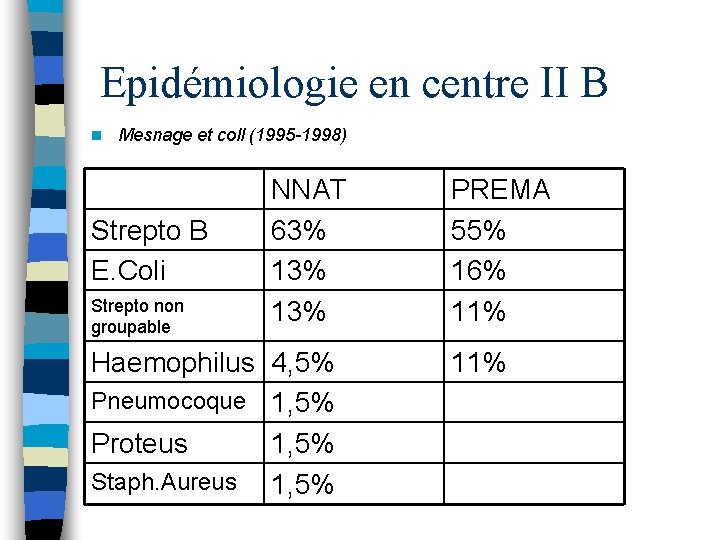
Epidémiologie en centre II B n Mesnage et coll (1995 -1998) Strepto B E. Coli Strepto non groupable NNAT 63% 13% Haemophilus 4, 5% Pneumocoque 1, 5% Proteus 1, 5% Staph. Aureus 1, 5% PREMA 55% 16% 11%
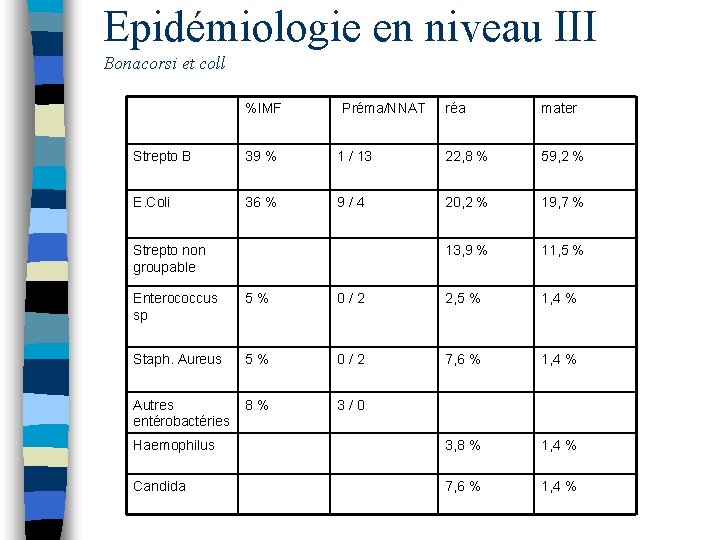
Epidémiologie en niveau III Bonacorsi et coll %IMF Préma/NNAT réa mater Strepto B 39 % 1 / 13 22, 8 % 59, 2 % E. Coli 36 % 9 / 4 20, 2 % 19, 7 % 13, 9 % 11, 5 % Strepto non groupable Enterococcus sp 5 % 0 / 2 2, 5 % 1, 4 % Staph. Aureus 5 % 0 / 2 7, 6 % 1, 4 % Autres entérobactéries 8 % 3 / 0 Haemophilus 3, 8 % 1, 4 % Candida 7, 6 % 1, 4 %

Incidence selon le niveau de soins n Strepto B: NNAT (60 -80%) » PREMA (10 -40%) n BGN (E. Coli): PREMA (40 -60%) résistance à l’Ampi (25 -60%) Fièvre maternelle; RPDE>12 H; ATB récente>24 h n Disparition de Listéria Intérêt des données locales…

Mode de contamination Anténatale et pernatale: -Chorioamniotite ( par le LA ou par un foyer d’endométrite) -Au passage de la filière génitale -Par voie sanguine n Post-natale: Nosocomiale: contamination par des germes de l’environnement hospitalier ( KT) n

Prévention n Streptocoque B: Dépistage systématique par PV au 8ème mois Antibiothérapie per-partum Bilan bactériologique chez le NN présentant un facteur de risque n Listériose: Prévention de la contamination alimentaire Identifier et traiter tout Sd grippal

Prévention des infections postnatales nosocomiales Maitrise de la prescription d’ATB n Hygiène: n -Conception et assainissement régulier des locaux -Stérilisation du matériel médical -Organisation de la chaine alimentaire -Observance par les soignants d’une hygiène personnelle et vestimentaire, des différents protocoles de lavage des mains et d’une aseptie rigoureuse des soins à risque

Conséquences de l’antibioprophylaxie Baisse des IMF SB de 70 -80% (5, 9 à 1, 7/1000) Effets délétères: Augmentation IMF à E. Coli (3, 2 à 6, 8/1000) résistance aux aminopéni prescription d’ATB (29 à 47%)
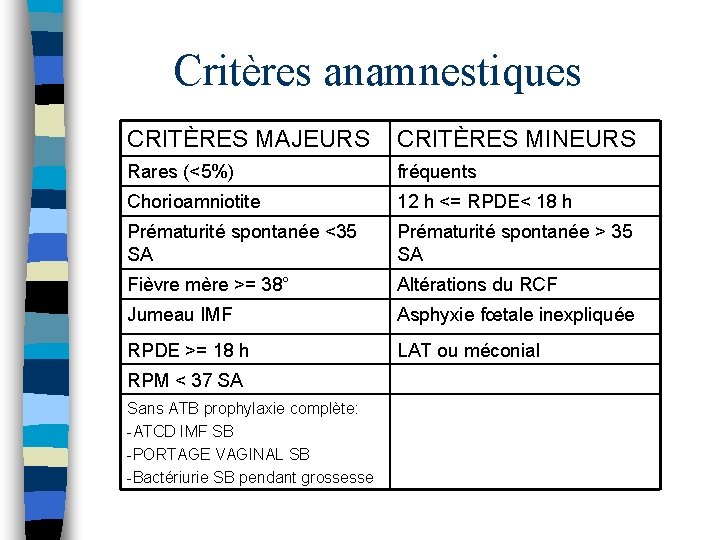
Critères anamnestiques CRITÈRES MAJEURS CRITÈRES MINEURS Rares (<5%) fréquents Chorioamniotite 12 h <= RPDE< 18 h Prématurité spontanée <35 SA Prématurité spontanée > 35 SA Fièvre mère >= 38° Altérations du RCF Jumeau IMF Asphyxie fœtale inexpliquée RPDE >= 18 h LAT ou méconial RPM < 37 SA Sans ATB prophylaxie complète: -ATCD IMF SB -PORTAGE VAGINAL SB -Bactériurie SB pendant grossesse

Signes cliniques d’IMF n Tout NN qui va mal sans raison apparente est à priori suspect d’infection n Aucun SC n’est spécifique n Le TTT est d’autant plus efficace qu’il est débuté précocement n L’IMF est souvent asymptomatique initialement

Signes cliniques d’IMF Fièvre >37° 8 ou variation de la t° de régulation de l’incubateur n Troubles hémodynamiques n (pâleur, TRC>3 s , collapsus) Détresse respiratoire, Apnées n Signes neurologiques n (Mouvements anormaux, fontanelle bombante, geignements, troubles de conscience, troubles du tonus) n Signes cutanés (purpura, ictère)

Bilan biologique suspicion d’IMF n NFS peu contributive GB<5000/mm 3 ou >25000/mm 3, GB immatures n Marqueurs sériques de l’inflammation ( ascension précoce IL 6 à h 12; pas en routine) n CRP Augmente entre h 6 -H 12 après le début de l’infection, culmine à h 24 -h 48 Sensibilité meilleure si dosage entre h 8 - h 12 Sensibilité 98% pour dosage à H 18 -H 24

Intérêts et limites de la CRP n Faux positifs: inhalation méconiale; contusion musculaire; surfactant exogène n Une ascension modérée de la CRP , isolée, nécessite de répéter les dosages n Suivi efficacité TTT; adaptation durée n VPN de 3 CRP<10 mg/l = 99, 7%

Bilan bactério si suspicion d’IMF Liquide gastrique (direct et culture) n Deux prélèvements périphériques n Indications: n Signes cliniques Fièvre mère>=38° pdt travail ou dans les 6 h suivantes RPM avant travail; RPDE>= 12 h LAT ou méconial; prématurité Tachycardie fœtale ou altération du RCF; APGAR < 7 à 5 mn Portage maternel de strepto B sans antibiothérapie complète (<4 h) n Pas d’indication en cas de portage Strepto B si antibioprophylaxie complète, accouchement et enfant normaux

Bilan bactériologique n Liquide gastrique ( Spécificité et VPP modestes, bonne VPN) n Placenta ( frottis + culture) pour IMF supposées hématogènes (listéria, pyélo, fièvre mère) n Hémocultures maternelles n Hémocultures NN examen de référence, voie périph ou KTVO

Récupérer en urgence le direct du PG car oriente: n Streptocoque si cocci gram+ n Escherichia Coli si bacille gram n Listéria si bacille gram + n Mais toute colonisation n’est pas synonyme d’infection

Hémoculture nouveau-né n Prélever au moins 1 ml ( voire 2 ml), surtout si fièvre maternelle n Faible Sensibilité ( 60 %) n 1 seule hémoculture suffisante mais nécessaire n Incubation 5 jours n Culture positive en 48 h si sepsis

Ponction lombaire n Indications: AEG; Signes neuro; sepsis; hémoc. positive n PL peu rentable si hémoculture négative PL traumatiques 22% + LCR insuffisant 26, 3% = 28 à 37% de ponctions inutilisables n Incidence méningite < h 72 faible 0, 25 cas/1000 n Recherche Ag solubles SB ou E. Coli K 1, utile si ATB maternelle ou néonatale

ECBU n Non recommandé n Recherche Ag solubles SB non recommandée n Incidence infection urinaire rare (0, 1 à 1%) n Mauvaise Sensibilité ; risque retard TTT n Test positif = prélèvements périphériques positifs

Indications d’ATB d’emblée chez le NN asymptomatique même si l’antibioprophylaxie a été complète -contexte à haut risque (chorioamniotite, IMF chez le jumeau) -Mère fébrile>38° 5 C -Mère fébrile >=38°C + 1 critère majeur -Prématurité inexpliquée + 1 critère -NNAT + >= 3 critères 1 critère majeur + direct PG positif avec nombreux CG+

Indications d’ATB d’emblée chez le NN asymptomatique en l’absence d’antibioprophylaxie per partum n n n Fièvre maternelle >= 38° 5 C Prématurité + un critère Fièvre mère 38 -38, 5°C + un critère Trois critères ou plus autres que fièvre mère Direct PG positif avec nombreux CG +
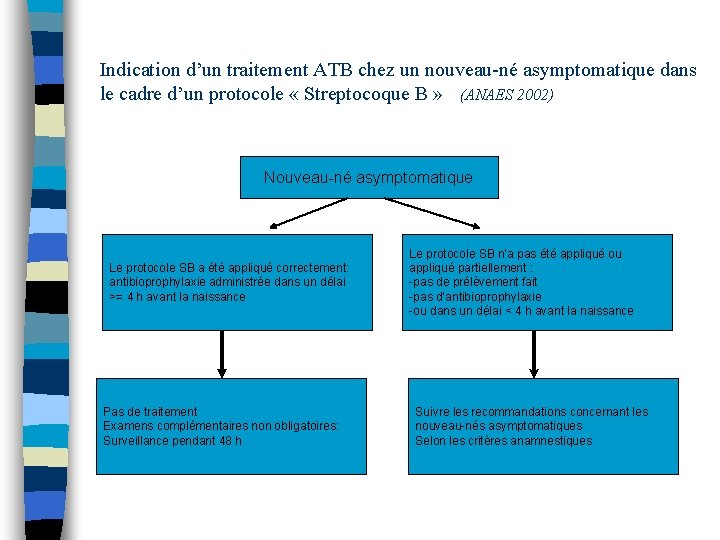
Indication d’un traitement ATB chez un nouveau-né asymptomatique dans le cadre d’un protocole « Streptocoque B » (ANAES 2002) Nouveau-né asymptomatique Le protocole SB a été appliqué correctement: antibioprophylaxie administrée dans un délai >= 4 h avant la naissance Pas de traitement Examens complémentaires non obligatoires: Surveillance pendant 48 h Le protocole SB n’a pas été appliqué ou appliqué partiellement : -pas de prélèvement fait -pas d’antibioprophylaxie -ou dans un délai < 4 h avant la naissance Suivre les recommandations concernant les nouveau-nés asymptomatiques Selon les critères anamnestiques
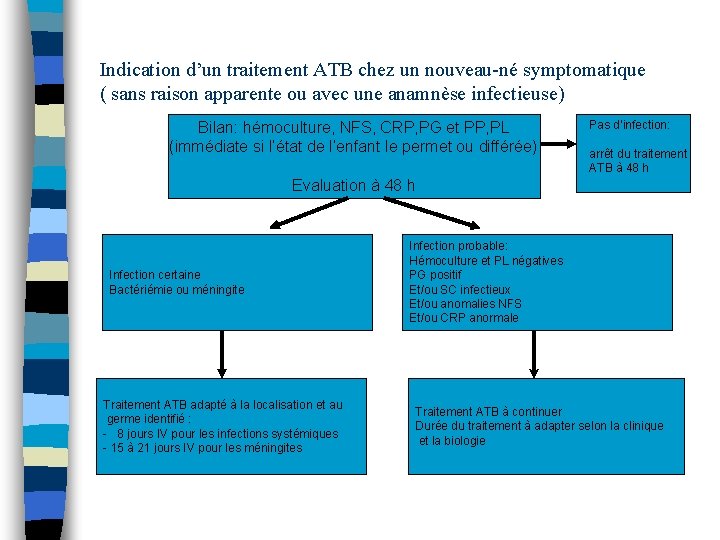
Indication d’un traitement ATB chez un nouveau-né symptomatique ( sans raison apparente ou avec une anamnèse infectieuse) Bilan: hémoculture, NFS, CRP, PG et PP, PL (immédiate si l’état de l’enfant le permet ou différée) Pas d’infection: arrêt du traitement ATB à 48 h Evaluation à 48 h Infection certaine Bactériémie ou méningite Traitement ATB adapté à la localisation et au germe identifié : - 8 jours IV pour les infections systémiques - 15 à 21 jours IV pour les méningites Infection probable: Hémoculture et PL négatives PG positif Et/ou SC infectieux Et/ou anomalies NFS Et/ou CRP anormale Traitement ATB à continuer Durée du traitement à adapter selon la clinique et la biologie

Indications de TTT ultérieur Culture positive Selon la CRP à h 12 - h 24 n Indication bilan? CRP à J 3? Culture négative chez mère ayant reçu ATB prophylaxie incomplète avec cultures négatives

Durée du traitement d’une IMF confirmée n Aminosides: – 2 inj°, espacées de 24 -48 h selon AG et SC – IMF sévère ou germe particulier: prolonger n Béta lactamines: – IV adaptée au germe – Bactériémie: 8 j – Méningite 15 -21 j selon germe

Voie d’administration n Parentérale: – Voie IM déconseillée ( effets locaux, douleur) n’est acceptable qu’en cas exceptionnel

Surveillance des nouveau-nés n Impérative dans les 12 premières heures n Surveillance au moins 48 h pour tous les NN normaux ou suspects d’infection n 95% des IMF surviennent dans les 48 premières heures

RUBÉOLE CONGÉNITALE Virus à ARN; Maladie bénigne chez l’enfant n Contagiosité 8 j avant et après l’éruption n Infection maternelle en cours de grossesse: < 5/ 100000 n Fréquence de la rubéole congénitale: Moins d’ 1 cas sur 100000 naissances vivantes n

Rubéole congénitale: Transmission materno-foetale 60 à 90 % au premier trimestre Risque majeur de malformations avant 12 SA n 50% entre 12 et 16 SA Ils présenteront le plus souvent une surdité. n Après 16 SA, il est rare d’observer des anomalies congénitales n 25% entre 23 -26 SA n Au cours du 3 ème trimestre, la transmission est de nouveau fréquente (>90%), mais ses conséquences seront minimes ou absentes chez le NN

Rubéole congénitale Signes chez le fœtus et l’enfant n Mort fœtale in utero n Retard de croissance intra-utérin n Lésions d’organes: – cerveau ( déficience intellectuelle, microcéphalie, diplégie spastique) – Œil ( cataracte) – Oreille interne ( surdité neuro-sensorielle) – Cœur ( cardiopathies septales)

Rubéole congénitale: Diagnostic anténatal Il est proposé en cas de contact d’une femme enceinte non immunisée avec un patient infecté. n Une primo-infection prouvée du premier trimestre fait discuter l’indication d’une IMG n Sérologie +/- amniocentèse après 18 SA pour PCR ( voire PSF après 22 SA) n On affirme la primo-infection rubéoleuse si: n – – Ascension des Ig. G ou séroconversion avec Ig. M positifs Faible avidité des Ig. G Présence d’Ig. M dans le sang fœtal Identification du génome viral dans le LA

Rubéole congénitale: Prévention n Sérologie préconceptionnelle – Toute femme séronégative doit pouvoir bénéficier d’une vaccination, sous contraception efficace, avant de démarrer une grossesse. – Cette vaccination est proposée à toute femme séronégative, en post-partum immédiat.

Varicelle congénitale: VZV ( varicelle zona virus) Transmission materno-foetale: Faible dans les 2 premiers trimestres (8%) mais élevée au 9ème mois – Accouchement prématuré ou avortement – Varicelle congénitale précoce Maximum de risques pour le fœtus entre 8 -20 SA Le plus souvent asymptomatique après 20 SA, avec risque de zona dans la petite enfance. Le risque d’atteinte fœtale est faible après 24 SA (<1%)

Varicelle congénitale: Risques foetaux n Varicelle congénitale précoce: – Lésions neurologiques (microcéphalie, atrophie corticale, hydrocéphalie…) – Lésions ophtalmologiques ( microphtalmie, choriorétinite, cataracte…) – Hypoplasie d’un membre, aplasie cutanée (cicatrices en zig-zag, hypopigmentées) – RCIU

Varicelle congénitale: Risques périnataux En cas de varicelle maternelle dans la semaine qui précède ou qui suit la naissance, risque de varicelle néonatale dans 25 -50% des cas n En l’absence de traitement: mortalité 25 -30% n Complications: n – surinfection cutanée à staphylocoques – Pneumonie et atteinte multiviscérale

Varicelle congénitale: Incidence n Immunité des femmes enceintes: 95% n Risque de primo-infection: 1à 5/10000 grossesses en France. Moins de 500 cas par an en France n Complication maternelle: pneumonie varicelleuse (13 -16%)

Varicelle congénitale: Prévention n Pour les femmes enceintes non immunisées: – Prévention primaire: • Éviter le contage ( incubation moyenne: 14 J) • Vaccination préconceptionnelle – Prévention secondaire: • Sérologie varicelle si contage +/- gammaglobulines spécifiques moins de 3 j après le contage ou bien Aciclovir dans les 7 j suivant le contage

CAT en cas de Varicelle maternelle en cours de grossesse Surveillance échographique mensuelle +/- IRM au 3 ème trimestre n L’intérêt de l’amniocentèse est controversé: n une PCR négative permet de rassurer la femme mais une PCR positive est 2 fois sur 3 sans conséquence néonatale n Traitement par Aciclovir IV : – si éruption 8 -10 J avant l’accouchement – si forme grave ( indication maternelle)

CAT en cas de varicelle entre 5 j avant et 2 j après l’accouchement n Tocolyse pour retarder l’accouchement de quelques jours (Passage transplacentaire des anticorps protecteurs) n Aciclovir IV chez le NN

Varicelle congénitale: Bilan néonatal Sérologie virale n Suivi ophtalmologique n n Une varicelle acquise au premier mois de vie justifie un traitement par Aciclovir IV. Isoler tout malade présentant la varicelle.

Infection congénitale à CMV ( herpès virus 5) Diagnostic n Primo-infection asymptomatique (90%) ou syndrome pseudo-grippal (10%) Exceptionnellement: anémies, hépatites, pneumonies, encéphalites n Récurrences asymptomatiques n Sérologie CMV avec étude de l’avidité des anticorps ( permet de déterminer le type et la date approximative du début de l’infection) n PCR pour détection et quantification de l’ADN viral

Infection congénitale à CMV Transmission materno-foetale n 30 -40% lors d’une primo-infection Dont: n -10% infection prénatale sévère -10% séquelles neurosensorielles - 80% asymptomatiques 0, 5 -3% lors d’une récurrence – Risque d’atteinte fœtale délétère faible, probablement en raison de la présence d’Ac maternels protecteurs

Infection materno-fœtale à CMV Incidence n Le CMV touche au total 1 à 8 % des grossesses n La primo-infection touche 1 à 5 % des grossesses n Environ 50% des femmes sont séronégatives n 0, 3 à 2, 2% de toutes les naissances viables

Infection materno-fœtale à CMV Signes d’appels échographiques § § § § § Augmentation de l’épaisseur du placenta RCIU global et harmonieux Hydramnios ou oligoamnios Anasarque; ascite; hépatosplénomégalie Hyperéchogénicité du grèle; péritonite méconiale Épanchement pleural ou péricardique Microcéphalie; porencéphalie; lissencéphalie Dilatation ventriculaire; hypoplasie cérébelleuse Calcifications périventriculaires ou sous corticales

Infection congénitale à CMV Diagnostic anténatal Isolement du virus sur culture cellulaire n Quantification du virus par PCR d’ADN viral dans le liquide amniotique prélevé entre 21 et 23 SA et 6 à 9 semaines après la date présumée de la séroconversion. Mais la place de l’amniocentèse est fortement discutée car la positivité ne présume en rien de l’atteinte fœtale n +/- ponction de sang fœtal réservée aux foetopathies graves n n ( anémie, thrombocytémie, érythroblastose, cytolyse hépatique)

Infection congénitale à CMV Diagnostic anténatal n Echographie fœtale: valeur pronostique Meilleur moyen de suivi de l’atteinte foetale n +/- IRM cérébrale fœtale n L’IMG ne se justifie qu’en présence de lésions cérébrales fœtales visibles à l’échographie. – Attention aux dérives de l’IMG: d’après une simulation de dépistage généralisé aux RU sur 200000 femmes enceintes, on aboutirait à 218 IMG pour 16 enfants porteurs de handicap sévère!

Infection congénitale à CMV Diagnostic clinique chez le nouveau-né n n n n n Prématurité inexpliquée Purpura thrombopénique ou pétéchies Hépatosplénomégalie, ictère Hypotrophie; microcéphalie Dilatation ventriculaire; hypoplasie cérébelleuse Calcifications périventriculaires Hypotonie; troubles du rythme respiratoire Choriorétinite +/- atrophie optique Pneumopathie interstitielle; lésions osseuses

Infection congénitale à CMV Diagnostic biologique chez le nouveau-né n Transaminases élevées n Hyperbilirubinémie n Lymphocytose; thrombocytopénie ou anémie n Anomalies de l’hémostase: CIVD n Anomalies du LCR: méningite lymphocytaire avec hyperprotéinorachie

Infection congénitale à CMV Diagnostic chez le nouveau-né Isolement du virus dans l’urine ou la salive dans les deux premières semaines de vie n Culture cellulaire ou PCR d’ADN viral +/- quantification de la virémie (sang; LCR) n n Si diagnostic tardif, faire PCR sur carton de dépistage

Infection congénitale à CMV Examens chez le nouveau-né n Virurie CMV dans la première semaine n NFS n Echographie transfontanellaire n FO (choriorétinite) n Dépistage auditif ( déficit auditif neurosensoriel qui touche jusqu’à 65% des NN symptomatiques et jusqu’à 25% des NN asymptomatiques) n Vers 5 semaines: FO, ETF, PEAs

Infection congénitale à CMV Traitement n Le Ganciclovir ne doit être prescrit qu’en mesurant les effets bénéfices-risques chez un enfant dont les atteintes organiques sont majeures.

Infection congénitale à CMV Pronostic n n n En France, sur 770000 naissances 6350 primo-infections 2220 fœtus infectés dont 90% asympt 3345 Récurrences 690 fœtus infectés asymptomatiques 467 enfants séquelles neurosensorielles Dans les formes symptomatiques: 90% Séquelles: -déficit psychomoteur: 50% - surdité: 50% - choriorétinite 5 -20%
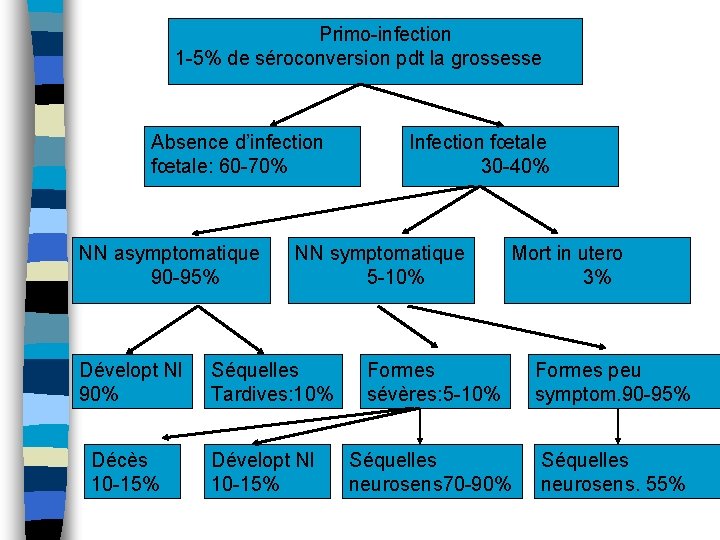
Primo-infection 1 -5% de séroconversion pdt la grossesse Absence d’infection fœtale: 60 -70% NN asymptomatique 90 -95% Dévelopt Nl 90% Décès 10 -15% Infection fœtale 30 -40% NN symptomatique 5 -10% Séquelles Tardives: 10% Dévelopt Nl 10 -15% Mort in utero 3% Formes sévères: 5 -10% Formes peu symptom. 90 -95% Séquelles neurosens 70 -90% Séquelles neurosens. 55%

Infection congénitale à CMV Pronostic à long terme n n n Les séquelles peuvent se révéler progressivement dans les premières années de vie. . CMV= première cause de surdité infantile Hypotonie évoluant vers une spasticité Retard psychomoteur Cécité par choriorétinite Dysplasie de l’émail

Infection congénitale à CMV Surveillance post-natale n La surdité peut évoluer pendant les 7 premières années de vie. – Otoémissions acoustiques et PEA/ an n L’atteinte oculaire peut évoluer après un intervalle libre et progresser durant les premières années de vie. – Examen ophtalmologique avec FO/ an

Infection congénitale à CMV Prévention Recherches en vue d’un vaccin… n Mesures d’hygiène pendant la grossesse: n – Éviter tout contact avec les urines, la salive et les larmes des jeunes enfants Retarder la mise en route d’une nouvelle grossesse après une infection à CMV n Prévention du risque transfusionnel n Traiter le lait maternel par congélation ou pasteurisation avant de l’utiliser dans l’alimentation de l’enfant à risque n

Parvovirus B 19 Généralités n Mégalérythème épidémique ou 5 ème maladie n Passe presque toujours inaperçue n 50% des enfants de 5 ans sont immunisés n L’infection peut induire une anémie, et plus rarement une thrombopénie ou une neutropénie

Parvovirus B 19 Epidémiologie n 40% des femmes sont séronégatives n Dont 1, 5% feraient une séroconversion pendant la grossesse n Transmission materno-fœtale: 30% n 1500 fœtus seraient contaminés chaque année en France

Parvovirus B 19 Signes chez le foetus n Anémie transitoire n Myocardite n Formes sévères: anasarque n Mort fœtale in utéro estimée à 10% des séroconversions maternelles ( surévaluée? ) Si le fœtus survit, la guérison sans séquelles est possible.

Infection congénitale à Parvovirus Diagnostic n Sérologie parvovirus si: – Éruption de nature indéterminée chez la femme enceinte ou dans son entourage – Anasarque foeto-placentaire • Si sérologie négative: controler 15 j après • Si Ig. G positifs et Ig. M négatifs: immunité ancienne • Si Ig. M positifs: séroconversion récente

Parvovirus B 19 En cas de séroconversion Surveillance échographique étroite pendant 3 mois à la recherche de signes d’anémie fœtale ( lame d’ascite, hydramnios, puis anasarque) n En cas d’anasarque, prise en charge en centre très spécialisé pour prélèvement de sang fœtal ( NFS, Ig. M, PCR) et transfusion ou exsanguino-transfusion in utéro. n

Infections périnatales par le Virus Herpès n HSV 2 : herpès génital n Plus rarement: HSV 1 ( herpès labial) n Mode de contamination: Passage dans la filière génitale dans 90% des cas 5% in utéro 5% dans le post-partum

Virus herpès Diagnostic en anté-natal n n n n Avortement ou accouchement prématuré RCIU Microcéphalie Choriorétinite Septicémie herpétique Méningo-encéphalite Atteintes viscérales et cutanéo-muqueuses

Virus herpès Diagnostic à la naissance: 3 formes cliniques Précoce: J 2 -J 7: septicémie ( atteinte pluriviscérale, CIVD+/- atteinte SNC) la plus sévère : 90% de décès n Vers J 12: forme limitée au SNC Méningoencéphalite ( fièvre, troubles digestifs, troubles neurologiques vers J 18) n Formes locales: infection limitée à la peau et aux muqueuses…( mais dans 20% des cas des formes « locales » n la PCR Herpès est positive dans le LCR).

Infection congénitale à virus Herpès Incidence < 1/ 10000 naissances n Risque évalué à 1/1000 en cas d’ATCD d’Herpès génital n Dans 2/3 des cas, l’infection est révélatrice de l’herpès maternel n Transmission materno-fœtale: n – 50 -75% si primo-infection – 2 -5% si poussée d’herpès récurrent en pré-partum

Pronostic de l’herpès néonatal n Mortalité: 50% n Le traitement par Aciclovir diminue la mortalité à 15% n Risque de séquelles neurologiques: 50%

Herpès néonatal Prévention avant la naissance Traitement antiviral au 9ème mois chez les femmes ayant des récurrences herpétiques fréquentes. n Si herpès génital ou lésions suspectes à l’accouchement: n – Prélèvement cervical pour recherche virale – Césarienne avant le début du travail en cas de primo-infection ou quand récurrence dans les 8 j précédants n Désinfection de la filière génitale (Bétadine)

Herpès néonatal Prévention à la naissance n Eviter interventions instrumentales et manœuvres favorisant la contamination n Savonnage du NN à la Bétadine, bien rincer n Désinfection oculaire systématique par collyre Aciclovir pendant 5 j. n En cas d’herpès labial, précautions d’hygiène et surveillance du NN

Suspicion d’Herpès congénital Bilan néonatal n Recherche virale: prélèvements œil, nasopharynx, urines, à répéter tous les 3 j. n +/- ponction lombaire avec dosage d’interféron dans le LCR et le sang

Herpès néonatal Traitement Adapté au risque de contamination n Risque majeur: Primo-infection, à fortiori dans le dernier mois n – Aciclovir IV 15 -21 Jours n Risque modéré: Récurrence plus de 8 j avant l’accouchement, RPDE>6 h, VB sans désinfection… – Discuter l’indication d’Aciclovir PO n Risque mineur: Césarienne précoce avec RPDE < 6 h, absence de lésions maternelles et prélèvement récent négatif

Infection périnatale par le virus de l’hépatite B Généralités n Infections in utéro exceptionnelles n Transmission périnatale et post-natale n NN presque toujours asymptomatique n Passage à la chronicité 90% n Maladie plus sévère que chez l’adulte: risque élevé de cirrhose et de carcinome hépato-cellulaire

Infection périnatale à virus hépatite B Incidence n Ag HBs positif chez: – 0, 15% des femmes enceintes – 1 -3% dans les régions parisienne et Lyonnaise – 5 -8% dans les populations immigrées d’Afrique noire et d’Asie du Sud-Est

Infection périnatale à virus Hépatite B Risque de transmission périnatale en cas de portage chronique n Si portage chronique Ag HBs: 15% n Si ADN viral présent: 90 -100% n Si ADN viral négatif et Ac anti Hbe négatif: 10 -20% n Proche de 0% si Ac anti Hbe positif

Infection périnatale par l’hépatite B Prévention Dépistage systématique: Sérologie obligatoire au 6ème mois de grossesse: Ag HBs n Dans les 12 -24 premières heures de vie: n – Injection d’immunoglobulines anti-HBs – Vaccination anti-hépatite B en un site différent avant h 48 Cette prophylaxie réduit le risque de transmission de plus de 90% L’allaitement maternel est autorisé si la sérovaccination a été bien conduite

Infection périnatale à virus Hépatite B Bilan et suivi de l’enfant n Suivi médical pédiatrique poursuite de la vaccination à un et deux mois n Sérologie hépatite B à effectuer à un an NB: il est aussi conseillé de vacciner les enfants dont le père appartient à une population à risque

Infection périnatale à virus Hépatite C Généralités n Facteurs de risque: toxicomanie IV; transfusion avant 1991; population originaire d’Afrique noire n Diagnostic: Sérologie Hépatite C réalisée au 6 ème mois dans les populations à risque n Incidence: 1% des femmes enceintes

Infection périnatale à virus Hépatite C Transmission materno-foetale n 5 -10% chez les enfants de mère virémique ( ARN viral +) n 28% en cas de co-infection HVC + HIV n NN presque toujours asymptomatique n Risque d’Hépatite C chronique

Infection périnatale à virus Hépatite C Prévention n Pas de vaccin n Préférer la voie basse pour l’accouchement n Allaitement maternel: informer la mère du risque théorique quoique minime de passage du virus dans le lait. n L’allaitement est déconseillé pour les femmes ARN +

Infection périnatale à virus Hépatite C Bilan et suivi de l’enfant n Suivi pédiatrique indispensable n Sérologie HVC et recherche de l’ARN viral à 6 mois et 1 an n Si ARN viral positif: suivi spécialisé tous les 3 mois n Vaccinations anti Hépatites A et B

Toxoplasmose Généralités n Parasite: Toxoplasma Gondii n Diagnostic: – < 20% des cas: fièvre; adénopathies; céphalées; fatigue Primo-infection souvent asymptomatique

Toxoplasmose congénitale Transmission materno-foetale n Environ 30%. Taux corrélé avec le terme n Premier trimestre: 4 -14% – Rare mais grave n Deuxième trimestre: 17 -29% n Troisième trimestre: > 50% – Souvent latente avec risque de choriorétinite dans l’enfance ou l’adolescence

Toxoplasmose congénitale Diagnostic n En début de grossesse: – Avortement – Mort in utéro – Foetopathie: • Lésions de vascularite et de nécrose cérébrale – Encéphalite +/- hydrocéphalie – Calcifications intra-craniennes • Ascite; épanchements pleural et péricardique • Myocardite; Hépatite: placentite…

Toxoplasmose congénitale Incidence n n n 50% des femmes sont séronégatives Le risque d’infection maternelle pendant la grossesse est de 1, 5% Primo-infections: 7à 10/1000 grossesses Fœtus atteints: 1 à 3 / 1000 naissances vivantes 700 à 2000 cas par an en France

Toxoplasmose congénitale Pronostic n 2 -3% des enfants naissent gravement atteints. (microcéphalie; retard mental; convulsions; surdité) n L’affection est latente dans plus de 80% des cas, avec risque de choriorétinite ultérieure.

Toxoplasmose congénitale Diagnostic anténatal Sérologies effectuées dans le même labo n Si séroconversion: faire une amniocentèse à partir de 18 SA, au minimum 4 semaines après la date estimée de l’infection maternelle. n – PCR – Inoculation à la souris n Recherche de signes échographiques ( écho mensuelle)

Toxoplasmose congénitale Diagnostic anténatal (2) n Plus difficile en l’absence de sérologie préconceptionnelle ou quand la première sérologie montre Ig. G et Ig. M n Le diagnostic repose alors sur des techniques d’avidité et sur la cinétique des anticorps

Toxoplasmose congénitale Prévention n Conseils aux femmes séronégatives: – – – Se laver les mains avant et après toute manipulation d’aliments Faire cuire suffisamment les viandes (>65°C) bœuf, mouton, porc, cheval Laver soigneusement crudités et salades Nettoyer les ustensiles et les surfaces ayant servi à la prépa des aliments Utiliser des gants pour nettoyer la litière du chat, jardiner n Sérologie mensuelle chez les femmes enceintes non immunisées ( depuis 1978 en France)

Toxoplasmose congénitale Bilan néonatal (suite) n Echographie transfontanellaire n Examen ophtalmologique: FO n Ponction lombaire à discuter ( inutile si séroconversion avant le 3 ème trimestre avec échographies normales et bilan post-natal négatif.

Toxoplasmose congénitale Traitement maternel en cas de séroconversion n Avant 30 SA: – Si PCR -: Rovamycine jusqu’à l’acc – Si PCR+ sans signes écho: • Malocid/ Adiazine ou Fansidar/ acide Folique – Si PCR + avec signes écho: IMG proposée n Après 30 SA: – D’emblée Malocid/ Adiazine ou Fansidar/ acide Folique – Éventuel déclenchement en fin de grossesse

Toxoplasmose congénitale Traitement du nouveau-né n NN symptomatique ou forte suspicion ( PCR+): – Adiazine+ Malocid ou Fansidar+ ac. Folique pendant 1 an – Surveillance NFS/10 -15 j ( leucopénie) Suspicion faible: traitement si bilan post-natal positif n Séroconversion récente sans bilan fœtal effectué: discuter TTT d’emblée n Rovamycine inutile n

Toxoplasmose congénitale Bilan néonatal: ( biologie) n Envoi du placenta en parasitologie pour inoculation à la souris n Sérologie toxoplasmose maternelle et au cordon pour profil immunologique comparé mère/ enfant n Sérologie toxoplasmose et NFS prélevées à J 3 ( avec dépistages)

Toxoplasmose congénitale Dépistage des séroconversions tardives Contrôle sérologie toxoplasmose entre J 15 et J 21 après l’accouchement chez les femmes non immunisées. n Dans 6% des cas, c’est seulement le suivi sérologique au delà du 3 ème mois de vie qui conduira au diagnostic, en raison de la persistance des Ig. G qui, en l’absence de toxoplasmose congénitale, disparaissent en moins d’une année n

Entérocolite ulcéro-nécrosante Définition n Nécrose de la muqueuse intestinale n Facteurs favorisants: – Prématurité – Souffrance fœtale périnatale – Anoxie – Mauvais état hémodynamique – Infection – Alimentation hyperosmolaire

Entérocolite ulcéro-nécrosante Diagnostic clinique n Occlusion secondaire dont le début se fait souvent vers la première semaine de vie, mais peut être aussi très rapide dès les premières heures, ou retardé au delà du 1 ier mois chez le grand prématuré.

Entérocolite ulcéro-nécrosante Signes cliniques: Phase de début n Installation d’un iléus avec résidus gastriques n Ballonnement abdominal douloureux n Rectorragies n Signes infectieux cliniques et biologiques

Entérocolite ulcéro-nécrosante Signes radiologiques n Phase de début: – Distension des anses grêles – Stagnation des anses sur les clichés successifs n Diagnostic formel: – Pneumatose de la paroi intestinale ( petites bulles d’air dessinant un double contour des segments concernés). – +/- pneumatose portale

Entérocolite ulcéro-nécrosante Evolution n Rétrocession spontanée n Perforation – Péritonite stercorale avec pneumopéritoine (croissant clair sous paroi abdo sur Rx abdomen de face rayon horizontal) – Péritonite cloisonnée (anses agglutinées) avec plastron palpable entraînant la persistance de l’occlusion n Sténose cicatricielle

Entérocolite ulcéro-nécrosante Traitement médical n Antibiothérapie efficace sur les entérobactéries et les germes anaérobies. n Drogues vasopressives améliorant la circulation mésentérique n Aspiration gastrique n Sédation n Fréquemment ventilation artificielle

Entérocolite ulcéro-nécrosante Traitement chirurgical n Indications opératoires: – Péritonite généralisée: entérostomie en amont des lésions +/- résection des anses nécrosées – Indication secondaire devant un plastron ne cédant pas sous traitement médical – Sténose cicatricielle: résection anastomose en un temps ( le plus souvent)

Entérocolite ulcéro-nécrosante Pronostic n Affection grave dont l’incidence diminue du fait de la meilleure prise en charge des prématurés. n Mortalité: 15 -20% n Pronostic fonction du terrain et de l’étendue des lésions. n Séquelles: syndrome du grèle court
- Slides: 101