Les infections nonatales bactriennes Infections prcoces Infections maternofoetale

Les infections néonatales bactériennes Infections précoces Infections maternofoetale précoce<72 h Infections tardives Infections maternofoetale tardive Infections nosocomiales ou iatrogène

introductions Définitions physiopatho dignostic positif

objectifs Définir Reconnaitre les nouveau-ne à risque d’infection citer les germes les plus fréquents Préciser l’antibiothérapie probabiliste surveiller un nouveau-né suspect d’infection

définitions Les infections néonatales bactériennes: sont définies par la présence d’un agent bactérien dans un milieux normalement stérile: sang et ou le LCR

introduction l’infection maternofoetale représente une cause importante de mortalité et de morbidité néonatale fréquente et graves: 4%des naissances, 10%déces N DGC et TRT précoce

Les infections maternofoetales: les infections fœtales infections néonatales infections post natales Les infections post natales

Infections maternofoetale le 1 er mois vie , ↔ 5 millions de morts 15% de mortalité ds les pays industrialisé Incidence: 10% des naissances vivantes Evolution très rapide Absence de signes spécifiques Dépassement rapidement les capacités de défense de l’organisme et les possibilités thérapeutiques Dgc doit etre précoce Basé sur des facteurs de risques d’infection Trt ATB présomptif

Physiopathologie de la colonisation à l’infection Le nouveau-né se colonise durant les 5 1 er jours de vie: TD, peau, VAS Colonisation perturbé par transmission un germe pathogène, mère, envir Translocation digestif de bactéries, pellulation favorisé/antibiothérapie Déficit physiologique de l’immunité Déficit fonctionnel des lymphocytes T ds la production des lymphokines Immunité potentielle , pas encore de mémoire Déficit humoral cmpensé par les Ig. G maternelle qui traverse le placenta par un mécanisme actif en fin grossesse

3 modes de contaminations: A/INFECTION MATERNOFOEATEL 1)Voie systémique transplacentaire: bactériemie maternel ou foyer infectieux maternel ou foetoannexiel 2)Voie ascendante: colonisation du LA par un germe pathogène, flore vaginal; +/RPM 3)Lors du passage dans la flore vaginale: ingestion, inhalation, ou atteinte cutanéomuqueuse →Infection amniotique et rupture de la poche des eaux : Risque d’IN X par 10 à 100 après 24 h Fréquence ↗ si amniotite bactérienne →IMF et propriétés antibactériennes du LA : Le LA contient plusieurs facteurs s’opposant à la croissance bactérienne (peptide+Zinc) Activité inhibitrice contre E. Coli (68%), SB (36%) Risque infectieux fonction de la concentration bactérienne dans le LA B/INFECTIONS NOSOCOMIALES: Post-natal: nosocomiale : germe de l’environnement hospitalier

ETIOLOGIES Les 3 germes classiques: Streptococcus AGALACTIAE 37% Echerichia coli 20% Listéria monocytogène exceptionnel<1% Les autres germes: Staphylocoque auréus Klebsiella penumonie Pseudomonas aerogénosa Protéus, hémophilus influenzae, autres BGN La nature du germe varie avec des facteurs géographiques et avec le temps Nécessité d’adapter l’antibiothérapie à l’ecologie bactérienne

Diagnostic positif Critères anamnéstiquees Critères mineurs Critères majeurs ATCD d’infection à SB fraterie PRSENCE D 4 UN SB au SB Liquide amniotique teinté 35 ≥prématurité ≤ 37 Fièvre maternelle avant le début du travail ≥ 38° Liquide amniotique fétide Chorioamniotite 18 ≥ 12 H ouverture PDE≤ 18 H Prématurité spontanée <35 sem RPM <37 SA avant le debut du W d Infection maternelle sévère Durée ouverture PDE ≥ 18 h Tachycardie >170 C/mn T° maternelle ≥ 38° Jumeau atteint d’une IMF souffrance fœtale inéxpliqué infection maternelle urinaire non traité moins Anomalies du RCF: tachycardie foetale 48 H

Critères cliniques Tout nouveau-né qui va mal sans raison apparente est suspect d’infection Hypothermie ou hyperthermie Détresse respiratoire geignement, apnées; cyanose Ballonement abdominal, refus de téter, résidus gastriques importants, Signes cardiovasculaire: tachycardie, Troubles hémodynamiques. Signes neurologiques: fontanelle bombante. Difficultés alimentaires HSPM Signes cutanés: purpuras, eruption, ictère Troubles digestifs : vomissements, balonnement abdominal, refus de boire Ictère précoce

2 tableaux réalisés Les infections généralisés graves : expression pulmonaire, et ou hémodyanamique , choc infectieux Iiaire à une incompétence myocardique à cocci gram+, entérobactéries Méningites bactériennes forme grave : mortalité, et séquelles élévé: abcés, ventriculite, infarctus ischémohémmoragique Aucun signe n’est spécifique Initialment Asymptomatique

Formes cliniques infection fœtale: chorioamniotite, précocité, gravité infection néonatale: signes de choc septique débutant, signes de DRS, signes neuroméningé infection post natale 4, 12 sem à strepto B

Critères biologiques Signes hématologiques: FNS/ -Hyperleucocytose ≥ 25000 ou ≤ 5000 -Plaquettes <100000 -Hb 13 g Signes biochimiques: Marquers seriques de l’inflammation -CRP à H 12≥ 20 mg/l - interleukines 100 mg/ml -Procalcitonines≥ 5 microg/l Autres: Hyperglycémie Acidose métabolique

Signes bactériologiques Prélèvements centraux périphérique Hémocultures Ponction lombaire indiquée (AEG, anlies neuro) prélèvements liquide gastrique oreille anus liquide amniotique Hémoculture positif Antigènes solubles sang, LCR Chez la mère: hémoculture, prélevement

Cocci positif prenant le gram: strepto. B Bacille ne prenant pas le gram escherchia coli Cocci ne prenant pas le gram listéria monocytogène

Infections maternofoetale tardives J 15, J 30(J 7 -3 mois), infections à strepto incidence: 4 -8/1000 Mortalité: 10% Transmission horizontale mère, entourrage. Contamination par les germes du tube digestif. Facteurs de risque: prématurité, antibiothérapie, nutrition parentérale prolongée, hospitalisation prolongée germes en causes: staphylocoque, entérobactéries, entérocoq ue, streptocoque lait maternel

Traitement 1 Toute infection probable ou certaine impose une ATB sans délai AEG ou absence d’orientation: 3 ATB Clamoxyl 200 mg/kg/J+ en 2 fois claforan+200 mg/kg/J en 2 fois Amiklin 15 mg/kg/J 1 seule fois si suspicion de BGN bithérapie claforan+amiklin si suspicion de listériose bithérapie clamoxyl+amiklin si suspition de SB bithérapie péni. G+amiklin

Traitement 2 A H 48 h: infection certaine , germe isolé ds le sang, ou LCR , adaptation de l’ATB/antibiogramme HMC+, ou PL+ Ecoli: claforan SB peni. G 100000 u/kg/j Listériose: ampicilline 200 mg/kg/j Les autres selon antibiogramme Durée du traitement Septicémie: 8 j, après négativation bactériologique Méningite: 15 j, après négativation bactériologique

Traitement 3 À H 48, infection probable, prélevements bactériologi+ autres que le sang et le LCR Examen clinique non normalisé, pl, CRP≥ 20 mg/l Poursuite du TRT ATB pdt 8 j examen clinique normal, CRP≥ 20 mg/l, poursuite du TRT pdt 5 jours A H 48, infection non confirmé, prélèvements bactériologiques stériles , examen clinique normalisé à H 48 h et CRP<20 mg/l Arrêt du TRT au bout de 48 h

Infections nosocomiales Infections nosocomiales Taux élévé en réanimation 14% Sites les svt atteint sang et poumons Infection d’origine Endogène a pt de départ digestif: stase, ATB Exogène: prothèse: cathéter central, sonde endotrachéale, drain
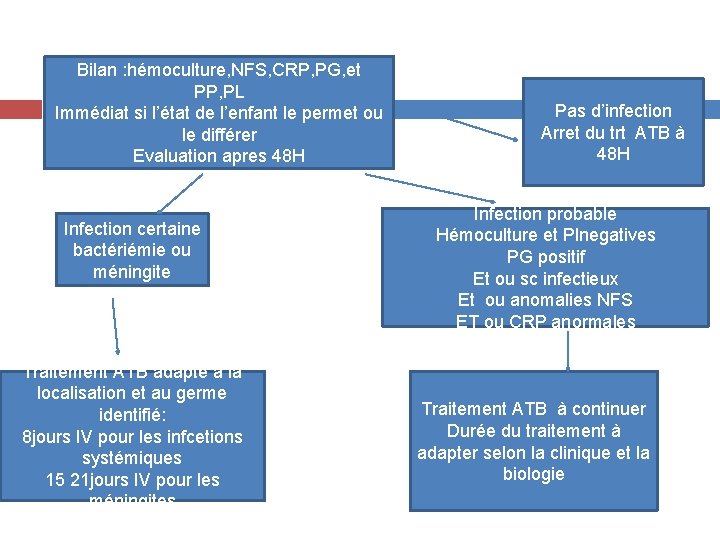
Bilan : hémoculture, NFS, CRP, PG, et PP, PL Immédiat si l’état de l’enfant le permet ou le différer Evaluation apres 48 H Infection certaine bactériémie ou méningite Traitement ATB adapté à la localisation et au germe identifié: 8 jours IV pour les infcetions systémiques 15 21 jours IV pour les méningites Pas d’infection Arret du trt ATB à 48 H Infection probable Hémoculture et Plnegatives PG positif Et ou sc infectieux Et ou anomalies NFS ET ou CRP anormales Traitement ATB à continuer Durée du traitement à adapter selon la clinique et la biologie

Indications d’ATB d’emblee chez nne asymptomatique: en l’absence d’antibioprophylaxie: Fièvre maternelle ≥ 38, 5 c prématurité+un critère Fievre mère 38 -38, 5°C+ un critère Trois critères ou plus autre que fièvre mère Direct PG positif avec nombreux CG+ Protocole SB ds un délai <4 H Surveillance au moins 48 h pour tous les Nnnormaux ou suspects d’infection 95% des IMF surviennent ds les 48 premières heures

Prevention Dépister et traiter les mères(strepto, herpes) hygiène et asepsie, accouchement , lavage des mains, gel hydroalcoolique, blouse par enfant allaitement maternel maitrise de la prescription d’antibiotique hygiène: stérilisation du matériel médical organisation de la chaine alimentaire observance par les soignants: hygiène personnelle et vestimentaire protocole de lavage des mains asepsie rigoureuse

LES INFECTIONS PARASITAIRES La toxoplasmose: Infection parasitaire à toxoplasma gondii Contamination : Ingestion de viande crue, aliments contaminés Risque d’infection fœtale croit avec l’age gestationnel Transmission maternofoetale 30% plus élevé en fin de grossesse 160/1000 femmes enceinte ne sont pas protégées 10/160 contracte une infection toxoplasmique 4/10 vont contaminer leurs enfant La contamination est plus fréquent au 3ème trimèstre

Transmission maternofoetale 1 er trimestre : 4 -14%, rare mais grave 2ème trimestre 10 et 24 sem: fréquence +gravité se conjuguent: 17 à 29% 3ème trimestre › 50%: latente , risque de choriorétinite dans l’enfance ou l’adolescence Tout femme séronégative : sérologie mensuelle : dépister une séroconversion

4 tableaux cliniques réalisés 1 er trimèstre: MFIU, avortement 3ème trimèstre: formes latentes a révélation tardif, RPM, CR 2ème trimèstre Troubles neurologiques: microcéphalie, hydrocéphalie, convulsion s, déficit moteur, retard psychomoteur, strabisme, nystagmus, cécité, calcifications Anomalies viscérales: ictère, éruption cutané, troubles hémorragi

Que faire devant une sérologie positive en l’absence de prélèvements antérieurs? Serologie positive à en Ig. Gavec Ig. M: un 2ème prélevement Ig. G, 3 sem après le premier L’augmentation significative du titre d’Ig. G authentifie le caractère évolutif de la toxo Un taux stable d’ig. G affirmant une contamination au moins 2 mois avant le premier prélèvement Séroconversion maternelle indication du dgc anténatal: seroconversion : un 2ème sérum doit etre prélevé ds les 48 h : prescription sans délai par la spiramycine en attendant la réalisation d’un dgc anténata. L

Diagnostic anténatal: Sérologies effectués dans le même labo. si séroconversion: amniocentèse 18 S +4 s après l’infection PCR Inoculation à la souris Signes spécifiques indirects: signes sérologiques présence d’Ig. M fœtales , d’Ig. G Si Ig. M+Ig. G/dgc difficile: étude cinétique des anticorps Ø Recherche de signes échographique : écho mensuelle

SIGNES ECHOGRAPHIQUES D’appel D’INFECTION FŒTALE Au niveau cérébral: microcéphalie, dilatation des ventricules cérébraux, hyperechogénicité; arenchymateuse. epanchement des séreuses: hydrothorax, pericardite, ascite NIveau. digestif: hyperechogénicité. digestive, , calcifica tions hépatiques spléniques Au niveau placentaire: aug de son épaisseur sup à 5 cm Anasarque foetoplacentaire signe d ’appel fréquent

Diagnostic 1 En début de grossesse: Avortement Mort in utéro 2 Foetopathie: encéphalite+-hydrocéphalie calcifications intracraniennes ascite, épanchement pleural, péricardique myocardite, hépatite, placentite 2/ 3 des enfants naissent gravement atteints: RM, surdité, convulsions 3 80% affection latente avec risque de chorioamniotite

Traitement maternel en cas de séroconversion Avant 30 sem Si pcr – rovamycine jusqu’à l’accouchement Si PCR+ sans signes echo: malocid/adiazine ou fansidar acide folique Si pcr+ avec signes écho IMG proposé Après 30 S D’emblé malocid adiazine ou fansidar acide folique Eventuel déclenchement en fin de grossesse

Traitement du nouveau-né Nn asymptomatique ou PCR+ Adiazine+Malocid ou fansidar+acide folique pdt 1 an Suspition faible trt si bilan post natal positif Séroconversion récente sans bilan fœtal effectué discuter trt d’emblé Rovamycine inutile

Dépistage des séroconversions tardives Contrôle sérologique toxo entre j 15 et j 21 femmes non immunisées 6% suivi sérologique du 3ème mois conduit au dgc Ig. G disparraissent en 1 année

prévention Conseils aux femmes séronégatives Se laver les mains avant et après manipulations d’aliments Laver soigneusement crudités et salades Nettoyer les ustensiles et les surfaces ayant servi à la préparation des aliments Faire cuire suffisamment les viandes ≥ 65°C, bœuf, mouton Utiliser les gants pour nettoyer la litière du chat, jardinier Sérologie mensuelle chez les femmes enceintes non immunisées

Les infections virales/Embryofoetopathies virales La rubéole congénitale le virus de la rubéole est l’un des agents pathogènes les plus dangereux pour l’embryofoetopathie la rubéole congénitale survient après passage du virus , lors d’une primoinfection maternelle ds la circulation <1 Ocas /an en france

Transmission maternofoetale 60 -90% au 1 er trimestre Risque majeur de malformations avant 12 sem 50%entre 12 et 16 sem Ils présenteront le plus svt une surdité 25% entre 23 -26 SA 3ème trimestre: transmission fréquente sup 90%

Embryopathie rubéolique: Mort fœtale in utéro Retard de croissance intrautérin Lésions d’organes: Cerveau déficience intelectuelle, microcéphalie, diplégie spastique Œil cataracte Oreille interne surdité neurosensorielle Cœur cardiopathie septale

Dgc anténatal femme enceinte non immunisée avec un patient infecté avant 9 sem Primoinfection prouvé du 1 er trimèstre indication d’une IMG Sérologie +/- amniocentèse après 18 sem pour PCR+PSF Primo-infection rubéolique: ↗Ig. G ou séroconversion avec Ig. M positifs Présence d’Ig. M ds le sang fœtal Identification du génome viral ds le LA

Prévention: Toute femme séronégatif doit pouvoir bénéficier d’une vaccination sous contraception efficace 3 mois avant de démarrer une grossesse Cette vaccination est proposée à toute femme séronégative , en post-partum immédiat

Le cytomégalovirus La plus fréquente des infections virales du nouveauné, 0, 5 -2, 7% des naissances Principale cause d’hanticape neurosensorielle acquis durant la grossesse. Contamination fœtale transplacentaire

Infection maternofoetale à CMV Formes asymptomatique 90% Formes symptomatiques Infections congénitales généralisée 10%: Prématurité inexpliquée purpuras thrombopénique. hépatosplénomégalie, ictère. Hypotrophie, microcéphalie. Dilatation ventriculaire, hypoplasie Pneumopathie interstitielle, lésions osseuses

Signes d’appels échographiques Aug de l’épaisseur du placenta RCIU global et harmonieux Anasarque, ascite, hépatosplénomégalie Hyperéchogénicité du grèle , péritonite méconiale Épanchement pleural ou péricardique Microcéphalie, porencéphalie, lissencéphalie Dilatation ventriculaire Calcifications péri ventriculaire

Dgc anténatal amniocentèse: devant un RCIU, CMV et Ig. M ds le sg fœtale PSF Echographie fœtale: lésions fœtales et leur suivi L’IRM cérébral fœtale Dgc post natal isolement du virus ds les urines et nasopharynx la salive, culture cellulaire ou PCR NFS Echographie transfontanellaire FO Dépistage auditif
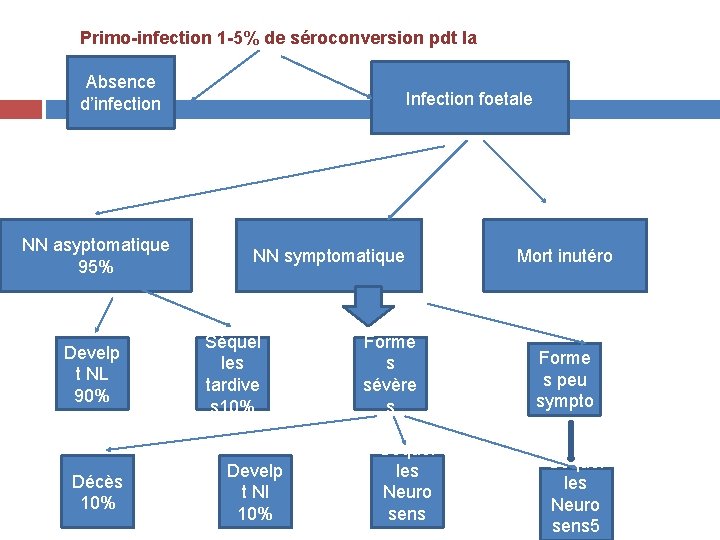
Primo-infection 1 -5% de séroconversion pdt la grossesse Absence Infection foetale d’infection NN asyptomatique 95% Develp t NL 90% Décès 10% NN symptomatique Séquel les tardive s 10% Develp t Nl 10% Forme s sévère s Séquel les Neuro sens Mort inutéro Forme s peu sympto Séquel les Neuro sens 5

Traitement Le ganciclovir: Si atteintes organiques majeures

Prévention congénitale à CMV Eviter tout contact avec les urines, salive, larmes Retarder la mise en route d’une nouvelle grossesse après une infection à CMV prévention du risque transfusionnel Traiter le lait maternel par congélation ou pasteurisation avant de l’utiliser ds l’alimentation de l’enfant à risque
HERPES NEONATAL Incidence faible 3/100000 naissances 2 virus HSV 1 et HSV 2 sont en cause HSV 2: herpès génital HSV 1 Herpès labial Contamination pernatale surtout par le HSV 2 qui siège au niveau du tractus génital. le choix du mode d’accouchement dépend de l’examen gynécologique En début du travail , devant des lésions, herpétiques, l’accouchement sera réalisé par voie haute Contamination anténatal possible Contamination postnatale surtout observé avec le HSV 1

Dgc a la naissance Précoce: <J 7 septicémie+/-atteinte du SNC/ décès 50% J 12: formes limités au SNC/méningoencéphalite Formes locales infection limité à la peau et aux muqueuses

Formes cliniques: Signes cliniques après 6 - 14 jours Formes systémiques: atteinte septicémique avec ou sans atteinte du système nerveux central Sd hémorragiques aboutissant au décès ds 90% des cas Méningoencéphalite 40% associant: troubles du comportement, convulsions, méningite lymphocytaire EEG+IRM/atteintes bitemporales Formes localisées: œil, peau; bouche kératoconjonctivite lésions cutanés, erythème , lésions ulcérés de la muqueuse buccale: vésicule, bulles

Prévention avant la naissance Trt aciclovir au 9ème mois des femmes+si récurrences herp Si herpès génital ou lésions suspectes à l’accouchement césarienne avant le début du travail si infection< 8 J Désinfection de la filière génitale bétadine Risque modéré récurrence sup 8 j avant l’accouche RPMsup 6 h, VB sans désinfection: aciclovir discuté Risque mineur: césarienne précoce avec RPDE<6 h, absences de lésions maternelles et prélèvement récent nég

Prévention à la naissance Savonnage du nne à la bétadine bien rincer Désinfection oculaire systématique collyre aciclovir pdt 5 j Herpès labial, précautions d’hygiène et surveillance du nné Prélèvement œil, nasopharynx, urines/ 3 J Pl dosage interféron ds le LCR et sang
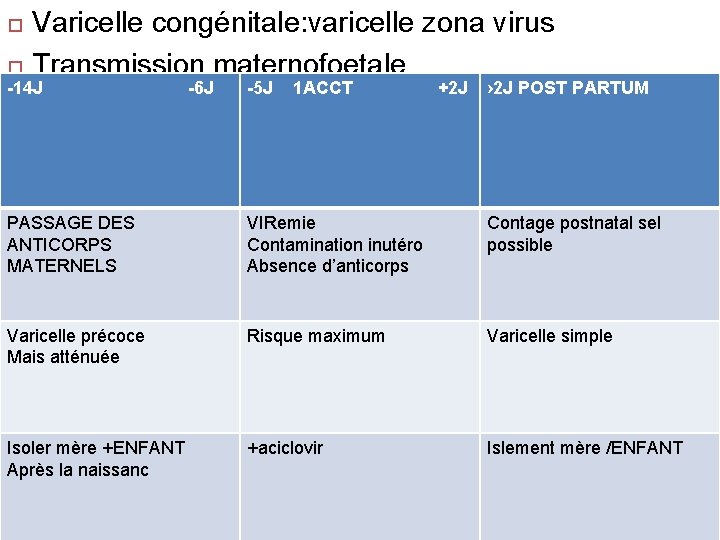
Varicelle congénitale: varicelle zona virus Transmission maternofoetale -14 J -6 J -5 J 1 ACCT +2 J › 2 J POST PARTUM Faible <6 mois Élévé au 9èmois PASSAGE DES ANTICORPS MATERNELS VIRemie Contamination inutéro Absence d’anticorps Contage postnatal sel possible Varicelle précoce Mais atténuée Risque maximum Varicelle simple Isoler mère +ENFANT Après la naissanc +aciclovir Islement mère /ENFANT

aspects cliniques: Atteinte fœtale: avant 8 SA/ avortement, malformations Entre 8 -20 SA foetopathie varicelleuse Après 20 SA risque de zona postnatal Atteinte neonatale: varicèlle congénitale: forme léthale par pneumopathieet ou encéphalite Foetopathies varicelleuse: RCIU Aplasies cutanés Anomalies neurologiques hydrocéphalie, atrophie corticale, microcéphalie Anomalies oculaires microphtalmie, catarcte, choriorétinite Anomalies squelettiques Atteintes viscérales multiples;
- Slides: 55