Analiza objtociowa miareczkowa zadania z rozwizaniem cz II

Analiza objętościowa (miareczkowa) zadania z rozwiązaniem / cz. II Ø Ø ü ü Ø alkacymetria – wiadomości wprowadzające, krzywe miareczkowania: mocnego kwasu mocną zasadą, słabego kwasu mocną zasadą, przykładowe zadania z rozwiązaniem

Alkacymetria – alkalimetria – acydymetria v Alkacymetria – dział analizy miareczkowej dot. ilościowego oznaczania kwasów lub zasad mianowanymi (o ściśle określonym stężeniu molowym) roztworami zasad lub kwasów. v Podstawową reakcją alkacymetrii jest reakcja: Ø kationów hydroniowych (oksoniowych) pochodzących z dysocjacji kwasów, Ø anionów wodorotlenkowych pochodzących z dysocjacji zasad, w wyniku której powstają niezdysocjowane cząsteczki wody: Ø H 3 O+(c) + OH-(c) ↔ 2 H 2 O(c)

Alkacymetria – alkalimetria – acydymetria / cd. v Mianowany roztwór kwasu lub zasady (titrant) wprowadza się do analizowanej próbki (analit) w takiej ilości, aby osiągnąć punkt równoważnikowy (PR): Ø PR – punkt, w którym liczba moli (milimoli) dodanego odczynnika jest stechiometrycznie równa liczbie moli (milimoli) oznaczanego składnika w analizowanym roztworze, Ø odczyn roztworu w punkcie PR zależy od charakteru powstającej soli: Ø p. H = 7 w punkcie PR występuje wyłącznie w przypadku powstawania soli mocnych zasad i mocnych kwasów, które nie ulegają hydrolizie,

Alkacymetria – alkalimetria – acydymetria / cd. Ø przebieg reakcji (reakcji zobojętnia) kontroluje się: ü wizualnie poprzez zastosowany wskaźnik kwasowozasadowy (indykator), którego zmiana barwy wskazuje na zakończenie reakcji, ü z użyciem pehametru elektronicznego (odczyt p. H roztworu lub SEM - siły elektromotorycznej), ü punkt, w którym następuje zmiana barwy indykatora określa się mianem punktu końcowego miareczkowania (PK), ü PK z reguły nie pokrywa się z PR, różnicę określa się jako błąd miareczkowania Bm – jego wielkość określa się liczbą moli (milimoli) titranta lub stosunkiem - wyrażeniami:

Alkacymetria – alkalimetria – acydymetria / cd. v Wskaźniki (indykatory) alkacymetryczne kwasowozasadowe: Ø wprowadza się do analitu (roztworu miareczkowanego), zmianę barwy obserwuje się wizualnie, Ø zakres zmiany barwy wskaźnika (interwał zmiany barwy – do uchwycenia przez wzrok człowieka wynosi ok. 10% obecności jednej z barw wskaźnika) zawarty jest w przedziale 2 -ch jednostek p. H = p. Ka ± 1 (100 – krotna zmiana stężenia H+ w roztworze, p – ułamek zmiareczk. ), Ø wskaźniki kwasowo-zasadowe powinny ostro zmieniać barwę w punkcie PR, zmiana barwy powinna nastąpić pod wpływem niewielkiej ilości roztworu miareczkującego (titranta)

Alkacymetria – alkalimetria – acydymetria / cd. v Oznaczenia alkacymetryczne można przeprowadzić: Ø miareczkowanie mocnej zasady mocnym kwasem, Ø miareczkowanie mocnego kwasu mocną zasadą, Ø miareczkowanie słabej zasady mocnym kwasem, Ø w każdym z w/w przypadków, w miarę wprowadzania titranta, w roztworze analitu zachodzi zmiana stężenia kationów wodorowych lub anionów wodorotlenowych (zmiana p. H roztworu), Ø ilościowy przebieg zmiany p. H w roztworze ilustruje krzywa miareczkowania (zmiana p. H w zależności od Vtitranta lub ułamka zmiareczkowania analitu w roztworze).
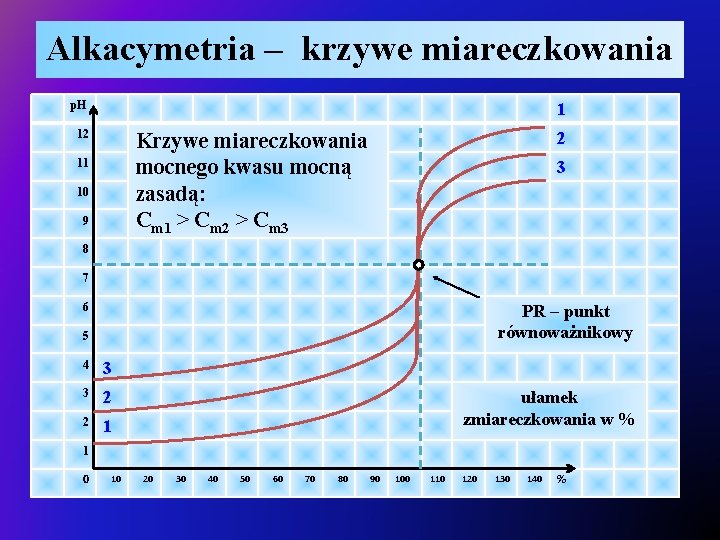
Alkacymetria – krzywe miareczkowania p. H 1 12 2 Krzywe miareczkowania mocnego kwasu mocną zasadą: Cm 1 > Cm 2 > Cm 3 11 10 9 3 8 7 6 PR – punkt równoważnikowy 5 4 3 3 2 2 1 ułamek zmiareczkowania w % 1 0 10 20 30 40 50 60 70 80 90 100 110 120 130 140 %

Alkacymetria – krzywe miareczkowania v. Krzywe miareczkowania mocnego kwasu mocną zasadą: Cm 1 > Cm 2 > Cm 3 : Ø im większe stężenie molowe titranta, tym większy jest skok miareczkowania, Øw przypadku miareczkowania mocnego kwasu HR mocną zasadą Me. OH: Cm. HR = [H 3 O+], Ø krzywe miareczkowania mocnego kwasu mocną zasadą konstruuje się w oparciu o wyrażenia: ü lub

Alkacymetria – krzywe miareczkowania / cd. v. Krzywe miareczkowania mocnego kwasu mocną zasadą: Cm 1 > Cm 2 > Cm 3 : cd. Øw punkcie równoważnikowym (PR) [H 3 O+[ = [OH-] = = 1 ∙ 10 -7 mol/dm 3, Øpo przekroczeniu punktu równoważnikowego (PR) w miareczkowanym roztworze będzie nadmiar anionów OH-, których stężenie będzie równe stężeniu molowym zasady (w łącznej objętości) po reakcji z kwasem:

Alkacymetria – krzywe miareczkowania / cd. v. Krzywe miareczkowania mocnego kwasu mocną zasadą: Øw punkcie równoważnikowym (PR) [H 3 O+[ = [OH-] = = 1 ∙ 10 -7 mol/dm 3, Øpo przekroczeniu punktu równoważnikowego (PR) w miareczkowanym roztworze będzie nadmiar anionów OH-, których stężenie będzie równe stężeniu zasady po reakcji: ü p. H = - log [H 3 O+] lub p. H = 14 – p. OH lub ü gdzie: p. KH 2 O = - log. KH 2 O /ujemny logarytm stałej dysocjacji H 2 O.
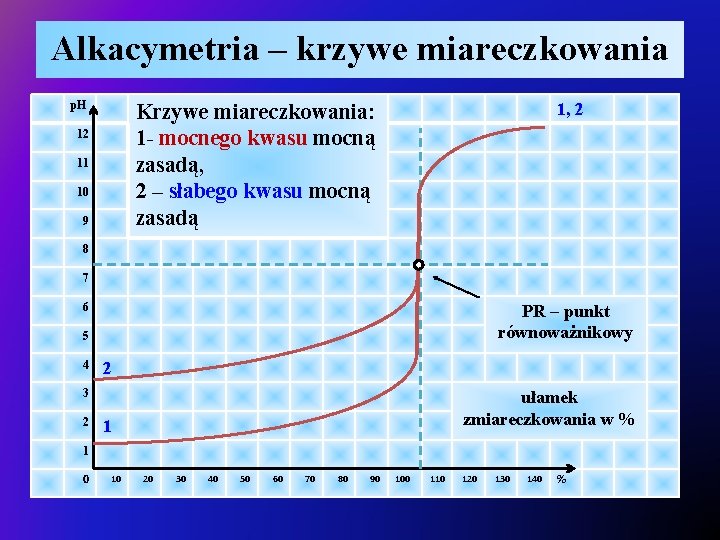
Alkacymetria – krzywe miareczkowania p. H 1, 2 Krzywe miareczkowania: 1 - mocnego kwasu mocną zasadą, 2 – słabego kwasu mocną zasadą 12 11 10 9 8 7 6 PR – punkt równoważnikowy 5 4 2 3 2 ułamek zmiareczkowania w % 1 1 0 10 20 30 40 50 60 70 80 90 100 110 120 130 140 %

Alkacymetria – krzywe miareczkowania v Krzywe miareczkowania: 1 - mocnego kwasu mocną zasadą, 2 – słabego kwasu mocą zasadą Ø Przypadek – krzywa 2: ü w początkowym punkcie miareczkowania stężenie kationów [H+] nie jest równe stężeniu molowemu roztworu kwasu, ü słaby kwas jest zdysocjowany w niewielkim stopniu, a stężenie kationów zależy od stałej dysocjacji: ü po dodaniu porcji roztworu zasady powstaje sól i pozostaje nadmiar słabego kwasu – powstaje roztwór buforowy,

Alkacymetria – krzywe miareczkowania Ø Przypadek 2 / cd. : ü w roztworze buforowym [H 3 O+] zależy od Ka kwasu oraz od stosunku niezobojętnionego kwasu do stężenia powstałej soli w reakcji zobojętnienia (Cmkwasu : Cmsoli), ü stężenie powstałej soli jest stechiometrycznie równe do ilości wprowadzonej zasady, jeżeli do Vkwasu ∙ Cmkwasu / N kwasu wprowadzono Vzasady ∙ Cmzasady / N zasady to: • liczna milimoli niezobojętnionego kwasu: Nkw. = Vkw. ∙ Cmkw. – Vzas. ∙ Cmzas. , • liczba milimoli soli: Nsoli = Vzas. ∙ Cmzas. (w przp. HR + Me. OH) ü stężenie molowe kationów H 3 O+ oblicza się z wyrażenia:

Alkacymetria – krzywe miareczkowania Ø Przypadek 2 / cd. : ü p. H roztworu oblicza się: p. H = - log [H 3 O+] lub z wyrażenia ü w oparciu o powyższe wyrażenia oblicza się stężenie kationów wodorowych lub p. H od początkowego miareczkowania słabego kwasu mocną zasadą aż do osiągnięcia PR – punktu równoważnikowego, ü w punkcie PR powstaje hydrolizująca sól słabego kwasu i mocnej zasady, a stężenie molowe [H 3 O+] / p. H oblicza się:

Alkacymetria – krzywe miareczkowania Ø Przypadek 2 / cd. : ü po przekroczeniu PR w roztworze znajduje się nadmiar zasady i jej sól, stężenie H 3 O+ i p. H oblicza się w wyrażeń: ü krzywe miareczkowania (mocnego kwasu mocną zasadą – krzywa 1), słabego kwasu mocną zasadą – krzywa 2) po przekroczeniu PR pokrywają się, ponieważ w roztworze znajduje się wyłącznie nadmiar mocnej zasady i jej sól,

Alkacymetria – krzywe miareczkowania Ø Przypadek 2 / cd. : ü skok krzywej miareczkowania w przypadku miareczkowania słabego kwasu mocną zasadą zależy od stężenia roztworów, jak i również od wartości stałej dysocjacji elektrolitycznej słabego kwasu (Ka), ü na krzywej miareczkowania 2 przed osiągnięciem PR występuje przegięcie, którego położenie odpowiada 50% - owemu zobojętnienia kwasu, ü w punkcie przegięcia p. H = p. Ka, ponieważ w tym punkcie stosunek stężenia kwasu do stężenia soli jest równy jedności.

Alkacymetria – przykładowe zadania v Zad. 1 Ø 25 cm 3 kwasu HCl o stężeniu 0, 14 mol/dm 3 zmiareczkowano roztworem KOH o stężeniu 0, 15 mol/dm 3 do p. H = 4. Oblicz bezwzględny i względny błąd miareczkowania. Ø obliczenie objętości zasady w punkcie końcowym – PK: ü VKOH = 23, 33 cm 3,

Alkacymetria – przykładowe zadania v Zad. 1 / rozwiązanie cd. : Ø obliczenie błędu bezwzględnego: ü ∆VKOH = VKOH/PK – VKOH/PR = 23, 33 cm 3 – 22, 4 cm 3 ü ∆VKOH = 1, 07 cm 3 Ø obliczenie błędu względnego:

Alkacymetria – przykładowe zadania v Zad. 2 Ø Oblicz względny błąd miareczkowania w trakcie oznaczania 40 cm 3 kwasu mrówkowego o stężeniu 0, 065 mol/dm 3 z użyciem roztworu zasady potasowej o stężeniu 0, 14 mol/dm 3, jeżeli p. H w punkcie PK miało wartość 6, 7 a stała dysocjacji kwasu mrówkowego Ka = 1, 78 ∙ 10 -4. v Rozwiązanie: Ø obliczenie VKOH w punkcie równoważnikowym - PR: Ø obliczenie objętości zasady w punkcie końcowym – PK: ü w punkcie PK przy p. H = 6, 7 jest niewielki nadmiar kwasu mrówkowego, który z solą tworzy roztwór buforowy, ü jeżeli p. H = 6, 7 to: ü [H 3 O+] = 10 -p. H = 10 -6, 7 = 2 ∙ 10 -7 mol/dm 3

Alkacymetria – przykładowe zadania v Zad. 2 / Rozwiązanie cd. Ø obliczenie objętości zasady w punkcie końcowym – PK / cd. : ü 0, 24948 VKOH = 6, 408 cm 3, VKOH = 25, 685 cm 3 Ø obliczenie błędu względnego miareczkowania:

Alkacymetria – przykładowe zadania v Zad. 3 Ø 40 cm 3 kwasu bromowodorowego o stężeniu 0, 125 mol/dm 3 zmiareczkowano z użyciem roztworu zasady sodowej o stężeniu 0, 15 mol/dm 3 roztworu zasady sodowej. Oblicz: a) p. H w początkowym punkcie miareczkowania, b) po dodaniu 20 cm 3 roztworu Na. OH, c) w punkcie PR, d) po podaniu 40 cm 3 roztworu Na. OH

Alkacymetria – przykładowe zadania v Zad. 3 cd. / rozwiązanie - ppkt. b i c: Ø ü ü ü obliczenie p. H po dodaniu 20 cm 3 roztworu Na. OH – ppkt b: NHBr = VHBr ∙ Cm. HBr = 40 cm 3 ∙ 0, 125 mmol/cm 3 = 5 mmol, NNa. OH = VNa. OH ∙ Cm. Na. OH = 20 cm 3 ∙ 0, 15 mmol/dm 3 = 3 mmol, w roztworze znajduje się zdysocjowana sól i niewielka ilość całkowicie zdysocjowanego kwasu HBr ü ∆NHBr = NHBr – NNa. OH = 5 mmol – 3 mmol = 2 mmol, ü p. H = - log [H 3 O+] = - log 0, 0333 = 1, 48 Ø obliczenie p. H w punkcie PR - ppkt c: ü w punkcie PR w roztworze jest zdysocjowana sól i w równowadze molowej kationy oraz aniony w wyniku autodysocjacji wody: [H 3 O+] = [OH-] = 1 ∙ 10 -7 mol/dm 3 ü p. H = - log 1 ∙ 10 -7 = 7

Alkacymetria – przykładowe zadania v Zad. 3 / rozwiązanie / ppkt d : Ø obliczenie p. H po dodaniu 40 cm 3 roztworu Na. OH: ü NHBr = VHBr ∙ Cm. HBr = 40 cm 3 ∙ 0, 125 mmol/cm 3 = 5 mmol, ü NNa. OH = VNa. OH ∙ Cm. Na. OH = 40 cm 3 ∙ 0, 15 mmol/dm 3 = 6 mmol, ü w roztworze znajduje się zdysocjowana sól i niewielka ilość całkowicie zdysocjowanej zasady sodowej, ü ∆NNa. OH = NNa. OH – NHBr = 6 mmol – 5 mmol = 1 mmol, ü [OH-] = 0, 0166 mol/dm 3, ü p. OH = - log [OH-] = - log 0, 0166 = 1, 78 ≈ 1, 8 , ü p. H = 14 – p. OH = 14 – 1, 8 = 12, 2

Alkacymetria – przykładowe zadania v Zad. 4 Ø Analizowaną próbkę zawierająca KHCO 3 i K 2 CO 3 rozpuszczono w wodzie destylowanej a otrzymany roztwór rozcieńczono do objętości 100 cm 3. 50 cm 3 otrzymanego roztworu poddano miareczkowaniu: wobec fenoloftaleiny zużywając 6, 5 cm 3 kwasu HCl o stężeniu 0, 3 mol/dm 3, następnie domiareczkowano wobec oranżu metylowego tym samym kwasem zużywając 12, 6 cm 3. Oblicz zawartość w/w soli w mieszaninie. v Rozwiązanie: Ø miareczkowanie wobec fenoloftaleiny ü K 2 CO 3 + HCl KHCO 3 + KCl ü domiareczkowanie wobec oranżu metylowego ü KHCO 3 + HCl CO 2 + H 2 O + KCl

Alkacymetria – przykładowe zadania v Zad. 4 / rozwiązanie cd. : Ø masy molowe: MKHCO 3= 0, 1 g/mmol; MK 2 CO 3= 0, 138 g/mmol, Ø NHCl zużyta w miareczkowaniu wobec fenoloftaleiny: ü NHCl = VHCl + Cm. HCl = 6, 5 cm 3 ∙ 0, 3 mmol/cm 3 = 1, 95 mmol, Ø w/w ilość NHCl zużyto na domiareczkowanie powstałego KHCO 3 wobec oranżu metylowego: ü m. K 2 CO 3= 2 ∙ NHCl ∙ MK 2 CO 3 = 2 ∙ 1, 95 mmol ∙ 0, 138 g/mmol = = 0, 538 g w 50 cm 3, m. K 2 CO 3= 2 ∙ 0, 538 g = 1, 076 g w 100 cm 3, Ø NHCl zużyta do domiareczkowania wobec oranżu metylowego KHCO 3 zawartego w wyjściowej mieszaninie: ü NHCl = VHCl ∙ Cm. HCl – 1, 95 mmol = 12, 6 cm 3 ∙ 0, 3 mmol/cm 3 – - 1, 95 mmol = 1, 83 mmol, ü m. HKCO 3 = NHCl ∙ MHKCO 3= 1, 83 mmol ∙ 0, 1 g/mmol = 0, 183 g w 50 cm 3, m. HKCO 3 = 2 ∙ 0, 183 g = 0, 366 g w 100 cm 3.

Alkacymetria – przykładowe zadania v Zad. 5 Ø Roztwór kwasu HBr o objętości 50 cm 3 i stężeniu 0, 15 mol/dm 3 zobojętniono roztworem zasady sodowej o stężeniu 0, 2 mol/dm 3. Oblicz p. H roztworu: a) w początkowym punkcie miareczkowania, b) po 30% zobojętnienia kwasu, c) po 80% zobojętnienia kwasu, d) po 105% roztworu Na. OH w stosunku do roztworu HBr. v Rozwiązanie: Ø a) obliczenie p. H roztworu w punkcie początkowym: ü [H 3 O+] = Cm. HBr = 0, 15 mol/dm 3, ü p. H = - log [H 3 O+] = - log 0, 15 = 0, 8239 ≈ 0, 82

Alkacymetria – przykładowe zadania v Ø ü • ü Zad. 5 – Rozwiązanie cd: b) obliczenie p. H po 30% zobojętnieniu kwasu: obliczenie liczby NHBr po 30% zobojętnieniu: ∆NHBr = 0, 7∙VHBr∙Cm. HBr= 0, 7∙ 50 cm 3∙ 0, 15 mmol/cm 3 = 5, 25 mmol, obliczenie liczby NNa. OH i objętości zasady niezbędnej do zobojętnienia w 30%: • NNa. OH = 0, 3∙VHBr∙Cm. HBr= 0, 3∙ 50 cm 3∙ 0, 15 mmol/cm 3=2, 25 mmol, ü obliczenie stężenia kwasu po zobojętnieniu łącznej objętości: • ü obliczenie p. H roztworu po 30% zobojętnieniu: • p. H = - log [H 3 O+] = - log 0, 086 = 1, 0655 ≈ 1, 07

Alkacymetria – przykładowe zadania v Ø ü • ü Zad. 5 – Rozwiązanie cd: c) obliczenie p. H po 80% zobojętnieniu kwasu: obliczenie liczby NHBr po 80% zobojętnieniu: ∆NHBr = 0, 2∙VHBr∙ Cm. HBr= 0, 2∙ 50 cm 3 ∙ 0, 15 mmol/cm 3 = 1, 5 mmol, obliczenie liczby NNa. OH i objętości zasady niezbędnej do zobojętnienia w 80%: • NNa. OH = 0, 8 ∙ VHBr∙ Cm. HBr= 0, 8 ∙ 50 cm 3∙ 0, 15 mmol/cm 3= 6 mmol, ü obliczenie stężenia kwasu po zobojętnieniu łącznej objętości: • ü obliczenie p. H roztworu po 30% zobojętnieniu: • p. H = - log [H 3 O+] = - log 0, 019 = 1, 72 ≈ 1, 7

Alkacymetria – przykładowe zadania v Zad. 5 – Rozwiązanie cd: Ø d) po 105% roztworu Na. OH w stosunku do roztworu HBr. ü obliczenie liczby milimoli nadmiaru NNa. OH : • ∆NNa. OH = 0, 05 ∙VHBr ∙ Cm. HBr= 0, 05 ∙ 50 cm 3 ∙ 0, 15 mmol/cm 3 = = 0, 375 mmol, ü obliczenie liczby objętości zasady niezbędnej do zmiar. w 105% ü obliczenie stężenia zasady po zobojętnieniu łącznej objętości: • ü obliczenie p. H roztworu po 105% zobojętnieniu: • p. OH = - log [OH-] = - log 0, 042 = 2, 377 ≈ 2, 4 • p. H = 14 – 2, 4 = 11, 6

Alkacymetria – przykładowe zadania v Zad. 6 Ø Do roztworu kwasu octowego o objętości 25 cm 3 i stężeniu 0, 25 mol/dm 3, którego Ka = 1, 738 ∙ 10 -5 wprowadzono 8 cm 3 roztworu KOH o stężeniu 0, 15 mol/dm 3. Oblicz p. H w tym punkcie na krzywej miareczkowania. v Rozwiązanie: Ø obliczenie liczby milimoli kwasu i zasady oraz soli: ü NCH 3 COOH = Vr ∙ Cmr = 25 cm 3 ∙ 0, 25 mmol/cm 3 = 6, 25 mmol, ü NKOH = Vr ∙ Cmr= 8 cm 3 ∙ 0, 15 mmol/cm 3 = 1, 2 mmol, jest to jednocześnie liczba milimoli CH 3 COONa, ü roztwór jest buforem zawierającym kwas octowy i jego sól,

Alkacymetria – przykładowe zadania v Zad. 6 – rozwiązanie cd. : Ø obliczenie liczby milimoli nadmiaru kwasu i p. H roztworu: ü ∆N = 6, 25 mmol – 1, 2 mmol = 5, 05 mmol, ü p. H = - log [H 3 O+] = - log 7, 3 ∙ 10 -5 = 5 – 0, 86 = 4, 14

Alkacymetria – przykładowe zadania v Zad. 7 Ø Do roztworu wody amoniaklnej o objętości 50 cm 3 i stężeniu 0, 4 mol/dm 3, której Kb = 1, 778 ∙ 10 -5 wprowadzono 25 cm 3 roztworu HCl o stężeniu 0, 3 mol/dm 3. Oblicz p. H w tym punkcie na krzywej miareczkowania. v Rozwiązanie: Ø obliczenie liczby milimoli kwasu i zasady oraz soli: ü NNH 3(aq) = Vr ∙ Cmr = 50 cm 3 ∙ 0, 4 mmol/cm 3 = 20 mmol, ü NHCl = Vr ∙ Cmr= 25 cm 3 ∙ 0, 3 mmol/dm 3 = 7, 5 mmol, jest to jednocześnie liczba milimoli NH 4 Cl, ü roztwór jest buforem zawierającym kwas zasadę i jej sól,

Alkacymetria – przykładowe zadania v Zad. 7 – rozwiązanie cd. : Ø obliczenie liczby milimoli nadmiaru zasady i p. H roztworu: ü ∆N = 20 mmol – 7, 5 mmol = 12, 5 mmol, ü p. OH = - log [OH-] = - log 2, 96 ∙ 10 -5 = 5 - 0, 47 = 4, 53 ü p. H = 14 – 4, 53 = 9, 47 ≈ 9, 5

Alkacymetria – przykładowe zadania v Zad. 8 Ø Obliczyć wartość skoku krzywej miareczkowania w granicach ± 0, 5 cm 3 roztworu miareczkującego od punktu PR w trakcie oznaczania 25 cm 3 roztworu HCl o stężeniu 0, 4 mol/dm 3 roztworem KOH o stężeniu 0, 4 mol/dm 3. v Rozwiązanie: Ø w punkcie PR przy tych samych stężeniach VHCl = VKOH Ø obliczenie objętości roztworu przy niedomiareczkowaniu: ü Vr = VHCl + VKOH – 0, 5 cm 3 = 25 cm 3 + 25 cm 3 – 0, 5 cm 3 = = 49, 5 cm 3, Ø obliczenie nadmiaru milimoli kwasu: ü ∆NHCl = VHCl ∙ Cm. HCl – VKOH ∙ Cm. KOH = = 25 cm 3 ∙ 0, 4 mmol/cm 3 - 24, 5 cm 3 ∙ 0, 4 mmol/cm 3 = = 0, 2 mmol

Alkacymetria – przykładowe zadania v Zad. 8 – rozwiązanie cd. : Ø obliczenie stężenia molowego HCl w roztworze i jego p. H: ü p. H 1 = - log [H 3 O+] = - log 4 ∙ 10 -3 = 3 – 0, 6 = 2, 4 Ø obliczenie objętości roztworu przy przemiareczkowaniu: ü Vr = VHCl + VKOH + 0, 5 cm 3 = 25 cm 3 + 25 cm 3 + 0, 5 cm 3 = = 50, 5 cm 3, Ø obliczenie nadmiaru milimoli kwasu: ü ∆NKOH = VKOH ∙ Cm. KOH – VHCl ∙ Cm. HCl = = 25, 5 cm 3 ∙ 0, 4 mmol/cm 3 - 25 cm 3 ∙ 0, 4 mmol/cm 3 = = 0, 2 mmol

Alkacymetria – przykładowe zadania v Zad. 8 – rozwiązanie cd. : Ø obliczenie stężenia molowego KOH w roztworze i jego p. H: ü p. OH = - log [OH-] = - log 3, 96 ∙ 10 -3 ≈ 3 – 0, 6 ≈ 2, 4 , ü p. H 2 = 14 – p. OH = 14 – 2, 4 = 11, 6 Ø obliczenie skoku krzywej miareczkowania w przedziale ± 0, 5 cm 3: ü ∆p. H = p. H 2 – p. H 1 = 11, 6 – 2, 4 = 9, 2

Alkacymetria – przykładowe zadania v Zad. 9 Ø Obliczyć wartość skoku krzywej miareczkowania w granicach ± 0, 2 cm 3 roztworu miareczkującego od punktu PR w trakcie oznaczania 30 cm 3 roztworu HCOOH, którego Ka wynosi 1, 778 ∙ 10 -4 o stężeniu 0, 2 mol/dm 3 roztworem KOH o stężeniu 0, 2 mol/dm 3. v Rozwiązanie: Ø w przypadku niedomiareczkowania (30 cm 3 kwasu/ 29, 8 cm 3 zasady) roztwór jest buforem, zawierającym: Ø nadmiar milimol kwasu : ü NHCOOH = (30 cm 3 – 29, 8 cm 3) ∙ 0, 2 mmol/cm 3 = 0, 04 mmol, Ø milimoli mrówczanu potasu: ü NHCOOK = VKOH ∙ Cm. KOH = 29, 8 cm 3 ∙ 0, 2 mmol/cm 3 = = 5, 96 mmol,

Alkacymetria – przykładowe zadania v Zad. 9 – rozwiązanie cd. : Ø w przypadku przemiareczkowania (30 cm 3 kwasu/ 30, 2 cm 3 zasady): Ø nadmiar milimoli zasady: ü NKOH = (30, 2 cm 3 – 30 cm 3) ∙ 0, 2 mmol/cm 3 = 0, 04 mmol, Ø objętość roztworu: ü Vr = VKOH ∙ VHCOOH = 30, 2 cm 3 + 30 cm 3 = 60, 2 cm 3,

Alkacymetria – przykładowe zadania v Zad. 9 – rozwiązanie cd. : Ø obliczenie wartości skoku krzywej miareczkowania: ü ∆p. H = 10, 8 – 5, 9 = 4, 9
- Slides: 39




























































